Method Article
Un metodo di coltura per mantenere le cellule staminali ematopoietiche umane quiescenti
In questo articolo
Riepilogo
Questo protocollo consente il mantenimento in vitro di cellule staminali ematopoietiche umane quiescenti imitando il microambiente del midollo osseo utilizzando abbondanti acidi grassi, colesterolo, concentrazioni più basse di citochine e ipossia.
Abstract
Le cellule staminali ematopoietiche umane (HSC), come altri HSC di mammiferi, mantengono l'ematopoiesi per tutta la vita nel midollo osseo. Gli HSC rimangono quiescenti in vivo, a differenza dei progenitori più differenziati, ed entrano rapidamente nel ciclo cellulare dopo chemioterapia o irradiazione per trattare lesioni del midollo osseo o coltura in vitro. Imitando il microambiente del midollo osseo in presenza di abbondanti acidi grassi, colesterolo, bassa concentrazione di citochine e ipossia, gli HSC umani mantengono la quiescenza in vitro. Qui viene descritto un protocollo dettagliato per il mantenimento degli HSC funzionali allo stato quiescente in vitro. Questo metodo consentirà studi sul comportamento degli HSC umani in condizioni fisiologiche.
Introduzione
Le cellule staminali ematopoietiche (HSC) e le cellule progenitrici multipotenti (MPP) formano coordinativamente un serbatoio per il rifornimento continuo di cellule differenziate per mantenere l'ematopoiesi per tutta la vitanell'uomo 1. La quiescenza del ciclo cellulare è una caratteristica prominente degli HSC, differenziandoli dagli MPP2. Convenzionalmente, si pensa che gli HSC risiedano all'apice della gerarchia del sistema ematopoietico, producendo tutte le cellule del sangue differenziate. Questo modello gerarchico è stato per lo più dedotto dagli esperimenti di trapianto3. Tuttavia, studi recenti hanno indicato che le dinamiche degli HSC differiscono in vivo rispetto a quelle degli esperimenti suitrapianti 4,5,6,7. Esperimenti di tracciamento del lignaggio utilizzando diversi sistemi di codifica a barre hanno rivelato che gli HSC murini fenotipiche non sono un tipo di cellula unico che contribuisce all'ematopoiesi allo stato stazionario, e MPP, che mostrano una limitata attività di autorinnozione su impostazioni di trapianto, forniscono continuamente cellule del sangue mature4,5,8. Al contrario, il contributo degli HSC alle cellule mature viene migliorato dopo la lesione del midollo osseo4. Ciò può essere attribuito a drastiche alterazioni nel microambiente a seguito dell'ablazione del midollo osseo, incluso il trapianto di midollo osseo. Sebbene l'applicazione del tracciamento del lignaggio delle cellule murine alle cellule umane sia difficile, l'analisi filogenetica che combina l'isolamento delle colonie derivate da una singola cellula e il sequenziamento dell'intero genoma ha rivelato una proprietà simile del sistema ematopoietico, in cui sia gli HSC che gli MPP sono responsabili della produzione giornaliera di cellule mature7. Pertanto, sebbene il trapianto sia essenziale per esaminare l'attività dell'HSC murina o umana, sono necessari altri modelli sperimentali per comprendere i comportamenti degli HSC in condizioni fisiologiche.
I metodi di coltivazione per gli HSC sono stati studiati in dettaglio per comprenderne le applicazioni cliniche e le caratteristiche. Gli HSC umani possono essere espansi in vitro utilizzando una combinazione di citochine, ricostituzione di matrici extracellulari, rimozione di antagonisti di autorinnoto, co-coltura con cellule mesenchimali o endoteliali, aggiunta di albumina o sua sostituzione, trasduzione di fattori di trascrizione di autorinnozione e aggiunta di composti di piccolemolecole 9,10. Alcuni di questi metodi, tra cui l'aggiunta di piccoli composti SR111 e UM17112, sono stati testati in studi clinici con risultati promettenti9. Considerando la natura quiescente degli HSC in vivo, mantenere gli HSC con un ciclo cellulare minimo è fondamentale per ricapitolare il comportamento HSC in vitro. Gli HSC quiescenti e proliferano presentano l'ingresso differenziale del ciclocellulare 13,lo statometabolico 14e la tolleranza contro le sollecitazioni multiple15 . I metodi utilizzati per mantenere la quiescenza degli HSC umani in vitro sono limitati.
Imitando il microambiente del midollo osseo (ipossia e ricco di lipidi) e ottimizzando la concentrazione di citochine, gli HSC umani possono essere mantenuti indifferenziati e quiescenti in coltura. Ricapitolando la natura quiescente degli HSC in vitro migliorerà la comprensione delle proprietà allo stato stazionario degli HSC e consentirà la manipolazione sperimentale degli HSC.
Protocollo
Il protocollo segue le linee guida del National Center for Global Health and Medicine. Tutte le procedure sperimentali eseguite sui topi sono approvate dal Comitato nazionale per la salute e la medicina degli animali.
NOTA: Una panoramica del protocollo è illustrata nella figura 1.
1. Preparazione lipidica
- Sciogliere i seguenti lipidi in metanolo in tubi di vetro alle concentrazioni indicate: palmitato di sodio, 16 mg/ml; oleato di sodio, 30 mg/mL; e colesterolo, 4 mg/mL. Conservare la soluzione lipidica a -30 °C e scongelare il campione prima dell'uso.
- Mescolare le soluzioni lipidiche preparate nella fase 1.1 in un tubo di vetro fresco alle dosi necessarie per ottenere la concentrazione finale di palmitato 100 μg/mL, oleato 100 μg/ml e colesterolo 20 μg/ml. Ad esempio, quando si preparano 10 ml di mezzi di coltura, mescolare 62,5 μL di soluzione di palmitato, 33 μL di soluzione di oleato e 50 μL di soluzione di colesterolo nel tubo di vetro.
- Evaporare il metanolo passando il gas azoto attraverso la soluzione lipidica(figura 2A e 2B). Se il gas azoto non è disponibile, passare l'aria attraverso la soluzione utilizzando un ausilio per pipette.
- Evaporare completamente il metanolo rimanente riscaldando il tubo di vetro in un bagno d'acqua a 37 °C(Figura 2C).
NOTA: L'uso di un'alta concentrazione di gas N2 nello spazio confinato è potenzialmente dannoso. Sebbene il volume utilizzato nel protocollo per evaporare il metanolo sia limitato e quindi sia considerato sicuro, la ventilazione adeguata della stanza e l'etichettatura di aree con concentrazioni potenzialmente elevate di gas N2 è importante in caso di perdita di gas imprevista.
2. Preparazione media
- Preparare il mezzo Aquila modificato di Dulbecco (DMEM)/F12 medium (con HEPES e glutammina). Aggiungere la penicillina e la streptomicina solfato al mezzo fino alla concentrazione finale di 50 unità e 50 μg/mL, rispettivamente. Il mezzo DMEM/F12 contenente antibiotici può essere conservato a 4 °C per almeno 2 mesi.
- Aggiungere il 4% w/v di albumina di siero bovino (BSA) al mezzo eagle modificato di Dulbecco (DMEM)/F12 medium (con HEPES e glutammina).
- Regolare il pH del mezzo in pH 7.4-7.8 utilizzando la soluzione NaOH, in genere a pH 7.6.
- Aggiungere il mezzo al tubo di vetro preparato al passaggio 1. Per ottenere una soluzione con la massima solubilità, si consiglia l'aggiunta di 3-15 mL di mezzo.
- Sciogliere completamente i lipidi per sonicazione (ottimale: più di 20 minuti di sonicazione). Dopo lo scioglimento della BSA e dei lipidi, il campione deve essere conservato a -80 °C e utilizzato entro 2 mesi. Scongelare immediatamente prima dell'uso.
- Aggiungere 1/1.000 della miscela insulina, transferrina, selenite di sodio e etano ammina (ITS-X) al DMEM/F12. Filtrare il mezzo misto utilizzando un filtro da 0,22 μm (designato come "supporto di coltura"). Prima dell'uso, aggiungere il fattore delle cellule staminali umane (SCF) e la trombopoietina umana (TPO) ai mezzi di coltura ad una concentrazione finale di 3 ng/mL ciascuno. Dopo aver aggiunto le citochine e l'ITS-X, il mezzo non può essere conservato.
- Tampone di colorazione: Aggiungere il 10% di FCS alla salina tamponata con fosfato (PBS) priva di Ca e Mg. Questa soluzione può essere conservata a 4 °C per 2 settimane.
- Supporto di scongelamento: aggiungere il 10% di FCS al DMEM/F12. Questa soluzione è monoa uso.
- Soluzione di calcio di citochina: Sciogliere ogni SCF umano o TPO umano in PBS (Ca- e Mg-free) a 20 μg/mL. Questa soluzione può essere conservata a -80 °C per almeno un anno senza perdita di attività. Una volta scongelato, conservare la soluzione stock a 4 °C e utilizzare entro 1 mese.
NOTA: Esaminare il lotto dopo ogni acquisto per evitare variazioni nei contaminanti in BSA. Coltura HSC allo stesso tempo con diversi lotti di BSA ed esaminare il numero HSC fenotipico al giorno 7 come descritto di seguito. Se un batch BSA mostra un numero o una frequenza bassi di celle CD34+ (ad esempio meno della metà del numero di celle di input), evitare di utilizzare questo batch.
3. Preparazione del midollo osseo umano CD34+ cellule
- Acquistare cellule umane CD34+ midollo osseo e conservare le cellule in azoto liquido fino all'uso. In alternativa, le cellule del midollo osseo di un volontario sano o cellule del sangue del cordone ombelicale fresco possono essere utilizzate previa approvazione da parte del comitato etico dell'istituto e del consenso del donatore.
- Riscaldare 10 ml di mezzi di scongelamento in un tubo conico da 15 ml in un bagno d'acqua a 37 °C.
- Scongelare le cellule congelate in fiale in un bagno d'acqua a 37 °C entro 2 minuti. Dopo aver pulito la fiala con il 70% di etanolo per rimuovere i contaminanti, trasferire le cellule nel tubo conico da 15 ml contenente il mezzo prerifampto dal passo 3.2.
- Centrifugare il tubo da 15 ml a 200 × g per 15 minuti a temperatura ambiente. Aspirare attentamente il supernatante per mantenere intatto il pellet (lasciando < 50 μL di mezzo). Rimorsi le cellule con il mezzo rimanente e trasferirle in un tubo da 1,5 ml sul ghiaccio.
NOTA: L'esposizione a campioni di origine umana direttamente nella mucosa, compreso l'occhio o il tessuto ferito, può causare infezioni da agenti patogeni noti o sconosciuti; pertanto, guanti e occhiali sono raccomandati quando si maneggiano cellule umane. Anche se le cellule CD34+ acquistate sono negative per il virus dell'epatite B (HBV), il virus dell'epatite C (HCV) e il virus dell'immunodeficienza umana 1 (HIV1), è necessario eseguire un attento monitoraggio secondo le linee guida istituzionali in caso di incidenza dell'esposizione. Seguire le linee guida istituzionali quando si smaltino i materiali esposti alle cellule umane.
4. Smistamento degli HSC
- Etichettare le cellule con anticorpi coniugati con fluorocromo. Mescolare 50 μL di tampone di colorazione più 10 μL di anti-CD34-FITC, 2 μL di anti-CD38-PerCP-Cy5.5, 5 μL di anti-CD90-PE-Cy7 e 10 μL di anti-CD45RA-PE. Rimosogliere il pellet cellulare nella miscela di anticorpi. Incubare le cellule per 30 minuti a 4 °C al buio.
- Aggiungere 1 mL di tampone di colorazione per lavare gli anticorpi. Centrifugare i tubi a 340 × g per 5 min a 4 °C. Scartare il supernatante.
- Rimosoppo il pellet cellulare in 0,5 mL di tampone di colorazione + 0,1% di ioduro di propidio. Trasferire la sospensione in un tubo da 5 ml utilizzando un filtro da 40 μm.
- Gate gli HSC fenotipico all'interno della frazione PI-CD34+CD38-CD90+CD45RA- utilizzando il FACS Aria-IIIu e ordinare le celle in un tubo da 1,5 ml riempito con 500 μL di mezzi dicoltura (Figura 3). Utilizzando la strategia di gating illustrata nella figura 3, ~10% delle celle CD34+ dovrebbe essere HSC fenotipico. Registrare il numero di cella ordinato per calcolare il volume del supporto per rimpiosi le celle nel passaggio 5.3.
NOTA: La strategia di gating viene eseguita come descritto inprecedenza 16 mentre si omette la colorazione del marcatore di lignaggio data la bassa espressione dei marcatori di lignaggio nella frazione CD34+CD38- da individui sani17 . - Centrifugare le cellule ordinate a 340 × g per 5 min a 4 °C e scartare il supernatante. Aspirare con cura il supernatante per garantire che il pellet rimanga intatto.
- Conservare le celle ordinate sul ghiaccio fino alla coltura.
NOTA: La compensazione della fluorescenza della sovrapposizione spettrale deve essere eseguita durante il primo esperimento.
5. Coltura cellulare
- Trasferire 200 μL del supporto di coltura contenente citochine preparate nel passaggio 2 in piastre flat-bottom da 96 pozzi.
- Per evitare l'evaporazione del mezzo, riempire tutti i pozzi inutilizzati con 100-200 μL di PBS.
- Rimescolare gli HSC ordinati nei mezzi di coltura senza citochine a 60 cellule/μL.
- Aliquota 600 HSC/pozzo (10 μL di sospensione cellulare) in ogni pozzo. Il numero di cella può essere modificato. Meno di 300 cellule porteranno a maggiori variazioni tecniche, e quindi sono necessari più pozzi per condizione per rilevare le differenze biologiche. Coltivare più di 1000 cellule in un singolo pozzo dovrebbe essere evitato a causa della privazione di citochine / nutrienti o dell'accumulo di citochine / chemiochine sfavorevoli.
- Coltura delle cellule in un incubatore multi-gas umidificato a 37 °C in un'atmosfera del 5% di CO2 e dell'1% O2.
- Per le colture di età superiore a 7 giorni, si consiglia di sostituire metà del volume multimediale ogni 3-4 giorni. Aspirare con cura 100 μL di supporti pipettando e aggiungere 100 μL di mezzi di coltura appena preparati contenenti citochine ad ogni pozzo. I mezzi di coltura devono essere prerifapidi a 37 °C.
6. Analisi dei fenotipi marcatori mediante citometria del flusso
NOTA: Sebbene le cellule debbano essere analizzate dopo 7 giorni di coltura, la durata delle impostazioni cultura può essere modificata.
- Scartare 170 μL del mezzo utilizzando una pipetta a 8 canali.
- Etichettare le cellule con la miscela di anticorpi. Mescolare 0,5 μL di anti-CD34-FITC, 0,1 μL di anti-CD38-PerCP-Cy5.5, 0,25 μL di anti-CD90-PE-Cy7, 0,5 μL di anti-CD45RA-PE e 9 μL di tampone di colorazione per bene. Aggiungere 10 μL della miscela alla piastra da 96 pozzetti e incubare le cellule per 30 minuti a 4 °C al buio.
- Per lavare gli anticorpi, aggiungere 100 μL di tampone di colorazione ai pozzi e centrifugare le piastre a 400 × g per 5 min a 4 °C utilizzando bassa accelerazione e decelerazione media.
- Aspirare con cura 100 μL del supernatante per mantenere le cellule sul fondo dei pozzi, quindi rimescolare le cellule in 200 μL di tampone di colorazione + 0,1% v/v di PI + 1% v/v di microsfere fluorescenti (ad esempio, fluorosfere Flow-Check).
- Impostare lo strumento di citometria a flusso. Acquisire dati per i campioni in modalità rapida con modalità campione misto su e volumi di assorbimento di 100 μL.
- Esportare i dati in formato FCS e analizzarli utilizzando software come FlowJo. I numeri cellulari possono essere determinati usando il conteggio delle perline fluorescenti della microsfera. Ad esempio, se il ricercatore aggiunge 2000 perline per pozzo e il conteggio delle perline è 700, moltiplicare il numero di cellule di ogni frazione per 2000/700 per stimare il numero totale di cellule della frazione nel pozzo.
NOTA: Le microsfere fluorescenti sono tossiche per le cellule coltivate a causa della presenza di formaldeide. Ciò può indurre la morte cellulare durante l'analisi. Ridurre al minimo il numero di pozzi (<50 pozzi) analizzati continuamente per evitare distorsioni.
7. Trapianto di HSC umani
NOTA: L'attività di ripopolamento delle cellule coltivate viene convalidata mediante trapianto a topi immunodifesa. Tutte le procedure devono essere approvate dai comitati per gli esperimenti sugli animali o dai loro equivalenti.
- Come donatori, preparare un numero sufficiente di topi IMMUNODEFICIENT NOD-SCID-Il2rg-null (NOG) a 8-12 settimane. Poiché i topi NOG sono altamente suscettibili alle infezioni, mantenere le gabbie di allevamento il più pulite possibile e nutrire i topi con una dieta sterilizzata e acqua.
- Coltura un numero adeguato di HSC per il trapianto come descritto nella fase 5. Ad esempio, quando 5000 HSC (equivalente giorno 0) vengono trapiantati su 6 topi riceventi, coltura 35.000-40.000 HSC in 40 pozzi di una piastra da 96 po '(200 μL di mezzi di coltura per pozzo) o in 8 pozzi di una piastra da 24 pozzi (1 mL di mezzi di coltura per pozzo). Coltura delle cellule per 2 settimane con variazioni semi-mediali ogni 3-4 giorni in un incubatore multi-gas umidificato a 37 °C con 5% CO2 e 1% O2. La durata delle impostazioni cultura può essere modificata.
- Irradiare topi NOG a 2,5 Gy a 6-24 ore prima del trapianto.
- Raccogliere gli HSC coltivati in tubi da 1,5 ml. Centrifugare i tubi a 340 ×g per 5 min a 4°C.
- Aspirare con cura i supernaganti e rimorsi le cellule in tampone sterile di colorazione ghiacciata a una densità cellulare di 5000 HSC (equivalente giorno 0) per 200 μL. Trasferire questa sospensione a tubi in polipropilene da 3 ml. Per sterilizzare il tampone di colorazione, filtrarlo utilizzando un filtro da 0,22 μm.
- Prima del trapianto, anestetizza i topi per inalazione di sevoflurane o isoflurane.
- Per trapiantare 5000 HSC coltivati (equivalente giorno 0), iniettare 200 μL della sospensione cellulare nella vena della coda o nel seno orbitale retrò dei topi NOG irradiati nella fase 7.1 utilizzando una siringa da 1 ml e un ago calibro 27. Gli HSC del midollo osseo appena isolati o scongelati possono essere trapiantati come controllo. I guanti devono essere sterilizzati con 70% v/v etanolo tra ogni procedura.
8. Analisi della frequenza delle cellule di origine umana nel sangue periferico
- Per esaminare il ripopolamento delle cellule umane, raccogliere il sangue periferico a 1, 2 e 3 mesi dopo il trapianto.
- Prima di raccogliere il sangue periferico, anestetizzare i topi per inalazione di sevoflurane.
- Raccogliere 40-80 μL di sangue periferico dal seno retro-orbitale utilizzando tubi capillari di vetro eparinizzato e sospendere questo campione in 1 ml di PBS + eparina (1 U/mL) in tubi da 1,5 ml.
- Centrifugare la sospensione del sangue a 340 × g per 3 min a 4 °C. Scartare il supernatante e resospendare il pellet in 1 mL di PBS + 1,2% w/v dextran (200 kDa) per 45 min a temperatura ambiente.
- Trasferire il supernatante su un altro tubo da 1,5 ml e centrifugare a 340 × g per 3 min.
- Per lalisi dei globuli rossi, resuspend le cellule in 0,17 MNH 4Cl per 5 min.
- Centrifugare la sospensione cellulare 340 × g per 3 min a 4 °C. Rimondivare le cellule in 50 μL di tampone di colorazione contenente 0,3 μL di blocco Fc anti-mouse. Incubare questo campione a 4 °C per 5 min.
- Aggiungere i seguenti anticorpi per la colorazione marcatore di superficie: 0,3 μL di cd45-PE-Cy7 del mouse, 0,3 μL ter-119-PE-Cy7, 0,3 μL di CD45-BV421 umano, 0,3 μL di CD13-PE umano, 1,2 μL di CD33-PE umano, 0,3 μL di CD19-APC umano, 0,3 μL di CD3-APC-Cy7 umano. Incubare le cellule a 4 °C per 15 minuti.
- Lavare una volta con 1 mL di tampone di colorazione e centrifuga a 340 × g per 5 min a 4 °C.
- Scartare il supernatante e resospendare le cellule in 200 μL di tampone di colorazione + 0,1% v/v di PI.
- Trasferire la sospensione cellulare su una piastra a fondo piatto da 96 po 'e acquisire dati utilizzando il citometro di flusso in modalità rapida con la modalità del campione mix attiva e un volume di assorbimento di 100 μL.
- Esportare i dati in formato FCS per l'analisi utilizzando software come FlowJo.
- Impostare il citometro di flusso. Acquisire i dati per i campioni in modalità rapida con la modalità campione mix e un volume di assorbimento di 100 μL.
- Esportare i dati in formato FCS per l'analisi utilizzando software come FlowJo.
Risultati
Dopo 7 giorni di ristrutturazione degli HSC purificati, fino all'80% delle celle ha visualizzato fenotipi marcatori di CD34+CD38- (Figura 4A). Il numero totale di cellule dipendeva dalla concentrazione di citochine (Figura 4B). Concentrazioni più elevate di SCF e TPO hanno indotto l'ingresso nel ciclo cellulare, la proliferazione e la differenziazione (figura 4B). Il numero di HSC fenotipi caratterizzati dai fenotipi marcatori di CD34+CD38-CD90+CD45RA- è aumentato in proporzione alle concentrazioni di SCF o TPO (Figura 4B), mentre la frequenza tra le cellule totali è diminuita (Figura 4C). Il numero totale di cellule era uguale nelle combinazioni 1,5 ng/mL SCF e 4 ng/mL TPO e 3 ng/mL SCF 3 e 2 ng/mL TPO, suggerendo che gli HSC sono quiescenti durante l'attivazione minima del ciclo cellulare. Date le differenze individuali, la titolazione della citochina è raccomandata per ogni donatore di midollo osseo.
Dopo 3 mesi di trapianto di HSC di midollo osseo adulto coltivato, la ricostituzione può essere valutata come la loro frequenza nel sangue periferico delle cellule CD45+ murine CD45- Ter119- umane. Tre lignaggi, tra cui le cellule CD19+ B, le cellule mieloidi CD13/CD33+ e le cellule T CD3+ sono stati ricostituiti in topi NOG trapiantati con HSC appena scongelati o HSC coltivati (Figura 5).
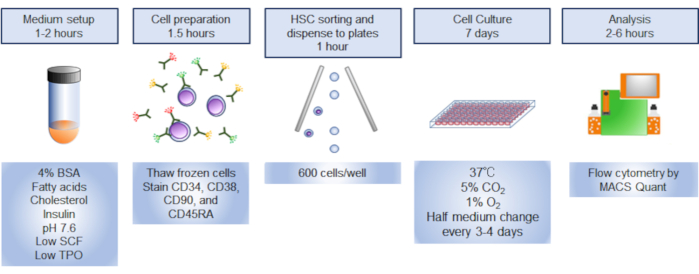
Figura 1. Panoramica della procedura. Il riassunto grafico della procedura prevedeva lo smistamento, la ristrutturazione e l'analisi delle cellule staminali ematopoietiche umane (HSC). Clicca qui per visualizzare una versione più grande di questa figura.
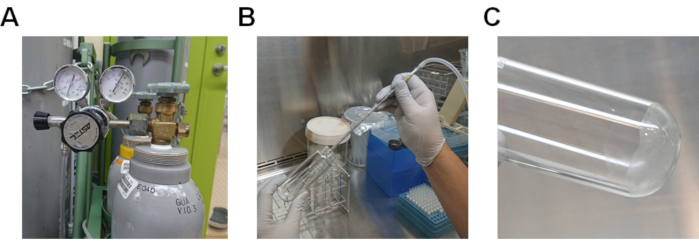
Figura 2. Procedura per evaporare il metanolo dalla soluzione lipidica. A) Bombola di gas azoto con regolatore di gas. B) Procedura per il passaggio del gas azoto attraverso la soluzione lipidica sciolta in metanolo. C) Lipidi che aderiscono al fondo del tubo di vetro. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3. Strategia di gating per lo smistamento degli HSC. I grafici mostrano celle GATED CD34+CD38-CD90+CD45RA . Circa il 10% delle celle CD34+ erano HSC fenotipiche. Fare clic qui per visualizzare una versione più ampia di questa figura.
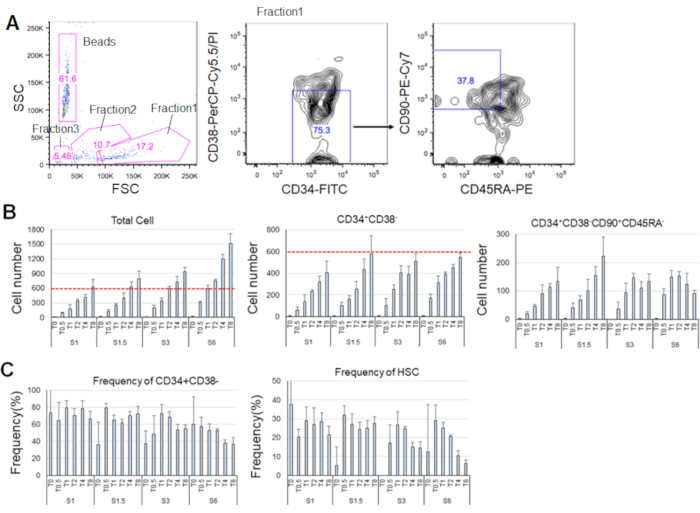
Figura 4. Numeri di cella rappresentativi dopo 7 giorni di ristrutturazione. A) Posto di smistamento cellulare rappresentativo attivato dalla fluorescenza dopo aver coltivato gli HSC in SCF (3 ng/mL) e TPO (2 ng/mL). La frazione 1 è stata arricchita per le cellule vive, la frazione 2 è stata arricchita per le cellule morte e la frazione 3 è stata arricchita per i detriti. I numeri colorati in rosa indicano la frequenza (%) della frazione recinta. B) Numero di tutte le celle HSC, CD34+CD38- celle e CD34+CD38-CD90+CD45RA- dopo aver coltivato 600 HSC nelle condizioni di citochina indicate. Le linee tratteggiate rosse indicano il numero iniziale di celle di input. S: SCF, T: TPO. Media ± deviazione standard, n = 4. I numeri successivi a S e T indicano la concentrazione (ng/mL) di ogni citochina. C) Frequenza di CELLULE CD34+CD38- e CD34+CD38-CD90+CD45RA- nelle condizioni citochine indicate. S: SCF, T: TPO. Media ± deviazione standard, n = 4. Le barre di errore per le celle coltivate in SCF (1 ng/mL) e TPO (0 ng/mL) sono state omesse a causa dei loro valori elevati (rispettivamente 37,7 e 47,9). Clicca qui per visualizzare una versione più grande di questa figura.
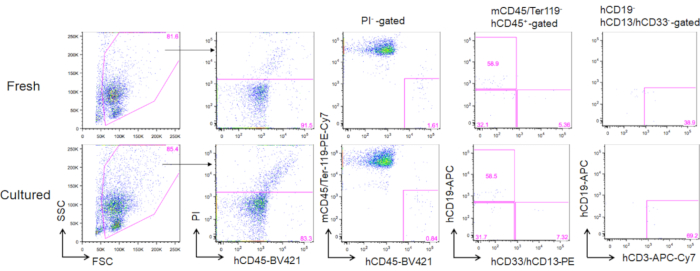
Figura 5. Grafici FACS rappresentativi di topi donatori dopo 3 mesi di trapianto. Un totale di 5000 HSC coltivati al tempo fresco (pannelli superiori) e 2 settimane coltivati (3 ng/mL SCF e 3 ng/mL TPO; pannelli inferiori) sono stati trapiantati in topi NOG. hCD19 contrassegna le cellule B umane, hCD13 e hCD33 contrassegnano le cellule mieloidi umane e hCD3 contrassegna le cellule T umane. Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Recentemente, sono stati segnalati diversi metodi per espandere gli HSC con differenziazioneminima 18,19,20,21. Sebbene questi metodi siano eccellenti, gli HSC sono costretti ad attivare i loro cicli cellulari in presenza di alti livelli di citochine, che differisce dalla situazione in vivo in cui gli HSC mostrano un ciclo minimo. Questo protocollo è utile per mantenere gli HSC quiescenti, come osservato in vivo, ricapitolando il microambiente del midollo osseo.
Coltivando gli HSC umani in condizioni basse di citochine, ricche di lipidi e ipossiche, gli HSC hanno mostrato un ciclo minimo mantenendo i loro fenotipi marcatori. Il passo critico in questo protocollo è la preparazione di mezzi contenenti un'alta concentrazione di acidi grassi e colesterolo e basse concentrazioni e coltura di citochine sotto ipossia (Fase 1, Fase 2 e Fase 4). Senza colesterolo e/o acidi grassi, il tasso di mantenimento degli HSC a basse concentrazioni di citochine diminuiscedi 22. Anche la coltivazione di cellule in condizioni ipossiche è importante, come riportato in precedenza23.
Le condizioni di coltura erano simili a quelle utilizzate per gli HSC murini, ad eccezione delle concentrazioni di citochine. Gli HSC murini sopravvivono senza TPO, mentre gli HSC umani richiedono almeno 2 ng/mL di TPO con 3 ng/mL di SCF22. Poiché la concentrazione di TPO è molto più alta di quella nel siero umano (~100 pg/mL), le condizioni utilizzate in questo protocollo possono mancare di fattori specifici per sostenere la sopravvivenza degli HSCumani. L'aggiunta del ligando FLT3LG riduce leggermente il requisito per TPO di mantenere gli HSC22.
Gli HSC umani richiedono concentrazioni più elevate di colesterolo rispetto agli HSC murini, presumibilmente a causa dell'incapacità di indurre l'espressione di enzimi sintetizzativi del colesterolo e della suscettibilità alla lipotossicità sotto alte concentrazioni (>400 μg/mL) di acidi grassi22. Sebbene sia stata testata solo la combinazione di acidi palmitico, oleico, linoleico e stearico, che si trovano abbondantemente nel siero umano, altre combinazioni di lipidi dovrebbero essere valutate per ridurre la lipotossicità e migliorare il tasso di mantenimento degli HSC funzionali.
Sebbene l'attività di ripopolamento degli HSC umani coltivati nei topi immunodifesa dopo due settimane dicoltura sia stata confermata 22, questo sistema di coltura non riassume completamente le funzioni di nicchia degli HSC in vivo. Si è riferito che l'espressione di CD45RA aumenta e la capacità di ripopolamento è inferiore a quella degli HSC appena ordinati22. Tuttavia, le concentrazioni di sostanze nutritive, come glucosio, amminoacido, piruvato e insulina, che vengono aggiunte al mezzo a livelli sovrafisiologici, possono essere ottimizzate. I contaminanti in BSA possono anche compromettere il mantenimento degli HSC18,25. Inoltre, alcune cellule coltivate subiscono la morte cellulare, mentre altre subiscono la divisione cellulare; pertanto, il mantenimento del numero totale di cellule potrebbe non indicare lo stato quiescente di ciascuna cella.
Nonostante questi limiti, le condizioni culturali descritte nel protocollo sviluppato nel presente studio aiuteranno a far progredire la ricerca e l'ingegneria degli HSC, in particolare in condizioni quasi fisiologiche. Le condizioni colturali che mantengono gli HSC con una differenziazione minima e l'attività ciclistica sarebbero adatte per testare composti biologici e chimici che agiscono specificamente sugli HSC, manipolare gli HSC attraverso la trasduzione del lentivirus o l'editing del genoma senza la perdita di staminali e chiarire il passo iniziale di trasformazione indotto dai geni associati alla leucemia.
Divulgazioni
Gli autori non dichiarano alcun conflitto di interessi associato a questo studio.
Riconoscimenti
Ringraziamo M. Haraguchi e S. Tamaki per il supporto tecnico e la gestione di laboratorio e K. Shiroshita per aver scattato fotografie. HK è stato sostenuto in parte dalla sovvenzione KAKENHI di MEXT/JSPS (sovvenzione n. 19K17847) e dal National Center for Global Health and Medicine. KT è stato sostenuto in parte da sovvenzioni KAKENHI di MEXT/JSPS (sovvenzioni n. 18H02845 e 18K19570), Centro nazionale per la salute e la medicina globale (sovvenzioni n. 26-001 e 19A2002), AMED (n. sovvenzione). JP18ck0106444, JP18ae0201014 e JP20bm0704042), Ono Medical Research Foundation, Kanzawa Medical Research Foundation e Takeda Science Foundation.
Materiali
| Name | Company | Catalog Number | Comments |
| Human bone marrow CD34+ progenitor cells | Lonza | 2M-101C | |
| NOD/Shi-scid,IL-2RγKO Jic | In-Vivo Science Inc. | https://www.invivoscience.com/en/nog_mouse.html | |
| Anti-human CD34-FITC (clone: 581) | BD biosciences | Cat# 560942; RRID: AB_10562559 | |
| Anti-human CD38-PerCP-Cy5.5 | BD biosciences | Cat# 551400; RRID: AB_394184 | |
| Anti-human CD45RA-PE | BD biosciences | Cat# 555489; RRID: AB_395880 | |
| Anti-human CD90-PE-Cy7 (clone: 5E10) | BD biosciences | Cat# 561558; RRID: AB_10714644 | |
| Anti-human CD13-PE (clone: WM15) | BioLegend | Cat# 301703; RRID: AB_314179 | |
| Anti-human CD33-PE (clone: WM53) | BD biosciences | Cat# 561816; RRID: AB_10896480 | |
| Anti-human CD19-APC (clone: SJ259) | BioLegend | Cat# 363005; RRID: AB_2564127 | |
| Anti-human CD3-APC-Cy7 (clone: SK7) | BD biosciences | Cat# 561800; RRID: AB_10895381 | |
| Anti-human CD45-BV421 (clone: HI30) | BD biosciences | Cat# 563880; RRID:AB_2744402 | |
| Anti-mouse CD45-PE-Cy7 (clone: 30-F11) | BioLegend | Cat# 103114; RRID: AB_312979 | |
| Anti-mouse Ter-119-PE-Cy7 (clone: TER-119) | BD biosciences | Cat# 557853; RRID: AB_396898 | |
| Fc-block (anti-mouse CD16/32) (clone: 2.4-G2) | BD Biosciences | Cat# 553142; RRID: AB_394657 | |
| Phosphate buffered saline | Nacalai Tesque | Cat# 14249-24 | |
| Fetal bovine serum | Thermo Fisher Scientific | Cat# 26140079 | |
| DMEM/F-12 medium | Thermo Fisher Scientific | Cat# 11320-033 | |
| ITS-X | Thermo Fisher Scientific | Cat# 51500056 | |
| Penicillin | Meiji Seika | PGLD755 | |
| Streptomycin sulfate | Meiji Seika | SSDN1013 | |
| Bovine serum albumin | Sigma Aldrich | Cat# A4503 | |
| Sodium palmitate | Tokyo Chemical Industry Co., Ltd. | Cat# P0007 | |
| Sodium oleate | Tokyo Chemical Industry Co., Ltd. | Cat# O0057 | |
| Cholesterol | Tokyo Chemical Industry Co., Ltd. | Cat# C0318 | |
| Ammonium Chloride | Fujifilm | Cat# 017-2995 | |
| Sodium Hydrogen Carbonate | Fujifilm | Cat# 191-01305 | |
| EDTA 2Na | Fujifilm | Cat# 345-01865 | |
| Heparine Na | MOCHIDA PHARMACEUTICAL CO., LTD. | Cat# 224122557 | |
| Sevoflurane | Fujifilm | Cat# 193-17791 | |
| Dextran | Nacalai Tesque | Cat# 10927-54 | |
| Recombinant Human SCF | PeproTech | Cat# 300-07 | |
| Recombinant Human TPO | PeproTech | Cat# 300-18 | |
| Recombinant human Flt3 ligand | PeproTech | Cat# 300-19 | |
| Propidium iodide | Life Technologies | Cat# P3566 | |
| Flow-Check Fluorospheres | Beckman Coulter | Cat# 7547053 | |
| FlowJo version 10 | BD Biosciences | https://www.flowjo.com/solutions/flowjo | |
| AutoMACS Pro | Miltenyi Biotec | N/A | |
| FACS Aria3u | BD Biosciences | N/A | |
| VELVO-CLEAR VS-25 (sonicator) | VELVO-CLEAR | N/A | |
| Nitrogen gas cylinder | KOIKE SANSHO CO., LTD | N/A | |
| Gas regulator | Astec | Cat# IM-055 | |
| Multigas incubator | Astec | Cat# SMA-30DR | |
| Glass tube, 16 mL | Maruemu corporation | N-16 | |
| Glass tube, 50 mL | Maruemu corporation | NX-50 | |
| Millex-GP Syringe Filter Unit, 0.22 µm, polyethersulfone, 33 mm, gamma sterilized | Merck Millipore | SLGPR33RS |
Riferimenti
- Scala, S., Aiuti, A. In vivo dynamics of human hematopoietic stem cells: novel concepts and future directions. Blood Advances. 3 (12), 1916-1924 (2019).
- Trumpp, A., Essers, M., Wilson, A. Awakening dormant haematopoietic stem cells. Nature Reviews Immunology. 10 (3), 201-209 (2010).
- Laurenti, E., Gottgens, B. From haematopoietic stem cells to complex differentiation landscapes. Nature. 553 (7689), 418-426 (2018).
- Sun, J., et al. Clonal dynamics of native haematopoiesis. Nature. 514 (7522), 322-327 (2014).
- Busch, K., et al. Fundamental properties of unperturbed haematopoiesis from stem cells in vivo. Nature. 518 (7540), 542-546 (2015).
- Lee-Six, H., et al. Population dynamics of normal human blood inferred from somatic mutations. Nature. 561 (7724), 473-478 (2018).
- Osorio, F. G., et al. Somatic Mutations Reveal Lineage Relationships and Age-Related Mutagenesis in Human Hematopoiesis. Cell Reports. 25 (9), 2308-2316 (2018).
- Rodriguez-Fraticelli, A. E., et al. Clonal analysis of lineage fate in native haematopoiesis. Nature. 553 (7687), 212-216 (2018).
- Pineault, N., Abu-Khader, A. Advances in umbilical cord blood stem cell expansion and clinical translation. Experimental Hematology. 43 (7), 498-513 (2015).
- Wilkinson, A. C., Igarashi, K. J., Nakauchi, H. Haematopoietic stem cell self-renewal in vivo and ex vivo. Nature Reviews Genetics. 21 (9), 541-554 (2020).
- Wagner, J. E., et al. Phase I/II Trial of StemRegenin-1 Expanded Umbilical Cord Blood Hematopoietic Stem Cells Supports Testing as a Stand-Alone Graft. Cell Stem Cell. 18 (1), 144-155 (2016).
- Cohen, S., et al. Hematopoietic stem cell transplantation using single UM171-expanded cord blood: a single-arm, phase 1-2 safety and feasibility study. Lancet Haematology. 7 (2), 134-145 (2020).
- Laurenti, E., et al. CDK6 levels regulate quiescence exit in human hematopoietic stem cells. Cell Stem Cell. 16 (3), 302-313 (2015).
- Ito, K., Suda, T. Metabolic requirements for the maintenance of self-renewing stem cells. Nature Reviews Molecular Cell Biology. 15 (4), 243-256 (2014).
- Mendelson, A., Frenette, P. S. Hematopoietic stem cell niche maintenance during homeostasis and regeneration. Nature Medicine. 20 (8), 833-846 (2014).
- Majeti, R., Park, C. Y., Weissman, I. L. Identification of a hierarchy of multipotent hematopoietic progenitors in human cord blood. Cell Stem Cell. 1 (6), 635-645 (2007).
- Xie, W., et al. Detection of molecular targets on the surface of CD34+CD38- bone marrow cells in myelodysplastic syndromes. Cytometry A. 77 (9), 840-848 (2010).
- Wilkinson, A. C., et al. Long-term ex vivo haematopoietic-stem-cell expansion allows nonconditioned transplantation. Nature. 571 (7763), 117-121 (2019).
- Bai, T., et al. Expansion of primitive human hematopoietic stem cells by culture in a zwitterionic hydrogel. Nature Medicine. 25 (10), 1566-1575 (2019).
- Boitano, A. E., et al. Aryl hydrocarbon receptor antagonists promote the expansion of human hematopoietic stem cells. Science. 329 (5997), 1345-1348 (2010).
- Fares, I., et al. Cord blood expansion. Pyrimidoindole derivatives are agonists of human hematopoietic stem cell self-renewal. Science. 345 (6203), 1509-1512 (2014).
- Kobayashi, H., et al. Environmental Optimization Enables Maintenance of Quiescent Hematopoietic Stem Cells Ex Vivo. Cell Reports. 28 (1), 145-158 (2019).
- Danet, G. H., Pan, Y., Luongo, J. L., Bonnet, D. A., Simon, M. C. Expansion of human SCID-repopulating cells under hypoxic conditions. Journal of Clinical Investigation. 112 (1), 126-135 (2003).
- Kikushige, Y., et al. Human Flt3 is expressed at the hematopoietic stem cell and the granulocyte/macrophage progenitor stages to maintain cell survival. Journal of Immunology. 180 (11), 7358-7367 (2008).
- Ieyasu, A., et al. An All-Recombinant Protein-Based Culture System Specifically Identifies Hematopoietic Stem Cell Maintenance Factors. Stem Cell Reports. 8 (3), 500-508 (2017).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon