È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Ecografia Endobronchiale Radiale e Broncoscopia a Navigazione Elettromagnetica con Fluoroscopia per la Diagnosi delle Lesioni Polmonari Perifere
In questo articolo
Riepilogo
La diagnosi di piccoli tumori polmonari è piuttosto difficile utilizzando un broncoscopio da solo. La broncoscopia a navigazione elettromagnetica viene utilizzata per localizzare la lesione, in modo simile al sistema di posizionamento globale. L'ecografia endobronchiale radiale e la fluoroscopia confermano la posizione corretta e monitorano il prelievo.
Abstract
La diagnosi del cancro ai polmoni utilizzando un broncoscopio flessibile è una procedura sicura con un rischio molto basso di complicanze. La broncoscopia ha un'elevata accuratezza diagnostica per le lesioni endobronchiali, ma non è all'altezza del campionamento delle lesioni periferiche. Pertanto, sono state inventate diverse modalità per guidare il broncoscopio verso la lesione e confermare la posizione del tumore prima del campionamento dei tessuti.
La fluoroscopia viene utilizzata durante la broncoscopia per fornire un'immagine a raggi X 2D del torace durante la procedura. Il broncoscopio e gli strumenti saranno visibili, così come le lesioni se più grandi di 2,0-2,5 cm. L'ecografia endobronchiale radiale (rEBUS) consiste in una sonda ecografica, abbastanza piccola da essere inserita nel canale di lavoro del broncoscopio. La sonda ecografica viene utilizzata per distinguere tra tessuto consolidato, come il tessuto tumorale, e il normale parenchima polmonare pieno d'aria. La broncoscopia a navigazione elettromagnetica (ENB) crea un modello 3D dell'albero bronchiale da scansioni di tomografia computerizzata (TC) del paziente. Prima della broncoscopia, viene pianificato un percorso dalla trachea alla lesione, per creare una guida in tempo reale del broncoscopio verso la lesione durante la procedura, in modo simile al sistema di posizionamento globale. Lo scopo di questo articolo è quello di descrivere un approccio graduale all'esecuzione della broncoscopia con rEBUS e fluoroscopia, broncoscopia con ENB, rEBUS e fluoroscopia. Nella sezione di discussione verranno discussi i pro e i contro di ciascuna modalità.
Introduzione
Il cancro ai polmoni è uno dei tipi di cancro più comuni in tutto il mondo e la principale causa di decessi correlati al cancro1. È stato quindi suggerito lo screening per il cancro del polmone con tomografia computerizzata (TC) a basso dosaggio per diagnosticare i pazienti prima che si manifestinoi sintomi 2. Gli stadi bassi sono spesso rilevati come piccole lesioni polmonari o noduli. Da uno dei più grandi studi di screening condotti nei Paesi Bassi, sappiamo che queste lesioni sono spesso localizzate nei 2/3 esterni del parenchima polmonare e sono quindi definite come tumori polmonari periferici 3,4. Per determinare se una lesione è maligna, è necessario un campione di tessuto. Questo può essere ottenuto in diversi modi come la biopsia chirurgica per escissione, la biopsia con ago trans-toracico o l'endoscopia con broncoscopio 5,6, quest'ultima con un minor rischio di complicanze rispetto alla chirurgia e all'approccio trans-toracico e un metodo preferibile per diagnosticare una popolazione anziana in aumento con notevoli comorbidità. La resa diagnostica, tuttavia, è ancora inferiore rispetto alle altre modalità5.
Il broncoscopio consente l'ispezione visiva della trachea e dei bronchi principali, ma quando i bronchi si ramificano in segmenti e sottosegmenti, localizzare una piccola lesione è paragonabile a trovare un ago in un pagliaio. Pertanto, sono state sviluppate diverse modalità aggiuntive per guidare il broncoscopio verso la lesione e confermare la posizione di un tumore prima del campionamento dei tessuti7. Lo scopo di queste modalità è quello di aumentare la resa diagnostica del prelievo endoscopico di tessuto ed espandere la portata del broncoscopio verso la pleura, dove altrimenti vengono eseguite agobiopsie trans-toraciche 8,9.
La fluoroscopia con arco a C fornisce un'immagine a raggi X 2D del torace durante la broncoscopia. Può essere utilizzato per visualizzare la posizione del broncoscopio e delle pinze per le biopsie transbronchiali (TBB) per evitare di campionare la pleura e le strutture vascolari del 1/3 intermedio del parenchima polmonare quando si eseguono TBB casuali. Quando si diagnostica il cancro del polmone, la fluoroscopia può essere utilizzata per guidare l'endoscopio verso una posizione "approssimativa" della lesione. Le lesioni sono solitamente visibili alla fluoroscopia quando il diametro è di circa 2-2,5 cm o superiore a10. Lo svantaggio della fluoroscopia sono le proprietà dell'immagine 2D, che rendono impossibile sapere se l'endoscopio si trova davanti, dietro o al centro della lesione11. Tuttavia, la fluoroscopia viene utilizzata anche per confermare che gli strumenti per biopsia si trovino nella posizione desiderata durante il campionamento se la presenza di un tumore è stata confermata con l'ecografia endobronchiale radiale (rEBUS)12.
rEBUS è stato descritto per la prima volta nel 1992 da Hürter et al. ed è sempre più utilizzato nell'iter diagnostico delle lesioni polmonari periferiche13. Questa modalità sfrutta il fatto che il tessuto polmonare pieno d'aria non conduce onde ultrasoniche, mentre il tessuto più denso apparirà come un consolidamento quando viene scansionato utilizzando una sonda ecografica. rEBUS è composto da una sonda a ultrasuoni circolare e rotante, un'unità di azionamento a ultrasuoni e una guaina di guida utilizzata per proteggere la sonda garantendo al contempo la corretta posizione degli strumenti per biopsia14. rEBUS può essere utilizzato da solo o insieme ad altre modalità come la broncoscopia a navigazione elettromagnetica (ENB)15,16,17.
L'ENB viene utilizzato per localizzare una lesione polmonare periferica18. Il sistema utilizza un programma software e una TAC del paziente. Dalla TAC viene generato un modello virtuale delle vie aeree del paziente e l'operatore disegna un percorso dalla trachea alla lesione. Viene quindi creato un campo elettromagnetico intorno al torace del paziente e il software sincronizza questo campo con il campo virtuale generato dalla TAC, aiutando così l'operatore a seguire il percorso prepianificato durante la broncoscopia, in modo simile alla tecnologia Global Positioning System. ENB non fornisce conferme in tempo reale della localizzazione del tumore. ENB può essere combinato con la fluoroscopia e rEBUS19,20. Virtual Navigation Bronchoscopy (VBN) è il predecessore di ENB e consiste in un software per la creazione del modello virtuale dell'albero bronchiale insieme a un percorso verso la lesione. Il sistema non include la navigazione in tempo reale, ma il percorso può essere visualizzato durante la broncoscopia21,22. I nuovi sistemi incorporano VBN con la fluoroscopia, ma l'uso di VBN non sarà descritto nel seguente protocollo23.
Sistemi ENB
Attualmente, due aziende producono sistemi per ENB, il sistema SPiN di Olympus e il sistema superDimension e l'ILLUMISITE, entrambi venduti da Medtronic. Il protocollo descriverà una procedura che utilizza il sistema superDimension, che attualmente ha il maggior numero di pubblicazioni. Tuttavia, molte fasi della procedura sono intercambiabili.
Il seguente protocollo descriverà come eseguire rEBUS in fluoroscopia e ENB + rEBUS in fluoroscopia in ambito clinico. Le procedure possono essere facilmente eseguite in sedazione cosciente e anestesia generale. Il protocollo non descriverà alcun metodo per la sedazione. Nella sezione di discussione verranno presentati i pro e i contro di ciascuna procedura.
Access restricted. Please log in or start a trial to view this content.
Protocollo
Il protocollo in questo articolo descrive la pratica clinica standard. Non è stata necessaria alcuna autorizzazione da parte del comitato etico. Le immagini nel protocollo non contengono informazioni che possono essere utilizzate per identificare i pazienti.
1. Ecografia endobronchiale radiale
- Preparazione per la procedura
- Esaminare la TAC per verificare la presenza di segni di bronco e la posizione della lesione prima della procedura.
- Calibrare la sonda ecografica, la guaina guida e gli strumenti per biopsia scelti prima dell'esame, assicurandosi che lo strumento raggiunga la stessa posizione della sonda ecografica quando viene inserito nella guaina guida.
- Eseguire un esame sistematico dell'albero bronchiale e dei segmenti come descritto in "Broncoscopia sistematica: l'approccio dei 4 punti di riferimento"24.
- Posizionare l'arco a C sul paziente e regolarlo fino a quando la lesione non è visibile nell'immagine.
- Inserire la punta del broncoscopio nel segmento o sottosegmento in cui è più probabile che sia presente la lesione.
- Far avanzare la guaina guida e la sonda sotto la guida della fluoroscopia fino a quando la punta del foglio guida metallico non è adiacente o all'interno della lesione.
- Avanzare e attivare la sonda. Ora sul monitor apparirà un'immagine ecografica.
- Se la sonda è circondata da un tumore o da un tessuto denso, apparirà un consolidamento concentrico (vedi Figura 1A). Cerca un consolidamento grigio e omogeneo con un bordo iperecogeno verso il tessuto polmonare normale.
- Se la sonda è posizionata adiacente alla lesione, l'immagine sarà eccentrica (vedi Figura 1B).
- Se la sonda è posizionata nel tessuto polmonare normale, apparirà solo un'immagine sparsa di aria (vedere Figura 1C).
- Con lesioni meno dense come lesioni a vetro smerigliato, tessuto infiammatorio o atelettasia, verrà presentata un'immagine più eterogenea e meno definita (vedi Figura 1D). Ciò è causato da aria (iperecogena) o fluido (ipoecogeno) intrappolati nei bronchi.
- Se non si verifica un consolidamento corrispondente alla lesione sulla TAC, regolare la guaina guida e la sonda fino a ottenere il posizionamento corretto.
- Salvare l'immagine fluoroscopica della posizione in cui la sonda ecografica fornisce il miglior consolidamento (verrà utilizzata nel passaggio 1.3.2).
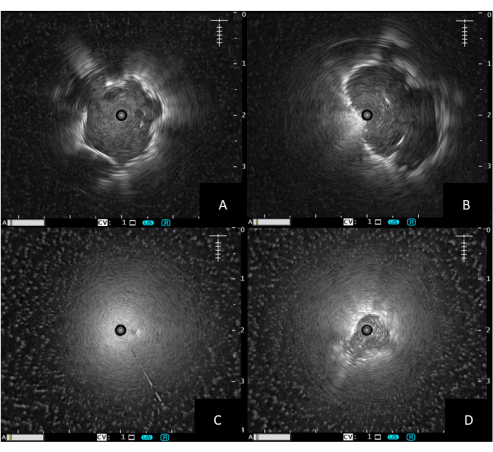
Figura 1: Immagini ecografiche EBUS radiali. (A) Consolidamento concentrico, (B) Consolidamento eccentrico, (C) Immagine ecografica diffusa in aria, (D) Consolidamento irregolare. Abbreviazione: EBUS = ecografia endobronchiale. Clicca qui per visualizzare una versione più grande di questa figura.
- Prelievo di tessuti
- Rimuovere la sonda ecografica dalla guaina di guida e inserire una pinza o un altro strumento di campionamento a scelta.
- Confrontare il posizionamento della pinza con il posizionamento della sonda ecografica sullo schermo dell'arco a C, assicurandosi che il campionamento venga eseguito nella posizione corretta (vedere la Figura 2). Verificare il posizionamento del forcipe, soprattutto se il paziente tossisce. Raccogliere un minimo di 10-15 campioni utilizzando una pinza e confermare la posizione corretta rimuovendo la pinza e inserendo la sonda ecografica ogni quattro o cinque campioni.
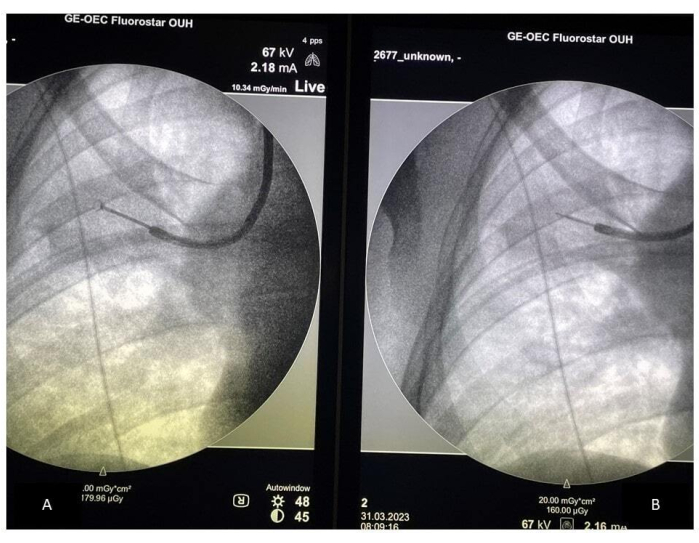
Figura 2: Campionamento guidato dalla fluoroscopia. (A) Posizionamento della pinza durante il campionamento; (B) Posizionamento della sonda rEBUS. Abbreviazione: rEBUS = ecografia endobronchiale radiale. Clicca qui per visualizzare una versione più grande di questa figura.
2. Broncoscopia a navigazione elettromagnetica
NOTA: La seguente procedura si basa sul sistema superDimension di Medtronic.
- La fase di pianificazione
- Prima della procedura, valutare le immagini TC. Assicurarsi che l'immagine sia di alta qualità, preferibilmente con fette non più spesse di 1,5 mm, e registrata durante l'inspirazione per espandere completamente le vie aeree rivelando i bronchi che portano alla lesione25.
- Utilizzare il software per creare un modello 3D dell'albero bronchiale, dove viene pianificato il percorso verso la lesione, partendo dalla lesione e spostandosi verso la trachea.
NOTA: Se non è possibile stabilire un percorso verso la lesione sulla base delle scansioni, l'ENB non è la modalità corretta per il paziente.
- Registrazione
- Posizionare il paziente su una tavola. Posizionare i tre sensori sul torace per compensare i movimenti durante la respirazione.
- Iniziare la procedura con una broncoscopia sistematica24.
- Inserire il canale di lavoro esteso (EWC) e la guida localizzabile nel canale di lavoro del broncoscopio finché la punta della guida localizzabile non è visibile.
- Bloccare la guida localizzabile.
- Premere Avvia registrazione sulla macchina o utilizzare il pedale.
- Inserire il broncoscopio gradualmente in ciascun bronco lobare, iniziando controlateralmente e terminando nel lobo con la lesione. La posizione e i movimenti vengono registrati dal sistema e le informazioni vengono utilizzate per abbinare la registrazione delle vie aeree del paziente al modello 3D dell'albero bronchiale creato sulla base della TAC. Inizia la registrazione sul lato opposto alla lesione e termina il più vicino al bersaglio.
- Quando il sistema mostra che tutti i lobi sono registrati, premere Rivedi registrazione per vedere se i punti di registrazione corrispondono al modello 3D virtuale. In caso di mancata corrispondenza, ripetere i passaggi 2.2.5-2.2.7 (vedere la Figura 3D).
- Navigazione
- Premere il pedale per iniziare la navigazione. Il software mostrerà un percorso verso l'obiettivo. Utilizzare la navigazione centrale nelle vie aeree più grandi, visualizzando l'immagine video della telecamera insieme a un'immagine del percorso nel modello 3D delle vie aeree (vedere la Figura 3A).
- Seguire il percorso pianificato fino a quando non è possibile avanzare ulteriormente nell'oscilloscopio.
- Sblocca il CAE e la guida localizzabile.
- Passa dalla navigazione centrale alla navigazione periferica premendo il pedale.
NOTA: La navigazione periferica viene utilizzata durante l'avanzamento del CAE. Durante questa parte, il modello 3D delle vie aeree è visibile insieme alle immagini TC della scansione. Il bersaglio è contrassegnato da una palla verde e da un reticolo, che fornisce la direzione e la distanza dal bersaglio (vedi Figura 3B). - Mantenere il bersaglio sul lato destro assicurandosi che il percorso sia illuminato ("giusto e luminoso"). Far avanzare il CAE, assicurandosi che il percorso verso i bronchi appaia aperto sulle immagini TC.
NOTA: L'EWC è manovrabile e può essere ruotato nella direzione desiderata (assi X, Y e Z) per raggiungere il bersaglio. - Una volta che il bersaglio si trova al centro del reticolo, con una distanza di 0,4-0,9 mm dal bersaglio, la navigazione è completa.
NOTA: Si raccomanda che la guida localizzabile non si trovi a 0,0 mm dalla distanza, poiché ciò può causare l'estensione dello strumento per biopsia oltre il bersaglio. - Bloccare il CER in posizione e ritrarre la guida localizzabile dal cannocchiale.

Figura 3: Navigazione elettromagnetica Navigazione broncoscopica. (A) Navigazione centrale, (B) Navigazione periferica, (C) Registrazione di revisione con un buon allineamento, (D) TC a divergenza corporea. Abbreviazione: CT = tomografia computerizzata. Clicca qui per visualizzare una versione più grande di questa figura.
3. Fluoroscopia, rEBUS e campionamento dei tessuti
NOTA: Una volta retratta la guida localizzabile, la fluoroscopia può essere utilizzata senza disturbare il campo elettromagnetico.
- Posizionare l'arco a C sul paziente e regolarlo fino a quando la lesione non è visibile nell'immagine.
- Confermare la corretta posizione dell'EWC utilizzando la fluoroscopia e inserendo la sonda rEBUS come descritto al punto 1.2.5. Se l'EWC non si trova nella lesione sottoposta a fluoroscopia o non appare un consolidamento utilizzando rEBUS, la posizione deve essere regolata come descritto nei passaggi 1.2.4-1.2.6.
NOTA: La divergenza CT-corpo si verifica quando l'allineamento tra il modello 3D costruito e i punti di registrazione in tempo reale è distorto; Il bersaglio contrassegnato non sarà nella posizione della lesione. - Una volta raggiunta e confermata la posizione corretta, eseguire il campionamento dei tessuti come descritto nei passaggi 1.3.1-1.3.2.
Access restricted. Please log in or start a trial to view this content.
Risultati
La tecnica descritta facilita il campionamento delle lesioni polmonari periferiche. L'EBUS radiale e la fluoroscopia aiuteranno il broncoscopista a confermare la presenza di una lesione prima del campionamento del tumore (vedi Figura 1 e Figura 2). Aggiungendo ENB, il broncoscopista viene guidato nel punto corretto invece di cercare la lesione. La fase di pianificazione fornisce al broncoscopista un percorso verso la lesione, un...
Access restricted. Please log in or start a trial to view this content.
Discussione
Questo articolo presenta un approccio pratico per l'esecuzione di rEBUS ed ENB con fluoroscopia. La seguente discussione è l'opinione degli autori e si basa sull'esperienza clinica pratica di due centri.
Suggerimenti e trucchi
rebus
Prima delle procedure, l'app Chest CT sectional walker può essere utilizzata per verificare in quale segmento si trova la lesione14. Tuttavia, poiché l'anatomia de...
Access restricted. Please log in or start a trial to view this content.
Divulgazioni
Medtronic ha gentilmente prestato l'attrezzatura ENB al Centro di Simulazione dell'Ospedale Universitario di Odense, per uno studio condotto da A. Juul. Medtronic non ha partecipato alla stesura di questo articolo
Riconoscimenti
Gli autori desiderano ringraziare tutti i broncoscopisti del Dipartimento di Medicina Respiratoria dell'Ospedale Universitario di Odense per aver fornito le immagini per l'articolo.
Access restricted. Please log in or start a trial to view this content.
Materiali
| Name | Company | Catalog Number | Comments |
| Bronchoschope | Olympus | ||
| Edge Extended working channel | Medtronic | ||
| Edge locatable guide | Medtronic | ||
| Guide sheath kit | Olympus | ||
| OEC fluorostar | GE healthcare | C-arm for fluoroscopy | |
| Probe Driving Unit | Olympus | ||
| Radial EBUS probes | Olympus | ||
| superDimension | Medtronic | Navigation system |
Riferimenti
- Ferlay, J., et al. Cancer statistics for the year 2020: an overview. Int J Cancer. , (2021).
- Adams, S. J., et al. Lung cancer screening. Lancet. 401 (10374), 390-408 (2022).
- Horeweg, N., et al. Characteristics of lung cancers detected by computer tomography screening in the randomized NELSON trial. Am J Respir Crit Care Med. 187 (8), 848-854 (2013).
- Vilmann, P., et al. Combined endobronchial and oesophageal endosonography for the diagnosis and staging of lung cancer. Eur Resp J. 46 (1), 40-60 (2015).
- Schreiber, G., McCrory, D. C. Performance characteristics of different modalities for diagnosis of suspected lung cancer: summary of published evidence. Chest. 123, 115-128 (2003).
- Callister, M. E. J., et al. British Thoracic Society guidelines for the investigation and management of pulmonary nodules: accredited by NICE. Thorax. 70, (2015).
- Shulman, L., Ost, D. Advances in bronchoscopic diagnosis of lung cancer. Curr Opin Pulm Med. 13 (4), 271-277 (2007).
- Eberhardt, R., Gompelmann, D., Herth, F. J. Electromagnetic navigation in lung cancer: research update. Expert Rev Respir Med. 3 (5), 469-473 (2009).
- Han, Y., et al. Diagnosis of small pulmonary lesions by transbronchial lung biopsy with radial endobronchial ultrasound and virtual bronchoscopic navigation versus CT-guided transthoracic needle biopsy: A systematic review and meta-analysis. PLoS One. 13 (1), 0191590(2018).
- Deng, C., et al. Small lung lesions invisible under fluoroscopy are located accurately by three-dimensional localization technique on chest wall surface and performed bronchoscopy procedures to increase diagnostic yields. BMC Pulm Med. 16 (1), 166(2016).
- Sánchez-Font, A., et al. Endobronchial ultrasound for the diagnosis of peripheral pulmonary lesions. A controlled study with fluoroscopy. Arch Bronconeumol. 50 (5), 166-171 (2014).
- Tanner, N. T., et al. Standard bronchoscopy with fluoroscopy vs thin bronchoscopy and radial endobronchial ultrasound for biopsy of pulmonary lesions: a multicenter, prospective, randomized trial. Chest. 154 (5), 1035-1043 (2018).
- Hürter, T., Hanrath, P. Endobronchial sonography: feasibility and preliminary results. Thorax. 47 (7), 565-567 (1992).
- Zhang, L., Wu, H., Wang, G. Endobronchial ultrasonography using a guide sheath technique for diagnosis of peripheral pulmonary lesions. Endosc Ultrasound. 6 (5), 292-299 (2017).
- Song, J. Y., et al. Efficacy of combining multiple electromagnetic navigation bronchoscopy modalities for diagnosing lung nodules. J Clin Med. 11 (24), 7341(2022).
- Zheng, X., et al. A novel electromagnetic navigation bronchoscopy system for the diagnosis of peripheral pulmonary nodules: a randomized clinical trial. Ann Am Thorac Soc. 19 (10), 1730-1739 (2022).
- Sainz Zuñiga, P. V., Vakil, E., Molina, S., Bassett, R. L., Ost, D. E. Sensitivity of radial endobronchial ultrasound-guided bronchoscopy for lung cancer in patients with peripheral pulmonary lesions: an updated meta-analysis. Chest. 157 (4), 994-1011 (2020).
- Criner, G. J., et al. Interventional bronchoscopy. Am J Respir Crit Care Med. 202 (1), 29-50 (2020).
- Eberhardt, R., Anantham, D., Ernst, A., Feller-Kopman, D., Herth, F. Multimodality bronchoscopic diagnosis of peripheral lung lesions: a randomized controlled trial. Am J Respir Crit Care Med. 176 (1), 36-41 (2007).
- Folch, E. E., et al. Electromagnetic navigation bronchoscopy for peripheral pulmonary lesions: one-year results of the prospective, multicenter NAVIGATE study. J Thorac Oncol. 14 (3), 445-458 (2019).
- Asano, F., et al. A virtual bronchoscopic navigation system for pulmonary peripheral lesions. Chest. 130 (2), 559-566 (2006).
- Asano, F., et al. Virtual bronchoscopic navigation without X-ray fluoroscopy to diagnose peripheral pulmonary lesions: a randomized trial. BMC Pulm Med. 17 (1), 184(2017).
- Tsai, Y. M., Kuo, Y. S., Lin, K. H., Chen, Y. Y., Huang, T. W. Diagnostic performance of electromagnetic navigation versus virtual navigation bronchoscopy-guided biopsy for pulmonary lesions in a single institution: potential role of artificial intelligence for navigation planning. Diagnostics (Basel). 13 (6), 1124(2023).
- Cold, K. M., Vamadevan, A., Nielsen, A. O., Konge, L., Clementsen, P. F. Systematic bronchoscopy: the four landmarks approach). J Vis Exp. (196), (2023).
- Pritchett, M. A., Bhadra, K., Calcutt, M., Folch, E. Virtual or reality: Divergence between preprocedural computed tomography scans and lung anatomy during guided bronchoscopy. J Thorac Dis. 12 (4), 1595-1611 (2020).
- Ost, D. E., et al. Diagnostic yield and complications of bronchoscopy for peripheral lung lesions. Results of the AQuIRE Registry. Am J Resp Crit Care Med. 193 (1), 68-77 (2016).
- McGuire, A. L., Myers, R., Grant, K., Lam, S., Yee, J. The diagnostic accuracy and sensitivity for malignancy of radial-endobronchial ultrasound and electromagnetic navigation bronchoscopy for sampling of peripheral pulmonary lesions: Systematic review and meta-analysis. J Bronchology Interv Pulmonol. 27 (2), 106-121 (2020).
- Oki, M., et al. Guide sheath versus non-guide sheath method for endobronchial ultrasound-guided biopsy of peripheral pulmonary lesions: a multicentre randomised trial. Eur Respir J. 59 (5), 2101678(2022).
- Korevaar, D. A., et al. Added value of combined endobronchial and oesophageal endosonography for mediastinal nodal staging in lung cancer: a systematic review and meta-analysis. Lancet Respir Med. 4 (12), 960-968 (2016).
- Micames, C. G., McCrory, D. C., Pavey, D. A., Jowell, P. S., Gress, F. G. Endoscopic ultrasound-guided fine-needle aspiration for non-small cell lung cancer staging: A systematic review and metaanalysis. Chest. 131 (2), 539-548 (2007).
- Farr, A., et al. Endobronchial ultrasound: launch of an ERS structured training programme. Breathe. 12 (3), 217(2016).
- Bellinger, C., Poon, R., Dotson, T., Sharma, D. Lesion characteristics affecting yield of electromagnetic navigational bronchoscopy. Respir Med. 180, 106357(2021).
- Laursen, C. B., et al. Ultrasound-guided lung biopsy in the hands of respiratory physicians: diagnostic yield and complications in 215 consecutive patients in 3 centers. J Bronchology Interv Pulmonol. 23 (3), 220-228 (2016).
- Oki, M., et al. Value of adding ultrathin bronchoscopy to thin bronchoscopy for peripheral pulmonary lesions: A multicentre prospective study. Respirology. 28 (2), 152-158 (2023).
- McGuire, A. L., Myers, R., Grant, K., Lam, S., Yee, J. The diagnostic accuracy and sensitivity for malignancy of radial-endobronchial ultrasound and electromagnetic navigation bronchoscopy for sampling of peripheral pulmonary lesions: Systematic review and meta-analysis. J Bronchology Interv Pulmonol. 27 (2), 106-121 (2020).
- Folch, E. E., et al. Electromagnetic navigation bronchoscopy for peripheral pulmonary lesions: one-year results of the prospective, multicenter NAVIGATE study. J Thorac Oncol. 14 (3), 445-458 (2019).
- Pritchett, M. A., Bhadra, K., Calcutt, M., Folch, E. Virtual or reality: divergence between preprocedural computed tomography scans and lung anatomy during guided bronchoscopy. J Thorac Dis. 12 (4), 1595-1611 (2020).
- Dunn, B. K., et al. Evaluation of electromagnetic navigational bronchoscopy using tomosynthesis-assisted visualization, intraprocedural positional correction and continuous guidance for evaluation of peripheral pulmonary nodules. J Bronchology Interv Pulmonol. 30 (1), 16-23 (2023).
- Juul, A. D., et al. Does the addition of radial endobronchial ultrasound improve the diagnostic yield of electromagnetic navigation bronchoscopy? A systematic review. Respiration. 101 (9), 869-877 (2022).
- Silvestri, G. A., et al. An evaluation of diagnostic yield from bronchoscopy: the impact of clinical/radiographic factors, procedure type, and degree of suspicion for cancer. Chest. 157 (6), 1656-1664 (2020).
- Silvestri, G. A., et al. A bronchial genomic classifier for the diagnostic evaluation of lung cancer. N Engl J Med. 373 (3), 243-251 (2015).
- Rozman, A., Zuccatosta, L., Gasparini, S. Dancing in the dark. Respiration. 101 (9), 814-815 (2022).
- Casal, R. F., et al. What exactly is a centrally located lung tumor? Results of an online survey. Ann Am Thorac Soc. 14 (1), 118-123 (2016).
Access restricted. Please log in or start a trial to view this content.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon