このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
固体 CO2発生源としてドライアイスを使用して密閉容器で適度な圧力を達成します。
要約
ここで CO2の低-中程度の圧力の下で簡単な反応容器で反応を実行するためのプロトコルを提案する.反応は、単に高価なまたは複雑な機器やセットアップを必要とせず、完全にドライアイスの形で二酸化炭素を投与することによってさまざまな血管で実行できます。
要約
ここはドライアイスと適度な CO2圧力に軽度の下で反応を実行する一般的な方法が提示されます。この技術は、適度な圧力を達成するための特殊な装置の必要性がなくなるより専門的な設備とより丈夫な反応容器で高い圧力を達成するためにも使用することができます。反応の最後に、室温でのオープニングでバイアルを簡単に減圧されることができます。現在の例で CO2を推定演出グループとにアミン基板、有機金属反応中に酸化を防ぐ方法として提供しています。簡単に追加されるだけでなく演出のグループも削除されます、真空下で監督のグループを削除する広範な浄化のための必要があります。この戦略により、脂肪族アミンの安易な γ-C(sp3)-H arylation とさまざまな他のアミン系の反応に適用される可能性があります。
概要
通常、化学反応でガス状の化合物の使用が必要なは、特殊な機器と手順1,2。ベンチ スケールでのガスは高圧レギュレータ3を使用してタンクから直接追加できます。極低温条件4、5の下でガスを凝縮する代替方法です。役に立つ、これらの戦略はバルブは、同時に多数の反作用を実行のコストがかさむことができます特殊な圧リアクターの使用を必要です。これは、ため大きく率が低下スクリーニングどちらの反応で進むことができます。その結果、化学者は、別の方法を使用してこれらの化合物を導入することが望ましい発見したの。アンモニアは、これらの塩と無料アンモニア6弱い平衡を利用して、異なるアンモニウム カルボン酸塩を用いた反応に追加できます。還元は、H27のキャリアとしてギ酸アンモニウムまたはヒドラジンなどの化合物と可燃性の水素ガスの使用を回避するオレフィン ・ カルボニル、ニトロ基の還元反応の重要な戦略です。この地域に関心の別のガスは一酸化炭素8 -CO 生成されたその場で金属カルボニル錯体9,10から解放することができますまたはから脱力ルボニル化によって生成できる代わりにソースおよび formamides11,12,13またはクロロホルム14,15など。
この点で重要な開発を収めていない 1 つのガスは二酸化炭素16です。この理由の 1 つは、CO2を含む多くの変換も必要な高温高圧、したがって特殊な原子炉17,18に自動的に追いやられています。ただし反応触媒の開発の CO219,20,21,22の大気圧下でのこれらの反作用の多数を実行を容易にした最近の努力。我々 は最近、γ C (3sp) を仲介する二酸化炭素が使用する反応を発見した-脂肪族アミン23H arylation。この戦略は、アミド24,25,26,27,28, スルホンアミドを含む静的な演出グループアプローチの利点を結合する期待されていた29,30,31,ヒドラゾン35やチオカルボニル33,34, 32-基づく一時的な演出グループ(減少ステップ経済)36、併せてグループ (化学 robusticity) を演出 37,38,39。
反応は、CO2の大気圧下で発生する可能性が、Schlenk 設定画面の反応が非常に証明の必要性が低下します。さらに、わずかに導いた圧力を増加させる反応収率の向上が簡単に達成できなかったシュレンク管を使用します。我々 したがって代替戦略を求められて、その後識別そのドライアイス簡単に使用できるさまざまな中等度を達成するために炭酸ガスの必要量を導入する反応容器に追加できる CO2の固体ソースとして圧力 (図 1)。同様の戦略はクロマトグラフィーと抽出アプリケーション40,41,42,43、液体 CO2を生成する方法としてはかなり一般的な合成に使用率が低いのに 44。この戦略を活用した並列アクセス適度な CO2間の圧力の 2 20 気圧能力ながら反応の急速に画面大量に私たちのグループが反応の収率の向上に重要な許可。これらの条件の下でプライマリ (1 °) および二次 (2 °) アミンの両方が電子豊富な電子貧しい芳香族ハロゲン化物と arylated をすることができます。
プロトコル
注意: 1) 次のプロトコルとみなされている繰り返し試験による安全。しかし、バイアル、反応全体をシールするときに注意が必要、反応を開くときに、特に反応の不均一性とバイアルは機器の故障につながる可能性があります。バイアルは、使用する前に物理的な欠陥の検査する必要があります。バイアルはブラストシールドのいくつかのフォームの背後に配置する必要があります。 またはフード サッシ バイアルの事件を防ぐために密封する必要があります後にすぐに失敗します。2) 少量の CO2使用による窒息の少しチャンスがあるが反応セットアップをする必要がありますと同様ヒューム フード、換気の良い場所で開かれました。3) ドライアイス寒剤であり深刻な組織の損傷を引き起こすことができます。注意は、直接接触を制限するなど低温手袋を使用して、凍傷を避けるためにそれを操作しながらしたがってする必要があります。4) ドライアイスは、水蒸気、質量が CO2 (s)のみに機械的に使用前にドライアイスを剥離する必要があることを意味が凝縮されます。これはドライアイスを単に摩擦によって達成することができます 1 つの指の間やより安全には手袋やタオルなどの保護層で 1 つの指の間にそれをこすりします。
1. 7.5 mL バイアル (除外されていない空気) の反応
- ドライ 7.5 mL バイアルに攪拌棒を追加します。
- バイアルに酢酸パラジウム (6.7 mg、0.03 ミリ モル) を追加します。
- バイアルに銀トリフルオロ酢酸 (99.9 mg, 0.45 ミリ モル) を追加します。
- バイアルにヨウ化フェニル (92.3 mg, 0.45 ミリ モル) を追加します。
- Tertを追加-アミル アミン (26.3 mg、0.30 ミリ モル) バイアルを。
- バイアルに酢酸 (1.0 mL) を追加します。
注: サイズをバイアルに解決の容積の比率は重要、ドライアイスの添加によって CO2の即時の昇華が機械的に転置できる溶媒の場合はあまりにも多くは反応容器のサイズを基準にして使用します。 - バイアルに脱イオン水 (21.7 μ L、12.1 ミリ モル) を追加します。
- ドライアイス (26.3 mg, 0.60 mmol) の重量を量るし、すぐにまたすぐにシールに PTFE ライニングのキャップと瓶を確保しながら、バイアルにドライアイスを追加します。
注: すべての操作は昇華と CO2追加の少量の脱出を防ぐためにおよそ 5 秒以内実行必要があります (これが冷凍酢酸ドライアイスの周りの形成によって遅くなる)。追加 CO2の量はおおよその値になり、我々 の手でいくつかの mg の偏差が許されています。 - 室温で 15 分間密封された反応バイアルをかき混ぜます。
- 反応容器を 110 ° C で事前に加熱されたプレートに転送し、冷却できるようにする前に 14 時間かき混ぜます。
- 冷却すると、慎重に CO2を発散するバイアルを開きます。
- すべて、揮発真空中での削除します。
注: バイアルにこの操作を実行することができます。 またはソリューションは大きな丸底フラスコに転送できます。 - 反応混合物を 1.2 M HCl(aq) (6 mL) を加え、15 分間空気に開いているかき混ぜます。
- その他 1.2 洗浄, 漏斗に水性画分を転送 M HCl (4 mL) と 1:1 ジエチル エーテル ・ ヘキサンの混合物 (3 x 8 mL) で抽出。
注: この有機洗浄過剰フェニル ヨウ化および他の中立的な副産物が含まれます、破棄することができます。 - 中和し、飽和 NH4オハイオ州(aq)の添加による基本的な水溶液を作る (10 mL は良い出発点である)。
- ジクロロ メタン (2 x 10 mL) で水層を抽出します。
- 4、そのフィルターは tared サンプルにバイアル、ナ2で合わせた有機画分を乾燥します。
- 蒸発の溶媒真空中で、黄色の油としては、製品 (2-メチル-4-フェニル-butanamine) を与えます。
2. 反応 (パージ条件 – 空気除外) 7.5 mL バイアル
- ドライ 7.5 mL バイアルに攪拌棒を追加します。
- バイアルに酢酸パラジウム (6.7 mg、0.03 ミリ モル) を追加します。
- バイアルに銀トリフルオロ酢酸 (99.9 mg, 0.45 ミリ モル) を追加します。
- バイアルにヨウ化フェニル (92.3 mg, 0.45 ミリ モル) を追加します。
- Tertを追加-アミル アミン (26.3 mg、0.30 ミリ モル) バイアルを。
- バイアルに酢酸 (1.0 mL) を追加します。
注: サイズをバイアルに解決の容積の比率は重要、ドライアイスの添加によって CO2の即時の昇華が機械的に転置できる溶媒の場合はあまりにも多くは反応容器のサイズを基準にして使用します。 - バイアルに脱イオン水 (21.7 μ L、12.1 ミリ モル) を追加します。
- バランスにバイアルを風袋、ドライアイスの約 98 mg を追加して、すぐにPTFE ライニング キャップと瓶のシールに続いて、約 26 mg の最終的な質量を達成するまでに昇華する CO2を許可します。
メモ: 望ましい場合は、この手順をさらにバイアルから空気を除外するドライアイスの大きな質量を持つ実行できます。水が生じるとここのようにできない場合があります水の最も効果的な戦略敏感な反応に注目すべきです。 - 室温で 15 分間密封された反応バイアルをかき混ぜます。
- 反応容器を 110 ° C で事前に加熱されたプレートに転送し、冷却できるようにする前に 14 時間かき混ぜます。
- 冷却すると、慎重に CO2を発散するバイアルを開きます。
- すべて、揮発真空中での削除します。
注: バイアルにこの操作を実行することができます。 またはソリューションは大きな丸底フラスコに転送できます。 - 反応混合物に 1.2 M HCl(aq) (6 mL) を加え、15 分間空気に開いているかき混ぜます。
- その他 1.2 洗浄, 漏斗に水性画分を転送 M HCl (4 mL) と 1:1 ジエチル エーテル ・ ヘキサンの混合物 (3 x 8 mL) で抽出。
注: この有機洗浄過剰フェニル ヨウ化および他の中立的な副産物が含まれます、破棄することができます。 - 中和し、飽和 NH4オハイオ州(aq)の添加による基本的な水溶液を作る (10 mL は良い出発点である)。
- ジクロロ メタン (2 x 10 mL) で水層を抽出します。
- 4、そのフィルターは tared サンプルにバイアル、ナ2で合わせた有機画分を乾燥します。
- 黄色の油としては、製品 (2-メチル-4-フェニル-butanamine) を与える溶媒を真空中で蒸発させます。
3. 40 mL バイアル (除外されていない空気) の反応
- 乾燥 40 mL バイアルに攪拌棒を追加します。
- バイアルに酢酸パラジウム (33.5 mg、0.15 ミリ モル) を追加します。
- バイアルに銀トリフルオロ酢酸 (499.5 mg、2.25 mmol) を追加します。
- バイアルにヨウ化フェニル (461.5 mg、2.25 mmol) を追加します。
- バイアルに tert アミル アミン (131.5 mg、1.5 mmol) を追加します。
- バイアルに酢酸 (5.0 mL) を追加します。
注: サイズをバイアルに解決の容積の比率は重要、ドライアイスの添加によって CO2の即時の昇華が機械的に転置できる溶媒の場合はあまりにも多くは反応容器のサイズを基準にして使用します。 - バイアルに脱イオン水 (108.5 μ L、6.02 mmol) を追加します。
- ドライアイス (131.5 mg、3.0 ミリ モル) の重量を量るし、すぐにまたすぐに PTFE ライニングのキャップと瓶を密封するために確保しながら、バイアルにドライアイスを追加します。
注: すべての操作は昇華と CO2追加の少量の脱出を防ぐためにおよそ 5 秒以内実行必要があります (これが冷凍酢酸ドライアイスの周りの形成によって遅くなる)。追加 CO2の量はおおよその値になり、我々 の手でいくつかの mg の偏差が許されています。 - 室温で 15 分間密封された反応バイアルをかき混ぜます。
- 反応容器を 110 ° C で事前に加熱されたプレートに転送し、冷却できるようにする前に 14 時間かき混ぜます。
- 冷却すると、慎重に CO2を発散するバイアルを開きます。
- すべて、揮発真空中での削除します。
注: バイアルにこの操作を実行することができます。 またはソリューションは大きな丸底フラスコに転送できます。 - 反応混合物を 1.2 M HCl(aq) (30 mL) を加え、15 分間空気に開いているかき混ぜます。
- その他 1.2 洗浄, 漏斗に水性画分を転送 M HCl (20 mL) と 1:1 ジエチル エーテル ・ ヘキサンの混合物 (3 x 8 mL) で抽出。
注: この有機洗浄過剰フェニル ヨウ化および他の中立的な副産物が含まれます、破棄することができます。 - 中和し、飽和 NH4オハイオ州(aq)の添加による基本的な水溶液を作る (10 mL は良い出発点である)。
- ジクロロ メタン (2 x 20 mL) で水層を抽出します。
- 4、そのフィルターは tared サンプルにバイアル、ナ2で合わせた有機画分を乾燥します。
- 蒸発の溶媒真空中で、黄色の油としては、製品 (2-メチル-4-フェニル-butanamine) を与えます。
4. 35 mL 圧力管 (除外されていない空気) の反応
- 35 mL の乾燥の圧力管に攪拌棒を追加します。
- 圧力管に酢酸パラジウム (6.7 mg、0.03 ミリ モル) を追加します。
- 圧力管に銀トリフルオロ酢酸 (132.5 mg, 0.6 モル) を追加します。
- 圧力管にヨウ化フェニル (183.6 mg、0.9 ミリ モル) を追加します。
- 追加 2-メチル-N-(3-methylbenzyl) ブタン-2-アミン (57.4 mg, 0.3 mmol) 圧力管へ。
- 1,1,1,3,3,3、続いて、バイアルに酢酸 (1.0 mL) を追加-hexafluoroisopropanol (1.0 mL)。
注: サイズをバイアルに解決の容積の比率は重要、ドライアイスの添加によって CO2の即時の昇華が機械的に転置できる溶媒の場合はあまりにも多くは反応容器のサイズを基準にして使用します。 - 圧力管に脱イオン水 (21.7 μ L、1.2 モル) を追加します。
- ドライアイス (1.32 g、30 mmol) の重量を量るし、すぐにまたすぐにシールする適切なテフロン スクリュー キャップで圧力管を確保しながら圧力管にドライアイスを追加します。
注: すべての操作は昇華と CO2追加の少量の脱出を防ぐためにおよそ 5 秒以内実行必要があります (これが冷凍酢酸ドライアイスの周りの形成によって遅くなる)。追加 CO2の量はおおよその値になり、我々 の手でいくつかの mg の偏差が許されています。 - 密閉反応容器を室温で 15 分間かき混ぜます。
- 反応容器を 90 ° C で事前に加熱されたプレートに転送し、クールに許可する前に 24 時間かき混ぜます。
- 冷却すると、オーバー キャップ、タオルやパッドを入れられた手袋を置くし、CO2を発散する圧力管を慎重に開いています。
- すべて、揮発真空中での削除します。
注: この操作は、適切なアダプターで圧力管で実行できます。 またはソリューションは大きな丸底フラスコに転送できます。 - 反応混合物を 1.2 M HCl(aq) (12 mL) を加え、15 分間空気に開いているかき混ぜます。
- その他 1.2 洗浄, 漏斗に水性画分を転送 M HCl (8 mL) と 1:1 ジエチル エーテル ・ ヘキサンの混合物 (3 x 8 mL) で抽出。
注: この有機洗浄過剰フェニル ヨウ化および他の中立的な副産物が含まれます、破棄することができます。 - 中和し、飽和 NH4オハイオ州(aq)の添加による基本的な水溶液を作る (10 mL は良い出発点である)。
- ジクロロ メタン (2 x 10 mL) で水層を抽出します。
- 4、そのフィルターは tared サンプルにバイアル、ナ2で合わせた有機画分を乾燥します。
- 蒸発の溶媒真空中で、与える製品 (黄色の油として 2-Methyl-N-(3-methylbenzyl)-4-phenylbutan-2-amine)。
結果
これらのプロトコルに続いて2大気二酸化炭素 CO が必要な化学反応を達成するために適切な量と反応バイアルを充電することが可能です。ステップ 1 で達成される圧力が部分的な溶媒和により観測された圧力、室温で 2 気圧の近くにあるし、する必要がありますが約 3 気圧 (この値の定量のための議論を参照してください) に計算されます。反応条件下で約 2.6 ...
ディスカッション
ファン ・ デル ・ ワールスの状態方程式を使用して、これらのシステムのおおよその圧力は計算される45をすることができます。
式 1: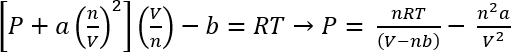
プロトコル 1 の条件下での CO2の 26.3 mg nを与えることが想定 = 10-4 mols x 5.98
開示事項
演出グループとしてルイス ・基本的な基板の C-H 活性化のための CO2の使用は現在米国仮特許 #62/608, 074 の焦点であります。
謝辞
著者はこの仕事の部分的なサポートで、トレド大学からスタートアップの資金調達としてアメリカの化学社会のハーマン ・ フラッシュ財団からの資金を確認したいです。反応圧力を測定するための適切な圧力計を開発して彼の支援のため氏トーマス納を認めた氏スティーブ分解する Modar が有益な議論に感謝しました。
資料
| Name | Company | Catalog Number | Comments |
| 7.5 mL Sample Vial with Screw Cap (Thermoset) | Qorpak | GLC-00984 | Can be reused. |
| 40 mL Sample Vial with Screw Cap (Thermoset) | Qorpak | GLC-01039 | Can be reused. |
| Pressure Tube, #15 Thread, 7" Long, 25.4 mm O.D. | Ace Glass | 8648-06 | Can be reused. |
| Pie-Block for 2 Dram Vials | ChemGlass | CG-1991-P14 | Can be reused. |
| Pie-Block for 10 Dram Vials | ChemGlass | CG-1991-P12 | Can be reused. |
| 3.2 mm PTFE Disposable Stir Bars | Fisher | 14-513-93 | Can be reused. |
| C-MAG HS 7 Control Hotplate | IKA | 20002695 | |
| Analytical Weighing Balance | Sartorius | QUINTIX2241S | |
| Double-Ended Micro-Tapered Spatula | Fisher Scientific | 21-401-10 | |
| Hei-VAP Advantage - Hand Lift Model with G5 Dry Ice Condenser Rotary Evaporator | Heidolph | 561-01500-00 | |
| Bump Trap 14/20 Joint | ChemGlass | CG-1322-01 | |
| tert-Amyl amine | Alfa Aesar | B24639-14 | Used as received. |
| 2-Methyl-N-(3-methylbenzyl)butan-2-amine | N/A | N/A | Prepared from reductive amination of tert-amyl amine and 3-tolualdehyde in the presence of sodium borohydride in methanol. |
| Palladium Acetate | Chem-Impex International, Inc. | 4898 | Used as received. |
| Silver Trifluoroacetate | Oakwood Chemicals | 007271 | Used as received. |
| Phenyl Iodide | Oakwood Chemicals | 003461 | Used as received. |
| Acetic Acid | Fisher Chemical | A38 | Used as received. |
| 1,1,1,3,3,3-Hexafluoroisopropanol | Oakwood Chemicals | 003409 | Used as received. |
| Deionized Water | Obtained from in-house deionized water system. | ||
| Dry Ice | Carbonic Enterprises Dry Ice Inc. | Non-food grade dry ice. | |
| Concentrated Hydrochloric Acid | Fisher Chemical | A144SI | Diluted to a 1.2 M solution prior to use. |
| Diethyl Ether, Certified | Fisher Chemical | E138 | Used as received. |
| Hexanes, Certified ACS | Fisher Chemical | H292 | Used as received. |
| Saturated Ammonium Hydroxide | Fisher Chemical | A669 | Used as received. |
| Dichloromethane | Fisher Chemical | D37 | Used as received. |
| Sodium Sulfate, Anhydrous | Oakwood Chemicals | 044702 | Used as received. |
| 250 mL Separatory Funnel | Prepared in-house by staff glassblower. | ||
| 100 mL Round Bottom Flask | Prepared in-house by staff glassblower. | ||
| Scientific Disposable Funnel | Caplugs | 2085136030 | |
| Borosilicate Glass Scintillation Vials, 20 mL | Fisher Scientific | 03-337-15 | |
| 5 mm O.D. Thin Walled Precision NMR Tubes | Wilmad | 666000575 | |
| Chloroform-d | Cambridge Isotope Laboratories, Inc. | DLM-7 | Used as received. |
参考文献
- Verboom, W. Selected Examples of High-Pressure Reactions in Glass Microreactors. Chemical Engineering and Technology. 32 (11), 1695-1701 (2009).
- Schettino, V., Bini, R. Constraining Molecules at the Closest Approach: Chemistry at High Pressure. Chemical Society Reviews. 36, 869-880 (2007).
- Hemminger, O., Marteel, A., Mason, M. R., Davies, J. A., Tadd, A. R., Abraham, M. A. Hydroformylation of 1-Hexene in Supercritical Carbon Dioxide Using a Heterogeneous Rhodium Catalyst. 3. Evaluation of Solvent Effects. Green Chemistry. 4, 507-512 (2002).
- Mo, F., Dong, G. Regioselective Ketone α-Alkylation with Simple Olefins via Dual Activation. Science. 345 (6192), 68-72 (2014).
- Schultz, A. G., Kirincich, S. J., Rahm, R. Asymmetric Organic Synthesis. Preparation and Birch Reduction-Alkylation of 2-Methyl-3,4-Dihydroisoquinolin-1-ones. Tetrahedron Letters. 36 (26), 4551-4554 (1995).
- Dong, L., Aleem, S., Fink, C. A. Microwave-Accelerated Reductive Amination Between Ketones and Ammonium Acetate. Tetrahedron Letters. 51 (39), 5210-5212 (2010).
- Wang, D., Astruc, D. The Golden Age of Transfer Hydrogenation. Chemical Reviews. 115 (13), 6621-6686 (2015).
- Morimoto, T., Kakiuchi, K. Evolution of Carbonylation Catalysis: No Need for Carbon Monoxide. Angewandte Chemie International Edition in English. 43 (42), 5580-5588 (2004).
- Iranpoor, N., Firouzabadi, H., Motevalli, S., Talebi, M. Palladium-Free Aminocarbonylation of Aryl, Benzyl, and Styryl Iodides and Bromides by Amines Using Mo(CO)6 and Norbornadiene. Tetrahedron. 69 (1), 418-426 (2013).
- Ren, W., Yamane, M. Mo(CO)6-Mediated Carbamoylation of Aryl Halides. Journal of Organic Chemistry. 75 (24), 8410-8415 (2010).
- Wang, H., Dong, B., Wang, Y., Li, J., Shi, Y. A Palladium-Catalyzed Regioselective Hydroesterification of Alkenylphenols to Lactones with Phenyl Formate as CO Source. Organic Letters. 16 (1), 186-189 (2014).
- Zhang, Y., Chen, J. -. L., Chen, Z. -. B., Zhu, Y. -. M., Ji, S. -. J. Palladium-Catalyzed Carbonylative Annulation Reactions Using Aryl Formate as a CO Source: Synthesis of 2-Substituted Indene-1,3(2H)-Dione Derivatives. Journal of Organic Chemistry. 80 (21), 10643-10650 (2015).
- Wan, Y., Alterman, M., Larhed, M., Hallberg, A. Dimethylformamide as a Carbon Monoxide Source in Fast Palladium-Catalyzed Aminocarbonylations of Aryl Bromides. Journal of Organic Chemistry. 67 (17), 6232-6235 (2002).
- Gockel, S. N., Hull, K. L. Chloroform as a Carbon Monoxide Precursor: In or Ex Situ Generation of CO for Pd-Catalyzed Aminocarbonylations. Organic Letters. 17 (13), 3236-3239 (2015).
- Zhao, H., Du, H., Yuan, X., Wang, T., Han, W. Iron-Catalyzed Carbonylation of Aryl Halides with Arylborons Using Stoichiometric Chloroform as the Carbon Monoxide Source. Green Chemistry. 18, 5782-5787 (2016).
- Chen, P., Xu, C., Yin, H., Gao, X., Qu, L. Shock Induced Conversion of Carbon Dioxide to Few Layer Graphene. Carbon. , 471-476 (2017).
- Iijima, T., Yamaguchi, T. Efficient Regioselective Carboxylation of Phenol to Salicylic Acid with Supercritical CO2 in the Presence of Alumnium Bromide. Journal of Molecular Catalysis A: Chemical. 295 (1-2), 52-56 (2008).
- Jevtovikj, I., Manzini, S., Hanauer, M., Rominger, F., Schaub, T. Investigations on the Catalytic Carboxylation of Olefins with CO2 Towards α, β-Unsaturated Carboxylic Acid Salts: Characterization of Intermediates and Ligands as well as Substrate Effects. Dalton Transactions. 44, 11083-11094 (2015).
- Juliá-Hernández, F., Moragas, T., Cornella, J., Martin, R. Remote Carboxylation of Halogenated Aliphatic Hydrocarbons with Carbon Dioxide. Nature. 545, 84-88 (2017).
- North, M., Pasquale, R. Mechanism of Cyclic Carbonate Synthesis from Epoxides and CO2. Angewandte Chemie International Edition. 48 (16), 2946-2948 (2009).
- Yeung, C. S., Dong, V. M. Beyond Aresta's Complex: Ni- and Pd-Catalyzed Organozinc Coupling to CO2. Journal of the American Chemical Society. 130 (25), 7826-7827 (2008).
- Zhu, D. -. Y., Fang, L., Han, H., Wang, Y., Xia, J. -. B. Reductive CO2 Fixation via Tandem C-C and C-N Bond Formation: Synthesis of Spiro-Indopyrrolidines. Organic Letters. 19 (16), 4259-4262 (2017).
- Kapoor, M., Liu, D., Young, M. C. Carbon Dioxide Mediated C(sp3)–H Arylation of Amine Substrates. J. Am. Chem. Soc. , (2018).
- Zhang, Y. -. F., Zhao, H. -. W., Wang, H., Wei, J. -. B., Shi, Z. -. J. Readily Removable Directing Group Assisted Chemo- and Regioselective C(sp3)-H Activation by Palladium Catalysis. Angewandte Chemie International Edition. 54 (46), 13686-13690 (2015).
- He, G., Chen, G. A Practical Strategy for the Structural Diversification of Aliphatic Scaffolds Through the Palladium-Catalyzed Picolinamide-Directed Remote Functionalization of Unactivated C(sp3)-H Bonds. Angewandte Chemie International Edition. 50 (22), 5192-5196 (2011).
- Nack, W. A., Wang, X., Wang, B., He, G., Cheng, G. Palladium-Catalyzed Picolinamide-Directed Iodination of Remote ortho-C-H Bonds of Arenes: Synthesis of Tetrahydroquinolines. Beilstein Journal of Organic Chemistry. 12, 1243-1249 (2016).
- Feng, P., Li, M., Ge, H. Room Temperature Palladium-Catalyzed Decarboxylative ortho-Acylation of Acetanilides with α-Oxocarboxylic Acids. Journal of the American Chemical Society. 132 (34), 11898-11899 (2010).
- Coomber, C. E., Benhamou, L., Bučar, D. -. K., Smith, P. D., Porter, M. J., Sheppard, T. D. Silver-Free Palladium-Catalyzed C(sp3)-H Arylation of Saturated Bicyclic Amine Scaffolds. Journal of Organic Chemistry. 83 (5), 2495-2503 (2018).
- Mei, T. -. S., Wang, X., Yu, J. -. Q. Pd(II)-Catalyzed Amination of C-H Bonds Using Single-Electron or Two-Electron Oxidants. Journal of the American Chemical Society. 131 (31), 10806-10807 (2009).
- Xie, W., Yang, J., Wang, B., Li, B. Regioselective Ortho Olefination of Aryl Sulfonamide via Rhodium-Catalyzed Direct C-H Bond Activation. Journal of Organic Chemistry. 79 (17), 8278-8287 (2014).
- Rodriguez, N., Romero-Revilla, J. A., Fernández-Ibáñez, M. &. #. 1. 9. 3. ;., Carretero, J. C. Palladium-Catalyzed N-(2-pyridyl)sulfonyl-Directed C(sp3)-H γ-Arylation of Amino Acid Derivatives. Chemical Science. 4, 175-179 (2013).
- Zheng, Y., Song, W., Zhu, Y., Wei, B., Xuan, L. Pd-Catalyzed Acetoxylation of γ-C(sp3)-H Bonds of Amines Directed by a Removable Bts-Protecting Group. Journal of Organic Chemistry. 83 (4), 2448-2454 (2018).
- Jain, P., Verma, P., Xia, G., Yu, J. -. Q. Enantioselective Amine α-Functionalization Via Palladium-Catalysed C-H Arylation of Thioamides. Nature Chemistry. 9, 140-144 (2017).
- Tran, A. T. Practical Alkoxythiocarbonyl Auxiliaries for Ir(I)-Catalyzed C-H Alkylation of Azacycles. Angewandte Chemie International Edition. 56 (35), 10530-10534 (2017).
- Huang, Z., Wang, C., Dong, G. A Hydrazone-Based exo-Directing Group Strategy for β-C-H Oxidation of Aliphatic Amines. Angewandte Chemie International Edition. 55 (17), 5299-5303 (2016).
- Xu, Y., Young, M. C., Wang, C., Magness, D. M., Dong, G. Catalytic C(sp3)-H Arylation of Free Primary Amines via an in situ Generated Exo-Directing Group. Chemie International Edition. 55 (31), 9084-9087 (2016).
- Liu, Y., Ge, H. Site-Selective C-H Arylation of Primary Aliphatic Amines Enabled by a Catalytic Transient Directing Group. Nature Chemistry. 9, 26-32 (2017).
- Wu, Y., Chen, Y. -. Q., Liu, T., Eastgate, M. D., Yu, J. -. Q. Pd-Catalyzed γ-C(sp3)-H Arylation of Free Amines Using a Transient Directing Group. Journal of the American Chemical Society. 138 (44), 14554-14557 (2016).
- Yada, A., Liao, W., Sato, Y., Murakami, M. Buttressing Salicylaldehydes: A Multipurpose Directing Group for C(sp3)-H Bond Activation. Angewandte Chemie International Edition. 56 (4), 1073-1076 (2017).
- Baldwin, B. W., Kuntzleman, T. S. Liquid CO2 in Centrifuge Tubes: Separation of Chamazulene from Blue Tansy (Tanacetum annum) Oil via Extraction and Thin-Layer Chromatography. Journal of Chemical Education. 95 (4), 620-624 (2018).
- McKenzie, L. C., Thompson, J. E., Sullivan, R., Hutchison, J. E. Green Chemical Processing in the Teaching Laboratory: A Convenient Liquid CO2 Extraction of Natural Products. Green Chemistry. 6, 355-358 (2004).
- Hudson, R., Ackerman, H. M., Gallo, L. K., Gwinner, A. S., Krauss, A., Sears, J. D., Bishop, A., Esdale, K. N., Katz, J. L. CO2 Dry Cleaning: A Benign Solvent Demonstration Accessible to K-8 Audiences. Journal of Chemical Education. 94, 480-482 (2017).
- Barcena, H., Chen, P. An Anesthetic Drug Demonstration and an Introductory Antioxidant Activity Experiment with "Eugene, the Sleepy Fish.". Journal of Chemical Education. 93, 202-205 (2016).
- Bodsgard, B. R., Lien, N. R., Waulters, Q. T. Liquid CO2 Extraction and NMR Characterization of Anethole from Fennel Seed: A General Chemistry Laboratory. Journal of Chemical Education. 93, 397-400 (2016).
- Fishbane, P. M., Gasiorowicz, S. G., Thornton, S. T. . Physics for Scientists and Engineers. , (2005).
- Rumpf, B., Xia, J., Maurer, G. Solubility of Carbon Dioxide in Aqueous Solutions Containing Acetic Acid or Sodium Hydroxide in the Temperature Range from 313 to 433 K and at Total Pressures up to 10 MPa. Industrial & Engineering Chemistry Research. 37, 2012-2019 (1998).
- Luo, J., Larrosa, I. C-H Carboxylation of Aromatic Compounds Through CO2 Fixation. ChemSusChem: Chemistry & Sustainability, Energy & Materials. 10, 3317-3332 (2017).
- Manjolinho, F., Arndt, M., Gooßen, K., Gooßen, L. J. Catalytic C-H Carboxylation of Terminal Alkynes with Carbon Dioxide. ACS Catalysis. 2, 2014-2021 (2012).
- Banerjee, A., Dick., G. R., Yoshino, T., Kanan, M. W. Carbon Dioxide Utilization via Carbonate-Promoted C-H Carboxylation. Nature. 531, 215-219 (2016).
- Fei, H., Sampson, M. D., Lee, Y., Kubiak, C. P., Cohen, S. M. Photocatalytic CO2 Reduction to Formate Using a Mn(I) Molecular Catalyst in a Robust Metal-Organic Framework. Inorganic Chemistry. 54, 6821-6828 (2015).
- Chabolla, S. A., Yang, J. Y. For CO2 Reduction, Hydrogen-Bond Donors Do the Trick. ACS Central Science. 4, 315-317 (2018).
- Kim, D., Kley, C. S., Li, Y., Yang, P. Copper Nanoparticle Ensembles for Selective Electroreduction of CO2 to C2-C3 Products. Proceedings of the National Academy of Sciences of the United States of America. , C2-C3 (2017).
- Liu, Q., Wu, L., Jackstell, R., Beller, M. Using carbon dioxide as a building block in organic synthesis. Nature Communications. 6, 5933-5945 (2015).
- Hâncu, D., Green, J., Beckman, E. J. H2O2 in CO2 Sustainable Production and Green Reactions. Accounts of Chemical Research. 35, 757-764 (2002).
- Ballivet-Tkatchenko, D., Camy, S., Condoret, J. S., Lichtofouse, E., Scwarzbauer, J., Robert, D. Carbon Dioxide, a Solvent and Synthon for Green Chemistry. Environmental Chemistry. , 541-552 (2005).
- Hyatt, J. A. Liquid and Supercritical Carbon Dioxide as Organic Solvents. Journal of Organic Chemistry. 49, 5097-5101 (1984).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved