Method Article
細胞外小胞分析のための凍結破壊電子顕微鏡
要約
我々は、癌性尿路上皮細胞に由来する細胞外小胞(EV)の単離および凍結破砕のためのプロトコルを提示する。凍結破壊技術は、EVの直径と形状、そしてユニークな特徴としてEV膜の内部組織を明らかにしました。これらは、EVがレシピエント膜とどのように相互作用するかを理解する上で非常に重要です。
要約
細胞外小胞(EV)は、細胞から細胞外空間に放出される膜限定構造であり、細胞間通信に関与している。EVは、マイクロベシクル(MV)、エキソソーム、アポトーシス小体の3つの小胞集団からなる。EVの制限膜は、レシピエント細胞との相互作用に決定的に関与しており、生物学的に活性な分子のレシピエント細胞への移動につながり、その結果、それらの挙動に影響を与える可能性がある。凍結破壊電子顕微鏡技術は、生体膜の内部組織を研究するために使用されます。ここでは、培養がん尿路上皮細胞からのMV単離と、レプリカの急速凍結、破砕、作製、洗浄、透過型電子顕微鏡による解析の過程におけるMVの凍結骨折のプロトコールを紹介します。この結果は、単離のためのプロトコールが、MVの形状およびサイズに対応する均質なEVの集団をもたらすことを示している。膜内粒子は、主に制限膜の原形質面に見られる。したがって、凍結破壊は、膜タンパク質のMVの直径、形状、および分布を特徴付けるために選択される技術です。提示されたプロトコルは、EVの他の集団にも適用可能である。
概要
細胞外小胞(EV)は、細胞から細胞外空間に放出される膜限定小胞である。EVの3つの主要な集団は、エキソソーム、微小小胞(MV)、およびアポトーシス小体であり、それらはその起源、サイズ、および分子組成が異なる1,2,3。EVの組成は、ドナー細胞の分子プロファイルおよびその生理学的状態(すなわち、健康または罹患)を反映する4,5。これにより、EVはヒト疾患の診断、予後、治療に大きな可能性を秘めており、個別化医療6,7,8での使用に有望な医療応用が期待されています。
EVはセルラー間通信のメディエーターです。それらは生物学的に活性なタンパク質、脂質、およびRNAを含み、レシピエント細胞における生物学的プロセスに干渉し、その挙動を変える可能性がある9,10。しかしながら、EV制限膜の組成は、レシピエント細胞膜との相互作用にとって極めて重要である。
EVの供給源は体液とコンディショニングされた培地です。EV母集団を絶縁するには、適切な絶縁技術を使用する必要があります。例えば、10,000×gでの遠心分離はMVに富む画分を生じ、一方、≥100,000×gの遠心力はエキソソーム11,12に富む画分をもたらす。EVの分離分率は、純度、サイズ、形状の観点から検証する必要があります。そのために、国際細胞外小胞学会2018は、電子顕微鏡、原子間力顕微鏡、および光学顕微鏡ベースの超解像顕微鏡13の3つのクラスの高解像度イメージング技術を推奨しました。これらの技術のいずれも、EV膜内部に関する情報を提供することはできません。
凍結破壊電子顕微鏡は、凍結試料を破砕して内部構造を明らかにする技術であり、特に膜内部のビューを与える。サンプル調製のステップは、(1)急速凍結、(2)破砕、(3)レプリカの作成、および(4)レプリカ14の洗浄である。ステップ1では、サンプルを(任意選択で)化学的に固定し、グリセロールで凍結保護し、液体フロンで凍結する。ステップ2では、凍結標本は、膜二重層の内部を露出させる凍結破壊ユニットで破断される。ステップ3では、露出した破断面を白金(Pt)と炭素(C)で影付けしてレプリカを生成します。工程4では、有機材料を除去する。レプリカを透過型電子顕微鏡(TEM)で分析する。顕微鏡写真を正確に解釈するには、適切な向きのガイドラインに従わなければなりません14,15.簡単に説明すると、顕微鏡写真における影の方向は、顕微鏡写真を配向させる(すなわち、Pt陰影の方向を決定する)ための基準であり、その結果、凸および凹形状を決定する(図1)。膜二重層の破断面と呼ばれる2つの内部図は、凍結破砕によって膜を分割した結果として見ることができる:原形質面(P面)および外形質面(E面)。P面は細胞原形質に隣接する膜小葉を表し、E面は細胞外空間に隣接する膜小葉を表す。内在性膜タンパク質およびそれらの会合は、膜内粒子14、15を突出していると見なされる。
ここでの目標は、凍結破壊技術を適用して、MVのサイズ、形状、および制限膜の構造の観点からMVを特徴付けることです。ここでは、ヒト浸潤性膀胱癌性尿路上皮細胞に由来するMVの単離および凍結破砕のためのプロトコルを提示する。
プロトコル
1. がん性尿路上皮細胞の培養とEVの単離
注:ヒト浸潤性膀胱癌尿路上皮(T24)細胞株からEVを取得するためのプロトコルが提示されている。しかしながら、培養条件は、他の細胞型を使用するように最適化されなければならない。
- 3つのフラスコ(75cm2の増殖面)に3×104細胞/cm2の密度のT24細胞をプレートし、37°Cおよび5%CO2で3日間CO2インキュベーター内で細胞を培養することから始めます(図2A)。
- 5%ウシ胎児血清(FBS)、4 mM Glutamax、100 mg/mL ストレプトマイシン、および 100 U/mL ペニシリンを添加した A-DMEM と F12 の 1:1 (v/v) 混合物で T24 細胞用の培養液を使用します。
注: 次の分離により、MV で強化された EV が得られます。単離を開始する前に、光学顕微鏡で細胞を検査し、生存率およびコンフルエントを確認する(図2B)。T24細胞が70%のコンフルエントに達したら、馴化培養培地からEVの回収を開始する。
- 5%ウシ胎児血清(FBS)、4 mM Glutamax、100 mg/mL ストレプトマイシン、および 100 U/mL ペニシリンを添加した A-DMEM と F12 の 1:1 (v/v) 混合物で T24 細胞用の培養液を使用します。
- フラスコ(T75)からピペットでMVsで培養培地を円錐形遠沈管に集めます(図2C)。遠心分離機を300× g で4°Cで10分間遠心分離する(図2D)。
- 上清をピペットで新しい遠沈管に慎重に集めます(図2E)。
- 上清を2,000 × gで4°Cで20分間遠心分離する。
- ピペットで上清を新しい遠沈管に慎重に集めます。
- 10,000 × g で4°Cで40分間遠心分離する。 チューブの底に白っぽいペレットがあるかどうかを確認します。
メモ:必要に応じて、遠心分離機のローターを必要なgフォースに達するように交換します。EVペレットは、遠沈管の底部に白いペレットとして見えます(図2F)。ピペッティング中にペレットを失わないように、その場所にマークを付けます(図2G)。 - 上清をピペットで慎重に捨てます。ペレットに 1.5 mL の PBS を加え、MV を含むペレットを再懸濁します。懸濁液を新しい遠沈管に入れます。
- 10,000 × g で40分間遠心分離し、チューブの底に白いペレットが存在するかどうかを確認します。
注:EVペレットは、遠沈管の底部に白い斑点として表示されます。ピペッティング中にペレットを失うのを避けるために、その場所にマークを付けます。 - 上清をピペットで慎重に捨てます。固定液、2.5%グルタルアルデヒドを0.1 Mカコジル酸ナトリウム緩衝液(pH 7.2)に穏やかに加える。4°Cで20分間放置する(図2H)。
注意:グルタルアルデヒドとカコジル酸ナトリウムは有毒です。ヒュームフードで作業し、保護手袋を着用し、適切に廃棄してください。 - 固定液をピペットで慎重に取り除きます。洗浄バッファー(0.1 Mカコジル酸ナトリウムバッファー)をペレットに加えます。ペレットを再懸濁せずに4°Cで10分間放置する。
2. EVの凍結
注:凍結する前に、まずグリセロールでサンプルを凍結保護してください。
- 0.1 Mカコジル酸ナトリウム緩衝液を調製する。洗浄バッファーを取り出し、0.1 M カコジル酸バッファーに 50 μL の 30% グリセロールを加えます。EVを静かに再懸濁して、溶液を均質にします。4°Cで30分間インキュベートする。
- 超音波浴中で中央ピットで銅キャリアをクロロホルムで5分間洗浄します(図3A)。複数のサンプルを使用する場合は、それらを空気乾燥させ、色でマークします(図3B)。使用するまでは、キャリアを乾燥した清潔な場所(例えば、ペトリ皿のレンズペーパーの上)に保管してください。素手でキャリアに触れないでください。
- ピペット、溶液、ろ紙、ピンセット、実体顕微鏡、フロンと液体窒素(LN2)を入れたデュワーフラスコ、金属棒、およびクライオバイアルを準備します。LN2で冷却します。
警告: LN2 および冷却されたフロンを取り扱うときは、保護具を着用し、それに応じて作業してください。
- ピペット、溶液、ろ紙、ピンセット、実体顕微鏡、フロンと液体窒素(LN2)を入れたデュワーフラスコ、金属棒、およびクライオバイアルを準備します。LN2で冷却します。
- 凍結する前にEVを再び吊り下げてください。気泡の形成を避けてください。
メモ: 手順 2.4 ~ 2.7 を素早く実行します。 - 実体顕微鏡下で作業します(図3C)。1.5~1.7 μLのサンプルを銅キャリアの中央ピットに移し、サンプルをエッジ上にこぼさずに、銅キャリアエッジよりも高い位置まで凸状の液滴を作ります(図3D)。オーバースピルが発生した場合は、ろ紙を使用してキャリアの外輪を乾燥させます。
- 固化したフロンを金属棒で混ぜ合わせ、再び液化します(図3E)。
- ピンセットで銅キャリアの外輪をつかみ、ピンセットを8秒間軽く振って冷却されたフロンに浸します(図3F)。8秒後、LN2で満たされた別のデュワーフラスコにキャリアを素早く移します。
- サンプルの破砕または LN2 への保管を直ちに続行します。後者の場合、クライオビアルに印を付け、バイアルとピンセットの先端をLN2に沈めて冷却します(図3G)。LN 2 の下で、凍結した銅キャリアをバイアルに集めて閉じ、凍結破砕するまで LN2 コンテナ (図 3H) に保管します。
3. EVの破砕とレプリカ作り
メモ: 凍結破砕ユニットは、製造元の取扱説明書に従って準備してください。(図4A)。ユニットのチャンバーを清掃します。プラチナ(Pt/C)ガンとカーボン(C)ガンをそれぞれ45°と90°の角度で配置します(図4B)。
- ユニット真空システムを起動します。6.6 × 10-2 Pa(5 × 10-4 Torr)の圧力に達したら、ユニットチャンバを-150°Cまで冷却します。
- 凍結サンプルを含む銅キャリアを、乾式ピンセットを使用して凍結破砕ユニットに移します(図4C)。凍結転写を使用するか、サンプルの融解と氷結晶の堆積を避けるために速く作業してください。キャリアをサンプルテーブルに固定します。
- 真空が再び6.6 × 10-2 Pa(5 × 10-4 Torr)に達するまで待ってから、ナイフの温度を-100 °Cに設定します(図4D)。
- 真空が1.0 × 10-3 Pa(8 × 10-6 Torr)に達するまで待ちます。
- 双眼鏡でサンプルを観察し、ナイフに注意深く近づけます(図4E)。
- ナイフの電動移動をオンにしてサンプルの切片化を開始し(図4F)、サンプルの表面が滑らかになるまで(図4G)切削します。
- 破砕のために、ナイフの電動運動をオフにし、ナイフのゆっくりとした手動制御で進行し、それによってサンプルを破砕する(図4H)。破断面が影になるまで氷の結晶や破片の形成から保護するために、破断したサンプルの上にナイフを動かします。
- 45°でPtシャドーイングを続行します(図4I、J)。
- ストップウォッチを用意するか、凍結破砕ユニットの水晶モニターをオンにして、サンプルのPtの厚さを監視できるようにします。水晶振動子モニターで測定したPt層の推奨厚さは2.5nmで、これは所定の高張力および電流での4秒のシャドーイングに相当します(すなわち、Ptシャドーイングの速度は0.63nm/sです)。
- シャドウイングを開始する前に、ナイフをサンプルから遠ざけます。Pt/Cガン(1,600V)にハイテンションをかけ、電流を60mAに増やします。Ptの火花が現れ、サンプルに影を落とし始めるはずです。この時点で、4秒のカウントダウンを開始するか、水晶振動子モニター上のPtの位置を観察して見つけます。
メモ:C層の推奨厚さは2.5nmで、これは所定の高張力および電流での10秒のシャドーイングに相当します。 - Ptの所望の厚さが得られたら、電流および高張力をオフにする。
- C シャドーイングを 90° で続行します (つまり、C シャドウイングの速度は 0.25 nm/s です)。
- Cガン(1,900V)にハイテンションをかけ、電流を90mAに上げると、Cの火花が現れてサンプルに影を落とし始めます。その時点で、10秒のカウントダウンを開始します。Cの所望の厚さが得られたら、電流および高張力をオフにする。
4. レプリカのクリーニングとレプリカ分析
- サンプルテーブルの銅キャリアを使用し、ピンセットで磁器12ウェルプレート内の室温の蒸留水に移します(図4K)。レプリカは水面に浮かび、キャリアは沈みます(図4L)。
- 蒸留水からワイヤーループでレプリカを次亜塩素酸ナトリウムを含む井戸に移します。ふたをして、ヒュームフードに室温で一晩放置する。
警告: 次亜塩素酸ナトリウムは有毒です。ヒュームフードで作業し、保護手袋を着用し、適切に廃棄してください。 - レプリカをddH2Oに移し、30分間洗浄する。これを3回繰り返します。
- ワイヤループでレプリカをメッシュ銅TEMグリッド(例えば、正方形またはハニカム100メッシュ以上)に転写する。グリッドを2時間空気乾燥させ、顕微鏡検査までグリッド収納ボックスに保管します。
注:一般に、グリッドは暗く乾燥した室温条件下で数ヶ月間保管することができます。 - TEM顕微鏡を使用してレプリカを画像化し、顕微鏡写真を取得します。
- これを行うには、レプリカ付きのTEMグリッドを挿入し、製造元の取扱説明書に従ってTEMイメージングを開始します。80 kV または 100 kV で作業します。
- サンプルを検査し、TEMのカメラで低倍率および高倍率で顕微鏡写真を取得します。
- MVの顕微鏡写真を分析します。MV直径の測定には、フィジー/ImageJソフトウェア16を使用してください。MVの直径は、Hallett et al.17によると、顕微鏡写真での測定の4/π倍です。
結果
MVsは、示差遠心分離後に癌尿路上皮T24細胞の馴化培地から単離した。プロトコールに従って、EV画分は、白色ペレットとして見なされたときに10,000×gでの遠心分離後に最初に検出された(図2G)。
次に、EVを上記のプロトコルに従って処理し、TEMで検討した。Pt/Cシャドウイングでは、比較的大きなレプリカが生成され(図4L)、クリーニングステップ中に小さなフラグメントに分割されることがよくありました。大きなレプリカとその小さな断片をTEMグリッド上でピッキングし、顕微鏡下で比較した。結果は、サイズに関係なくレプリカ表面の品質に差を示さなかったため、すべて使用できます。低倍率検査では、i)均質な表面(背景)、ii)凹面および凸状の球面プロファイル(小胞)、およびiii)損傷した表面の領域(アーチファクト; 図5A)。典型的な人工物は、破裂、ひだ、および不規則な調光影(すなわち、試料上の氷結晶堆積物のレプリカ)として見られた。また、細胞破片や細胞小器官は見られず、サンプルの純度を確認していることに注意することも重要です(図5B)。
単離された小胞は、一般に、3つ以上のクラスターに集められたか、または個々に分布していた(図5B)。小胞は球状であり、これは単離、固定、および凍結中の超構造の良好な保存を示す(図5C)。時折見られた「フラットボール」および細長い小胞(図5C)は、おそらく調製物のアーチファクトであり、その後の小胞径の測定には含まれていなかった。可視プロファイルの直径は238.5nm(±8.0nm、n = 190)であり、Hallettらによって提案された補正係数を考慮すると17は、304nm(±10nm; 図5D)。このサイズは、100nm~1000nmのMVの直径範囲に相関し、使用される絶縁プロトコルの有効性を証明します。小胞の画像と直径の決定により、分離物中のEVがMVで濃縮されていることが明確に確認されました。
レプリカの分析により、MV制限膜のP面およびE面の組織が明らかになった。MVは、破壊面を反映した凹状および凸状の丸い形状(図5C、E、F)として観察された。凸形状は、E面(すなわち、膜の破壊された外怱小葉; 図5E)。EVのエキゾプラズム面は滑らかで均一な外観をしていた。凹形状はP面に対応しています(図5F)。P面では、平滑な膜内にいくつかの突出した膜内粒子が見られた(図5C、F)。これは、がん尿路上皮T24細胞から単離されたMVが低量の膜タンパク質しか含まないことを意味する。
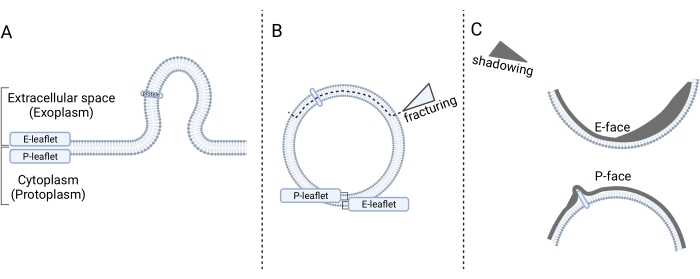
図1:凍結破砕後の膜決定の概略的提示 (A)原形質膜から細胞外空間への微小小胞芽。(B)マイクロベシクルは、凍結分画までP-およびE-膜リーフレットで制限され、リーフレットを分割し、フラクチャードフェイスと呼ばれるリーフレットの内部ビューを露出させる。(C)Pt/Cシャドーイング後、細胞質に面した凸形状の原形質面(P面)と細胞外空間に面した凹形の体外相(E面)の2つの骨折面が識別可能である。 図 1 は、 Biorender.com を使用して作成されました。 この図の拡大版を表示するには、ここをクリックしてください。
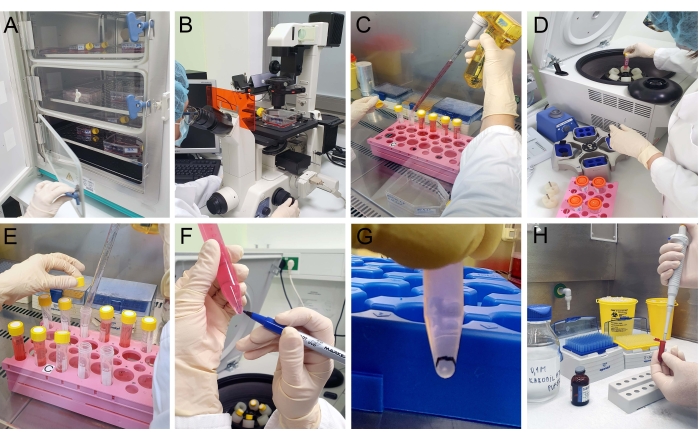
(A)CO2インキュベーター内で増殖させたT24細胞を(B)光学顕微鏡で検査し、MV単離前に生存率とコンフルエントを確認します。(C)細胞培養培地を回収し、(D)上清が回収されるたびに、(E)300×gおよび2,000×gで連続して遠心分離する。(F,G)10,000×gでの遠心分離の後、ペレットを示す白い斑点が見え、マーキングされる。上清を除去し、(H)固定液を再懸濁することなくペレットに慎重に添加する。この図の拡大版を表示するには、ここをクリックしてください。

図3:EVの凍結 (A) 中央ピットのある風乾式のきれいな銅キャリアは、(B)加工前にマークされています。マイクロベシクルをグリセロールに再懸濁して均質なサンプルを得、(C)実体顕微鏡下でクーパー担体の中央ピットに添加する。(D)中央ピットに凸状の滴を形成するようにサンプルの体積を追加する必要があります。(E)凍結直前に、LN2冷却フロンを金属棒と混合してフロンを液化する。(F) サンプルをフロンに沈めて凍結し、(G) LN2 に移送します。(H)凍結サンプルを含むキャリアは、クライオバイアルに回収し、LN2 Dewarコンテナに保管することができます。 この図の拡大版を表示するには、ここをクリックしてください。

図4:凍結破砕とレプリカの作成(A)凍結破砕ユニットユニットチャンバ(B)の内部には、白金(Pt)とカーボン(C)の電子銃、ナイフ、サンプルテーブルがあります。(C)破砕を開始するために、試料と共にキャリアが試料テーブルに移され、(D)凍結破砕ユニットが冷却され、真空が確立される。(E)切片化は、(F)ナイフの電動移動によって行われるが、破砕は手動で行うことが好ましい。(G)切片化前のサンプルおよび(H)破砕後のサンプル。(I)破砕直後にレプリカが作られる。(j)このプロセスの間、Ptは試料上に影を落とす。プラチナの影は、チャンバー内の明るい光(火花)として見られます。(k)試料担体を水で満たされた磁器井戸に集める。(l)洗浄工程中に次亜塩素酸ナトリウム溶液中に浮遊するレプリカ(矢印)。この図の拡大版を表示するには、ここをクリックしてください。

図5:凍結破壊およびPt/CシャドーMVの電子顕微鏡写真(A)凍結破壊および影付きEVペレットの概要(i)より低い倍率で。均質な表面は背景(ii)、明るい領域はレプリカの破裂(iii)、暗い領域はレプリカの折り目(アスタリスク)、不規則な暗い影は氷の結晶(2つのアスタリスク)によるものです。(B) 面が凹面と凸面を持つ丸型EVのクラスター。(C) EVの高倍率化EV膜のP面を呈する凸状破断では、膜内粒子(矢印)および平滑な表面のパッチ(矢じり)が見られる。細長い(星形)と平らなボール形(2つの星)の細胞外小胞が見つかります。(d)単離された尿路上皮MVの平均直径は、Hallettらによって提案され±サイズ測定値によれば、304nmから10nmである17。データは、SEM ±平均として表示されます。(E,F) MV の E 面と P 面。凡例: 矢印 = P 面の膜内粒子、丸で囲まれた矢印 = Pt/C シャドウイングの方向。スケールバー:A = 10 μm、B-F = 400 nm。この図の拡大版を表示するには、ここをクリックしてください。
ディスカッション
MVやその他の孤立したEVの集団の特性評価は、「オミックス」研究や機能研究などの下流分析を開始する前に、まず最初に行うことが最も重要です11,18。本明細書では、ヒト浸潤性膀胱癌尿路上皮T24細胞からEVsを遠心分離により単離し、凍結破壊電子顕微鏡による分析のために提供されたプロトコールに従って、単離画分がMVs11、13に富化されていることを実証した。MVの単離物には細胞破片または細胞小器官がなく、単離精製プロトコルの成功が確認された。
プロトコルの重要なステップである化学薬品の固定と凍結の組み合わせは、EVの球形12を保持しました。しかしながら、凍結破砕17によりEV径を評価する場合には注意が必要である。骨折はサンプルをランダムに通過するので、MV膜は赤道面と非赤道面に分割されます。凍結破壊標本および影付き標本の画像を解析するための厳密な方法を提供するために、Hallettらは、平均小胞径が画像上の小胞径の実際のサイズの4/π倍であることを示した17。それを考慮して、T24セルのEVの直径は304nmと計算され、MVの理論的なサイズ分布範囲である100-1000nm19に収まりました。
凍結破砕は、EVを視覚化するために最も広く使用されているTEM技術であるネガティブ染色を補うことができます。ネガティブ染色により、サンプルは一般的に化学的に固定され、乾燥され、TEMグリッドに付着し、ウラニル溶液と対比されます。メディアを支えないと、EVは崩壊しがちで、カップ型の外観になります。凍結破砕によって、我々はMVが球体であり、細胞外空間および体液におけるその形状を反映することを示す12。これにより、私たちの結果は、クライオ超薄切20におけるEVの観測結果とも一致しています。
凍結破壊技術の重要な利点は、EVがレシピエント膜にどのように標的化され、相互作用するかを理解する上で重要な要素である制限膜の内部組織を解決する能力である。ここでは、MVの膜を分析しましたが、凍結破砕により、他のEV集団の膜組織が明らかになる可能性があります。MVは原形質膜の出芽によって形成される。したがって、原形質膜タンパク質およびタンパク質クラスターは、MV膜中に見出されることが期待される。我々の結果は、T24細胞からのMVが膜内粒子を含み、内在性膜タンパク質を提示することを裏付けた。E面とP面との間の粒子分布に基づいて、MVsで観察される粒子は、尿路上皮細胞特異的である膜貫通タンパク質ウロプラキンであると予想するのが妥当である21,24。観察された粒子はまばらであり、これは尿路上皮発癌中のウロプラキンの減少を報告する以前の研究に従っている21、22、23。しかしながら、MV膜のタンパク質組成をさらに調査するために、凍結骨折レプリカ免疫標識(FRIL)技術の使用が推奨される。FRILは、提示された凍結骨折技術のアップグレードであり、抗体認識24,25によってレプリカ中のタンパク質の同一性を明らかにすることに専念している。要約すると、フリーズフラクチャ技術は、EV制限膜の特性評価、ならびに単離されたEV画分の形状、サイズ、および純度に適した電子顕微鏡技術である。提示されたプロトコルは、孤立したEVの他の集団の評価にも使用することができる。したがって、凍結破砕技術は、EV制限膜の組織を探求する研究のための国際細胞外小胞学会ガイドラインに含める価値があります。
開示事項
著者は利益相反がないと宣言しています。
謝辞
この研究は、スロベニア研究庁(研究コア資金なし)によって資金提供されました。P3-0108およびプロジェクトJ7-2594)およびMRIC UL IP-0510インフラストラクチャプログラム。この研究は、COST(欧州科学技術協力)の支援を受けて、周産期デリバティブの研究を治療アプローチに変換するためのCOST Action CA17116国際ネットワーク(SPRINT)に貢献しています。著者らは、Linda Štrus、Sanja Čabraja、Nada Pavlica Dubarič、Sabina Železnikに、細胞培養とサンプルの準備に関する技術的支援を、Marko Vogrinc、Ota Širca Roš、Nejc Debevecにビデオの準備に関する技術的支援に感謝したい。
資料
| Name | Company | Catalog Number | Comments |
| A-DMEM | ThermoFisher Scientific, USA | 12491015 | |
| Balzers freeze-fracture device | Balzers AG, Liechtenstein | Balzers BAF 200 | |
| Centrifuge | Eppendorf, Germany | model 5810R | |
| CO2 incubator HeraCell | Heraues, Germany | ||
| Copper carriers | Balzers | BB 113 142-2 | 100+ mesh |
| Copper grids | SPI, United States | 2010C | |
| Culture flask T75 | TPP, Switzerland | growing surface 75 cm2 | |
| F12 (HAM) | Sigma-Aldrich, Germany | 21765029 | |
| FBS | Gibco, Life Technologies, USA | 10500064 | |
| Glazed Porcelain Plate 6 Well | Fischer Sientific, United States | 50-949-072 | |
| Glycerol | Kemika, Croatia | 711901 | final concentration 30 % (v/v) |
| Glutaradehyde | Serva, Germany | 23114.01 | final concentration 2.5 % (v/v) |
| GlutaMAX | Gibco, Life Technologies | 35050-079 | final concentration 4 mM |
| Penicillin | Gibco, Life Technologies | 15140163 | final concentration 100 U/ml |
| Phase-contast inverted microscope | Nikon, Japan | model Eclipse | |
| Rotor | Eppendorf, Germany | A 4-44 | |
| Rotor | Eppendorf, Germany | F-34-6-38 | |
| Serological pipetts | TPP, Switzerland | 50mL volume | |
| Sodium hypochloride solution in water | Carlo Erba, Italy | 481181 | |
| Stereomicroscope | Leica, Germany | ||
| Streptomycin | Gibco, Life Technologies | 35050038 | final concentration 100 mg/mL |
| Transmission electron microscope | Philips, The Netherlands | model CM100 | working at 80 kV |
| Tweezers | SPI, United States |
参考文献
- Raposo, G., Stoorvogel, W. Extracellular vesicles: Exosomes, microvesicles, and friends. The Journal of Cell Biology. 200 (4), 373-383 (2013).
- Willms, E., Cabanas, C., Mager, I., Wood, M. J. A., Vader, P. Extracellular vesicle heterogeneity: Subpopulations, isolation techniques, and diverse functions in cancer progression. Frontiers in Immunology. 9, 738(2018).
- van Niel, G., D'Angelo, G., Raposo, G. Shedding light on the cell biology of extracellular vesicles. Nature Reviews Molecular Cell Biology. 19, 213-228 (2018).
- Cocucci, E., Racchetti, G., Meldolesi, J. Shedding microvesicles: Artefacts no more. Trends in Cell Biology. 19 (2), 43-51 (2009).
- Urabe, F., et al. Extracellular vesicles as biomarkers and therapeutic targets for cancer. American Journal of Physiology-Cell Physiology. 318 (1), 29-39 (2020).
- Tricarico, C., Clancy, J., D'Souza-Schorey, C. Biology and biogenesis of shed microvesicles. Small GTPases. 8 (4), 220-232 (2017).
- Georgantzoglou, N., Pergaris, A., Masaoutis, C., Theocharis, S. Extracellular vesicles as biomarkers carriers in bladder cancer: Diagnosis, surveillance, and treatment. International Journal of Molecular Sciences. 22 (5), 2744(2021).
- Słomka, A., Urban, S. K., Lukacs-Kornek, V., Żekanowska, E., Kornek, M. Large extracellular vesicles: Have we found the holy grail of inflammation. Frontiers in Immunology. 9, 2723(2018).
- Han, L., Lam, E. W. F., Sun, Y. Extracellular vesicles in the tumor microenvironment: Old stories, but new tales. Molecular Cancer. 18 (1), 59(2019).
- Muralidharan-Chari, V., Clancy, J. W., Sedgwick, A., D'Souza-Schorey, C. Microvesicles: Mediators of extracellular communication during cancer progression. Journal of Cell Science. 123, 1603-1611 (2010).
- Kowal, J., et al. Proteomic comparison defines novel markers to characterize heterogeneous populations of extracellular vesicle subtypes. Proceedings of the National Academy of Sciences of the United States of America. 113 (8), 968-977 (2016).
- Thery, C., Amigorena, S., Raposo, G., Clayton, A. Isolation and characterization of exosomes from cell culture supernatants and biological fluids. Current Protocols in Cell Biology. , Chapter 3, Unit 3.22 (2006).
- Thery, C., et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): A position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. Journal of Extracellular Vesicles. 7 (1), 1535750(2018).
- Severs, N. J. Freeze-fracture electron microscopy. Nature Protocols. 2 (3), 547-576 (2007).
- Severs, N. J., Robenek, H. Freeze-fracture cytochemistry in cell biology. Methods in Cell Biology. 88, 181-186 (2008).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529(2017).
- Hallett, F. R., Nickel, B., Samuels, C., Krygsman, P. H. Determination of vesicle size distributions by freeze-fracture electron microscopy. Journal of Electron Microscopy Technique. 17 (4), 459-466 (1991).
- Nigro, A., et al. Selective loss of microvesicles is a major issue of the differential centrifugation isolation protocols. Scientific Reports. 11, 3589(2021).
- Szatanek, R., et al. The methods of choice for extracellular vesicles (EVs) characterization. International Journal of Molecular Sciences. 18 (6), 1153(2017).
- Iliev, D., et al. Stimulation of exosome release by extracellular DNA is conserved across multiple cell types. The FEBS Journal. 285 (16), 3114-3133 (2018).
- Zupančič, D., Zakrajšek, M., Zhou, G., Romih, R. Expression and localization of four uroplakins in urothelial preneoplastic lesions. Histochemistry and Cell Biology. 136 (4), 491-500 (2011).
- Wu, X. R., Manabe, M., Yu, J., Sun, T. T. Large scale purification and immunolocalization of bovine uroplakins I, II, and III. Molecular markers of urothelial differentiation. The Journal of Biological Chemistry. 265 (31), 19170-19179 (1990).
- Kreft, M. E., Hudoklin, S., Jezernik, K., Romih, R. Formation and maintenance of blood-urine barrier in urothelium. Protoplasma. 246 (1-4), 3-14 (2010).
- Kreft, M. E., Robenek, H. Freeze-fracture replica immunolabelling reveals urothelial plaques in cultured urothelial cells. PLoS One. 7 (6), 38509(2012).
- Robenek, H., et al. Topography of lipid droplet-associated proteins: Insights from freeze-fracture replica immunogold labeling. Journal of Lipids. 2011, 409371(2011).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved