Method Article
세포 밖 소포 분석을 위한 동결-골절 전자 현미경 검사
요약
우리는 암성 비뇨생식기 세포로부터 기원되는 세포밖 소포(EVs)의 분리 및 동결 파쇄를 위한 프로토콜을 제시한다. 동결 파괴 기술은 EV의 직경과 모양, 그리고 EV 멤브레인의 내부 조직을 독특한 특징으로 드러냈다. 이는 EV가 수신자 멤브레인과 어떻게 상호 작용하는지 이해하는 데 매우 중요합니다.
초록
세포밖 소포(EVs)는 세포로부터 세포외 공간으로 방출되는 막-제한 구조이며 세포간 통신에 연루된다. EV는 소포의 세 개체군, 즉 마이크로베시클 (MV), 엑소좀 및 아폽토시스 체로 구성됩니다. EVs의 제한 막은 수용자 세포와의 상호 작용에 결정적으로 관여하며, 이는 생물학적 활성 분자를 수용자 세포로 전달하고 결과적으로 그들의 행동에 영향을 줄 수 있습니다. 동결 골절 전자 현미경 기술은 생물학적 막의 내부 조직을 연구하는 데 사용됩니다. 여기에서는 배양된 암 비뇨생식기 세포로부터 MV를 분리하고 MV의 동결 파괴를 급속 동결, 파쇄, 복제본 제작 및 세척하는 단계, 투과 전자 현미경으로 분석하는 프로토콜을 제시합니다. 결과는 분리를 위한 프로토콜이 MVs의 모양 및 크기에 상응하는 EVs의 균질한 집단을 산출한다는 것을 보여준다. 막내 입자는 주로 제한적인 막의 원형질 면에서 발견된다. 따라서 동결 골절은 MV의 직경, 모양 및 막 단백질의 분포를 특성화하기 위해 선택한 기술입니다. 제시된 프로토콜은 EV의 다른 집단에 적용 가능하다.
서문
세포밖 소포 (EVs)는 세포로부터 세포외 공간으로 방출되는 막 제한 소포이다. EV의 세 가지 주요 개체군은 엑소좀, 마이크로베시클 (MV) 및 세포사멸체이며, 기원, 크기 및 분자 구성 1,2,3이 다릅니다. EVs의 조성은 공여체 세포의 분자 프로파일과 그의 생리학적 상태 (즉, 건강 또는 병에 걸린 상태)4,5를 반영한다. 이것은 EV에게 인간 질병의 진단, 예후 및 치료에 엄청난 잠재력을 부여하며, 개인화 된 의학 6,7,8에 사용하기위한 유망한 의료 응용 프로그램을 가지고 있습니다.
EV는 세포 간 통신의 중재자입니다. 그들은 생물학적 활성 단백질, 지질 및 RNA를 함유하고 있으며, 이는 수용자 세포의 생물학적 과정을 방해하고 그 행동을 바꿀 수 있습니다 9,10. 그러나, EV 제한 막의 조성은 수용자 세포막과의 상호작용에 결정적이다.
EV의 공급원은 체액과 컨디셔닝 배양 배지입니다. EV 집단을 분리하기 위해서는 적절한 분리 기술이 사용되어야 한다. 예를 들어, 10,000 × g에서 원심분리하면 MVs가 농축된 분획을 산출하는 반면, ≥100,000 ×g의 원심력은 엑소좀11,12로 농축된 분획을 산출한다. EV의 분리된 분율은 순도, 크기 및 모양 측면에서 검증되어야 합니다. 이를 위해 2018 년 국제 세포 밖 소포 학회 (International Society for Extracellular Vesicles)는 전자 현미경, 원자력 현미경 및 광 현미경 기반 초해상도 현미경13의 세 가지 종류의 고해상도 이미징 기술을 권장했습니다. 이러한 기술 중 어느 것도 EV 멤브레인 내부에 대한 정보를 제공 할 수 없습니다.
동결 파괴 전자 현미경 검사는 냉동 된 시편을 깨뜨려 내부 구조를 드러내는 기술로, 특히 멤브레인 내부를 볼 수 있습니다. 샘플 준비의 단계는 (1) 급속 동결, (2) 파쇄, (3) 복제본 제작, 및 (4) 복제본 세척(14)이다. 단계 1에서, 샘플은 (임의로) 화학적으로 고정되고, 글리세롤로 동결보호되고, 액체 프레온에서 냉동된다. 단계 2에서, 동결된 시편은 동결 파괴 유닛에서 파단되고, 이는 막 이중층의 내부를 노출시킨다. 단계 3에서, 노출된 파단된 면들은 백금(Pt) 및 탄소(C)로 그림자를 드리워 복제본을 생성한다. 단계 4에서, 유기 물질은 제거된다. 복제물은 투과 전자 현미경 (TEM)에서 분석된다. 현미경 사진의 정확한 해석을 위해서는 적절한 방향14,15에 대한 지침을 따라야합니다. 간략하게, 현미경 사진에서 그림자의 방향은 현미경 사진을 배향시키고(즉, Pt 섀도잉의 방향을 결정하기 위해), 결과적으로 볼록하고 오목한 형상을 결정하기 위한 참조이다(그림 1). 막 이중층의 골절 된 얼굴이라고 불리는 두 개의 내부 뷰는 동결 파쇄에 의해 막을 분할 한 결과로 볼 수 있습니다 : 원형질 얼굴 (P-face)과 외인성 얼굴 (E-face). P-페이스는 세포 원형질에 인접한 막 전단지를 나타내고, E-face는 세포외 공간에 인접한 막 전단지를 나타낸다. 일체형 막 단백질과 이들의 연관성은 막내 입자(14,15)를 돌출하는 것으로 보인다.
여기서, 목표는 MVs를 그들의 제한 멤브레인의 크기, 모양 및 구조 측면에서 특성화하기 위해 동결 파괴 기술을 적용하는 것이다. 여기에서, 우리는 인간 침습성 방광 암 비뇨생식기 세포로부터 기원되는 MVs의 분리 및 동결 파쇄를 위한 프로토콜을 제시한다.
프로토콜
1. 암성 비뇨생식기 세포 배양 및 EV의 분리
주: 인간 침습성 방광암 비뇨기피 (T24) 세포주로부터 EVs를 수득하기 위한 프로토콜이 제시된다. 그러나, 배양 조건은 다른 세포 유형을 사용하도록 최적화되어야 한다.
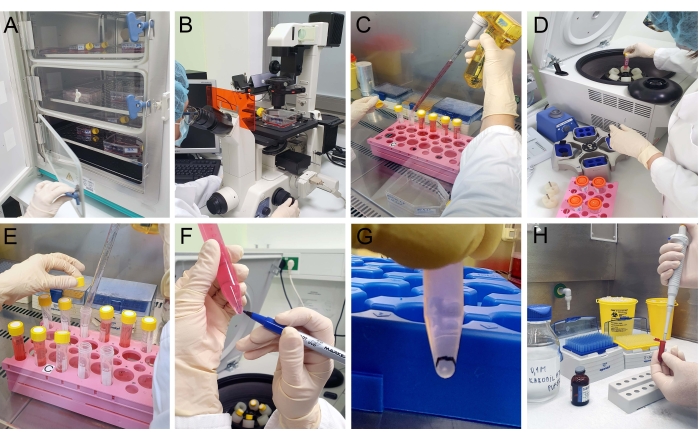
- 3 × 10 4 세포/cm2의 밀도를 갖는T24 세포를 3개의 플라스크 (성장 표면 75 cm2)에 플레이트하고, 세포를 37°C 및 5%CO2에서 3일 동안CO2 인큐베이터에서 배양하는 것으로 시작한다 (도 2A).
- 5% 태아 소 혈청(FBS), 4 mM 글루타맥스, 100 mg/mL 스트렙토마이신 및 100 U/mL 페니실린으로 보충된 A-DMEM과 F12의 1:1(v/v) 혼합물에서 T24 세포에 대한 배양 배지를 사용하십시오.
참고: 다음 분리는 MV에서 강화된 EV를 산출합니다. 분리를 시작하기 전에 광학 현미경으로 세포를 검사하여 생존력과 합류성을 확인하십시오 (그림 2B). T24 세포가 70% 합류할 때 컨디셔닝 배양 배지로부터 EVs를 수집하기 시작한다.
- 5% 태아 소 혈청(FBS), 4 mM 글루타맥스, 100 mg/mL 스트렙토마이신 및 100 U/mL 페니실린으로 보충된 A-DMEM과 F12의 1:1(v/v) 혼합물에서 T24 세포에 대한 배양 배지를 사용하십시오.
- 플라스크(T75)에서 피펫이 있는 MVs를 갖는 배양 배지를 원뿔형 원심분리 튜브로 수집한다(그림 2C). 4°C에서 10분 동안 300 × g 에서 원심분리한다(도 2D).
- 상층액을 피펫이 있는 새로운 원심분리 튜브에 조심스럽게 모으십시오(그림 2E).
- 상층액을 4°C에서 20분 동안 2,000 × g에서 원심분리한다.
- 피펫으로 상층액을 조심스럽게 수집하여 새로운 원심 분리 튜브에 넣으십시오.
- 4°C에서 40분 동안 10,000 × g 에서 원심분리한다. 튜브 바닥에 희끄무레 한 펠릿이 있는지 확인하십시오.
주: 필요한 경우 원심분리기 로터를 교체하여 필요한 g-force에 도달하십시오. EV 펠릿은 원심분리 튜브의 바닥에 백색 펠릿으로 보인다 (도 2F); 피펫팅 중에 펠릿이 손실되지 않도록 위치를 표시하십시오(그림 2G). - 피펫으로 상청액을 조심스럽게 버리십시오. 펠렛에 PBS 1.5 mL를 첨가하고 MV를 함유하는 펠렛을 재현탁시켰다. 현탁액을 새로운 원심분리 튜브에 넣는다.
- 4°C에서 40분 동안 10,000 × g 에서 원심분리하고, 튜브의 바닥에 백색 펠릿의 존재를 조사한다.
참고 : EV 펠릿은 원심 분리기 튜브의 바닥에 흰색 패치로 보입니다. 피펫팅 중에 펠릿이 손실되지 않도록 위치를 표시하십시오. - 피펫으로 상청액을 조심스럽게 버리십시오. 0.1 M 소듐 카코딜레이트 완충액 (pH 7.2)에 고정제, 2.5% 글루타르알데히드를 부드럽게 첨가한다. 4°C에서 20분 동안 그대로 두십시오(그림 2H).
주의: 글루타르알데히드와 카코딜레이트나트륨은 독성이 있습니다. 흄 후드에서 작업하고, 보호 장갑을 착용하고, 적절하게 버리십시오. - 조심스럽게 피펫으로 고정 장치를 제거하십시오. 펠렛에 세척 완충액(0.1 M 소듐 카코딜레이트 완충액)을 첨가한다. 펠렛을 재현탁시키지 않고 4°C에서 10분 동안 방치한다.
2. EV의 냉동
참고 : 동결하기 전에 먼저 글리세롤로 샘플을 냉동 보호하십시오.
- 0.1 M 소듐 카코딜레이트 버퍼를 준비한다. 세척 완충액을 제거하고 0.1 M 카코딜레이트 완충액에 30% 글리세롤 50 μL를 첨가한다. EV를 부드럽게 재현탁하여 용액을 균질하게 만듭니다. 4°C에서 30분 동안 인큐베이션한다.
- 클로로포름으로 초음파 욕조의 중앙 구덩이로 구리 캐리어를 5 분 동안 청소하십시오 (그림 3A). 공기 건조시키고 여러 샘플을 사용하는 경우 색상으로 표시하십시오 (그림 3B). 사용할 때까지 캐리어를 건조하고 깨끗한 장소(예: 페트리 접시의 렌즈 용지)에 보관하십시오. 맨손으로 캐리어를 만지지 마십시오.
- 피펫, 용액, 여과지, 핀셋, 입체 현미경, 프레온 및 액체 질소 (LN2)가있는 Dewar 플라스크, 금속 막대 및 냉동 장치를 준비하십시오. LN2로 식히십시오.
주의: LN2 및 냉각 프레온을 취급할 때 보호 장비를 착용하고 그에 따라 작업하십시오.
- 피펫, 용액, 여과지, 핀셋, 입체 현미경, 프레온 및 액체 질소 (LN2)가있는 Dewar 플라스크, 금속 막대 및 냉동 장치를 준비하십시오. LN2로 식히십시오.
- 정지하기 전에 EV를 다시 일시 중단하십시오. 기포의 형성을 피하십시오.
참고: 2.4-2.7단계를 빠르게 수행하십시오. - 입체 현미경으로 작업하십시오 (그림 3C). 1.5-1.7μL의 샘플을 구리 캐리어의 중앙 구덩이로 옮겨 샘플을 가장자리 위로 쏟아내지 않으면서 구리 캐리어 에지보다 높은 볼록한 드롭을 만듭니다(그림 3D). 과다 유출의 경우 여과지를 사용하여 캐리어의 외부 링을 건조시킵니다.
- 응고된 프레온을 금속 막대와 혼합하여 다시 액화시킵니다(그림 3E).
- 핀셋으로 구리 캐리어의 외부 링을 잡고 핀셋을 부드럽게 흔들면서 냉각 프레온에 8초 동안 담그십시오(그림 3F). 8초 후, 캐리어를LN2로 채워진 다른 Dewar 플라스크로 신속하게 옮깁니다.
- 파쇄를 즉시 진행하거나 샘플을LN2에 저장한다. 후자의 경우, 냉동 장치를 표시하고 바이알과 핀셋 팁을 LN2 에 담그면 식힙니다(그림 3G). LN2 아래에서 냉동 구리 운반선을 바이알에 모아 닫은 다음 동결 파쇄될 때까지 LN2 용기(그림 3H)에 보관합니다.
3. EV의 파쇄 및 복제본 만들기
주: 제조업체의 작동 지침에 따라 동결 파쇄 장치를 준비하십시오. (도 4A). 장치의 챔버를 청소하십시오. 백금(Pt/C)과 탄소(C) 총을 각각 45° 및 90°의 각도로 배치합니다(그림 4B).
- 단위 진공 시스템을 시작합니다. 6.6 × 10-2 Pa (5 × 10-4 Torr)의 압력에 도달하면 장치 챔버를 -150 °C로 냉각하십시오.
- 냉동 샘플이 있는 구리 캐리어를 건조 핀셋을 사용하여 동결 파쇄 장치로 옮깁니다(그림 4C). 냉동 이송을 사용하거나 샘플을 해동하고 얼음 결정이 증착되는 것을 피하기 위해 빠르게 작업하십시오. 캐리어를 샘플 테이블에 고정합니다.
- 진공이 다시 6.6 × 10-2 Pa (5 × 10-4 Torr)에 도달 할 때까지 기다린 다음 나이프 온도를 -100 °C로 설정하십시오 (그림 4D).
- 진공이 1.0 × 10-3 Pa (8 × 10-6 Torr)에 도달 할 때까지 기다리십시오.
- 쌍안경으로 샘플을 관찰하고 조심스럽게 칼에 접근하십시오 (그림 4E).
- 나이프의 전동 이동(그림 4F)을 켜서 샘플을 단면화하고 샘플 표면이 매끄럽게 될 때까지 단면화합니다(그림 4G).
- 파쇄를 위해 나이프의 전동 운동을 끄고 나이프의 느린 수동 제어를 진행하여 샘플을 파쇄합니다 (그림 4H). 파괴 된 표면이 그림자가 될 때까지 얼음 결정과 파편을 형성하지 않도록 보호하려면 칼을 골절 된 샘플 위로 옮깁니다.
- Pt 섀도잉을 45°에서 진행합니다(그림 4I, J).
- 스톱워치를 준비하거나 동결 파쇄 장치에서 석영 크리스탈 모니터를 켜면 샘플의 Pt의 두께를 감독 할 수 있습니다. 석영 크리스털 모니터에서 측정된 Pt 층의 권장 두께는 2.5nm이며, 이는 주어진 높은 장력 및 전류에서 4초의 섀도잉에 해당합니다(즉, Pt 섀도잉의 속도는 0.63nm/s임).
- 섀도잉을 시작하기 전에 칼을 샘플에서 멀리 옮깁니다. Pt/C 주포(1,600V)에 높은 장력을 적용하고 전류를 60mA로 증가시킵니다. Pt의 스파크가 나타나야 하며 샘플의 그림자가 나타나기 시작해야 합니다. 이 시점에서 4초 카운트다운을 시작하고 석영 크리스탈 모니터에서 Pt의 위치를 관찰하고 찾습니다.
참고: C 층의 권장 두께는 2.5nm이며, 이는 주어진 높은 장력과 전류에서 10초의 그림자에 해당합니다. - 원하는 Pt의 두께를 얻을 때 전류와 높은 장력을 끄십시오.
- 90°에서 C 섀도잉을 진행합니다(즉, C 섀도잉의 속도는 0.25nm/s임).
- C 건 (1,900 V)에 높은 장력을 적용하고 전류를 90mA로 늘리면 C의 스파크가 나타나고 샘플이 그림자를 드리우기 시작해야합니다. 그 순간 10 초 카운트 다운을 시작하십시오. 원하는 두께의 C가 얻어지면 전류와 높은 장력을 끄십시오.
4. 복제본 및 복제본 분석 정리
- 샘플 테이블의 구리 캐리어를 사용하여 핀셋으로 도자기 12웰 플레이트의 실온에서 증류수로 옮깁니다(그림 4K). 복제본은 물 표면에 떠 있고 캐리어는 가라앉습니다(그림 4L).
- 와이어 루프가있는 복제본을 증류수에서 차아 염소산 나트륨이있는 우물로 옮깁니다. 뚜껑을 덮고 실온에서 밤새 흄 후드에 두십시오.
주의: 차아염소산나트륨은 독성이 있습니다. 흄 후드에서 작업하고, 보호 장갑을 착용하고, 적절하게 버리십시오. - 복제본을ddH2O로 옮기고 30분 동안 세척한다. 3 번 반복하십시오.
- 와이어 루프가 있는 복제본을 메쉬 구리 TEM 그리드(예: 정사각형 또는 벌집 100+ 메쉬)로 전송합니다. 그리드를 2 시간 동안 공기 건조시킨 다음 현미경 검사가있을 때까지 그리드 저장 상자에 보관하십시오.
참고: 일반적으로 그리드는 어둡고 건조한 실내 온도 조건에서 몇 달 동안 보관할 수 있습니다. - TEM 현미경을 사용하여 복제본을 이미지화하고 현미경 사진을 얻습니다.
- 이렇게 하려면 복제본이 있는 TEM 그리드를 삽입하고 제조업체의 사용 설명서에 따라 TEM 이미징을 시작합니다. 80kV 또는 100kV에서 작업합니다.
- 샘플을 검사하고 TEM의 카메라로 더 낮은 배율과 높은 배율로 현미경 사진을 얻습니다.
- MV의 현미경 사진을 분석합니다. MV 직경을 측정하려면 피지/ImageJ 소프트웨어(16)를 사용하십시오. MV의 직경은 Hallett et al.17에 따르면 현미경 사진에서 측정 한 값의 4/π 배입니다.
결과
MVs는 차등 원심분리 후 암 비뇨생식기 T24 세포의 컨디셔닝 배지로부터 분리하였다. 프로토콜에 따라, EV 분획은 백색 펠릿으로 보일 때 10,000 × g에서 원심분리 후 먼저 검출되었다 (도 2G).
다음으로, EVs를 상기 프로토콜에 따라 처리하고 TEM 하에서 검사하였다. Pt/C 섀도잉은 비교적 큰 복제본을 생성했으며(그림 4L) 청소 단계에서 자주 작은 조각으로 분해됩니다. 큰 복제본과 그들의 작은 조각은 TEM 그리드에서 선택되고 현미경으로 비교되었습니다. 결과는 크기에 관계없이 복제본 표면의 품질에 차이가 없음을 보여 주었으므로 모두 사용할 수 있습니다. 낮은 배율 검사는 i) 균질 표면 (배경), ii) 오목하고 볼록한 구형 프로파일 (소포), 및 iii) 손상된 표면의 영역 (아티팩트; 도 5A). 전형적인 유물은 파열, 주름 및 불규칙한 조광기 그림자 (즉, 표본 상의 얼음 결정 퇴적물의 복제본)로 보였다. 또한 세포 파편이나 세포 소기관이 보이지 않아 샘플의 순도를 확인하는 것도 중요합니다 (그림 5B).
분리된 소포는 일반적으로 세 개 이상의 클러스터에 수집되거나 개별적으로 분포되었다(도 5B). 소포는 구형이었으며, 이는 격리, 고정 및 동결 중에 울트라 구조를 잘 보존한다는 것을 나타냅니다 (그림 5C). 때때로 볼 수 있었던 "플랫 볼"과 길쭉한 소포 (그림 5C)는 아마도 준비의 유물이었으며 소포 직경의 후속 측정에 포함되지 않았습니다. 가시 프로파일의 직경은 238.5 nm (±8.0 nm, n = 190)였으며, 이는 Hallett et al.17에 의해 제안 된 보정 계수를 고려하여, 304 nm (±10 nm)의 평균 소포 직경에 상응한다; 도 5D). 크기는 100nm와 1000nm 사이의 MV의 직경 범위와 상관 관계가 있으며 사용 된 분리 프로토콜의 효과를 입증합니다. 직경 결정과 함께 소포의 이미지는 분리 된 EV가 MV로 풍부하다는 것을 분명히 확인했습니다.
복제본의 분석은 MV 제한 막의 P-페이스 및 E-페이스의 조직을 밝혀냈다. MV는 골절면을 반사하는 오목하고 볼록한 둥근 모양으로 관찰되었으며(그림 5C, E, F). 볼록한 형상은 E-면(즉, 멤브레인의 골절된 외인성 전단지; 그림 5E). EV의 외인성 얼굴은 매끄럽고 균일 한 외관을 가졌습니다. 오목한 모양은 P면에 해당합니다(그림 5F). P면에서는 매끄러운 멤브레인 내에서 몇 개의 돌출된 막내 입자가 보였다(도 5C, F). 이는 암 비뇨생식기 T24 세포로부터 분리된 MV가 단지 낮은 양의 막 단백질만을 함유한다는 것을 의미한다.
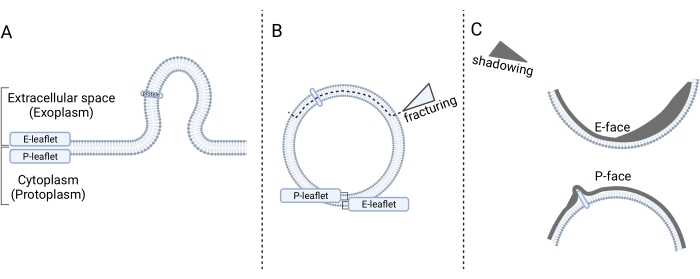
도 1: 동결파쇄 후 막 결정의 개략적인 제시 . (A) 마이크로베시클은 원형질막으로부터 세포외 공간으로 새싹을 틔운다. (B) 마이크로베시클은 동결 분획화될 때까지 P- 및 E-막 전단지로 제한되며, 이는 전단지를 분할하고 골절된 면이라고 불리는 전단지의 내부 전망을 노출시킨다. (C) Pt / C 그림자 처리 후, 두 개의 골절 된 얼굴을 식별 할 수 있습니다 : 세포질 (원형질)을 향한 볼록한 모양의 원형질 얼굴 (P-face)과 세포외 공간을 향한 오목한 모양의 외인성 얼굴 (E-face). 그림 1은 Biorender.com 를 사용하여 만들었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
도 2: EVs의 단리. (A) CO2 인큐베이터에서 성장한T24 세포를 MV 분리 전에 이들의 생존력 및 합류성을 확인하기 위해 (B) 광학 현미경으로 조사하였다. (c) 세포 배양 배지를 수집하고, (D) 상층액이 수집될 때마다 300 × g 및 2,000 × g에서 연속적으로 원심분리한다. (F, G) 10,000 × g에서 원심분리 후, 펠렛을 나타내는 백색 패치가 보이고 표시된다. 상청액을 제거하고 (H) 고정제를 재현탁하지 않고 조심스럽게 펠렛에 첨가합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3: EV의 동결 . (A) 중앙 구덩이가 있는 공기 건조된 깨끗한 구리 운반선은 (B) 처리 전에 표시되어 있습니다. 마이크로베시클은 글리세롤에 재현탁되어 균질한 샘플을 수득하고, (C) 입체현미경 하에서 쿠퍼 담체의 중앙 구덩이에 첨가한다. (D) 중앙 구덩이에 볼록한 방울을 형성하도록 샘플의 부피를 추가해야합니다. (E) 동결 직전에 LN2-냉각 프레온을 금속 막대와 혼합하여 프레온을 액화시킨다. (F) 샘플을 프레온에 침지시켜 동결시킨 다음, (G) LN2로 옮긴다. (H) 동결된 샘플을 갖는 운반체는 냉동 상태로 수집되어LN2 Dewar 컨테이너에 저장될 수 있다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 4: 동결 파쇄 및 복제본 만들기. (A) 동결 파쇄 장치. 단위 챔버(B) 내부에는 백금(Pt) 및 탄소(C) 전자총, 나이프, 및 샘플 테이블이 있다. (C) 파쇄를 시작하기 위해, 샘플과 함께 캐리어를 샘플 테이블로 옮기고, (D) 동결 파쇄 유닛을 냉각하고, 진공이 확립된다. (E) 단면화는 칼의 전동 (F) 운동에 의해 수행되지만 파쇄는 수동으로 수행하는 것이 바람직합니다. (G) 절편화 전 및 (H) 파쇄 후 샘플. (I) 파쇄 직후, 복제본이 만들어진다. (J) 이 과정 동안, Pt는 샘플에 그림자가 드리워진다. 플래티넘 섀도잉은 챔버에서 밝은 빛 (스파크)으로 간주됩니다. (K) 샘플 담체는 물로 잘 채워진 도자기에 수집된다. (l) 세척 단계 동안 차아염소산나트륨 용액에 부유하는 복제물(화살표). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 5: 동결 파단 및 Pt/C 섀도우드 MV의 전자 현미경 사진. (A) 낮은 배율에서 동결 파단 및 섀도우된 EV 펠릿의 개요. 균질 표면은 배경 (ii), 밝은 영역은 복제본 (iii)의 파열, 어두운 영역은 복제본의 주름 (별표), 불규칙한 조광기 그림자는 얼음 결정 (별표 두 개)으로 인한 것입니다. (B) 오목하고 볼록한 표면을 가진 둥근 모양의 EV의 클러스터. (C) EV의 높은 배율. EV 멤브레인의 P면을 나타내는 볼록한 골절에서는 막내 입자 (화살표)와 매끄러운 표면 (화살촉)의 패치가 보입니다. 길쭉한 (별)과 평평한 공 모양 (두 개의 별)이있는 세포 밖 소포가 발견됩니다. (d) 분리된 비뇨생식기 MVs의 평균 직경은 Hallett et al.17에 의해 제안된 바와 같은 크기 측정에 따라 304 nm ± 10 nm이다. 데이터는 MV의 평균 ± SEM. (E,F) E-페이스 및 P-페이스로 제시됩니다. 범례: 화살표 = P면의 막내 입자, 둘러싸인 화살표 = P-C 섀도잉의 방향. 스케일 바: A = 10 μm, B-F = 400 nm. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
MV 또는 격리 된 EV의 다른 집단의 특성화는 "omics"연구 또는 기능 연구11,18과 같은 다운 스트림 분석을 시작하기 전에 시작하는 것이 가장 중요합니다. 본원에서, 인간 침습성 방광암 비뇨생식기 T24 세포로부터의 EVs를 원심분리에 의해 단리하고, 동결파괴 전자 현미경에 의한 분석을 위해 제공된 프로토콜에 따라, 단리된 분획이 MVs11,13에서 풍부하다는 것을 입증하였다. MVs의 분리에는 세포 파편이나 소기관이 없었으며 성공적인 분리 및 정제 프로토콜을 확인했습니다.
프로토콜의 중요한 단계인 화학적 고정과 동결의 조합은 EV(12)의 구형 형상을 유지하였다. 그러나, 동결 파쇄(17)에 의해 EV 직경을 평가할 때는 주의가 필요하다. 골절이 샘플을 무작위로 통과하기 때문에 MV 멤브레인은 적도 및 비 적도 평면으로 분할됩니다. 동결 파단 및 그림자 표본의 이미지를 분석하기위한 엄격한 방법을 제공하기 위해 Hallett et al.은 평균 소포 직경이 이미지17의 실제 소포 직경의 4/π 배임을 보여주었습니다. 이를 고려하여, T24 세포로부터의 EVs는 304 nm의 직경을 갖는 것으로 계산되었으며, 이는 MV의 이론적 크기 분포 범위인 100-1000 nm19에 적합하다.
동결 파쇄는 EV를 시각화하기 위해 가장 광범위하게 사용되는 TEM 기술인 음성 염색을 보완 할 수 있습니다. 음성 염색에 의해, 샘플은 일반적으로 화학적으로 고정되고, 건조되고, TEM 그리드에 부착되고, 우라닐 용액과 대조된다. 지원 매체가 없으면 EV가 붕괴되는 경향이 있으므로 컵 모양의 모양이됩니다. 동결 파쇄에 의해, 우리는 MV가 세포외 공간과 체액(12)에서 그들의 형태를 반영하는 구체들임을 보여준다. 이에 의해, 우리의 결과는 또한 냉동 초박형 섹션20에서 EV의 관찰과 일치합니다.
동결 파괴 기술의 중요한 장점은 EV가 수용자 멤브레인을 표적으로 삼고 상호 작용하는 방식을 이해하는 핵심 요소인 제한 멤브레인의 내부 조직을 해결할 수 있는 능력입니다. 여기에서, 우리는 MV의 멤브레인을 분석했지만, 동결 파쇄는 EV의 다른 집단의 막 조직을 나타낼 수 있습니다. MVs는 원형질막 출아에 의해 형성되고; 따라서, 원형질막 단백질 및 단백질 클러스터는 MV 막에서 발견될 것으로 예상된다. 우리의 결과는 T24 세포의 MV가 막내 입자를 함유하여 필수적인 막 단백질을 제시한다는 것을 뒷받침했습니다. E-face와 P-face 사이의 입자 분포에 기초하여, MVs에서 관찰된 입자가 비뇨생식기 세포 특이적21,24인 막횡단 단백질 우로플라킨일 것으로 예상하는 것이 합리적이다. 관찰된 입자는 희소하였고, 이는 비뇨생식기 발암 동안 우로플라킨의 감소를 보고한 이전 연구에 따른것이다 21,22,23. 그러나, MV 막의 단백질 조성을 더 조사하기 위해, 동결-파괴 복제 면역-표지(FRIL) 기술의 사용이 권장된다. FRIL은 제시된 동결 파괴 기술의 업그레이드이며 항체 인식24,25에 의해 복제본에서 단백질의 동일성을 밝히는 데 전념하고 있습니다. 요약하면, 동결 파괴 기술은 단리된 EV 분획의 형상, 크기 및 순도뿐만 아니라 EV 제한 멤브레인의 특성화에 적합한 전자 현미경 기술이다. 제시된 프로토콜은 또한 분리된 EV들의 다른 집단들의 평가를 위해 사용될 수 있다; 따라서, 동결 파쇄 기술은 EV 제한 막의 조직을 탐구하는 연구를위한 국제 세포 밖 소포 학회 지침에 포함시킬 가치가 있습니다.
공개
저자는 이해 상충을 선언하지 않습니다.
감사의 말
이 연구는 슬로베니아 연구 기관 (연구 핵심 자금 없음)에 의해 자금 지원되었다. P3-0108 및 프로젝트 J7-2594) 및 MRIC UL IP-0510 인프라 프로그램. 이 연구는 COST (유럽 과학 기술 협력)의 지원을 받아 주산기 유도체에 대한 연구를 치료 접근법 (SPRINT)으로 번역하기위한 COST Action CA17116 국제 네트워크에 기여합니다. 저자는 세포 배양 및 샘플 준비에 대한 기술적 도움을 주신 Linda Štrus, Sanja Čabraja, Nada Pavlica Dubarič 및 Sabina Železnik에게 감사 드리며 Marko Vogrinc, Ota Širca Roš 및 Nejc Debevec에게 비디오 준비에 기술적 인 도움을 주신 것에 대해 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| A-DMEM | ThermoFisher Scientific, USA | 12491015 | |
| Balzers freeze-fracture device | Balzers AG, Liechtenstein | Balzers BAF 200 | |
| Centrifuge | Eppendorf, Germany | model 5810R | |
| CO2 incubator HeraCell | Heraues, Germany | ||
| Copper carriers | Balzers | BB 113 142-2 | 100+ mesh |
| Copper grids | SPI, United States | 2010C | |
| Culture flask T75 | TPP, Switzerland | growing surface 75 cm2 | |
| F12 (HAM) | Sigma-Aldrich, Germany | 21765029 | |
| FBS | Gibco, Life Technologies, USA | 10500064 | |
| Glazed Porcelain Plate 6 Well | Fischer Sientific, United States | 50-949-072 | |
| Glycerol | Kemika, Croatia | 711901 | final concentration 30 % (v/v) |
| Glutaradehyde | Serva, Germany | 23114.01 | final concentration 2.5 % (v/v) |
| GlutaMAX | Gibco, Life Technologies | 35050-079 | final concentration 4 mM |
| Penicillin | Gibco, Life Technologies | 15140163 | final concentration 100 U/ml |
| Phase-contast inverted microscope | Nikon, Japan | model Eclipse | |
| Rotor | Eppendorf, Germany | A 4-44 | |
| Rotor | Eppendorf, Germany | F-34-6-38 | |
| Serological pipetts | TPP, Switzerland | 50mL volume | |
| Sodium hypochloride solution in water | Carlo Erba, Italy | 481181 | |
| Stereomicroscope | Leica, Germany | ||
| Streptomycin | Gibco, Life Technologies | 35050038 | final concentration 100 mg/mL |
| Transmission electron microscope | Philips, The Netherlands | model CM100 | working at 80 kV |
| Tweezers | SPI, United States |
참고문헌
- Raposo, G., Stoorvogel, W. Extracellular vesicles: Exosomes, microvesicles, and friends. The Journal of Cell Biology. 200 (4), 373-383 (2013).
- Willms, E., Cabanas, C., Mager, I., Wood, M. J. A., Vader, P. Extracellular vesicle heterogeneity: Subpopulations, isolation techniques, and diverse functions in cancer progression. Frontiers in Immunology. 9, 738(2018).
- van Niel, G., D'Angelo, G., Raposo, G. Shedding light on the cell biology of extracellular vesicles. Nature Reviews Molecular Cell Biology. 19, 213-228 (2018).
- Cocucci, E., Racchetti, G., Meldolesi, J. Shedding microvesicles: Artefacts no more. Trends in Cell Biology. 19 (2), 43-51 (2009).
- Urabe, F., et al. Extracellular vesicles as biomarkers and therapeutic targets for cancer. American Journal of Physiology-Cell Physiology. 318 (1), 29-39 (2020).
- Tricarico, C., Clancy, J., D'Souza-Schorey, C. Biology and biogenesis of shed microvesicles. Small GTPases. 8 (4), 220-232 (2017).
- Georgantzoglou, N., Pergaris, A., Masaoutis, C., Theocharis, S. Extracellular vesicles as biomarkers carriers in bladder cancer: Diagnosis, surveillance, and treatment. International Journal of Molecular Sciences. 22 (5), 2744(2021).
- Słomka, A., Urban, S. K., Lukacs-Kornek, V., Żekanowska, E., Kornek, M. Large extracellular vesicles: Have we found the holy grail of inflammation. Frontiers in Immunology. 9, 2723(2018).
- Han, L., Lam, E. W. F., Sun, Y. Extracellular vesicles in the tumor microenvironment: Old stories, but new tales. Molecular Cancer. 18 (1), 59(2019).
- Muralidharan-Chari, V., Clancy, J. W., Sedgwick, A., D'Souza-Schorey, C. Microvesicles: Mediators of extracellular communication during cancer progression. Journal of Cell Science. 123, 1603-1611 (2010).
- Kowal, J., et al. Proteomic comparison defines novel markers to characterize heterogeneous populations of extracellular vesicle subtypes. Proceedings of the National Academy of Sciences of the United States of America. 113 (8), 968-977 (2016).
- Thery, C., Amigorena, S., Raposo, G., Clayton, A. Isolation and characterization of exosomes from cell culture supernatants and biological fluids. Current Protocols in Cell Biology. , Chapter 3, Unit 3.22 (2006).
- Thery, C., et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): A position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. Journal of Extracellular Vesicles. 7 (1), 1535750(2018).
- Severs, N. J. Freeze-fracture electron microscopy. Nature Protocols. 2 (3), 547-576 (2007).
- Severs, N. J., Robenek, H. Freeze-fracture cytochemistry in cell biology. Methods in Cell Biology. 88, 181-186 (2008).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529(2017).
- Hallett, F. R., Nickel, B., Samuels, C., Krygsman, P. H. Determination of vesicle size distributions by freeze-fracture electron microscopy. Journal of Electron Microscopy Technique. 17 (4), 459-466 (1991).
- Nigro, A., et al. Selective loss of microvesicles is a major issue of the differential centrifugation isolation protocols. Scientific Reports. 11, 3589(2021).
- Szatanek, R., et al. The methods of choice for extracellular vesicles (EVs) characterization. International Journal of Molecular Sciences. 18 (6), 1153(2017).
- Iliev, D., et al. Stimulation of exosome release by extracellular DNA is conserved across multiple cell types. The FEBS Journal. 285 (16), 3114-3133 (2018).
- Zupančič, D., Zakrajšek, M., Zhou, G., Romih, R. Expression and localization of four uroplakins in urothelial preneoplastic lesions. Histochemistry and Cell Biology. 136 (4), 491-500 (2011).
- Wu, X. R., Manabe, M., Yu, J., Sun, T. T. Large scale purification and immunolocalization of bovine uroplakins I, II, and III. Molecular markers of urothelial differentiation. The Journal of Biological Chemistry. 265 (31), 19170-19179 (1990).
- Kreft, M. E., Hudoklin, S., Jezernik, K., Romih, R. Formation and maintenance of blood-urine barrier in urothelium. Protoplasma. 246 (1-4), 3-14 (2010).
- Kreft, M. E., Robenek, H. Freeze-fracture replica immunolabelling reveals urothelial plaques in cultured urothelial cells. PLoS One. 7 (6), 38509(2012).
- Robenek, H., et al. Topography of lipid droplet-associated proteins: Insights from freeze-fracture replica immunogold labeling. Journal of Lipids. 2011, 409371(2011).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유