JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
Telomere G - 오버행 구조의 시험 Trypanosoma brucei
요약
Telomeres는 염색체의 안정성을 위해 필수이며 telomere G - 오버행 구조는 telomerase - 중재 telomere의 유지 보수를 위해 필수적입니다. 우리는 최근 telomere G - 오버행 구조의 검출을위한 두 가지 방법을 채택했습니다 Trypanosoma brucei 이는 인 겔 하이브 리다이 제이션 및 설명됩니다 내고 - 중재 뇌관 확장, 기본 있습니다.
초록
telomere G - 오버행 구조는 효모, 척추 동물, 그리고 Trypanosoma brucei 등 많은 eukaryotes에서 발견되었습니다. 그것은 드 노보 telomere DNA 합성에 대한 telomerase를위한 기판 역할 및 telomere 유지 보수에 대한 것이 중요합니다. T는 brucei은 가축의 인간과 nagana에 수면병 일으키는 protozoan 기생충이다. 일단 감염된 포유류의 호스트, T. brucei 세포 정기적으로 숙주의 면역 공격을 회피하기 위해 표면 항원을 전환됩니다. 우리는 최근에 보여준 그 T. brucei telomere 구조 T.에 대한 중요 표면 항원 유전자 발현의 조절에 중요한 역할을 brucei의 pathogenesis. 그러나, T. brucei telomere 구조는 광범위이 전문 구조 분석 방법의 한계로 인해 연구되지 않았습니다. 우리는 이제 성공적으로 하이브리드화 및 telomere G - 오버행 구조의 심사 T.의 뉴클레오 티드 telomere 터미널의 결정을위한 어댑터 내고 방법에 대한 결합 - 중재 뇌관 확장 방법 - 겔의 기본을 채택했습니다 brucei 세포. 여기서는 자세하게 프로토콜을 설명하고 그들의 다양한 장점과 한계를 비교합니다.
프로토콜
1. 검색 T. brucei Telomere 네이티브를 사용하여 G - 오버행 인 겔 하이브 리다이 제이션 3
원리 (그림 1) 기본 조건, 최종 레이블 (CCCTAA) 4 (TELC) oligo 프로브는 단일 좌초 telomere G - 오버행 영역에 잡종 수 있습니다. 하이브리드화 강도는 오버행의 길이에 비례합니다. 변성 및 중화 후, 동일한 프로브는 전체 telomere 지역에 잡종을하실 수 있습니다. 하이브리드화 강도는 총 telomere의 DNA 금액을 나타냅니다하고 읽어 컨트롤로 사용할 수 있습니다. 본 실험의 두 가지 표준 컨트롤 T. 같은 신호를 얻을 수 없습니다 최종 레이블 (TTAGGG) 4 (TELG) oligo 프로브를 사용하여 하이브리드화 아르 brucei 세포는 원시 TELC 하이브 리다이 제이션 신호를 제거해야하는, telomere C - 오버행 구조를하지 않으며, 사전 하이브리드화 이러한 엑소 I 또는 엑소 T와 같은 3' - 특정 단일 좌초 exonucleases와 게놈 DNA를 처리합니다.
1 단계. 펄스 필드 겔 전기 영동 (PFGE)에 대한 DNA 플러그 준비
손상 염색체는 PFGE로 구분됩니다. 따라서, 게놈 DNA는 DNA의 플러그로 준비가되어 있습니다.
- 혈류 양식 세포의 100 ML (1.5 -2 만 셀 / ML에서) 또는 procyclic 전지 (10000000 셀 / ML에서) 20 ML과 함께 시작합니다.
- 낮은 용융 점 L 버퍼 (LMP) 아가로 오스 (0.01 M 트리스가 • CL 산도 7.6, 0.02 M NaCl, 0.1 M EDTA (에틸렌 다이아 민 테트라 초산) 산도 8.0)과 50가 따뜻하게 ° C. 1.6 %를 디졸브
- 1.5 krpm에서 원심 분리하여 세포를 수확 10 분 4 ° C. 5,000,000 세포 / ML의 최종 농도 L 버퍼로 뜨는 및 resuspend 세포 펠렛을 제거합니다.
- 10 분 42-50 ° C에서 세포 현탁액을 품어.
- 세포 1 볼륨에 LMP 아가로 오스 1 볼륨을 추가합니다. 잘하지만 빨리 섞는다.
- 일회용 플러그 금형 (BioRad)의 각 웰에 세포 현탁액의 나누어지는 85 μL.
- 50-10 분 후 또는 때까지 플러그는 전송 플러그 15 ML 코니컬 튜브 5 ML의 L 버퍼 / 1 % Sarkosyl로로, 확정됩니다. 250 MG / ML proteinase K 또는 proteinase K 분말의 핀치 100 μL를 추가 잘 혼합하고, 50 품어 ° C를 48 시간을위한.
- 버퍼를 삭제, 두 번 L 버퍼의 5 ML과 플러그를 씻고 다른 48 시간을위한 proteinase K의 소화를 반복합니다. 다시 신선한 L 버퍼와 플러그를 씻으십시오. 저장소가 4 플러그 ° L 버퍼에 C. 이 플러그는 2 주 이내에 사용해야합니다.
2 단계. 별도 그대로 T. 펄스 필드 겔 전기 영동을 사용하여 brucei 염색체
- 아가로 오스 겔 준비
- 0.5 X TBE 버퍼와 요리사 DRII (BioRad) 단위의 젤 실행 실로 전송로부터 2-3 패를 준비합니다. 실행중인 온도를 설정 펌프를 시작한 후 냉각 장치를 시작합니다.
- 0.5 X TBE 버퍼의 1.2 % 아가로 오스 겔 100 ML를 준비합니다. 쿨 아가로 오스는 겔 트레이를 설정하는 동안.
- 샘플 순서를 결정합니다. DNA 표준을 포함하는 것을 잊지 말아주세요. 빗를 건조하고 평평한 표면에 그것을 믿는다. 해당 치아에 각 DNA 플러그를 놓습니다. 플러그가 치아에 붙어 있도록 열망에 의해 DNA 플러그 주위에 과도한 버퍼를 제거합니다.
- 빗를 삽입하지 않고 아가로 오스 젤 하거라. 그것이 40-50 ° C (몇 분)에 진정하자, 천천히 젤에 연결된 플러그와 빗를 삽입합니다. 플러그는 빗을를 밀어하지 않는지 확인합니다. 젤 응고하자. 천천히 젤에서 빗질을 제거합니다.
- 펄스 필드 겔 전기 영동
120 시간 12에서 700 S - 1500 S 펄스, 2.5 V / cm, ° C : 요리사 DRII 단위로 젤을 실행합니다.
3 단계. 아가로 오스 겔 스테인과 destain
다음 0.5 X TBE의 부드러운 락을 1 시간에 대한 Ethidium의 브로마이드없이 1 시간을위한 RT에서 0.5 X TBE에 1μg / ML Ethidium의 브로마이드로 겔 스테인. 젤의 사진을 가져가라.
4 단계. 아가로 오스 겔 건조
3mm 왓먼 용지의 두 레이어에있는 아가로 오스 겔을 플레이스 및 플라스틱 포장으로 젤 커버. RT (겔이 가열해서는 안됩니다 50 이상 ° C DNA 샘플의 변성을 피하기 위해).에서 젤 건조 각각 건조 2 4 시간 후 마른 사람과 함께 젖은 왓먼 용지를 교체합니다. 젤 완전히 건조 될 때까지 건조 유지. 이것은 건조기에 따라 하루 정도 걸릴 수 있습니다.
단계 5. oligo 프로브를 라벨
10 × 폴리 뉴클레오 타이드 키나제 (PNK) 버퍼, 5 μL 1 μL와 50 μL / NG TELC 또는 TELG oligo 1 μL를 섞어 γ [32P] ATP, ddH 2 O 2 μL, 그리고 T4 PNK 1 μL. 37 ° C 1 시간을위한 부화. 반응 혼합물에 TNES 버퍼 (10 MM Club 호텔 트리스, 산도 8.0, 100 MM NaCl, 10 MM EDTA (에틸렌 다이아 민 테트라 초산), 산도 8.0, 1 % SDS) 90 μL를 추가합니다.
oligoes을 라벨 있지만, G - 25 컬럼을 준비 : 3 CC 주사기로 일부 글라스 울을 넣고 피펫 팁로 단단히 내려 것들. Sephadex 잘 G - 25 (autocl로 주사기를 채우3 ML 표시) TE에 aved. 그것이 무게로 정착합시다. 라벨 프로브를 정화하려면 열 위에 프로브를로드합니다. TNES 버퍼 700 μL로 씻어 및 TNES 버퍼 600 μL와 elute. 또는, 미니 빠른 스핀을 사용하여 레이블 프로브 정화 ™ 열 (로체 응용 과학).
6 단계 : 하이브 리다이 제이션
- 간단히 증류수의 건조 겔을 습식 및 겔에 붙어있는 왓먼 용지를 멀리 세척
- 하이브 리다이 제이션 가방에 젤을 넣고 (0.25M 나 2 HPO 4 pH7.2, 1 밀리미터 EDTA (에틸렌 다이아 민 테트라 초산), 7퍼센트 SDS, 1퍼센트 BSA, 0.22 μm의 필터를 통해 필터링) hybridiztion 버퍼 20 ML를 추가합니다. ° C 부드러운 락을 최소한 1 시간 50에서 물을 욕조에 품어.
- 사전 하이브 리다이 제이션 버퍼를 제거합니다. 5 분 라벨 프로브를 삶아 신선한 하이브리드화 버퍼의 25 ML에 추가, 0.22 μm의 주사기 필터와 혼합 필터 소독 및 하이브리드화 가방에 직접 하이브 리다이 제이션 믹스를 추가합니다. 따뜻한 물로 얕은 용기에 가방과 장소를 밀봉합니다. 물 목욕으로 전체 컨테이너를 놓습니다. 부드러운 락을 함께 ° C 하루 50 알을 품다.
- 하이브 리다이 제이션 가방에 작은 오프닝 컷. 많은 하이브 리다이 제이션 혼합 가능한 밖으로 기름을 붓고 50 ML 코니컬 튜브에 저장합니다. -20 ° C.에 냉동 프로브를 유지 하이브리드화 가방에서 젤을 제거하고 용기에 넣어.
이 단계에있는 것 전부가 뜨거워 및 광범위한 세척 (벤치, 스크린, 가위, ETC. 장갑 더블 레이어를 착용해야합니다을! 니즈 것입니다! - 50 30 분 4 X SSC에 젤 와시 ° C. 신선한 세척 버퍼로 교체하고 두 번 반복합니다.
- 50 4 X SSC/0.1 % SDS에서 젤 와시 ° C.
- 3mm 왓먼의 종이에 젤 넣고 가볍게 젤 건조.
- 플라스틱 포장으로 젤 싸서 ~ 3 일 phosphorimager에 노출
- phosphorimager 스캔
- 30 분 RT에서 denaturing 버퍼 (1.5 M NaCl, 0.5 M NaOH)에 젤 알을 품다
- 중화 버퍼에서 젤 와시 (3 M NaCl, 0.5 M 트리스 • / Club 호텔의 산도 7.0) 30 분 앳 Rt
- 3 분위한 증류수로 씻어
- 1 시간 55 ° C에서 사전은 - 잡종
- 동일한 프로브 함유 55 ° C 야간에 하이브리드화 믹스를 사용하여 하이브 리다이 제이션을 반복합니다.
- 55를 제외하고 위에 설명된대로 와시 ° C.
- 젤 싸서 ~ 2 시간에 대한 phosphorimager에 노출.
- phosphorimager 스캔. 변성 후 얻은과 변성 전에 얻은 하이브리드화 신호를 정상화.
2. 어댑터 내고 6 뉴클레오 티드 Telomere 터미널을 결정
원리 (그림 2A & 2B) : 5 G - 오버행의 끝 '최종 표시된 고유 oligonucleotide는 3 출혈도 잡았입니다. 이것은 구체적인 보완 안내 oligo에 어닐링에 의해 수행됩니다. telomere G - 오버행 터미널 시퀀스와 호환만이 유일 / 가이드 oligo 어댑터 베어링 시퀀스는 출혈도 잡았 것입니다. T.에 대한 brucei, telomeres는 TTAGGG 반복의 여섯 가지 세포핵 중 하나를 종료할 수 있습니다. 따라서 여섯 가지 가이드 oligoes는 (TG1 - TG6, 그림 2A) 사용됩니다. 결합 후, DNA는 제한 endonucleases로 소화하고 아가로 오스 겔에서 해결되었습니다.
- 독특한 oligo의 키나제 치료.
10X PNK 버퍼 3 μL 10 pmole / μL 독특한 oligo 6 μL를 혼합, 5 μL γ [32 P] ATP, ddH 2 O 14 μL와 T4 PNK 2 μL (10 U). 37 ° C 1 시간을위한 혼합물을 품어. - 비법인 핫 뉴클레오 티드를 제거합니다.
비법인 뜨거운 ATP를 제거하고 용출 버퍼의 60 μL (최종 농도가 ~ 1 pmole / μL 것입니다)와 함께 최종 레이블 oligo를 elute하는 Qiaquick 염기 제거 키트를 사용하십시오. - 가이드 oligo 고유의 oligo를 (어댑터를 만들려면) 어닐링.
각 가이드 oligo 1 μL 어닐링 버퍼 (200 MM NaCl, 100 MM 트리스 - HCL pH는 8.0) 2 μL에 고유한 oligo 투석을 10 μL를 추가합니다. 85 ° C 열 블록에 튜브를 넣고 열을 차단을 해제하십시오. RT로 냉각 튜브 및 열 블록을 봅시다. 이것은 몇 시간이 소요됩니다. 경우 서둘러, 전송 튜브 65-5 분 후 각 ° C, 37 ° C 다음 다음 RT에게 그것은 식지. - Ligate 어댑터는 게놈 DNA를 총.
그대로 게놈 DNA 2.5 μL하기 위해, 5 X Ligase 버퍼, annealed oligos 10 μL, ddH 2 O 2.5 μL, 그리고 T4 DNA Ligase의 1 μL 4 μL를 추가합니다. ° C 하루 16 알을 품다. - 제한 Endonuclease의 소화
결합 제품의 20 μL 10 X 코 버퍼 4 3 μL, AluI 및 MboI 각 1.5 μL, 그리고 ddH 2 O. 4 μL를 추가 ° C 야간 37 혼합물을 품어. - 전기 영동.
각 샘플 10 X 오렌지 G 염색 (50 % 글리세롤, 0.5 % 오렌지 G) 3 μL를 추가합니다. 0.2 μg / ML의 Ethidium의 브로마이드와 함께 0.5 X TBE에서 20X20 cm 0.7 % 아가로 오스 겔의 DNA 샘플을로드합니다. 다음, 30 분 30V에서 실행합니다높은 전압하지만 1000 V HR의 총 120V 이하로 ontinue. DNA 마커 옆에 통치자로 젤의 사진을 가져가라. - 건조 겔 및 노출.
DE81 필터 종이와 3mm 왓먼 용지의 두 레이어의 레이어에있는 아가로 오스 젤을 넣고 플라스틱 포장으로 젤 커버. RT에서 건조 겔. 하룻밤 phosphorimager에 건조 겔을 폭로.
3. 결합의 중재 프라이머 확장 6
원리 (그림 2A 및 2C) : 독특한 oligonucleotide는 어댑터 (가이드) oligo에서의 상호 보완적인 시퀀스에 의해 결정, 3 'G - 오버행 특정 터미널 시퀀스에 출혈도 잡았 있습니다. 정화 후, G-overhang/unique oligo에 annealed 남아있는 레이블 가이드 oligo는 스트랜드 변위 및 5' - 3 'exonuclease 활동이 부족 T4의 DNA 중합 효소를 사용하여 SS - DS의 교차점까지 확장 입문서이다. 프라이머 확장 제품은 따라서 G - 오버행의 길이를 제공합니다.
- 가이드 독특한 oligoes의 키나제 치료
- 10 × PNK 버퍼, 20 μL 5 X ligase 버퍼 (10 MM ATP 포함), T4 PNK 3 μL (30 U), 그리고 ddH 2 O 47 μL의 10 μL 10 pmole / μL 독특한 oligo 20 μL를 혼합 . 37 ° C 60 분 혼합물을 품어.
- 10 × PNK 버퍼, 2 μL 1 μL 10 pmole / μL 가이드 oligo 1 μL를 섞어 γ [32 P] ATP, T4 PNK 1 μL (10 U), 그리고 ddH 2 O. 5 μL 37 ° C 60 분 혼합물을 품어.
- 가이드 oligo 독특한 oligo를 어닐링
1.5 ML Eppendorf 튜브에 최종 레이블 가이드 oligo (oligo를 안내하는 고유의 2시 1분 비율은 모든 가이드 oligo가 annealed 것을 보장의 phosphorylated 독특한 oligo와 10 μL (10 pmole) 10 μL (20 pmole)를 추가 ). oligoes를 어닐링을위한 프로토콜 II에서 설명한 동일한 절차를 따르십시오. - telomere 엔드에 annealed 가이드 / 독특한 oligo 어댑터를 Ligate
DNA의 결합에 대한 프로토콜 II에서 설명한 동일한 절차를 따르십시오. - 석출물의 아세트산 나트륨의 10분의 1 볼륨 DNA와 -80에서 얼음처럼 차가운 에탄올 2.5 볼륨 ° C 30 분. 15 분 12 krpm, 4 ° C에서 DNA 펠렛을 스핀. 에탄올 70 %와 DNA를 씻고 ddH 2 O. 10 μL의 팔레트를 해산
- 프라이머 확장
각 10 μL의 DNA 샘플 2 10 × T4의 DNA 중합 효소 버퍼의 μL, 1 MG / ML BSA 1 μL, 25 MM dATP, dCTP 1 μL, 그리고 dTTP 각 T4의 DNA 중합 효소 1 μL (3 U) 추가 그리고 ddH 2 O. 3 μL
효소, 버퍼 등 각 DNA 샘플을 마스터 믹스 나누어지는 적절한 양의 마스터 믹스를 확인하십시오. 30 ° C 30 분 알을 품다. 다음 반응에 즉시 0.5M EDTA (에틸렌 다이아 민 테트라 초산) 1.2 μL를 추가합니다. - 전기 영동
10 % 아크릴 아미드 / 7 M urea/1xTBE 젤의 확장 제품을 실행합니다. 각 샘플 4 μL를로드합니다. 로드하기 전에 10 분 샘플을 끓여. 파란색 염료가 젤 하단에 도달할 때까지 1X TBE에서 800V에서 실행합니다. 65 젤 드라이 ° C 30 분 RT에서 다음 30 분 및 2 시간에 대한 phosphorimager에 노출.
10 % polyacrylamide 젤 100 ML를 준비하려면, 10X TBE 10 ML을 추가, 증류수 30 ML에 요소의 41g과 40 % 아크릴 아미드 용액 (아크릴 아미드 / 비스 - 아크릴 아미드 29:1) 21 ML을 풀다. 유리 접시를 조립. 오른쪽 젤 쏟아져 전에 10 % APS 1 ML와 TEMED 100 μL를 추가합니다. 젤 붓고하고 거품을 방지하려고합니다.
4. 대표 결과 :
검색 T. 기본 인 겔 하이브 리다이 제이션을 사용 brucei telomere G - 오버행 구조
그대로 T. PFGE으로 구분 brucei의 염색체는 그림 3A와 3B (왼쪽 패널)에 표시됩니다. T.는 brucei 세포는 일반적으로 모든 minichromosomes의 ~ 100 사본, 유사한 크기를 (50-150킬로바이트)를 포함하고 젤에 동일한 위치 (MC)로 마이 그 레이션. 이 사실로 인해, TELC oligo 프로브, telomere G - 오버행 신호가 minichromosomes (그림 3A, 중앙 패널)에서 가장 눈에 띄는이다와 하이브리드화 후. TELG oligo 프로브와 하이브리드화 일반적으로 하이브리드화 어떤 신호를 얻을 수 없습니다 (그림 3B, 중앙 패널) 때문에 T. brucei 세포는 telomere C - 오버행 구조가 없습니다. TELC 또는 TELG oligo 프로브 하나와 변성 및 중화, 하이브리드화 모든 염색체 종료 (그림 3A 및 3B, 오른쪽 패널)에 telomere 신호를 공개한다 후에.
어댑터 내고 의해 염기 telomere 터미널 결정
각 차선의 DNA의 동일한 금액을 로딩하면이 분석을 위해 필수적이며, 이것은 젤의 Ethidium의 브로마이드 얼룩으로 표시됩니다. 예를 들어 그림 4A, 왼쪽 패널에 표시됩니다.
이 프로토콜에서 최종 라벨 고유 oligo 및 가이드 oligo 어댑터는 염색체 끝에 출혈도 잡았 때 가이드 oligo와 호환됩니다 시퀀스로 끝나는 telomere G - overhangs. 시 독특한 oligo이 최종 분류는 제정신을, 결합 제품은 방사성하고 강력한 신호를 제공합니다. 그림 4A, 오른쪽 패널에 표시된 차선 1 unique/TG1 어댑터의 대량이 telomere 끝에 출혈도 잡았되었음을 나타내는 강력한 신호를 제공합니다. TG1은 '5'CCCTAA3의 끝 순서가 있습니다. 따라서 telomere G - overhangs는 5'TTAGGG3 '이 어댑터 종료 출혈도 잡았. 결합 제품에 대한 상당한 금액 TTAGGG로 끝나는 telomeres는 T.에 지배되는 나타내는 다른 가이드 oligoes를 사용하지 관찰 brucei 세포.
3 '걸리다 특정 nucleases 아르 엑소 I 또는 엑소 T와 게놈 DNA를 처리, 내고 실제로 telomere에서 이어진 나타내는 내고 제품의 손실 (그림 4A, 오른쪽 패널, 차선 2 & 3) 결과 G - 오버행 구조
결합의 중재 프라이머 확장
내고없이, 최종 레이블 가이드 oligo 22 NT 깁니다. 로딩 종료하면 - 레이블 가이드 oligo는 대조군과 크기의 표식 역할을합니다. (그림 4B, 레인 11, 별표 끝을 나타내는 레이블 가이드 oligo). 우리는 일반적으로 또한 대부분 잔류 이외의 변성 어댑터있는이 대조군 (그림 4B, 레인 11, 오픈 삼각형)에서 ~ 44 NT의 밴드를 관찰합니다. 염색체 끝에 결합 후, 확장 제품의 크기는 G - 오버행 구조의 길이를 나타냅니다. 대부분의 T. 5'TTAGGG3에 brucei telomere G - overhangs 끝 '(그림 4A). 그러나 이러한 G - overhangs이 제품은 더 이상 가이드 oligo 자체 (그림 4B, 레인 10) 이상하지 않는 출혈도 잡았 TG1 가이드 oligo의 연장으로서, (단 ~ 10 NT 길이) 매우 짧은 것으로 나타나지만, 그들은 결합을 허용 TG1 어댑터 (그림 4A, 오른쪽 패널, 레인 1). TG4 어댑터의 단지 소량이 telomere 종료 (그림 4A, 오른쪽 패널, 레인 6) 출혈도 잡았지만, 출혈도 잡았 TG4에서 확장 제품은 긴 제품이 있기 때문에 (그림 4B, 레인 7, 화살표 머리) 훨씬 더 이상 ~ 55 NT. 따라서, 우리는 T.의 telomere 두 가지 유형의 G - 오버행을 관찰 brucei 세포. 하지만 5'TTAGGG3 '의 주된 telomere G - overhangs 엔드 겨우 ~ 10 NT 있습니다. 5'GGGTTA3에 몇 telomere G - overhangs 엔드 '는하지만, 40 NT 길이 최대 개까지하실 수 있습니다. G - 걸리다 두 종류 엑소 T (또는 엑소 I) 치료 (; 그림 4B, 레인 1, 화살표 그림 4A, 오른쪽 패널, 레인 2, 3, 7)에 민감합니다.

그림 1. 기본 인 겔 하이브 리다이 제이션의 원리. 왼쪽, 기본 조건, 최종 분류 TELC oligo 프로브는 단일 좌초 G 풍부한 telomere 오버행과 잡종 수 있습니다. 하이브 리다이 제이션의 강도는 telomere의 G - 오버행의 길이를 나타냅니다. 맞아요, 변성 후, TELC oligo 프로브는 telomere의 DNA와 잡종을 것입니다. 이 하이브 리다이 제이션의 강도는 telomere DNA의 총 금액을 나타냅니다하고 읽어 컨트롤로 사용되며, 최종 G - 오버행 수준은 변성 후 얻은하여 네이티브 하이브리드화 신호를 나누어 계산됩니다.
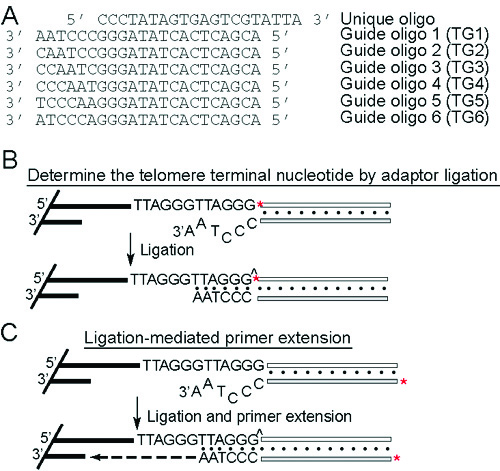
그림 2. 독특한 여섯 안내 oligoes의 어댑터 내고과 결합의 중재 프라이머 확장의 원리. (A) 시퀀스. (B) 어댑터 내고 의해 염기 telomere 터미널을 확인합니다. 독특한 oligo는 최종 표시된 (빨간색 별표로 표시), 가이드 oligoes에 annealed 및 telomere 끝까지 출혈도 잡았. 독특한 / 가이드 어댑터가 터미널 telomere 순서 어댑터가 출혈도 잡았 수와 호환되는 3 '오버행을지지 때만. (C) 내고 중재 뇌관 확장에서 가이드 oligo는 최종 표시된 (빨간색 별표로 표시)와 염색체 끝을 출혈도 잡았 전에 독특한 oligo에 annealed. 단지 G - 오버행과 호환 3 '오버행을 간직한 독특한 / 가이드 어댑터가 출혈도 잡았 것입니다. ^ 출혈도 잡았 phophordiester 결합을 나타냅니다. unligated oligo의 쌍 제거 후 프라이머 확장 스트랜드 변위와 '5' - 3 exonuclease 활동 부족 T4의 DNA 중합 효소와 함께 진행됩니다. 확장 가이드 oligo의 마지막 길이 따라서 G - 오버행의 길이를 나타냅니다.
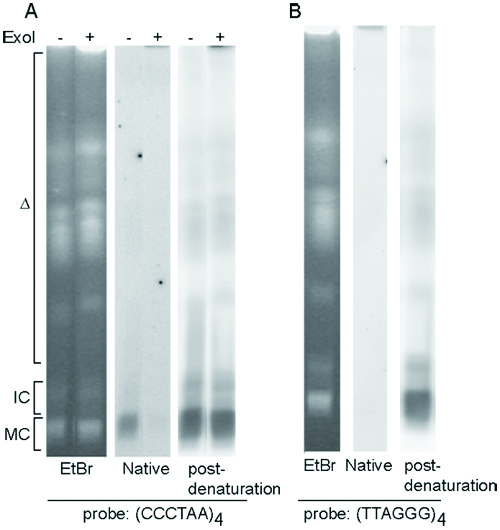
그림 3. T. brucei telomere G - 오버행 구조 분석 네이티브로 인 겔 하이브 리다이 제이션. TELC oligo 프로브와 (과)에서 - 겔 하이브 리다이 제이션. TELG oligo 프로브와 (B) 인 겔 하이브 리다이 제이션. 모두에서 (A)와 (B) 왼쪽, Ethedium의 브로마이드 자국 PFG. 중간, 기본 하이브리드화 결과. 맞아, 포스트 변성의 하이브리드화 결과. 야생 형 T. brucei 세포가 사용되었습니다. 전 게놈 DNA를 취급 손상 또는 엑소는 PFGE로 구분했다. 열기 삼각형 megabase 염색체의 약자로, IC, 중간 크기의 염색체, MC, minichromosomes.
"/>
그림 4. T. brucei telomere G - 오버행 구조가 결합 - 중재 뇌관 확장에 의해 분석. (A) 대부분의 T. brucei telomere G - overhangs '는 5'TTAGGG3에 종료할 수 있습니다. 왼쪽 Ethedium 브로마이드 스테인드 DNA 젤. DNA의 약 동일한 금액은 각 레인에로드됩니다. 맞아, 건조 후 동일한 젤의 노출 결과. 그대로, 엑소는 I - 처리 또는 표시와 같은 엑소 T - DNA 처리는 여섯 가지 최종 레이블 가이드 / 독특한 oligo 어댑터 출혈도 잡았습니다. (B) T. brucei의 telomeres 짧은 G - overhangs 있습니다. 손상 또는 엑소 T - 치료를 게놈의 DNA는 T4의 DNA 중합 효소를 사용하여 뇌관 확장 다음 여섯 가지 가이드 / 독특한 oligo 어댑터 출혈도 잡았습니다. 최종 분류 TG4 oligo는 대조군 (레인 11)으로로드되었습니다. oligo 자체는 22 NT (*)를 실행뿐만 아니라 ~ 44 NT (Δ)에 약해요 신호를 주었다. 오직 unique/TG4 어댑터는 상당히 더 이상 가이드 oligo 자체 (화살표 머리, 레인 7) 이상의 확장 제품이 나왔고.
토론
Trypanosoma brucei은 인간의 질병을 자고됩니다. 이 질병은 치료 왼쪽면, 필연적으로 치명적이다. T는 포유류의 호스트에서 brucei 전지는 정기적으로 너무 호스트의 면역 공격 7 피하기 위해 같은 antigenic 변화을 받고있다. 따라서 그것은 T.을 제거하는 것은 매우 어렵습니다 감염되면 brucei 세포가 설정됩니다. 우리는 최근 telomeres가 T.의 표현 규제에 중요...
공개
감사의 말
우리는 과학적인 토론과 통찰력 제안에 대한 박사 캐롤린 가격 감사드립니다. 이 작품은 NIH 부여 AI066095 (비보 리튬 PI)에 의해 지원됩니다.
자료
| Name | Company | Catalog Number | Comments |
| SeaKem LE Agarose | Lonza Inc. | 50004 | |
| Agarose Type VII (low melting agarose) | Sigma-Aldrich | A4018 | |
| Proteinase K, recombinant, PCR grade | Roche Group | 03 115801001 | |
| Exo I | New England Biolabs | M0293 | |
| Exo T | New England Biolabs | M0265 | |
| T7 exonuclease | New England Biolabs | M0263 | |
| T4 DNA polymerase | New England Biolabs | M0203 | |
| QIAquick nucleotide removal kit | Qiagen | 28304 |
참고문헌
- Munoz-Jordan, J. L., Cross, G. A., de Lange, T., Griffith, J. D. t-loops at trypanosome telomeres. EMBO J. 20, 579-588 (2001).
- Li, B., Espinal, A., Cross, G. A. M. Trypanosome telomeres are protected by a homologue of mammalian TRF2. Mol Cell Biol. 25, 5011-5021 (2005).
- Wellinger, R. J., Wolf, A. J., Zakian, V. A. Saccharomyces telomeres acquire single-strand TG1-3 tails late in S phase. Cell. 72, 51-60 (1993).
- McElligott, R., Wellinger, R. J. The terminal DNA structure of mammalian chromosomes. EMBO J. 16, 3705-3714 (1997).
- Harrington, L. A., Greider, C. W. Telomerase primer specificity and chromosome healing. Nature. 353, 451-454 (1991).
- Jacob, N. K., Skopp, R., Price, C. M. G-overhang dynamics at Tetrahymena telomeres. Embo J. 20, 4299-4308 (2001).
- Barry, J. D., McCulloch, R. Antigenic variation in trypanosomes: enhanced phenotypic variation in a eukaryotic parasite. Adv Parasitol. 49, 1-70 (2001).
- Yang, X., Figueiredo, L. M., Espinal, A., Okubo, E., Li, B. RAP1 is essential for silencing telomeric variant surface glycoprotein genes in Trypanosoma brucei. Cell. 137, 99-109 (2009).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유