Method Article
Bioluminescence 이미징을 사용하여 종양 성장과 치료에 반응 이후 분석 Intracranial 뇌종양의 Xenografts 구축
요약
루시페라제 - 수정된 인간의 뇌 종양의 xenografts은 종양 성장과 bioluminescence 이미징을 사용하여 치료에 대한 응답의 후속 모니터링과 athymic 생쥐에 intracranially 설정할 수 있습니다. 생존 분석과 함께, bioluminescence 모니터링 뇌 종양 치료를위한 고려되는 요법의 사전 임상 시험을위한 필수적인 연구 도구입니다.
초록
인간의 뇌 종양 세포를 사용하여 이식 모델은 여러 해 동안 신경 종양학 연구에 필수적인 기능을 제공합니다. 과거에는 인간의 종양 이종 이식의 설립에 가장 일반적으로 사용되는 절차는 immunocompromised 생쥐에서 수집된 세포의 피하 주입 다음에 문화 flasks에서 세포의 수집 구성되어. 이 방법은 아직도 많은 실험실에서 자주 사용을보고 반면, 뇌 종양의 인스턴스에 해당 neuroanatomical 구조로 종양 세포 주사를 필요 orthotopic 이종 이식 설립으로 지난 10 년간 강조에 큰 변화를가되었습니다. intracranial 이종 이식 설립은 캘리퍼스의 사용, orthotopic 뇌종양의 이종 이식 모델 대한 강조의 변화에 의해 직접 측정을 통해 종양의 성장과 같은를 모니터하는 능력을 제거하기 때문에 호스트 동물에 종양 부담을 평가하는 비침습 영상의 활용을 necessitated있다. 현재 사용 가능한 이미징 방법, bioluminescence 모니터링은 일반적으로 감도, 편의 및 비용 최고의 조합을 제공하는 것으로 간주됩니다. 여기, 우리는 orthotopic 뇌종양의 설립, 그리고 실험 치료법을 테스트할 때 종양 성장과 치료에 반응을 감시하기위한 절차를 보여줄 것입니다.
프로토콜
1. 종양 세포의 준비.
종양 athymic 마우스의 피하 성장으로, 또는 세포 배양에서 증식에서 인간의 뇌 종양의 xenografts에 대한 세포 중 공급 수 있습니다. 두 세포 소스의 이용은 세포 주입하는 방법의 시범과 함께 아래에 설명되어 있습니다.
조직이 처음 셀 집합 서스펜션 만들기 1 반복적인 pipetting하여 메스 후 기계 방해와 다진 어디에 intracranial 구획로 전송하기 위해 피하 종양에서 세포를 준비하려면, excised 측면 종양은, 문화, 요리에 배치됩니다. 셀 집계 정지 후 intracranial 사출에 적합한 단일 세포 현탁액을 생산하기 위해 필터 70 μm의 나일론 메쉬를 통해 전달됩니다. 세포 현탁액은 1000 4 10 분 RPM ° C, 그리고 최종 작업 농도 (아래 참조)을 구하는 혈청이없는 미디어의 적절한 볼륨에있는 세포 펠렛을 resuspending 전에 aspirated 뜨는에서 centrifuged입니다. intracranial 이식을 위해 설립된 세포 라인을 준비하는 경우, 전지가 다음과 같은 2 위에 표시된 셀을 centrifuging하고 resuspending, neurosphere 서스펜션 문화를 수집하여 trypsinizing monolayers에 의해 수확, 또는 있습니다. 주입된 세포의 숫자가 분사의 neuroanatomical 위치에 변수에 따라 달라집니다. brainstem 주사 3, 5 X 10 4 세포처럼 몇 가지가 0.5 μL 주입하는 반면 supratentorial 주사에 대한 우리가 일상적으로, 혈청 프리 미디어 (DMEM) 3 μL에 3-5 X 10 5 세포를 주입. 권장보다 큰 볼륨을 주입하는 것은 결과 exophytic (그림 1)가 아닌 intracranial 종양의 성장과 함께, 바늘 트랙트를 통해 종양 세포 환류이 발생할 수 있습니다. intracranial 주사에 대한 샘플을 철수 후, 남아있는 세포 현탁액을 주입 시리즈의 구성원 간의 intracranial 종양 설립을 완료하는 동안 적절한 농도를 유지하기 위해 자주 혼합 내용과 함께 얼음에 배치해야합니다.
2. 종양 세포 주입
참고는 아래에서 설명하는 모든 절차는 캘리포니아 샌프란 시스코 대학에서 기관 동물 사용 및 관리위원회의 검토와 승인되었습니다.
- 외과 영역 등 2 % chlorhexidine 솔루션으로, 살균제 모든 표면을 분사하여 준비되어야합니다. 소독제를 사용한 후 다음과 같은 소모품은 외과 영역에 배치되어야합니다
- 마우스 체온을 유지하기 위해 가열 패드
- 2 % chlorhexidine을 포함한 3 % 과산화수소를 포함하는 하나 하나, 2 작은 배양 접시
- 무균 거즈 및 면화 면봉
- 멸균 일회용 scalpels
- Autoclaved 외과 스테이플러
- 마취에 대한 주입 마취를 사용해야합니다, 일반적으로 케타민을 - xylazine 혼합합니다.
- 마우스 anesthetized되면, 두피는 멸균 거즈의 조각 chlorhexidine 용액에 담근 여러 번 보라고하여 준비가되어 있습니다. 아이 연고는 절차를 수행하는 동안 충분한 수분을 유지하기 위해 적용해야합니다. 멸균 메스를 사용하여 길이 약 1cm, parieto - 후두 골을 통해 화살 절개를 완료하십시오. 노출된 두개골 표면은 다음 3 % 과산화수소 용액에 담가 면봉을 사용하여 청소합니다. bregma은 (비디오 참조)이 시점에서 명확해야합니다.
- 종양 세포의 주입을위한 좌표는 종양 설립 원하는 사이트에 따라 달라질 수 있습니다. 다음은 우리가 많은 뇌종양 환자는 종양 개발을 경험되는 neuroanatomical 위치에 했습니다만 종양 설립 2를 사용하는 프로 시저를 나타냅니다. 뇌종양 연구에 대한 관심의 다른 위치 brainstem 종양 3 해부학 모델링 폰스, 그리고 meningeal 종양의 위치 4 모델링 경막하 주사를 포함합니다. 사전 종양 세포 주입으로, 따라서 종양 세포 (동영상 참조)의 분사에 대한 개방을 만드는, bregma 및 코로나 치료 앞쪽에 1mm의 오른쪽에있는 2mm에 찔린 두개골에 멸균 25 게이지 날카로운 바늘을 사용합니다. 이 절차는 생쥐와 쥐 (쥐 22 게이지 바늘) 모두 잘 작동합니다.
- 전에 주사기로 세포를 그리기 위해 손가락으로 눌러서하여 세포 현탁액의 내용을 섞는다. 공기 방울을 생성하지 않도록주의하고, 세포 현탁액의 원하는 금액으로 주사기를로드합니다. 주사기의 외부는 다음 extracranial 종양 설립과 성장 (그림 1A)을 예방하는 데 도움이됩니다 어떤 자기편 세포의 무료 외관을 닦아 알코올 면봉과 청소해야합니다. 적절한 주입 깊이가 달성되었는지 확인하려면, P20 pipetteman 팁의 지적 끝에서 3mm를 잘라 메스를 사용합니다. 팁의이 섹션은 주사기를 통해 장착할 수 있으며 사출 깊이를 제한하는 역할을하며, 또한 보장됩니다 TI주사기 바늘의 P는 두개골의 아래쪽에서 3mm이다. 두개골에 주사기의 직각을 플레이스와 이전에 만든 구멍, 천천히 세포 현탁액 (3μL 현탁액이 1 분 동안 주입한다)을 주입. 주사 삽입의 부적 절한 각도가 세포와 후속 척추 보급 (그림의 1B : 오른쪽)의 심실 분사가 발생할 수 있습니다 주입 완료되면 다른 잠시 동안 자리에 바늘을두고, 다음 천천히 (동영상 참조) 취소 : 다음 단계를 줄일 도움이 될 것입니다 종양 세포 환류.
- intracranial 종양 세포 주입 5 남의 도움이없는 또는 무료 직접 접근 방식의 대안으로, 하나는 일반적으로보다 일관된 분사 위치를 장려 작은 동물 stereotactic 프레임을 (배선의 개요 패널 F)를 사용하지만, 할 수의 상당한 양의 비용 절차 시간. 무료 직접 접근 방법을 사용할 때 작은 동물 stereotactic 프레임과 함께 최대한의 주입 속도가 약 15 생쥐 / 시간이지만 우리의 경험에서는 두 외과 직원, 많은 60 마우스 / 시간을 주입하실 수 있습니다. 절차적 편의 쥐가 많은 시리즈를 주입 때 중요한 고려 사항이며, 주입으로 종양 세포가, 얼음에 남아있는 시간을 줄일 수 있습니다.
- 살균 건조 면봉을 사용하여 3 % 과산화수소와 건조와 두개골을 청소합니다. 구멍에 멸균 뼈 왁스를 적용합니다. 포셉 사용하여 닫습니다 두개골과 주식을 통해 함께 두피를 그립니다. 최적의 치유 들어, 두피는 서로에 대한 두피의 각 측면의 진피 (아래쪽으로부터 아래쪽)로 잘라해야합니다. 잘라 두피는 다음 포스트 수술 고통 구호를위한 피하 주사에 의해 관리 Chlorhexidine 솔루션 및 buprenorphine를 사용하여 청소해야합니다.
- 그들이 걸을되고 정상적인 활동을 유지하기 전까지 사후 operatively 모든 생쥐를 모니터링합니다. 일반적으로, 복구 시간은 30 분 정도입니다.
3. 종양 성장의 Bioluminescence 모니터링
- 배경. Bioluminescence 이미징 (BLI)가 luciferin의 산화를 기반으로 [(-) -2 - D - (60 - 히드록시 20 benzothiazolyl) thiazone - 4 - 카르복실산] 산소와 아데노신 삼인산 (ATP)의 존재 인치 이 반응은 빛을 방출 결과와 광자로 화학 에너지를 변환 효소 루시페라제에 의해 촉매이다. 인간의 세포는 luciferin 기판의 존재에 발광 빛의 수있는 유일한 루시페라제 - 표현 전지 (아래 참조) 루시페라제 표현을 수정할 수 있습니다. 종양 성장과 생체내의 치료에 대한 응답의 매우 민감한 모니터링을 허용, 루시페라제 - 수정 종양 세포에서 발광 방출을 검출 매우 유리한 신호 대 잡음 비율이 그러한 luciferin 취급 호스트 동물에서 최소한의 배경 발광이있다. 또한, 루시페라제 및 기판, luciferin는 포유 동물 세포에 무독성으로 표시되었으며, 우리는 해당 수정되지 않은 세포 루시페라제 상대를 표현 세포 사이에 기능적인 차이를 관찰 없습니다. Luciferin은 쉽게함으로써 루시페라제 - 수정된 세포를 포함 모든 구역의 이미지를 허용, 세포 점막과 intraperitoneal 후 혈액 뇌 장벽 (IP) 또는 정맥 주사 (IV) 주사 생쥐의 교차. 루시페라제 - 수정된 세포에서 방출되는 빛의 광자 방출과 스펙트럼의 수준은 마우스 및 쥐 같은 작은 연구 동물의 조직에 침투하는 적절한이며, 낮은 조명 이미징 카메라와 외부 검색하실 수 있습니다. bioluminescence 이미징의 비침 투 자연은 종양 성장과 개별 동물 과목에서 치료 반응의 반복 모니터링을 허용합니다.
- 이식 세포의 소스는 안정 반딧불 루시페라제 표현 수정해야합니다. 이러한 세포 소스는 구입, 또는 루시페라제의 제정 표현 건설되었습니다 lentivirus을 사용하여 개별 실험실에서 생산 수 있습니다. 우리는 강력하게 반복있는 개별 동물 과목 종양 부담의 변화에 정확하게 표시를 제공하기 위해 정량 발광 이미징에 필요한 생체내에 루시페라제의 안정적인 세포 표현을 보장하기 위해, 오히려 플라스미드보다 루시페라제 인코딩 lentivirus와 수정된 세포의 사용을 권장 실험 과정 중에 몇 군데.
- BLI 모니터링. 우리는 종양 세포 주입에 따라 일주를 시작, 양적 bioluminescence 이미징 (qBLI) 1X - 2X 주간을 실시하는 것이 좋습니다. 우리 qBLI은 IVIS 루미나 영상 역 (칼리퍼 생명 과학)을 사용하여 실시하고, 우리의 결과는 유사한 데이터가 IVIS 루미나, IVIS 150 또는 200 IVIS 이미징 스테이션을 사용하여 얻을 수있다 표시이다. 이미징을위한 준비, 마우스는 주사 후 12 분 군데 쥐, intraperitoneal 주입을 통해 케타민을 / Xylazine과 관리 luciferin (D - Luciferin의 칼륨 소금, 150 MG / kg, 칼리퍼 생명 과학)와 동시에 anesthetized 있습니다. luciferin의 pharmacokinetics에 따르면 adminis 사이의 시간luciferin 및 세포 발광의 결정 tration 최대 발광 방출 및 검출의 가장 큰 감도를 얻기 위해서는, luciferin의 10-15분 게시물 주입 사이 여야합니다. 10~15분 시간 간격 이내에 선택한 시간의 길이는 몇 군데되는 동물 사이에서 상수로 유지 관리해야합니다. 그것은 BLI 읽을 luciferin 및 취득의 분사 사이의 시간 길이의 일관성을 유지하기 위해 매우 중요합니다. 신호의 intracranial 지역을 포함한 관심 영역은 생활 이미지 소프트웨어 (그림 2)를 사용하여 정의하고 있으며, 총 photons/s/sr/cm2는 (평방 cm 당 steradian 당 초당 광자) (동영상 참조) 기록됩니다.
- 데이터 분석. 종양 성장과 치료 반응은 개별 동물 모니터링 반면, 우리는 높은 종양 반응에 관한 결론의 확실한 통계를 높이기위한 최소한 8 치료 그룹을 권장하거나, 치료, 그것의 부족. 6,7를 읽고 해당 최대한의 전처리의 발광과 치료 처방의 완료 이후에 제시 qBLI 결과에 관련하여, 발광의 수치는 각 마우스의 발광을 나누어 정규화 값으로 변환하는 동안 취득합니다. 생존 분석을 위해, 카플란 - 마이어 견적 도구 (Traffic Estimator)는 8 사용하고, 생존 곡선이 생성하는에서, 그리고 중간 생존 값 결정. 생존 곡선 사이의 차이는 로그 순위 테스트 9를 사용 비교됩니다.
- 치료 및 치료 종양의 후속 분석을 위해 두뇌의 검색. 동물 안락사되면, 마우스의 두뇌는 빠르게 (동영상 참조) excised, 그리고 중 종양과 형태학 immunohistochemistry의 후속 분석을 위해 포르말린에 배치하거나, 표본 냉동 OCT에 탑재되어야한다.
4. 대표 결과
연속 의미 발광 값이 진행성 종양의 성장을 지시하기 전까지 그림 3A에 표시된 예제에서는 intracranial 종양 세포 주사를받은 생쥐는 intracranial 발광에 대한 모니터링했고,되는 시간 치료는 일 34시 (회색 화살표 시작 시작되었습니다 erlotinib 150 밀리그램 매일 관리 필수 안락사까지 / kg). 각각의 마우스에 대한 발광 값은 최종 전처리 이미징 값으로 정규화 각 마우스에 대한 후속 발광의 판독과 함께 치료를 시작 당시 1 정규화 값으로 설정됩니다. 예를 들어, 발광 6.0 증가했다 일 34시 2.0 X 10 7 광자 / 초, 중 최종 미리 치료 발광 읽기와 마우스는 하루에 38에서 X 10 7 광자 / 초, 하루 38 표준 발광의 가치를했을 3.0. 정규 bioluminescence 및 제어 및 치료 그룹에 해당하는 표준 오류를 평균은 각 이미징 시점에 대한 꾸몄다 있습니다. 이 예제에서는 의미 정규 발광에 큰 차이가 이후의 시간 지점에서 추가 증가를 보여주는 의미 그룹 발광의 차이와 치료의 개시 (일 38)에 이후 첫 번째 이미징 시점에 분명합니다. 대부분의 경우에서와 같은 qBLI로 표시 요법의 안티 종양 활동이 같은 경우가 여기 (그림 3B)이며, 생존에 해당하는 큰 차이 (즉, P <0.05)와 함께합니다. 패널 3C 및 3D보기 인접 hematoxylin & eosin 및 마우스 두뇌의 안티 EGFR 묻은 부분 sectioning 위해 포르말린 이후 파라핀 - 퍼가기의 resected 두뇌의 배치에 따라, 안락사 시점에서 획득.
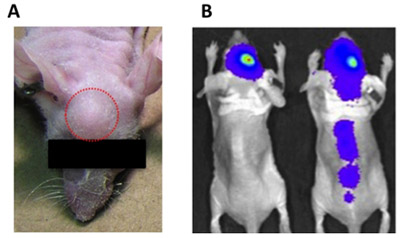
그림 1. intracranial 사출 오류 징후. A) Exophytic (extracranial) 종양의 성장 (빨간색 동그라미)가 너무 큰 주사 볼륨, 주사기에 부착된 잔여 세포 현탁액으로 인해 발생할 수, 또는 종양 세포를 주입 후 너무 빨리 주사기를 철수에서. B) 심실로 종양 세포를 주입하면, 제대로 주입 종양 세포와는 달리, 사출 사이트 (왼쪽 마우스)에 현지 숙박하는 신호를 종양의 척추 보급 (오른쪽 마우스)을 일으킬 수 있습니다.
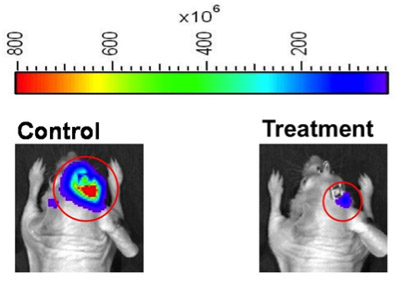
치료 반응 실험의 그림 2. 히트지도 이미지 컨트롤에서 마우스에 대한 대표 bioluminescence 강도의 표현 (왼쪽)과 치료 (오른쪽) 그룹. 생활 이미지 소프트웨어는 관심의 영역을 (빨간 동그라미) 정의로 설정할 수 있습니다, 또는 악기 연산자는 수동으로 관심 영역을 정의할 수 있습니다. 같은 그림 건설에 다음과 같이 이미지를 사용하는 경우, 우리는 악기의 연산자는 동물 과목 간의 bioluminescence 차이의 범위의 시각적 표현을 제공하기 위해 같은 bioluminescence 열지도 범위를 (그림의 상단 부분)를 사용하여 열지도 이미지를 표시하는 것이 좋습니다.
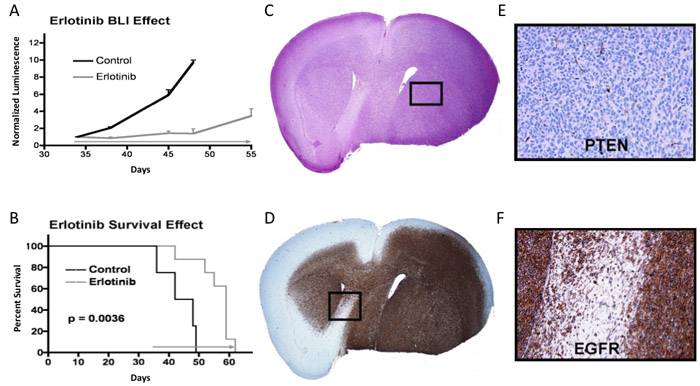
그림 3. Bioluminescence, 생존, 그리고 치료 반응은 분명있는 실험에서 종양 조직 분석. 표준 오차와 제어 및 치료 그룹의 마우스에 대한 의미 bioluminescence의 판독의) 플롯은 각 이미징 포인트 지적했다. B) 같은 마우스의 생존의 줄거리, P - 값은 로그 순위 테스트 7을 통해 결정됩니다. 종양과 마우스 뇌의 C) H & E 스테인드 섹션을 참조하십시오. D) EGFR 스테인드 섹션을 참조하십시오. 종양 억제 단백질 PTEN에 대한 부정적인 얼룩을 보여주는 패널 E와 함께 각각 패널 C와 D,에서 표시 영역의 E와 F)은 배율.
토론
Orthotopic (intracranial) 뇌종양의 이종 이식의 설립은 치료 응답을 테스트하기 위해 모델링 CNS 암 10 적절한 microenvironment를 제공합니다. 모델링 이러한 유형의 또한 두뇌와 실험 에이전트가 환자의 임상 시험 평가 고급할지 여부를 결정하는 매우 중요한 뇌 종양에 치료 접근에 관한 정보를 제공합니다. intracranial 이종 이식 종양의 양을 직접 같은 캘리퍼스로로 측정할 수 없기 때문에, intracranial 종양의 성장과 치료에 대한 응답의 길이 모니터링 누구의 주요 목표는 실험을위한 가장 실용적인 방법으로 우리의 경험 나타내는 bioluminescence 이미징과 비침습 영상을 필요로 치료 종양 반응 정도를 평가합니다. bioluminescence 이미징의 결과가 동물 주제 생존 분석과 결합되면 두 데이터 집합이 실험 치료 효능을 평가하기위한 강력하고 안정적인 접근 방식을 제공합니다.
마지막으로, intracranial 뇌종양의 xenografts가 치료의 morphologic와 분자 효과를 평가하기 위해 euthanized 동물 과목에서 수확되는 매우 중요하고, 이것에 대한 우리는 이후 분석을 위해 resected 두뇌 보존과 안락사의 시간에 전체 뇌 절제술을 선호합니다.
이전 프레 젠 테이션이 뇌 종양 연구와 관련된하였습니다 반면, 개념은 확실하게 설치류에 orthotopic 모델링 의무가 다른 인간의 암에 generalizeable 있습니다.
공개
감사의 말
자료
| Name | Company | Catalog Number | Comments |
| Disposable Scapels | Feather Safety Razor Co, Ltd. | 2975 | No.21 |
| Heating Pad | Dunlap | HP950 | |
| Gauze | Fisher Scientific | 22028563 | |
| Cotton Swabs | Fisher Scientific | 23-400-100 | |
| 2% Chlorhexidine | Fisher Scientific | NC9756995 | |
| 3% Hydrogen Peroxide | Fisher Scientific | H312P-4 | |
| 25g Needle | BD Biosciences | 305122 | |
| 10ul Hamilton Sharp Microsyringe | Hamilton Co | 20734 | |
| Skin Stapler and Staples | Stoelting Co. | 59020 | |
| Stereotaxic Frame | Stoelting Co. | 51725 | |
| Living Image Software |  Caliper Life Sciences Caliper Life Sciences | ||
| D-luciferin | Gold Biotechnology | LUCK-1G | Potassium Salt |
| Xenogen Lumina |  Caliper Life Sciences Caliper Life Sciences |
참고문헌
- Giannini, C., Sarkaria, J. N., Saito, A., Uhm, J. H., Galanis, E., Carlson, B. L., Schroeder, M. A., James, C. D. Patient Tumor EGFR and PDGFRA Gene Amplifications Retained in an Invasive Intracranial Xenograft Model of GBM. Neuro-Oncol. 7, 164-176 (2005).
- Ozawa, T., Wang, J., Hu, L. J., Bollen, A. W., Lamborn, K. R., Deen, D. F. Growth of human glioblastomas as xenografts in the brains of athymic rats. In Vivo. 1, 55-60 (2002).
- Hashizume, R., Ozawa, T., Dinca, E. B., Banerjee, A., Prados, M. D., James, C. D., Gupta, N. A human brainstem glioma xenograft model enabled for bioluminescence imaging. J Neurooncol. , (2009).
- Baia, G. S., Dinca, E. B., Ozawa, T., Kimura, E. T., McDermott, M. W., James, C. D., VandenBerg, S. R., Lal, A. An orthotopic skull base model of malignant meningioma. Brain Pathol. 2, 172-179 (2007).
- Ozawa, T., James, C. D., Van Meir, E. Human Brain Tumor Cell and Tumor Tissue Transplantation Models. CNS Cancer: Models, Markers, Prognostic Factors, Targets, and Therapeutic Approaches. , 147-162 (2009).
- Sarkaria, J. N., Yang, L., Grogan, P. T., Kitange, G. J., Carlson, B. L., Schroeder, M. A., Galanis, E., Giannini, C., Wu, W., Dinca, E. B., James, C. D. Identification of Molecular Characteristics Correlated with Glioblastoma Sensitivity to EGFR Kinase Inhibition Through Use of an Intracranial Xenograft Test Panel. Mol. Cancer Ther. 6, 1167-1174 (2007).
- Dinca, E. B., Sarkaria, J. N., Schroeder, M. A., Carlson, B. L., Voicu, R., Gupta, N., Berger, M. S., James, C. D. Bioluminescence Monitoring of Intracranial Glioblastoma Xenograft Response to Primary and Salvage Temozolomide Therapy. J. Neurosurg. 107, 610-616 (2007).
- Kaplan, E. L., Meier, P. Non-parametric estimation from incomplete observations. J. Am. Stat. Assoc. 53, 457-481 (1958).
- Peto, R., Peto, J. Asymptotically efficient rank invariant procedures. J. R. Stat. Soc. Ser. A. Stat. Soc. 135, 185-207 (1972).
- Camphausen, K., Purow, B., Sproull, M., Scott, T., Ozawa, T., Deen, D. F., Tofilon, P. J. Influence of in vivo growth on human glioma cell line gene expression: convergent profiles under orthotopic conditions. Proc. Natl. Acad. Sci. U. S. A.. 102, 8287-8292 (2005).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유