Method Article
하이브리드 μCT-FMT 및 촬상 화상 해석
* 이 저자들은 동등하게 기여했습니다
요약
We describe a protocol for hybrid imaging, combining fluorescence-mediated tomography (FMT) with micro computed tomography (µCT). After fusion and reconstruction, we perform interactive organ segmentation to extract quantitative measurements of the fluorescence distribution.
초록
형광 매개 단층 촬영 (FMT)는 생체 내에서 형광 분포의 종 방향 및 정량이 가능하고 신규 한 프로브의 생체 분포를 평가하고 수립 분자 프로브 또는 리포터 유전자를 이용하여 질병의 진행을 평가하기 위해 사용될 수있다. 예를 들면 해부학 적 양상과 조합은, 마이크로 컴퓨터 단층 촬영 (μCT), 이미지 분석 및 형광 재건 유리하다. 우리는 정량적 측정을 추출하는 데 필요한 화상 처리 단계를 포함한 멀티 모달 μCT-FMT 이미징을위한 프로토콜을 기술한다. 마우스를 준비하고, 촬상을 수행 한 후, 복합 데이터 세트가 등록된다. 이어서, 개선 된 형광 재구성 고려 마우스의 형상을 취하는, 수행된다. 정량 분석을 위해, 기관 세그먼테이션은 대화 형 분할 도구를 사용하여 해부학 적 데이터에 기초하여 생성된다. 마지막으로, 생체 분포 CUrves 일괄 처리 기능을 사용하여 생성됩니다. 우리는 뼈와 관절 결합 공지 프로브의 생체 분포를 평가함으로써 상기 방법의 적용을 나타낸다.
서문
형광 매개 단층 촬영라고도 형광 분자 단층 (FMT)는 정량적 같은 마취 된 쥐 또는 인간의 신체 조직, 예를 들면, 유방이나 손가락 관절 등 미만성 조직에서 형광 분포를 평가하기위한 유망한 기술이다. 세포 내 해상도 1 표면의 촬상 대상을 허용 비 침습적 현미경 기술에 대조적으로, FMT는 저해상도이 낮아지기 수 ㎝, 깊이 형광 소스 삼차원 재구성을 허용한다. 5 - 많은 대상으로 형광 프로브는 이미지 혈관 신생, 세포 사멸, 염증 등 2 사용할 수 있습니다. 일부 프로브는, 기동 있습니다 예를 들어., 형광 색소의 unquenching로 이어지는 특정 효소 절단에 의해. 또한, 형광 단백질을 발현하는 리포터 유전자는 종양 세포의 이동을 추적하기 위해 6, 예를 들면, 묘화 될 수있다.
FMT는 강하게 예를 들어, 2,7 또는 자기 공명 영상 (8) μCT, 해부학 적 양상과 조합의 혜택. 독립형 FMT 장치 상업적 9 사용할 수 있지만, 형광 이미지는 해부학 적 기준 정보없이 해석하기가 어렵다. 최근 우리는 융합 해부학 화상 데이터보다 강력한 분석을 가능하게한다는 10, 표시 할 수 있었다. 해부학 적 데이터는 또한 정확한 광학 모델링 및 형광 재 (11)에 대한 중요한 마우스의 외형으로 사전 지식을 제공하기 위해 사용될 수있다. 또한, 광 산란 및 흡수 맵 조직 유형의 분할을 사용하여 추정 된 계수 12,13 특정 클래스를 할당하여 할 수있다. 근적외선 들어 헤모글로빈 멜라닌 모피 14 게다가 마우스에서 주요 흡수이다. 상대 혈액량은 크기 순서에 의해 지역적으로 변화하기 때문에, 흡수지도 콴 특히 중요titative 형광 재 (13).
비 침습적 촬상 장치를 사용하는 하나의 장점은 생쥐 여러 시점에서, 즉, 종 방향으로 묘화 될 수 있다는 것이다. 이는 프로브의 동적 거동, 즉, 타겟 축적, 배설물 및 생체 분포를 평가하기 위해 10, 15, 또는 질병의 진행 (16)을 평가하는 것이 중요하다. 여러 시점에서 여러 생쥐 촬상하면, 이미지 데이터 집합의 다량 발생한다. 비교를 활성화하려면 다음은 잘 정의되고 문서화 된 프로토콜로, 체계적으로, IE에서 취득해야한다. 스캔의 다수의 이미지 데이터로부터 양적 측정 값을 추출하는 데 필요한 화상 분석을위한 도전을 제기.
본 연구의 목적은 여러 연구에 걸쳐 10,13,15,17,18 우리가 사용하는 최적화 μCT-FMT 촬상 프로토콜의 상세한 설명을 제공하는 것이다. 우리는 기술데이터 세트가 생성되는 방법, 시각 처리하고 분석 하였다. 이것은 19 수산화 인회석에 결합 설립 분자 프로브, OsteoSense를 사용 입증되고, 화상 골 질환에 사용될 수 있으며,이 개조. 동물과 관련된 모든 절차는 동물 보호에 대한 정부 심의위원회에 의해 승인되었다.
프로토콜
프로토콜은 다음 단계의 상세한 설명이 포함 우선, 팬텀 또는 마우스와 봉형 마우스 베드 이미징을 위해 준비된다. 이어서 전신 스캔 μCT에서 획득된다. 그 후 마우스 침대는 두 개의 스캔이 (위 거꾸로) 취득 FMT로 전송됩니다. 이것은 여러 시점에서 여러 생쥐에 대해 반복 될 수있다. 데이터 수집의 완료 후에, 데이터는 내보내고 자동 세그멘테이션 (Definiens 소프트웨어 라이센스를 요구)뿐만 아니라, 화상 융합 및 (Imalytics 전임상 소프트웨어 라이센스를 요구하는) 형광 재를 사용하도록 정렬 될 필요가있다. 마지막으로 장기 대화식 형광 프로브의 생체 분포를 정량화하기 위해 분할되는 방법을 멀티 모드 데이터 세트가 시각화 방법과 같다.
1. 팬텀 준비
주 : 팬텀 이미징 시스템을 시험하는 데 유용하지만, 또한 사실상 교정을 결정할새로운 프로브 R.
- 200ml의 물, 2 % 아가로 오스 1.8 g 이산화 티탄 분말, 50 ㎕의 트리 판 블루 용액을 준비한다. 끓는 후 약 8cm 길이 3cm 폭 1.5 cm 높이의 직사각형 형태로 솔루션을 입력합니다.
- μCT 형광 조영제의 혼합을 포함하는, 피펫 팁을 사용하여 가상 선으로 여러 형광 개재물을 준비한다. 흠을 만들려면, 피펫 팁을 잘라 라이터로 봉인.
- 용액이 응고 후, 팬텀에 흠을 넣습니다. 불규칙한 형상을 달성하고 복합 마우스 홀더에 맞도록 팬텀의 일부를 버려야.
- 새로운 프로브에 대한 보정 계수를 결정하기 위해, 일부 팬텀 검사가 필요합니다. 이 경우, 기본 FMT 팬텀은 프로브의 공지 된 양으로 혼합하여 사용된다. 증가 된 정확도를 같이 포함 내부 동일한 산란 계수를 수신하기 위해 용액에 4 % 지질 에멀젼을 추가팬텀의 나머지. 또한 쉽게 화상 분석 μCT 조영제 소량 (2 %)를 추가한다.
2. 마우스 준비
참고 : μCT-FMT 이미징은 마취 헤어 제거하는 등 특별한 준비가 필요합니다.
- 칠일 이미징 전에 엽록소가없는 음식에 마우스를 놓습니다. 이것은 배경 신호를 감소시키고 750 nm의 아래 FMT 채널 특히 중요 할 것이다.
- 모든 동물 실험은 마취하에 수행됩니다. 마우스가 잠들 때까지 공기 (유량 5 L / 분)에서 2 % 이소 플루 란으로 채워진 챔버에 마우스를 놓고 마취를 시작합니다. 부드러운 발가락이나 피부 곤란에 의한 근육 TONUS의 휴식을 확인하여 (예., 턱 근육) 적절한 마취를 확인합니다. 마취를 유지하기 위해, (레이트 1 L / min의 흐름 공기 중에서 2 % 이소 플루 란) 마우스의 코에 배치되어 튜브를 사용하여 이소 플루 란 어플리케이션을 계속한다. 눈 drynes을 방지하기 위해서들, 마취 된 쥐에 수의사 연고를 사용합니다.
- 조영제를 주입하기 위해, 테이프를 이용하여 가열 패드에 마취 된 마우스를 고정한다. 꼬리 정맥에 카테터 (튜브에 부착 된 주사기 바늘)를 놓고 형광 조영제를 주입 (예를 들어, 2 nmol의를 5 ㎖의 최대 주입량 / kg 체중, 즉, 30g 마우스 150 μL)와.
- 털이 마우스를 스캐닝하기위한 스캐닝 영역을 미리를 면도해야한다. 이를 위해, 면도기 나 제모 크림을 사용합니다. 생쥐의 일부 변종은 머리 제거 크림에서 발진을 개발할 수 있습니다. 따라서, 피부 변화에 대한 쥐를 모니터링하고 필요한 경우 치료에 대한 수의학 직원에게 문의하십시오. 새로운 마우스 균주를 사용하는 경우 또한, 동물의 소수에 내성을 테스트한다.
- (속도 1 L / 분 흐름, 공기의 2 % 이소 플루 란) μCT 및 FMT 이미징 동안 마취 마우스를 유지합니다.
3. 마우스 침대 준비
참고 : μCT-FMT 주사를 들어, 멀티 모드를 사용μCT 및 FMT에 모두 맞는 마우스 침대.
- 촬영하기 전에, 물티슈와 마우스 침대를 청소하십시오. 이 아크릴 유리가 손상 될 수 있기 때문에 에탄올을 사용하지 마십시오. 이 자동화 된 마커 검출을 방해 할 수 있기 때문에, 마커 물이 없는지 확인합니다.
- 복합 마우스 침대의 나사를 열고 상단 부분을 제거합니다.
- 마우스 침대에 마취 가스 튜브를 연결하고 테이프로 고정하세요.
- 마우스 침대에 마취 마우스를 놓고 가스 튜브에 코를 넣어. 마우스의 머리가 마우스 침대의 전면 표시 등 (그림 1)에 있는지 확인합니다.
- 마우스를 최적으로 FMT의 시야를 사용하는 마우스 침대의 중간에 있는지 확인합니다.
- 마우스 침대를 닫고 마우스가 긴밀하게 유지 될 때까지 나사를 조입니다. 마우스가 흉부 호흡의 움직임을 시각적으로 모니터링하여 지속적으로 호흡 할 수 있는지 확인합니다.
4. μCT 나는maging
주 : 전신 스캔은 μCT를 사용하여 수행됩니다. 생성 된 데이터는 해부학 향상된 형광 재건 및 이미지 분석을 위해, 이미지 합성을 위해 요구된다.
- μCT에 마우스로 마우스 침대를 놓습니다. 마우스는 μCT에 "꼬리 먼저"가는 길에 배치되어 있는지 확인합니다. 이것은 자동 융합 중요하다.
- μCT 뚜껑이 폐쇄 될 때 마취를 유지하기 위해, μCT의 케이스를 통해 가스를 채널에 튜브를 연결합니다. 먼저 마우스 침대에서 긴 튜브를 분리하고이를 μCT의 외부에있는 커넥터에 연결합니다. 그런 다음 μCT 내부 커넥터에 나머지 끝을 연결합니다.
- μCT에 마우스 침대를 운전. 가스 튜브가 느슨하지 않고 회전 갠트리에 의해 잡힐 수 있는지 확인합니다. 필요한 경우, 테이프를 이용하여 그것을 고정하세요. 마우스 침대의 홀더의 단면에 튜브를 삽입합니다.
- μCT를 닫고 topogram을 획득. 융합과 재건을 위해 중요하다 마우스와 마우스 침대의 상당 부분을 충당하기 위해 두 개 이상의 subscans을 선택합니다.
- 서브 스캔 당 90 s의 스캔 시간을 필요로 하나의 전체 회전시 1,032 X 1,012 픽셀 (720) 전망을 취득의 HQd-6565-360-90라는 μCT 검사 프로토콜을 선택합니다. 튜브는 전압이 65 kV의 전류 1.0 mA에서 작동된다. 또한, 방사선 량과 검사 시간을 줄일 스캔 프로토콜 스캔 시간 서브 스캔 당 29의와 516 X 506 픽셀 (720) 전망을 획득 SQD - 6565-360-29를 선택합니다.
- μCT 스캔을 시작합니다. 파란색 막대는 진행 상태를 나타냅니다. subscans 이후 취득됩니다. 저체온증 유체 손실 때문에 단 몇 분의 짧은 검사 시간의 문제가되지 않습니다. 이 자동에서 사용자를 보호하기 위해 검색을 방해하기 때문에 스캔하는 동안 μCT의 뚜껑을 열지 마십시오방사선.
- 스캐닝이 완료되면, 덮개를 열 마취제 튜브를 연결하고 FMT에 수송하는 홀더로부터 마우스 베드 분리.
5. FMT 이미징
참고 : 직접 μCT 검사 후, 마우스가 개선 된 형광 재건을 위해 함께 사용되는 두 개의 구성 (최대 거꾸로)에 FMT에서 스캔됩니다.
- FMT에 마우스 침대를 배치하기 전에 FMT에 대한 (속도 1 L / min의 유량, 공기의 2 % 이소 플루 란) 마취 가스 공급을 켭니다. FMT 제어 소프트웨어를 사용하여, 환자의 적절한 수의 (즉, 마우스)와 함께 연구 그룹을 만듭니다. (나열되지 않은 새로운 프로브를 사용 OsteoSense) 영상에 사용되는 프로브를 선택합니다.
- FMT에 마우스로 복합 마우스 침대 캐리. 긴가요 마취 가스 튜브는 가스 유동을 유지한다. FMT에 마우스 침대를 삽입하기 전에주의 깊게부터 튜브를 제거FMT 내부에 필요하지 않습니다. 마우스 침대의 나사를 돌려 피하십시오.
- ( "머리 처음") 먼저 빨간색 표시와 FMT에 마우스 침대를 놓습니다. 이미지 융합 μCT과 일치하는 중요합니다.
- FMT를 닫습니다.
- 올바른 연구 그룹과 대상을 선택합니다. FMT의 요구 채널 선택 (OsteoSense 750EX를 들어, 750 nm의 채널을 사용).
- 설명, 예를 추가합니다. "위로"또는 "아래"와 "캡처"를 눌러 개요 스캔을 획득. 이보기의 전체 필드의 반사 이미지를 캡처한다. 그렇지 않으면 3D가 연속적으로 스캔 획득 할 수 없기 때문 "반사율 이미지 만"을 선택하지해야합니다.
- 3 차원 스캔 이미지 매개 변수를 조정합니다. 마우스 최대한 포함 시야 확대. 일반적으로, 머리와 꼬리는 완전히 그러나, 시야에 적합하지 않습니다. 클릭 "고급(221); 및 이미지 설정을 확인합니다. 각각 5000 및 50000에 정상 및 조명 최소 / 최대에 3mm, 감도 설정 샘플링 밀도.
- FMT 스캔을 시작하는 "스캔"을 클릭 클릭 "재건 대기열에 추가"를. 더 긴 노출 시간이 두꺼운 물체 필요하기 때문에, 크기 및 마우스의 두께에 따라, 약 5 내지 15 분 걸릴 것이다. 장치 저체온증을 피하기 촬상 가열 챔버를 포함한다.
- 스캔 후, 거꾸로 마우스를 포함한 마우스 침대를 뒤집어 다른 검색을 획득. 이것은 형광 재건을위한 추가 데이터를 제공한다.
- μCT 및 FMT-스캔이 완료되고 마우스가 마취에서 깨어 났을 때 주변에 도보 또는 흉골 드러 누움을 유지하기 위해, 예를 들어 충분한 의식을 회복 할 때까지,이 방치하지 않습니다.
6. 이미지 퓨전 및 재건
참고 : 후연구 끝에 μCT-FMT 주사, 예를 들면, 완료는, 수집 된 데이터는 자동화 된 이미지 합성 및 형광 재를 사용하도록 정렬 될 필요가있다.
- 추가 처리를 위해 검사를 정렬하려면, 연구를위한 폴더를 만듭니다. 각 μCT-FMT 스캔의 경우, 이름이 마우스 ID와 시점, 예를 들면., M01_02h을 포함하는 하나의 하위 폴더를 만들 수 있습니다.
- 각 μCT-FMT는 스캔, .fmt 파일과 FMT 검사 (위, 아래)를 내보내고 "_up.fmt"또는 "_down.fmt"하나 끝나는 파일 이름을 사용하여 하위 폴더에 저장합니다. 각 .fmt 파일 취득한 원 데이터를 포함하고, 즉, 그러한 노출 시간 등의 카메라, 메타 데이터에 의해 취득 된 여기 및 발광 이미지 및 FMT에 의해 생성 된 형광 재구성.
- μCT 소프트웨어를 사용하여, 등방성 복셀 크기 35 μm의와 재건을 만들 수 있습니다. 부드러운 재건 커널 (T10)을 선택합니다. 그래서 시야를 조정표지를 포함한 전체 마우스 침대가 포함된다. 출력 형식으로 MIFX / 원료를 선택하고 복원을 시작합니다. 복원이 완료되면 μCT-FMT 검사의 하위 폴더에 μCT 재건 파일을 이동합니다.
- 모든 검사에 대한 μCT 및 FMT 데이터를 내 보냅니다. 각 하위 폴더가 두 .fmt (위, 아래) 파일과 MIFX / RAW 형식으로 μCT 재구성이 포함되어 있는지 확인합니다. 완전성을 확인하기> 메뉴 -> CT-FMT-을 선택 Imalytics 전임상 소프트웨어를 사용하여 완전성을 확인합니다. 오류 목록은 파일이나 μCT 재구성 .fmt 누락 된 것으로 나타날 수 있습니다. 오류를 수정하고 모든 오류가 해결 될 때까지 완성도를 확인합니다.
- 메뉴 -> CT-FMT-> 설정을 사용하여 Definiens 소프트웨어의 서버 이름을 확인하고 필요한 경우 조정합니다. 기본값은 HTTP입니다 : // localhost를 : 8184, Definiens 소프트웨어가 같은 컴퓨터에 설치되어 있다고 가정. Definiens 소프트웨어 AU를 수행하는 다음 단계에서 필요한마우스 침대와 마커의 tomated 분할.
- 전체 연구를위한 자동화 μCT-FMT 융합을 수행 할 Imalytics 전임상 소프트웨어에서 메뉴 -> CT-FMT-> 퓨즈 그룹을 클릭합니다. μCT-FMT 검사 및 연구 폴더에 접미사 "패키지"평행 폴더에 결과 당이 작업은 몇 분 정도 걸립니다. 이 파일 추가 분석을 위해 관련된 (μCT 데이터와 융합 공급 업체에서 제공하는 FMT 재건)의 작은 부분 집합이 포함되어 있습니다.
- 지도 (13) 흡수의 생성을 포함하고 산란 형광 재건을 수행 할 Imalytics 전임상 소프트웨어에서 메뉴 -> CT-FMT-> 재구성 그룹 (FMT)를 클릭합니다. 처리 GPU 가속 20 비록 각 재구성 마우스의 크기에 따라 1 내지 4 시간을 필요로한다. 결과는 패키지 폴더에 저장됩니다. 참고 : 높은 처리량을 가능하게하기 위해, 우리는 현재 56 GPU를 GPU 클러스터에서 이러한 복원을 수행합니다.
7. 이미지 분석
참고 : 이미지 데이터의 정량적 측정을 추출하려면, 병변 및 기관의 세분화가 필요합니다.
- 일단 세트를 융합하고 재구성되는 모든 데이터는 Imalytics 전임상 소프트웨어를 사용하여 스캔 각 μCT-FMT에 대한 분할을 만들 수 있습니다.
- 언더로 μCT 파일과 오버레이 형광 파일을로드합니다. 를 눌러 "3D"는 볼륨 렌더링을 켜고 데이터 세트를 검사합니다.
- 세그먼트 폐에, 메뉴 -이> 클래스 -> 클래스를 추가하고 "TMP"라는 이름의 클래스를 만들기를 클릭합니다. 이것은 또한 상황에 맞는 메뉴를 통해 수행 할 수 있습니다. 새로운 클래스를 작성하면 자동으로 다음 분할 작업을위한 출력 클래스로 설정합니다.
- 세그먼트에 μCT 데이터 세트에서 낮은 강도의 모든 영역을 임계 작업을 수행 (클릭 아래 메뉴 -> Segmentation-> Thresholding->를 입력 600). 지금 TMP 클래스 MO 외부 공기를 포함뿐만 아니라 폐 조직을 사용한다.
- "폐"클래스를 만듭니다. "지역 채우기"작업을 수행 외부 공기로부터 폐를 분리, (> 인 지역 채우기 무제한 영역을 채우기> 폐에 마우스 오른쪽 버튼으로 클릭하고 메뉴 - 선택).
- 그것은 더 이상 필요하지 않기 때문에 TMP 클래스를 삭제합니다.
- 세그먼트 볼록 영역, 예를 들면., 방광, 낙서 모드를 사용합니다. 첫 번째 클래스 "방광"을 만들 수 있습니다.
- F1 키를 눌러 모든 낙서를 삭제합니다.
- 컴퓨터 마우스를 사용하여, 방광의 경계를 묘사 할 낙서를 그린다.
- F3을 눌러 빨간색 오버레이로 표시 임시 마스크 낙서로 둘러싸인 영역을 채우기 위해. 반복적으로 (모든 슬라이스 방향으로) 더 낙서를 추가하고 충분한 정확도가 달성 될 때까지 F3 키를 누르십시오. 일반적으로, 10 조각의 낙서는 충분하다.
- F4를 눌러 "방광"로 임시 마스크를 저장합니다.
- 세그먼트에 다음과 같이 진행같은 심장과 신장 등의 볼록 지역. 대부분의 영역은, 예를 들면., 위 또는 간은 약간 볼록 영역들에 의해 근사 될 수있다.
- 세그먼트 척추에, 먼저 "뼈"클래스를 만들 수 있습니다.
- 모든 밝은 복셀을 분류하는 임계 작업을 수행 ContextMenu-> Thresholding-> 위를 선택합니다 (예 :., 1,600 위) "뼈"로.
- 이 골격의 많은 다른 부분, 예를 들면., 리브와 연결되어 있기 때문에 영역 충전 작업은 세그먼트 척추 실패. 반복적으로 낙서 그리기와 두개골, 갈비뼈, 그리고 성례의 뼈에서 척추를 분리 F2 키를 눌러 몇 절단 작업을 수행합니다.
- 마지막으로, 클래스 "척추"를 만들고 척추를 얻을 수있는 지역 충전 작업을 수행 (척추에 마우스 오른쪽 버튼으로 클릭하고 ContextMenu-을 선택> 지역 - 채우기> 제한 지역을 기입).
- 일 내부의 파일로 분할 저장μCT-FMT 스캔의 전자 하위 폴더. 일괄 처리를 사용하려면, organs.seg, 예를 들어, 일관성있는 이름을 사용합니다.
- 평균 형광 강도, 부피와 각 클래스의 총 금액 (평균과 볼륨의 제품을)를 포함하는 스프레드 시트를 생성하기 위해,> 클래스 통계 (오버레이) 메뉴 -> 통계 %를 선택합니다.
- 모든 μCT-FMT 스캔의 모든 지역에 대한 값을 포함하는 단일 스프레드 시트를 생성하려면> 일괄 -> 일괄 통계 메뉴 -> 일괄 -> 설정 일괄 설정을 클릭 한 다음 메뉴 -을 클릭합니다. 이것은 즉, 각 μCT-FMT 스캔 하나 생성하고 많은 스프레드 시트 파일을 병합의 노력을 방지 할 수 있습니다.
8. 프로브 교정
- 프로브의 다른 공지 된 양의 요구와 프로브에 대한 교정 계수를 계산하기 위해, 여러 μCT-FMT 팬텀 스캔은, 예를 들어 (단계 1.4 참조)., 100 pmol의 50 pmol의 25 pmol의 0 pmol의로.
- 에 설명 된대로 팬텀를 스캔FMT에서 섹션 4 팬텀 스캔 또한 5. 상하 검사가 필요합니다.
- 데이터를 내보내고 6 절에 기술 된 바와 같이 융합과 재구성을 수행합니다.
- 세그먼트 (1,200 이상) 임계 화하여 각 스캔 μCT 데이터를 사용하여 포함 및 지역 충전.
- 측정 된 형광 양의 스프레드 시트를 생성하고 확정 된 금액의 함수로 플롯. 선형 회귀 적합의 기울기를 계산합니다. 이 프로브에 대한 교정 인자이다.
결과
우리는 하이드 록시 아파타이트에 결합하여 표적 프로브 OsteoSense의 생체 분포를 평가하기 위해 설명한 프로토콜을 적용 하였다. 3 마우스 (C57BL / 6 APOE - / - AHSG - / - 더블 녹아웃 마우스, 10 주)는 몇 군데 있었다 전과 15 분, 2 시간, 4 시간, 6 시간, 2 nmol의의 OsteoSense의 정맥 주사 후 24 시간. 우리의 소프트웨어가 자동으로 복합 마우스 베드에 내장 마커 검출 (도 1,도 2A, B) FMT (도 2C, D)에 의해 수행되는 형광 재건 해부학 μCT 데이터의 융합을 활성화. OsteoSense은 방광의 저 분자량, 빠른 신장 배설 따라서 높은 신호 프로브 때문에 예상된다. FMT의 형광 재건의 융합은 방광 (그림 2C, D) 외부 잘못 신호 등의 문제를 한 것으로 밝혀졌습니다. FMT는 마우스의 실제 형상을 알고있는 블록 형상을 가정하지 않기 때문에 이러한 문제가 발생한다. 오우R 재건 μCT 데이터로부터 정확한 형상을 결정하고, 산란을 발생 및 흡수는 방광 (도 2E, F)에서 특히 분명하다 나은 신호 위치 파악과 더 정확한 형광 재구성을 가능하게하기 위해 (13)을 매핑한다.
해당 지역에 복원 된 형광을 지정하려면, 우리는 대화 형으로 우리의 소프트웨어 (그림 3)를 사용하여 여러 장기를 분할. (18) 검사 각각에 대해 7 영역은 μCT 데이터, 즉., 심장, 폐, 간, 신장, 척추, 방광과 대장에 기초 분단 하였다. 이어서, 소프트웨어 (126)의 각 영역에 대한 평균 형광 농도를 계산하는데 사용 하였다. 다행히도, 소프트웨어는 모든 값을 계산하고 하나의 스프레드 시트들을 저장 배치 모드를 제공한다.
형광의 분포를 가시화하기 위해, 3D 렌더링은 각 시점에 대해 생성 된,비교 윈도우 설정 (도 4a-F)를 사용. 장기 정량 값을 사용하여, 생체 내 분포는 세 마우스 (도 4G) 위에 장기 평균값에 의해 계산 하였다. 주입 전에 취득한 사전 검사는 무시할 배경 신호를 보여 주었다. 15 분 주사 후, 가장 강한 신호 때문에 빠른 신장 배설, 방광에 출연했다. 이후의 시점에서, 나머지 프로브는 뼈와 관절에 축적되었다.

그림 1. 모드의 마우스 침대. (A) 복합 마우스 침대 단단히 마우스를 잡고 두 아크릴 유리판이 포함되어 있습니다. 긴축은 두 개의 나사를 사용하여 조정됩니다. 마우스 침대 이미지 융합에 대한 마커 (빈 구멍)가 포함되어 있습니다. 마취 가스는 t에 집착하는 유연한 튜브를 사용하여 공급원숭이. (B) 마우스 베드는 금속 홀더에 부착되고, 회전 갠트리 μCT의 중심에 유지된다. 그렇지 않으면 표식 잘못 잘못된 융합 선도 할당 될 수 있기 때문에 (C)는, 마우스 침대 및 금속 홀더 사이의 갭을 피한다. 마취 가스 튜브는 튜브 커넥터에 연결해야합니다. (D)는 마우스 침대는 올바른 자동화 융합을 활성화하려면 전면 처음으로 FMT에 삽입해야합니다. (E) 마커가 자동 마커 검출 및 융합에 사용되는 FMT 카메라에 볼 수 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
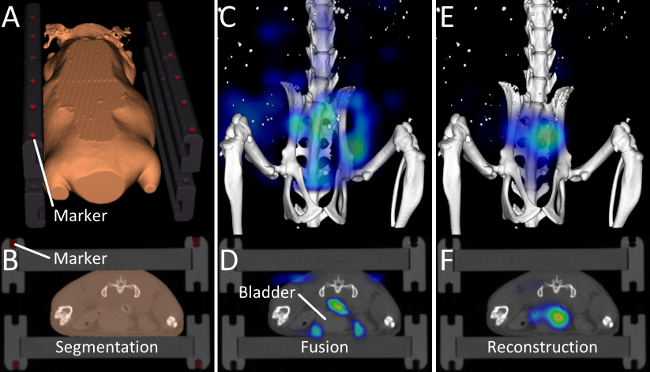
그림 2. 이미지 퓨전 및 재건. (A, B) 마커와 양해 각서 (MOU)의 외형SE는 자동 분할 알고리즘에 의해 결정된다. (C, D) OsteoSense의 주사 후 15 분은, 프로브의 상당량이 이미 방광으로 배설되고있다. μCT 데이터와 공급 업체가 제공하는 재건을 융합 한 후, 문제가 표시됩니다. 신호의 대부분은 방광 주위 아니지만 방광 안에 표시 어떤 신호도 공중에 나타난다. FMT는 블록 모양의 마우스를 가정하기 때문에이 문제가 발생합니다. μCT 데이터에서 파생 된 마우스의 모양을 사용하여 (E, F) 우리의 개선 된 형광 재건, 방광 내부의 형광의 더 나은 현지화의 결과는. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
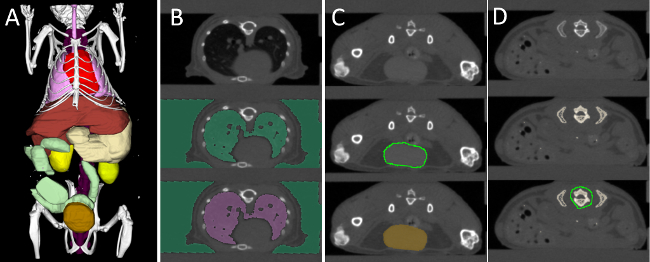
그림 3. 대화 형 장기 Segmentat. 이온 (A)의 형광 분포를 정량화하기 위해, 여러 가지 장기 분할된다 : 심장 (적색), 폐 (분홍색), 간 (브라운), 위장 (베이지 색), 척추 (보라색), 신장 (황색), 소장 (녹색) 그리고 방광 (금). (B)를 강력하게 주변 조직에 비해 대조되는 폐는, 임계 값 및 지역 충전을 사용하여 분할된다. 이러한 방광, 신장, 심장 등 (C) 라운드 기관, "낙서"를 사용하여 분할된다. 더 복잡한 모양, 예를 들면, 간, 위장 (D) 기관은 점진적으로 낙서를 사용하여 분할된다. 척추 세그먼트에, 높은 임계 값은 세그먼트에 모든 뼈를 적용됩니다. 그런 다음 몇 가지 뼈, 예를 들면. 척추가 남을 때까지, 리브, 절단한다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
페이지 내에서 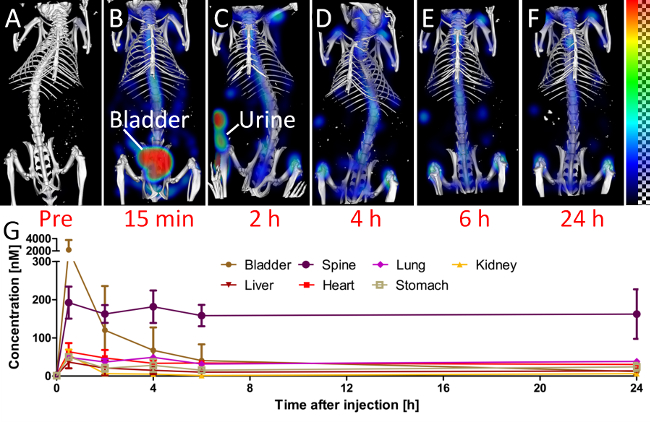
그림 4. 생체 분포. 생체 분포를 평가하기 위해, 마우스는 여러 시점 (AF)에서 검색됩니다. (가) 사전 검사는, 주입하기 전에, 750 nm의 채널에서 약간의 배경 신호를 보여줍니다. (B) 15 분 주사 후, 프로브의 상당량 방광 이미. 마우스 밖에서 형광 결과 (C)을 2 시간 시점에서, 마우스 배뇨했다. 이후의 시점 (DF)에서, 신호는 척추와 무릎, 뼈 및 관절, 즉.에서 우세하게 나타난다. (사) 정량화 형광 농도는 선택된 기관에 대해 표시됩니다.
토론
우리는 기술과 복합 μCT-FMT 이미징을위한 프로토콜을 적용 할 수 있습니다. 17,21 - 우리는 상업적으로 이용 가능하고 널리 사용되는 FMT 및 μCT 장치 3,11,15를 사용합니다. 프로토콜이 특정 FMT를 요구하지만,이 μCT 예와 유사한 기능과 유사한 주사 파라미터와 다른 μCT 의해 대체 될 수 있고, 시야각은 마커를 포함 마우스 침대 커버 할만큼 커야한다.
FMT는 μCT 또는 MRI (21)과 결합하지 않고 생체 분포 분석에 사용 된, 그러나, 해부학 적 데이터 세그먼트가 μCT 데이터 (10)에서 볼 수있는 장기 경계에 기초 할 수 있기 때문에, 재현성을 높이기 위해 유리하다. 집적 μCT-FMT 장치 2,7- 개발되었지만, 이것들은 아직 시판되지 않는다. 또한, 두 개의 분리 된 장치의 사용은 배관, 즉 허용한다. 그 다음, 마우스를 CA먼저 마우스가 처리량을 증가시키기 위해, FMT에있는 동안 N μCT에 이미징 될 수있다.
수동 작업 부하를 줄이기 위해, 우리는 자동화 된 마커 검출 및 융합을 수행합니다. 또한, 마우스의 형상은 자동 분할되고,이 정보는 크게 형광 재구성 11,13,22을 향상시킨다. 양적 형광 재건, 흡수 및 산란지도는 13, 23를 필요합니다. 우리는 μCT 데이터의 자동 분할 및 여러 가지 조직 유형의 알려진 산란 계수 할당 (폐, 뼈, 피부, 지방, 그리고 남아있는 부드러운 조직) (24)에 의해 산란지도를 유도. 다음으로, 우리는 심장 및 간 13, 20는 물론 관류 기관 특히 중요 광학 원시 데이터로부터 흡수 맵을 재구성.
여러 시점에서 여러 마우스 스캔하면 신속하게 데이터의 다수를 초래하여 분석 할 설정한다. biodis 들어기여도 연구는 여러 기관은 각각 μCT-FMT 스캔을 위해 분할 할 필요가있다. 마우스 새롭게 반복적 마우스 침대에 배치되어 있기 때문에 불행히도, 세그먼테이션이 재사용 될 수 없다. 우리는 우리 연구소에서 개발 한 대화 형 분할을위한 도구를 사용하지만, 다른 도구는 25 적절할 수 있습니다. 이 같은 타원과 큐브 (26)와 같은 간단한 모양보다 복잡한 기관에 더 적합하기 때문에 우리는 복셀 현명한 세분화를 생성합니다. 자동화 된 전체 동물 세그멘테이션 더 수동 부하 (27)를 감소하는 것이 유용 할 것이지만, 대화식 분할 도구 여전히 세그멘테이션 오류를 수정하기 위해 요구된다. 또한, 자동 분할 도구는 제대로 병리 등의 특별한 경우를 거의 예상 할 수 없습니다. 우리는 원시 μCT 스캔을 사용하기 때문에, 예컨대 비장 등의 기관 일부는 심지어 수동 세그먼트 매우 어렵다. 조영제는 도움이 될,하지만 내약성에 문제가있다 그것은 maintai 어렵다길이 영상을 통해 NA 정상 조영제의 분포.
우리 팬텀 연구 형광 재건 형상 정보를 사용할 때, 신호 위치 파악이 개선되어있는 것을 알 수있다. 생체가 유사한 개선 이른 시점에 대한 프로브의 다량 이미 (주입 후 15 분), 명백한 방광. 하이드 록시 아파타이트 결합 프로브는 뼈와 관절에 축적한다. 이것이 즉, 신호가 이미 주입 후 척추 15 분에서 명확하게 볼 수 있습니다 발생 얼마나 빨리 현저하다. 이것은 아마 대상 지역 패스트 넘쳐 확산을 가능 프로브의 낮은 분자량에 기인한다. 프로브는 대상 하이드 록시 아파타이트에 공유 결합과 결합되지 않은 프로브는 배설된다. 이후 시점의 경우, 6 시간 및 주입 후 24 시간 사이의 척추에서의 신호 강도는, 아마도 상대적으로 안정적으로 유지 거의 광 재 때문에형광 표백제 깊은 마우스로 아파. 우리의 연구를 위해, 우리는 주입 전에 취득한 스캔으로 분명 낮은 배경 형광 결과 750 nm의 채널을 사용했다. 보다 낮은 파장들에서, 더 많은 배경 신호 (28)를 기대할 수있다.
요약하면, 우리는 시중에서 판매하는 FMT 및 μCT 장치를위한 멀티 모달 이미징 프로토콜을 설명합니다. 우리는 조합이 형광 재건을위한 혜택을 제공 것으로 나타났다. 우리는 생체 분포 곡선 대화식 장기 분할 및 일괄 처리를 이용하여 화상 데이터의 대량 추출되는 방법을 예시한다. 우리는이 표준화 된 워크 플로우는 신약 개발과 형광 표지 된 프로브를 사용하여 다른 영상 연구에 도움이 될 수 있다고 생각합니다.
공개
펠릭스 Gremse는 Gremse-IT, 필립스와 RWTH 아헨 대학의 실험 분자 영상의 부서와 협력하여 의료 영상 분석 소프트웨어 및 서비스를 제공하는 스타트 업 회사의 설립자이자 소유자입니다.
감사의 말
우리는 팬텀 실험을 수행하기위한 마렉 WEILER 감사합니다. 이 작품은 유럽 연구위원회 (ERC 시작 부여 309495 : NeoNaNo)에 의해 지원되었다, 노르 트라 인 베스트 팔렌의 독일 연방 주 (노르 트라 인 베스트 팔렌, High-Tech.NRW/EU-Ziel 2 programm에 (EFRE) ForSaTum), 독일 교육 및 연구 (BMBF)에 대한 정부 (재정 지원 프로그램 가상 간 (0315743), LungSys (0315415C), LungSys2 (0316042F), Photonik Forschung 독일 (13N13355)), RWTH 아헨 대학 (나는 3 TM 종자 기금), 필립스 연구 (아헨, 독일).
자료
| Name | Company | Catalog Number | Comments |
| FMT (Fluorescence molecular tomography) FMT2500 LX | PerkinElmer | FMT2000 | Device for fluorescence molecular tomography |
| µCT (micro computed tomography) Tomoscope Duo | CT Imaging GmbH | Tomoscope Duo | Device for micro computed tomography |
| Multimodal Mouse Bed | CT Imaging GmbH | Experimental builder | Partially transparent animal holder |
| IsoFlo (isoflurane, USP) | Abbott | 05260-05 | Isoflurane Inhalation anesthesia |
| Small animal anesthesia system | Harvard apparatus | 726419 | Complete Isoflurane Table-Top System |
| Chlorophyll-free mouse food | Ssniff | E15051 | low chlorophyll / low fluorescence food |
| OsteoSense 750EX | PerkinElmer | NEV10053EX | Animal FMT contrast agent |
| Portex Fine Bore Polythene Tubing | Smith medical | 800/100/120 | Tube for injection catheter |
| Sterican 30g | BBraun | 4656300 | Hypodermic needle for catheter |
| Imeron | Altana pharma | INLA F.1/0203/3.5337.69 | CT contrast agent for the phantom inclusions |
| Agarose | Sigma | 90-12-36-6 | Agarose for phantom production |
| TiO2 | Applichem | A1900,1000 | Titanium oxyde as phantom scattering agent |
| Trypan blue | Fluka | 93595 | Trypan blue to adjust phantom light propagation |
| Cy7 | Lumiprobe | 15020 | Fluorochrome for the phantom inclusions |
| Lipovenoes 20% | Fresenius Kabi | 3094740 | Lipid emulsion, scattering agent for FMT contrast agents |
| Definiens Developer XD Server | Definiens AG | Server XD | Software platform for automated segmentation |
| Imalytics Preclinical | ExMI/Gremse-IT | Version 2.0.1 | Software for image fusion, reconstruction and analysis |
| NVIDIA Geforce Titan | Asus | GTXTITAN6GD5 | High end computer graphics card, 6GB Memory |
참고문헌
- Hoffman, R. M., Yang, M. Subcellular imaging in the live mouse. Nature Protocols. 1 (2), 775-782 (2006).
- Ale, A., Ermolayev, V., Herzog, E., Cohrs, C., Angelis, M. H., Ntziachristos, V. FMT-XCT: in vivo animal studies with hybrid fluorescence molecular tomography-X-ray computed tomography. Nature Methods. 9 (9), 615-620 (2012).
- Eaton, V. L., Vasquez, K. O., Goings, G. E., Hunter, Z. N., Peterson, J. D., Miller, S. D. Optical tomographic imaging of near infrared imaging agents quantifies disease severity and immunomodulation of experimental autoimmune encephalomyelitis in vivo. Journal of Neuroinflammation. 10 (138), (2013).
- Lederle, W., Arns, S., et al. Failure of annexin-based apoptosis imaging in the assessment of antiangiogenic therapy effects. EJNMMI Research. 1 (26), (2011).
- Ntziachristos, V., Tung, C. -. H., Bremer, C., Weissleder, R. Fluorescence molecular tomography resolves protease activity in vivo. Nature Medicine. 8 (7), (2002).
- Hoffman, R. M. The multiple uses of fluorescent proteins to visualize cancer in vivo. Nature Reviews Cancer. 5 (10), 796-806 (2005).
- Schulz, R. B., Ale, A., et al. Hybrid system for simultaneous fluorescence and x-ray computed tomography. IEEE Transactions on Medical Imaging. 29 (2), 465-473 (2010).
- Stuker, F., Baltes, C., et al. Hybrid small animal imaging system combining magnetic resonance imaging with fluorescence tomography using single photon avalanche diode detectors. IEEE Transactions on Medical Imaging. 30 (6), 1265-1273 (2011).
- Leblond, F., Davis, S. C., Valdés, P. A., Pogue, B. W. Preclinical Whole-body Fluorescence Imaging: Review of Instruments, Methods and Applications. Journal of Photochemistry and Photobiology B: Biology. 98 (1), 77-94 (2010).
- Kunjachan, S., Gremse, F., et al. Noninvasive optical imaging of nanomedicine biodistribution. ACS Nano. 7 (1), 252-262 (2013).
- Radrich, K., Ale, A., Ermolayev, V., Ntziachristos, V. Improving limited-projection-angle fluorescence molecular tomography using a co-registered x-ray computed tomography scan. Journal of Biomedical Optics. 17 (12), 126011 (2012).
- Freyer, M., Ale, A., Schulz, R. B., Zientkowska, M., Ntziachristos, V., Englmeier, K. -. H. Fast automatic segmentation of anatomical structures in x-ray computed tomography images to improve fluorescence molecular tomography reconstruction. Journal of Biomedical Optics. 15 (3), 036006 (2010).
- Gremse, F., Theek, B., et al. Absorption Reconstruction Improves Biodistribution Assessment of Fluorescent Nanoprobes Using Hybrid Fluorescence-mediated Tomography. Theranostics. 4 (10), 960-971 (2014).
- Cheong, W. -. F., Prahl, S. A., Welch, A. J. A review of the optical properties of biological tissues. IEEE Journal of Quantum Electronics. 26 (12), 2166-2185 (1990).
- Doleschel, D., Mundigl, O., et al. Targeted near-infrared imaging of the erythropoietin receptor in human lung cancer xenografts. Journal of Nuclear Medicine: Official Publication, Society of Nuclear Medicine. 53 (2), 304-311 (2012).
- Al Rawashdeh, W., Arns, S., et al. Optical tomography of MMP-activity allows a sensitive non-invasive characterization of the invasiveness and angiogenesis of SCC-xenografts. Neoplasia. 16 (3), 235-246 (2014).
- Kunjachan, S., Pola, R., et al. Passive versus Active Tumor Targeting Using RGD- and NGR-Modified Polymeric Nanomedicines. Nano Letters. 14 (2), 972-981 (2014).
- Schober, A., Nazari-Jahantigh, M., et al. MicroRNA-126-5p promotes endothelial proliferation and limits atherosclerosis by suppressing Dlk1. Nature Medicine. 20 (4), 368-376 (2014).
- Aikawa, E., Nahrendorf, M., et al. Osteogenesis associates with inflammation in early-stage atherosclerosis evaluated by molecular imaging in vivo. Circulation. 116 (24), 2841-2850 (2007).
- Gremse, F., Höfter, A., Schwen, L., Kiessling, F., Naumann, U. GPU-Accelerated Sparse Matrix-Matrix Multiplication by Iterative Row Merging. SIAM Journal on Scientific Computing. , C54-C71 (2015).
- Vasquez, K. O., Casavant, C., Peterson, J. D. Quantitative Whole Body Biodistribution of Fluorescent-Labeled Agents by Non-Invasive Tomographic Imaging. PLoS ONE. 6 (6), e20594 (2011).
- Theek, B., Gremse, F., et al. Characterizing EPR-mediated passive drug targeting using contrast-enhanced functional ultrasound imaging. Journal of Controlled Release. 182 (1), 83-89 (2014).
- Hyde, D., Schulz, R., Brooks, D., Miller, E., Ntziachristos, V. Performance dependence of hybrid x-ray computed tomography/fluorescence molecular tomography on the optical forward problem. Journal of the Optical Society of America. A, Optics, Image Science, and Vision. 26 (4), 919-923 (2009).
- Jacques, S. L. Optical properties of biological tissues: a review. Physics in Medicine and Biology. 58 (11), R37 (2013).
- Loening, A. M., Gambhir, S. S. AMIDE: a free software tool for multimodality medical image analysis. Molecular Imaging. 2 (3), 131-137 (2003).
- Gremse, F., Schulz, V. Qualitative and Quantitative Data Analysis. Small Animal Imaging. , 363-378 (2011).
- Baiker, M., Milles, J., et al. Atlas-based whole-body segmentation of mice from low-contrast Micro-CT data. Medical Image Analysis. 14 (6), 723-737 (2010).
- Sevick-Muraca, E. M., Rasmussen, J. C. Molecular imaging with optics: primer and case for near-infrared fluorescence techniques in personalized medicine. Journal of Biomedical Optics. 13 (4), 041303 (2008).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유