É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Protocolo clínico de produzir tecido adiposo-derivado do estroma Vascular fração para a regeneração da cartilagem potenciais
Neste Artigo
Resumo
Aqui, apresentamos um protocolo para produzir uma tecido adiposo-derivado do estroma vascular fração e sua aplicação para melhorar as funções de joelho Regenerando o tecido da cartilagem, como em pacientes humanos com osteoartrite.
Resumo
Osteoartrite (OA) é uma das mais comuns doenças debilitantes. Recentemente, várias tentativas foram feitas para melhorar as funções dos joelhos usando diferentes formas de células-tronco mesenquimais (MSCs). Na Coreia, concentrados de medula óssea e cordão hemoderivados células-tronco foram aprovadas pela Korean Food and Drug Administration (KFDA) para regeneração da cartilagem. Além disso, uma tecido adiposo-derivado do estroma vascular fração (SVF) foi autorizada pelo KFDA para injeções conjuntas em pacientes humanos. SVF autóloga derivadas de tecido adiposo contém matriz extracelular (ECM), além de células-tronco mesenquimais. ECM excreta várias citocinas que, juntamente com o ácido hialurónico (HA) e o plasma rico em plaquetas (PRP) ativado pelo cloreto de cálcio, podem ajudar o MSCs para regenerar a cartilagem e melhorar as funções do joelho. Neste artigo, apresentamos um protocolo para melhorar as funções do joelho Regenerando o tecido da cartilagem, como em pacientes humanos com OA. O resultado do protocolo foi primeiramente relatado em 2011, seguido por algumas publicações adicionais. O protocolo envolve lipoaspiração para obter lipoaspirates autólogo que são misturados com colagenase. Esta mistura de lipoaspirates-colagenase é então cortada e homogeneizada para remover grandes de tecido fibroso que pode entupir a agulha durante a injeção. Depois disso, a mistura é incubada para obter SVF derivadas de tecido adiposo. O resultante SVF derivadas de tecido adiposo, contendo tecido adiposo-derivado MSCs e restos de ECM, é injetado em joelhos de pacientes, combinados com HA e cloreto de cálcio ativado PRP. Incluem-se três casos de pacientes que foram tratados com nosso protocolo, resultando em melhora da amplitude de movimento, juntamente com provas de MRI de cartilagem hialina, como tecido, inchaço e dor no joelho.
Introdução
Células-tronco mesenquimais (MSCs) são conhecidas por terem a capacidade de regenerar a cartilagem1,2,3,4,5,6. Elas podem ser facilmente obtidas de várias fontes: sangue do cordão umbilical, medula óssea e tecido adiposo, entre muitos outros. Entre essas fontes, o tecido adiposo é a única fonte onde um número suficiente de MSCs pode ser obtido sem qualquer expansão da cultura para regenerar a cartilagem em ambientes clínicos7,8. Autólogo de medula óssea do estroma vascular fração (SVF) pode ser facilmente obtida também. No entanto, o número de células-tronco contida na medula expandida não-cultura é muito baixa7,8. Sangue do cordão umbilical pode conter um número suficiente de MSCs. No entanto, o sangue do cordão umbilical não é uma fonte prontamente disponível de SVF autólogo.
Numerosos métodos de processamento de tecido adiposo para obter SVF estão disponíveis para aplicações clínicas. Entre estes, o método de obtenção MSCs de tecido adiposo usando colagenase, desenvolvida e confirmada pelo Zuk et al 5 , 6, é muito bem aceito. Este método de usar colagenase foi modificado para aplicações clínicas em Ortopedia. A fim de ser aplicada a situações clínicas, o sistema deve ser um sistema fechado para manter a esterilidade, mantendo a conveniência. Uma modificação particular apresentada neste artigo envolve homogeneização do lipoaspirates. Lipoaspirates tamanhos pequenos são digeridos relativamente mais rápido do que os maiores que estão resultando na repartição desigual de tecido adiposo. Além disso, estes lipoaspirates de tamanhos maiores pode produzir tecidos fibrosos que podem entupir as seringas e agulhas durante a execução conjunta de injeções9,10. Para evitar esses problemas, o lipoaspirates pode ser homogeneizado por corte e picagem a lipoaspirates antes da incubação com colagenase. O SVF derivadas de tecido adiposo resultante pode conter mais uniforme da matriz extracelular (ECM) em comparação com lipoaspirates que não são homogeneizadas11. O ECM quebrado contido o SVF pode funcionar como um andaime12.
Em 2009, foi autorizada pela Korean Food and Drug Administration (KFDA) quando processado dentro de uma instalação médica com processamento mínimo, por um médico13SVF autóloga derivadas de tecido adiposo. Depois, SVF autóloga derivadas de tecido adiposo tem sido utilizada como um agente potencial para melhorar as funções do joelho em pacientes de osteoartrite (OA) potencialmente regenerando tecido de cartilagem, como10,14,15 , 16 , 17 , 18 .
Em 2011, Pak mostrou pela primeira vez que derivadas de tecido adiposo as células-tronco (ASCs) contidas no SVF derivadas de tecido adiposo podem melhorar as funções de joelho potencialmente regenerar o tecido da cartilagem, como em pacientes humanos de OA quando injetado com rico em plaquetas plasma (PRP) 14. Além disso, Pak et al relataram dados de segurança em 2013 envolvendo 91 pacientes. A taxa de eficácia média relatada nesses dados de segurança foi 67%15. Posteriormente, estudos adicionais por Pak et al mostraram joelho melhorou funções potencialmente devido a regeneração do tecido de cartilagem, como em pacientes com um menisco lacrimal e condromalacia patelas10,16,17 ,18. Com base em artigos relatados, é sabido que o número de células-tronco contida em 100 g de tecido adiposo processado pelo protocolo apresentado neste artigo pode variar de 1.000.000-40,000,000 dependendo características8, dos pacientes 19 , 20 , 21 , 22 , 23.
Aqui, apresentamos um protocolo clínico do joelho humano OA usando SVF autóloga derivadas de tecido adiposo com HA e PRP ativado com cloreto de cálcio. A primeira versão do presente protocolo clínico, envolvendo um sistema fechado, manual para manter a esterilidade, foi relatada em 201114. O protocolo idêntico foi otimizado, manutenção de esterilidade e foi relatado em 2013 e 201610,15. Aqui, o protocolo otimizado é apresentado. A visão esquemática do protocolo é apresentado na Figura 1.
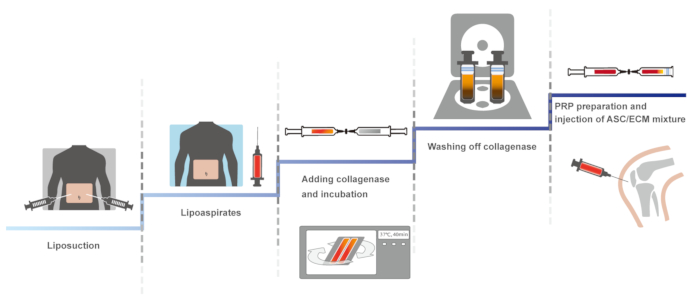
Figura 1: A visão esquemática do protocolo. Clique aqui para ver uma versão maior desta figura.
Protocolo
A aprovação e o consentimento para relatar após relatos de casos dispensadas pelo Comité do Conselho de revisão institucional Myongji University (MJUIRB). Além disso, este protocolo clínico foi em conformidade com as diretrizes da declaração de Helsinque e regulamento do KFDA. Para os procedimentos, consentimento informado foram obtido de pacientes.
1. lipoaspiração
Nota: Execute com técnica estéril.
- Use os seguintes critérios de inclusão: (1) provas de MRI da fase 3 OA; (2) masculino ou feminino; (3) mais de 18 anos de idade; (4) suficiente tecido adiposo de (100-110 g) para lipoaspiração; (5) falta de vontade de prosseguir com a intervenção cirúrgica; (6) a falha do tratamento conservador; e a dor incapacitante em curso (7).
- Use os seguintes critérios de exclusão: (1) doença inflamatória ou tecido conjuntivo ativa pensado para impactar a condição de dor (ou seja,lúpus, artrite reumatoide, fibromialgia); (2) ativo transtorno endócrino que possa afetar a condição de dor (ou seja,, hipotireoidismo, diabetes); (3) ativo distúrbio neurológico que possa afetar a condição de dor (ou seja,, neuropatia periférica, esclerose múltipla); (4) doença pulmonar ativa, que exigem o uso de medicação; e (5) sem histórico de injeções de esteroides conjuntas últimos 3 meses.
- Trazer o paciente para uma sala de cirurgia com uma capa de A de classe de risco biológico e coloque ele (ou ela) em posição supina.
- Limpe a área abdominal do paciente com 5% de betadine (povidone-iodo) e armar o paciente utilizando a técnica estéril, expondo a área limpa do abdômen para a lipoaspiração.
- Cerca de 5 cm infero-lateralmente a partir do umbigo, anestesiamos dois locais (um na esquerda e o outro no lado direito do umbigo) da incisão para fazer usando 2 mL de lidocaína a 2% sem epinefrina com uma agulha (25 gauge, 1½ polegadas) em uma seringa de 5 mL através da injeção de cada site a nível epidérmico.
- Anestesia o local da incisão para fazer usando 5 mL de solução tumescente (500 mL de normal salina, 40 mL de lidocaína a 2%, 20 mL de bupivacaína a 0,5%, 0,5 mL de epinefrina 1: 1000) em uma seringa de 10 mL com agulha (calibre 25, 1½ polegadas).
- Fazer 2 incisões de 0,5 cm aproximadamente 5 cm abaixo do umbigo lateralmente por beliscar a pele para aumentar a profundidade do nível subcutâneo.
- Usando lâmina n º 11, picar a pele levantada para penetrar ao nível subcutâneo, mas não para penetrar através da parede abdominal.
- Usando a cânula de calibre 16 cm 20, anestesia o nível subcutâneo da área conjunto inferior de abdômen, que é to-be-aspirada, com 700 a 800 mL da solução tumescente.
- Após acabamento infiltração do conjunto inferior abdômen com a solução tumescente, preparar um aparelho de lipoaspiração conectando-se uma cânula de 3,0 mm, ligada a um 60 mL (ou um 30ml) seringa para lipoaspiração manual ou uma cânula especialmente concebidos 3,0 mm conectado a um kit de centrífuga, uma seringa de sistema fechado, com a finalidade de manter a esterilidade, conectado a uma máquina de vácuo para a lipoaspiração assistida por vácuo.
- Execute a lipoaspiração para obter 100-110 g de tecido adiposo, excluindo a solução tumescente. Ao realizar a lipoaspiração, tecido adiposo será obtido junto com a solução tumescente, que deve ser separada e removida.
- Para separar a solução tumescente, primeiro pela gravidade, transfira o tecido adiposo no kit centrífuga a uma seringa de 60 mL e a seringa para baixo (ou seja, que a parte da seringa é na parte inferior). Por esperando 5-6 min, o tecido adiposo e o fluido tumescente serão separados. Remova o fluido na parte inferior da seringa pressionando a parte superior do êmbolo da seringa.
- Execute as etapas acima 1.9-1.11 até que tenha sido acumulado um total de 100-110 g de tecido adiposo (lipoaspirates) pelo joelho.
2. preparação da mistura ASC/ECM com sistema fechado estéril
- Após a separação da solução tumescente por gravidade e acumulando 50-55 g de lipoaspirates por cada kit de 60 mL centrífuga, um sistema fechado estéril, colocar os kits de 2 centrífuga em um balde de recipiente de centrífuga e girar a 1600 x g por 5 min, condensação a lipoaspirates e separando o fluido do tecido adiposo. Neste processo de mais condensa-se, o lipoaspirates pode produzir óleo gorduroso, em certos casos.
- Ser cauteloso para não agitar, remover a tampa de segurança e o plug na parte inferior do kit centrífuga.
- Remova o fluido de fundo pressionando lentamente para baixo na parte superior do êmbolo do kit centrífuga.
- Seringa de 60ml separado, dissolva 10mg de colagenase (5 mg de colagenase específico para o tecido conjuntivo24 ) e 5 mg de colagenase específico para tecido adiposo25com 50 mL de solução salina.
- Misturar aproximadamente 25-30 mL de lipoaspirate condensado com colagenase dissolvido (5 mg de colagenase específico para tecido conjuntivo) e 5 mg de colagenase específico para o tecido adiposo a uma proporção de 1:1 (v: v) conectando-se a seringa de 60 mL para um kit de centrífuga usando um conector especializado.
- Misture bem o lipoaspirate condensada e a colagenase, empurrando o conteúdo entre a seringa de 60 mL e os kits de centrífuga usando uma vara ou um traficante.
- Transfira a mistura da lipoaspirate e a colagenase volta para seringas de 60 mL.
- Conecte cada seringa de 60 mL contendo a mistura com um homogeneizador que contém lâminas.
- Conecte uma seringa de 60ml vazio à outra extremidade do homogenizador.
- Empurre a mistura na outra seringa de 60ml através do homogenizador para 4 -6 vezes, resultando em corte e picagem do lipoaspirate.
- Transferir o lipoaspirate homogeneizado e a mistura de colagenase volta para kits de centrífuga 60 mL através de um conector especializado
- Coloque os kits de centrífuga num recipiente para ser colocado em uma incubadora que tenha sido previamente aquecida a 37 ° C.
- Incube os kits de dois centrífuga com a mistura homogeneizada a 37 ° C por 40 min enquanto roda a 45 rpm.
- Após o 40 min de incubação, remova o recipiente da incubadora de forma estéril. Em seguida, remover os kits de centrífuga e colocá-los em uma máquina centrífuga.
- Centrifugar as misturas a 800 x g por 5 min separar o SVF derivadas de tecido adiposo.
- Após a centrifugação, remover o sobrenadante (que inclui a colagenase e digerido o tecido adiposo) de cada kits de centrífuga, removendo a tampa da seringa na parte superior do êmbolo e colocando uma seringa de 30 mL no êmbolo abertura através do bloqueio de seringa conexão.
- Lentamente, pressione para baixo a parte do barril da seringa de 30 mL para o sobrenadante encher a seringa de 30 mL.
- Pressione para baixo o barril de seringa de 30 mL até os último 3-4 mL de fundo do kit centrífuga, deixando apenas o último 3-4 mL de SVF derivadas de tecido adiposo. O sobrenadante será Descartado.
- Remova a seringa de 30 mL da parte superior do êmbolo e encha a seringa com dextrose 5% em solução de Ringer lactato (D5LR).
- Anexando-se a seringa de 30 mL, cheia de D5LR na parte superior do atuador de abertura, preencher os kits de centrífuga, contendo 3-4 mL de SVF derivadas de tecido adiposo, com D5LR até 55 mL.
- Remova a seringa de 30 mL, cap o êmbolo e centrifugue os kits de centrifugar novamente a 300 x g durante 4 min.
- Repita as etapas 2.17-2.21 para um total de 4 lavagens. A colagenase utilizada é xenogénica. Portanto, a maioria de colagenase é removido por 4 lavagens. No entanto, para aprovação da FDA, ajuste fino do protocolo pode ser necessário remover completamente os resíduos de colagenase em volume final, embora a quantidade atual de resíduos de colagenase pode ser insignificante o suficiente para os pacientes que não têm qualquer clínico efeitos colaterais.
- Após a centrifugaçãoth 4, a fim de obter o SVF final para a injeção, remova a tampa de segurança e o plug na abertura inferior do kit centrífuga, sem tremer ou transformar o kit de centrífuga.
- Anexe uma seringa de 20 mL para o fundo do kit centrífuga abertura usando um conector especialmente projetado.
- Puxe o êmbolo da seringa várias vezes e volta a agitar-se as células que se instalaram na parte inferior do kit centrífuga.
- Remover o volume total desejado o SVF contendo ASCs e ECM juntamente com outras células e tecidos (geralmente cerca de 3-4 mL de cada kit de centrífuga para injeções de articulação de joelho).
3. PRP preparação com técnica estéril
- Enquanto preparava o ASCs e ECM, desenhe com 2,5 mL de solução de anticoagulante citrato dextrose 30 mL de sangue autólogo.
- Transferi o sangue desenhado para os kits de centrífuga de 60 mL.
- Centrifugar o sangue extraído a 730 x g por 5 min e retire o sobrenadante para um novo kit de centrífuga de 60 mL. Centrifugue o sobrenadante a 1300 x g durante 4 min, resultando em 3-4 mL de PRP.
- Antes da injeção, adicionar 3% (p/v) de cloreto de cálcio na proporção de 10:2 (PRP: cloreto de cálcio, v: v) para a PRP para ativá-lo.
- Adicione 0,5% (p/v), como um andaime, HA para o PRP ativado com cloreto de cálcio. Estes ASCs com ECM, juntamente com o PRP, ativado pelo cloreto de cálcio, e HA defende a mistura ASC/ECM.
4. ASC/ECM baseada na mistura de tratamento
- Limpe o joelho do paciente com 5% de betadine e armá-lo de forma estéril.
- Palpe o anterior do joelho para o espaço articular entre os ossos da tíbia e fêmur.
- Anestesia o local da injeção superficialmente com lidocaína diluído (1 mL de lidocaína a 1% diluída com 4 mL de solução salina) da pele apenas fora da cápsula articular.
- Anestesia o interior da cápsula articular com ropivacaína diluída (ropivacaína a 0,75% 1ml diluída com 3 mL de solução salina).
- Misture 2 mL de HA para o 6-8 mL de SVF contido em uma seringa de 20 mL através do conector de seringa-para-seringa.
- Usando um conector de seringa-para-seringa, adicione 0,4 mL de cloreto de cálcio para o 3-4 mL de PRP que já foi preparado autólogo e estar pronto em uma seringa de 5 mL.
- Combine o 3,5-4,5 mL de cloreto de cálcio PRP em uma seringa de 5 mL com 8-10 mL de mistura SVF/HA em um 20ml seringa através de seringa para seringa conector.
- Imediatamente injete a mistura (cerca de 12-15 mL) lentamente a articulação tíbio-femoral anterior dos joelhos usando agulha de calibre 18 de 38 mm, com ou sem a orientação do ultra-som.
- Após a injeção, curativo no local da injeção com pressão dobrando a gaze de algodão 4 x 4 4 vezes e colocação de fitas sobre a gaze dobrada de 4 x 4.
- Instrua o paciente a permanecer ainda por 60 min permitir a fixação da célula.
- Instrua o paciente a limitar as atividades para o mínimo de 1 semana após a alta da clínica.
- Retornar à clínica para três injeções adicionais de PRP ativado por cloreto de cálcio durante 3 semanas.
5. acompanhamento pós-tratamento de
- Avalie o paciente na semana de 2, 4 e 16 (18 ou 22) para melhoria da dor em termos de escala analógica visual (VAS) e melhoria da função em termos de parâmetros de terapia física. Determine o índice de classificação funcional (FRI), VAS e amplitude de movimento (ROM) como descrito anteriormente,26,,27.
- Acompanhar o paciente por pós-tratamento MRI 3 meses após o tratamento.
Resultados
Três pacientes (uma mulher de 87 anos, com estágio 3 OA, um homem de 68 anos, com estágio 3 OA, e uma mulher de 60 anos com estágio 3 OA) sem qualquer passado significativo histórico médico apresentado à clínica com dor persistente no joelho e desejado para o potencial tratamento de SVF autólogo derivadas de tecido adiposo. Todos os três pacientes tinham seu joelho examinado por um cirurgião ortopédico e ofereceram-se para ter a substituição total do joelho (TKR) e estavam r...
Discussão
Em 2001, Zuk et al. células-tronco isoladas de tecido adiposo por quebrar a matriz de colágeno com colagenase6. Depois, o grupo mostrou que essas células-tronco isoladas de tecido adiposo pode transformar em cartilagem e outros tecidos da mesoderme, na origem, provando que essas células-tronco eram mesenquimais na origem.
Da mesma forma, o procedimento apresentado neste artigo é um protocolo modificado para aplicar o método semelhante para pacientes human...
Divulgações
Os autores não têm nada para divulgar.
Agradecimentos
O autor reconhece que o apoio da equipe do Mipro clínica médica e o desenho de figura por Mariana/David Lee. Este trabalho foi apoiado por bolsas de investigação do Bio & programa de desenvolvimento de tecnologia médica da NRF financiada pelo MSIT (número NRF-2017M3A9E4078014); e o nacional Research Foundation da Coreia (NRF) financiado pelo Ministério da ciência e TIC (números NRF-2017R1A2B4002315 e NRF-2016R1C1B2010308).
Materiais
| Name | Company | Catalog Number | Comments |
| Material | |||
| 5% Betadine (povidone-iodine) | Firson Co., Ltd. | 657400260 | |
| 2% Lidocaine | Daehan Pharmaceutical Co. | 670603480 | |
| Tumescent solution | Myungmoon Pharm. Co. Ltd. | N01BB01 | The solution was composed of 500 mL normal saline, 40 mL 2% lidocaine, 20 mL 0.5% marcaine, and 0.5 mL epinephrine 1:1000. |
| Liberase TL and TM research grade | Roche Applied Science | 5401020001 | |
| D5LR | Dahan Pharm. Co., Ltd. | 645101072 | Dextrose 5% in lactated Ringer's solution |
| Anticoagulant citrate dextrose solution | Fenwal, Inc. | NDC:0942-0641 | The solution was composed of 0.8% citric acid, 0.22% sodium citrate, and 0.223% dextrose. |
| 3% (w/v) Calcium chloride | Choongwae Pharmaceutical Co. | 644902101 | |
| 0.5% (w/v) HA (Hyaluronic acid ) | Dongkwang pharm. Co., Ltd. | 645902030 | |
| 0.25% Ropivacaine | Huons Co., Ltd. | 670600150 | |
| Equipment | |||
| 3.0 mm Cannula | WOOJU Medical Instruments Co. | ML30200 | |
| 60-mL Luer-Lock syringe | BD (Becton Dickinson) | 309653 | |
| Centrifuge Barrel Kit | CPL Co., Ltd. | 30-0827044 | |
| Tissue homogenizer that contains blades | CPL Co., Ltd. | 30-0827045 | |
| Rotating incubator mixer | Medikan Co., Ltd | MS02060092 | |
| Centrifuge | Hanil Scientific Inc. | CE1133 | |
| Magnetic Resonance Imaging | Philips Medical Systems Inc. | 18068 | |
| Ultrasound Imaging System | Samsung Medison co., Ltd | CT-LK-V10-ICM-09.05.2007 |
Referências
- Arnoczky, S. P. Building a meniscus. Biologic considerations. Clinical Orthopaedics and Related Research. (367 Suppl), S244-S253 (1999).
- Barry, F. P. Mesenchymal stem cell therapy in joint disease. Novartis Foundation Symposium. 249, 86-241 (2003).
- Usuelli, F. G., et al. Adipose-derived stem cells in orthopaedic pathologies. British Medical Bulletin. 124 (1), 31-54 (2017).
- Zhang, H. N., Li, L., Leng, P., Wang, Y. Z., Lv, C. Y. Uninduced adipose-derived stem cells repair the defect of full-thickness hyaline cartilage. Chinese Journal of Traumatology. 12 (2), 92-97 (2009).
- Zuk, P. A., et al. Human adipose tissue is a source of multipotent stem cells. Molecular Biology of the Cell. 13 (12), 4279-4295 (2002).
- Zuk, P. A., et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Engineering. 7 (2), 211-228 (2001).
- Baer, P. C., Geiger, H. Adipose-derived mesenchymal stromal/stem cells: tissue localization, characterization, and heterogeneity. Stem Cells International. 2012, 812693 (2012).
- Zhu, Y., et al. Adipose-derived stem cell: a better stem cell than BMSC. Cell Biochemistry and Function. 26 (6), 664-675 (2008).
- Bellei, B., Migliano, E., Tedesco, M., Caputo, S., Picardo, M. Maximizing non-enzymatic methods for harvesting adipose-derived stem from lipoaspirate: technical considerations and clinical implications for regenerative surgery. Scientific Reports. 7 (1), 10015 (2017).
- Pak, J., Lee, J. H., Park, K. S., Jeong, B. C., Lee, S. H. Regeneration of Cartilage in Human Knee Osteoarthritis with Autologous Adipose Tissue-Derived Stem Cells and Autologous Extracellular Matrix. BioResearch Open Access. 5 (1), 192-200 (2016).
- Alexander, R. W. Understanding Adipose-derived Stromal Vascular Fraction (AD-SVF) Cell Biology and Use on the Basis of Cellular, Chemical, Structural and Paracrine Components: A Concise Review. Journal of Prolotherapy. 4, e855-e869 (2012).
- Benders, K. E., et al. Extracellular matrix scaffolds for cartilage and bone regeneration. Trends in Biotechnology. 31 (3), 169-176 (2013).
- Korean Food and Drug Administration (KFDA). Cell therapy: Rules and Regulations. KFDA. , (2009).
- Pak, J. Regeneration of human bones in hip osteonecrosis and human cartilage in knee osteoarthritis with autologous adipose-tissue-derived stem cells: a case series. Journal of Medical Case Reports. 5, 296 (2011).
- Pak, J., Chang, J. J., Lee, J. H., Lee, S. H. Safety reporting on implantation of autologous adipose tissue-derived stem cells with platelet-rich plasma into human articular joints. BMC Musculoskeletal Disorders. 14, 337 (2013).
- Pak, J., Lee, J. H., Kartolo, W. A., Lee, S. H. Cartilage Regeneration in Human with Adipose Tissue-Derived Stem Cells: Current Status in Clinical Implications. BioMed Research International. 2016, 4702674 (2016).
- Pak, J., Lee, J. H., Lee, S. H. A novel biological approach to treat chondromalacia patellae. PLoS One. 8 (5), e64569 (2013).
- Pak, J., Lee, J. H., Lee, S. H. Regenerative repair of damaged meniscus with autologous adipose tissue-derived stem cells. BioMed Research International. 2014, 436029 (2014).
- Aust, L., et al. Yield of human adipose-derived adult stem cells from liposuction aspirates. Cytotherapy. 6 (1), 7-14 (2004).
- De Ugarte, D. A., et al. Comparison of multi-lineage cells from human adipose tissue and bone marrow. Cells Tissues Organs. 174 (3), 101-109 (2003).
- Guilak, F., et al. Clonal analysis of the differentiation potential of human adipose-derived adult stem cells. Journal of Cellular Physiology. 206 (1), 229-237 (2006).
- Mitchell, J. B., et al. Immunophenotype of human adipose-derived cells: temporal changes in stromal-associated and stem cell-associated markers. Stem Cells. 24 (2), 376-385 (2006).
- Oedayrajsingh-Varma, M. J., et al. Adipose tissue-derived mesenchymal stem cell yield and growth characteristics are affected by the tissue-harvesting procedure. Cytotherapy. 8 (2), 166-177 (2006).
- . Liberase TL information available from Sigma Millipore online Available from: https://www.sigmaaldrich.com/catalog/product/roche/05401020001?lang=en®ion=US (2018)
- . Liberase TM information available from Sigma Millipore online Available from: https://www.sigmaaldrich.com/catalog/product/roche/Libtmro?lang=en®ion=US (2018)
- Childs, J. D., Piva, S. R. Psychometric properties of the functional rating index in patients with low back pain. European Spine Journal. 14 (10), 1008-1012 (2005).
- Price, D. D., McGrath, P. A., Rafii, A., Buckingham, B. The validation of visual analogue scales as ratio scale measures for chronic and experimental pain. Pain. 17 (1), 45-56 (1983).
- Pilgaard, L., Lund, P., Rasmussen, J. G., Fink, T., Zachar, V. Comparative analysis of highly defined proteases for the isolation of adipose tissue-derived stem cells. Regenerative Medicine. 3 (5), 705-715 (2008).
- D'Ambrosi, R., Indino, C., Maccario, C., Manzi, L., Usuelli, F. G. Autologous Microfractured and Purified Adipose Tissue for Arthroscopic Management of Osteochondral Lesions of the Talus. Journal of Visualized Experiments. (131), e56395 (2018).
- Packer, J. D., Chang, W. T., Dragoo, J. L. The use of vibrational energy to isolate adipose-derived stem cells. Plastic Reconstructive Surgery-Global Open. 6 (1), e1620 (2018).
- Hanke, C. W., Bernstein, G., Bullock, S. Safety of tumescent liposuction in 15,336 patients. National survey results. Dermatologic Surgery. 21 (5), 459-462 (1995).
- Illouz, Y. G. Complications of liposuction. Clinics in Plastic Surgery. 33 (1), 129-163 (2006).
- Dixit, V. V., Wagh, M. S. Unfavourable outcomes of liposuction and their management. Indian Journal of Plastic Surgery. 46 (2), 377-392 (2013).
- Lehnhardt, M., et al. Major and lethal complications of liposuction: a review of 72 cases in Germany between 1998 and 2002. Plastic and Reconstructive Surgery. 121 (6), 396e-403e (2008).
- Iyer, S. S., Rojas, M. Anti-inflammatory effects of mesenchymal stem cells: novel concept for future therapies. Expert Opinion on Biological Therapy. 8 (5), 569-581 (2008).
- Zhang, J., Middleton, K. K., Fu, F. H., Im, H. J., Wang, J. H. HGF mediates the anti-inflammatory effects of PRP on injured tendons. PLoS One. 8 (6), e67303 (2013).
- Li, N. Y., Yuan, R. T., Chen, T., Chen, L. Q., Jin, X. M. Effect of platelet-rich plasma and latissimus dorsi muscle flap on osteogenesis and vascularization of tissue-engineered bone in dogs. Journal of Oral and Maxillofacial Surgery. 67 (9), 1850-1858 (2009).
- Parsons, P., et al. The biological effect of platelet rich-plasma on the fracture healing process. The Journal of bone and joint surgery. British volume. 91-B, 293 (2009).
- Wu, W., Chen, F., Liu, Y., Ma, Q., Mao, T. Autologous injectable tissue-engineered cartilage by using platelet-rich plasma: experimental study in a rabbit model. Journal of Oral and Maxillofacial Surgery. 65 (10), 1951-1957 (2007).
- Cooper, T. W., Eisen, A. Z., Stricklin, G. P., Welgus, H. G. Platelet-derived collagenase inhibitor: characterization and subcellular localization. Proceedings of the National Academy of Sciences of the United States of America. 82 (9), 2779-2783 (1985).
- Uzuki, M., Sawai, T. A. A comparison of the affinity of sodium hyaluronate of various molecular weights for degenerated cartilage: a histochemical study using hyaluronic acid binding protein. International Congress Series. 1223, 279-284 (2001).
- Pagano, C., et al. Molecular and morphometric description of adipose tissue during weight changes: a quantitative tool for assessment of tissue texture. International Journal of Molecular Medicine. 14 (5), 897-902 (2004).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados