Method Article
Análise espacial bidimensional automatizada de sondas FRET de molécula única móvel
Neste Artigo
Resumo
Este artigo apresenta um método para análise espiostemporal de sondas móveis, de uma molécula, baseadas em Förster, utilizando microscopia de fluorescência widefield. O kit de ferramentas de software recém-desenvolvido permite a determinação de traços de tempo smFRET de sondas móveis, incluindo a eficiência correta do FRET e as posições moleculares, em função do tempo.
Resumo
Transferência de energia de ressonância Förster de uma molécula única (smFRET) é uma técnica versátil que relata distâncias no subnômetro até a faixa de nanômetros. Tem sido usado em uma ampla gama de experimentos biológicos biofísicos e moleculares, incluindo a medição de forças moleculares, caracterização da dinâmica conformacional das biomoléculas, observação da colocalização intracelular de proteínas e determinação dos tempos de interação receptor-ligante. Em uma configuração de microscopia de campo largo, os experimentos são tipicamente realizados usando sondas imobilizadas pela superfície. Aqui, é apresentado um método que combina rastreamento de molécula única com experimentos de smFRET de excitação alternada (ALEX), permitindo a aquisição de traços de tempo smFRET de sondas superficiais, mas móveis em membranas plasmáticas ou bicamadas lipídicas suportadas por vidro. Para a análise dos dados registrados, foi desenvolvida uma coleta automatizada de software de código aberto apoiando (i) a localização de sinais fluorescentes, (ii) rastreamento de partículas únicas, (iii) determinação de quantidades relacionadas ao FRET, incluindo fatores de correção, (iv) verificação rigorosa de traços smFRET e (v) apresentação intuitiva dos resultados. Os dados gerados podem ser convenientemente usados como entrada para posterior exploração via software especializado, por exemplo, para a avaliação do comportamento difuso das sondas ou a investigação de transições de FRET.
Introdução
A transferência de energia de ressonância de Förster (FRET) tem sido um grande impulsionador em pesquisas biológicas e biofísicas moleculares, pois permite a investigação de processos em resolução de subnômetros. Como a eficiência da transferência de energia entre fluoroforos doadores e aceitadores depende fortemente da distância entre corantes no subnômetro para o nanômetro, tem sido efetivamente usada como uma régua espectrística para explorar a conformação estática e dinâmica das biomoléculas1,2,3,4. Além disso, o fenômeno FRET tem sido amplamente utilizado para estudos de colocalização de proteínas associadas à membrana e intracelulares em um nível a granel5,6. Nas últimas duas décadas, o método foi adaptado para monitoramento de eventos smFRET7, o que ajudou a aumentar substancialmente a resolução temporal e espacial e resolveu até subpopulações raras em amostras heterogêneas. Equipados com essas técnicas, foram adquiridos insights únicos na dinâmica das máquinas moleculares, como a taxa de processamento de transcrição da polimerase RNA II8, a velocidade de replicação das polimerases de DNA 9,10, a taxa de translocação nucleossomo11, a taxa de emenda de transcrição e a taxa de paralisação dos conjuntos 12, a atividade das subpopulações ribossômicas13, e a velocidade de caminhada de motores de kinesin1414 , para citar alguns. As durações de interação receptor-ligante15 e forças moleculares16 foram quantificadas.
Estudos smFRET baseados em intensidade normalmente dependem de emissões sensibilizadas para medir a eficiência do FRET: um divisor de feixe no caminho de emissão separa espacialmente a luz originária de fluoroforos doadores e aceitadores após a excitação do doador, permitindo a quantificação das intensidades individuais de fluorescência. A eficiência pode ser posteriormente calculada como a fração de fótons emitidos pelo aceitador em relação à contagem total de fótons17. Além disso, a excitação aceitadora após a excitação do doador (ALEX) permite a medição da estequiometria dos eventos FRET, auxiliando na discriminação entre sinais verdadeiros de baixo FRET de sinais decorrentes, por exemplo, de sondas com um fluoroforeiro aceitador fotobleachado18.
Experimentos fret de molécula única são comumente realizados de duas maneiras. Primeiro, uma pequena região no volume da amostra é iluminada usando um microscópio confocal. Moléculas de sonda única em solução estão animadas quando se difundem dentro do volume focal. Com esta técnica, podem ser utilizados detectores rápidos de contagem de fótons, permitindo a resolução de tempo sub-microsegundo. Em segundo lugar, as sondas são especificamente imobilizadas em superfícies e monitoradas via microscopia de campo largo, muitas vezes usando a configuração de reflexão interna total (TIR) para minimizar a fluorescência de fundo. A imobilização da sonda permite tempos de gravação muito mais longos do que usar a primeira abordagem. Além disso, o campo de visão maior permite o monitoramento de múltiplas sondas em paralelo. A necessidade de uma câmera torna este método lento em comparação com o descrito acima. A resolução de tempo é limitada ao milissegundo para o segundo intervalo.
Se forem necessários traços de longo tempo, por exemplo, para estudar processos dinâmicos em uma escala de milissegundo a segunda vez, o primeiro método não é aplicável, pois as explosões de fluorescência são tipicamente muito curtas. A segunda abordagem falha sempre que a imobilização não é viável, por exemplo, em experimentos de células vivas com sondas difundindo dentro da membrana celular. Além disso, observou-se que os sistemas de modelos biológicos podem variar drasticamente sua resposta dependendo da mobilidade da superfície contatada16.
Embora os experimentos combinados de rastreamento de smFRET e single-particle que gravam testes FRET móveis tenham sido realizados no passado19, não há software disponível publicamente para a avaliação dos dados. Isso levou ao desenvolvimento de uma nova plataforma de análise, que permite a determinação de múltiplas propriedades de sondas fluorescentes móveis, incluindo eficiência smFRET e estequiometria, posições com precisão de subcontomínuo e intensidades de fluorescência como funções do tempo. Métodos para filtrar os traços resultantes examinando o comportamento de branqueamento passo a passo, distâncias mais próximas do vizinho, intensidades de emissão e outros traços foram estabelecidos para escolher exclusivamente moléculas de sonda única sintetizadas e funcionais corretamente. O software também suporta técnicas experimentais e analíticas recentemente acordadas em um estudo multilaboratório para produzir dados smFRET confiáveis e quantitativos17. Em particular, a implementação adere aos procedimentos validados para o cálculo da eficiência do FRET e da estequiometria. As intensidades de fluorescência após a excitação do doador no canal de emissão de doadores IDD e no canal de emissão aceitador IDA são utilizadas para o cálculo da aparente eficiência do FRET Eapp usando eq (1).
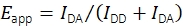 (1)
(1)
Com a ajuda da intensidade da fluorescência no canal de emissão aceitador após a excitação aceitante IAA, a estoquiometria aparente é calculada usando Eq (2).
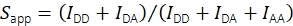 (2)
(2)
A eficiência FRET E e o estequiometria S podem ser derivados de Eapp e Sapp considerando quatro fatores de correção.
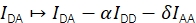
α descreve o vazamento da fluorescência do doador no canal de emissão do aceitador e pode ser determinado usando uma amostra contendo apenas fluoroforos doadores ou analisando partes de trajetórias onde o aceitador foi branqueado. δ corrige para a excitação direta do aceitador pela fonte de luz de excitação do doador e pode ser medido usando uma amostra com fluoroforos aceitádores ou analisando partes de trajetórias onde o doador foi branqueado.
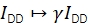 .
.
γ dimensiona o IDD para corrigir a eficiência de detecção divergente nos canais de emissão de doadores e aceitadores e diferentes eficiências quânticas dos fluoroforos. O fator pode ser computado analisando o aumento da intensidade do doador após o branqueamento aceitador em trajetórias com alta eficiência de FRET20 ou estudando uma amostra com múltiplos estados fret discretos.
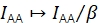
β dimensiona a IAA para corrigir a eficiência díspare da excitação de doadores e aceitadores. Se γ foi determinada através da análise de branqueamento aceitante, β poderia ser calculada a partir de uma amostra da relação doador-aceitador conhecido21. Caso contrário, a amostra de FRET multi-estado também rende β.
Juntas, as correções permitem o cálculo da eficiência fret corrigida utilizando Eq (3).
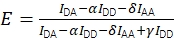 (3)
(3)
e a estequiometria corrigida utilizando Eq (4).
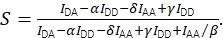 (4)
(4)
Idealmente, a estequiometria corrigida para uma relação doador-aceitador de 1:1 dá S = 0,5. Na prática, uma redução da relação sinal-ruído produz uma disseminação dos valores medidos de S, dificultando a discriminação de sinais somente de doadores (S = 1) e sinais somente de aceitadores (S = 0). Os traços de tempo resultantes podem ser usados como entrada para uma análise mais detalhada das trajetórias de uma molécula única para obter informações como perfis de força espesso16, mobilidade dos eventos de molécula única22 ou cinética de transição entre diferentes estados1.
O protocolo a seguir descreve parâmetros experimentais e procedimentos para experimentos de rastreamento smFRET, bem como o princípio de trabalho por trás da análise de dados usando o recém-desenvolvido conjunto de software. Para a aquisição de dados experimentais, recomenda-se a utilização de uma configuração de microscopia atendendo aos seguintes requisitos: i) capacidade de detecção da emissão de moléculas de corante único; ii) iluminação de campo largo: em particular para experimentos com células vivas, recomenda-se a configuração de reflexão interna total (TIR23,24,25); iii) separação espacial da luz de emissão de acordo com o comprimento de onda de tal forma que a fluorescência doador e aceitadora seja projetada em diferentes regiões do mesmo chip de câmera25 ou câmeras diferentes; iv) modulação de fontes de luz para excitação doador e aceitadora com precisão de milissegundo, por exemplo, utilizando lasers diretamente moduladores ou modulação através de moduladores acousto-ópticos. Isso permite a iluminação e stroboscópica para minimizar o fotobleaching de fluoroforos, bem como a excitação alternada para determinar estequiometrias; v) saída de um arquivo por sequência de imagem gravada em um formato que pode ser lido pelo pacote PIMS Python26. Em particular, os arquivos TIFF de várias páginas são suportados.
Protocolo
1. Pré-requisitos de software
- Instale a distribuição Python miniconda27 (versão Píton mínima necessária: 3.7).
- Abra um prompt Anaconda no menu Iniciar do Windows, ou abra um terminal e execute conda ativar se usar Linux ou macOS.
- Habilite o repositório de pacote conda-forge mantido pela comunidade28 executando os seguintes comandos:
conda config --adicionar canais conda-forge
conda config --conjunto channel_priority rigoroso
conda update --all - Instale os pacotes Python necessários executando:
conda instalar opencv trackpy lmfit ipympl scikit-learn pyqt sdt-python jupyterlab - Familiarize-se com o JupyterLab, a interface de usuário do software de análise (consulte a documentação do software29).
- Instale o sistema de controle da versão git , que será usado mais tarde para baixar e atualizar o software de análise. Se estiver usando o Linux, use o software de gerenciamento de pacotes da distribuição para baixar e atualizar. Caso contrário, execute:
conda instalar git - Instale opcionalmente o pacote Sidecar Python para exibir conjuntos de dados após filtrar etapas durante a análise:
conda instalar sidecar
2. Medição de amostras
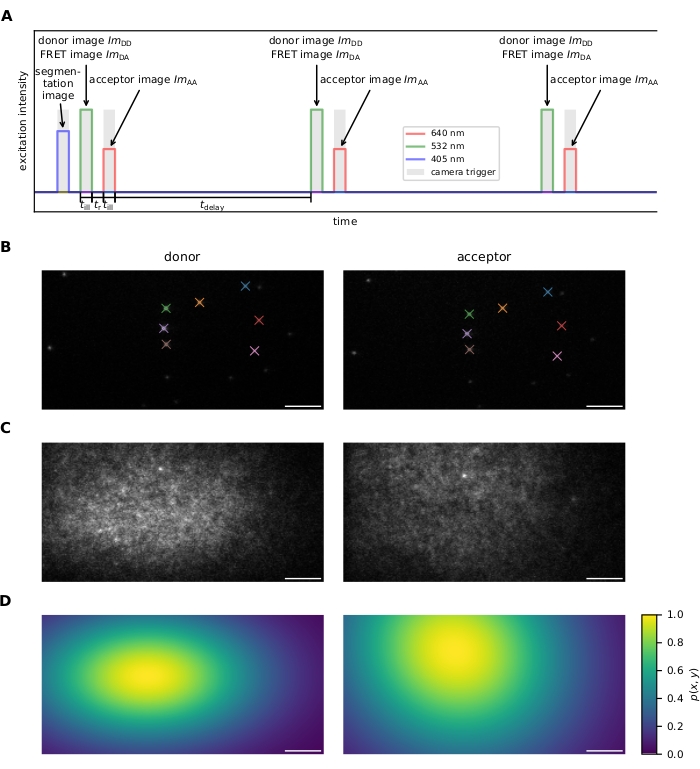
Figura 1: Aquisição de Imagens. (A) Sequência de excitação. Depois de gravar uma imagem opcional de uma célula carregada de corante usando o laser de 405 nm, doador e aceitador são animados alternadamente e repetidamente para o till tempo de iluminação usando lasers de 532 nm e 640 nm, respectivamente. O tempo tr entre doador e excitação aceitante deve ser longo o suficiente para permitir a leitura de imagem pela câmera. O tempo de atraso pode ser usado para ajustar a taxa de quadros de aquisição e, portanto, o período de tempo de observação antes do fotobleaching. Este painel é modificado a partir de 16. (B) Os marcadores fiduciais são utilizados para o cálculo das transformações coordenadas entre os dois canais de emissão. Fiduciais correspondentes são indicados por cor. Várias imagens deslocadas devem ser gravadas para garantir que todo o campo de visão seja coberto. (C) Os perfis a laser para correção de campo plano são registrados usando uma amostra densamente rotulada. O perfil do aceitador é registrado e fotobleached, seguido da aquisição do perfil do doador. Várias imagens devem ser tiradas em diferentes regiões amostrais, mediadas e suavizadas para mitigar a influência das imperfeições da amostra (por exemplo, o ponto brilhante no centro-topo da imagem). (D) Mapa de correção flatfield p(x,y) calculado a partir de 20 perfis de laser registrados como descrito em C. Abreviaturas: FRET = Transferência de energia de ressonância förster; ImDD = imagem de emissão de doadores após excitação de doadores; ImDA = imagem de emissão de aceitação após excitação de doadores; ImAA = imagem de emissão de aceitação após excitação de doadores. Barras de escala = 5 μm. Clique aqui para ver uma versão maior desta figura.
- Ao usar uma câmera EMCCD (com um dispositivo acoplado a cargas multiplicadora de elétrons), permita que o ganho EM observe sinais de molécula única em altas razões de sinal para ruído (consulte as instruções do fabricante).
- Sequência de excitação (ver Figura 1A para mais detalhes).
- Registro opcional de uma imagem para segmentação para restringir a análise de dados a determinadas regiões no campo de visão. Por exemplo, excitar as células fura-2 carregadas usando um laser de 405 nm e capturar sua emissão em torno de 510 nm para avaliar apenas sondas localizadas em interfaces entre células e bicamadas lipídicas suportadas (SLBs). Consequentemente, espere o tempo tr para permitir a leitura da câmera.
NOTA: Nas câmeras EMCCD, o TR depende do número de linhas na região de interesse escolhida (ROI). Portanto, escolher um PEQUENO ROI pode ser vantajoso porque reduz o atraso entre os quadros e o tamanho dos dados registrados. Além disso, a habilitação do modo de transferência de quadros permite uma redução adicional do tr. - Alternadamente excitar doadores e fluoroforos aceitos repetidamente.
- Excite o doador para um till de tempo de iluminação (5-10 ms é tipicamente curto o suficiente para evitar o desfoque de movimento) ao mesmo tempo em que aciona a câmera.
- Espere o tempo tr para permitir a leitura da câmera.
- Excite o aceitador enquanto aciona a câmera.
- Espere por um tempo tdelay.
NOTA: Este deve ser mais longo do que tr para habilitar a leitura pela câmera, mas pode ser escolhido arbitrariamente. Deve equilibrar os requisitos para resolução de tempo e comprimento do traço. - Repetição de passos 2.2.2.1-2.2.2.4. Escolha o número de repetições para ser grande o suficiente para garantir o fotobleaching de pelo menos um fluoróforo por sonda dentro do campo de visão, o que permite a análise de fotobleaching stepwise para discriminação de sinais de molécula única a partir de agregados.
NOTA: A escolha adequada das intensidades do laser de estapimento e excitação geralmente requer alguma experimentação: Quanto maior o tempo de iluminação e maiores as intensidades do laser, melhor é a relação sinal-ruído nas imagens resultantes, mas quanto menor são os traços de tempo resultantes.
- Registro opcional de uma imagem para segmentação para restringir a análise de dados a determinadas regiões no campo de visão. Por exemplo, excitar as células fura-2 carregadas usando um laser de 405 nm e capturar sua emissão em torno de 510 nm para avaliar apenas sondas localizadas em interfaces entre células e bicamadas lipídicas suportadas (SLBs). Consequentemente, espere o tempo tr para permitir a leitura da câmera.
- Grave um número suficiente de filmes para cada amostra.
3. Medidas adicionais para a determinação de fatores de correção
- Registo uma série de marcadores fiduciais colocados aleatoriamente visíveis em ambos os canais de emissão para registro de imagem (ou seja, encontrar a transformação que mapeia coordenadas do canal de emissão de doadores para o canal de emissão de aceitadores e vice-versa). Veja a Figura 1B.
NOTA: O registro de imagem é realizado pelo software; ver passo 6.1.4. - Meça o perfil de intensidade tanto para fontes de luz de excitação do doador quanto do aceitador para correção de campo plano (ou seja, corrigindo para excitação inhomogênea em todo o campo de visão). Para isso, prepare uma amostra com alta densidade de sondas FRET e primeiro adquira uma imagem após a excitação aceitadora, seguida de fotobleaching do aceitador e posterior gravação de uma imagem após a excitação do doador. Para maior estabilidade, repita várias vezes em diferentes regiões amostrais. Veja a Figura 1C,D. Alternativamente, registo uma amostra decorada apenas com a molécula do doador e uma segunda amostra decorada apenas com fluoroforos aceitas.
NOTA: A correção de flatfield é realizada pelo software de análise; ver passo 8.1.2. - Registo uma amostra de molécula única (como na seção 2) de uma sonda sem um fluoróforo aceitor para determinar o vazamento de emissões de doadores no canal de aceitação.
NOTA: O vazamento de doadores também pode ser computado a partir dos traços de tempo das sondas reais após o branqueamento do aceitador. Se um número suficiente de tais eventos for registrado, nenhuma medida adicional é necessária. Ambas as opções são suportadas pelo software de análise; consulte Informações Suplementares, seção 3.15. - Adquira gravações de uma sonda sem fluoróforo doador para quantificação da excitação aceitadora direta pela fonte de luz de excitação do doador.
NOTA: A excitação direta do aceitador também pode ser derivada dos traços de tempo das sondas reais após o branqueamento do doador. Se um número suficiente de tais eventos for registrado, nenhuma medida adicional é necessária. Ambas as opções são suportadas pelo software de análise; consulte Informações Suplementares, seção 3.15. - Registo uma amostra de molécula única com duas eficiências distintas de FRET para corrigir as diferentes eficiências de detecção dos canais de emissão do doador e aceitador e diferentes rendimentos quânticos dos corantes.
NOTA: Tais amostras podem ser, por exemplo, junções Holliday1, que flutuam entre duas conformações, ou barras de DNA que têm pares DE FRET ligados a distâncias diferentes e bem definidas. Se os testes apresentarem eficiências fret altas e suficientemente constantes, a correção também pode ser calculada a partir de eventos de branqueamento aceitadores dos traços de tempo das sondas, nesse caso não são necessárias medidas adicionais. Ambas as opções são suportadas pelo software de análise; consulte Informações Suplementares, seção 3.15.
4. Algoritmos de localização de moléculas únicas
NOTA: Várias etapas de análise requerem localização de molécula única. Escolha entre um algoritmo de ajuste gaussiano30 e computação de centro de massa31, dependendo da densidade do sinal, fundo e relação sinal-ruído.
- Para executar o encaixe gaussiano, escolha o algoritmo 3D-DAOSTORM30 através das respectivas interfaces de usuário.
NOTA: O 3D-DAOSTORM foi projetado para distinguir sinais uniformemente com funções de propagação de pontos sobrepostas. Embora isso seja geralmente uma vantagem, ele vem com uma ressalva: sinais únicos e brilhantes são ocasionalmente identificados como dois adjacentes, o que pode confundir o algoritmo de rastreamento e resultar na detecção de duas trajetórias curtas em vez de uma única longa.
Defina os seguintes parâmetros (para detalhes, consulte a documentação da biblioteca sdt-python32, que fornece a implementação do algoritmo).- raio: Defina o valor inicial σ da função de ajuste gaussiano em pixels, dependendo do tamanho efetivo do pixel.
-
limiar: Defina uma amplitude mínima (ou seja, o valor mais brilhante do pixel, corrigido para o fundo local estimado) para que um máximo de intensidade local seja adequado.
NOTA: O limiar é, sem dúvida, o parâmetro mais importante. Se definido muito baixo, o ruído pode ser considerado um sinal de fluorescência, e sinais brilhantes podem ser equipados com dois gaussianos. Se definidos muito alto, sinais escuros não são adequados. -
modelo: Ajuste para 2d para caber gaussianos circulares.
NOTA: Os outros modelos não são aplicáveis aos dados smFRET. -
encontrar filtro: Aplique um filtro antes de encontrar maxima local para reduzir o ruído, o que é útil em situações de baixa relação sinal-ruído. Esta pode ser i) identidade: sem filtro; ii) Crocker-Grier: filtro de bandpass do algoritmo Crocker-Grier31,33; ou iii) Gaussian: um borrão gaussiano com σ definido pelo parâmetro sigma.
NOTA: Para Crocker-Grier, o parâmetro de tamanho do feito. deve ser aproximadamente o raio de uma função de spread de ponto em pixels.
NOTA: A montagem é realizada utilizando dados brutos não filtrados. -
min. distância: Coloque dois sinais prospectivos separados por menos de min. pixels de distância por um único gaussiano.
NOTA: Isso pode ajudar no cenário acima mencionado onde um sinal brilhante é detectado erroneamente como dois sinais adjacentes. - Faixa de tamanho: Selecione σ mínima e máxima dos ajustes para remover detecções de sinais espúrios devido ao ruído.
- Escolha o algoritmo Crocker-Grier através das respectivas interfaces de usuário para executar a computação central de massa (um algoritmo refinado31 baseado na ideia de Crocker e Grier33).
NOTA: Este algoritmo é muito robusto mesmo em cenários baixos de sinal para ruído e em lidar com sinais com uma gama de intensidades, mas não pode encaixar moléculas com funções de propagação de ponto sobrepostas precisamente.- raio: Defina o raio (em pixels) de um disco grande o suficiente para conter toda a função de propagação de pontos.
-
thresh.: Defina a amplitude mínima (pixel mais brilhante acima do plano de fundo estimado) para que um máximo de intensidade local seja analisado.
NOTA: Se estiver muito baixo, o ruído pode ser considerado um sinal de fluorescência. Se definidos muito alto, sinais escuros não são adequados. -
massa thresh.: Defina a intensidade total mínima (soma dos valores de pixel corrigidos por fundo) de um sinal a ser analisado.
NOTA: As mesmas considerações acima se aplicam.
5. Inicialização do software
- Baixe scripts de análise. Em um prompt Anaconda , navegue até uma pasta para salvar a análise (usando o comando cd ) e execute
git clone https://github.com/schuetzgroup/fret-analysis.git pasta alvo- Substitua a pasta de destino por um nome descritivo, como 2021-06-14_Force-FRET-experiment.
NOTA: O software de análise acabará nesta pasta; certifique-se de que esta pasta não exista de antemão. Recomenda-se baixar uma cópia dos scripts de análise para cada experimento. Dessa forma, é possível revisitar a análise mais tarde, recordar os parâmetros utilizados e fazer alterações.
- Substitua a pasta de destino por um nome descritivo, como 2021-06-14_Force-FRET-experiment.
- Copie os cadernos do Jupyter (01). Tracking.ipynb, 02. Análise.ipynb, 03. Plots.ipynb) na pasta recém-criada (a partir de agora referida como pasta raiz). Se esta for a primeira vez que usar o software, obtenha-os a partir dos notebooks subpastos da pasta raiz.
NOTA: Se já foram analisados conjuntos de dados semelhantes, copiar os notebooks de um experimento anterior pode ser uma opção conveniente, pois os parâmetros podem ter mudado apenas ligeiramente. - Inicie o servidor JupyterLab executando o seguinte comando no prompt da Anaconda para abrir uma janela do navegador da Web exibindo o JupyterLab.
laboratório jupyter
NOTA: O navegador é apenas a interface, enquanto o processo em execução no prompt Anaconda está fazendo o trabalho real. Como consequência, fechar a janela do navegador tem apenas um efeito mínimo; a sessão pode ser restaurada acessando http://localhost:8888. No entanto, interromper o processo jupyterLab no prompt ou fechar o prompt encerrará a análise, levando à perda de trabalho não salvo. - Na janela do navegador JupyterLab, use o painel esquerdo para navegar até a pasta raiz. Clique duas vezes no 01. Tracking.ipynb para iniciar o primeiro notebook. Após o lançamento, procure uma nova guia para aparecer, que exibe caixas, as chamadas células, do código Python.
NOTA: Todos os notebooks Jupyter apresentam comentários descrevendo a funcionalidade de cada célula de código. Além disso, a documentação para cada chamada de método pode ser exibida colocando o cursor de texto imediatamente antes da abertura ( e pressione Shift+Tab. - Consulte a Figura 2 para obter uma visão geral do processo de análise de dados.
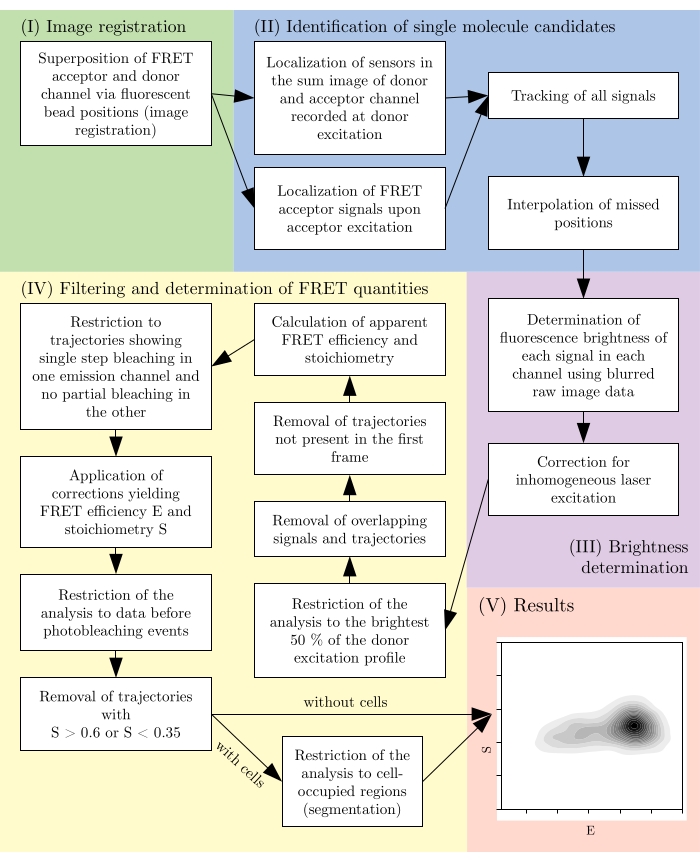
Figura 2: Visão geral de um oleoduto de análise típico. Observe que as etapas de filtragem estão sujeitas à adaptação de acordo com o design experimental. Este número é modificado a partir de 16. Abreviação: FRET = Transferência de energia de ressonância förster. Clique aqui para ver uma versão maior desta figura.
NOTA: Dados de amostra para testar o software podem ser baixados a partir de https://github.com/schuetzgroup/fret-analysis/releases/tag/example_files
6. Análise de localização, rastreamento e intensidade de fluorescência de moléculas únicas (01). Tracking.ipynb).
- Use o 01. Rastreamento.ipynb Caderno jupyter para a análise confiável dos valores de intensidade de fluorescência de sinais de molécula única, que é adaptado para a quantificação precisa, particularmente de sinais fracos frequentemente ocorrendo em medições de FRET (por exemplo, devido a baixos sinais de doadores em eventos de alto FRET e vice-versa).
NOTA: Para isso, a integração direta das intensidades de pixels nos dados brutos com correção para o fundo local é implementada. Para capturas de tela de cada etapa de análise e descrição dos parâmetros de chamada de função, consulte o Informações suplementares.- Especifique a sequência de iluminação para permitir a seleção de quadros de excitação de doadores e aceitadores, bem como quadros para segmentação de imagens a partir de sequências de imagem gravadas.
NOTA: Como o software permite o processamento de dados registrados com protocolos de iluminação arbitrária, é necessário indicar qual quadro em uma sequência de imagem foi adquirido enquanto excita que tipo de fluorophore; consulte Informações Suplementares, seção 1.2, passo 3. Os números de quadros da sequência de imagem original são preservados. - Descreva e carregue conjuntos de dados. Analise vários conjuntos de dados ao mesmo tempo, desde que sejam gravados usando as mesmas configurações de iluminação. Atribua um identificador e um padrão que corresponda aos respectivos nomes de arquivos de sequência de imagem a cada conjunto de dados. Além disso, defina conjuntos de dados específicos para fins especiais, como registros de marcadores fiduciários para registro de imagens, perfis de luz de excitação para correção de flatfield e, opcionalmente, amostras somente de doadores e aceitadores para determinar fatores de correção.
- Selecione canais de emissão em imagens brutas se ambos os canais forem gravados usando uma única câmera. Para isso, use o widget gráfico apropriado para selecionar as regiões apropriadas para emissão de doadores e aceitadores.
- Localize marcadores fiduciais em ambos os canais de emissão e realize o registro de imagens. Use a interface de usuário fornecida para encontrar os parâmetros apropriados para o algoritmo de localização tanto para os canais de emissão do doador quanto do aceitador. Consulte a seção 4 para obter informações sobre algoritmos de localização suportados.
NOTA: Marcadores fiduciais distribuídos aleatoriamente podem ser identificados nos canais de emissão pela distribuição espacial de seus vizinhos mais próximos (Figura 1B). Uma implementação personalizada do algoritmo proposto para microscopia de iluminação de plano seletivo34 na biblioteca sdt-python corresponde automaticamente à posição de cada marcador no canal de emissão de doadores com a posição no canal de emissão de aceitadores. Uma transformação T mapeando as coordenadas do canal de emissão de doadores para as coordenadas do canal de emissão do aceitador é encontrada através de um ajuste linear de menos quadrados de uma transformação afim para as posições dos marcadores35. RansAC é usado para responder por outliers, como posições erroneamente combinadas da etapa anterior. - Localize as sondas FRET independentemente sobre a excitação de doadores e aceitadores em todos os quadros e mescle os resultados em uma tabela que contém o número do quadro original, coordenadas bidimensionais e um identificador referente ao arquivo de imagem de origem.
NOTA: Para isso, o software fornece interfaces de usuário para encontrar opções apropriadas para o algoritmo de localização.- Localize as sondas FRET sobre a excitação dos doadores na soma das imagens obtidas a partir do IMDD de emissão de doadores e da emissão de aceitadores ImDA, que dificilmente dependem da eficiência do FRET. Para obter informações sobre as opções para o algoritmo de localização, consulte a seção 4.
NOTA: Cada imagem de soma é calculada transformando ImDD usando a transformação T obtida anteriormente a partir do registro de imagem e adicionada pixelwise ao ImDA. - Localize as sondas após a excitação aceitadora no canal de emissão aceitador ImAA (consulte a seção 4 para obter detalhes sobre os algoritmos de localização).
- Localize as sondas FRET sobre a excitação dos doadores na soma das imagens obtidas a partir do IMDD de emissão de doadores e da emissão de aceitadores ImDA, que dificilmente dependem da eficiência do FRET. Para obter informações sobre as opções para o algoritmo de localização, consulte a seção 4.
- Realize a medição da intensidade de rastreamento e fluorescência.
- Especifique a sequência de iluminação para permitir a seleção de quadros de excitação de doadores e aceitadores, bem como quadros para segmentação de imagens a partir de sequências de imagem gravadas.
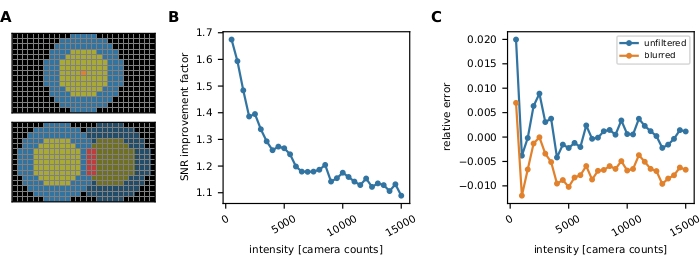
Figura 3: Medição da intensidade de molécula única. (A) Para um fluoróforo localizado no pixel laranja, seu Iuncorr de intensidade não corrigida é determinado por resumir todas as intensidades de pixels dentro de um disco (pixels amarelos e laranjas) grandes o suficiente para cobrir todos os pixels afetados pelo sinal: 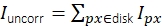 . O fundo local é computado como a média dos pixels em um anel (pixels azuis) ao redor do disco:
. O fundo local é computado como a média dos pixels em um anel (pixels azuis) ao redor do disco: 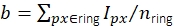 , onde nring é o número de pixels no anel. A intensidade de fluorescência I é o resultado de subtrair o fundo da intensidade não corrigida, I = Iuncorr - b × ndisk, onde ndisk é o número de pixels no disco. O raio do círculo é especificado através do parâmetro feat_radius do método de rastreamento. A largura do anel é dada pelo parâmetro bg_frame. Se a função de propagação de ponto de um sinal se sobrepor ao anel de fundo de outro (painel inferior), os pixels afetados (vermelho) ão excluídos da análise de fundo local. Se as funções de spread de dois pontos se sobreporem, as intensidades de fluorescência não podem ser calculadas de forma confiável e, portanto, descartadas. (B, C) Simulações mostram que a aplicação de um desfoque gaussiano com um desvio padrão de 1 pixel melhora a relação sinal-ruído até um fator de perto de 2 em baixas intensidades de fluorescência (B) e introduz quase nenhum erro (leve subestimação de menos de 1%, (C))16. Além disso, o erro relativo (imeas - Itruth)/Itruth, onde a verdade é o solo e Imeas é o resultado da análise) é constante sobre toda a faixa de intensidade e, portanto, cancela para quantidades racionmétricas como eficiências de FRET e estequiometrias. Todas as parcelas são baseadas em trabalhos publicados anteriormente16. Abreviaturas: SNR = relação sinal-ruído; FRET = Transferência de energia de ressonância förster. Clique aqui para ver uma versão maior desta figura.
, onde nring é o número de pixels no anel. A intensidade de fluorescência I é o resultado de subtrair o fundo da intensidade não corrigida, I = Iuncorr - b × ndisk, onde ndisk é o número de pixels no disco. O raio do círculo é especificado através do parâmetro feat_radius do método de rastreamento. A largura do anel é dada pelo parâmetro bg_frame. Se a função de propagação de ponto de um sinal se sobrepor ao anel de fundo de outro (painel inferior), os pixels afetados (vermelho) ão excluídos da análise de fundo local. Se as funções de spread de dois pontos se sobreporem, as intensidades de fluorescência não podem ser calculadas de forma confiável e, portanto, descartadas. (B, C) Simulações mostram que a aplicação de um desfoque gaussiano com um desvio padrão de 1 pixel melhora a relação sinal-ruído até um fator de perto de 2 em baixas intensidades de fluorescência (B) e introduz quase nenhum erro (leve subestimação de menos de 1%, (C))16. Além disso, o erro relativo (imeas - Itruth)/Itruth, onde a verdade é o solo e Imeas é o resultado da análise) é constante sobre toda a faixa de intensidade e, portanto, cancela para quantidades racionmétricas como eficiências de FRET e estequiometrias. Todas as parcelas são baseadas em trabalhos publicados anteriormente16. Abreviaturas: SNR = relação sinal-ruído; FRET = Transferência de energia de ressonância förster. Clique aqui para ver uma versão maior desta figura.
- Escolha opções apropriadas para o trackpy36algorithm usado para vincular localizações de sonda FRET em trajetórias. Em particular, defina a distância máxima de pesquisa de um quadro para o outro e o número de quadros consecutivos para os quais um sinal pode passar despercebido, o que pode ocorrer devido ao branqueamento ou localizaçãos perdidas.
NOTA: Essas lacunas são preenchidas via interpolação entre as posições anteriores e as seguintes. Estas posições interpoladas são marcadas e usadas apenas mais tarde para leitura de valores de intensidade, mas não para análise de difusão. As faixas são analisadas no sistema de coordenadas do canal de emissão de aceitação. Para análise da intensidade da fluorescência (etapa 6.1.6.2), as faixas são adicionalmente transformadas no sistema de coordenadas do canal de emissão de doadores utilizando a transformação inversa T-1 obtida via registro de imagem (ver etapa 6.1.4). - Selecione opções para o algoritmo de cálculo de intensidade de fluorescência (consulte Figura 3A para obter detalhes). Especificar i) o raio de um disco que, quando centrado na posição de um sinal, contém todos os pixels afetados por esse sinal e ii) a largura de um anel em torno de cada disco usado para determinar o fundo local.
NOTA: Para reduzir o ruído nas medições de intensidade obtidas, um desfoque gaussiano com um desvio padrão de 1 pixel é aplicado às imagens (Figura 3B,C).
- Use a funcionalidade do software de análise para processar dados de imagem auxiliares de sequências de imagens.
- Extrair imagens adicionais gravadas para facilitar a segmentação (ver etapa 2.2.1, marcada por s na sequência de excitação (ver Informações Suplementares, seção 1.2, etapa 3).
- Determine perfis de luz de excitação de doadores e aceitadores em todo o campo de visão a partir de imagens gravadas em uma amostra densamente rotulada (ver passo 3.2).
NOTA: A média pixel a pixel é calculada a partir das imagens para calcular os perfis de luz. A linha de base da câmera está subtraída. As imagens são borradas usando um filtro gaussiano para reduzir os efeitos devido a impurezas amostrais. Finalmente, as imagens resultantes são divididas pixelwise pelo seu valor máximo para obter as coordenadas de mapeamento do perfil p(x,y) no intervalo [0,1].
7. Visualização de trajetórias de FRET (opcional)
- Use o aplicativo inspetor para exibir faixas de molécula única em dados de imagem bruta e as intensidades de fluorescência correspondentes e eficiências de FRET aparentes e estequiometrias.
NOTA: Esta é uma ferramenta valiosa para avaliar a validade dos parâmetros escolhidos e aceitar manualmente ou rejeitar traços de tempo individuais. Consulte Informações Suplementares para obter uma captura de tela e informações detalhadas de uso.
8. Análise e filtragem de dados de molécula única (02. Análise.ipynb)
- Use o 02. Análise.ipynb Jupyter caderno para análise e filtragem dos dados de molécula única obtidos através do 01. Rastreamento.ipynb caderno. Veja os passos abaixo para um pipeline de análise típico.
NOTA: Diferentes questões científicas e projetos experimentais podem exigir ajustes das configurações. O uso de notebooks Jupyter permite fácil adaptação, omitindo, reorganizando e alterando etapas de análise. Para capturas de tela de cada etapa de análise e descrição dos parâmetros de chamada de função, consulte Informações suplementares.- Executar etapas iniciais de filtragem.
- Descartar sinais com sobreposição de pontos funciona, pois é difícil determinar suas intensidades de fluorescência de forma confiável.
- No caso da iluminação inhomogênea, aceite apenas sinais localizados em regiões bem iluminadas dentro do campo de visão para garantir uma boa relação sinal-ruído.
- Se estudar o FRET intramolecular, restrinja a análise às trajetórias presentes desde o início da sequência de imagem para garantir que todas as etapas de branqueamento sejam registradas e possam ser devidamente avaliadas posteriormente durante a análise de fotobleaching passo a passo.
NOTA: Ao realizar experimentos com sondas FRET intermoleculares, em que fluoroforos doadores e aceitadores não fazem parte de um complexo pré-formado, pode não ser viável restringir a análise a trajetórias inicialmente presentes.
- Execute a correção de flatfield, que utiliza os perfis de fonte de luz de excitação obtidos na etapa 6.1.7.2 para reverter as variações de intensidade de fluorescência dependentes da posição causadas pela iluminação inhomogênea.
NOTA: A intensidade de fluorescência I(x,y) de uma sonda na posição (x,y) é corrigida via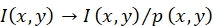 ; ver Figura 1C,D.
; ver Figura 1C,D. - Calcule o aparente Eapp de eficiência de FRET (ou seja, a fração de energia transmitida do fluorophore doador para o fluorophore aceitor) e o aparente estoquiometria Sapp (ou seja, o número de fluoroforos doadores divididos pelo número total de fluoroforos dentro de um ponto limitado por difração).
NOTA: Ao traçar E vs. S para cada ponto de dados, é possível distinguir alterações nas eficiências de FRET medidos devido à mudança na distância aceitadora de doadores das alterações devido a alterações na estequiometria18. Isso permite a diferenciação entre E = 0 devido à separação de corante de E = 0 devido à ausência de um aceitador ativo. As parcelas E-S são utilizadas ao longo da análise como ferramenta de avaliação da qualidade; ver a Figura 4 como um exemplo. - Realize a análise stepwise de fotobleaching para a discriminação entre sondas uni moleculares e agregados. Escolha aceitar uma das seguintes opções.
NOTA: Para este fim, o software de análise aplica uma implementação personalizada32 do algoritmo de detecção de ponto de mudança PELT37 separadamente à intensidade de fluorescência após excitação de doadores (IDD + IDA) e excitação aceitadora (IAA).- Escolha a opção 1, em que o fluorforeiro aceitante descolore em um único passo, enquanto o doador não apresenta branqueamento parcial (ou seja, não há nenhum passo de branqueamento para intensidade não-zero).
NOTA: Esta opção rejeita ainda mais as trajetórias em que o doador branqueia antes do aceitador em uma única etapa. A opção 1 é a escolha preferida em caso de altas taxas de fotobleaching aceitante. - Escolha a opção 2, em que o doador branqueia em uma única etapa enquanto não houver clareamento parcial do aceitador.
NOTA: Esta opção rejeita ainda mais as trajetórias em que o doador branqueia após o aceitador em uma única etapa. A opção 2 é a escolha preferida em caso de altas taxas de fotobleaching de doadores. - Escolha a opção 3, em que tanto o fluorohore branquea em um único passo, enquanto o outro não alveja parcialmente.
NOTA: A opção 3 dá maior flexibilidade do que as opções 1 e 2 e seria a preferência sugerida para análise de dados. - Escolha a opção 4, em que os fluoroforos doadores e aceitantes que apresentem fotobleaching de passo único ou nada de fotobleaching.
NOTA: A opção 4 é preferida em caso de baixas taxas de fotobleaching.
- Escolha a opção 1, em que o fluorforeiro aceitante descolore em um único passo, enquanto o doador não apresenta branqueamento parcial (ou seja, não há nenhum passo de branqueamento para intensidade não-zero).
- Calcule os fatores de correção para o vazamento de emissões de doadores no canal de aceitação α, δ de excitação aceitadora direta, eficiências de detecção γ e eficiência de excitação β 17.
- Use os fatores de correção para calcular a eficiência DO FRET E a partir da eficiência aparente Eapp e da estequiometria S do aparente stoichiometria Sapp.
- Execute mais etapas de filtragem. Selecione apenas pontos de dados antes do primeiro evento de branqueamento em cada trajetória. Além disso, aceite apenas trajetórias com pelo menos 75% dos pontos de dados satisfazendo 0,35 < S < 0,6 para restringir a análise a sondas de molécula única (os números são ajustáveis).
NOTA: Os limites superiores e inferiores devem ser escolhidos de acordo com a disseminação da população de interesse versus as populações a serem excluídas da análise (por exemplo, apenas para doadores e somente aceitadores). Com base na experiência, 0,35 < S < 0,6 se mostrou uma boa escolha para muitas situações experimentais. - Realize a segmentação de imagens através de métodos de limiar global ou adaptável35 nas imagens auxiliares apropriadas (ver etapas 2.2.1 e 6.1.7) para restringir a análise a regiões distintas dentro do campo de visão.
NOTA: Isso permite, por exemplo, avaliação exclusiva de sondas localizadas em uma interface cell-SLB ou em uma estrutura padronizada.
- Executar etapas iniciais de filtragem.
9. Plotagem de resultados e análises posteriores (03. Plot.ipynb)
NOTA: Consulte informações suplementares para capturas de tela do notebook Jupyter e descrição dos parâmetros de chamada de função.
- Crie gráficos E-S para verificar se sinais de estequiometria incorreta foram corretamente identificados e removidos.
- Plote histogramas de eficiências fret para fornecer uma visão geral bem estabelecida das distribuições de eficiência do FRET. Agrupar os histogramas para comparação conveniente de resultados de diferentes experimentos.
- Avalie os dados mais adiante (por exemplo, análise de difusão, conversão de eficiências de FRET para forças em experimentos usando sensores de força molecular ou análise de transição) dentro do notebook aproveitando bibliotecas científicas python.
NOTA: Os dados também podem ser exportados em muitos formatos de arquivo como entrada para outros softwares de análise.
Resultados
Uma variedade de informações de baixo e alto nível pode ser extraída de trilhas smFRET dependendo da questão científica do experimento. Aqui, são apresentados exemplos de pipelines de análise com sondas analógicas e digitais: um sensor de força molecular baseado em peptídeo16 e uma sonda de DNA com comutação estocástica de sua conformação38, respectivamente. Consulte a Figura 5 para o princípio de design e trabalho destas sondas.
Após a execução dos algoritmos de localização e rastreamento, conforme descrito no protocolo, o pacote oferece múltiplas ferramentas de visualização de dados para otimizar os parâmetros iniciais e as etapas subsequentes do filtro: (i) visualização de eventos smFRET individuais, (ii) segmentação opcional de imagem para analisar dados em determinadas regiões de interesses, (iii) monitoramento de etapas de filtro via incisoologia FRET versus estoquiometria (E-S). A visualização dos dados de molécula única é apresentada na Figura 6.
Finalmente, os eventos FRET filtrados são representados por um enredo E-S e um histograma de eficiência FRET (Figura 4). O enredo E-S é uma ferramenta útil para otimizar as etapas de filtragem acima mencionadas e investigar o resultado final. Sensores FRET parcialmente branqueados ou incompletamente rotulados podem ser excluídos pelo seu valor de estequiometria. Os parâmetros de mobilidade podem ser investigados traçando um caminho de trajetória individual em um enredo x-y (Figura 6) ou um enredo de deslocamento quadrado médio (MSD) (Figura 4). O primeiro método é especialmente útil para discriminar o celular a partir de eventos imobilizados, enquanto o segundo é usado para calcular o coeficiente de difusão.
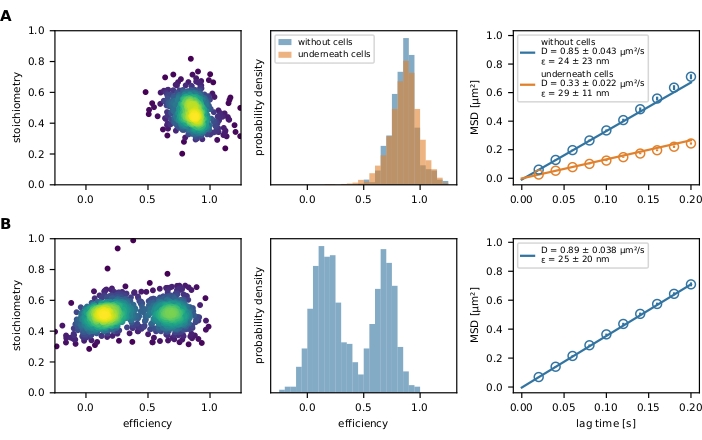
Figura 4: Saída exemplar. (A) A eficiência do FRET é plotada versus estequiometria (enredo E-S) para uma população do sensor de força molecular (painel esquerdo) decorando uma bicamada lipídica suportada por vidro e tensa por uma célula T. Apenas uma nuvem populacional é visível. O respectivo histograma de eficiências de FRET exemplifica a diferença entre uma população de sensores de força na presença e ausência de células (painel médio). Não se pode observar mudança para menor eficiência de FRET da população de sensores na presença de células T, indicando pouco ou nenhum alongamento dependente da força do módulo do sensor. O enredo MSD dessas condições experimentais confirma que a população do sensor de força sob uma célula T se move consideravelmente mais lenta do que suas contrapartes desvinculadas (painel direito). (B) A mesma análise foi realizada com o sensor de DNA de junção holliday decorando uma bicamada lipídica de fluido suportada por vidro. A trama E-S mostra claramente duas populações, que também são aparentes no histograma de eficiência da FRET. O gráfico MSD indica a presença de uma população de sensores em movimento rápido. Abreviaturas: FRET = Transferência de energia de ressonância förster; MSD = deslocamento quadrado médio. Clique aqui para ver uma versão maior desta figura.
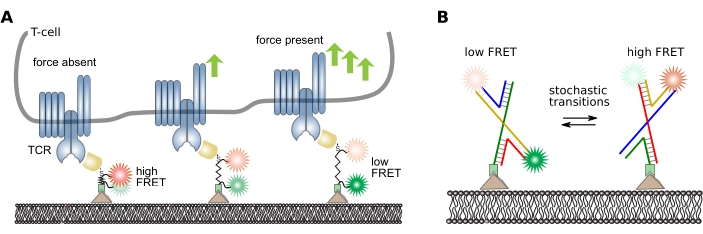
Figura 5: Princípio de design e trabalho das sondas FRET intramolecular. (A) Sensor de peptídeo analógico para quantificação de forças moleculares mecânicas. Os fluoroforos doadores e aceitantes estão covalentemente ligados a ambos os lados da espinha dorsal do peptídeo. O módulo do sensor é especificamente ligado a um ligante específico, que por sua vez liga um receptor de interesse de superfície residente em células (aqui, um fragmento de anticorpo especificamente reconhecendo a cadeia beta do receptor de células T). Após a ligação receptor-ligante, a força é exercida, e o módulo do sensor se estende e eventualmente recua após o decote da ligação. Este painel é modificado a partir de 16. (B) Sensor de DNA digital para quantificação de transições de FRET. O sensor FRET é composto por quatro fios de DNA formando uma junção Holliday. O doador e o fluoróforo aceitor estão covalentemente ligados a dois fios. As junções holliday frequentemente mudam sua conformação dependendo das condições de tampão circundantes. A comutação estocástica dessas conformações pode ser monitorada quantificando a eficiência do FRET de sondas individuais. Abreviaturas: TCR = receptor de células T; FRET = Transferência de energia de ressonância förster. Clique aqui para ver uma versão maior desta figura.
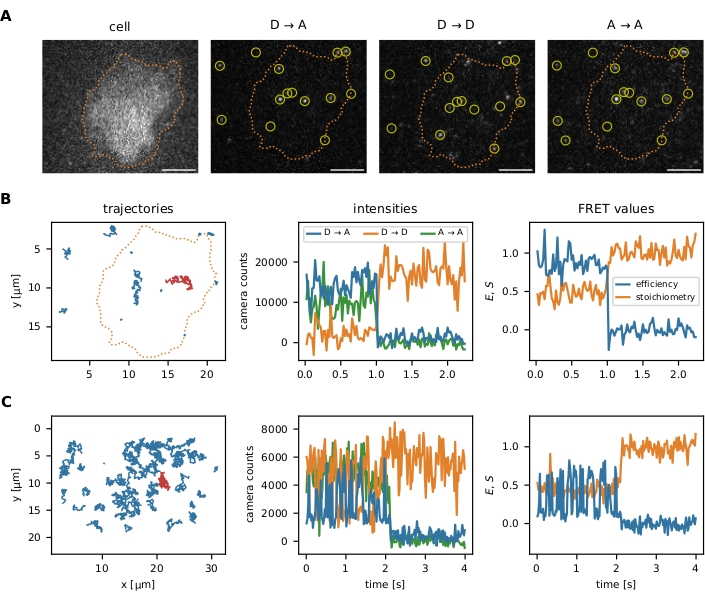
Figura 6: Exemplos de localização e rastreamento de sondas FRET. (A) A eficiência do FRET e a estequiometria de eventos individuais são calculadas quantificando a intensidade do fluorohore doador após a excitação do doador (D → D), o fluorohore acceptor após a excitação do doador (D → A) e o fluoróforo aceitor após a excitação aceitadora (A → A). A filtragem do vizinho mais próximo evita o viés ao sobrepor funções de propagação de pontos de emissores próximos. A segmentação de imagens permite que o usuário escolha certos eventos smFRET localizados dentro de uma área de interesse (por exemplo, uma célula ou um micropattern). Como exemplo de segmentação de imagem, as células T foram manchadas com Fura-2 (exibidas à esquerda) e submetidas a limiares adaptativos para identificar as bordas celulares (linha pontilhada laranja). Barras de escala = trajetórias smFRET de 5 μm. (B) utilizando o sensor de força molecular. Trajetórias individuais podem ser traçadas no plano x-y , visualizando seu comportamento de difusão e localização (painel esquerdo). Além disso, as intensidades de cada trajetória podem ser traçadas ao longo do tempo para identificar transições de FRET ou passos de branqueamento (painel do meio mostra a trajetória vermelha do painel esquerdo). A eficiência e a estequiometria de FRET resultantes podem ser visualizadas de forma semelhante (painel direito). (C) trajetórias smFRET usando o sensor de DNA de junção Holliday. HBSS + 12 mM MgCl2 foi utilizado como tampão durante as medições. Além do aparente passo de branqueamento do aceitador perto do final da sequência desses exemplos, a frequência de transições de FRET para cada sensor pode ser determinada. As junções holliday alternam sua conformação com uma alta frequência, enquanto o sensor de força molecular não exibe transições DE FRET. Essas informações possibilitam ajustar as condições experimentais, como o atraso entre os quadros, para aumentar ou reduzir o número de transições observadas. Abreviaturas: FRET = Transferência de energia de ressonância förster; smFRET = fret de molécula única; HBSS = Solução de sal balanceada da Hank. Clique aqui para ver uma versão maior desta figura.
Informações Suplementares: Localização e rastreamento de moléculas únicas (01). Tracking.ipynb). Clique aqui para baixar este Arquivo.
Discussão
Este artigo detalha um pipeline para as gravações automatizadas e a análise quantitativa dos dados smFRET originados de moléculas de sondas móveis e superficiais. Complementa as duas abordagens predominantes para experimentos smFRET, envolvendo sondas imobilizadas de superfície ou sondas difundindo em solução dentro e fora de um volume de excitação confocal17. Fornece a eficiência correta do FRET e as posições moleculares em função do tempo. Pode, portanto, ser usado como entrada para programas de análise especializados, por exemplo, para quantificar cinética de transição1, histogramas FRET39 ou difusão bidimensional22.
O software é lançado sob uma licença gratuita e de código aberto aprovada pela Open Source Initiative que concede ao usuário o direito perpétuo de livre uso, modificação e redistribuição. O Github foi escolhido como uma plataforma de desenvolvimento e distribuição para facilitar a obtenção do software e participar do processo de desenvolvimento, reportando bugs ou contribuindo com o code40. Escrito em Python, o software não depende de componentes proprietários. A escolha dos notebooks Jupyter como interfaces de usuário facilita a inspeção de dados a cada etapa de análise e permite a adaptação e ampliação do pipeline especificamente para o sistema experimental em mãos. A biblioteca sdt-python32 serve como base e implementa funcionalidade para avaliar dados de microscopia de fluorescência, como localização de molécula única, análise de difusão, análise de intensidade de fluorescência, registro de canal de cores, análise de colocalização e manuseio de ROI.
Em princípio, o rastreamento de partículas únicas pode ser realizado em sistemas uni, bi ou tridimensionais. Aqui, o pipeline de análise de molécula única foi adaptado para o estudo de sistemas móveis 2D. Essa escolha espelha a disponibilidade de sistemas simples, como bicamadas lipídicas (SLBs) suportadas por planar, para apresentar sondas fluorescentes móveis. Tais sistemas lipídicos de bicamadas são tipicamente compostos de dois ou mais moieties fosfolipídios, onde a fração a granel determina os parâmetros físico-químicos chave do SLB (como fase e viscosidade), e a fração menor fornece locais de apego para biomoléculas. Esses locais de apego podem ser fosfolipídios biotinilados para plataformas de proteína baseadas em avidin ou streptavidin ou fosfolipídios conjugados níquel-NTA para plataformas proteicas com tags histidina41. A escolha da plataforma apropriada para a vinculação de proteínas ao SLB depende da questão científica. Os leitores podem consultar a literatura16,38,42, por exemplo, de estratégias empregadas com sucesso. A densidade de sondas na amostra deve ser suficientemente baixa para evitar funções de propagação de pontos sobrepostas; tipicamente, menos de 0,1 moléculas por μm2 são recomendadas. Consulte a seção de resultados representativos (em particular, Figura 6) para um exemplo mostrando uma densidade de sonda adequada. O método de análise também é aplicável a moléculas de proteínas rotuladas fluorescentes únicas na membrana plasmática das células vivas.
Um aspecto crítico dos experimentos smFRET é a produção e caracterização das próprias sondas FRET. Ao escolher fluoroforos para um par DESU, seu raio Förster deve coincidir com as distâncias inter-corantes esperadas43. Corantes resistentes ao fotobleaching são preferidos, pois produzem traços de longo prazo. No entanto, para taxas elevadas de branqueamento, uma espécie de fluorforeiro pode ser utilizada para reconhecer eventos multiemistros originários de moléculas colocalizadas através da análise de fotobleaching stepwise; ver o passo 8.1.4 na seção protocolo. Os pares fluoróforos devem ser ligados especificamente e covalentemente às moléculas de interesse, formando pares FRET intra ou intermolecular.
A combinação do SMFRET com outras técnicas prontamente disponíveis pode aumentar sua resolução espacial além do limite de difração (via STED44). O algoritmo de rastreamento smFRET apresentado aqui amplia a aplicabilidade da abordagem para novas configurações experimentais e sistemas de modelos. Isso inclui estudos de (i) alterações cinéticas na estequiometria das biomoléculas móveis, (ii) associação dinâmica de biomoléculas móveis, (iii) a taxa de reações enzimáticas de reagentes livremente difundidores, e (iv) a cinética das alterações conformacionais das biomoléculas móveis. Os dois primeiros exemplos requerem sistemas de modelos que mostrem FRET intermolecular, ou seja, doador e aceitador são conjugados para separar entidades biomoleculares de interesse. Estes últimos exemplos podem fazer uso de biosensores portadores de doador e aceitador dentro da mesma entidade molecular (FRET intramolecular).
Sensores intramoleculares baseados em FRET podem fornecer informações sobre alterações conformais intrínsecas de biomoléculas1,2,3,4, alterações conformais causadas por carga de força endógena ou externa (sensores de força molecular16), ou concentrações de íons no nano ambiente, como cálcio45 e pH46 . Dependendo do sistema de modelo e da plataforma de ancoragem preferida, tais eventos smFRET podem ser rastreados em 2D ou 3D: (i) o rastreamento planar de eventos smFRET pode ser empregado para a quantificação dos tempos de interação receptor-ligante dentro de uma membrana plasmática, a associação de cascatas de amplificação de sinal ancorado em membrana e as alterações estequiomárias dos receptores de superfície; (ii) o rastreamento de volume de eventos smFRET pode ser usado para qualquer sonda FRET intra ou intermolecular em células vivas ou em sistemas reconstituídos in vitro.
O método de rastreamento smFRET foi desenvolvido principalmente com sondas FRET intramolecular em mente. Essas sondas apresentam um número fixo e bem conhecido de rótulos fluorescentes, fato que foi explorado para rejeitar dados de moléculas agglomeradas e incorretamente sintetizadas (por exemplo, incompletamente rotuladas), bem como de sondas onde um dos fluoroforos foi fotobleachado. No entanto, ajustando as etapas de filtragem, o método também pode ser aplicado a sondas FRET intermoleculares. Por exemplo, em vez de aceitar apenas moléculas com um único doador e um único fluoróforo aceitor, pode-se examinar as trajetórias espaciais de corantes doadores e aceitadores e selecionar, por exemplo, para co-difundir trajetórias de aceitadores de doadores.
Como o algoritmo 3D-DAOSTORM tem suporte para determinar a posição de um sinal ao longo do eixo óptico através do astigmatismo devido a uma lente cilíndrica no caminho do feixe de emissão, experimentos 3D poderiam ser facilmente integrados ao pipeline de análise. Neste caso, o sinal de aceitação sobre a excitação aceitante serviria para determinar a estequiometria e a posição axial. O software de análise também pode ser empregado para avaliar dados de experimentos com sondas imobilizadas utilizando seu grande grau de esquemas de automação e filtragem. De fato, os conjuntos de dados de eficiência smFRET das junções Holliday imobilizadas em bicamadas em fase de gel38 foram analisados usando uma versão inicial do software.
Divulgações
Os autores não declaram conflitos de interesse.
Agradecimentos
Este trabalho foi apoiado pelos projetos do Fundo Austríaco de Ciência (FWF) P30214-N36, P32307-B e pelo LS13-030 do Fundo de Ciência e Tecnologia de Viena (WWTF).
Materiais
| Name | Company | Catalog Number | Comments |
| 1,2-dioleoyl-sn-glycero-3-[(N-(5-amino-1-carboxypentyl)iminodiacetic acid)succinyl] (nickel salt) (Ni-NTA-DOGS) | Avanti Polar Lipids | 790404P | |
| 1,2-dioleoyl-sn-glycero-3-phosphocholine (DOPC) | Avanti Polar Lipids | 850375P | |
| 1-palmitoyl-2-oleoyl-glycero-3-phosphocholine (POPC) | Avanti Polar Lipids | 850457P | |
| α Plan-FLUAR 100x/1.45 oil objective | Zeiss | 000000-1084-514 | |
| Axio Observer microscope body | Zeiss | ||
| Bandpass filter | Chroma Technology Corp | ET570/60m | donor emission filter |
| Bandpass filter | Chroma Technology Corp | ET675/50m | acceptor emission filter |
| conda-forge | conda-forge community | community-maintaned Python package repository for Anaconda/miniconda | |
| Coverslips 60 mm x 24 mm #1.5 | MENZEL | ||
| Dichroic mirror | Semrock Inc | FF640-FDi01-25×36 | separation of donor and acceptor emission |
| Dichroic mirror (quad band) | Semrock Inc | Di01-R405/488/532/635-25×36 | separation of excitation and emission light |
| DPBS | Sigma-Aldrich | D8537 | |
| FCS | Sigma-Aldrich | F7524 | for imaging buffer |
| fret-analysis | Schütz group at TU Wien | Python package for smFRET data analysis; version 3 | |
| Fura-2 AM | Thermo Fisher Scientific | 11524766 | |
| HBSS | Sigma-Aldrich | H8264 | for imaging buffer |
| iBeam Smart 405-S 405 nm laser | Toptica Photonics AG | ||
| iXon Ultra 897 EMCCD camera | Andor Technology Ltd | ||
| Lab-Tek chambers (8 wells) | Thermo Fisher Scientific | 177402PK | for sample preparation and imaging |
| Millenia Prime 532 nm laser | Spectra Physics | ||
| miniconda | Anaconda Inc. | Python 3 distribution. Min. version: 3.7 | |
| Monovalent streptavidin (plasmids for bacterial expression) | Addgene | 20860 & 20859 | |
| OBIS 640 nm laser | Coherent Inc | 1185055 | |
| Optosplit II | Cairn Research | ||
| Ovalbumin | Sigma-Aldrich | A5253 | for imaging buffer |
| Plasma cleaner | Harrick Plasma | PDC-002 | |
| sdt-python | Schütz group at TU Wien | Python library for data analysis; version 17 | |
| TetraSpek bead size kit | Thermo Fisher Scientific | T14792 | Randomly distributed, immobilized fiducial markers for image registration |
| USC500TH Ultrasound bath | VWR | for SUV formation |
Referências
- McKinney, S. A., Déclais, A. -. C., Lilley, D. M. J., Ha, T. Structural dynamics of individual holliday junctions. Nature Structural Biology. 10 (2), 93-97 (2002).
- Wang, S., Vafabakhsh, R., Borschel, W. F., Ha, T., Nichols, C. G. Structural dynamics of potassium-channel gating revealed by single-molecule FRET. Nature Structural & Molecular Biology. 23 (1), 31-36 (2015).
- Hellenkamp, B., Wortmann, P., Kandzia, F., Zacharias, M., Hugel, T. Multidomain structure and correlated dynamics determined by self-consistent FRET networks. Nature Methods. 14 (2), 174-180 (2016).
- Kilic, S., et al. Single-molecule FRET reveals multiscale chromatin dynamics modulated by HP1α. Nature Communications. 9 (1), 235 (2018).
- Stryer, L. Fluorescence energy transfer as a spectroscopic ruler. Annual Review of Biochemistry. 47 (1), 819-846 (1978).
- Wu, P. G., Brand, L. Resonance energy transfer: Methods and applications. Analytical Biochemistry. 218 (1), 1-13 (1994).
- Qiao, Y., Luo, Y., Long, N., Xing, Y., Tu, J. Single-molecular förster resonance energy transfer measurement on structures and interactions of biomolecules. Micromachines. 12 (5), 492 (2021).
- Malkusch, N., Dörfler, T., Nagy, J., Eilert, T., Michaelis, J. smFRET experiments of the RNA polymerase II transcription initiation complex. Methods. 120, 115-124 (2017).
- Lee, J. -. B., et al. Single-molecule views of MutS on mismatched DNA. DNA repair. 20, 82-93 (2014).
- Phelps, C., Israels, B., Jose, D., Marsh, M. C., von Hippel, P. H., Marcus, A. H. Using microsecond single-molecule FRET to determine the assembly pathways of T4 ssDNA binding protein onto model DNA replication forks. Proceedings of the National Academy of Sciences of the United States of America. 114 (18), E3612-E3621 (2017).
- Deindl, S., Zhuang, X. Monitoring conformational dynamics with single-molecule fluorescence energy transfer: Applications in nucleosome remodeling. Methods in Enzymology. 513, 59-86 (2012).
- Crawford, D. J., Hoskins, A. A., Friedman, L. J., Gelles, J., Moore, M. J. Single-molecule colocalization FRET evidence that spliceosome activation precedes stable approach of 5' splice site and branch site. Proceedings of the National Academy of Sciences of the United States of America. 110 (17), 6783-6788 (2013).
- Wang, Y., Xiao, M., Li, Y. Heterogeneity of single molecule FRET signals reveals multiple active ribosome subpopulations. Proteins. 82 (1), 1-9 (2014).
- Mori, T., Vale, R. D., Tomishige, M. How kinesin waits between steps. Nature. 450 (7170), 750-754 (2007).
- Huppa, J. B., et al. TCR-peptide-MHC interactions in situ show accelerated kinetics and increased affinity. Nature. 463 (7283), 963-967 (2010).
- Göhring, J., et al. Temporal analysis of T-cell receptor-imposed forces via quantitative single molecule FRET measurements. Nature Communications. 12 (1), 2502 (2021).
- Hellenkamp, B., et al. Precision and accuracy of single-molecule FRET measurements-a multi-laboratory benchmark study. Nature Methods. 15 (9), 669 (2018).
- Kapanidis, A. N., et al. Fluorescence-aided molecule sorting: Analysis of structure and interactions by alternating-laser excitation of single molecules. Proceedings of the National Academy of Sciences of the United States of America. 101 (24), 8936-8941 (2004).
- Sakon, J. J., Weninger, K. R. Detecting the conformation of individual proteins in live cells. Nature Methods. 7 (3), 203-205 (2010).
- McCann, J. J., Choi, U. B., Zheng, L., Weninger, K., Bowen, M. E. Optimizing methods to recover absolute FRET efficiency from immobilized single molecules. Biophysical Journal. 99 (3), 961-970 (2010).
- Lee, N. K., et al. Accurate FRET measurements within single diffusing biomolecules using alternating-laser excitation. Biophysical Journal. 88 (4), 2939-2953 (2005).
- Asher, W. B., et al. Single-molecule FRET imaging of GPCR dimers in living cells. Nature Methods. 18 (4), 397-405 (2021).
- Joo, C., Ha, T. . Single-molecule FRET with total internal reflection microscopy. (12), 1223-1237 (2012).
- Joo, C., Ha, T. Objective-type total internal reflection microscopy (excitation) for single-molecule FRET. Cold Spring Harbor Protocols. 11, 1189-1191 (2012).
- Joo, C., Ha, T. Objective-type total internal reflection microscopy (emission) for single-molecule FRET. Cold Spring Harbor Protocols. 11, 1192-1194 (2012).
- Allan, D. B., Caswell, T., van der Wel, C. M., Dimiduk, T. . Soft-matter/pims: PIMS v0.5. , (2020).
- Anaconda Inc. . Miniconda. , (2021).
- conda-forge community. . The conda-forge project: community-based software distribution built on the conda package format and ecosystem. , (2015).
- . . JupyterLab Contributors Notebooks - JupyterLab documentation. , (2021).
- Babcock, H., Sigal, Y. M., Zhuang, X. A high-density 3D localization algorithm for stochastic optical reconstruction microscopy. Optical Nanoscopy. 1 (6), (2012).
- Gao, Y., Kilfoil, M. L. Accurate detection and complete tracking of large populations of features in three dimensions. Optics Express. 17 (6), 4685 (2009).
- Schrangl, L. . sdt-python: Python library for fluorescence microscopy data analysis (v17.1). , (2021).
- Crocker, J. C., Grier, D. G. Methods of digital video microscopy for colloidal studies. Journal of Colloid and Interface Science. 179 (1), 298-310 (1996).
- Preibisch, S., Saalfeld, S., Schindelin, J., Tomancak, P. Software for bead-based registration of selective plane illumination microscopy data. Nature Methods. 7 (6), 418-419 (2010).
- Bradski, G. The OpenCV library. Dr. Dobb's Journal: Software Tools for the Professional Programmer. 25 (11), 120-123 (2000).
- Allan, D. B., Caswell, T., Keim, N. C., van der Wel, C. M., Verweij, R. W. Soft-matter/trackpy: Trackpy v0.5.0. Zenodo. , 4682814 (2021).
- Killick, R., Fearnhead, P., Eckley, I. A. Optimal detection of changepoints with a linear computational cost. Journal of the American Statistical Association. 107 (500), 1590-1598 (2012).
- Schrangl, L., Göhring, J., Schütz, G. J. Kinetic analysis of single molecule FRET transitions without trajectories. The Journal of Chemical Physics. 148 (12), 123328 (2018).
- Santoso, Y., Torella, J. P., Kapanidis, A. N. Characterizing single-molecule FRET dynamics with probability distribution analysis. ChemPhysChem. 11 (10), 2209-2219 (2010).
- Schrangl, L. Single-molecule FRET analysis software (3.0). Zenodo. , (2021).
- Nye, J. A., Groves, J. T. Kinetic control of histidine-tagged protein surface density on supported lipid bilayers. Langmuir. 24 (8), 4145-4149 (2008).
- Platzer, R., et al. Unscrambling fluorophore blinking for comprehensive cluster detection via photoactivated localization microscopy. Nature Communications. 11 (1), 4993 (2020).
- Johnson, I., Spence, M. . The molecular probes handbook: A guide to fluorescent probes and labeling technologies. , (2010).
- Szalai, A. M., et al. Super-resolution imaging of energy transfer by intensity-based STED-FRET. Nano Letters. 21 (5), 2296-2303 (2021).
- Miyawaki, A., et al. Fluorescent indicators for Ca2+ based on green fluorescent proteins and calmodulin. Nature. 388 (6645), 882-887 (1997).
- Zhai, B., Zhai, S., Hao, R., Xu, J., Liu, Z. A FRET-based two-photon probe for in vivo tracking of pH during a traumatic brain injury process. New Journal of Chemistry. 43 (43), 17018-17022 (2019).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados