Method Article
Конфокальная лазерная сканирующая микроскопия динамики кальция в острых срезах ткани поджелудочной железы мыши
В этой статье
Резюме
Представлены препараты острых срезов ткани поджелудочной железы и их использование в конфокальной лазерной сканирующей микроскопии для изучения динамики кальция одновременно в большом количестве живых клеток, в течение длительных периодов времени и с высоким пространственно-временным разрешением.
Аннотация
Острый срез ткани поджелудочной железы мыши представляет собой уникальный препарат in situ с сохраненной межклеточной связью и тканевой архитектурой, который влечет за собой значительно меньше изменений, вызванных препаратом, чем изолированные островки, ацинусы, протоки или дисперсные клетки, описанные в типичных исследованиях in vitro. Комбинируя острый срез ткани поджелудочной железы с визуализацией кальция живыми клетками в конфокальной лазерной сканирующей микроскопии (CLSM), сигналы кальция могут быть изучены в большом количестве эндокринных и экзокринных клеток одновременно, с одноклеточным или даже субклеточным разрешением. Чувствительность позволяет обнаруживать изменения и позволяет изучать межклеточные волны и функциональную связность, а также изучать зависимость физиологических реакций клеток от их локализации в островковых и паракринных отношениях с другими клетками. Наконец, с точки зрения благополучия животных, запись сигналов от большого количества клеток одновременно снижает количество животных, необходимых в экспериментах, способствуя 3R-замене, сокращению и уточнению принципа.
Введение
Поджелудочная железа млекопитающих представляет собой крупную экзокринную и эндокринную железу. Экзокринная часть составляет 96-99% от общего объема поджелудочной железы и состоит из ацинушек и протоков. Эндокринная часть состоит из большого количества островков Лангерганса, составляющих оставшиеся 1-4% от общего объема поджелудочной железы1. Экзокринная часть выделяет основные пищеварительные ферменты, которые расщепляют богатые энергией полимеры в пище, а также богатую бикарбонатами жидкость, которая соединяется с другими желудочно-кишечными выделениями, чтобы обеспечить среду, подходящую для действия ферментов. Эндокринная часть выделяет гормоны, которые регулируют постпрандиальное распределение, хранение и межпрандиальное высвобождение богатых энергией питательных веществ. Хотя экзокринная ткань относительно недоразвита, а эндокринная относительно хорошо развита при рождении, первая быстро перерастает вторую при отлученииот груди 2,3,4. Ранние исследования функции поджелудочной железы ознаменовали рождение современной физиологии, и за основными методологическими достижениями в этой области последовали крупные научные прорывы5. Работа с поджелудочной железой технически сложна из-за сложной структуры железы, но также является большой мотивацией из-за таких заболеваний, как рак поджелудочной железы, панкреатит и диабет, которые представляют серьезную угрозу для общественного здравоохранения и для которых необходимы новые терапевтические подходы.
Изолированные островки6, ацины 7,8 и фрагменты протоков разрабатывались и использовались в течение десятилетий в качестве методов золотого стандарта благодаря их преимуществам по сравнению с клеточными линиями и первичными диспергированными эндокринными, ацинарными и протоковыми клетками 9,10. Несмотря на заметно улучшенную функцию изолированных клеточных коллективов, эти методы по-прежнему сопряжены со значительным механическим и ферментативным напряжением, изолируют клетки от окружающих тканей и, таким образом, не имеют паракринных взаимодействий и механической поддержки, и, самое главное, сопровождаются значительными изменениями нормальной физиологии 11,12,13 . Острый срез ткани поджелудочной железы мыши был разработан в 2001 году из предполагаемой необходимости разработки экспериментальной платформы, аналогичной срезам мозга, гипофиза и надпочечников с сохраненными межклеточными контактами, паракринными взаимодействиями, мезенхимой и тканевой архитектурой, а также без некоторых из наиболее важных недостатков метода золотого стандарта в исследовании островков того времени - изолированных островков12, 14. Среди этих недостатков - повреждение самых внешних слоев, отсутствие доступности основных островковых районов и необходимость культивирования, что, возможно, оказывает важное влияние на идентичность и физиологию клеток12,15. Кроме того, метод среза ткани позволяет проводить исследования на животных моделях с сильно нарушенной архитектурой островков, где невозможно изолировать островки или когда выход островков чрезвычайно низок при традиционной изоляции 16,17,18,19,20,21.
Кроме того, срез больше подходит для изучения морфологических изменений во время развития диабета и панкреатита, например, поскольку он позволяет лучше просматривать всю ткань, а также совместим с изучением региональных различий. Важно отметить, что, несмотря на раннюю ориентацию на эндокринную часть, метод среза ткани по своей сути позволяет изучать экзокринные компоненты 9,22,23. В течение первого десятилетия после его введения метод использовался для электрофизиологических исследований бета-14,24,25,26,27,28,29 иальфа-30,31 клеток, а также для изучения морфологического и функционального созревания поджелудочной железы 2,3 . Десять лет спустя, в 2013 году, метод был успешно адаптирован для визуализации кальция в живых клетках островковых клеток с использованием CLSM для характеристики их реакций на глюкозу32, их функциональных паттернов связности33 и взаимосвязи между мембранным потенциалом и внутриклеточным кальцием путем объединения флуоресцентного красителя кальция с мембранным потенциальным красителем34. Позже в том же году метод был также использован для оценки динамики кальция в ацинарных клетках22,35. В течение следующих лет срезы ткани поджелудочной железы использовались в ряде различных исследований и успешно адаптировались к тканям свиней и человека 9,36,37,38,39,40,41. Тем не менее, взятые вместе, визуализация кальция - в срезах ткани поджелудочной железы мыши в целом и в островках в частности - по-прежнему в основном выполняется этой группой. Одна из основных причин этого может заключаться в сочетании технически сложной подготовки среза ткани, необходимости конфокального микроскопа и довольно сложного анализа данных. Основная цель настоящего документа состоит в том, чтобы сделать этот мощный метод более доступным для других потенциальных пользователей.
Уже есть несколько отличных методологических статей, подробно посвященных подготовке срезов тканей и использованию срезов для структурных и секреционных исследований, но не для конфокальной визуализации кальция 9,42,43. Поэтому в данной работе основное внимание уделяется некоторым дополнительным советам и приемам при приготовлении срезов, этапам, критически важным для успешной загрузки красителя, получения изображения, а также основным этапам анализа базовых данных кальция. Поэтому этот вклад следует рассматривать как дополняющий, а не как альтернативу вышеупомянутому методу. Аналогичным образом, визуализация кальция в срезах ткани поджелудочной железы мыши должна рассматриваться как экспериментальный подход, который будет использоваться для ответа на конкретные вопросы, и, таким образом, является дополнением, а не абсолютной альтернативой другим подходам к визуализации кальция в физиологии поджелудочной железы, таким как изолированные протоки или ацины, изолированные островки, органоиды, островки, пересаженные в переднюю камеру глаза, и записи in vivo 11,44,45,46,47,48. Перспективность визуализации кальция в срезах ткани поджелудочной железы мыши, вероятно, лучше всего иллюстрируется недавними успешными записями динамики кальция в островковых мезенхимальных клетках, таких как перициты49 и макрофаги50, а также в клетках протоков23.
протокол
ПРИМЕЧАНИЕ: Все эксперименты проводились в строгом соответствии с институциональными руководящими принципами по уходу и использованию животных в исследованиях. Протокол был одобрен Администрацией Республики Словении по безопасности пищевых продуктов, ветеринарному сектору и защите растений (номер разрешения: 34401-35-2018/2).
1. Подготовка срезов ткани поджелудочной железы
ПРИМЕЧАНИЕ: Подготовка острых срезов ткани поджелудочной железы мыши для визуализации кальция с использованием CLSM требует ряда инструментов, различных растворов и протекает в серии критических этапов, которые схематично представлены на рисунке 1 и подробно описаны ниже.
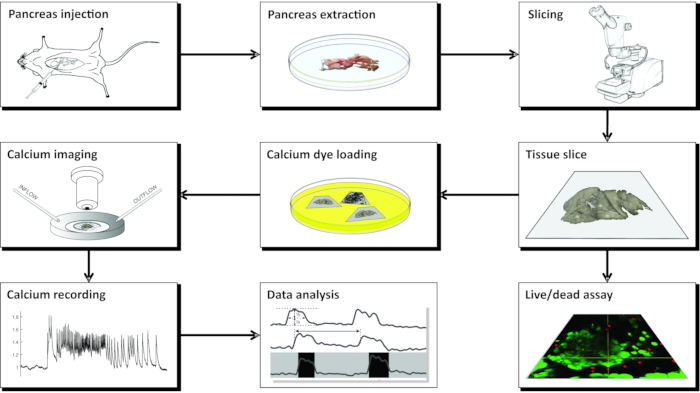
Рисунок 1: Схема рабочего процесса. Схематическое представление всех этапов процесса подготовки среза ткани поджелудочной железы, начиная с введения агарозы в общий желчный проток с последующим извлечением поджелудочной железы и нарезкой. Приготовленные ломтики могут быть использованы для оценки жизнеспособности ткани с помощью набора Live/Dead или окрашены датчиком кальция. После окрашивания они готовы к визуализации. Записи, полученные в процессе визуализации, затем используются для анализа данных. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
- Приготовление растворов
ПРИМЕЧАНИЕ: Все растворы должны быть приготовлены заранее и могут храниться в холодильнике при температуре 4-8 °C до одного месяца. Для приготовления и хранения срезов тканей необходимо приблизительно 0,5 л внеклеточного раствора (ECS) с 6 мМ глюкозы и 0,3 л буфера 4-(2-гидроксиэтил)-1-пиперазинетансульфоновой кислоты (HEPES). Для 1 дня визуализации кальция с перифузионной системой, установленной на скорости потока 1-2 мл / мин, необходимо приблизительно 0,5 л ECS.- Внеклеточный раствор с глюкозой 6 мМ
- Готовят 1 л ECS, содержащего 125 мМ NaCl, 26 мМ NaHCO3, 6 мМ глюкозы, 6 мМ молочной кислоты, 3 мМ мио-инозитола, 2,5 мМ KCl, 2 мМ Na пирувата, 2 мМ CaCl2, 1,25 мМ2PO4, 1 мМ MgCl2 и 0,5 мМ аскорбиновой кислоты. Тщательно перемешайте, пока все ингредиенты полностью не растворятся. Возьмите 50 мкл ECS в микроцентрифужную трубку объемом 0,5 мл, поместите ее на осмометр в соответствии с инструкциями производителя и проверьте осмолярность.
ПРИМЕЧАНИЕ: Осмолярность должна быть 300-320 мОсм. Для стимуляции бета-клеток используют растворы с более высокими концентрациями глюкозы. Чтобы обеспечить физиологическое значение рН 7,4 во время нарезки и экспериментов, постоянно пузырьки ECS с карбогеном (т.е. газовой смесью 95% O2 и 5% CO2) при барометрическом давлении. Простая система пузырьков может быть настроена путем присоединения одного конца 5-миллиметровой кремниевой трубки к источнику карбогена (т.е. газовому баллону под давлением), а другой конец трубки помещен непосредственно в баллон, содержащий ECS. - Альтернативно, готовят 10-кратный запас, содержащий 1250 мМ NaCl, 260 мМ NaHCO3, 30 мМ мио-инозитол, 25 мМ KCl, 20 мМ Na пируват, 12,5 мМ2PO4 и 5 мМ аскорбиновой кислоты. При необходимости ЭКС, содержащей 6 мМ глюкозы, смешивают 100 мл бульона с 2 мл 1 МCaCl2, 1 мл 1 ММгCl2, 0,455 мл 13,2 мл молочной кислоты и 1,08 г глюкозы и заливают двойной дистиллированной водой до 1 л. При необходимости используйте различные количества глюкозы для получения других концентраций глюкозы.
- Готовят 1 л ECS, содержащего 125 мМ NaCl, 26 мМ NaHCO3, 6 мМ глюкозы, 6 мМ молочной кислоты, 3 мМ мио-инозитола, 2,5 мМ KCl, 2 мМ Na пирувата, 2 мМ CaCl2, 1,25 мМ2PO4, 1 мМ MgCl2 и 0,5 мМ аскорбиновой кислоты. Тщательно перемешайте, пока все ингредиенты полностью не растворятся. Возьмите 50 мкл ECS в микроцентрифужную трубку объемом 0,5 мл, поместите ее на осмометр в соответствии с инструкциями производителя и проверьте осмолярность.
- Буфер HEPES с глюкозой 6 мМ
- Готовят 0,5 л HEPES-буферного раствора (HBS), содержащего 150 мМ NaCl, 10 мМ HEPES, 6 мМ глюкозы, 5 мМ KCl, 2 мМ CaCl2 и 1 мМ MgCl2; титровать до рН = 7,4 с 1 М NaOH.
ПРИМЕЧАНИЕ: Если карбоген недоступен, этот буфер можно использовать для всех этапов вместо ECS.
- Готовят 0,5 л HEPES-буферного раствора (HBS), содержащего 150 мМ NaCl, 10 мМ HEPES, 6 мМ глюкозы, 5 мМ KCl, 2 мМ CaCl2 и 1 мМ MgCl2; титровать до рН = 7,4 с 1 М NaOH.
- Агароза (1,9% мас.)
- Перед прогревом водяная баня до 40 °C.
- Добавьте 0,475 г агарозы с низкой температурой плавления и 25 мл ECS, содержащего 6 мМ глюкозы, в колбу Эрленмейера и поместите колбу в микроволновую печь на максимальной мощности на несколько секунд, пока она не начнет кипеть. Достаньте колбу из духовки и закрутите ее несколько раз, пока агароза не растворится полностью. Переложите колбу с жидкой агарозой на предварительно расплавленную водяную баню при 40 °C, чтобы охладить агарозу до нужной температуры и сохранить ее жидкой до инъекции. Закрепите колбу стабилизирующим свинцовым кольцом.
ПРИМЕЧАНИЕ: Агарозу можно приготовить заранее и хранить в холодильнике. Перед использованием разогрейте агарозу в микроволновой печи до тех пор, пока она не разжижится, и переложите колбу Эрленмейера на водяную баню предварительно расплавленной до 40 °C. Агароза может быть повторно использована до 5x. При повторном использовании за пределами 5x он станет плотным и его будет сложнее вводить.
- Внеклеточный раствор с глюкозой 6 мМ
- Инъекции поджелудочной железы с агарозой
ПРИМЕЧАНИЕ: Разделы 1.2 и 1.3 объясняют подготовку срезов ткани, которые могут быть использованы для различных экспериментальных целей, таких как визуализация кальция, электрофизиология, иммуногистохимия, исследования секреции и структурные/микроанатомические исследования.- Заполните шприц объемом 5 мл жидкой агарозой из колбы Эрленмейера на водяной бане с этапа 1.1.3.2, удалите все пузырьки и установите иглу весом 30 г. Защитите иглу колпачком, а наполненный шприц держите обратно на водяной бане иглой, обращенной вниз, и весь объем агарозы ниже поверхности воды. Закрепите шприц стабилизирующим свинцовым кольцом таким образом, чтобы кольцо прижимало шприц к стенке водяной бани.
ПРИМЕЧАНИЕ: Будьте осторожны, чтобы не втолкнуть агарозу в иглу, так как она быстро затвердеет и заблокирует иглу. Если температура в помещении низкая, и если инъекция выполняется менее опытным человеком, увеличьте температуру водяной бани до 42 °C, чтобы получить некоторое дополнительное время для инъекции. - Наполните ведро со льдом и поместите в него бутылку, содержащую ECS. Пузырите ECS постоянно со скоростью 1,5 мл / мин с карбогеном при барометрическом давлении и комнатной температуре, чтобы обеспечить оксигенацию и рН 7,4.
- Жертвуйте мышью, вводя высокую концентрацию CO2 с последующим вывихом шейки матки. Приложите все усилия, чтобы свести к минимуму страдания животных.
- Работая под стереомикроскопом, получите доступ к брюшной полости с помощью лапаротомии (рисунок 2А). Осторожно переверните кишечник в левую сторону мыши (с анатомической точки зрения мыши), чтобы обнажить общий желчный проток. Используйте щипцы, чтобы слегка приподнять дуоденальную часть, и найти большой дуоденальный сосочек-сосочек Фатера. Зажмите общий желчный проток в дуоденальном сосочке с помощью гемостата (рисунок 2B, C) для предотвращения утечки агарозы из протока в двенадцатиперстную кишку.
ПРИМЕЧАНИЕ: Чтобы предотвратить утечку агарозы в двенадцатиперстную кишку и далее вверх и вниз в желудочно-кишечном тракте, поместите гемостат таким образом, чтобы он также зажимал двенадцатиперстную кишку как проксимально, так и дистально из сосочков. Лучше всего использовать для этой цели изогнутый гемостат. - Небольшими острыми щипцами доберитесь под общий желчный проток, и разорвите мембрану, которая прикрепляет проток к ткани поджелудочной железы. Для лучшего визуального контроля и более легкой инъекции очистите проток как можно больше жира и соединительной ткани.
- Поместите проток перпендикулярно на крупные щипцы (рисунок 2D) и введите подготовленную жидкую агарозу в проксимальную часть общего желчного протока (рисунок 2D). Обязательно сильно сжимайте шприц, так как агароза вязкая. Продолжайте заполнять поджелудочную железу до тех пор, пока она не станет беловатой и слегка растянутой или не менее 20-30 с.
ПРИМЕЧАНИЕ: Это наиболее важный этап в подготовке среза. Если есть какие-либо перегибы в протоковом дереве поджелудочной железы, осторожно поднимите или оттяните поджелудочную железу от шприца, чтобы выровнять их. Не решайте, когда прекратить инъекцию, основываясь на объеме, вводимом из шприца, поскольку обратный поток в точке инъекции и прямая утечка в двенадцатиперстную кишку обычно намного выше, чем объем, вводимый в протоковое дерево поджелудочной железы. Важно отметить, что успешные инъекции могут быть выполнены при практически незаметных изменениях объема шприца. - Извлеките шприц и медленно вылейте 20 мл пузырькового ледяного ECS при 0-4 °C из бутылки на поджелудочную железу, чтобы охладить ткань и затвердеть агарозу.
- Аккуратно извлеките поджелудочную железу с помощью щипцов и тонких ножниц. Поместите извлеченную поджелудочную железу в чашку Петри толщиной 100 мм, содержащую ~ 40 мл ледяного ECS, и осторожно переместите ее, чтобы вымыть. Переведите поджелудочную железу в свежую чашку Петри толщиной 100 мм, содержащую ~40 мл ледяного ECS.
- Из хорошо введенной части поджелудочной железы, которая выглядит беловатой (рисунок 3А), разрезают до 6 блоков ткани размером 0,1-0,2см3 , используя щипцы и жестко разрезанные ножницы. Очистите их от любой соединительной и жировой ткани.
- Наполните 35-миллиметровую нелипкую нижнюю чашку Петри примерно 5 мл жидкой агарозы при 40 °C, перенесите в нее тканевые блоки и немедленно положите чашку Петри на лед, чтобы охладить ее и затвердеть агарозу.
ПРИМЕЧАНИЕ: То, как блоки поджелудочной железы попадают в агарозу, определяет способ их разрезания во время нарезки. Опытные экспериментаторы могут попытаться точно настроить положение блоков в течение нескольких мгновений до того, как агароза затвердеет при размещении на льду. - После того, как агароза с тканевыми блоками затвердеет, переверните чашку Петри вверх дном на плоскую гладкую поверхность, такую как крышка чашки Петри 100 мм, и удалите агарозу, аккуратно разрезав половиной лезвия бритвы в край между боковой стенкой чашки Петри и агарозой. Лезвием бритвы разрезайте отдельные кубики агарозы, каждый из которых содержит один блок ткани, заботясь о том, чтобы каждый блок ткани был окружен агарозой. Приклейте блоки агарозы на образец пластины вибратома цианоакрилатным клеем (рисунок 3B).
- Заполните шприц объемом 5 мл жидкой агарозой из колбы Эрленмейера на водяной бане с этапа 1.1.3.2, удалите все пузырьки и установите иглу весом 30 г. Защитите иглу колпачком, а наполненный шприц держите обратно на водяной бане иглой, обращенной вниз, и весь объем агарозы ниже поверхности воды. Закрепите шприц стабилизирующим свинцовым кольцом таким образом, чтобы кольцо прижимало шприц к стенке водяной бани.
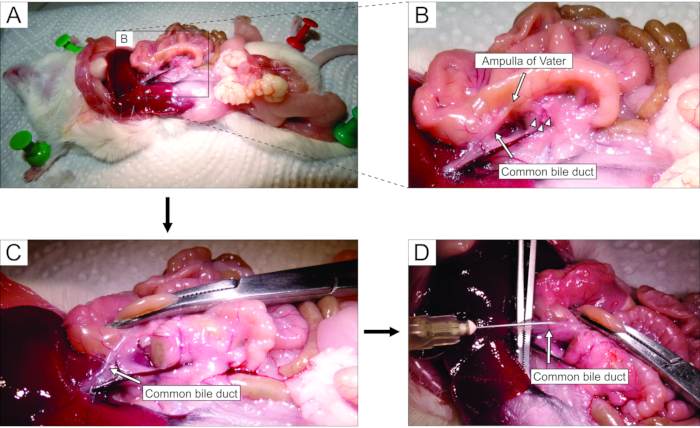
Рисунок 2: Инъекция агарозы в общий желчный проток. (А) Открыть брюшную полость, и обнажить органы в брюшной полости. (B) Увеличенная часть области, заключенная прямоугольником в панели А. Белое пятно на двенадцатиперстной кишке (обозначено стрелкой) указывает на ампулу Фатера. Островки Лангерганса обозначаются наконечниками стрел. (C) Зажмите ампулу Фатера изогнутым гемостатом и слегка приподнимите ее, чтобы обнажить и осторожно растянуть общий желчный проток (стрелка). (D) Каннуляция общего желчного протока и инъекция 1,9% раствора агарозы с использованием шприца 5 мл и иглы 30 г. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
- Разрезание на ломтики
- Заполните режущую камеру вибратома ~0,15 л ледяного ECS и постоянно пузырьковайте карбогеном. Окружите режущую камеру льдом и добавьте в режущую камеру 2 кубика льда (~ 10 мл каждый), изготовленных из ECS с 6 мМ глюкозы. Установите лезвие бритвы для резки на вибратом и закрепите на своем месте пластину образца с блоками агарозы.
- Установите слайсер для резки блоков агарозы со скоростью от 0,05 до 1 мм/с и 70 Гц на срезы толщиной 140 мкм с площадью поверхности 20-100мм2. Для настройки среза следуйте инструкциям производителя.
- Сразу после каждого этапа резки поставьте на паузу слайсер, аккуратно соберите ломтики тонкой кистью и переложите их в 100-миллиметровую чашку Петри, заполненную 40 мл буфера HEPES с глюкозой 6 мМ при комнатной температуре (рисунок 3C).
ПРИМЕЧАНИЕ: Срезы могут храниться в буфере HEPES при комнатной температуре не менее 12 ч, и буфер следует менять каждые 2 ч.
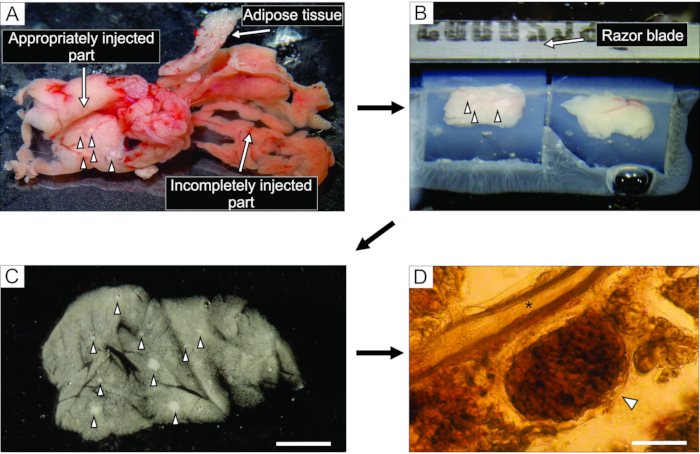
Рисунок 3: Подготовка и нарезка тканей поджелудочной железы. (А) Экстрагируется поджелудочная железа мыши после инъекции агарозы. Белая ткань слева указывает на хорошо введенную часть (дуоденальную часть), в то время как более красноватая часть справа показывает недостаточно введенную часть поджелудочной железы (селезеночная часть). (B) Вибратомная нарезка двух блоков ткани поджелудочной железы, встроенных в агарозу. (C) Острый срез ткани поджелудочной железы с островками Лангерганса, обозначенными наконечниками стрел. Шкала бар = 3000 мкм. (D) Острый срез ткани поджелудочной железы под световым микроскопом с островком Лангерганса, обозначенным наконечником стрелы, звездочкой обозначен проток поджелудочной железы. Шкала = 100 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
2. Живой / мертвый анализ с использованием LIVE / DEAD Viability / Cytotoxicity Kit для клеток млекопитающих
ПРИМЕЧАНИЕ: Для некоторых экспериментов полезно проверить жизнеспособность клеток в срезах (рисунок 4) с помощью анализа живых/мертвых следующим образом.
- Следуйте инструкциям производителя по размораживанию флаконов с реагентами LIVE/DEAD Viability/Cytotoxicity Kit, и непосредственно перед использованием готовьте рабочие растворы кальцеина AM. Используйте решения в течение одного дня.
- В центрифужной трубке объемом 15 мл смешайте 5 мкл 4 мМ кальциина AM (компонент A), 20 мкл гомодимера этидия-1 2 мМ (EthD-1, компонент B) и 10 мл фосфатно-буферного физиологического раствора Dulbecco (D-PBS) для получения рабочего раствора, содержащего примерно 2 мкМ кальциина AM и 4 мкМ EthD-1. Вихрь основательно.
- Используя тонкую кисть, аккуратно перенесите кусочки ткани в чашку Петри объемом 3 мл со свежим буфером HEPES, чтобы разбавить активность эстеразы сыворотки. Удалите буфер HEPES и покройте срезы 100-200 мкл (или более, если это необходимо) рабочего раствора с шага 2.2.
- Инкубировать ломтики в течение 30-45 мин при комнатной температуре в закрытой чашке Петри. Визуализируйте срезы ткани с помощью фильтров возбуждения/излучения в соответствии с рекомендациями производителя.
3. Загрузка кальциевого красителя
ПРИМЕЧАНИЕ: Флуоресцентные красители должны быть защищены от светового воздействия в течение всего процесса приготовления и загрузки красителя, а также во время обработки окрашенных срезов ткани. Оловянная фольга может быть использована для покрытия трубок или чашек Петри, содержащих кальциевый краситель.
- Подготовка красителя
- Растворяют содержимое одного флакона (50 мкг) клеточного проницаемого индикаторного красителя Ca2+ (возбуждение/излучение 495/523 нм; см. Таблицу материалов), 7,5 мкл диметилсульфоксида (ДМСО) и 2,5 мкл полаксамера (20% раствор в ДМСО; Таблица материалов) в 6,667 мл HBS, содержащего 6 мМ глюкозы в 15 мл завинчивающейся колпачковой трубки.
ПРИМЕЧАНИЕ: Этот конечный раствор содержит 6 мкМ индикаторного красителя Ca2+ , 0,11% DMSO и 0,037% полаксамера. - Аспирировать и выталкивать раствор в завинчивающуюся колпачковую трубку многократно пипеткой в течение 20 с; погружают трубку в ультразвуковую камеру ванны на 30 с, а вихрь на 30 с для улучшения солюбилизации. Aliquot 3,333 мл конечного раствора индикаторного красителя Ca2+ , приготовленного на этапе 3.1.1 в 5 мл чашки Петри.
- Растворяют содержимое одного флакона (50 мкг) клеточного проницаемого индикаторного красителя Ca2+ (возбуждение/излучение 495/523 нм; см. Таблицу материалов), 7,5 мкл диметилсульфоксида (ДМСО) и 2,5 мкл полаксамера (20% раствор в ДМСО; Таблица материалов) в 6,667 мл HBS, содержащего 6 мМ глюкозы в 15 мл завинчивающейся колпачковой трубки.
- Загрузка красителя
- Переложите подготовленные ломтики ткани из чашки Петри объемом 60 мл с HBS в чашки Петри объемом 5 мл, заполненные раствором красителя, осторожно подняв каждый срез ткани с помощью тонкой, мягкой красящей кисти и поместив его в раствор красителя. Инкубируйте до 10 кусочков ткани на чашку Петри.
- Поместите нагруженную кусочками чашку Петри на орбитальный шейкер при комнатной температуре, установленной для орбитального движения со скоростью 40 оборотов в минуту в течение 50 минут. Инкубируют ломтики в растворе красителя, подвергая воздействию окружающего воздуха при комнатной температуре, но защищая от света, накрыв чашку Петри оловянной фольгой.
- Хранение срезов
- Перенесите окрашенные срезы ткани из чашки Петри объемом 5 мл в чашку Петри объемом 60 мл, наполненную HBS без красителя, осторожно подняв их с помощью тонкой, мягкой кисти. Хранить до 20 ломтиков на чашку Петри.
ПРИМЕЧАНИЕ: Используйте срезы ткани для визуализации на этом этапе. Срезы ткани будут удерживать индикаторный краситель Ca2+ в течение нескольких часов. Выживание ломтиков и удержание красителя можно улучшить, поместив чашку Петри в изолированный контейнер, окруженный льдом. Это особенно важно, если необходимо транспортировать срезы, загруженные красителем. Кроме того, меняйте HBS каждые 2 часа.
- Перенесите окрашенные срезы ткани из чашки Петри объемом 5 мл в чашку Петри объемом 60 мл, наполненную HBS без красителя, осторожно подняв их с помощью тонкой, мягкой кисти. Хранить до 20 ломтиков на чашку Петри.
4. Визуализация кальция
- Настройка конфокального микроскопа
- Выберите соответствующее объективное увеличение в зависимости от интереса исследования. Выберите 20x и 25x (числовая диафрагма [NA] 0,77-1,00) для визуализации целого островка, нескольких ацинуров одновременно или более крупных воздуховодов. Выберите более высокие увеличения для изучения внутриклеточной динамики.
- Выберите режим съемки для покадровой съемки (например, покадровый, xyt или аналогичный режим). Установите точечное отверстие на 100-200 мкм.
- Установите световой тракт для зеленых флуорофоров: возбуждение на 488 нм, и сбор излучения на 500-700 нм. Предпочтительно выбирать детекторы с высокой квантовой эффективностью (например, арсенид галлия фосфид) над фотоумножительными детекторами.
- Настройка регистрирующей камеры и системы перифузии
- Установите камеру записи на регулируемую температуру ступени микроскопа и перифузионной системы (либо с гравитационной подачей, либо на основе перистальтического насоса, объем 1 мл). Расположите входное и выходное отверстие на дальних краях регистрирующей камеры, чтобы избежать извилины перфузата внутри камеры, и установите приток и отток равными значениями (1-2 мл/мин). Избегайте дрейфа высоты жидкого мениска и капель в перифузате.
- Установите температурный контроль системы перифузии на 37 °C. Начните перифузию нестимулирующим раствором и приготовьте стимулирующие растворы. Меняйте растворы с помощью моторизованных клапанов или вручную переключая растворы, питающие перифузионную систему.
- Рекордная динамика кальция
- Перенесите один срез ткани в записывающую камеру. Обездвижите срез ткани U-образной платиновой массой с подтянутой нейлоновой сеткой (например, из нейлоновых чулок). Избегайте размещения нейлоновых нитей над интересующей структурой.
- Найдите островок/ацинус/канал с помощью опции brightfield. Запустите живую визуализацию, чтобы позиционировать исследуемые структуры в поле зрения и настроить параметры изображения. Оптимизируйте отношение сигнал/шум, регулируя мощность лазера, усиление детектора и усреднение /биннинг линии, чтобы обеспечить визуализацию ячеек при сохранении минимальной мощности лазера.
- Отрегулируйте фокальную плоскость записи до ~15 мкм ниже поверхности разреза (рисунок 5), чтобы избежать записи из потенциально поврежденных клеток на поверхности разреза.
- Получайте изображения. Установите частоту дискретизации на 1-2 Гц для первоначального обнаружения отдельных колебаний и используйте резонансный сканер, способный к быстрому усреднению линии (8-20) с более высокой скоростью сбора (>10 Гц) для записи внутриклеточной активности Ca2+ ([Ca2+]IC). Допускайте интервал (например, 30% от общего времени выборки) между последовательными точечными освещениями для предотвращения фототоксичности. Запишите изображение с высоким разрешением (например, 1024 x 1024 пикселя, усреднение строки > 50) перед получением временных рядов (см. раздел 5).
ПРИМЕЧАНИЕ: Частота дискретизации 1-2 Гц ниже критерия Найквиста для частоты захвата для большинства ячеек, и форма сигнала будет недодискретизирована по умолчанию. - Обратитесь к онлайн-диаграмме, если она доступна в программном обеспечении для визуализации, чтобы получить мгновенную обратную связь о реакции подготовки, чрезмерном освещении, фотоотбеливании и механическом дрейфе. В случае высокой скорости отбеливания во время съемки остановите запись и уменьшите мощность лазера при одновременном увеличении усиления детектора для поддержания отношения сигнал/шум. В случае механического дрейфа проверьте натяжение между трубками/кабелями и ступенью микроскопа, а также утечку жидкости или изменение объема в камере записи. При желании попытайтесь исправить дрейф во время захвата вручную; однако обратите внимание, что это по своей сути даст ограниченные результаты.
ПРИМЕЧАНИЕ: Эндокринные клетки очень гетерогенны при околопороговых концентрациях. Достаточная продолжительность стимуляции необходима для выявления диапазона задержек активации/деактивации в отдельных клетках. Это особенно важно для точного обнаружения ответов в соответствии с высокостимулирующими протоколами. - Используйте кальциевую визуализацию для функционального различения эндо- и экзокринных клеток (рисунок 6). Для записи преходящей активности во время активации и деактивации применяйте стимулы, не останавливая запись.
- Сохраните данные после окончания экспериментов (рассмотрите возможность использования функции автосохранения). Выделите период охлаждения перед отключением питания лазера, чтобы не повредить лазеры во время процедуры отключения.
5. Анализ данных
- Визуально проверьте запись качественно, воспроизведя покадровое видео. Проверьте наличие дрейфов ячеек из поля зрения или оптической плоскости. Если произошел дрейф в оптической плоскости, используйте плагин коррекции дрейфа в ImageJ.
- Выберите интересующие регионы (ROI) с помощью программного обеспечения микроскопа или стороннего программного обеспечения. Используйте изображение с высоким разрешением, максимальную проекцию или среднее значение кадра в качестве ориентира для выбора ROI. Воспроизведите покадровое изображение, чтобы визуализировать ответные ячейки, которые не видны на эталонных изображениях. Расположите ROI таким образом, чтобы выбранная область ROI не перекрывалась с соседними ячейками, чтобы избежать перекрестных помех сигнала между ROI.
- Экспортируйте данные временных рядов в виде среднего значения ROI на кадр. Экспорт координат ROI.
- Корректировка данных временных рядов для отбеливания (рисунок 7A) путем использования комбинации экспоненциального и линейного соответствия, как описано
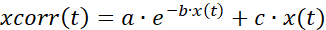 (1)
(1)
где x(t) обозначает флуоресцентный сигнал в точке времени t; xcorr(t) скорректированный сигнал в соответствующих точках времени; и a, b и c — параметры прилегания, вычисляемые как наименьшая сумма квадратов между corr(t) и x(t). - Анализ фазы активации и деактивации ответа (рисунок 7B). Рассчитайте первую производную данных временных рядов и определите зенит и надир производной, соответствующие активации и деактивации соответственно. Кроме того, можно вручную выбрать начало фазового увеличения. Сохраните и экспортируйте время активации/деактивации и соответствующие координаты ячейки.
- Проанализируйте фазу плато (рисунок 7C). Обнаружение отдельных колебаний путем порогового значения необработанных данных или путем порогового значения первой производной данных временных рядов. Определите начало и конец отдельного колебания как время, соответствующее половинной амплитуде колебания.
- Рассчитайте продолжительность и частоту отдельных колебаний для каждой ячейки. Рассчитайте обратное значение интервала между ударами (подходит для регулярных паттернов активности). В качестве альтернативы можно разделить число колебаний на временной интервал записи (подходит для нерегулярных паттернов активности).
- Рассчитайте активное время. Выразите активное время как сумму длительностей и разделите это значение на интервал времени. В качестве альтернативы можно умножить частоту и продолжительность, которые соответствуют колебанию.
ПРИМЕЧАНИЕ: Деление суммы длительностей на временной интервал дает надежные результаты, но имеет низкую статистическую дискриминацию, поскольку получается одна точка данных на ячейку. Умножение частоты и длительности колебаний обеспечивает временное разрешение от колебаний к колебаниям.
Результаты
Инъекция раствора агарозы в проток поджелудочной железы является наиболее важным этапом в подготовке среза ткани поджелудочной железы. Успешную инъекцию можно распознать по отбеливанию ткани поджелудочной железы, как видно на левой стороне рисунка 3А, в то время как неполностью введенная часть поджелудочной железы представлена на правой стороне рисунка 3А. Островки Лангерганса могут быть распознаны невооруженным глазом или под стереомикроскопом, и это помогает в разрезании соответствующих частей поджелудочной железы для последующего встраивания в блоки агарозы (рисунок 3B). В свежесрезанном срезе ткани поджелудочной железы мыши островки Лангерганса можно легко отличить от окружающей экзокринной ткани и мезенхимы в виде белых пятен под стереомикроскопом (рисунок 3C) или в виде коричневатых структур под световым микроскопом (рисунок 3D). Срезы ткани поджелудочной железы могут быть использованы для различных типов экспериментов в течение, по крайней мере, 12 ч после нарезки. В дополнение к грубой морфологической оценке под стереомикроскопом, световым микроскопом и функциональными реакциями клеток во время визуализации кальция может быть оценена жизнеспособность срезов ткани поджелудочной железы (рисунок 4).
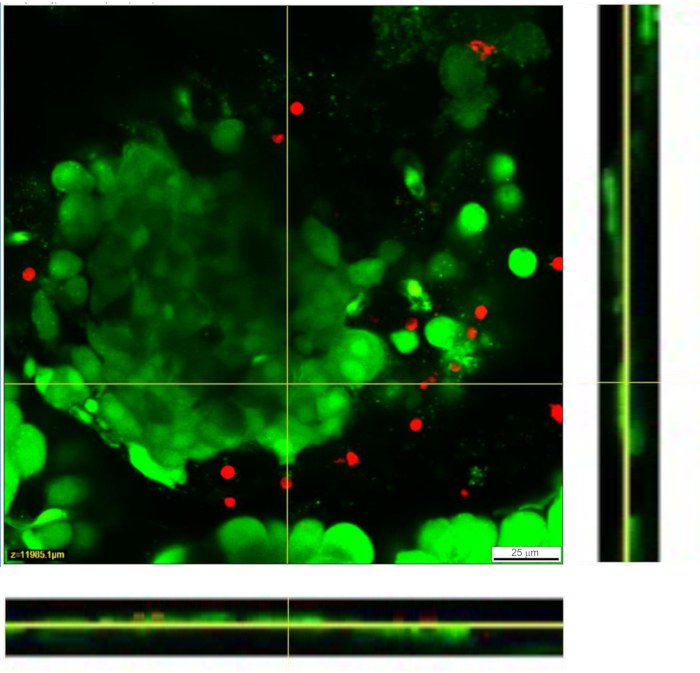
Рисунок 4: Жизнеспособность клеток внутри среза ткани. Жизнеспособность клеток определяли с помощью анализа Live/Dead. Живые клетки окрашиваются Calcein AM (показаны зеленым цветом), в то время как мертвые клетки окрашиваются гомодимером этидия-1 (показан красным цветом). Желтые линии обозначают положение поперечного сечения X-Y Z-стека, отображаемого внизу и справа. Полная глубина Z-стека составляет 88 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Для экспериментов с визуализацией кальция флуоресцентный индикатор кальция должен проникать через несколько слоев клеток. На рисунке 5А показана успешная загрузка клеточно-проницаемого индикаторного красителя Ca2+ в срез ткани поджелудочной железы, в котором могут быть распознаны отдельные островковые и ацинарные клетки. Напротив, срезы на рисунке 5B-D не являются оптимальными из-за неудачного проникновения красителя (рисунок 5B), отсутствия островковых клеток (рисунок 5C) и большого количества некротической ткани на поверхности (рисунок 5D). Такие срезы могут быть выброшены, проверены на наличие дополнительных островков, которые лучше разрезаны или окрашены (см. Таблицу 1 для устранения неполадок), или использованы для записи реакций экзокринных клеток.
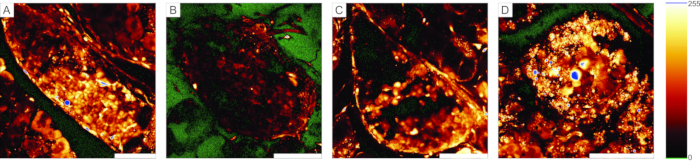
Рисунок 5: Примеры пригодных и непригодных для использования препаратов. (А) Пример успешного приготовления среза ткани поджелудочной железы с хорошо окрашенными клетками в островках Лангерганса, а также клетками протоков и окружающей ацинарной тканью. (B) Пример плохо окрашенного среза ткани. (C) Пример островка Лангерганса со структурными разрывами. (D) Пример островка Лангерганса, содержащего много мертвых клеток и много мусора. Таблица подстановки «свечение, свечение» справа отображает интенсивность 0 зеленым цветом и насыщенность синим. Шкала = 100 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Репрезентативные результаты визуализации кальция с использованием клеточно-проницаемого индикаторного красителя Ca2+ показаны на рисунке 6. На фиг.6А представлено изображение среза ткани поджелудочной железы с высоким разрешением, содержащее островок Лангерганса, ацинарную ткань и проток поджелудочной железы. Для лучшего различения эндокринная, экзокринная и протоковая часть среза ткани поджелудочной железы, представленная на рисунке 6А , окрашена на рисунке 6B. Использование соответствующих стимулов может функционально различать различные островковые клетки или островковые и неостровные клетки51. Бета-клетки обычно реагируют на стимуляцию квадратного импульса глюкозой с переходным увеличением [Ca2+]IC с последующими быстрыми колебаниями кальция на устойчивом плато (рисунок 6C, верхняя панель).
Поскольку все бета-клетки соединены в один большой функциональный синцитий, эти колебания также очень хорошо синхронизированы между различными клетками посредством распространения волн [Ca2+]IC 32,34,52,53,54 (Рисунок 7C). Более медленные [Ca2+]IC колебания с периодом 5-15 минут могут лежать в основе быстрых колебаний или даже быть преобладающим типом ответа55,56. Тот же простой протокол может выявить другие типы ответов, особенно на периферии островков (рисунок 6C, нижняя панель). Поскольку эти клетки не синхронизированы с бета-клетками и реагируют более быстрыми и нерегулярными колебаниями, которые уже присутствуют в условиях низкого уровня глюкозы или со снижением активности, такие ответы очень наводят на мысль о небета-клетках 21,32,57,58. Однако их окончательная функциональная характеристика требует более сложных протоколов с дополнительными шагами стимуляции или альтернативными подходами, которые обсуждаются ниже. Типичные ответы ацинарных и проточных клеток представлены на рисунке 6D и рисунке 6E соответственно. Обратитесь к литературе для получения более подробной информации об ацинарных и протоковых клетках 22,23,35.
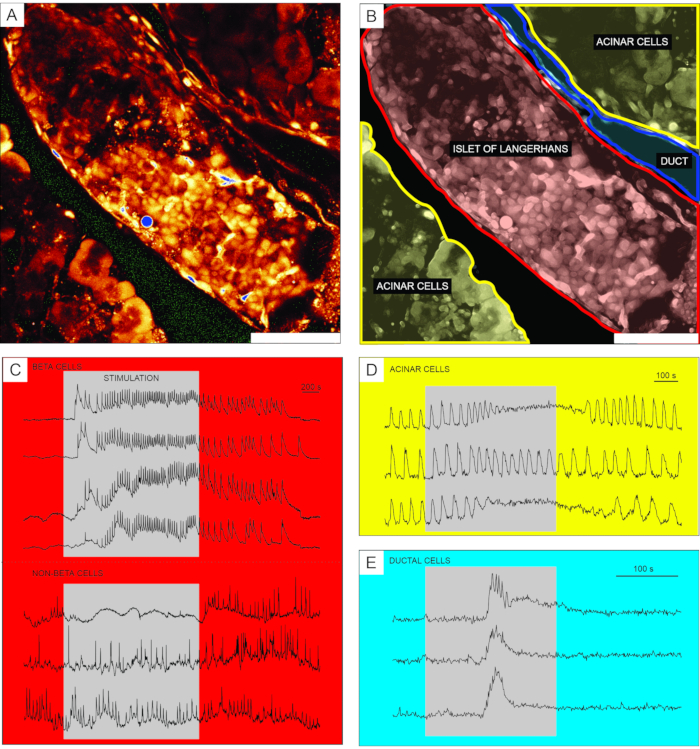
Рисунок 6: Репрезентативные результаты динамики кальция в различных типах клеток поджелудочной железы. (A) Изображение островка Лангерганса с высоким разрешением с окружающими тканями. Шкала = 100 мкм. (B) Разграничение отдельных частей ткани поджелудочной железы с ацинарной тканью, показанной желтым цветом, островком Лангерганса, показанным красным, и сегментом протокового дерева синим. Шкала bar = 100 мкм. (C) Типичные следы динамики кальция в бета- и предполагаемых небета-клетках при стимуляции глюкозой 12 мМ; 3 мМ глюкозы использовали для нестимулирующих состояний. Протоколы, которые могут быть использованы для более конкретной дискриминации небета-клеток, описаны в разделе обсуждения. (D) Типичный след кальциевой динамики ацинарных клеток, стимулируемых 25 нМ ацетилхолина. (E) Типичный след динамики кальция проточных клеток, стимулируемых 1 мМ хенодезоксихолевой кислоты. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
После успешной визуализации кальция данные сначала экспортируются и корректируются для отбеливания комбинацией экспоненциального и линейного соответствия, как описано в разделе протокола. Временные ряды до и после коррекции отбеливания представлены на рисунке 7А. После этого можно проанализировать несколько параметров в фазе активации и деактивации ответа, а также фазе плато. Задержка начала повышения [Ca2+]IC после стимуляции может быть измерена как представленная задержкойA на фиг.7B и неоднородностью задержек между отдельными клетками (задержкаA1). Те же параметры (задержкаD и задержкаD1) могут быть использованы для описания фазы деактивации. После начального переходного [Ca2+]IC повышения фаза плато в большинстве бета-клеток поджелудочной железы в островке характеризуется относительно регулярными высокочастотными [Ca2+]IC колебаниями. Фазу плато можно описать, проанализировав классические функциональные параметры. Схематическое представление длительности колебаний [Ca2+]IC , частоты и процента активного времени представлено на рисунке 7C. В кальциевой визуализации со скоростью захвата выше 10 Гц кальциевые волны, многократно распространяющиеся по островку, также могут быть четко распознаны (рисунок 7C).
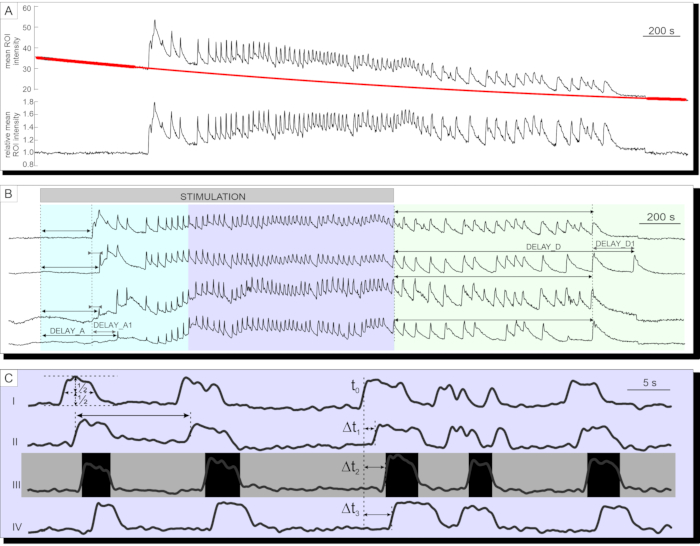
Рисунок 7: Анализ данных временных рядов. (A) Коррекция данных временных рядов для фотоотбеливания. (B) Анализ задержек активации после стимуляции и деактивации после прекращения стимуляции 12 мМ глюкозы. Длительность стимуляции обозначается светло-серой, затененной полосой на изображении. (C) Анализ нескольких параметров фазы плато: I) Длительность колебаний, определяемая на половинной высоте, II) частота колебаний, определяемая межколебательными интервалами. III) активное время как произведение частоты и длительности колебаний. I-IV) Задержки между колебаниями в любой данной волне колебаний, которые распространяются по островку Лангерганса, определяются задержками (Δt) во времени, при которых одна клетка достигает половинной высоты колебания. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Таблица 1. Пожалуйста, нажмите здесь, чтобы загрузить эту таблицу.
Обсуждение
Метод среза ткани поджелудочной железы является быстрым экспериментальным методом изучения морфологии и физиологии эндокринной и экзокринной частей поджелудочной железы в более законсервированном препарате in situ. Многие из преимуществ уже были отмечены во Введении. Стоит отметить, что в целом (т.е. не только для кальциевой визуализации) срезовый подход к изучению физиологии поджелудочной железы экономит время, поскольку не предполагает восстановительного периода после изоляции. Последнее не является абсолютно необходимым при всех типах экспериментов и использовании изолированных островков разных видов, но обычно используется для повышения чистоты, восстановления жизнеспособности и функциональности, а иногда и для сбора островков у нескольких доноров 59,60,61,62,63,64 . Однако в контексте визуализации кальция было обнаружено, что реакции бета-клеток зависят от продолжительности и условий культивирования, и это является важным источником вариаций, которые следует учитывать при использовании изолированных островков15,65. Тот же вопрос следует рассмотреть для срезов тканей, если их долгосрочная культивирование станет широко используемым вариантом в будущем22,36. Метод среза ткани также имеет высокий выход и, таким образом, потенциально уменьшает страдания животных и увеличивает статистическую мощность. Более того, как много ломтиков может быть получено от одного животного, так и потому, что ломтики выживают в течение длительных периодов времени, включая одно и то же животное или даже один и тот же островок как в экспериментальной, так и в контрольной группах, становится возможным.
Поскольку оригинальная архитектура и межклеточные коммуникации сохраняются, а также поскольку он совместим с рядом структурных анализов, электрофизиологических, методов визуализации и анализов секреции гормонов, этот метод особенно полезен для изучения функций поджелудочной железы, которые зависят от ненарушенных взаимодействий между отдельными клетками, например, чувствительности к секретагогам, паракринным и иммунным взаимодействиям между различными типами клеток, закономерности электрической активности, свойства динамики кальция, секреция различных гормонов. В частности, для визуализации кальция основными преимуществами использования срезов являются экспозиция островкового ядра и возможность получать сигналы от многих различных типов клеток с высоким разрешением. В зависимости от требований эксперимента и возраста животных толщина может варьироваться, срезы могут быть трансфектированы или получены от животных с генетически закодированными репортерами. Как более подробно объясняется ниже, последние два подхода также позволяют специфическую функциональную идентификацию и характеристику реакций от небета-клеток 31,66. Кроме того, островки из четко определенных частей органа могут быть изучены на предмет различий в отзывчивости или восприимчивости к заболеванию. Хотя они не требуют восстановительного инкубационного периода, их можно легко инкубировать с различными фармакологическими средствами, жирными кислотами, высоким содержанием глюкозы и цитокинами.
Самое главное, поскольку высокое разрешение достижимо в сочетании с одноклеточным или даже субклеточным разрешением, конфокальная визуализация кальция в срезах является одним из наиболее подходящих методов анализа кальциевых волн, функциональной связности и различных функциональных ролей клеток в отдельных частях островка54,67. Несмотря на ряд преимуществ, подход среза ткани имеет важные ограничения. Во-первых, это все еще, по крайней мере, частично нарушает островковую и экзокринную архитектуру, особенно на поверхности разреза, и меры предосторожности, такие как низкая температура, частый обмен растворами и мягкие и быстрые манипуляции, необходимы во время подготовки для предотвращения дополнительного механического и эндогенного ферментативного повреждения. Во-вторых, паттерны доставки питательных веществ и секретагога по-прежнему уступают пути in vivo, препарат отделен от системной иннервации, а межорганная обратная связь, например, между островком и его тканями-мишенями, невозможна, в отличие от подходов in vivo. В-третьих, максимальная толщина среза ограничена оксигенацией, доставкой питательных веществ и регулированием рН при ~ 200 мкм9. Кроме того, как подготовка срезов, так и визуализация требуют большой подготовки, а углубленный анализ данных кальция из длинных временных рядов и из многих клеток требует специальных знаний, которые часто не включены в инструментарий классического физиолога и требуют помощи физиков или специалистов по данным. Преимущество сохранения гомо- и гетеротипических взаимодействий также может усложнить анализ образцов из-за наличия сигналов от других клеток в интересующих областях. В зависимости от протоколов, активация других клеток может привести к косвенной дополнительной стимуляции или ингибированию наблюдаемой клетки.
Это может быть окончательно решено только с помощью подходов к деконволюции, более сложных протоколов стимуляции, включая вещества, которые блокируют некоторые косвенные эффекты, путем использования конкретных нокаутирующих животных и путем тщательного сравнения результатов с результатами других исследований, использующих более редукционистские методологии. Кроме того, если необходимы измерения секреции, следует иметь в виду, что некоторым срезам могут отсутствовать островки, а общая масса эндокринной ткани в одном срезе, как правило, низкая. Подготовка острых срезов ткани поджелудочной железы к визуализации включает в себя несколько критических этапов, обсуждаемых в следующих разделах и обобщенных в таблице 1, где читатель также может найти короткие, но важные советы по устранению неполадок. Во-первых, при приготовлении раствора агарозы порошок агарозы должен полностью раствориться, иначе нерастворенные частицы могут затруднить инъекцию. Держите однородный раствор агарозы при 37-45 °C, чтобы предотвратить затвердевание агарозы из-за слишком низкой температуры, с одной стороны, и предотвратить повреждение тканей из-за слишком высоких температур, с другой стороны. После использования оставшуюся агарозу можно хранить при 4 °C и повторно нагревать, хотя повторный повторный нагрев может привести к увеличению плотности из-за испарения воды, что в конечном итоге затрудняет или делает инъекцию невозможной.
Следующим критическим шагом в подготовке является правильное зажатие большого дуоденального сосочка. Белое пятно на двенадцатиперстной кишке указывает на соединение общего желчного протока и двенадцатиперстной кишки. Зажим, размещенный слишком проксимально, приведет к обструкции некоторых боковых поджелудочных ветвей общего протока, отключая инъекцию этих частей, тогда как зажим, размещенный слишком дистально, приведет к утечке агарозы через нижний путь сопротивления непосредственно в двенадцатиперстную кишку. Перед канюляцией общего желчного протока окружающая жировая ткань может быть аккуратно удалена для лучшей визуализации протока и большего контроля во время инъекции. Недостаточная точность при удалении окружающих тканей может привести к перфорации протока. Также важен выбор диаметра иглы, используемой для инъекции агарозы. У мышей предпочтительно используют иглу 30 Г; меньшие (32 или 33 г) иглы требуют больших усилий из-за высокой вязкости раствора агарозы и более склонны к обструкции. Однако, если они используются в сочетании с раствором агарозы более низкой плотности, они могут быть очень полезны для небольших штаммов мышей и молодых животных. В течение первых послеродовых дней агароза может быть альтернативно введена субкапсулярно, а не внутрипродукционно2. Использование игл с большим диаметром у мышей, скорее всего, приведет к повреждению общего желчного протока. Это также может произойти с правильным диаметром иглы, и щипцы могут помочь в удержании иглы на месте во время инъекции. Иглы большего диаметра могут быть единственным решением в случае больших протоков, как у крыс. Если игла слишком узкая, чтобы обеспечить плотное уплотнение, предотвращающее обратную утечку, лигатура может быть помещена вокруг нее при успешном входе в проток.
Инъекция агарозы требует некоторых усилий из-за вязкости раствора, и как только процесс инъекции начался, его не следует прерывать, так как раствор агарозы с низкой температурой плавления может затвердеть в игле или самых больших частях протокового дерева до завершения инъекции. Это приведет к плохому проникновению в ткани и худшей поддержке во время разреза. Проток всегда должен быть канюлят в точке, где соединяются левый печеночный проток и кистозный проток, образуя общий желчный проток. Если общий желчный проток становится перфорированным, многократно попробуйте канюлюгировать ближе к двенадцатиперстной кишке. Когда поджелудочная железа достаточно стабилизируется раствором агарозы и извлекается из брюшинной полости, разрезают небольшие кусочки хорошо вводимой ткани. Прежде чем встраивать их в агарозу, крайне важно удалить все жировые и соединительные ткани, поскольку их остатки делают нарезку более сложной. То же самое относится к кровеносным сосудам и остаткам протоков, за исключением случаев, когда они находятся в центре внимания эксперимента. В этом случае обязательно расположите их таким образом, чтобы было получено нужное поперечное сечение. При встраивании ткани в агарозу убедитесь, что температура соответствующая (37 ° C), и что ткань полностью окружена агарозой, так как силы во время нарезки вибратома могут вырвать ткань поджелудочной железы из блоков агарозы.
Быстрое высушивание тканевых блоков перед помещением их в агарозу путем их кратковременного размещения на бумажной салфетке может помочь предотвратить плохой контакт между тканью и агарозой на этом этапе. Во время затвердевания блоков агарозы поместите чашку Петри горизонтально и предотвратите контакт между тканью поджелудочной железы и дном чашки Петри. Если поджелудочная железа не полностью введена, процесс резки будет сложным. Поэтому постарайтесь уменьшить скорость резания, чтобы получить срезы ткани. Чтобы свести к минимуму повреждение клеток во время нарезки вибратома, регулярно заменяйте ECS (и кубики льда из ECS) в камере нарезки. Последний снизит активность ферментов поджелудочной железы, высвобождаемых из ацинарной ткани при нарезке. Толщина срезов также имеет решающее значение. Для динамики кальция и электрофизиологических экспериментов обычно разрезают 140 мкм срезы; однако, согласно цели исследования, толщина среза может варьироваться от 90 мкм до 200 мкм. Имейте в виду, что в более толстых срезах диффузия кислорода и питательных веществ будет ограничена, но они будут включать больше ткани. Кроме того, можно ожидать, что доля неразрезанных островков будет увеличиваться с увеличением толщины среза. Ломтики можно хранить в регулярно заменяемой ЭКС при комнатной температуре в течение нескольких часов или даже культивировать в соответствующей клеточной среде в течение нескольких дней; однако это может в конечном итоге повлиять на нормальную физиологию островковых клеток 3,22.
При приготовлении раствора красителя обеспечьте тщательное перемешивание всех компонентов и избегайте воздействия окружающего света. Срез поджелудочной железы состоит из многих клеточных слоев, и поглощение кальциевого красителя ограничено первыми несколькими наиболее поверхностными клеточными слоями, как описано ранее для изолированных островков58,68 и срезов гипофиза69. Однако, в отличие от изолированных островков, где окружающая капсула и внешние клеточные слои препятствуют проникновению красителя в более глубокие слои, срезы ткани обеспечивают доступ ко всей поверхности поперечного сечения островка, что позволяет одновременно измерять динамику кальция в сотнях клеток из всех слоев островка. Флуоресцентные индикаторы Ca2+ наиболее широко используются для измерения динамики кальция, и вместе с CLSM они позволяют записывать с высоким временным разрешением, достигающим нескольких сотен Гц. При выборе наиболее подходящего флуоресцентного индикатора Ca2+ учитывайте различные факторы, включая форму индикатора, которая влияет на метод загрузки ячейки, режим измерения (качественный или количественный) и константу диссоциации (Kd), которая должна находиться в интересующем диапазоне концентраций Ca2+ и зависит от pH, температуры, наличия Mg2+ и других ионов, а также связывание с белками. Поскольку сотовые сигналы Ca2+ обычно являются переходными, следует также учитывать константу скорости связывания Ca2+. Для измерения динамики [Ca2+]IC в клетках поджелудочной железы эта группа в основном использует клеточно-проницаемый индикаторный краситель Ca2+, описанный в этом протоколе (Таблица материалов), поскольку это длинноволновый индикатор с длинами волн излучения в спектре, где клеточная автофлуоресценция обычно менее проблематична, а энергия света возбуждения низкая, что снижает потенциал для клеточных фотоповреждений. Поскольку этот краситель флуоресцентный при низких концентрациях Ca2+, это облегчает определение исходного уровня [Ca2+]IC и увеличивает клеточную видимость перед стимуляцией. После связывания Ca2+ интенсивность флуоресценции красителя увеличивается в 14 раз, что позволяет обнаруживать даже незначительные изменения в [Ca2+]IC.
Для успешной визуализации кальция живыми клетками необходимо учитывать несколько важных аппаратных параметров, как описано в разделе протокола. Для визуализации живых клеток, где амплитуды сигнала низкие, а шансы фототоксичности высоки, объективы с более высоким NA предпочтительно используют для сбора большего количества света от образца. Если динамика кальция должна регистрироваться с высоким временным разрешением, используйте резонансный сканер вместо линейных гальванометров. Помимо выбора правильного объектива, использование высокочувствительных детекторов, таких как гибридные детекторы, которые требуют меньшей мощности лазера, позволяет избежать фототоксичности и фотоотбеливания. Это имеет особое значение для длительной визуализации кальция. Другими важными шагами в визуализации кальция являются настройки параметров качества изображения для получения временных рядов. Наиболее важными являются временное и пространственное разрешение. Поскольку динамика кальция сама по себе определяет наименьшее приемлемое временное разрешение, частота дискретизации должна быть, по крайней мере, в два раза выше ожидаемой частоты сигнала для обнаружения сигнала или даже в 10 раз выше, чтобы надежно обнаружить форму сигнала. При острых срезах ткани поджелудочной железы динамика кальция может быть измерена в сотнях клеток одновременно, и поэтому пространственное разрешение также важно. Это может быть улучшено за счет увеличения количества пикселей или за счет увеличения усреднения линии во время съемки в реальном времени. Однако из-за обратной зависимости между пространственным и временным разрешением необходим компромисс между обоими параметрами.
Если визуализация кальция должна быть выполнена в определенной клеточной популяции в поджелудочной железе, необходим стимул, способный функционально дифференцировать клетки внутри среза. Высокая глюкоза надежно и быстро активирует бета-клетки до колебательного паттерна, который накладывается на повышенный уровень кальция и высоко синхронизируется между всеми клетками в пределах островка 32,58,70. Бета-клетки являются наиболее многочисленным типом клеток в островке и расположены в основном в ядре островка у мышей. Тот же протокол стимуляции уменьшается и иногда существенно не изменяет разрыв в альфа-клетках 30,32,58,70,71,72. Для функционального различения альфа-клеток можно использовать низкую (3 мМ) глюкозу, глутамат или адреналин для увеличения их частоты или базальную [Ca2+]IC 21,72,73,74,75. Они составляют 10-20% островковых клеток и будут обнаружены на периферии островка1. Дельта-клетки также находятся на периферии. Они составляют всего ~ 5% от общего числа эндокринных клеток в островке и, как правило, активны в глюкозе 6 мМ и реагируют на стимуляцию глюкозы повышенной нерегулярной лопающей активностью от исходного уровня или слегка повышенным уровнем кальция 1,32,71,76. Грелин может быть использован для специфической стимуляции дельта-клеток 21,77,78,79 в экспериментах по визуализации кальция. Тем не менее, протоколы для специфической функциональной идентификации pp и epsilon клеток еще предстоит определить. Кроме того, 25 нМ ацетилхолин надежно активирует ацинарные клетки в разрывную активность 35,80,81. Кроме того, ряд других секретагов, таких как церуляин, холецистокинин и карбамилхолин, могут быть использованы для вызова реакций кальция в ацинарных клетках 22,40,82,83.
Наконец, 1 мМ хенодезоксихолевая кислота надежно вызывает кальциевые реакции в клетках протоков в срезах тканей; ангиотензин II, АТФ и некоторые другие секретагоги также могут быть использованы 11,23,84,85. Всякий раз, когда функциональная идентификация, основанная на характерных реакциях на специфические секретагоги и ингибиторы, недостаточна, генетически меченые животные31, трансфектированные клетки73 или иммуноцитохимия могут быть использованы для идентификации различных типов клеток 9,22,71,86 . За последние пару лет метод среза ткани был успешно адаптирован к тканям человека, открыв множество новых важных направлений исследований как в экзокрине41, так и в эндокринной физиологии 9,36,37,39. Интересно, что детальная оценка динамики кальция в островках человека была, как известно, трудной и еще предстоит исследовать более подробно87. В сочетании с передовой конфокальной микроскопией метод среза ткани поджелудочной железы позволил по-новому взглянуть на динамику кальция у мышей и, надеюсь, сделает то же самое для тканей человека.
Раскрытие информации
Авторы заявляют, что исследование проводилось при отсутствии какого-либо коммерческого или финансового интереса.
Благодарности
Работа, представленная в этом исследовании, была финансово поддержана Словенским исследовательским агентством (nos. П3-0396 и И0-0029, а также научно-исследовательские проекты Nos. J3-9289, N3-0048 и N3-0133) и Австрийским научным фондом / Fonds zur Förderung der Wissenschaftlichen Forschung (двусторонние гранты I3562--B27 и I4319--B30). Мы благодарим Марушу Рошер, Машу Чатер и Руди Млакара за отличную техническую помощь.
Материалы
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Analytical balance KERN ALJ 120-4 | KERN & SOHN GmbH | ALJ 160-4A | |
| Confocal microscope Leica TCS SP5 II Upright setup | Leica | 5100001578 | |
| Confocal microscope Leica TCS SP5 AOBS Tandem II setup | Leica | ||
| Cork pad 15 cm x 15 cm | |||
| Corning 15 mL centrifuge tubes | Merck KGaA, Darmstadt, Germany | CLS430790 | |
| Corning Round Ice Bucket with Lid, 4 L | Fischer Scientific, Leicestershire, UK | 432124 | |
| Double edge razor blade | Personna, USA | ||
| Dumont #5 - Fine Forceps | FST, Germany | 11254-20 | |
| Eppendorf Safe-Lock Tubes 0.5 mL | Eppendorf | 0030 121.023 | |
| Erlenmeyer flask 200 mL | IsoLab, Germany | 027.01.100 | |
| Fine Scissors - ToughCut | FST, Germany | 14058-11 | |
| Flat orbital shaker IKA KS 260 basic | IKA | Ident. No.: 0002980200 | |
| Glass lab bottle 1000 mL | IsoLab, Germany | 091.01.901 | |
| Hartman Hemostat, curved | FST, Germany | 13003-10 | |
| HCX APO L 20x/1.00 W HCX APO L (water immersion objective, 20x, NA 1.0) | Leica | 15507701 | |
| Measuring cylinder 25 mL | IsoLab, Germany | 015.01.025 | |
| Micromanipulator Control box SM-7, Keypad SM-7 | Luigs & Neumann | 200-100 900 7311, 200-100 900 9050 | |
| Microwave owen | Gorenje, Slovenia | MO20MW | |
| Osmometer Gonotec 010 | Gonotec, Berlin, Germany | OSMOMAT 010 Nr. 01-02-20 | |
| Paint brush | Faber-Castell, No.2 | Any thin soft round paint brush No.2, preferably black | |
| Paper towels | |||
| Perifusion pumps | Ismatec | ISM 827 | Reglo Analog MS - 4/8 |
| Petri dish 100/20 mm | Sarstedt | 83.3902 | |
| Petri dish 35/10 mm | Greiner bio-one | 627102 | |
| Petri dish 35 x 10 mm Nunclon Delta | Thermo Fischer Scientific, Waltham, MA USA | 153066 | NON-STICKY for agarose blocks |
| pH meter inoLab pH Level 1 | WTW, Weilheim, Germany | E163694 | |
| Pipette 1000 mL | Eppendorf | 3121 000.120 | |
| Pipette 50 mL | Eppendorf | 3121 000.066 | |
| Push pins 23 mm | Deli, Ningbo, China | E0021 | |
| Screw cap tube, 15 mL | Sarstedt | 62.554.502 | |
| Semken Forceps | FST, Germany | 11008-13 | |
| Stabilizing ring for Erlenmeyer flask | IsoLab, Germany | 027.11.048 | |
| Stereomicroscope Nikon SMZ 745 | Nikon, Melville, NY USA | ||
| Syringe Injekt Solo 5 mL | Braun, Melsungen, Germany | 4606051V | |
| Syringe needle 0.30 x 12 mm (30 G x 1/2") | Braun, Melsungen, Germany | 4656300 | |
| Temperature controller | Luigs & Neumann | 200-100 500 0150, 200-150-500-145 | Slice mini chamber, Temperature controller TC 07 |
| Tubings for perifusion system | Ismatec | SC0310 | Ismatec Pharmed 1.14 mm(ID) + silicone tubing 1.0 (ID) x 1.8 mm(OD) |
| Ultrasonic bath Studio GT-7810A | Globaltronics | ||
| Vibrotome Leica VT 1000 S | Leica, Nussloch, Germany | 14047235613 | |
| Volumetric flask 1000 mL | IsoLab, Germany | 013.01.910 | |
| Vortex mixer Neolab 7-2020 | Neolab | 7-2020 | |
| Water bath Thermo Haake open-bath circulator | Thermo Fisher Scientific | Z527912 | |
| Material/Reagent | |||
| Calcium chloride dihydrate - CaCl2.2H2O | Sigma Aldrich, Germany | C5080-500G | |
| D-(+)-glucose | Sigma Aldrich, Germany | G8270-1KG | |
| Dimethyl sulfoxide | Sigma Aldrich | D4540-100ML | |
| DL-lactic acid | Sigma Aldrich, Germany | L1250-500ML | |
| Dulbecco’s Phosphate Buffered Saline | Merck KGaA, Darmstadt, Germany | D8662-500ML | |
| Gas mixture containing 95% O2 and 5% CO2 at barometric pressure | |||
| Glue Wekem sekundenkleber WK-110 | Wekem GmbH, Bergkamen, Germany | WK 110-020 | |
| HEPES | Sigma Aldrich, Germany | H3375-250G | |
| L-(+)-ascorbic acid | Sigma Aldrich, Germany | A9,290-2 | |
| LIVE/DEAD Viability/Cytotoxicity Kit, for mammalian cells | Thermo Fischer Scientific, Waltham, MA USA | L3224 | |
| Magnesium chloride hexahydrate - MgCl2.2H2O | Sigma Aldrich, Germany | M2670-500G | |
| Myo-inositol | Sigma Aldrich, Germany | I5125-100G | |
| Oregon Green 488 BAPTA-1, AM | Invitrogen (Thermo FisherScientific) | O6807 | cell-permeable Ca2+ indicator (excitation/emission: 495/523 nm) |
| Pluronic F-127 (20% Solution in DMSO) | Invitrogen (Thermo Fisher Scientific) | P3000MP | polaxamer: nonionic triblock copolymer |
| Potassium chloride - KCl | Sigma Aldrich, Germany | 31248 | |
| SeaPlaque GTG agarose | Lonza, Rockland, USA | 50111 | |
| Sodium bicarbonate - NaHCO3 | Honeywell, Germany | 31437-500G | |
| Sodium chloride - NaCl | Honeywell, Germany | 31434-1KG | |
| Sodium hydroxide - NaOH | Sigma Aldrich, Germany | 30620 | |
| Sodium phosphate monobasic- NaH2PO4 | Sigma Aldrich, Germany | S0751-500G | |
| Sodium pyruvate | Sigma Aldrich, Germany | 15990-100G | |
| Software | |||
| FIJI | FIJI is an open source project | ||
| LASAF | Leica microsystems, Inc. | ||
| Matlab | Mathworks | ||
| Python | Python Software Foundation | Python is an open source project |
Ссылки
- Dolensek, J., Rupnik, M. S., Stozer, A. Structural similarities and differences between the human and the mouse pancreas. Islets. 7 (1), e1024405(2015).
- Meneghel-Rozzo, T., Rozzo, A., Poppi, L., Rupnik, M. In vivo and in vitro development of mouse pancreatic ß-cells in organotypic slices. Cell and Tissue Research. 316 (3), 295-303 (2004).
- Rozzo, A., Meneghel-Rozzo, T., Delakorda, S. L., Yang, S. B., Rupnik, M. Exocytosis of insulin: in vivo maturation of mouse endocrine pancreas. Annals of the New York Academy of the Sciences. 1152, 53-62 (2009).
- Dolenšek, J., Pohorec, V., Rupnik, M. S., Stožer, A. Pancreas physiology, challenges in pancreatic pathology. IntechOpen. Seicean, A. , (2017).
- Williams, J. A. The nobel pancreas: a historical perspective. Gastroenterology. 144 (6), 1166-1169 (2013).
- Lacy, P. E., Kostianovsky, M. Method for the isolation of intact islets of Langerhans from the rat pancreas. Diabetes. 16 (1), 35-39 (1967).
- Williams, J. A., Korc, M., Dormer, R. L. Action of secretagogues on a new preparation of functionally intact, isolated pancreatic acini. American Journal of Physiology. 235 (5), 517-524 (1978).
- Peikin, S. R., Rottman, A. J., Batzri, S., Gardner, J. D. Kinetics of amylase release by dispersed acini prepared from guinea pig pancreas. American Journal of Physiology. 235 (6), E743-E749 (1978).
- Marciniak, A., et al. Using pancreas tissue slices for in situ studies of islet of Langerhans and acinar cell biology. Nature Protocols. 9 (12), 2809-2822 (2014).
- Skelin, M., Rupnik, M., Cencic, A. Pancreatic beta cell lines and their applications in diabetes mellitus research. Altex-Alternatives to Animal Experimentation. 27 (2), 105-113 (2010).
- Molnar, R., et al. Mouse pancreatic ductal organoid culture as a relevant model to study exocrine pancreatic ion secretion. Laboratory Investigation. 100 (1), 84-97 (2020).
- Rupnik, M. The physiology of rodent beta-cells in pancreas slices. Acta Physiologica (Oxford, England). 195 (1), 123-138 (2009).
- Blinman, T. A., et al. Activation of pancreatic acinar cells on isolation from tissue: cytokine upregulation via p38 MAP kinase. American Journal of Physiology. Cell Physiology. 279 (6), C1993-C2003 (2000).
- Speier, S., Rupnik, M. A novel approach to in situ characterization of pancreatic ß-cells. Pflügers Archive: European Journal of Physiology. 446 (5), 553-558 (2003).
- Gilon, P., Jonas, J., Henquin, J. Culture duration and conditions affect the oscillations of cytoplasmic calcium concentration induced by glucose in mouse pancreatic islets. Diabetologia. 37 (10), 1007-1014 (1994).
- Huang, C., Gu, G. Effective isolation of functional islets from neonatal mouse pancreas. Journal of Visualized Experiments: JoVE. (119), e55160(2017).
- Szot, G. L., Koudria, P., Bluestone, J. A. Murine pancreatic islet isolation. Journal of Visualized Experiments: JoVE. (7), e255(2007).
- Qi, M., et al. Human pancreatic islet isolation: Part I: digestion and collection of pancreatic tissue. Journal of Visualized Experiments: JoVE. (27), e1125(2009).
- Qi, M., et al. Human pancreatic islet isolation: Part II: purification and culture of human islets. Journal of Visualized Experiments: JoVE. (27), e1343(2009).
- Stull, N. D., Breite, A., McCarthy, R., Tersey, S. A., Mirmira, R. G. Mouse islet of Langerhans isolation using a combination of purified collagenase and neutral protease. Journal of Visualized Experiments: JoVE. (67), e4137(2012).
- Hamilton, A., Vergari, E., Miranda, C., Tarasov, A. I. Imaging calcium dynamics in subpopulations of mouse pancreatic islet cells. Journal of Visualized Experiments: JoVE. (153), (2019).
- Marciniak, A., Selck, C., Friedrich, B., Speier, S. Mouse pancreas tissue slice culture facilitates long-term studies of exocrine and endocrine cell physiology in situ. PLoS ONE. 8 (11), e78706(2013).
- Gal, E., et al. A Novel in situ approach to studying pancreatic ducts in mice. Frontiers in Physiology. 10, 938(2019).
- Speier, S., Yang, S. B., Sroka, K., Rose, T., Rupnik, M. KATP-channels in beta-cells in tissue slices are directly modulated by millimolar ATP. Molecular and Cellular Endocrinology. 230 (1-2), 51-58 (2005).
- Speier, S., Gjinovci, A., Charollais, A., Meda, P., Rupnik, M. Cx36-mediated coupling reduces β-cell heterogeneity, confines the stimulating glucose concentration range, and affects insulin release kinetics. Diabetes. 56 (4), 1078-1086 (2007).
- Rose, T., Efendic, S., Rupnik, M. Ca2+-secretion coupling is impaired in diabetic Goto Kakizaki rats. The Journal of General Physiology. 129 (6), 493-508 (2007).
- Paulmann, N., et al. Intracellular serotonin modulates insulin secretion from pancreatic β-cells by protein serotonylation. PLoS Biology. 7 (10), e1000229(2009).
- Mandic, S. A., et al. Munc18-1 and Munc18-2 proteins modulate β-cell Ca2+ sensitivity and kinetics of insulin exocytosis differently. Journal of Biological Chemistry. 286 (32), 28026-28040 (2011).
- Dolensek, J., Skelin, M., Rupnik, M. S. Calcium dependencies of regulated exocytosis in different endocrine cells. Physiological Research. 60, S29-S38 (2011).
- Huang, Y. C., Rupnik, M., Gaisano, H. Y. Unperturbed islet α-cell function examined in mouse pancreas tissue slices. Journal of Physiology. 589 (2), 395-408 (2011).
- Huang, Y. C., et al. In situ electrophysiological examination of pancreatic α cells in the streptozotocin-induced diabetes model, revealing the cellular basis of glucagon hypersecretion. Diabetes. 62 (2), 519-530 (2013).
- Stožer, A., Dolenšek, J., Rupnik, M. S. Glucose-stimulated calcium dynamics in islets of Langerhans in acute mouse pancreas tissue slices. PLoS ONE. 8 (1), e54638(2013).
- Stožer, A., et al. Functional connectivity in islets of Langerhans from mouse pancreas tissue slices. PLoS Computational Biology. 9 (2), e1002923(2013).
- Dolenšek, J., Stožer, A., Skelin Klemen, M., Miller, E. W., Slak Rupnik, M. The relationship between membrane potential and calcium dynamics in glucose-stimulated beta cell syncytium in acute mouse pancreas tissue slices. PLoS ONE. 8 (12), e82374(2013).
- Perc, M., Rupnik, M., Gosak, M., Marhl, M. Prevalence of stochasticity in experimentally observed responses of pancreatic acinar cells to acetylcholine. Chaos. 19 (3), 037113(2009).
- Qadir, M. M. F., et al. Long-term culture of human pancreatic slices as a model to study real-time islet regeneration. Nature Communications. 11 (1), 3265-3265 (2020).
- Panzer, J. K., et al. Pancreas tissue slices from organ donors enable in situ analysis of type 1 diabetes pathogenesis. JCI Insight. 5 (8), e134525(2020).
- Cohrs, C. M., et al. Vessel network architecture of adult human islets promotes distinct cell-cell interactions in situ and is altered after transplantation. Endocrinology. 158 (5), 1373-1385 (2017).
- Cohrs, C. M., et al. Dysfunction of persisting beta cells is a key feature of early type 2 diabetes pathogenesis. Cell Reports. 31 (1), 107469(2020).
- Dolai, S., et al. Pancreatitis-induced depletion of syntaxin 2 promotes autophagy and increases basolateral exocytosis. Gastroenterology. 154 (6), 1805-1821 (2018).
- Liang, T., et al. Ex vivo human pancreatic slice preparations offer a valuable model for studying pancreatic exocrine biology. Journal of Biological Chemistry. 292 (14), 5957-5969 (2017).
- Panzer, J. K., Cohrs, C. M., Speier, S. Using pancreas tissue slices for the study of islet physiology. Methods in Molecular Biology. 2128, 301-312 (2020).
- Klemen, M., Dolenšek, J., Stožer, A., Rupnik, M. Exocytosis Methods. Thorn, P. 7, Humana Press. 127-146 (2014).
- Speier, S. Experimental approaches for high-resolution in vivo imaging of islet of Langerhans biology. Current Diabetes Reports. 11 (5), 420-425 (2011).
- Leibiger, I. B., Berggren, P. O. Intraocular in vivo imaging of pancreatic islet cell physiology/pathology. Molecular Metabolism. 6 (9), 1002-1009 (2017).
- Reissaus, C. A., et al. A Versatile, portable intravital microscopy platform for studying beta-cell biology in vivo. Scientific Reports. 9 (1), 8449(2019).
- Jacob, S., et al. In vivo Ca(2+) dynamics in single pancreatic beta cells. FASEB Journal. 34 (1), 945-959 (2020).
- Fernandez, J., Valdeolmillos, M. Synchronous glucose-dependent [Ca2+]i oscillations in mouse pancreatic islets of Langerhans recorded in vivo. FEBS Letters. 477 (1-2), 33-36 (2000).
- Almaca, J., Weitz, J., Rodriguez-Diaz, R., Pereira, E., Caicedo, A. The pericyte of the pancreatic islet regulates capillary diameter and local blood flow. Cell Metabolism. 27 (3), 630-644 (2018).
- Weitz, J. R., et al. Mouse pancreatic islet macrophages use locally released ATP to monitor beta cell activity. Diabetologia. 61 (1), 182-192 (2018).
- Tian, G., Sandler, S., Gylfe, E., Tengholm, A. Glucose- and hormone-induced cAMP oscillations in α- and β-cells within intact pancreatic islets. Diabetes. 60 (5), 1535-1543 (2011).
- Benninger, R. K., Zhang, M., Head, W. S., Satin, L. S., Piston, D. W. Gap junction coupling and calcium waves in the pancreatic islet. Biophysical Journal. 95 (11), 5048-5061 (2008).
- Santos, R. M., et al. Widespread synchronous Ca oscillations due to bursting electrical activity in single pancreatic islets. Pflügers Archive: European Journal of Physiology. 418 (4), 417-422 (1991).
- terk, M., et al. Assessing the origin and velocity of Ca2+ waves in three-dimensional tissue: Insights from a mathematical model and confocal imaging in mouse pancreas tissue slices. Communications in Nonlinear Science and Numerical Simulation. 93, 105495(2021).
- Gosak, M., et al. Critical and supercritical spatiotemporal calcium dynamics in beta cells. Frontiers in Physiology. 8, 1106(2017).
- Satin, L. S., Butler, P. C., Ha, J., Sherman, A. S. Pulsatile insulin secretion, impaired glucose tolerance and type 2 diabetes. Molecular Aspects in Medicine. 42, 61-77 (2015).
- Tengholm, A., Gylfe, E. Oscillatory control of insulin secretion. Molecular and Cellular Endocrinology. 297 (1-2), 58-72 (2009).
- Quesada, I., et al. Glucose induces opposite intracellular Ca2+ concentration oscillatory patterns in identified α- and β-cells within intact human islets of Langerhans. Diabetes. 55 (9), 2463-2469 (2006).
- Ferguson, J., Allsopp, R. H., Taylor, R. M., Johnston, I. D. Isolation and long term preservation of pancreatic islets from mouse, rat and guinea pig. Diabetologia. 12 (2), 115-121 (1976).
- Andersson, A. Isolated mouse pancreatic islets in culture: effects of serum and different culture media on the insulin production of the islets. Diabetologia. 14 (6), 397-404 (1978).
- Ramirez-Dominguez, M. Isolation of mouse pancreatic islets of Langerhans. Advances in Experimental Medicine and Biology. 938, 25-34 (2016).
- Carter, J., Dula, S., Corbin, K., Wu, R., Nunemaker, C. A practical guide to rodent islet isolation and assessment. Biological Procedures Online. 11 (1), 3-31 (2009).
- Daoud, J., Rosenberg, L., Tabrizian, M. Pancreatic islet culture and preservation strategies: advances, challenges, and future outlook. Cell Transplantation. 19 (12), 1523-1535 (2010).
- Zawalich, W. S., Yamazaki, H., Zawalich, K. C. Biphasic insulin secretion from freshly isolated or cultured, perifused rodent islets: comparative studies with rats and mice. Metabolism. 57 (1), 30-39 (2008).
- Roe, M. W., et al. Absence of effect of culture duration on glucose-activated alterations in intracellular calcium concentration in mouse pancreatic islets. Diabetologia. 38, 876-877 (1995).
- Shuai, H., Xu, Y., Yu, Q., Gylfe, E., Tengholm, A. Fluorescent protein vectors for pancreatic islet cell identification in live-cell imaging. Pflügers Archive. European Journal of Physiology. 468 (10), 1765-1777 (2016).
- Dolenšek, J., et al. Glucose-dependent activation, activity, and deactivation of beta cell networks in acute mouse pancreas tissue slices. bioRxiv. , (2020).
- QZhang, Q., et al. Cell coupling in mouse pancreatic beta-cells measured in intact islets of Langerhans. Philosophical Transactions. Series A, Mathematical, Physical, and Engineering Sciences. 366 (1880), 3503-3523 (2008).
- Sánchez-Cárdenas, C., Hernández-Cruz, A. GnRH-induced Ca2+-signalling patterns in mouse gonadotrophs recorded from acute pituitary slices in vitro. Neuroendocrinology. 91 (3), 239-255 (2010).
- Asada, N., Shibuya, I., Iwanaga, T., Niwa, K., Kanno, T. Identification of alpha- and beta-cells in intact isolated islets of Langerhans by their characteristic cytoplasmic Ca2+ concentration dynamics and immunocytochemical staining. Diabetes. 47 (5), 751-757 (1998).
- Nadal, A., Quesada, I., Soria, B. Homologous and heterologous asynchronicity between identified α-, β- and δ-cells within intact islets of Langerhans in the mouse. Journal of Physiology. 517 (1), 85-93 (1999).
- Shuai, H., Xu, Y., Yu, Q., Gylfe, E., Tengholm, A. Fluorescent protein vectors for pancreatic islet cell identification in live-cell imaging. Pflugers Archive: European Journal of Physiology. 468 (10), 1765-1777 (2016).
- Cabrera, O., et al. Glutamate is a positive autocrine signal for glucagon release. Cell Metabolism. 7 (6), 545-554 (2008).
- Li, J., et al. Submembrane ATP and Ca2+ kinetics in α-cells: unexpected signaling for glucagon secretion. FASEB Journal. 29 (8), 3379-3388 (2015).
- Hamilton, A., et al. Adrenaline stimulates glucagon secretion by Tpc2-dependent Ca(2+) mobilization from acidic stores in pancreatic α-cells. Diabetes. 67 (6), 1128-1139 (2018).
- Arrojo, E. D. R., et al. Structural basis for delta cell paracrine regulation in pancreatic islets. Nature Communications. 10 (1), (2019).
- DiGruccio, M. R., et al. Comprehensive alpha, beta and delta cell transcriptomes reveal that ghrelin selectively activates delta cells and promotes somatostatin release from pancreatic islets. Molecular Metabolism. 5 (7), 449-458 (2016).
- Adriaenssens, A. E., et al. Transcriptomic profiling of pancreatic alpha, beta and delta cell populations identifies delta cells as a principal target for ghrelin in mouse islets. Diabetologia. 59 (10), 2156-2165 (2016).
- Rorsman, P., Huising, M. O. The somatostatin-secreting pancreatic δ-cell in health and disease. Nature reviews. Endocrinology. 14 (7), 404-414 (2018).
- Petersen, C. C., Toescu, E. C., Petersen, O. H. Different patterns of receptor-activated cytoplasmic Ca2+ oscillations in single pancreatic acinar cells: dependence on receptor type, agonist concentration and intracellular Ca2+ buffering. The EMBO journal. 10 (3), 527-533 (1991).
- Thorn, P., Lawrie, A. M., Smith, P. M., Gallacher, D. V., Petersen, O. H. Local and global cytosolic Ca2+ oscillations in exocrine cells evoked by agonists and inositol trisphosphate. Cell. 74 (4), 661-668 (1993).
- Behrendorff, N., Floetenmeyer, M., Schwiening, C., Thorn, P. Protons released during pancreatic acinar cell secretion acidify the lumen and contribute to pancreatitis in mice. Gastroenterology. 139 (5), e1711-e1715 (2010).
- Criddle, D. N., et al. Cholecystokinin-58 and cholecystokinin-8 exhibit similar actions on calcium signaling, zymogen secretion, and cell fate in murine pancreatic acinar cells. American Journal of Physiology. Gastrointestinal and Liver Physiology. 297 (6), G1085-G1092 (2009).
- Venglovecz, V., et al. Effects of bile acids on pancreatic ductal bicarbonate secretion in guinea pig. Gut. 57 (8), 1468-3288 (2008).
- Maleth, J., Hegyi, P. Calcium signaling in pancreatic ductal epithelial cells: an old friend and a nasty enemy. Cell Calcium. 55 (6), 337-345 (2014).
- Nadal, A., Quesada, I., Soria, B. Homologous and heterologous asynchronicity between identified alpha-, beta- and delta-cells within intact islets of Langerhans in the mouse. Journal of Physiology. 517 (Pt 1), 85-93 (1999).
- Skelin Klemen, M., Dolenšek, J., Slak Rupnik, M., Stožer, A. The triggering pathway to insulin secretion: Functional similarities and differences between the human and the mouse β cells and their translational relevance. Islets. 9 (6), 109-139 (2017).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены