Method Article
Нормотермическая перфузия поджелудочной железы ex vivo для сохранения аллотрансплантатов поджелудочной железы перед трансплантацией
В этой статье
Резюме
Нормотермическая аппаратная перфузия ex vivo (NEVP) практически не исследовалась для сохранения аллотрансплантатов поджелудочной железы. Мы представляем инновационную методику консервации аллотрансплантатов поджелудочной железы перед трансплантацией.
Аннотация
Трансплантация поджелудочной железы (PTx) является лечебным лечением для людей, которые живут с бременем диагноза сахарного диабета (СД). Однако из-за нехватки органов и растущего числа пациентов, включенных в список для PTx, необходимы новые стратегии для увеличения количества доступных трансплантатов для трансплантации.
Статическое холодное хранение (SCS) считается золотым стандартом для стандартных критериев органов. Тем не менее, доноров со стандартными критериями (SCD) становится все меньше, и срочно необходимы новые стратегии, которые могут повысить скорость принятия органов от доноров с расширенными критериями (ECD).
Нормотермическая перфузия ex vivo (NEVP) — одна из стратегий, которая становится все более популярной за последние пару десятилетий. Этот метод сохранения уже успешно использовался в других органах (печень, почки и легкие), но был минимально изучен при трансплантации поджелудочной железы. Несколько статей, описывающих метод лечения поджелудочной железы, показывают небольшой успех, отек является одной из основных проблем. В следующей рукописи описывается успешный метод и установка NEVP, разработанные нашей группой для перфузии поджелудочной железы свиней.
Введение
Согласно Национальному статистическому отчету о диабете, в 2019 году в Соединенных Штатах проживало в общей сложности 28,7 миллиона человек с диагнозом диабета. Примерно у 1,8 миллиона из них был диагностирован диабет 1типа. PTx в настоящее время является наиболее эффективным и единственным лечебным средством для лечения осложненного сахарного диабета 1 типа2 и является процедурой, которая увеличивает продолжительность и качество жизни этих пациентов3.
Поджелудочная железа является наиболее часто выбрасываемым органом после извлечения от умерших доноров4. В связи с продолжающейся нехваткой органов и увеличением времени ожидания центры трансплантации используют больше трансплантатов поджелудочной железы из ECD, включая донорство после смерти от кровообращения (DCD)5. Необходимы стратегии безопасного сохранения, перфузии, оценки и восстановления аллотрансплантатов, поступающих от доноров с расширенными критериями.
НЭВП доказал свою эффективность в сохранении легких6, печени 7,8 и почечных трансплантатов 9,10. Однако количество групп, работающих над аппаратной перфузией поджелудочной железы, как гипотермической, так и нормотермической, а также количество публикаций немногочисленны и ограничены из-за отека трансплантата и травмы11,12,13,14.
Целью данного исследования является представление протокола нормотермической перфузии поджелудочной железы ex vivo (NEVPP) с использованием модели свиньи с целью в конечном итоге обеспечить платформу для длительного сохранения, оценки и восстановления органов перед трансплантацией. Это позволит другим исследовательским группам создать перфузионную модель для изучения аллотрансплантатов поджелудочной железы.
протокол
Все животные, использованные для этого исследования, получали гуманный уход в соответствии с «Принципами ухода за лабораторными животными», сформулированными Национальным обществом медицинских исследований, и «Руководством по уходу за лабораторными животными», опубликованным Национальными институтами здравоохранения, Онтарио, Канада. Все исследования были одобрены Комитетом по уходу за животными Общего научно-исследовательского института Торонто.
ПРИМЕЧАНИЕ: Этот протокол исследования основан на модели свиней. Трансплантат хранится в холоде в течение 2 ч, а затем подвергается нормотермической машинной перфузии в течение 3 ч до трансплантации (рис. 1).
1. Животные
- Используют самцов йоркширских свиней (40-50 кг).
2. Закупка органов
ПРИМЕЧАНИЕ: Предоперационная процедура и часть хирургической процедуры такие же, как и в предыдущих статьях, опубликованных нашей группой15 , и заключаются в следующем:
- Размещайте свиней в исследовательском центре не менее 7 дней, чтобы обеспечить акклиматизацию и снизить уровень стресса.
- Голодайте свиньям не менее 6 часов до введения анестезии.
- Успокоите свинью внутримышечной (IM) инъекцией мидазолама (0,15 мг/кг), кетамина (25 мг/кг) и атропина (0,04 мг/кг).
ПРИМЕЧАНИЕ: Это делается в жилом комплексе. - Переведите животное из помещения содержания в операционную (операционную), где будет выполнено извлечение органа.
- Положите свинью в положение лежа на спине на операционном столе и наденьте маску для лица с 2 л кислорода и 5% изофлурана, пока челюсть не расслабится.
- Визуализируйте голосовые связки с помощью ларингоскопа и опрыскайте их 2% лидокаином, чтобы предотвратить спазм во время интубации. Замените маску кислородом и изофлураном не менее чем на 30 секунд перед попыткой интубации.
- Введите эндотрахеальную трубку диаметром 7 мм и заблокируйте манжету 5 мл воздуха. Используйте капнометрию, чтобы убедиться, что трубка находится в правильном положении.
- Уменьшите содержание газа изофлурана до 2,5%. Включите аппарат искусственной вентиляции легких и установите его на 15-20 вдохов в минуту и дыхательный объем на 10-15 мл / кг массы тела. Постоянно контролируйте частоту сердечных сокращений и насыщение кислородом.
- Используя технику Сельдингера 16, введите катетер размером 8,5 Fr. x10 см в яремную вену (правую или левую).
- Используйте катетер яремной вены, чтобы начать инфузию фентанила (2,5 мл в 500 мл Рингера) со скоростью 250 мл / час.
- Проверьте мышечные рефлексы, чтобы определить глубину анестезии. Тонус челюсти является самым надежным мышечным рефлексом 17.
ПРИМЕЧАНИЕ: Если отмечается ригидность нижнечелюстных мышц, увеличьте инфузию изофлурана и/или фентанила.
3. Хирургическое вмешательство
- Продезинфицируйте и накройте операционное поле. Выполните разрез по средней линии от ксифоидной кости до лобкового симфиза. Расширьте операционное поле левым боковым разрезом для лучшего воздействия.
- Рассекают нижнюю полую вену (НПВ) от брюшной аорты. Далее освобождают аорту от окружающих тканей и перевязывают мелкие поясничные ветви аорты. Определите и поместите лигатуры вокруг обеих почечных артерий.
ПРИМЕЧАНИЕ: Лигатуры не должны быть завязаны в этот момент времени. - Как только задняя часть аорты освободится, проведите вокруг нее две лигатуры. Нижняя лигатура в конечном итоге будет перевязана чуть выше бифуркации подвздошной артерии, а верхняя лигатура будет перевязана на 5 см выше предыдущей связки.
- Рассеките печеночный очаг. Свяжите все артерии как можно ближе к печени. Определите общий желчный проток, поместите две лигатуры близко к печени и разделите структуру.
- Рассеките вокруг аорты, но не разрезайте в этот момент времени. Определите и рассеките вокруг надпеченочной части аорты и наложите на нее галстук.
ПРИМЕЧАНИЕ: Лигатуры не должны быть завязаны в этот момент времени. - Откройте малый мешок, чтобы лед охладил поджелудочную железу. Мобилизуйте поджелудочную железу как можно меньше перед промыванием.
- Вводят 500 МЕ гепарина на кг донорской массы через центральную линию. Подождите 5 минут и начните сбор крови в пакеты с цитратом, фосфатом, декстрозой, физиологическим раствором, аденином, глюкозой и маннитом (CPD/SAG-M) с помощью яремного катетера.
- Перевяжите нижнюю лигатуру аорты, канюляцию аорты линией заподлицо над бифуркационной стяжкой подвздошной кости и закрепите канюлю верхней завязкой. Перевязывают обе почечные артерии.
- Перевяжите надпеченочную аорту (перекрестный зажим) после того, как будет собрано достаточное количество крови (600 мл). Введите 10 мл хлорида калия для жертвоприношения.
- Инициируйте промывку раствором для консервации Университета Висконсина (UW). Вырежьте отверстие в воротной вене (как можно выше) и каву для вентиляции. Поместите лед в брюшную полость.
- Оцените С-образную петлю поджелудочной железы и двенадцатиперстной кишки после промывания 1 л раствора UW. При достаточном промывании приступают к рассечению, выявлению и пережатию брыжеечных сосудов. Замедлите промывку для второго литра UW.
- Извлеките трансплантат поджелудочной железы и сегмент полой или подвздошной вены для расширения воротной вены.
ПРИМЕЧАНИЕ: Трансплантат поджелудочной железы удаляется вместе с селезенкой. - Поместите орган в органный мешок, который помещается в бассейн, наполненный льдом.
4. Подготовка трансплантата поджелудочной железы за задним столом (рис. 2А)
- Удалите линию смыва с дистальной части аорты и закройте галстуком. Наполните органный мешок оставшимся раствором UW. Освободите поджелудочную железу от слипшихся тканей, в том числе селезенки.
- Выполните расширение воротной вены с использованием ранее восстановленной полой или подвздошной вены с проленом 6-0. Канюляция воротной вены и проксимального отдела аорты с помощью редуктора 1/4 дюйма x 3/8 дюйма.
- Канюляция дистальной части двенадцатиперстной кишки с помощью катетера Malecot и галстука. Зажмите конец катетера, чтобы избежать пролития содержимого двенадцатиперстной кишки. Наблюдал за брыжеечными сосудами с 4-0 Проленом.
- Зарегистрируйте вес трансплантата. Храните привой в статическом холодильном хранилище (SCS) до начала НЭЭС.
5. Нормотермическая перфузия поджелудочной железы ex vivo (NEVPP)
ПРИМЕЧАНИЕ: Перфузионный контур выполнен из неонатального сердечно-легочного шунтирования (рис. 3).
- Присоедините соответствующую трубку к оксигенатору и к венозному резервуару, а также артериальную линию к оттоку оксигенатора и поместите пузырьковый фильтр в его держатель. Подсоедините линию продувки, идущую от пузырькового фильтра, к венозному резервуару. Откройте крышку пузырькового фильтра, чтобы выпустить весь воздух.
- Соедините венозную линию с входом в венозный резервуар. Подсоедините диализный фильтр и трубку, в которую будет вливаться диализат. Подключите датчик расходомера, линии давления и датчик температуры. Подсоедините линии для отбора артериальных и венозных проб к портам для образцов.
- Поместите камеру поджелудочной железы (рис. 3) на стол Майонеза и введите артериальную и венозную трубку через отверстия, предназначенные для этой цели. Подключите и включите внешний нагревательный блок.
- Поместите всасывающую трубку внутрь роликового насоса и подсоедините один конец к трубке, выходящей из камеры, для сбора жидкости, а другой конец к венозному резервуару, чтобы собрать все потери перфузата.
- Подсоедините кислородную трубку (зеленую) к газовому баллону, содержащему углеводную смесь (95% O 2/5% CO2) и оксигенатору. Подсоедините трубку насосного агрегата нагревателя к оксигенатору.
- Зажимают линии артериального и венозного оттока, а также оттока венозного резервуара.
6. Подготовка перфузата и грунтовка контура
- Наполните венозный резервуар перфузатом (табл. 1).
- Используйте один шприцевой насос для непрерывного введения вазодилататора (эпопростенола) в дозе 8 мл / ч в артериальную линию. Используйте второй шприцевой насос для непрерывного введения ингибитора фермента непосредственно в венозный резервуар (15 мг, 10 мл / ч).
- Включите аппарат искусственного кровообращения (HLM) и включите панели давления, температуры и таймера. Включите насос нагревателя, чтобы нагреть перфузионный раствор до 38 °C. Откройте подачу O 2 / CO2.
- Снимите зажим трубки, расположенный на выходе из венозного резервуара, запустите центробежный насос и разгоните его до 1,500 об/мин. Зажмите трубку, минуя артериальный фильтр, и выпустите воздух из артериального фильтра. Обнулите линии артериального и венозного давления.
7. Перфузия трансплантата поджелудочной железы (рис. 2B)
- Откройте органный мешок, где хранится поджелудочная железа. Промыть 200 мл альбумина через артериальную канюлю. Извлеките поджелудочную железу изо льда и расположите внутри камеры органа. Убедитесь, что артериальная и венозная трубки свободны от воздуха.
- Отпустите зажим со стороны артерии и зажмите короткий путь между артериальной и венозной трубкой. Как только кровь начнет выходить из артериальной трубки, подключите линию к артериальной канюле. Установите артериальное давление на 20-25 мм рт.ст., регулируя скорость центробежного насоса. Подключите венозную трубку, как только кровь начнет выходить из венозной канюли.
- Вводите один флакон верапамила (2,5 мг / мл) непосредственно на артериальную сторону, когда поджелудочная железа полностью соединена и серьезных кровотечений не наблюдается.
- Непрерывно регистрируйте давление, артериальный кровоток, температуру и секрецию двенадцатиперстной кишки. Собирайте кровь, записывайте выход двенадцатиперстной кишки каждый час и ежечасно макроскопически оценивайте отек. Запишите параметры перфузии и возьмите образцы для анализа (образцы газов венозной и артериальной крови, а также образцы на амилазу, липазу и ЛДГ).
- Отсоедините артериальную и венозную трубки, когда перфузия закончится, извлеките трансплантат из камеры органа, промойте холодным UW и взвесьте. Храните трансплантат на льду в стерильном органном пакете до момента трансплантации.
Результаты
Предстоящие данные показывают репрезентативные результаты семи экспериментов с использованием модели извлечения донорской поджелудочной железы с сердцебиением. После канюляции аорты, промывки раствором UW и извлечения поджелудочной железы трансплантаты держали на ГКС в течение 2 часов, пока готовили эритроциты. НЭЭС выполнялась в этой модели в течение 3 часов, что мы считали наименьшим количеством времени, необходимым для перфузии, если оценка и восстановление трансплантата планируется в будущем. Образцы и измерения регистрировались в часовые сроки. (0 = исходный уровень, сразу после подключения органа к цепи, 1 = 1 ч, 2 = 2 ч, 3 = 3 ч).
Трансплантаты поджелудочной железы были помещены в камеру органа, которая была специально разработана для этой цели и включает в себя нагреватель (дополнительный файл). Целью НЭЭС является обеспечение околофизиологической среды для органа. Для этого артериальное давление было установлено в пределах 20-25 мм рт.ст. при всех перфузиях. Давление и расход измерялись на протяжении всей перфузии и оставались стабильными (рис. 4). Метаболическую активность оценивали путем расчета потребления кислорода трансплантатом по следующей формуле: [(pO 2 art-pO2ven) *поток / вес] (рис. 5). Измерения pH, натрия, кальция и HCO3 находились в пределах физиологических значений в течение всей перфузии (рис. 6). Уровни лактата и калия снижались во время перфузии и достигали близких к норме значений через 3 ч (рис. 7). Поскольку схема представляет собой замкнутую систему, ожидается, что уровни амилазы и липазы будут увеличиваться во время перфузии (рис. 8). Однако увеличение уровней, по-видимому, не коррелирует с повреждением трансплантата (рис. 9). Полуколичественная шкала использовалась для оценки некроза жира и паренхимы, а также целостности островковых клеток. (0 - без изменений, 1 - легкие изменения, 2 - умеренные изменения, 3 - тяжелые изменения). Это было сделано патологоанатомом, слепым к экспериментальным группам, и никаких признаков панкреатита не наблюдалось.
Аллотрансплантаты поджелудочной железы взвешивали до и после перфузии для оценки отека (табл. 2).
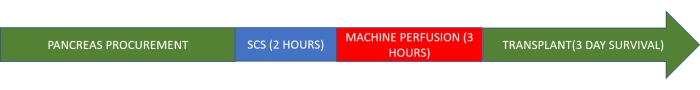
Рисунок 1. Протокол исследования. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 2. Поджелудочная железа до и после перфузии. (А) Перед перфузией. (Б) После перфузии. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
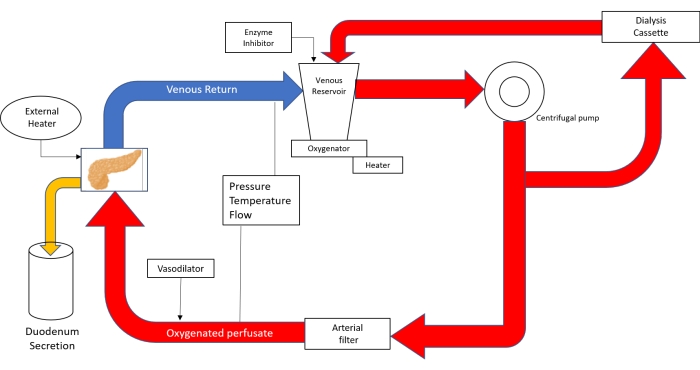
Рисунок 3. Схематический чертеж перфузионного контура. С применением технологии неонатального искусственного кровообращения; Перфузат вливается в венозный резервуар, а затем с помощью центробежного насоса перемещается в оксигенатор. После выхода из оксигенатора контур делится на трубку, которая отправляет перфузат в диализную кассету и обратно в резервуар, и трубку, которая идет к артериальному фильтру. После прохождения артериального пузырькового фильтра перфузат с давлением 20-25 мм рт.ст. через аорту в поджелудочную железу. Венозный отток приводит перфузат обратно в венозный резервуар. (Адаптировано из 18). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
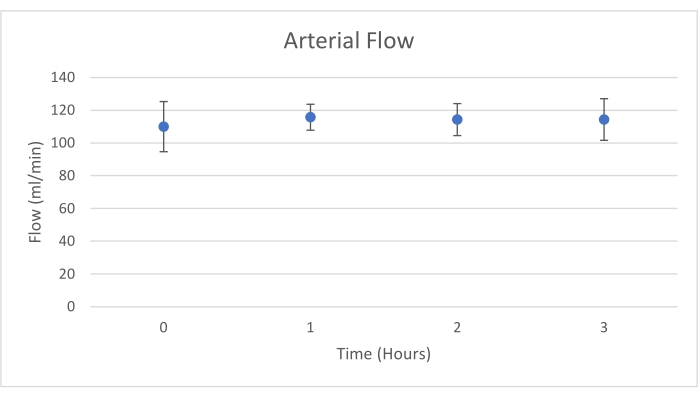
Рисунок 4. Средний артериальный кровоток со стандартным отклонением (мл/мин). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
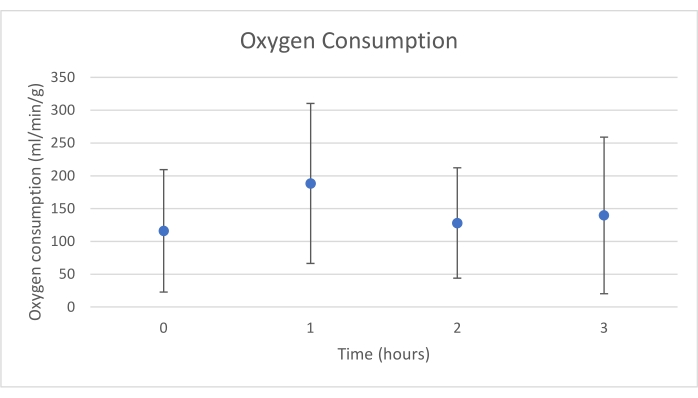
Рисунок 5. Среднее потребление кислорода со стандартным отклонением (мл/мин/г). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
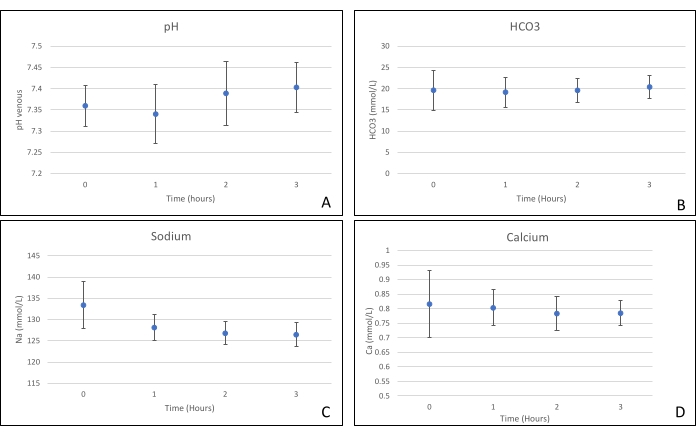
Рисунок 6. (A) Средние измерения pH, (B) HCO3, (C) натрия и (D) кальция со стандартными отклонениями. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
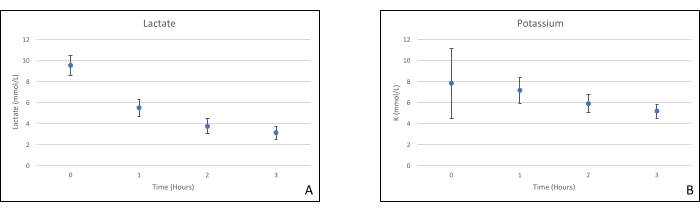
Рисунок 7. (A) Средние измерения лактата и (B) калия со стандартными отклонениями. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
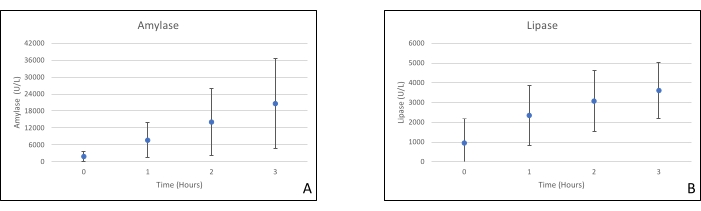
Рисунок 8. (A) Средние измерения амилазы и (B) липазы со стандартными отклонениями. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
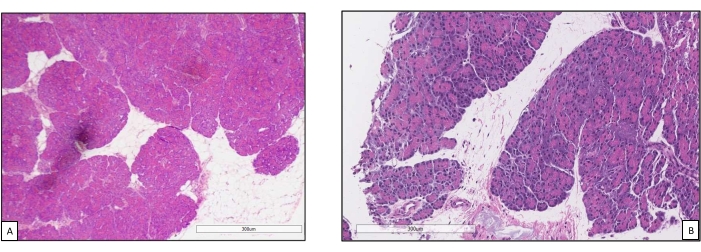
Рисунок 9. Основные биопсии до и после перфузии. (A) Нормальная паренхима поджелудочной железы до машинной перфузии18. (B) Постперфузионная биопсия с хорошей сохранностью ацинусов поджелудочной железы и островковых клеток. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
| Ингредиент | Количество |
| Лактат Рингера | 260 мл |
| Раствор Стина | 195 мл |
| Промытые эритроциты | 162,5 мл |
| Вода двойного обратного осмоса (DRO) | 35 мл |
| Гепарин (10000 МЕ / 10 мл) | 1,3 мл |
| Бикарбонат натрия (8.4%) | 10,4 мл |
| Глюконат кальция (10%) | 1,3 мл |
| Метилпреднизолон (Солу-Медрол) | 325 мг |
| Апротинин | 15 мг |
Таблица 1. Перфузатный состав.
| Вес до | Вес после | Прибыль | Разница в % | |
| Кейс 1 | 244 г | 240 г | -4 г | -1.63 |
| Кейс 2 | 154 г | 164 г | 10 г | 6.49 |
| Кейс 3 | 184 г | 245 г | 61 г | 33.15 |
| Кейс 4 | 190 г | 226 г | 36 г | 18.94 |
| Кейс 5 | 198 г | 307 г | 109 г | 55.05 |
| Кейс 6 | 205 г | 315 г | 107 г | 51.44 |
| Кейс 7 | 193 г | 256 г | 63 г | 32.64 |
Таблица 2. Вес до и после перфузии.
Дополнительный файл: Изготовленная на заказ камера поджелудочной железы для перфузии. Разработано в сотрудничестве с механическим цехом программы медицинской физики и радиационной медицины в онкологическом центре принцессы Маргарет. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Обсуждение
Данное исследование демонстрирует, что стабильный НВПП может быть достигнут для аллотрансплантатов поджелудочной железы с минимальным гистологическим повреждением через 3 ч перфузии с ранее представленной установкой. Параметры перфузии, такие как артериальный кровоток, давление, pH, HCO3 и Na, остаются стабильными во время перфузии, и мы наблюдали снижение и стабилизацию K и лактата.
Крайне важно как можно меньше манипулировать трансплантатом во время заготовки, подготовки заднего стола и перфузии. Также очень важно держать жесткий контроль артериального давления. Поскольку поджелудочная железа является органом низкого давления, повышение давления может привести к необратимому повреждению органа.
Подготовка заднего стола для этого исследования отличается от подготовки человеческих трансплантатов (рис. 2А). Поскольку поджелудочная железа была единственным органом, полученным от свиней, мы смогли взять часть аорты, которая включает чревный ствол и верхнюю брыжеечную артерию. Что касается воротной вены, то было выполнено расширение с использованием подвздошной вены. В случае человеческих трансплантатов подготовка заднего стола должна производиться так же, как и при трансплантации, с использованием подвздошных трансплантатов для реконструкции артерий и удлинения портала19.
Этот метод может быть ограничен сложностью настройки. Мы решили добавить диализную кассету после того, как заметили сильный отек трансплантата, когда обходились без него. Для этих экспериментов также была построена специально изготовленная органная камера, которая содержала внешний источник тепла, который оказался полезным для оптимальной перфузии трансплантатов.
Существует несколько исследований, описывающих нормотермическую перфузию поджелудочной железы ex vivo . В большинстве этих исследований отек, по-видимому, является основным ограничивающим фактором. Насколько нам известно, этот метод является единственным сообщением об использовании диализной кассеты для контроля отека.
Нормотермическая перфузия поджелудочной железы ex vivo все еще находится в зачаточном состоянии по сравнению с другими органами. Современные протоколы сосредоточены на донорах с расширенными критериями (DCD), улучшении перфузата, более длительном времени перфузии и биомаркерах для оценки повреждения трансплантата во время перфузии. Уровни амилазы и липазы, по-видимому, не являются надежными маркерами, поскольку мы используем закрытую систему и, по-видимому, не коррелируют с гистопатологией20. До сих пор нашей группе также удалось пересадить аллотрансплантаты поджелудочной железы после перфузии с хорошими результатами18.
Мы надеемся, что благодаря постоянному совершенствованию этой технологии эта технология будет применима к клинической трансплантации и позволит оценивать и восстанавливать аллотрансплантаты поджелудочной железы. Мы надеемся, что в конечном итоге это приведет к более широкому использованию трансплантата, сокращению времени ожидания для пациентов и улучшению результатов лечения пациентов
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Никакой.
Материалы
| Name | Company | Catalog Number | Comments |
| Alburex 5 | CSL Behring AG | 187337 | 25 g of Albumin (human) in 500 mL of buffered diluent |
| Aprotinin from bovine lung | Sigma-Aldrich | A1153 | |
| Belzer UW Cold storage solution | Bridge to life Ltd | 4055 | |
| Calcium gluconate (10%) | Fresenius Kabi Canada Ltd (Toronto, ON) | C360019 | |
| Composelect (blood collection bags) | Fresenius Kabi Canada Ltd | PQ31555 | |
| Epoprostenol | GlaxoSmithKline Inc. | 218761 | |
| Heart lung machine, Stöckert S3 | Sorin Group Canada Inc. | Custom made | Centrifugal pump, roller pump, control panel (sensors for pressure, flow, temperature, bubbles, and level), oxygen blender, heater unit |
| Hemoflow, Fresenius Polysulfone | Fresenius Medical Care North America | 0520165A | |
| Heparin (10000 IU/10 mL) | Fresenius Kabi Canada Ltd | C504710 | |
| Lactated Ringer's solution | Baxter | JB2324 | |
| Neonatal cardiopulmonary bypass techonolgy | Sorin Group Canada Inc | Custom made | Dideco perfusion tubing systems, centrifugal blood pump (Revolution), arterial blood filter, microporous hollow fibre memebrane oxygenator), cannulas |
| Pancreas chamber | Custom made | With external heater | |
| Percutaneous Sheath Introducer Set with Integral Hemostasis Valve/side Port for use with 7-7.5 Fr Catheters | Arrow International LLC | SI-09880 | |
| Sodium bicarbonate (8.4%) | Fresenius Kabi Canada Ltd | C908950 | |
| Solu-Medrol | Pfizer Canada Inc. | 52246-14-2 | |
| Steen | XVIVO | 19004 | |
| Urethral catheter | Bard Inc | 86020 | 20 Fr, malecot model drain |
| Verapamil | Sandoz Canada Inc. | 8960 |
Ссылки
- . National Diabetes Statistics Report | Diabetes | CDC Available from: https://www.cdc.gov/diabetes/data/statistics-report/index.html (2022)
- Shyr, Y. M., Wang, S. E., Chen, S. C., Shyr, B. U. Reappraisal of pancreas transplantation. Journal of the Chinese Medical Association JCMA. 82 (7), 531-534 (2019).
- Dholakia, S., et al. Pancreas transplantation: past, present, future. American Journal of Medicine. 129 (7), 667-673 (2016).
- Johnson, P., Sharples, E., Sinha, S., Friend, P. J. Pancreas and islet transplantation: pancreas and islet transplantation in diabetes mellitus. Transplantation Surgery. , 205-217 (2021).
- Kopp, W. H., et al. Pancreas transplantation with grafts from donors deceased after circulatory death: 5 years single-center experience. Transplantation. 102 (2), 333-339 (2018).
- Cypel, M., et al. Normothermic ex vivo lung perfusion in clinical lung transplantation. The New England Journal of Medicine. 364 (15), 1431-1440 (2011).
- Nasralla, D., et al. A randomized trial of normothermic preservation in liver transplantation. Nature. 557 (7703), 50-56 (2018).
- Selzner, M., et al. Normothermic ex vivo liver perfusion using steen solution as perfusate for human liver transplantation: First North American results. Liver Transplantation: Official Publication of the American Association for the Study of Liver Diseases and the International Liver Transplantation Society. 22 (11), 1501-1508 (2016).
- Hosgood, S. A., Thompson, E., Moore, T., Wilson, C. H., Nicholson, M. L. Normothermic machine perfusion for the assessment and transplantation of declined human kidneys from donation after circulatory death donors. The British Journal of Surgery. 105 (4), 388-394 (2018).
- Urbanellis, P., et al. Normothermic ex vivo kidney perfusion improves early dcd graft function compared with hypothermic machine perfusion and static cold storage. Transplantation. 104 (5), 947-955 (2020).
- Barlow, A. D., et al. Use of ex vivo normothermic perfusion for quality assessment of discarded human donor pancreases. American Journal of Transplantation: Official Journal of the American Society of Transplantation and the American Society of Transplant Surgeons. 15 (9), 2475-2482 (2015).
- Kumar, R., et al. Ex vivo normothermic porcine pancreas: A physiological model for preservation and transplant study. International journal of surgery. 54, 206-215 (2018).
- Hamaoui, K., et al. Development of pancreatic machine perfusion: translational steps from porcine to human models. The Journal of Surgical Research. 223, 263-274 (2018).
- Prudhomme, T., et al. Successful pancreas allotransplantations after hypothermic machine perfusion in a novel diabetic porcine model: a controlled study. Transplant International: Official Journal of the European Society for Organ Transplantation. 34 (2), 353-364 (2021).
- Kaths, J. M., et al. Normothermic ex vivo kidney perfusion for the preservation of kidney grafts prior to transplantation. Journal of Visualized Experiments: JoVE. (101), e353 (2015).
- Graham, A. S., Ozment, C., Tegtmeyer, K., Lai, S., Braner, D. A. V. Central venous catheterization. The New England Journal of Medicine. 356 (21), 21 (2009).
- Swindle, M. M. . Swine in the Laboratory Surgery, Anesthesia, Imaging, and Experimental Techniques. , (2015).
- Mazilescu, L. I., et al. Normothermic ex situ pancreas perfusion for the preservation of porcine pancreas grafts. American Journal of Transplantation. , (2022).
- Fridell, J. A., et al. Preparation of the pancreas allograft for transplantation. Clinical transplantation. 25 (2), (2011).
- Nassar, A., Liu, Q., Walsh, M., Quintini, C. Normothermic ex vivo perfusion of discarded human pancreas. Artificial Organs. 42 (3), 334-335 (2018).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены