Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Клинический протокол производства жировой ткани производные стромальные сосудистой дроби для потенциальных регенерации хряща
В этой статье
Резюме
Здесь мы представляем протокол производить жировой ткани производные стромальные сосудистой дроби и ее применение для улучшения функции коленного сустава путем регенерировать ткани хряща человека больных с остеоартрозом.
Аннотация
Остеоартрит (ОА) является одним из наиболее распространенных негативных расстройств. Недавно были предприняты многочисленные попытки улучшить функции колени с помощью различных форм мезенхимальных стволовых клеток (МСК). В Корее, костного концентраты и шнур стволовые клетки крови производные были одобрены Корейский продовольствия и наркотиков администрации (КФДА) для регенерации хряща. Кроме того жировой ткани, полученных стромальные сосудистой дроби (СФДВ) было разрешено от КФДА для совместных инъекций в человека пациентов. Аутологичные жировой ткани производные СФДВ содержит внеклеточного матрикса (ECM) помимо мезенхимальных стволовых клеток. ECM выделяет различные цитокины, которые, наряду с гиалуроновой кислоты (HA) и тромбоцитов богатые плазмы (PRP) активируются хлористого кальция, может помочь MSCs для регенерации хряща и улучшить функции коленного сустава. В этой статье мы представили протокол для улучшения функции коленного сустава путем регенерировать ткани хряща человека больных ОА. В результате протокол впервые сообщалось в 2011 году последовали несколько дополнительных публикаций. Протокол включает Липосакция для получения аутологичной lipoaspirates, смешиваются с коллагеназы. Эта смесь lipoaspirates коллагеназа затем вырежьте и гомогенизированные для удаления больших фиброзной ткани, которые могут засорить иглы во время инъекции. После этого смесь инкубированы для получения жировой ткани производные СФДВ. Результате жировая ткань производные СФДВ, содержащие жировой ткани производные MSCs и пережитков ECM, вводят в колени пациентов, в сочетании с ха и хлорида кальция активирован ОТР. Включены три случая пациентов, которые лечились с нашими протоколом, что приводит к повышению колено боль, отек и диапазон движения наряду с МРТ доказательства гиалинового хряща как ткани.
Введение
Знаны, что имеют возможность регенерации хряща1,2,3,4,5,6мезенхимальных стволовых клеток (МСК). Они могут быть легко получены из различных источников: костного мозга, пуповинной крови и жировой ткани, среди многих других. Среди этих источников жировой ткани является единственным источником, где можно получить достаточное количество MSCs без какого-либо расширения культуры для регенерации хряща в клинических параметров7,,8. Аутологичные костного стромальные сосудистой дроби (СФДВ) может быть легко получены также. Однако количество стволовых клеток, содержащихся в расширенной костного мозга-культура является очень низким7,8. Пуповинной крови может содержать достаточное количество MSCs. Однако пуповинной крови не является доступный источник аутологичной СФДВ.
Многочисленные методы обработки жировой ткани для получения СФДВ доступны для клинического применения. Среди них, метод получения MSCs из жировой ткани с помощью коллагеназы, разработаны и подтверждена Зук и др. 5 , 6, очень хорошо приняли. Этот метод использования коллагеназы был изменен для клинического применения в ортопедии. Для того, чтобы применяться к клинических параметров, система должна быть закрытой системы для поддержания стерильности при сохранении удобства. Один частности изменения, представленные в этой статье включает гомогенизацию lipoaspirates. Малого размера lipoaspirates перевариваются относительно быстрее, чем крупные, которые приводят к неравномерное распределение жировой ткани. Кроме того эти большего размера lipoaspirates может производить фиброзной ткани, которые засоряют шприцы и иглы при выполнении совместных инъекций9,10. Для того, чтобы предотвратить эти проблемы, lipoaspirates может гомогенизированные резки и мясорубки lipoaspirates до инкубации с коллагеназы. Результате жировая ткань производные СФДВ может содержать более равномерным внеклеточного матрикса (ECM), по сравнению с lipoaspirates, которые не являются гомогенизированные11. Разбитых ECM, содержащихся в СФДВ может работать как леска12.
В 2009 году аутологичной жировой ткани производные СФДВ позволило Корейский продовольствия и наркотиков администрации (КФДА) при обработке в медицинское учреждение с минимальной обработкой врач13. Впоследствии аутологичные жировой ткани производные СФДВ был использован как потенциального агента для улучшения функций колена в больных остеоартрит (ОА), потенциально регенерировать ткани хряща10,14,15 , 16 , 17 , 18 .
В 2011 году Пак в первый раз показал, что жировая ткань производные стволовых клеток (ИСС) содержащихся в жировой ткани, полученных СФДВ может улучшить функции коленного сустава, потенциально регенерации хрящевой ткани человека больных ОА, когда вводят с тромбоцитов богатые плазмы (PRP) 14. Кроме того Пак et al. сообщили о безопасности данных в 2013 году с участием 91 пациентов. Средняя эффективность в этом безопасность данных составила 67%15. Впоследствии дополнительные исследования Пак et al. показали улучшение коленного функции потенциально вследствие регенерации хрящевой ткани у больных с мениска слезы и Хондромаляция голени10,16,17 ,18. На основании статей сообщалось, известно, что количество стволовых клеток, содержащихся в 100 г жировой ткани, обрабатываемых протоколом, представленные в этой статье может варьироваться от 1 000 000-40,000,000 в зависимости от пациентов характеристики8, 19 , 20 , 21 , 22 , 23.
Здесь мы представляем клинический протокол человека коленного OA, аутологичной СФДВ, жировой ткани, полученных с помощью га и ОТР, активированный с хлорид кальция. Первая версия этой клинических протокола, связанных с закрытыми, ручной системы для поддержания стерильности, было сообщено в 201114. Идентичные протокол был оптимизирован, сохранение стерильности и было сообщено в 2013 и 201610,15. Здесь представлен оптимизированный протокол. Схематический обзор протокола представлена на рисунке 1.
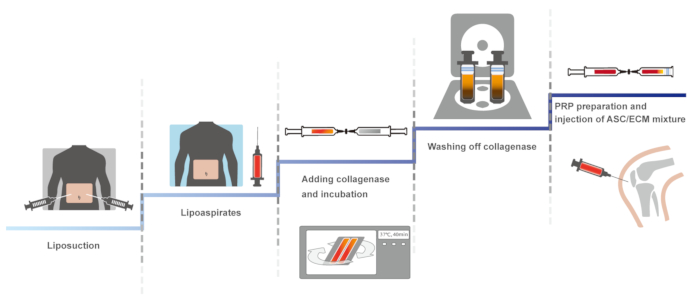
Рисунок 1: схема Обзор протокола. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
протокол
Одобрения и согласия представить следующие доклады были waived Комитетом (MJUIRB) Мёнгчжийский университета институциональных Наблюдательный Совет. Кроме того этот клинический протокол был в соответствии с руководящими принципами Хельсинкской декларации и регулирование КФДА. Для выполнения процедур осознанного согласия были получены из пациентов.
1. липосакция
Примечание: Выполнение с стерильных.
- Используйте следующие критерии включения: (1) МРТ доказательства этапа 3 OA; (2) мужского или женского пола; (3) старше 18 лет; (4) достаточно жировой ткани (100-110 г) для липосакции; (5) нежелание приступить хирургического вмешательства; (6) неудачи консервативное управление; и (7) отключение постоянной боли.
- Используйте следующие критерии исключения: (1) активного заболевания воспалительного или соединительной ткани, как считается, воздействие состояние боли (т.е., волчанка, ревматоидный артрит, фибромиалгия); (2) активный эндокринных расстройств, которые могут повлиять на состояние боли (т.е.,, гипотиреоз, сахарный диабет); (3) активные неврологические расстройства, которые могут повлиять на состояние боли (т.е.,, периферической нейропатии, рассеянный склероз); (4) активные болезнь легких, требующих использования лекарств; и (5) не история совместных инъекции стероидов последние 3 месяца.
- Привести пациента в операционной комнате с капюшоном A класса биологической и место его (или ее) в лежачем положении.
- Чистота области живота пациента с 5% Бетадин (повидон йод) и драпировка пациента с использованием метода стерилизации, подвергая очищаемой области живота для липосакции.
- Приблизительно в 5 см infero боков от пупка, анестезировать двух сайтов (один слева, а другой на правой стороне пупка) разрез к-быть-с (25, 1½ дюймов) иглы в 5-мл шприц 2 мл 2% лидокаин без адреналина путем инъекций каждого сайта на уровне эпидермиса.
- Анестезировать сайт разрез к-быть-с 5 мл раствора Тумесцентная (500 мл обычной соли, 40 мл 2% лидокаин, 20 мл 0,5% Бупивакаин, 0,5 мл эпинефрин 1: 1000) в 10-мл шприц с иглой (25 колеи, 1½ дюймов).
- Сделайте 2 разрезов 0.5 см примерно 5 см ниже пупка боково, щипал кожу, чтобы повысить глубину уровня подкожной.
- С помощью лезвия № 11, совать поднял кожу проникают до уровня подкожной, но не проникают через брюшную стенку.
- С помощью канюли 20 см 16-го калибра, анестезировать подкожной уровень всей нижней области живота, которая является к-быть-liposuctioned, с 700 до 800 мл раствора Тумесцентная.
- После отделки проникновение всей нижней части живота с Тумесцентная решения, подготовить аппарат липосакция, подключив 3,0 мм канюля, подключенных к 60 мл (или 30 мл) шприц для ручной липосакция или специально разработанные 3,0 мм канюля, подключенных к Центрифуга комплект, закрытой системе шприц с целью сохранения стерильности, подключен к вакуумные машины для вакуум-липосакция.
- Проведения липосакции для получения 100-110 г жировой ткани, исключая Тумесцентная решения. При выполнении липосакции, жировой ткани будет получен вместе с Тумесцентная решение, которое должны быть отделены и удалены.
- Чтобы отделить Тумесцентная решение, сначала под действием силы тяжести, передать 60 мл шприц жировой ткани в комплект центрифуги и поместите шприц вниз (т.е. та часть шприца внизу). Подождав 5-6 мин, жировой ткани и Тумесцентная жидкости будут разделены. Удалите жидкость в нижней части шприц, нажав на верхней части поршень шприца.
- Выполните перечисленные выше действия 1.9-1.11, до тех пор, пока накоплен в общей сложности 100-110 г жировой ткани (lipoaspirates) за колено.
2. Подготовка смеси ASC/ECM с стерильных закрытой системы
- После разделения Тумесцентная решения по тяжести и накапливается 50-55 g lipoaspirates за каждый комплект центрифуги 60 мл, стерильные закрытой системы, место 2 центрифуги наборы в центрифуге контейнера ведро и спина на 1600 x g 5 мин, конденсационные lipoaspirates и разделение жидкости из жировой ткани. В этом процесс дальнейшего конденсируется, жирное масло, в некоторых случаях может привести к lipoaspirates.
- Быть осторожным, чтобы не поколебать, снять предохранительную крышку и подключите в нижней части комплекта центрифуги.
- Удаление нижней жидкости нажав медленно вниз на верхней части поршень комплект центрифуги.
- На отдельных 60 мл шприц Растворите 10 мг коллагеназы (5 мг коллагеназы, специфических для соединительной ткани24 ) и 5 мг коллагеназы, специфических для жировой ткани25с 50 мл физиологическим.
- Смешать примерно 25-30 мл конденсированных lipoaspirate с растворенными коллагеназы (5 мг коллагеназы, специфических для соединительной ткани) и 5 мг коллагеназы, специфических для жировой ткани в соотношении 1:1 (v: v) путем соединения 60 мл шприц с комплектом центрифуги с помощью Специализированный разъем.
- Тщательно перемешайте конденсированных lipoaspirate и коллагеназы, нажав содержание между 60 мл шприц и центрифуги наборы с помощью лозы или толкача.
- Передача смеси lipoaspirate и коллагеназы 60 мл-шприцы.
- Подключите каждый 60 мл шприц, содержащие смесь с гомогенизатор ткани, которая содержит лезвия.
- Соединить другой конец гомогенизатор пустой 60 мл шприц.
- Нажмите смесь других 60 мл шприца через гомогенизатор для 4 -6 раз, резки и фарша из lipoaspirate.
- Передать смесь коллагеназы и гомогенизированное lipoaspirate обратно в 60 мл центрифуги наборы через специализированный разъем
- Место центрифуги наборы в контейнере, чтобы быть помещены в инкубатор, который был предварительно нагретой на 37 ° C.
- Инкубируйте две центрифуги комплекты с Гомогенизированные смеси при 37 ° C 40 мин при вращении на 45 об/мин.
- После 40 минут инкубации снимите контейнер из инкубатора в стерильных моды. Затем удалите центрифуги наборы и поместите их в центрифуги машины.
- Центрифуга смеси на 800 x g 5 мин отделить жировой ткани производные СФДВ.
- После центрифугирования удалите супернатант (которая включает в себя коллагеназы и переваривается жировой ткани) из каждого центрифуги наборы, удалив колпачок шприца на вершине поршень и размещение 30 мл шприц на поршень открытия через шприц блокировки подключение.
- Медленно нажимайте часть ствола 30 мл шприц для супернатант заполнить в 30 мл шприц.
- Нажмите вниз баррель 30 мл шприц все, вплоть до последних 3-4 мл в нижней части комплекта центрифуги, оставляя только последние 3-4 мл жировой ткани производные СФДВ. Супернатант отбрасывается.
- Удаление 30 мл шприц из верхней части плунжера и заполните шприц с 5% декстрозы в раствор лактат Рингера (D5LR).
- Присоединив 30 мл шприц, заполнены с D5LR на вершине поршень открытия, заполните центрифуги комплекты, содержащие 3-4 мл жировой ткани производные СФДВ, с D5LR до 55 мл.
- Удаление 30 мл шприц, крышка поршень и центрифуги центрифуги наборы снова на 300 x g на 4 мин.
- Повторите шаги 2.17-2.21 для в общей сложности 4 мойки. Используемые коллагеназы ксеногенные. Таким образом большинство коллагеназы удаляется 4 мойки. Однако для утверждения FDA, тонкой настройки протокола может быть необходимо полностью удалить остатки коллагеназы в окончательном объеме, хотя текущее количество коллагеназы остатков может быть достаточно незначительным для пациентов, которые не имеют любые клинические побочные эффекты.
- После 4й центрифугирования для того чтобы получить окончательный счет для инъекций, удалите крышку безопасности и вилку на нижней открытия комплект центрифуги, без встряхивания или поворачивая комплект центрифуги.
- Прикрепите 20 мл шприц на дно комплект центрифуги, открытие с помощью специально разработанных соединителя.
- Потяните поршень шприца и обратно несколько раз встряхнуть клетки, которые поселились в нижней части комплекта центрифуги.
- Удалить желаемый объем СФДВ, содержащие ИСС и ECM, а также другие клетки и ткани (обычно около 3-4 мл из каждого комплекта центрифуги для колена совместного инъекции).
3. PRP подготовка с стерильных
- При подготовке ИСС и ECM, нарисуйте 30 мл с 2,5 мл раствора декстрозы антикоагулянт цитрат аутологичной крови.
- Передать Рисованные крови комплекты центрифуги 60 мл.
- Центрифуга Рисованные кровь на 730 x g 5 минут и удалить супернатант в новый комплект центрифуги 60 мл. Центрифуга супернатант в 1300 x g 4 минут, что приводит к 3-4 мл ОТР.
- Прямо перед инъекцией, добавить 3% (w/v) хлорид кальция в соотношении 10:2 (ОТР: хлорид кальция, v: v) для политики репликации Паролей для того чтобы активировать его.
- Добавьте 0,5% (w/v) Ха, как леска, ОТР, активированный с хлорид кальция. Эти ИСС с ECM, наряду с ОТР, активированный, хлорид кальция, и Ха стенд для смеси ASC/ECM.
4. ASC/ECM смесь на основе лечения
- Очистить колено пациента с 5% Бетадин и драпировка ее стерильной образом.
- Ощупывайте передней колена для совместного пространства между бедренной и большеберцовой костей.
- Анестезировать укола поверхностно с разбавленным лидокаина (1 мл 1% лидокаина, разбавленным с 4 мл физиологическим) из кожи просто вне капсулы сустава.
- Анестезировать внутри суставной капсулы с разбавленным ропивакаина (ропивакаина 0,75% 1 мл разбавляют 3 мл физиологическим).
- Смешайте 2 мл HA до 6-8 мл СФДВ, содержащихся в 20 мл шприца через шприц шприц соединитель.
- С помощью соединителя шприц шприц, добавьте 0,4 мл хлорида кальция в 3-4 мл аутологичной ОТР, который уже подготовлен и готов в 5-мл шприц.
- 3.5-4.5 мл хлорида кальция ОТР в шприц 5 мл в сочетании с 8-10 мл смеси HA/СФДВ в 20 мл шприца через шприц шприц соединитель.
- Сразу же, медленно inject смесь (около 12-15 мл) в передней tibio бедренного сустава коленям, используя 38-мм 18-иглы, с или без указания УЗИ.
- После инъекции бандаж инъекции с давлением, складывания 4 x 4 хлопчатобумажной марли 4 раза и поместив ленты над сложенном марлевые 4 x 4.
- Проинструктируйте пациента оставаться еще на 60 мин для клеток вложения.
- Проинструктируйте пациента, чтобы ограничить деятельность для минимальной 1 недели после выписки из клиники.
- Вернуться в клинику для трех дополнительных инъекций ОТР, активированную хлорид кальция за 3 недели.
5. после лечения следить
- Оценить пациента на неделе 2, 4 и 16 (18 или 22) для боли улучшение с точки зрения визуального аналоговой шкале (VAS) и улучшение функции с точки зрения параметров физической терапии. Определите функциональные рейтинг индекса (Пт), VAS и диапазон движения (ROM), как описано в26,27.
- Следить за пациента после лечения МРТ 3 месяца после лечения.
Результаты
Трое больных (один 87-летняя женщина с этап 3 ОА, 68-летний мужчина с этапа 3 ОА, и один 60-летняя женщина с этапа 3 ОА) без каких-либо значительных прошлом медицинской истории представил в клинику с стойких колено боль и желаемого для потенциальных Аутологичные жировой ткани...
Обсуждение
В 2001 году Зук и др. изолированные стволовых клеток из жировой ткани, разбив коллагеновой матрицы с коллагеназы6. Впоследствии группа показала, что эти стволовые клетки из жировой ткани может превратить в хрящ и других тканях мезодермы в происхождения, доказав, что эти с...
Раскрытие информации
Авторы не имеют ничего сообщать.
Благодарности
Автор признает поддержку от сотрудников медицинской клиники Mipro и дизайн Jaepil/Дэвид ли рисунок. Эта работа была поддержана научно-исследовательских грантов от био и медицинской программы развития технологии НРФ, финансируемого MSIT (номер СР 2017M3A9E4078014); и Национальный исследовательский фонд из Кореи (СР НАТО) финансируется министерством науки и ИКТ (числа СР 2017R1A2B4002315 и СР 2016R1C1B2010308).
Материалы
| Name | Company | Catalog Number | Comments |
| Material | |||
| 5% Betadine (povidone-iodine) | Firson Co., Ltd. | 657400260 | |
| 2% Lidocaine | Daehan Pharmaceutical Co. | 670603480 | |
| Tumescent solution | Myungmoon Pharm. Co. Ltd. | N01BB01 | The solution was composed of 500 mL normal saline, 40 mL 2% lidocaine, 20 mL 0.5% marcaine, and 0.5 mL epinephrine 1:1000. |
| Liberase TL and TM research grade | Roche Applied Science | 5401020001 | |
| D5LR | Dahan Pharm. Co., Ltd. | 645101072 | Dextrose 5% in lactated Ringer's solution |
| Anticoagulant citrate dextrose solution | Fenwal, Inc. | NDC:0942-0641 | The solution was composed of 0.8% citric acid, 0.22% sodium citrate, and 0.223% dextrose. |
| 3% (w/v) Calcium chloride | Choongwae Pharmaceutical Co. | 644902101 | |
| 0.5% (w/v) HA (Hyaluronic acid ) | Dongkwang pharm. Co., Ltd. | 645902030 | |
| 0.25% Ropivacaine | Huons Co., Ltd. | 670600150 | |
| Equipment | |||
| 3.0 mm Cannula | WOOJU Medical Instruments Co. | ML30200 | |
| 60-mL Luer-Lock syringe | BD (Becton Dickinson) | 309653 | |
| Centrifuge Barrel Kit | CPL Co., Ltd. | 30-0827044 | |
| Tissue homogenizer that contains blades | CPL Co., Ltd. | 30-0827045 | |
| Rotating incubator mixer | Medikan Co., Ltd | MS02060092 | |
| Centrifuge | Hanil Scientific Inc. | CE1133 | |
| Magnetic Resonance Imaging | Philips Medical Systems Inc. | 18068 | |
| Ultrasound Imaging System | Samsung Medison co., Ltd | CT-LK-V10-ICM-09.05.2007 |
Ссылки
- Arnoczky, S. P. Building a meniscus. Biologic considerations. Clinical Orthopaedics and Related Research. (367 Suppl), S244-S253 (1999).
- Barry, F. P. Mesenchymal stem cell therapy in joint disease. Novartis Foundation Symposium. 249, 86-241 (2003).
- Usuelli, F. G., et al. Adipose-derived stem cells in orthopaedic pathologies. British Medical Bulletin. 124 (1), 31-54 (2017).
- Zhang, H. N., Li, L., Leng, P., Wang, Y. Z., Lv, C. Y. Uninduced adipose-derived stem cells repair the defect of full-thickness hyaline cartilage. Chinese Journal of Traumatology. 12 (2), 92-97 (2009).
- Zuk, P. A., et al. Human adipose tissue is a source of multipotent stem cells. Molecular Biology of the Cell. 13 (12), 4279-4295 (2002).
- Zuk, P. A., et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Engineering. 7 (2), 211-228 (2001).
- Baer, P. C., Geiger, H. Adipose-derived mesenchymal stromal/stem cells: tissue localization, characterization, and heterogeneity. Stem Cells International. 2012, 812693 (2012).
- Zhu, Y., et al. Adipose-derived stem cell: a better stem cell than BMSC. Cell Biochemistry and Function. 26 (6), 664-675 (2008).
- Bellei, B., Migliano, E., Tedesco, M., Caputo, S., Picardo, M. Maximizing non-enzymatic methods for harvesting adipose-derived stem from lipoaspirate: technical considerations and clinical implications for regenerative surgery. Scientific Reports. 7 (1), 10015 (2017).
- Pak, J., Lee, J. H., Park, K. S., Jeong, B. C., Lee, S. H. Regeneration of Cartilage in Human Knee Osteoarthritis with Autologous Adipose Tissue-Derived Stem Cells and Autologous Extracellular Matrix. BioResearch Open Access. 5 (1), 192-200 (2016).
- Alexander, R. W. Understanding Adipose-derived Stromal Vascular Fraction (AD-SVF) Cell Biology and Use on the Basis of Cellular, Chemical, Structural and Paracrine Components: A Concise Review. Journal of Prolotherapy. 4, e855-e869 (2012).
- Benders, K. E., et al. Extracellular matrix scaffolds for cartilage and bone regeneration. Trends in Biotechnology. 31 (3), 169-176 (2013).
- Korean Food and Drug Administration (KFDA). Cell therapy: Rules and Regulations. KFDA. , (2009).
- Pak, J. Regeneration of human bones in hip osteonecrosis and human cartilage in knee osteoarthritis with autologous adipose-tissue-derived stem cells: a case series. Journal of Medical Case Reports. 5, 296 (2011).
- Pak, J., Chang, J. J., Lee, J. H., Lee, S. H. Safety reporting on implantation of autologous adipose tissue-derived stem cells with platelet-rich plasma into human articular joints. BMC Musculoskeletal Disorders. 14, 337 (2013).
- Pak, J., Lee, J. H., Kartolo, W. A., Lee, S. H. Cartilage Regeneration in Human with Adipose Tissue-Derived Stem Cells: Current Status in Clinical Implications. BioMed Research International. 2016, 4702674 (2016).
- Pak, J., Lee, J. H., Lee, S. H. A novel biological approach to treat chondromalacia patellae. PLoS One. 8 (5), e64569 (2013).
- Pak, J., Lee, J. H., Lee, S. H. Regenerative repair of damaged meniscus with autologous adipose tissue-derived stem cells. BioMed Research International. 2014, 436029 (2014).
- Aust, L., et al. Yield of human adipose-derived adult stem cells from liposuction aspirates. Cytotherapy. 6 (1), 7-14 (2004).
- De Ugarte, D. A., et al. Comparison of multi-lineage cells from human adipose tissue and bone marrow. Cells Tissues Organs. 174 (3), 101-109 (2003).
- Guilak, F., et al. Clonal analysis of the differentiation potential of human adipose-derived adult stem cells. Journal of Cellular Physiology. 206 (1), 229-237 (2006).
- Mitchell, J. B., et al. Immunophenotype of human adipose-derived cells: temporal changes in stromal-associated and stem cell-associated markers. Stem Cells. 24 (2), 376-385 (2006).
- Oedayrajsingh-Varma, M. J., et al. Adipose tissue-derived mesenchymal stem cell yield and growth characteristics are affected by the tissue-harvesting procedure. Cytotherapy. 8 (2), 166-177 (2006).
- . Liberase TL information available from Sigma Millipore online Available from: https://www.sigmaaldrich.com/catalog/product/roche/05401020001?lang=en®ion=US (2018)
- . Liberase TM information available from Sigma Millipore online Available from: https://www.sigmaaldrich.com/catalog/product/roche/Libtmro?lang=en®ion=US (2018)
- Childs, J. D., Piva, S. R. Psychometric properties of the functional rating index in patients with low back pain. European Spine Journal. 14 (10), 1008-1012 (2005).
- Price, D. D., McGrath, P. A., Rafii, A., Buckingham, B. The validation of visual analogue scales as ratio scale measures for chronic and experimental pain. Pain. 17 (1), 45-56 (1983).
- Pilgaard, L., Lund, P., Rasmussen, J. G., Fink, T., Zachar, V. Comparative analysis of highly defined proteases for the isolation of adipose tissue-derived stem cells. Regenerative Medicine. 3 (5), 705-715 (2008).
- D'Ambrosi, R., Indino, C., Maccario, C., Manzi, L., Usuelli, F. G. Autologous Microfractured and Purified Adipose Tissue for Arthroscopic Management of Osteochondral Lesions of the Talus. Journal of Visualized Experiments. (131), e56395 (2018).
- Packer, J. D., Chang, W. T., Dragoo, J. L. The use of vibrational energy to isolate adipose-derived stem cells. Plastic Reconstructive Surgery-Global Open. 6 (1), e1620 (2018).
- Hanke, C. W., Bernstein, G., Bullock, S. Safety of tumescent liposuction in 15,336 patients. National survey results. Dermatologic Surgery. 21 (5), 459-462 (1995).
- Illouz, Y. G. Complications of liposuction. Clinics in Plastic Surgery. 33 (1), 129-163 (2006).
- Dixit, V. V., Wagh, M. S. Unfavourable outcomes of liposuction and their management. Indian Journal of Plastic Surgery. 46 (2), 377-392 (2013).
- Lehnhardt, M., et al. Major and lethal complications of liposuction: a review of 72 cases in Germany between 1998 and 2002. Plastic and Reconstructive Surgery. 121 (6), 396e-403e (2008).
- Iyer, S. S., Rojas, M. Anti-inflammatory effects of mesenchymal stem cells: novel concept for future therapies. Expert Opinion on Biological Therapy. 8 (5), 569-581 (2008).
- Zhang, J., Middleton, K. K., Fu, F. H., Im, H. J., Wang, J. H. HGF mediates the anti-inflammatory effects of PRP on injured tendons. PLoS One. 8 (6), e67303 (2013).
- Li, N. Y., Yuan, R. T., Chen, T., Chen, L. Q., Jin, X. M. Effect of platelet-rich plasma and latissimus dorsi muscle flap on osteogenesis and vascularization of tissue-engineered bone in dogs. Journal of Oral and Maxillofacial Surgery. 67 (9), 1850-1858 (2009).
- Parsons, P., et al. The biological effect of platelet rich-plasma on the fracture healing process. The Journal of bone and joint surgery. British volume. 91-B, 293 (2009).
- Wu, W., Chen, F., Liu, Y., Ma, Q., Mao, T. Autologous injectable tissue-engineered cartilage by using platelet-rich plasma: experimental study in a rabbit model. Journal of Oral and Maxillofacial Surgery. 65 (10), 1951-1957 (2007).
- Cooper, T. W., Eisen, A. Z., Stricklin, G. P., Welgus, H. G. Platelet-derived collagenase inhibitor: characterization and subcellular localization. Proceedings of the National Academy of Sciences of the United States of America. 82 (9), 2779-2783 (1985).
- Uzuki, M., Sawai, T. A. A comparison of the affinity of sodium hyaluronate of various molecular weights for degenerated cartilage: a histochemical study using hyaluronic acid binding protein. International Congress Series. 1223, 279-284 (2001).
- Pagano, C., et al. Molecular and morphometric description of adipose tissue during weight changes: a quantitative tool for assessment of tissue texture. International Journal of Molecular Medicine. 14 (5), 897-902 (2004).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены