Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Cromatografía de exclusión de tamaño para analizar la heterogeneidad de las vesículas de la membrana externa bacteriana
En este artículo
Resumen
Las vesículas bacterianas desempeñan un papel importante en la patogénesis y tienen aplicaciones biotecnológicas prometedoras. La heterogeneidad de las vesículas complica el análisis y el uso; por lo tanto, es necesario un método simple y reproducible para separar los diferentes tamaños de vesículas. Aquí, demostramos el uso de la cromatografía de exclusión de tamaño para separar vesículas heterogéneas producidas por Aggregatibacter actinomycetemcomitans.
Resumen
La pared celular de las bacterias Gram-negativas consiste en una membrana interna (citoplasmática) y externa (OM), separadas por una fina capa de peptidoglicano. A lo largo del crecimiento, la membrana externa puede sangrar para formar vesículas esféricas de la membrana externa (OMV). Estos OMV están involucrados en numerosas funciones celulares, incluida la entrega de carga a las células huésped y la comunicación con las células bacterianas. Recientemente, el potencial terapéutico de los OMV ha comenzado a ser explorado, incluyendo su uso como vacunas y vehículos de administración de medicamentos. Aunque los OMV se derivan del OM, durante mucho tiempo se ha apreciado que la carga de lípidos y proteínas del OMV difiere, a menudo significativamente, de la del OM. Más recientemente, se ha descubierto evidencia de que las bacterias pueden liberar múltiples tipos de OMV, y existe evidencia de que el tamaño puede afectar el mecanismo de su absorción por las células huésped. Sin embargo, los estudios en esta área están limitados por las dificultades para separar eficientemente los OMV de tamaño heterogéneo. La centrifugación por gradiente de densidad (DGC) se ha utilizado tradicionalmente para este propósito; sin embargo, esta técnica requiere mucho tiempo y es difícil de ampliar. La cromatografía de exclusión de tamaño (SEC), por otro lado, es menos engorrosa y se presta a la escala futura necesaria para el uso terapéutico de omV. Aquí, describimos un enfoque SEC que permite la separación reproducible de vesículas de tamaño heterogéneo, utilizando como caso de prueba, OMVs producidos por Aggregatibacter actinomycetemcomitans, que varían en diámetro desde menos de 150 nm hasta más de 350 nm. Demostramos la separación de OMV "grandes" (350 nm) y OMV "pequeños" (<150 nm), verificados por dispersión dinámica de luz (DLS). Recomendamos las técnicas basadas en SEC sobre las técnicas basadas en DGC para la separación de vesículas de tamaño heterogéneo debido a su facilidad de uso, reproducibilidad (incluido el usuario a usuario) y la posibilidad de escalar.
Introducción
Las bacterias gramnegativas liberan vesículas derivadas de su membrana externa, las llamadas vesículas de membrana externa (OMV), a lo largo del crecimiento. Estos OMV desempeñan un papel importante en la comunicación de célula a célula, tanto entre las bacterias y el huésped como entre las células bacterianas, al transportar una serie de biomoléculas importantes, incluyendo ADN / ARN, proteínas, lípidos y peptidoglicanos1,2. En particular, el papel de los OMV en la patogénesis bacteriana ha sido ampliamente estudiado debido a su enriquecimiento en ciertos factores de virulencia y toxinas3,4,5,6,7,8,9,10,11.
Se ha informado que los OMV varían en tamaño de 20 a 450 nm, dependiendo de la bacteria madre y la etapa de crecimiento, con varios tipos de bacterias que liberan OMVde tamaño heterogéneo8,12, 13,14,que también difieren en su composición proteica y mecanismo de entrada de la célula huésped12. H. pylori liberó OMVs que varían en diámetro de 20 a 450 nm, con los OMVs más pequeños que contienen una composición de proteínas más homogénea que los OMVs más grandes. Es importante destacar que se observó que las dos poblaciones de OMVs eran internalizadas por las células huésped a través de diferentes mecanismos12. Además, hemos demostrado que Aggregatibacter actinomycetemcomitans libera una población de OMV pequeños (<150 nm) junto con una población de OMV grandes (>350 nm), con los OMV que contienen una cantidad significativa de una toxina proteica secretada, leucotoxina (LtxA)15. Si bien el papel de la heterogeneidad omv en los procesos celulares es claramente importante, las dificultades técnicas para separar y analizar distintas poblaciones de vesículas han limitado estos estudios.
Además de su importancia en la patogénesis bacteriana, se han propuesto OMV para su uso en una serie de aplicaciones biotecnológicas, incluso como vacunas y vehículos de administración de medicamentos16,17,18,19,20. Para su uso traslacional en tales enfoques, se requiere una preparación limpia y monodispersa de vesículas. Por lo tanto, son necesarios métodos efectivos y eficientes de separación.
Más comúnmente, la centrifugación por gradiente de densidad (DGC) se utiliza para separar poblaciones de vesículas de tamaño heterogéneo de los desechos celulares, incluidos los flagelos y las proteínas secretadas21; el método también se ha reportado como un enfoque para separar subpoblaciones omv de tamaño heterogéneo12,13,14. Sin embargo, DGC consume mucho tiempo, es ineficiente y muy variable de usuario a usuario22 y, por lo tanto, no es ideal para escalar verticalmente. Por el contrario, la cromatografía de exclusión de tamaño (SEC) representa un enfoque escalable, eficiente y consistente para purificar OMVs21,23,24. Hemos encontrado que una columna SEC larga (50 cm), de flujo por gravedad, llena de medio de filtración de gel es suficiente para purificar y separar eficientemente las subpoblaciones de OMV. Específicamente, utilizamos este enfoque para separar los OMV de A. actinomycetemcomitans en subpoblaciones "grandes" y "pequeñas", así como para eliminar la contaminación de proteínas y ADN. La purificación se completó en menos de 4 h, y se logró la separación completa de las subpoblaciones de OMV y la eliminación de escombros.
Protocolo
1. Preparación de tampones
- Para preparar el tampón de lavado ELISA, agregue 3,94 g de Tris-base, 8,77 g de NaCl y 1 g de albúmina sérica bovina (BSA) a 1 L de agua desionizada (DI). Añadir 500 μL de polisorbato-20. Ajuste el pH a 7.2 usando HCl o NaOH.
- Para preparar el búfer de bloqueo, agregue 3,94 g de Tris-base, 8,77 g de NaCl y 10 g de BSA. Agregue 500 μL de polisorbato-20 a 1 L de agua DI. Ajuste el pH a 7.2 usando HCl o NaOH.
- Para preparar el tampón de elución (PBS), agregue 8.01 g de NaCl, 2.7 g de KCl, 1.42 g de Na2HPO4y 0.24 g de KH2PO4 a 1 L de agua DI. Ajuste el pH a 7.4 usando HCl o NaOH.
NOTA: Se puede hacer una solución 10x de este tampón y diluirla con agua DI según sea necesario.
2. Preparación de la muestra OMV
- Cultivar células de A. actinomycetemcomitans hasta la fase exponencial tardía (densidad óptica a 600 nm de 0,7). Pelletar las células centrifugando dos veces a 10.000 x g a 4 °C durante 10 min. Filtre el sobrenadante a través de un filtro de 0,45 μm.
- Concentre el sobrenadante libre de bacterias utilizando filtros de corte de peso molecular de 50 kDa. Ultracentrífuga la solución concentrada a 105.000 x g a 4 °C durante 30 min.
- Vuelva a colocar el pellet en PBS y ultracentrífuga de nuevo (105.000 x g a 4 °C durante 30 min.) Resuspend el pellet en 2 mL de PBS.
3. Embalaje de la columna S-1000
- Mezcle la botella de caldo del medio de filtración de gel con una varilla de agitación de vidrio y vierta en una botella de vidrio el volumen necesario para llenar la columna, más aproximadamente un 50% de exceso (aproximadamente 135 ml). Deje que estas cuentas se asienten hasta que se hayan asentado y luego decante el exceso de líquido. Resuspenda las perlas en tampón de elución, de modo que la solución final sea aproximadamente 70% (por volumen) de gel, 30% de tampón. Desgasificación de la solución al vacío.
- Monte la columna de vidrio verticalmente usando un soporte de anillo y llene con tampón de elución para humedecer las paredes de la columna. Drene el búfer hasta que solo quede aproximadamente 1 cm de tampón en la columna.
- Sin crear burbujas, pipetee cuidadosamente las cuentas en la columna, llenando la columna hasta la parte superior. Continúe drenando el exceso de amortiguación durante todo este proceso. Asegúrese de no dejar que las cuentas se asienten por completo antes de agregar cuentas adicionales a la parte superior de la columna. La columna debe embalarse a una altura de aproximadamente 2 cm por debajo de la parte inferior del depósito de la columna.
4. Carga de la muestra y recogida de fracciones
- Desgasificación del tampón de elución al vacío. Lave la columna con dos volúmenes de columna (180 ml) de tampón de elución.
- Permita que el búfer restante entre completamente en la columna. Una vez que el tampón haya alcanzado la parte superior de la capa de gel, pipetee cuidadosamente una muestra de 2 ml que contenga OMV (a una concentración de lípidos de aproximadamente 100 - 200 nmol / L) en la superficie de las perlas, teniendo cuidado de no molestar ninguna de las perlas en la parte superior de la columna. Permita que la muestra entre completamente en el gel, es decir, cuando no quede líquido por encima de la capa de gel.
- Agregue con cuidado y lentamente el tampón de elución en la parte superior de la columna de gel. No perturbe la capa superior del gel, ya que esto causará la dilución de la muestra.
- Coloque un solo tubo de 50 ml debajo de la columna y abra la columna. Recoge los primeros 20 mL del eluyente. Agregue un búfer de elución adicional a la parte superior de la columna, con cuidado, según sea necesario para garantizar que la columna nunca esté seca.
- Coloque una serie de tubos de 1,5 ml debajo de la columna. Inicie la columna y recoja una serie de muestras de 1 ml en cada tubo. A medida que se recolectan las muestras, continúe agregando un búfer de elución a la parte superior de la columna, según sea necesario. Repetir hasta que se hayan recogido 96 fracciones. Detenga la columna.
NOTA: Las muestras deben almacenarse a -20 °C para el almacenamiento a largo plazo o 4 °C para el almacenamiento a corto plazo hasta un análisis adicional. - Para limpiar la columna, ejecute un volumen de columna (90 ml) de 0,1 M NaOH a través de la columna. Ejecute dos volúmenes de columna (180 ml) de búfer de elución a través de la columna.
5. Análisis de muestras
- Para medir la concentración de lípidos en cada fracción, pipetee 50 μL de cada fracción en un solo pozo de una placa de 96 pozos. A cada pozo, agregue 2.5 μL de tinte lipofílico. Incubar durante 15 s. Mida la intensidad de fluorescencia en un lector de placas con una longitud de onda de excitación de 515 nm y una longitud de onda de emisión de 640 nm. Para calcular la fracción de todos los lípidos en cada muestra, sume todas las intensidades de emisión y divida cada intensidad individual por el total.
- Para medir la concentración de una proteína en particular, pipetee 100 μL de cada fracción en un solo pozo de una placa de inmuno-placa ELISA. Incubar a 25 °C durante 3 h.
- Decantar las muestras. Añadir 200 μL de tampón de lavado ELISA a cada pozo y decantar. Repetir cuatro veces para un total de cinco lavados.
- Añadir 200 μL de tampón de bloqueo a cada pozo e incubar durante 1 h a 25 °C. Decantar.
- Incubar placas con tampón de bloqueo de 100 μL más anticuerpo primario (1:10.000 para anticuerpos purificados; 1:10 para anticuerpos no purificados) durante la noche a 4 °C. Decantar.
- Añadir 200 μL de tampón de lavado ELISA a cada pozo y decantar. Repetir cuatro veces para un total de cinco lavados.
- Agregue 100 μL de tampón de lavado ELISA más anticuerpo secundario (1:30,000) a cada pozo. Incubar durante 1 h a 25 °C.
- Añadir 200 μL de tampón de lavado ELISA a cada pozo y decantar. Repetir cuatro veces para un total de cinco lavados.
- Añadir 100 μL de la solución de un solo paso de 3,3',5,5'-tetrametilbenzidina (TMB) e incubar durante 15-30 min o hasta que se desarrolle un color azul. Detenga la reacción TMB con 50 μL de la solución de parada.
- En un lector de placas, lea la absorbancia de cada pozo a una longitud de onda de 450 nm.
- Para medir la concentración total de proteínas, registre la absorbancia a una longitud de onda de 280 nm (A280)de cada fracción, utilizando un espectrofotómetro UV-vis.
Un esquema del protocolo se muestra en la Figura 1.
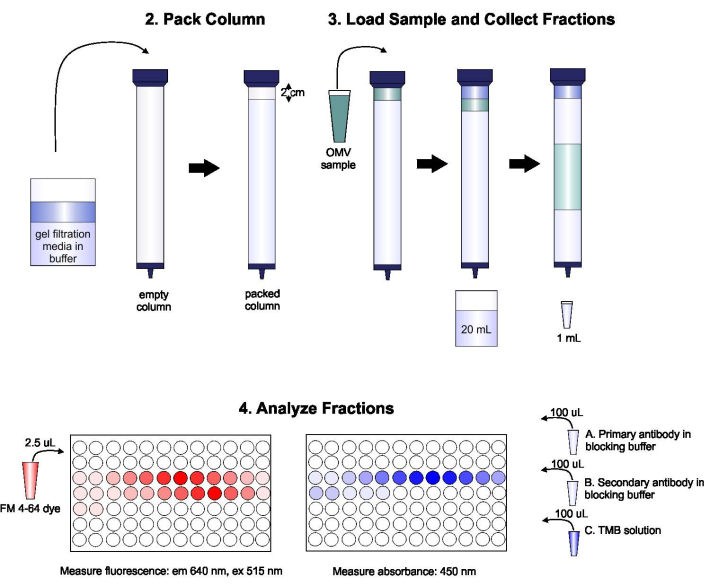
Figura 1: Esquema del procedimiento SEC. La columna se empaqueta con un medio de filtración de gel desgasificado cuidadosamente para evitar burbujas y discontinuidades, luego se lava con dos volúmenes de columna de tampón de elución. A continuación, la muestra se pipetea cuidadosamente en la parte superior del gel, sin interrumpir el embalaje del gel. La columna se abre y se ejecuta hasta que la muestra entra completamente en el gel. En este punto, el búfer se coloca en la parte superior de la columna y se recogen los primeros 20 ml de eluido. A continuación, se recoge una serie de fracciones de 1 ml. Estas fracciones se colocan en una placa de 96 pozos o una placa de inmunoplaca de 96 pozos para el análisis del contenido de lípidos y proteínas. Haga clic aquí para ver una versión más grande de esta figura.
Resultados
La Figura 2 muestra resultados representativos de este método. Los OMV producidos por A. actinomycetemcomitans cepa JP2 se purificaron por primera vez a partir del sobrenadante de cultivo utilizando ultracentrifugación15. Anteriormente encontramos que esta cepa produce dos poblaciones de OMVs, una con diámetros de unos 300 nm y otra con diámetros de unos 100 nm15. Para separar estas poblaciones de OMV, purificamos la muestra utiliz...
Discusión
Aquí, hemos proporcionado un protocolo para la separación simple, rápida y reproducible de subpoblaciones bacterianas omv. Aunque la técnica es relativamente sencilla, hay algunos pasos que deben realizarse con mucho cuidado para garantizar que se produzca una separación eficiente en la columna. En primer lugar, es esencial que el gel se cargue en la columna con cuidado y lentamente para evitar burbujas de aire. Hemos observado que dejar el gel a temperatura ambiente durante varias horas antes de cargar la columna p...
Divulgaciones
Los autores no tienen conflictos de intereses que informar.
Agradecimientos
Este trabajo fue financiado por la National Science Foundation (1554417) y los Institutos Nacionales de Salud (DE027769).
Materiales
| Name | Company | Catalog Number | Comments |
| 1-Step Ultra TMB-ELISA | Thermo Scientific | 34028 | |
| Amicon 50 kDa filters | Millipore Sigma | UFC905024 | |
| Bovine Serum Albumin (BSA) | Fisher Scientific | BP9704-100 | |
| ELISA Immuno Plates | Thermo Scientific | 442404 | |
| FM 4-64 | Thermo Scientific | T13320 | 1.5 x 50 cm |
| Glass Econo-Column | BioRad | 7371552 | |
| Infinite 200 Pro Plate Reader | Tecan | ||
| Potassium Chloride (KCl) | Amresco (VWR) | 0395-500G | |
| Potassium Phosphate Monobasic Anhydrous (KH2PO4) | Amresco (VWR) | 0781-500G | |
| Sephacryl S-1000 Superfine | GE Healthcare | 17-0476-01 | |
| Sodium Chloride (NaCl) | Fisher Chemical | S271-3 | |
| Sodium Phosphate Dibasic Anhydrous (Na2HPO4) | Amresco (VWR) | 0404-500G | |
| Tris Base | VWR | 0497-1KG | |
| Tween(R) 20 | Acros Organics | 23336-2500 |
Referencias
- Kuehn, M. J., Kesty, N. C. Bacterial outer membrane vesicles and the host-pathogen interaction. Genes and Development. 19, 2645-2655 (2005).
- Kulp, A., Kuehn, M. J. Biological functions and biogenesis of secreted bacterial outer membrane vesicles. Annual Reviews Microbiology. 64, 163-184 (2010).
- Kato, S., Kowashi, Y., Demuth, D. R. Outer membrane-like vesicles secreted by Actinobacillus actinomycetemcomitans are enriched in leukotoxin. Microbial Pathogenesis. 32 (1), 1-13 (2002).
- Nice, J. B., et al. Aggregatibacter actinomycetemcomitans leukotoxin is delivered to host cells in an LFA-1-independent manner when associated with outer membrane vesicles. Toxins. 10 (10), 414 (2018).
- Haurat, M. F., et al. Selective sorting of cargo proteins into bacterial membrane vesicles. Journal of Biological Chemistry. 286 (2), 1269-1276 (2011).
- Horstman, A. L., Kuehn, M. J. Enterotoxigenic Escherichia coli secretes active heat-labile enterotoxin via outer membrane vesicles. The Journal of Biological Chemistry. 275 (17), 12489-12496 (2000).
- Wai, S. N., et al. Vesicle-mediated export and assembly of pore-forming oligomers of the Enterobacterial ClyA cytotoxin. Cell. 115, 25-35 (2003).
- Balsalobre, C., et al. Release of the Type I secreted α-haemolysin via outer membrane vesicles from Escherichia coli. Molecular Microbiology. 59 (1), 99-112 (2006).
- Donato, G. M., et al. Delivery of Bordetella pertussis adenylate cyclase toxin to target cells via outer membrane vesicles. FEBS Letters. 586, 459-465 (2012).
- Kim, Y. R., et al. Outer membrane vesicles of Vibrio vulnificus deliver cytolysin-hemolysin VvhA into epithelial cells to induce cytotoxicity. Biochemical and Biophysical Research Communications. 399, 607-612 (2010).
- Maldonado, R., Wei, R., Kachlany, S. C., Kazi, M., Balashova, N. V. Cytotoxic effects of Kingella kingae outer membrane vesicles on human cells. Microbial Pathogenesis. 51 (1-2), 22-30 (2011).
- Turner, L., et al. Helicobacter pylori outer membrane vesicle size determines their mechanisms of host cell entry and protein content. Frontiers in Immunology. 9, 1466 (2018).
- Zavan, L., Bitto, N. J., Johnston, E. L., Greening, D. W., Kaparakis-Liaskos, M. Helicobacter pylori growth stage determines the size, protein composition, and preferential cargo packaging of outer membrane vesicles. Proteomics. 19 (1-2), 1800209 (2019).
- Rompikuntal, P. K., et al. Perinuclear localization of internalized outer membrane vesicles carrying active cytolethal distending toxin from Aggregatibacter actinomycetemcomitans. Infections and Immunity. 80 (1), 31-42 (2012).
- Nice, J. B., et al. Aggregatibacter actinomycetemcomitans leukotoxin is delivered to host cells in an LFA-1-independent manner when associated with outer membrane vesicles. Toxins. 10 (10), 414 (2018).
- Stevenson, T. C., et al. Immunization with outer membrane vesicles displaying conserved surface polysaccharide antigen elicits broadly antimicrobial antibodies. Proceedings of the National Academy of Sciences. 115 (14), 3106-3115 (2018).
- Gujrati, V., et al. Bioengineered bacterial outer membrane vesicles as cell-specific drug-delivery vehicles for cancer therapy. ACS Nano. 8 (2), 1525-1537 (2014).
- Huang, W., et al. Development of novel nanoantibiotics using an outer membrane vesicle-based drug efflux mechanism. Journal of Controlled Release. 317, 1-22 (2020).
- Chen, D. J., et al. Delivery of foreign antigens by engineered outer membrane vesicle vaccines. Proceedings of the National Academy of Sciences. 107 (7), 3099-3104 (2010).
- Chen, L., et al. Outer membrane vesicles displaying engineered glycotopes elicit protective antibodies. Proceedings of the National Academy of Sciences. 113 (26), 3609-3618 (2016).
- Singorenko, P. D., et al. Isolation of membrane vesicles from prokaryotes: A technical and biological comparison reveals heterogeneity. Journal of Extracellular Vesicles. 6 (1), 1324731 (2017).
- Zeringer, E., Barta, T., Li, M., Vlassov, A. V. Strategies for isolation of exosomes. Cold Spring Harbor Protocols. 2015 (4), 319-323 (2015).
- Benedikter, B. J., et al. Ultrafiltration combined with size exclusion chromatography efficiently isolates extracellular vesicles from cell culture media for compositional and functional studies. Science Reports. 7 (1), 15297 (2017).
- Mol, E. A., Goumans, M. J., Doevendans, P. A., Sluijter, J. P. G., Vader, P. Higher functionality of extracellular vesicles isolated using size-exclusion chromatography compared to ultracentrifugation. Nanomedicine. 13 (6), 2061-2065 (2017).
- Lally, E. T., Golub, E. E., Kieba, I. R. Identification and immunological characterization of the domain of Actinobacillus actinomycetemcomitans leukotoxin that determines its specificity for human target cells. Journal of Biological Chemistry. 269 (49), 31289-31295 (1994).
- Chang, E. H., Giaquinto, P., Huang, J., Balashova, N. V., Brown, A. C. Epigallocatechin gallate inhibits leukotoxin release by Aggregatibacter actinomycetemcomitans by promoting association with the bacterial membrane. Molecular Oral Microbiology. 35 (1), 29-39 (2020).
- Klimentová, J., Stulík, J. Methods of isolation and purification of outer membrane vesicles from gram-negative bacteria. Microbiological Research. 170, 1-9 (2015).
- Dauros Singorenko, P., et al. Isolation of membrane vesicles from prokaryotes: a technical and biological comparison reveals heterogeneity. Journal of Extracellular Vesicles. 6 (1), 1324731 (2017).
- Monguió-Tortajada, M., Gálvez-Montón, C., Bayes-Genis, A., Roura, S., Borràs, F. E. Extracellular vesicle isolation methods: rising impact of size-exclusion chromatography. Cellular and Molecular Life Sciences. 76 (12), 2369-2382 (2019).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados