È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Quantificazione della selettività delle caratteristiche visive del riflesso optocinetico nei topi
In questo articolo
Riepilogo
Qui descriviamo un protocollo standard per quantificare il riflesso optocinetico. Combina la stimolazione virtuale del tamburo e la video-oculografia, e consente quindi una valutazione precisa della selettività delle caratteristiche del comportamento e della sua plasticità adattativa.
Abstract
Il riflesso optocinetico (OKR) è un movimento oculare innato essenziale che viene innescato dal movimento globale dell'ambiente visivo e serve a stabilizzare le immagini retiniche. Per la sua importanza e robustezza, l'OKR è stato utilizzato per studiare l'apprendimento visuo-motorio e per valutare le funzioni visive di topi con diversi background genetici, età e trattamenti farmacologici. Qui, introduciamo una procedura per valutare le risposte OKR di topi con testa fissata con elevata precisione. La fissazione della testa può escludere il contributo della stimolazione vestibolare sui movimenti oculari, consentendo di misurare i movimenti oculari innescati solo dal movimento visivo. L'OKR è suscitato da un sistema di tamburi virtuali, in cui un reticolo verticale presentato su tre monitor di computer si sposta orizzontalmente in modo oscillatorio o unidirezionale a velocità costante. Con questo sistema di realtà virtuale, possiamo modificare sistematicamente i parametri visivi come la frequenza spaziale, la frequenza temporale/oscillante, il contrasto, la luminanza e la direzione dei reticoli e quantificare le curve di sintonizzazione della selettività delle caratteristiche visive. La video-oculografia a infrarossi ad alta velocità garantisce una misurazione accurata della traiettoria dei movimenti oculari. Gli occhi dei singoli topi sono calibrati per fornire l'opportunità di confrontare gli OKR tra animali di età, sesso e background genetico diversi. La potenza quantitativa di questa tecnica consente di rilevare i cambiamenti nell'OKR quando questo comportamento si adatta plasticamente a causa dell'invecchiamento, dell'esperienza sensoriale o dell'apprendimento motorio; Pertanto, rende questa tecnica una preziosa aggiunta al repertorio di strumenti utilizzati per indagare la plasticità dei comportamenti oculari.
Introduzione
In risposta agli stimoli visivi nell'ambiente, i nostri occhi si muovono per spostare lo sguardo, stabilizzare le immagini retiniche, tracciare bersagli in movimento o allineare le fovee di due occhi con bersagli situati a distanze diverse dall'osservatore, che sono vitali per una corretta visione 1,2. I comportamenti oculomotori sono stati ampiamente utilizzati come modelli attraenti di integrazione sensomotoria per comprendere i circuiti neurali in salute e malattia, almeno in parte a causa della semplicità del sistema oculomotorio3. Controllato da tre paia di muscoli extraoculari, l'occhio ruota nell'alveolo principalmente attorno a tre assi corrispondenti: elevazione e depressione lungo l'asse trasversale, adduzione e abduzione lungo l'asse verticale e intorsione ed estorsione lungo l'asse anteroposteriore 1,2. Un sistema così semplice consente ai ricercatori di valutare i comportamenti oculomotori dei topi in modo semplice e accurato in un ambiente di laboratorio.
Uno dei principali comportamenti oculomotori è il riflesso optocinetico (OKR). Questo movimento oculare involontario è innescato da lente derive o slittamenti di immagini sulla retina e serve a stabilizzare le immagini retiniche mentre la testa di un animale o l'ambiente circostante si muovono 2,4. L'OKR, come paradigma comportamentale, è interessante per i ricercatori per diversi motivi. In primo luogo, può essere stimolato in modo affidabile e quantificato con precisione 5,6. In secondo luogo, le procedure di quantificazione di questo comportamento sono relativamente semplici e standardizzate e possono essere applicate per valutare le funzioni visive di un'ampia coorte di animali7. In terzo luogo, questo comportamento innato è altamente plastico 5,8,9. La sua ampiezza può essere potenziata quando si verificano slittamenti retinici ripetitivi per lungo tempo 5,8,9 o quando il riflesso oculare vestibolare (VOR) del suo partner di lavoro, un altro meccanismo di stabilizzazione delle immagini retiniche innescato dall'input vestibolare2, è compromesso5. Questi paradigmi sperimentali di potenziamento OKR consentono ai ricercatori di svelare le basi del circuito alla base dell'apprendimento oculomotorio.
Due metodi non invasivi sono stati utilizzati principalmente per valutare l'OKR in studi precedenti: (1) video-oculografia combinata con un tamburo fisico 7,10,11,12,13 o (2) determinazione arbitraria dei giri della testa combinata con un tamburo virtuale6,14,15,16. Sebbene le loro applicazioni abbiano fatto scoperte fruttuose nella comprensione dei meccanismi molecolari e circuitali della plasticità oculomotoria, questi due metodi presentano ciascuno alcuni inconvenienti che limitano le loro capacità nell'esaminare quantitativamente le proprietà dell'OKR. In primo luogo, i tamburi fisici, con motivi stampati di strisce o punti bianchi e neri, non consentono cambi facili e rapidi di modelli visivi, il che limita in gran parte la misurazione della dipendenza dell'OKR da alcune caratteristiche visive, come la frequenza spaziale, la direzione e il contrasto delle griglie mobili 8,17. Invece, i test della selettività dell'OKR a queste caratteristiche visive possono beneficiare della stimolazione visiva computerizzata, in cui le caratteristiche visive possono essere convenientemente modificate da una prova all'altra. In questo modo, i ricercatori possono esaminare sistematicamente il comportamento dell'OKR nello spazio dei parametri visivi multidimensionali. Inoltre, il secondo metodo del test OKR riporta solo le soglie dei parametri visivi che innescano OKR distinguibili, ma non le ampiezze dei movimenti oculari o della testa 6,14,15,16. La mancanza di potenza quantitativa impedisce quindi di analizzare la forma delle curve di sintonizzazione e le caratteristiche visive preferite, o di rilevare sottili differenze tra i singoli topi in condizioni normali e patologiche. Per superare le limitazioni di cui sopra, la video-oculografia e la stimolazione visiva virtuale computerizzata sono state combinate per saggiare il comportamento dell'OKR nei recenti studi 5,17,18,19,20. Tuttavia, questi studi pubblicati in precedenza non hanno fornito sufficienti dettagli tecnici o istruzioni dettagliate e, di conseguenza, è ancora difficile per i ricercatori stabilire un tale test OKR per la propria ricerca.
Qui, presentiamo un protocollo per quantificare con precisione la selettività delle caratteristiche visive del comportamento OKR in condizioni fotopiche o scotopiche con la combinazione di video-oculografia e stimolazione visiva virtuale computerizzata. I topi sono fissati alla testa per evitare il movimento oculare evocato dalla stimolazione vestibolare. Una telecamera ad alta velocità viene utilizzata per registrare i movimenti oculari dei topi che osservano le griglie mobili con parametri visivi mutevoli. La dimensione fisica dei bulbi oculari dei singoli topi è calibrata per garantire l'accuratezza della derivazione dell'angolo dei movimenti oculari21. Questo metodo quantitativo permette di confrontare il comportamento OKR tra animali di età o background genetici diversi, o di monitorarne il cambiamento causato da trattamenti farmacologici o dall'apprendimento visuo-motorio.
Protocollo
Tutte le procedure sperimentali eseguite in questo studio sono state approvate dal Comitato per la cura degli animali locali di scienze biologiche, in conformità con le linee guida stabilite dal Comitato per la cura degli animali dell'Università di Toronto e dal Consiglio canadese per la cura degli animali.
1. Impianto di una barra per la testa sulla parte superiore del cranio
NOTA: Per evitare il contributo del comportamento VOR ai movimenti oculari, la testa del mouse viene immobilizzata durante il test OKR. Pertanto, una barra per la testa viene impiantata chirurgicamente sulla parte superiore del cranio.
- Anestetizzare un topo (femmina e maschio C57BL/6 di 2-5 mesi) con una miscela di isoflurano al 4% (v/v) e O2 in una camera a gas. Trasferire il topo su una piattaforma chirurgica personalizzata e ridurre la concentrazione di isoflurano all'1,5%-2%. Monitorare la profondità dell'anestesia controllando la risposta al pizzicamento delle dita dei piedi e la frequenza respiratoria durante l'intervento.
- Posiziona un termoforo sotto il corpo dell'animale per mantenere la sua temperatura corporea. Applicare uno strato di unguento lubrificante per gli occhi su entrambi gli occhi per proteggerli dalla secchezza. Copri gli occhi con un foglio di alluminio per proteggerli dall'illuminazione della luce.
- Iniettare carprofene per via sottocutanea alla dose di 20 mg/kg per ridurre il dolore. Dopo aver bagnato la pelliccia con un detergente per la pelle a base di gluconato di clorexidina, radere la pelliccia sulla parte superiore del cranio. Disinfettare due volte il cuoio capelluto esposto con alcol isopropilico al 70% e alcol clorexidina.
- Iniettare bupivacaina (8 mg/kg) per via sottocutanea nel sito di incisione, quindi rimuovere il cuoio capelluto (~1 cm2) con le forbici per esporre la superficie dorsale del cranio, compreso l'osso frontale posteriore, l'osso parietale e l'osso interparietale.
- Applicare diverse gocce di lidocaina all'1% ed epinefrina 1:100.000 sul cranio esposto per ridurre il dolore locale e il sanguinamento. Raschiare il cranio con una curette Meyhoefer per rimuovere la fascia e pulirlo con soluzione salina tamponata con fosfati (PBS).
NOTA: Il muscolo temporale è separato dal cranio per aumentare la superficie per l'attacco di una barra per la testa. - Asciugare il cranio soffiando delicatamente aria compressa verso la superficie del cranio fino a quando l'umidità non è sparita e l'osso diventa biancastro. Applicare un sottile strato di supercolla sulla superficie esposta del cranio, compreso il bordo del cuoio capelluto tagliato, seguito da uno strato di resina acrilica.
NOTA: La superficie del cranio deve essere priva di sangue o acqua prima dell'applicazione della supercolla. - Posizionare una barra di testa in acciaio inossidabile (vedere la Figura 1A) lungo la linea mediana sulla parte superiore del cranio. Applicare altra resina acrilica, partendo dal bordo della barra di testa fino a quando la base della barra di testa non è completamente incorporata nella resina acrilica. Applicare la resina acrilica due o tre volte per aumentare lo spessore.
- Attendere circa 15 minuti fino a quando la resina acrilica non si indurisce. Iniettare per via sottocutanea 1 mL di soluzione di ringer lattato. Quindi, rimetti il mouse in una gabbia posta su un termoforo fino a quando l'animale non è completamente mobile.
- Lasciare che il topo si riprenda nella gabbia di casa per almeno 5 giorni dopo l'intervento. Una volta che l'animale è in buona forma, fissa la sua testa con la barra della testa nella configurazione OKR per 15-30 minuti per familiarizzare con la fissazione della testa e l'ambiente sperimentale. Ripeti la familiarizzazione una volta al giorno per almeno 3 giorni.
2. Setup del tamburo virtuale e video-oculografia
- Montare tre monitor ortogonalmente l'uno all'altro per formare un involucro quadrato che copra ~270° dell'azimut e 63° dell'elevazione nello spazio visivo (Figura 1B a sinistra).
- Con una scheda grafica dedicata, unisci i tre monitor in un semplice display per garantire la sincronizzazione su tutti i monitor.
- Calibrare la luminanza dei monitor come descritto di seguito.
- Accendere il computer a cui sono collegati i monitor e attendere 15 minuti. Il riscaldamento è essenziale per avere una luminanza stabile.
- Modificare sistematicamente l'impostazione della luminosità sul monitor da 0 a 100 con incrementi di 25.
- Per ogni valore di luminosità, misurare la luminanza dei monitor sotto vari valori di pixel (0-255, incrementi di 15) con un misuratore di luminanza.
- Adattare la relazione tra luminanza e luminosità per il valore dei pixel 255 con la regressione lineare e stimare il valore di luminosità che dà origine a 160 cd/m2.
- Per ogni valore di pixel utilizzato nella misurazione della luminanza (passaggio 2.3.3), stimare la luminanza per il valore di luminosità derivato nel passaggio 2.3.4 in base alla regressione lineare. Utilizzare la funzione di potenza lum = A * pixel γ per adattare la relazione tra il nuovo set di valori di luminanza (sotto il valore di luminosità derivato in 2.3.4) e i corrispondenti valori di pixel per derivare il fattore gamma γe il coefficiente A. Questi verranno utilizzati per generare reticoli sinusoidali dei valori di luminanza desiderati.
- Impostare la luminosità di tutti e tre i monitor sui valori derivati nel passaggio 2.3.4 per assicurarsi che i valori di luminanza siano gli stessi per lo stesso valore di pixel.
- Genera un tamburo virtuale, che viene utilizzato per stimolare il comportamento OKR, con il toolkit di stimolazione visiva, come descritto di seguito.
- Presentare un reticolo sinusoidale verticale sui monitor e regolare il periodo (spaziatura tra le strisce) lungo l'azimut per garantire che la proiezione del reticolo sull'occhio abbia una frequenza spaziale costante (reticolo a tamburo; Figura 1B al centro e a destra).
- Assicurarsi che la testa dell'animale fissata al centro del recinto in modo che veda la griglia abbia una frequenza spaziale costante sulla superficie del tamburo virtuale.
- Modificare i parametri del reticolo mobile, come l'ampiezza oscillatoria, la frequenza spaziale, la frequenza temporale/oscillante, la direzione, il contrasto, ecc., nei codici di stimolazione visiva. Utilizzare due tipi di movimento visivo: (1) il reticolo si sposta in senso orario o antiorario in modo oscillatorio seguendo una funzione sinusoidale:
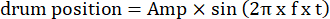
Qui, Amp è l'ampiezza della traiettoria del tamburo, f è la frequenza di oscillazione e t è il tempo (ampiezza di oscillazione: 5°; frequenza spaziale del reticolo: 0,04-0,45 cpd; frequenza di oscillazione: 0,1-0,8 Hz, corrispondente a una velocità di picco dello stimolo di 3,14-25,12 °/s [velocità del tamburo = Amp x 2π x f x cos (2π x f x t); contrasto: 80%-100%; luminanza media: 35-45 cd/m2; (2) il reticolo si sposta unidirezionalmente a velocità costante: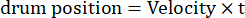
(Frequenza spaziale: 0,04-0,64 cpd; frequenza temporale: 0,25-1 Hz; velocità del tamburo = frequenza temporale/frequenza spaziale.)
- Impostare la video-oculografia come descritto di seguito.
- Per evitare il blocco del campo visivo dell'animale, posizionare uno specchio a infrarossi (IR) a 60° dalla linea mediana per formare un'immagine dell'occhio destro.
- Posizionate una telecamera a infrarossi sul lato destro dietro il mouse (Figura 1C a sinistra) per acquisire un'immagine dell'occhio destro.
- Montare la telecamera IR ad alta velocità su un braccio che consenta alla telecamera di ruotare di ± 10° attorno all'immagine dell'occhio destro (Figura 1C a destra).
- Utilizzare un fotodiodo collegato a uno dei monitor per fornire un segnale elettrico per sincronizzare i tempi della video-oculografia e della stimolazione visiva.
- Posizionare quattro diodi a emissione di luce IR (LED) supportati da bracci a collo d'oca attorno all'occhio destro per fornire un'illuminazione IR dell'occhio.
- Posizionare due LED IR sulla telecamera per fornire riferimenti di riflessione corneale (CR): uno è fissato sopra la telecamera (X-CR), mentre l'altro è sul lato sinistro della telecamera (Y-CR; Figura 1D).
- Misurare l'ingrandimento ottico del sistema di video-oculografia con un vetrino di calibrazione.
NOTA: I CR di riferimento vengono utilizzati per annullare i movimenti oculari traslazionali quando l'angolo dell'occhio viene calcolato in base ai movimenti oculari rotazionali.
- Fissare la testa dell'animale al centro del recinto formato dai monitor, come descritto di seguito.
- Fissa la testa dell'animale con la piastra della testa al centro del rig e mettila rivolta in avanti. Regolare l'inclinazione della testa in modo che gli occhi sinistro e destro siano livellati e gli angoli nasali e temporali degli occhi siano allineati orizzontalmente (Figura 1E).
- Muovere la testa dell'animale orizzontalmente mediante una regolazione grossolana fornita dall'apparecchio di fissazione della testa e una regolazione fine fornita da un tavolino di traslazione 2D, e verticalmente attraverso l'apparecchio di fissazione della testa e una coppia di supporti per pali, fino a quando l'occhio destro dell'animale non appare nel video in diretta della telecamera. Prima della calibrazione e della misurazione dei movimenti oculari, sovrapporre l'immagine dell'occhio destro dell'animale riflessa dallo specchio caldo con il punto di rotazione del braccio della telecamera (vedere i dettagli al punto 3.4 di seguito).
- Costruisci un involucro personalizzato attorno al rig OKR per bloccare la luce della stanza (Figura 1F).
3. Calibrazione dei movimenti oculari
NOTA: I movimenti oculari rotazionali sono calcolati in base ai movimenti della pupilla e al raggio dell'orbita dei movimenti pupillari (Rp, la distanza dal centro della pupilla al centro del bulbo oculare). Per ogni singolo mouse, questo raggio viene misurato sperimentalmente21.
- Fissare la testa dell'animale al centro del recinto formato dai tre monitor, come descritto al punto 2.6.1.
- Accendere la fotocamera e regolare i quattro LED che circondano l'occhio destro per ottenere un'illuminazione IR uniforme.
- Sotto guida visiva, regolare la posizione dell'occhio destro fino a quando non appare al centro del video, come descritto nel passaggio 2.6.2.
- Allineare l'immagine virtuale dell'occhio destro con il punto di rotazione del braccio della fotocamera, come descritto di seguito.
- Ruotare manualmente il braccio della fotocamera all'estremità sinistra (-10°). Spostare manualmente la posizione dell'occhio destro dell'animale sul piano orizzontale perpendicolare all'asse ottico con regolazione fine del tavolino di traslazione 2D (Figura 1C, freccia verde), fino a quando l'X-CR non si trova al centro orizzontale dell'immagine.
- Ruotare manualmente il braccio della fotocamera all'altra estremità (+10°). Se l'X-CR si allontana dal centro dell'immagine, spostare l'occhio destro lungo l'asse ottico con una regolazione fine fino a quando l'X-CR non arriva al centro (Figura 1C, freccia blu).
- Ripetere i passaggi 3.4.1-3.4.2 alcune volte fino a quando l'X-CR rimane al centro quando il braccio della fotocamera oscilla verso sinistra e verso destra. Se l'occhio destro si muove nel mezzo di una ripetizione, riavvia il processo di regolazione.
- Misurare la distanza verticale tra Y-CR e X-CR dopo aver bloccato il braccio della telecamera in posizione centrale. Accendere il LED Y-CR e registrare la sua posizione sul video, quindi passare al LED X-CR e registrare la sua posizione.
NOTA: La distanza verticale tra Y-CR e X-CR verrà utilizzata per derivare la posizione dell'Y-CR durante la misurazione dei movimenti oculari in cui è acceso solo il LED X-CR. - Misurare il raggio di rotazione della pupilla Rp, come descritto di seguito.
- Ruotare il braccio della telecamera all'estremità sinistra (-10°) e registrare le posizioni della pupilla (Pp1) e X-CR (PCR1) sul video.
- Quindi, ruotare il braccio della telecamera all'estremità destra (+10°) e registrare le posizioni della pupilla (Pp2) e X-CR (PCR2) sul video. Ripeti questo passaggio più volte.
NOTA: L'occhio destro dell'animale deve rimanere fermo durante ogni ripetizione, in modo che la quantità di movimenti della pupilla nel filmato rifletta accuratamente il grado di oscillazione del braccio della videocamera. - Sulla base dei valori sopra riportati, calcolare il raggio di rotazione della pupilla Rp (Figura 2A) con la seguente formula:
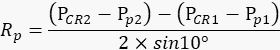
NOTA: La distanza tra il riflesso corneale e il centro della pupilla nello spazio fisico viene calcolata in base alla loro distanza nel filmato:
PCR - Pp = numero di pixel nel filmato x dimensione dei pixel del chip della fotocamera x ingrandimento
- Sviluppare la relazione tra Rp e diametro della pupilla, come descritto di seguito. Rp cambia quando la pupilla si dilata o si restringe; prossimamente, il suo valore è inversamente proporzionale alla dimensione della pupilla (Figura 2B in alto).
- Modificare sistematicamente la luminanza dei monitor da 0 a 160 cd/m2 per regolare la dimensione della pupilla.
- Per ogni valore di luminanza, ripetere il passaggio 3.6 8-10 volte e registrare il diametro della pupilla.
- Applicare la regressione lineare alla relazione tra Rp e diametro della pupilla in base ai valori misurati sopra per derivare la pendenza e l'intercetta (Figura 2B in basso).
NOTA: I valori anomali causati da movimenti oculari occasionali vengono rimossi prima del montaggio lineare. Per misurazioni ripetitive in più sessioni, la calibrazione deve essere eseguita una sola volta per un animale, a meno che il suo occhio non diventi più grande durante l'esperimento.
4. Registra i movimenti oculari dell'OKR
- Fissare un mouse nel rig seguendo i passaggi 3.1-3.4. Saltare questo passaggio se la registrazione avviene subito dopo l'esecuzione della calibrazione. Bloccare il braccio della fotocamera in posizione centrale.
- Impostare i monitor e l'animale per l'OKR scotopico come descritto di seguito. Salta questo passaggio per l'OKR fotografico.
- Copri lo schermo di ogni monitor con un filtro personalizzato, composto da cinque strati di pellicola a densità neutra (ND) da 1,2. Assicurarsi che la luce non fuoriesca attraverso lo spazio tra il filtro e il monitor.
- Spegni la luce della stanza. I seguenti passaggi vengono eseguiti con l'aiuto di un occhiale IR.
- Applicare una goccia di soluzione di pilocarpina (2% in soluzione fisiologica) sull'occhio destro e attendere 15 min. Assicurarsi che la goccia rimanga sull'occhio e non venga rimossa dal mouse. Se la soluzione viene rimossa dall'animale, applicare un'altra goccia di soluzione di pilocarpina. Questo riduce la pupilla a una dimensione adeguata per il tracciamento oculare in condizioni scotopiche.
NOTA: In condizioni scotopiche, la pupilla si dilata sostanzialmente in modo che il suo bordo sia parzialmente nascosto dietro la palpebra. Ciò influisce sulla precisione della stima del centro pupillare mediante video-oculografia. Il restringimento farmacologico della pupilla dell'occhio destro diminuisce il suo input visivo, e quindi gli stimoli visivi vengono presentati all'occhio sinistro. - Sciacquare l'occhio destro con soluzione fisiologica per lavare via accuratamente la soluzione di pilocarpina. Abbassare la tenda per sigillare completamente l'involucro, in modo da evitare che la luce parassita interferisca con la visione scotopica.
- Dare all'animale 5 minuti per adattarsi completamente all'ambiente scotopico prima di iniziare il test OKR.
- Eseguire il software di stimolazione visiva e il software di tracciamento oculare. Per la misurazione fotopica dell'OKR, assicurarsi che il reticolo del tamburo oscilli orizzontalmente con una traiettoria sinusoidale; per la misurazione dell'OKR scotopico, assicurarsi che il reticolo del tamburo si sposti a velocità costante da sinistra a destra, che è la direzione temporo-nasale in riferimento all'occhio sinistro.
NOTA: Quando la pupilla dell'occhio destro, ma non dell'occhio sinistro, viene ridotta dalla pilocarpina in condizioni scotopiche, l'OKR suscitato dalla stimolazione oscillatoria del tamburo è altamente asimmetrico. Pertanto, per la misurazione dell'OKR scotopico, l'occhio sinistro viene stimolato mentre viene monitorato il movimento dell'occhio destro. - Il software di tracciamento oculare misura automaticamente le dimensioni della pupilla, la posizione CR e la posizione della pupilla per ciascun fotogramma e calcola l'angolo di posizione dell'occhio in base alla seguente formula (Figura 2C):
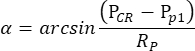
Qui, P CR è la posizioneCR, P p è la posizione della pupilla e Rp è il raggio di rotazione della pupilla. La distanza tra la riflessione corneale e il centro della pupilla nello spazio fisico viene calcolata in base alla loro distanza nel filmato:
PCR - Pp = numero di pixel nel filmato x dimensione dei pixel del chip della fotocamera x ingrandimento
Rp della dimensione della pupilla corrispondente è derivato in base al modello di regressione lineare nel passaggio 3.7.3 (Figura 2B in basso).
5. Analisi dei movimenti oculari dell'OKR con il software di analisi dell'occhio
- Elaborare le tracce oculari utilizzando un filtro mediano (finestra del filtro = 0,05 s) per rimuovere il rumore ad alta frequenza (Figura 3A al centro).
- Rimuovere le saccadi o il nistagmo come descritto di seguito.
- Stimare la velocità dell'occhio calcolando la derivata del primo ordine dei movimenti oculari (Figura 3A in basso). Identificare le saccadi o il nistagmo applicando una soglia di velocità di 50 °/s (Figura 3A in basso).
- Sostituire le saccadi o il nistagmo estrapolando le posizioni degli occhi durante questi movimenti oculari veloci dal segmento precedente alle saccadi o al nistagmo in base alla regressione lineare (Figura 3B).
- Calcolare l'ampiezza dei movimenti oculari OKR mediante trasformata di Fourier veloce (algoritmo di Goertzel) se il reticolo del tamburo oscilla (Figura 3C), oppure calcolare la velocità media dei movimenti oculari durante la stimolazione visiva se il reticolo del tamburo si muove a velocità costante in una direzione (Figura 3B in basso).
NOTA: L'ampiezza dei movimenti oculari oscillatori derivata dalla trasformata di Fourier è simile all'ampiezza derivata dall'adattamento della traiettoria dell'occhio con una funzione sinusoidale (Figura 3D). - Calcola il guadagno OKR. Per il movimento oscillatorio del tamburo, il guadagno OKR è definito come il rapporto tra l'ampiezza dei movimenti oculari e l'ampiezza dei movimenti del tamburo (Figura 3C a destra). Per il movimento unidirezionale del tamburo, il guadagno OKR è definito come il rapporto tra la velocità dell'occhio e la velocità del reticolo del tamburo (Figura 3B in basso).
Risultati
Con la procedura sopra descritta, abbiamo valutato la dipendenza dell'OKR da diverse caratteristiche visive. Le tracce di esempio mostrate qui sono state derivate utilizzando i codici di analisi forniti nel file di codifica supplementare 1 e il file grezzo delle tracce di esempio è disponibile nel file di codifica supplementare 2. Quando il reticolo del tamburo si spostava in una traiettoria sinusoidale (0,4 Hz), l'occhio dell'animale seguiva automaticamente il movimento del reticolo in...
Discussione
Il metodo del test comportamentale OKR qui presentato offre diversi vantaggi. In primo luogo, la stimolazione visiva generata dal computer risolve i problemi intrinseci dei tamburi fisici. Affrontando il problema che i tamburi fisici non supportano l'esame sistematico della frequenza spaziale, della direzione o dell'accordatura del contrasto8, il tamburo virtuale consente di modificare questi parametri visivi su base trial-by-trial, facilitando così un'analisi sistematica e quantitativa della sel...
Divulgazioni
Gli autori dichiarano di non avere interessi contrastanti.
Riconoscimenti
Siamo grati a Yingtian He per aver condiviso i dati della sintonizzazione della direzione. Questo lavoro è stato sostenuto da sovvenzioni della Fondazione canadese per l'innovazione e del Fondo di ricerca dell'Ontario (progetto CFI/ORF n. 37597), NSERC (RGPIN-2019-06479), CIHR (Project Grant 437007) e Connaught New Researcher Awards.
Materiali
| Name | Company | Catalog Number | Comments |
| 2D translational stage | Thorlabs | XYT1 | |
| Acrylic resin | Lang Dental | B1356 | For fixing headplate on skull and protecting skull |
| Bupivacaine | STERIMAX | ST-BX223 | Bupivacaine Injection BP 0.5%. Local anesthesia |
| Carprofen | RIMADYL | 8507-14-1 | Analgesia |
| Compressed air | Dust-Off | ||
| Eye ointment | Alcon | Systane | For maintaining moisture of eyes |
| Graphic card | NVIDIA | Geforce GTX 1650 or Quadro P620. | For generating single screen among three monitors |
| Heating pad | Kent Scientific | HTP-1500 | For maintaining body temperature |
| High-speed infrared (IR) camera | Teledyne Dalsa | G3-GM12-M0640 | For recording eye rotation |
| IR LED | Digikey | PDI-E803-ND | For CR reference and the illumination of the eye |
| IR mirror | Edmund optics | 64-471 | For reflecting image of eye |
| Isoflurane | FRESENIUS KABI | CP0406V2 | |
| Labview | National instruments | version 2014 | eye tracking |
| Lactated ringer | BAXTER | JB2324 | Water and energy supply |
| Lidocaine and epinephrine mix | Dentsply Sirona | 82215-1 | XYLOCAINE. Local anesthesia |
| Luminance Meter | Konica Minolta | LS-150 | for calibration of monitors |
| Matlab | MathWorks | version xxx | analysis of eye movements |
| Meyhoefer Curette | World Precision Instruments | 501773 | For scraping skull and removing fascia |
| Microscope calibration slide | Amscope | MR095 | to measure the magnification of video-oculography |
| Monitors | Acer | B247W | Visual stimulation |
| Neutral density filter | Lee filters | 299 | to generate scotopic visual stimulation |
| Nigh vision goggle | Alpha optics | AO-3277 | for scotopic OKR |
| Photodiode | Digikey | TSL254-R-LF-ND | to synchronize visual stimulation and video-oculography |
| Pilocarpine hydrochloride | Sigma-Aldrich | P6503 | |
| Post | Thorlabs | TR1.5 | |
| Post holder | Thorlabs | PH1 | |
| PsychoPy | open source software | version xxx | visual stimulation toolkit |
| Scissor | RWD | S12003-09 | For skin removal |
| Superglue | Krazy Glue | Type: All purpose. For adhering headplate on the skull |
Riferimenti
- Gerhard, D. Neuroscience. 5th Edition. Yale Journal of Biology and Medicine. , (2013).
- Distler, C., Hoffmann, K. P. . The Oxford Handbook of Eye Movement. , 65-83 (2011).
- Sereno, A. B., Bolding, M. S. . Executive Functions: Eye Movements and Human Neurological Disorders. , (2017).
- Giolli, R. A., Blanks, R. H. I., Lui, F. The accessory optic system: basic organization with an update on connectivity, neurochemistry, and function. Progress in Brain Research. 151, 407-440 (2006).
- Liu, B. H., Huberman, A. D., Scanziani, M. Cortico-fugal output from visual cortex promotes plasticity of innate motor behaviour. Nature. 538 (7625), 383-387 (2016).
- Prusky, G. T., Alam, N. M., Beekman, S., Douglas, R. M. Rapid quantification of adult and developing mouse spatial vision using a virtual optomotor system. Investigative Ophthalmology & Visual Science. 45 (12), 4611-4616 (2004).
- Stahl, J. S., van Alphen, A. M., De Zeeuw, C. I. A comparison of video and magnetic search coil recordings of mouse eye movements. Journal of Neuroscience Methods. 99 (1-2), 101-110 (2000).
- Faulstich, B. M., Onori, K. A., du Lac, S. Comparison of plasticity and development of mouse optokinetic and vestibulo-ocular reflexes suggests differential gain control mechanisms. Vision Research. 44 (28), 3419-3427 (2004).
- Katoh, A., Kitazawa, H., Itohara, S., Nagao, S. Dynamic characteristics and adaptability of mouse vestibulo-ocular and optokinetic response eye movements and the role of the flocculo-olivary system revealed by chemical lesions. Proceedings of the National Academy of Sciences. 95 (13), 7705-7710 (1998).
- Cahill, H., Nathans, J. The optokinetic reflex as a tool for quantitative analyses of nervous system function in mice: application to genetic and drug-induced variation. PLoS One. 3 (4), 2055 (2008).
- Cameron, D. J., et al. The optokinetic response as a quantitative measure of visual acuity in zebrafish. Journal of Visualized Experiments. (80), 50832 (2013).
- de Jeu, M., De Zeeuw, C. I. Video-oculography in mice. Journal of Visualized Experiments. (65), e3971 (2012).
- Kodama, T., du Lac, S. Adaptive acceleration of visually evoked smooth eye movements in mice. The Journal of Neuroscience. 36 (25), 6836-6849 (2016).
- Doering, C. J., et al. Modified Ca(v)1.4 expression in the Cacna1f(nob2) mouse due to alternative splicing of an ETn inserted in exon 2. PLoS One. 3 (7), e2538 (2008).
- Shi, C., et al. Optimization of optomotor response-based visual function assessment in mice. Scientific Reports. 8 (1), 9708 (2018).
- Waldner, D. M., et al. Transgenic expression of Cacna1f rescues vision and retinal morphology in a mouse model of congenital stationary night blindness 2A (CSNB2A). Translational Vision Science & Technology. 9 (11), 19 (2020).
- Tabata, H., Shimizu, N., Wada, Y., Miura, K., Kawano, K. Initiation of the optokinetic response (OKR) in mice. Journal of Vision. 10 (1), 1-17 (2010).
- Al-Khindi, T., et al. The transcription factor Tbx5 regulates direction-selective retinal ganglion cell development and image stabilization. Current Biology. 32 (19), 4286-4298 (2022).
- Harris, S. C., Dunn, F. A. Asymmetric retinal direction tuning predicts optokinetic eye movements across stimulus conditions. eLife. 12, e81780 (2023).
- van Alphen, B., Winkelman, B. H., Frens, M. A. Three-dimensional optokinetic eye movements in the C57BL/6J mouse. Investigative Ophthalmology & Visual Science. 51 (1), 623-630 (2010).
- Stahl, J. S. Calcium channelopathy mutants and their role in ocular motor research. Annals of the New York Academy of Sciences. 956, 64-74 (2002).
- Endo, S., et al. Dual involvement of G-substrate in motor learning revealed by gene deletion. Proceedings of the National Academy of Sciences. 106 (9), 3525-3530 (2009).
- Thomas, B. B., Seiler, M. J., Sadda, S. R., Coffey, P. J., Aramant, R. B. Optokinetic test to evaluate visual acuity of each eye independently. Journal of Neuroscience Methods. 138 (1-2), 7-13 (2004).
- Burroughs, S. L., Kaja, S., Koulen, P. Quantification of deficits in spatial visual function of mouse models for glaucoma. Investigative Ophthalmology & Visual Science. 52 (6), 3654-3659 (2011).
- Wakita, R., et al. Differential regulations of vestibulo-ocular reflex and optokinetic response by β- and α2-adrenergic receptors in the cerebellar flocculus. Scientific Reports. 7 (1), 3944 (2017).
- Dehmelt, F. A., et al. Spherical arena reveals optokinetic response tuning to stimulus location, size, and frequency across entire visual field of larval zebrafish. eLife. 10, e63355 (2021).
- Magnusson, M., Pyykko, I., Jantti, V. Effect of alertness and visual attention on optokinetic nystagmus in humans. American Journal of Otolaryngology. 6 (6), 419-425 (1985).
- Collins, W. E., Schroeder, D. J., Elam, G. W. Effects of D-amphetamine and of secobarbital on optokinetic and rotation-induced nystagmus. Aviation, Space, and Environmental Medicine. 46 (4), 357-364 (1975).
- Reimer, J., et al. Pupil fluctuations track fast switching of cortical states during quiet wakefulness. Neuron. 84 (2), 355-362 (2014).
- Sakatani, T., Isa, T. PC-based high-speed video-oculography for measuring rapid eye movements in mice. Neuroscience Research. 49 (1), 123-131 (2004).
- Sakatani, T., Isa, T. Quantitative analysis of spontaneous saccade-like rapid eye movements in C57BL/6 mice. Neuroscience Research. 58 (3), 324-331 (2007).
- Vinck, M., Batista-Brito, R., Knoblich, U., Cardin, J. A. Arousal and locomotion make distinct contributions to cortical activity patterns and visual encoding. Neuron. 86 (3), 740-754 (2015).
- Bradley, M. M., Miccoli, L., Escrig, M. A., Lang, P. J. The pupil as a measure of emotional arousal and autonomic activation. Psychophysiology. 45 (4), 602-607 (2008).
- Hess, E. H., Polt, J. M. Pupil size as related to interest value of visual stimuli. Science. 132 (3423), 349-350 (1960).
- Di Stasi, L. L., Catena, A., Canas, J. J., Macknik, S. L., Martinez-Conde, S. Saccadic velocity as an arousal index in naturalistic tasks. Neuroscience and Biobehavioral Reviews. 37 (5), 968-975 (2013).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon