È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Un sistema di test di flessione dorsale passiva della caviglia per un modello in vivo di tendinopatia indotta da uso eccessivo
In questo articolo
Riepilogo
Questo protocollo presenta un sistema di test utilizzato per indurre lesioni da fatica quantificabili e controllate in un tendine d'Achille di ratto per un modello in vivo di tendinopatia indotta da uso eccessivo. La procedura consiste nel fissare la caviglia del ratto a un attuatore articolare che esegue la flessione dorsale passiva della caviglia con uno script MATLAB scritto su misura.
Abstract
La tendinopatia è una condizione tendinea cronica che provoca dolore e perdita di funzionalità ed è causata da un sovraccarico ripetuto del tendine e da tempi di recupero limitati. Questo protocollo descrive un sistema di test che applica ciclicamente carichi meccanici tramite flessione dorsale passiva al tendine d'Achille del ratto. Il codice personalizzato consiste in misurazioni di carico pre e post-ciclico per valutare gli effetti del protocollo di carico insieme al regime di carico di fatica ciclico basato sul controllo di retroazione.
Per questo studio sono stati utilizzati 25 ratti Sprague-Dawley, con 5 ratti per gruppo che hanno ricevuto 500, 1.000, 2.000, 3.600 o 7.200 cicli di carichi di fatica. Sono state calcolate le differenze percentuali tra le misure di carico pre e post-ciclico dell'isteresi, della sollecitazione di picco e dei moduli di carico e scarico. I risultati dimostrano che il sistema può indurre vari gradi di danno al tendine d'Achille in base al numero di carichi applicati. Questo sistema offre un approccio innovativo per applicare diversi gradi quantificati e fisiologici di carichi ciclici al tendine d'Achille per un modello in vivo di lesione tendinea da uso eccessivo indotta dalla fatica.
Introduzione
Poiché i tendini collegano il muscolo all'osso e subiscono movimenti ripetitivi quotidiani per tutta la loro vita, sono altamente inclini a lesioni da uso eccessivo che sono dolorose e limitanti e provocano una compromissione della funzione meccanica, colpendo il 30-50% della popolazione1. Le tendinopatie sono condizioni croniche considerate lesioni da uso eccessivo a causa di movimenti di affaticamento ripetitivi e guarigione inadeguata ai livelli pre-lesione. Sia gli arti superiori che quelli inferiori sono comunemente colpiti, tra cui la cuffia dei rotatori, il gomito, il tendine d'Achille e il tendine rotuleo 2,3,4,5. La tendinopatia del tendine d'Achille è comune nelle attività che coinvolgono la corsa e il salto, in particolare gli atleti coinvolti nell'atletica leggera, nella corsa di media e lunga distanza, nel tennis e in altri sport con la palla, colpendo il 7-9% dei corridori 6,7. Le lesioni dovute alla corsa e al salto possono anche causare una limitata flessione dorsale della caviglia, che è un fattore di rischio per tendinopatie achille e rotulee 8,9,10. Pertanto, c'è bisogno di una migliore valutazione e caratterizzazione della tendinopatia, che questo studio può fornire come modello di ratto di flessione dorsale passiva della caviglia per lesioni del tendine d'Achille da uso eccessivo.
Il lavoro precedente che ha utilizzato modelli animali di piccole dimensioni è stato finalizzato allo studio dello sviluppo e dei marcatori della tendinopatia. Questi includono esercizi su tapis roulant, allungamento ripetitivo, carico tendineo diretto, iniezioni di collagenasi, chirurgia e studi in vitro 11,12,13,14,15,16. Sebbene la letteratura abbia beneficiato dell'identificazione di marcatori di danno derivanti dall'impiego di questi modelli di tendinopatia, le limitazioni includono il carico del tendine in movimenti articolari non fisiologicamente rilevanti, come nel caso del carico diretto del tendine, la non misurazione diretta dei carichi applicati, come per gli studi sul tapis roulant, e il non utilizzo di un uso eccessivo fisiologico, come nel caso delle iniezioni di collagenasi. tra gli altri. A tal fine, questo studio mirava a sviluppare un sistema che applica in modo non invasivo carichi quantificati al tendine d'Achille con l'applicazione di studi di tendinopatia indotta da uso eccessivo per colmare le lacune nei modelli di piccoli animali precedentemente sviluppati per la tendinopatia. Abbiamo condotto uno studio pilota per dimostrare che il sistema induce cambiamenti riproducibili nelle proprietà meccaniche in una serie di cicli di carico. Questo sistema consente al movimento e al carico fisiologicamente rilevanti di indurre un uso eccessivo, quantificando e misurando contemporaneamente le forze applicate e sperimentate dal tendine durante il regime di carico.
Protocollo
Questo studio è stato condotto in base all'approvazione dell'Institutional Animal Care and Use Committee (IACUC) presso il Beth Israel Deaconess Medical Center. Gli animali sono stati anestetizzati utilizzando isoflurano al 5% per l'induzione e al 2,5% per il mantenimento, ed è stata prestata attenzione per evitare l'ipotermia.
1. Impostazione del sistema di test
- Controlla la rotazione passiva della caviglia tramite un motore passo-passo per applicare una rotazione e una coppia costanti. Controlla il motore passo-passo con un microcontrollore. Utilizzare gli input del sistema di posizione e orientamento 3D per contrassegnare i gradi di rotazione. Utilizzare le uscite del sensore di coppia per fornire un controllo di retroazione per aumentare l'angolo di flessione dorsale se il limite alla soglia non viene raggiunto.
- Per iniziare, collegare il microcontrollore, il sensore di coppia, il posizionamento elettromagnetico 3D e il sistema di orientamento a un computer e all'alimentatore. Controlla il sistema personalizzato utilizzando un codice MATLAB sviluppato internamente (Figura 1). Scarica i file di codice MATLAB da GitHub e segui le istruzioni specifiche per l'esecuzione del codice dalle istruzioni della pagina GitHub (https://github.com/Nazarian-Lab/PassiveAnkleDorsiflexionSystem).
- Apri MATLAB con i file di codice. Aprire il software PDImfc per collegare il sistema di posizionamento e orientamento elettromagnetico 3D al programma MATLAB. Fare clic su Connetti | P&O continuo | StartSockExport(). Tenere aperta l'applicazione in background.
2. Ex-vivo e post mortem
- Sopprimere sei ratti Sprague-Dawley di 13 settimane tramite inalazione di CO2 e un metodo secondario di eutanasia tramite toracotomia. Sezionare il tendine d'Achille destro con il calcagno e la giunzione miotendinea intatti. Congelare a -20°C per eseguire prove meccaniche in un secondo momento. Dopo che il tendine è stato scongelato, sezionato con precisione e preparato per i test meccanici, eseguire il carico di trazione fino alla rottura per ottenere la resistenza alla trazione (UTS) del tendine (precarico a 0,1 N, precondizionamento per 10 cicli da 0,1 a 1 N, rampa fino alla rottura a uno spostamento costante di 0,1 mm/s). Utilizzare il 15% dell'UTS come input per consentire al sistema di eseguire il precondizionamento per una fase successiva, come descritto nel passaggio 3.4.
- Sopprimere un altro gruppo di cinque animali con la stessa procedura per le misurazioni del momento, del braccio e della deformazione. Eseguire una radiografia della gamba sinistra con la caviglia in flessione dorsale a 90° accanto a un righello come riferimento. Aprire l'immagine radiografica nelle Figi, utilizzando il righello nell'immagine come riferimento, misurare il braccio del momento tendineo dal centro di rotazione dell'articolazione della caviglia alla parte posteriore della caviglia da utilizzare come input nel codice MATLAB per convertire la forza in ingresso per il precondizionamento descritto nel passaggio 2.1 nel valore di coppia corrispondente e la conversione tra coppia e forza in uscita per l'analisi dei dati.
- Immobilizzare l'arto posteriore sinistro fissando due stecche per posizionare il ginocchio in piena estensione. Piegare leggermente la caviglia spingendo sulle dita dei piedi per assicurarsi che la rotazione della caviglia avvenga a causa del tendine isolato piuttosto che coinvolgere i tessuti molli circostanti ed è in tensione. Se non è in tensione o se c'è movimento nel ginocchio, richiudere la stecca.
- Esporre il tendine rimuovendo la pelle intorno al tendine d'Achille. Metti la colla su una perlina di alluminio da 1/32 di pollice, posizionala sul tendine libero più vicino alla giunzione miotendinea del tendine d'Achille e usa un batuffolo di cotone con soluzione fisiologica per rimuovere la colla in eccesso. Applicare ripetutamente la soluzione fisiologica sul tendine d'Achille durante il resto della procedura per garantire l'umidità del tessuto.
- Misurare l'area della sezione trasversale del tendine utilizzando un calibro digitale prima di applicare qualsiasi carico. Supponiamo che il tendine sia un'ellisse e misura la larghezza e lo spessore in triplice.
- Posiziona il ratto sulla piattaforma per tutto il corpo in posizione prona. Fissare la caviglia sull'attuatore articolare con una fascetta intorno alla caviglia e un'altra intorno alle dita dei piedi e fissare la spaccatura del ginocchio con due fascette. Ruotare l'asse in modo che la caviglia sia in piena flessione plantare.
- Collegare la penna di digitalizzazione del sistema di posizionamento e orientamento elettromagnetico 3D al computer e accendere l'alimentazione.
- Eseguire il codice di sistema (descritto in modo più dettagliato nel passaggio 3) per il numero specificato di cicli (in questo studio, sei ratti sottoposti a eutanasia hanno ricevuto 7.200 cicli).
- A 0, 500, 1.000, 2.000, 3.600 e 7.200 cicli per le misurazioni della deformazione ex vivo, mettere in pausa il regime di carico ciclico e misurare la lunghezza del tendine dal calcagno al tallone di alluminio con incrementi di 5° da 0 a 40° di flessione dorsale (il limite di attuazione dovuto ai vincoli fisici del sistema) utilizzando la penna di digitalizzazione 3D in triplice copia in modo alternato.
- Calcolare la deformazione tendinea a diversi angoli utilizzando le lunghezze ottenute dal punto 2.9, dove la lunghezza iniziale è a 0° di flessione dorsale per ogni numero di ciclo. Eseguire un adattamento lineare per ottenere la relazione tra l'angolo di flessione dorsale e la deformazione a ciascun numero di ciclo. Utilizzare questa relazione per convertire i dati angolari grezzi in deformazione per l'analisi dei dati.
- Calcolare l'area della sezione trasversale del tendine utilizzando un calibro digitale a 40° di flessione dorsale assumendo l'incomprimibilità (volume costante) con le misure della lunghezza del tendine a 0° e 40° e l'area della sezione trasversale misurata a 0°. Utilizzare quest'area della sezione trasversale per ogni numero di cicli per convertire la forza in sollecitazione per l'analisi dei dati (sollecitazione = forza / area della sezione trasversale).
3. Protocollo di carico meccanico
- Per questa sezione dello studio, sono stati utilizzati 25 ratti femmina di Sprague-Dawley di 11 settimane, con 5 ratti ciascuno assegnati in modo casuale a ricevere 500, 1.000, 2.000, 3.600 o 7.200 cicli di carico di fatica.
NOTA: Il precondizionamento, la calibrazione iniziale e la pre e post-misurazione richiedono circa 15 minuti per essere eseguiti e il regime di carico a fatica ciclico richiede 1 secondo per ciclo. Pertanto, il tempo più lungo in cui il ratto è sotto anestesia è di circa 2 ore, che è stato eseguito secondo i protocolli approvati dalla IACUC. - Collegare il microcontrollore, il sensore di coppia, il posizionamento elettromagnetico 3D e il sistema di orientamento a un computer e all'alimentatore. Controlla il sistema personalizzato utilizzando il codice MATLAB sviluppato internamente (Figura 1).
- Accendi il computer e apri MATLAB con i file di codice. Aprire il software PDImfc per collegare il sistema di posizionamento e orientamento elettromagnetico 3D al programma MATLAB. Fare clic su Connetti | P&O continuo | StartSockExport(). Tenere aperta l'applicazione in background.
- Indurre l'anestesia con isoflurano al 5% per inalazione in una camera di induzione. Dopo l'induzione, fissare l'animale sulla piattaforma per tutto il corpo con un elemento riscaldante a base d'acqua attaccato per mantenere la temperatura e sostenere l'anestesia con isoflurano al 2,5% tramite un attacco a cono nasale. Utilizzare un unguento umido sugli occhi per prevenire la secchezza durante l'anestesia.
- Posiziona il ratto sulla piattaforma per tutto il corpo in posizione prona. Fissare la caviglia sull'attuatore articolare con una fascetta intorno alla caviglia e un'altra intorno alle dita dei piedi e fissare la spaccatura del ginocchio con due fascette. Ruotare l'asse in modo che la caviglia sia in piena flessione plantare.
NOTA: Assicurarsi che le fascette non causino costrizione o lesioni, fare attenzione a stringerle e, se necessario, posizionare una garza tra la fascetta e la pelle per uno strato di protezione. - Per i seguenti passaggi relativi all'esecuzione del codice del sistema, fare clic su Esegui su MATLAB per ogni sezione del codice corrispondente al test di carico specifico.
- Eseguire il ciclo della caviglia 50 volte fino al 15% della sollecitazione di trazione ultima in base al valore della sollecitazione di trazione ultima del tendine d'Achille dalla trazione ex vivo alle prove di cedimento misurate in base al passaggio 2.1.
- Eseguire una prima calibrazione del tendine flettondolo dorsalmente tre volte a 12°. Utilizzare la pendenza della regione lineare della regione di carico della curva di isteresi per calcolare la regione esponenziale della curva.
- Flettere gradualmente la caviglia ad angoli crescenti fino a ottenere la regione esponenziale della curva calcolando la pendenza del picco della regione di carico della curva (calcolata utilizzando il codice MATLAB sviluppato internamente) o fino a quando non viene ruotata a 40°, a seconda dell'evento che si verifica per primo.
- All'angolo finale ottenuto, eseguire cinque misurazioni meccaniche cicliche come linea di base di precarico.
- Eseguire il regime di carico a fatica ciclico per un numero specificato di cicli (in questo studio, per 500, 1.000, 2.000, 3.600 o 7.200 cicli).
- Ogni 50 cicli, calcola la pendenza della porzione di carico della curva di isteresi (calcolata tramite il codice MATLAB sviluppato internamente) per assicurarti che sia ancora nella regione esponenziale. Aumentare l'angolo di flessione dorsale di 1° a meno che non sia già a 40° fino a raggiungere questa regione esponenziale.
- Al termine del regime di carico ciclico, eseguire cinque misurazioni meccaniche cicliche come misurazioni post-carico all'angolo inizialmente scelto per misurare le proprietà meccaniche del tendine.
- Rimuovere le fascette e la stecca. Rimettere l'animale nella camera di recupero. L'animale non viene lasciato incustodito fino a quando non ha ripreso conoscenza sufficiente, dopodiché viene riportato nella sua gabbia. Monitorare quotidianamente gli animali per eventuali segni clinici avversi e, se presenti, somministrare buprenorfina alla dose di 1,2 mg/kg per via sottocutanea una volta ogni 72 ore o eseguire l'eutanasia precoce. Sopprimere gli animali dopo 7 giorni di attività in gabbia tramite inalazione di CO2 e un mezzo secondario di eutanasia tramite toracotomia.
NOTA: L'applicazione di carico ciclico e le misurazioni meccaniche sono state ottenute con una maschera su misura composta da un sensore di coppia, un attuatore dell'articolazione della caviglia stampato in 3D e una cuccia per animali, un sistema di posizione e orientamento elettromagnetico 3D e un motore passo-passo che ruota un albero per ottenere la flessione dorsale, come precedentemente riportato dal nostro gruppo17. Questo sistema è controllato da uno script MATLAB menzionato nel passaggio 1.2. Il sensore di coppia e il sistema di posizione e orientamento acquisiscono i dati di coppia e posizione in tutto il protocollo di carico del sistema.
4. Analisi dei dati
- Caricare separatamente i dati pre e post misurazione in MATLAB.
- Convertire la coppia in sollecitazione in base al braccio del momento misurato dal punto 2.2 e all'area della sezione trasversale misurata al numero specificato di carichi applicati ottenuti dal passaggio 2.11 utilizzando le equazioni (1) e (2):
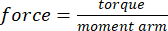 (1)
(1)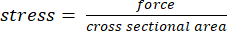 (2)
(2) - Convertite l'angolo in deformazione in base alla conversione ottenuta dal passo 2.10.
- Calcolare l'isteresi media (area compresa tra le curve di carico e scarico), la sollecitazione di picco (valore massimo di sollecitazione del ciclo) e i moduli di carico e scarico (accoppiamento lineare dell'ultimo 50% delle curve di carico e del primo 60% delle curve di scarico) per i cicli di pre e post misura.
- Calcolare la variazione percentuale delle proprietà meccaniche dal punto 4.4 tra i cicli di pre e post-misurazione.
Risultati
Con l'aumentare del numero di cicli applicati, si è verificata una maggiore riduzione delle proprietà meccaniche dei tendini in vivo . C'è stata una riduzione significativamente inferiore dell'isteresi e dei moduli di carico e scarico per il gruppo a 500 cicli rispetto ai gruppi a 3.600 e 7.200 cicli (p < 0,05) (Figura 2). Mentre c'è stata una significativa riduzione del picco di stress per ciclo dal gruppo 500 cicli al gruppo 3.600 cicli, non c'è stata alcuna riduzione signifi...
Discussione
Questo studio presenta un metodo per caricare ciclicamente il tendine d'Achille del ratto con un sistema di flessione dorsale passiva della caviglia per un modello di tendinopatia indotta da uso eccessivo in vivo . L'importanza del sistema risiede nella sua capacità di isolare il tendine d'Achille, applicare carichi quantificabili senza accedere chirurgicamente al tendine e misurare le proprietà del tendine in vivo .
Nel 2010, Fung et al. hanno presentato un modello di fat...
Divulgazioni
Gli autori non hanno conflitti di interesse da dichiarare.
Riconoscimenti
Vorremmo riconoscere i nostri sostegni finanziari: il Joe Fallon Research Fund, il Dr. Louis Meeks BIDMC Sports Medicine Trainee Research Fund, e una sovvenzione intramurale (AN), tutti da BIDMC Orthopaedics, insieme al supporto del National Institutes of Health (2T32AR055885 (PMW)).
Materiali
| Name | Company | Catalog Number | Comments |
| 1/32'' Aluminum beads | |||
| 2.5% isoflurane | |||
| 3D digitizing pen | Polhemus, Vermont, NH, USA | ||
| 3D electromagnetic positioning and orientation sensor | Polhemus, Vermont, NH, USA | ||
| 5% isoflurane | |||
| Customized device: 1) Assembly, sensors, 3D printed animal bed and ankle mount actuator | Assembled as described in manuscript | ||
| MATLAB code | MATLAB, Natick, MA, USA | ||
| Microcontroller | Ivrea, Italy | Arduino UNO, Rev3 | |
| Nose cone | |||
| Scalpel and scalpel holder | No. 11 scalpel | ||
| Sprague-Dawley rats | Charles River Laboratories, Wilmington, MA, USA | 11-13 weeks old | |
| Stepper driver | SparkFun Electronics, Niwot, CO 80503 | DM542T | |
| Stepper motor | SparkFun Electronics, Niwot, CO 80503 | 23HE30-2804S | |
| Straight forceps | |||
| Torque sensor assembly | Futek Inc., Irvine, CA, USA | FSH03985, FSH04473, FSH03927 | |
| Water heating pad |
Riferimenti
- Kaux, J. F., Forthomme, B., Goff, C. L., Crielaard, J. M., Croisier, J. L. Current opinions on tendinopathy. J Sports Sci Med. 10 (2), 238-253 (2011).
- Maffulli, N., Longo, U. G., Kadakia, A., Spiezia, F. Achilles tendinopathy. Foot Ankle Surg. 26 (3), 240-249 (2020).
- Teunis, T., Lubberts, B., Reilly, B. T., Ring, D. A systematic review and pooled analysis of the prevalence of rotator cuff disease with increasing age. J Shoulder Elbow Surg. 23 (12), 1913-1921 (2014).
- von Rickenbach, K. J., Borgstrom, H., Tenforde, A., Borg-Stein, J., McInnis, K. C. Achilles tendinopathy: evaluation, rehabilitation, and prevention. Curr Sports Med Rep. 20 (6), 327-334 (2021).
- Aicale, R., Oliviero, A., Maffulli, N. Management of Achilles and patellar tendinopathy: what we know, what we can do. J Foot Ankle Res. 13 (1), 59 (2020).
- Jarvinen, T. A., et al. Achilles tendon injuries. Curr Opin Rheumatol. 13 (2), 150-155 (2001).
- Silbernagel, K. G., Hanlon, S., Sprague, A. Current clinical concepts: conservative management of Achilles tendinopathy. J Athl Train. 55 (5), 438-447 (2020).
- Tayfur, A., et al. Are landing patterns in jumping athletes associated with patellar tendinopathy? A systematic review with evidence gap map and meta-analysis. Sports Med. 52 (1), 123-137 (2022).
- Malliaras, P., Cook, J. L., Kent, P. Reduced ankle dorsiflexion range may increase the risk of patellar tendon injury among volleyball players. J Sci Med Sport. 9 (4), 304-309 (2006).
- Backman, L. J., Danielson, P. Low range of ankle dorsiflexion predisposes for patellar tendinopathy in junior elite basketball players: a 1-year prospective study. Am J Sports Med. 39 (12), 2626-2633 (2011).
- Glazebrook, M. A., Wright, J. R., Langman, M., Stanish, W. D., Lee, J. M. Histological analysis of achilles tendons in an overuse rat model. J Orthop Res. 26 (6), 840-846 (2008).
- Carpenter, J. E., Flanagan, C. L., Thomopoulos, S., Yian, E. H., Soslowsky, L. J. The effects of overuse combined with intrinsic or extrinsic alterations in an animal model of rotator cuff tendinosis. Am J Sports Med. 26 (6), 801-807 (1998).
- Gao, H. G., et al. Increased serum and musculotendinous fibrogenic proteins following persistent low-grade inflammation in a rat model of long-term upper extremity overuse. PLoS One. 8 (8), e71875 (2013).
- Fung, D., et al. Early response to tendon fatigue damage accumulation in a novel in vivo model. J Biomech. 43 (2), 274-279 (2010).
- Ueda, Y., et al. Molecular changes to tendons after collagenase-induced acute tendon injury in a senescence-accelerated mouse model. BMC Musculoskelet Disord. 20 (1), 120 (2019).
- Bloom, E., et al. Overload in a rat in vivo model of synergist ablation induces tendon multi-scale structural and functional degeneration. J Biomech Eng. 145 (8), 081003 (2023).
- Williamson, P. M., et al. A passive ankle dorsiflexion testing system to assess mechanobiological and structural response to cyclic loading in rat Achilles tendon. J Biomech. 156, 111664 (2023).
- Oliveira, L. F., Peixinho, C. C., Silva, G. A., Menegaldo, L. L. In vivo passive mechanical properties estimation of Achilles tendon using ultrasound. J Biomech. 49 (4), 507-513 (2016).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon