Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Un modèle porcin ex vivo pour les essais hydrodynamiques de procédures expérimentales de valvules aortiques et de nouveaux dispositifs médicaux
Dans cet article
Résumé
Nous présentons une méthode de montage d’une valve aortique porcine sur un duplicateur d’impulsions afin de tester ses propriétés hydrodynamiques. Cette méthode peut être utilisée pour déterminer le changement de l’hydrodynamique après l’application d’une procédure expérimentale ou d’un nouveau dispositif médical avant son utilisation dans un modèle animal de grande taille.
Résumé
Les options pour tester de nouvelles procédures cardiaques et de nouveaux dispositifs médicaux d’investigation avant leur utilisation dans un modèle animal sont limitées. Dans cette étude, nous présentons une méthode de montage d’une valve aortique porcine dans un duplicateur d’impulsions afin d’évaluer ses propriétés hydrodynamiques. Ces propriétés peuvent ensuite être évaluées avant et après l’exécution de la procédure à l’étude et/ou l’application du dispositif médical d’investigation. La fixation du segment d’entrée présente une certaine difficulté en raison de l’absence de myocarde circonférentiel dans la voie d’écoulement ventriculaire gauche. Cette méthode résout ce problème en fixant le segment d’entrée à l’aide du feuillet antérieur de la valve mitrale, puis en suturant la paroi libre ventriculaire gauche autour de l’appareil d’entrée. Le segment d’écoulement est sécurisé simplement en insérant le dispositif dans une incision dans la face supérieure de l’arc aortique. Nous avons constaté que les spécimens avaient des propriétés hydrodynamiques significativement différentes avant et après la fixation tissulaire. Cette découverte nous a incités à utiliser des échantillons frais dans nos tests et devrait être prise en compte lors de l’utilisation de cette méthode. Dans notre travail, nous avons utilisé cette méthode pour tester de nouveaux matériaux de patchs intracardiaques à utiliser en position valvulaire en effectuant une procédure de néocuspidisation de la valve aortique (procédure d’Ozaki) sur les valves aortiques porcines montées. Ces vannes ont été testées avant et après la procédure afin d’évaluer le changement des propriétés hydrodynamiques par rapport à la vanne native. Nous présentons ici une plate-forme d’essais hydrodynamiques de procédures expérimentales de valve aortique qui permet la comparaison avec la valve native et entre différents dispositifs et techniques utilisés pour la procédure à l’étude.
Introduction
La valvulopathie aortique représente un fardeau important pour la santé publique, en particulier la sténose aortique, qui touche 9 millions de personnes dans le monde1. Les stratégies pour traiter cette maladie sont en cours d’évolution et comprennent la réparation de la valve aortique et le remplacement de la valve aortique. Dans la population pédiatrique en particulier, il existe une incitation importante à réparer plutôt qu’à remplacer la valve, car les prothèses actuellement disponibles sont sujettes à la dégénérescence valvulaire structurelle (SVD) et ne sont pas tolérantes à la croissance, nécessitant une réintervention pour un remplacement au fur et à mesure que le patient grandit. Même la procédure de Ross, qui consiste à remplacer la valve aortique (AV) malade par la valve pulmonaire native (PV), nécessite une prothèse ou un greffon en position pulmonaire qui est également sujet à la SVD et à une tolérance de croissance souvent limitée2. De nouvelles approches de la valvulopathie aortique sont en cours de développement, et il est nécessaire de les tester dans un contexte biologiquement pertinent avant de les appliquer dans un grand modèle animal.
Nous avons mis au point une méthode de test d’un VA porcin qui peut fournir des informations sur la fonction de la valve avant et après une procédure expérimentale ou l’application d’un nouveau dispositif médical. En montant l’AV porcin sur une machine à duplication d’impulsions disponible dans le commerce, nous sommes en mesure de comparer les caractéristiques hydrodynamiques couramment utilisées dans l’étude et, finalement, l’approbation des prothèses valvulaires, y compris la fraction de régurgitation (RF), la surface effective de l’orifice (EOA) et la différence de pression positive moyenne (PPD)3,4. L’intervention peut ensuite être affinée dans un contexte biologiquement pertinent avant d’être utilisée dans un grand modèle animal, limitant ainsi le nombre d’animaux nécessaires à la production d’une procédure ou d’une prothèse pouvant être utilisée chez l’homme. Les cœurs utilisés pour cette expérience peuvent être obtenus à partir de l’abattoir local ou de déchets de tissus provenant d’autres expériences, il n’est donc pas nécessaire de sacrifier un animal uniquement pour les besoins de cette expérience.
Dans le cadre de notre travail, nous avons utilisé cette méthode pour développer un nouveau matériau de patch pour la réparation et le remplacement des valves. Nous avons testé la fonction hydrodynamique d’une variété de matériaux de patch en effectuant une procédure de néocuspidisation de la valve aortique (procédure d’Ozaki 5,6,7) sur des AV porcins et en les testant dans le duplicateur d’impulsions avant et après la procédure. Cela nous a permis d’affiner le matériau en fonction de ses performances hydrodynamiques. Ainsi, cette méthode fournit une plate-forme pour les essais hydrodynamiques de procédures expérimentales et de nouveaux dispositifs médicaux destinés à être utilisés sur l’AV avant d’être appliqués dans un modèle animal de grande taille.
Protocole
Toutes les recherches ont été effectuées conformément aux directives institutionnelles pour les soins aux animaux.
1. Considérations et préparatifs de l’expérience
- Utilisez un duplicateur d’impulsions () approprié pour la simulation du débit cardiaque via l’AV. Le DP devra être en mesure d’accueillir du matériel biologique et d’être nettoyé.
- Utilisez les paramètres de DP appropriés pour tester l’AV : volume de déplacement de 70 mL et 70 battements par minute (débit cardiaque de 5 L/min), 35 % du cycle cardiaque en systole, gradient de pression transvalvulaire moyen de 100 mmHg, gradient de pression maximale de 120 et gradient de pression minimale de 80.
- Utilisez une solution saline normale à température ambiante (0,9 % de NaCl) comme milieu fluide.
- Localisez ou créez (à l’aide de l’impression 3D ou d’une méthode similaire) des dispositifs appropriés pour le montage de l’AV porcin pour les tests sur le.
- Utilisez des appareils calqués sur les appareils fournis avec le duplicateur d’impulsions avec les spécifications suivantes : assurez-vous que le diamètre intérieur de l’appareil est similaire au diamètre de l’AV étudié, que la longueur de l’accessoire est d’au moins 2 cm et que la largeur d’accessoire utilisable est d’au moins 4 cm (Figure 1).
- Utilisez des joints toriques en caoutchouc comme joints aux extrémités des luminaires.
- Prélever un échantillon de cœur après une cardiectomie (Figure 2A).
- Utilisez des échantillons cardiaques porcins provenant de l’abattoir ou des déchets de tissus provenant d’animaux qui sont par ailleurs en bonne santé et qui n’ont fait l’objet d’aucun protocole expérimental susceptible d’affecter leur cœur.
- Prélever un échantillon après une cardectomie ou effectuer une cardiectomie post-mortem, y compris la section de la veine cave supérieure, de la veine cave inférieure, de l’artère pulmonaire principale (AP), de toutes les veines pulmonaires et de l’aorte à la face distale de l’arc aortique.
REMARQUE : Des échantillons frais, moins de 6 h post-mortem ou conservés dans une solution saline stérile avec une solution antibiotique à 1 % (pénicilline et streptomycine) dans un réfrigérateur à 4 °C pendant un maximum de 7 jours, doivent être utilisés pour cette expérience. Les tissus fixés dans le formol ou le glutaraldéhyde produiront des résultats hydrodynamiques altérés en raison d’une rigidité accrue.

Figure 1 : Fixations personnalisées imprimées en 3D pour le montage des valves aortiques porcines sur le duplicateur d’impulsions. Comme indiqué dans le protocole, la longueur de l’accessoire doit être d’au moins 2 cm et la largeur utile de l’accessoire doit être d’au moins 4 cm. Veuillez cliquer ici pour voir une version agrandie de cette figure.
2. Résection des structures du côté droit
- Disséquer l’AP de l’aorte à l’aide de ciseaux de Metzenbaum jusqu’à ce que le tissu ventriculaire soit visible (Figure 2B).
- Disséquer et ligaturer avec de la soie lie les deux artères coronaires à leur origine à partir des sinus aortiques, en prenant soin de ne pas rétrécir les sinus.
- Transectez les artères coronaires distales aux liens de soie.
- Inciser le ventricule droit (RV) entre l’aorte et l’AP à la base de la valve pulmonaire à l’aide de ciseaux de Metzenbaum (Figure 2C).
- En commençant par l’avant, continuez l’incision sur le pourtour le long du septum interventriculaire pour enlever la paroi libre du RV (Figure 2D, E).
- Continuez l’incision vers l’arrière à travers l’anneau de la valve tricuspide le long du septum interauriculaire pour enlever tout le tissu auriculaire droit (Figure 2F).
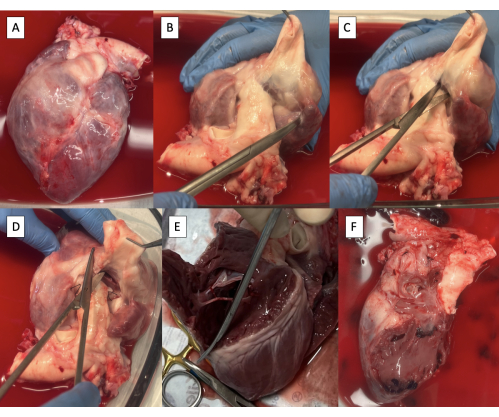
Figure 2 : Échantillon de cardectomie et résection des structures du côté droit. (A) Échantillon de cardectomie. (B) Artère pulmonaire principale disséquée de l’aorte jusqu’à ce que le tissu ventriculaire soit visible. (C) Inciser le ventricule droit (RV) à la base de la valve pulmonaire. (D) Continuer l’incision le long du septum interventriculaire vers l’avant. (E) Enlever la paroi libre de RV en continuant l’incision sur le pourtour le long du septum interventriculaire. (F) Spécimen dont les structures du côté droit ont été enlevées. Veuillez cliquer ici pour voir une version agrandie de cette figure.
3. Préparation de la voie d’écoulement ventriculaire gauche (LVOT) pour la canulation avec le dispositif
- Inciser l’oreillette gauche (LA) à travers l’ostium de la veine pulmonaire droite parallèle à l’aorte à l’aide de ciseaux de Metzenbaum (Figure 3A).
REMARQUE : Bien qu’il existe une variabilité limitée, l’anatomie de la veine pulmonaire porcine se termine généralement par deux ostia de la veine pulmonaire entrant dans le LA8. - Continuez l’incision vers la commissure antérolatérale de la valve mitrale (MV), en laissant une manchette d’au moins 3 mm de tissu auriculaire du côté de l’aorte.
- Couper l’excès de tissu LA en maintenant la coiffe de 3 mm de tissu auriculaire sur l’aorte et l’anneau MV sur le pourtour (Figure 3B).
- Prolongez l’incision sur le ventricule gauche (VG) à travers la commissure antérolatérale de la MV, en prenant soin de préserver le muscle papillaire antérolatéral (Figure 3C).
- Diviser les cordes tendineuses du muscle papillaire antérolatéral vers le feuillet postérieur MV, en préservant les attaches au feuillet antérieur MV.
- Continuez l’incision jusqu’à l’apex du cœur.
- Coupez l’excès de tissu VG sous les muscles papillaires, en préservant les deux muscles papillaires (Figure 3D).
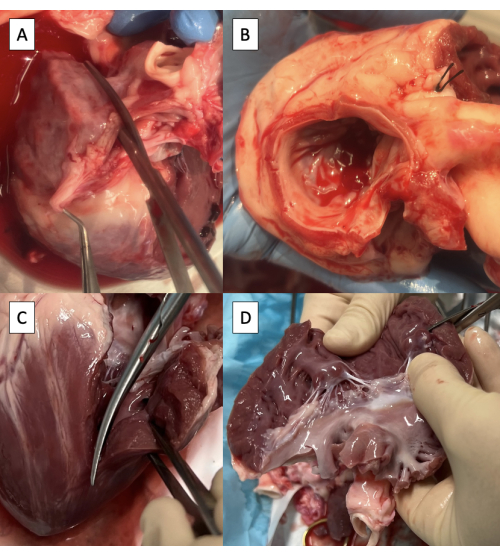
Figure 3 : Préparation de la voie d’écoulement ventriculaire gauche pour la canulation à l’aide du duplicateur d’impulsions. (A) Inciser l’oreillette gauche (LA) à travers l’ostium de la veine pulmonaire droite. (B) Excès de tissu LA coupé, en maintenant une coiffe d’au moins 3 mm de tissu auriculaire sur l’aorte et en maintenant l’anneau de la valve mitrale sur la circonférence. (C) Extension de l’incision sur le ventricule gauche (VG) à travers la commissure antérolatérale de la valve mitrale. (D) Enlever l’excès de tissu VG sous les muscles papillaires. Les ciseaux sont visibles dans le coin supérieur droit de l’image. Veuillez cliquer ici pour voir une version agrandie de cette figure.
4. Préparation de l’aorte pour la canulation avec le dispositif
- Retirez tout excès de tissu lymphatique, conjonctif ou pulmonaire de l’aorte (Figure 4A).
- Inciser la face supérieure de l’arc aortique de l’aorte descendante à l’artère sous-clavière gauche à l’aide de ciseaux de Metzenbaum (Figure 4B).
- Poursuivre l’incision sur la face supérieure de l’arc aortique de l’artère sous-clavière gauche jusqu’au tronc brachiocéphale (Figure 4C, D).
REMARQUE : Les branches de l’arc aortique porcin de distal à proximal comprennent l’artère sous-clavière gauche et le tronc brachiocéphale, qui donne naissance à l’artère sous-clavière droite, à l’artère carotide droite et à l’artère carotide gauche9.
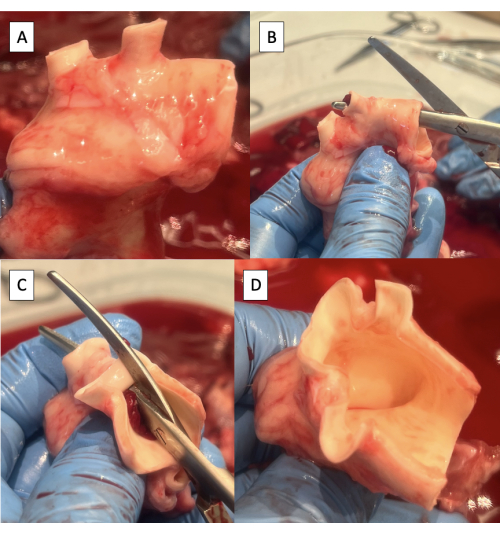
Figure 4 : Préparation de l’aorte pour la canulation à l’aide du duplicateur d’impulsions. (A) Arc aortique avec l’excès de tissu enlevé. Remarquez les deux vaisseaux de l’arc dans l’arc aortique porcin, le tronc brachiocéphale et l’artère sous-clavière gauche. (B) Début de l’incision le long de la face supérieure de l’arc aortique de l’aorte descendante à l’artère sous-clavière gauche. (C) Continuer l’incision le long de la face supérieure de l’arc aortique de l’artère sous-clavière gauche jusqu’au tronc brachiocéphale. (D) Incision de l’arc aortique terminée. Veuillez cliquer ici pour voir une version agrandie de cette figure.
5. Canulation du LVOT avec le luminaire
- Testez le positionnement de l’appareil dans le LVOT et coupez l’excès de tissu VG.
- Insérez le luminaire dans le LVOT sous le feuillet antérieur du MV.
- Enroulez le mur sans BT autour du luminaire.
- Coupez l’excès de tissu LV pour maintenir un enveloppement serré autour du luminaire.
- Enlever la moitié de l’épaisseur de la paroi libre du VG en commençant par le septum interventriculaire, en maintenant au moins 1 cm d’épicarde au bord libre pour maintenir l’intégrité de la ligne de suture (Figure 5A).
- Coupez 1 cm de tissu dans le coin supérieur de l’enveloppe murale sans LV (Figure 5A).
- Positionnez le luminaire dans le LVOT avec le trou de fixation de la tige de support à 1 cm derrière l’incision LV (Figure 5B).
- Veillez à ne pas insérer le luminaire trop loin dans le LVOT afin qu’il dilate l’anneau AV.
- Fixez le feuillet antérieur du MV au luminaire à l’aide d’un ou deux colliers de serrage de 6 pouces positionnés entre les cordes tendineuses du feuillet (figure 5C).
- Suturez la paroi libre BT autour de l’appareil (Figure 5D).
- Commencez par suturer la manchette du tissu LA de l’aorte à l’anneau MV à l’aide d’une simple suture courante avec une aiguille à pointe conique.
- Continuer la maille courante sur le LV sans déchirer le tissu LV.
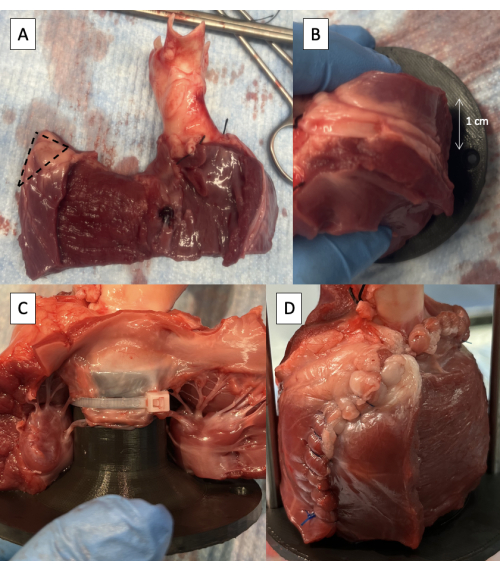
Figure 5 : Canulation de la voie d’écoulement ventriculaire gauche à l’aide du duplicateur d’impulsions. (A) Réduction de la moitié de l’épaisseur de la paroi libre du VG avec 1 cm d’épicarde maintenu au bord libre. La ligne pointillée indique la zone de 1 cm à enlever de l’angle supérieur de l’enveloppe murale sans BT. (B) Trou de fixation de la tige de support positionné à 1 cm derrière l’incision de paroi libre BT. (C) Attache zippée fixant le feuillet antérieur du MV à la fixation proximale. (D) Mur sans BT suturé autour de l’appareil. Veuillez cliquer ici pour voir une version agrandie de cette figure.
6. Canulation de l’aorte avec fixation et préparation finale pour le test
- Mesurez le diamètre de l’AV à l’aide de dilatateurs Hegar pour faciliter l’interprétation des résultats des tests de DP.
- Identifiez la position neutre de l’aorte en soulevant l’échantillon de la table en saisissant l’aorte (Figure 6A).
- Insérez le luminaire dans l’aorte, en prenant soin d’aligner les trous de fixation de la tige en position neutre de l’aorte.
- Vérifiez la longueur de l’éprouvette en insérant les tiges de support.
- Fixez le dispositif à l’aorte à l’aide d’un ou deux colliers de serrage de 6 pouces (Figure 6B).
- Fixez le LVOT autour du luminaire à l’aide d’un ou deux colliers de serrage de 8 pouces.
- Fixez les tiges de support en place à l’aide des vis fournies avec le jeu.
- Placez l’échantillon dans et commencez le test (Figure 6C, vidéo 1 et vidéo 2).
- Suturez les fuites au besoin.
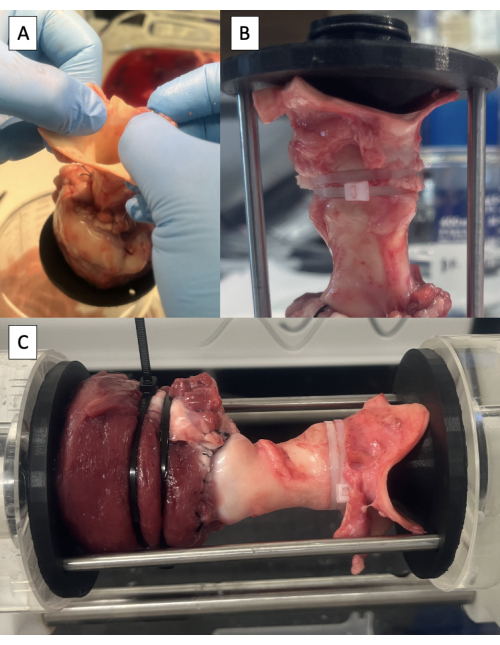
Figure 6 : Canulation de l’aorte et test dans le duplicateur d’impulsions. (A) Soulever l’échantillon de la table par l’aorte pour identifier la position neutre de l’aorte. (B) Fixation distale fixée dans l’aorte à l’aide de colliers de serrage. (C) Éprouvette montée dans le duplicateur d’impulsions pour les essais hydrodynamiques. Veuillez cliquer ici pour voir une version agrandie de cette figure.
7. Effectuer une procédure expérimentale
REMARQUE : Effectuez des procédures expérimentales telles que la procédure d’Ozaki décrite précédemment 5,6,7 et répétez les tests de DP.
- Si le tissu s’est desséché pendant l’intervention, serrez les colliers de serrage et renforcez la ligne de suture au besoin.
8. Entreposage à long terme de l’échantillon (si désiré)
- Placer l’échantillon dans le formol à 10 % pendant 168 h (1 semaine)10,11.
- Après la fixation des tissus, lavez l’échantillon avec de l’eau déminéralisée et placez-le dans de l’éthanol à 70 % pour un stockage à long terme.
Résultats
Les données représentatives recueillies à partir du duplicateur d’impulsions comprennent la fraction de régurgitation (RF), la surface effective de l’orifice (EOA) et la différence de pression positive moyenne (PPD). Les RF et EOA, en particulier, sont utilisés dans les normes ISO pour les valves prothétiques (ISO 5840) et seront importants à collecter si des produits valvulaires prothétiques sont à l’étude. Le PPD offre des informations sur la pression nécessaire pour ouvrir la valve et est couramment ...
Discussion
La méthode présentée ici fournit une plate-forme pour les essais hydrodynamiques de l’AV afin d’examiner l’effet d’une procédure expérimentale ou d’un nouveau dispositif médical. En montant la valve aortique native sur une machine à duplication d’impulsions, nous sommes en mesure de déterminer l’effet de la procédure expérimentale sur tous les paramètres hydrodynamiques utilisés dans la recherche et l’approbation de nouvelles prothèses valvulaires (ISO 5840). Cela permet d’affiner les proc?...
Déclarations de divulgation
Les auteurs n’ont aucun conflit d’intérêts financier pertinent à divulguer.
Remerciements
Nous tenons à remercier le laboratoire de la Dre Gordana Vunjak-Novakovic, y compris Julie Van Hassel, Mohamed Diane et Panpan Chen, de nous avoir permis d’utiliser les déchets de tissus cardiaques issus de leurs expériences. Ce travail a été soutenu par la Congenital Heart Defect Coalition à Butler, NJ, et les National Institutes of Health à Bethesda, MD (5T32HL007854-27).
matériels
| Name | Company | Catalog Number | Comments |
| 3D Printer | Ultimaker | Ultimaker S5 | Used for printing custom fixtures for hydrodynamic testing |
| Crile-Wood Needle Driver | Emerald Instruments | 2.0638.15 | Used for suturing ventricle |
| Debakey Forceps | Jarit | 320-110 | Used for dissection and sample preparation (can use multiple if working with an assistant) |
| Ethanol 200 proof | Decon Labs Inc. | DSP-MD.43 | Used for fixed tissue storage |
| Formalin 10% | Epredia | 5701 | Used for tissue fixation |
| Gerald Forceps | Jarit | 285-126 | Used for dissection and sample preparation |
| Glass jars | QAPPDA | B07QCP54Z3 | Used for tissue storage |
| Glutaraldehyde 25% | Electron Microscopy Sciences | 16400 | Used for tissue fixation |
| HEPES 1 M buffer solution | Fisher | BP299-100 | Used to make glutaraldehyde 0.6% |
| Mayo Scissors | Jarit | 099-200 | Used for cutting suture |
| Metzenbaum Scissors | Jarit | 099-262 | Used for dissection and sample preparation |
| O-ring | Sterling Seal & Supply Inc. | AS568-117 | Used as a gasket on the end of the 3D printed fixtures |
| Polylactic acid resin | Ultimaker | 1609 | Used for 3D printing fixtures |
| Polyproplene suture | Covidien | VP-762-X | Used for suturing ventricle, tapered needle |
| Pulse Duplicator | BDC Laboratories | HDTi-6000 | Used for hydrodynamic testing |
| Silk ties | Covidien | S-193 | Used for ligating coronary arteries |
| Tonsil Clamp | Aesculap | BH957R | Used for coronary artery dissection |
| Zip ties (6 inch) | Advanced Cable Ties, Inc. | AL-06-18-9-C | Used for securing sample to fixtures, 157.14 mm long (6 inches), 2.5 mm wide |
| Zip ties (8 inch) | GTSE | GTSE-20025B.1000 | Used for securing sample to fixtures, 203 mm long (8 inches), 2.5 mm wide |
Références
- Aluru, J. S., Barsouk, A., Saginala, K., Rawla, P., Barsouk, A. Valvular heart disease epidemiology. Medical Science. 10 (2), 32 (2022).
- Herrmann, J. L., Brown, J. W. Seven decades of valved right ventricular outflow tract reconstruction: The most common heart procedure in children. The Journal of Thoracic and Cardiovascular Surgery. 160 (5), 1284-1288 (2020).
- Rotman, O. M., Bianchi, M., Ghosh, R. P., Kovarovic, B., Bluestein, D. Principles of TAVR valve design, modelling, and testing. Expert Review of Medical Devices. 15 (11), 771-791 (2018).
- Pibarot, P., et al. Imaging for predicting and assessing prosthesis-patient mismatch after aortic valve replacement. JACC Cardiovascular Imaging. 12 (1), 149-162 (2019).
- Ozaki, S., et al. Aortic valve reconstruction using self-developed aortic valve plasty system in aortic valve disease. Interactive Cardiovascular and Thoracic Surgery. 12 (4), 550-553 (2011).
- Krane, M., Amabile, A., Ziegelmüller, J. A., Geirsson, A., Lange, R. Aortic valve neocuspidization (the Ozaki procedure). Multimedia Manual of Cardiothoracic Surgery. , (2021).
- Ozaki, S., et al. A total of 404 cases of aortic valve reconstruction with glutaraldehyde-treated autologous pericardium. The Journal of Thoracic and Cardiovascular Surgery. 147 (1), 301-306 (2014).
- Vandecasteele, T., et al. The pulmonary veins of the pig as an anatomical model for the development of a new treatment for atrial fibrillation. Anatomia Histollogia Embryologia. 44 (1), 1-12 (2015).
- Góes, A. M. O., et al. Comparative angiotomographic study of swine vascular anatomy: contributions to research and training models in vascular and endovascular surgery. Journal Vascular Brasilerio. 20, 20200086 (2021).
- Hołda, M. K., Klimek-Piotrowska, W., Koziej, M., Piątek, K., Hołda, J. Influence of different fixation protocols on the preservation and dimensions of cardiac tissue. Journal of Anatomy. 229 (2), 334-340 (2016).
- Hołda, M. K., Klimek-Piotrowska, W., Koziej, M., Tyrak, K., Hołda, J. Penetration of formaldehyde based fixatives into heart. Folia Medica Cracoviensia. 57 (4), 63-70 (2017).
- Spampinato, R. A., et al. Grading of aortic regurgitation by cardiovascular magnetic resonance and pulsed Doppler of the left subclavian artery: harmonizing grading scales between imaging modalities. International Journal of Cardiovascular Imaging. 36 (8), 1517-1526 (2020).
- Capps, S. B., Elkins, R. C., Fronk, D. M. Body surface area as a predictor of aortic and pulmonary valve diameter. The Journal of Thoracic and Cardiovascular Surgery. 119 (5), 975-982 (2000).
- Baumgartner, H., et al. Recommendations on the echocardiographic assessment of aortic valve stenosis: a focused update from the European Association of Cardiovascular Imaging and the American Society of Echocardiography. European Heart Journal - Cardiovascular Imaging. 18 (3), 254-275 (2017).
- Saisho, H., et al. An ex vivo evaluation of two different suture techniques for the Ozaki aortic neocuspidization procedure. Interactive Cardiovascular and Thoracic Surgery. 33 (4), 518-524 (2021).
- Saisho, H., et al. Ex vivo evaluation of the Ozaki procedure in comparison with the native aortic valve and prosthetic valves. Interactive Cardiovascular and Thoracic Surgery. 35 (3), (2022).
- Paulsen, M. J., et al. Comprehensive ex vivo comparison of 5 clinically used conduit configurations for valve-sparing aortic root replacement using a 3-dimensional-printed heart simulator. Circulation. 142 (14), 1361-1373 (2020).
- Al-Atassi, T., et al. Impact of aortic annular geometry on aortic valve insufficiency: Insights from a preclinical, ex vivo, porcine model. The Journal of Thoracic and Cardiovascular Surgery. 150 (3), 656-664 (2015).
- Sun, M., et al. A biomimetic multilayered polymeric material designed for heart valve repair and replacement. Biomaterials. 288, 121756 (2022).
- Waller, B. F., McKay, C., Van Tassel, J., Allen, M. Catheter balloon valvuloplasty of stenotic porcine bioprosthetic valves: Part I: Anatomic considerations. Clinical Cardiology. 14 (8), 686-691 (1991).
- Crick, S. J., Sheppard, M. N., Ho, S. Y., Gebstein, L., Anderson, R. H. Anatomy of the pig heart: comparisons with normal human cardiac structure. Journal of Anatomy. 193, 105-119 (1998).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon