Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Bir Geliştirilmesi
Bu Makalede
Özet
The current study describes the development and applications of a genetically engineered assay system based on the transfection of rat basophilic leukemia cells with the equine FcεRIα gene. Transfected cells express a functional receptor where the release of mediators of the allergic response can be activated by IgE and antigen.
Özet
The interaction of IgE with its high-affinity Fc receptor (FcεRI) followed by an antigenic challenge is the principal pathway in IgE mediated allergic reactions. As a consequence of the high affinity binding between IgE and FcεRI, along with the continuous production of IgE by B cells, allergies usually persist throughout life, with currently no permanent cure available. Horses, especially race horses, which are commonly inbred, are a species of mammals that are very prone to the development of hypersensitivity responses, which can seriously affect their performance. Physiological responses to allergic sensitization in horses mirror that observed in humans and dogs. In this paper we describe the development of an in situ assay system for the quantitative assessment of the release of mediators of the allergic response pertaining to the equine system. To this end, the gene encoding equine FcεRIα was transfected into and expressed onto the surface of parental Rat Basophil Leukemia (RBL-2H3.1) cells. The gene product of the transfected equine α-chain formed a functional receptor complex with the endogenous rat β- and γ-chains 1. The resultant assay system facilitated an assessment of the quantity of mediator secreted from equine FcεRIα transfected RBL-2H3.1 cells following sensitization with equine IgE and antigenic challenge using β-hexosaminidase release as a readout 2, 3. Mediator release peaked at 36.68% ± 4.88% at 100 ng ml-1 of antigen. This assay was modified from previous assays used to study human and canine allergic responses 4, 5. We have also shown that this type of assay system has multiple applications for the development of diagnostic tools and the safety assessment of potential therapeutic intervention strategies in allergic disease 6, 2, 3.
Giriş
Alerji bin beri bilinmektedir. Bir astım tedavisi Ebers Papirüs (~ 1550 BCE) olarak bilinen Antik Mısır tıbbi metinde açıklanan ve 7 tedavisinde bitkisel ilaçlar tartışıldı.
Günümüzde alerji T yardımcı hücre tür 2 (T H 2), bağışıklık sistemi kolu alerjenler olarak adlandırılan, çevresel antijenlere yanıt olarak immünoglobülin E (IgE) antikorlarının üretimi yön, bir tip I hipersensitivite cevabı olarak sınıflandırılır. Bunlar yaygın olarak bağışıklık sistemi hücreleri ile etkileşen ve IgE sentezi, sigara dumanı ya da dizel egzoz parçacıklar içinde parçacıklar geliştirmek göstermemektedir gibi interlökin-4 ve interlökin-13 8, 9 da dahil olmak üzere sentez ve pro-inflamatuar sitokinlerin salgılanmasını uyaran çeşitli maddelerdir 10.
Son 50 yılda sanayileşmiş ülkelerde alerjik belirtiler de artış etkisi bir arada atfedilmiştir'Hijyen Hipotezi' 11 tarafından önerilen TH 2 sitokinler tarafından baskın bir profil yönünde immün yanıtı kaydırmaya birleştirmek çevresel kirleticiler ve daha dezenfekte çevre için bir eğilim,.
Yukarıda belirtildiği gibi, insanlar alerjiden muzdarip olan tek memeli değildir. Özellikle atlar ve köpekler de klasik alerjik tepkiler geliştirebilir ve at alerji genetik ve çevresel faktörlere atfedilen insanlarda olduğu gibi 12 tarafından bir çalışma olduğunu göstermiştir. Sonuç olarak, bu hayvanlar bir kez klinik bulgular koymuş alerji genetik ve çevresel nedenler, hastalığa karşı duyarlılık onun ilerlemesi ve olası müdahale stratejileri arasındaki etkileşimi incelemek için iyi modeller sunuyoruz
1887 yılında, Stömmer, at kardiyovasküler sistem üzerindeki histamin etkisi insan ve at astım 13 arasındaki benzerliği açıklamak için ilk kişi olduİnsanlarda 14 çok benzer. Atlar da 15 yıllık 115.000.000.000 $ ABD bir bahis cirosu ile değer US $ 72 milyar at yarışı endüstrisinin temel taşı vardır.
En çağdaş yarış atları itibaren 1878 Lady Anne Blunt tarafından yetiştirilen Arap atları az sayıda torunlarıdır. Modern yarış atları yaygın performans yetenekleri seçmek için akrabası olan. Bunlar, allerjik tepkileri monte duyarlılıkları bunlardan biri genetik bozukluklar, yatkındır. Onlar da bile en ciddi alerjik insanlarda 16 1000 kat daha yüksek serum IgE seviyeleri var. At alerjik tepkiler genellikle böcek ısırığı hipersensitivitesi (IBH) 17, 18 olarak ortaya çıkmaktadır. Sebebiyle sokması dermatit IBH sonuçlar cinsi Culicoides böcekler oluşturur. At alerjik hastalığın diğer bir şekli tekrarlayan solunum yolu tıkanmaları (RAO), bu akciğerlerde ve solunum yollarında tecelli olmasıdır. Hışıltı ve laboratuarı ile karakterizedirORed nefes. RAO sık mantar sporlarına tepki olarak ortaya çıkar ve başka bir soruşturma bu 20 teyit edilmemiş olmasına rağmen, yüksek alerjen spesifik IgE düzeyleri bir çalışmada 19 RAO muzdarip atların kaydedilmiştir.
At alerjisi çalışmalar girişimi izlemeyi ve anti-at IgE monoklonal antikorları (mAb 'ler) 21, 22 geliştirerek ekuin IgE nötralize etrafında dönmektedir. Bundan başka, 23 tarafından yapılan çalışmada at yüksek afiniteli Fc reseptörün α hücre dışı etki üretimini tartışmaktadır at serumu IgE tespit etmek ve miktarını belirlemek için bir girişim zincirli (FcεRIα) reseptörü. Ledin 24 ile ilgili bir çalışma öz / non-self immünojenlerini kullanarak bağışıklık sistemini astarlanırsa serum IgE nötralize amaçlayan yeni bir yaklaşım anlatılmaktadır. Tüm bu çalışmalar, ancak, kendi protokollerinin güvenliğini ve etkinliğini test etmek etkili bir tahlil yoktu. Bu makalede, biz şimdi böyle bir tahlil sys sunmakβ-heksosaminidaz bırakma, hücre arabulucu degranülasyonunun bir göstergesi olarak, at FcεRIα ifade RBL-2H3.1 hücreleri üzerinde değerlendirilmiştir at sistemi ile ilgili tanı ve tedavi stratejilerinin çalışmaya uygulanabilir tem. Bu protokol, farklı türlerden elde edilen IgE için yüksek afinite reseptörünün IgE bağlama alanını kodlayan gen ile transfekte edilmiş, RBL hücrelerinde ve mühendislik tarif Önceki yayınlarda 25, 4, 5, 2, 3 dayanır. Protokol, sonuçları üçlü deneylerde standart sapma ± ortalama olarak sunulan bir β-heksosaminidaz salım deneyi gerçekleştirmek açıklar.
Salınım testi ilk Siraganian tarafından geliştirilen ve insan alerji incelemek için 25 Hook edildi. Dr. Reuben Siraganian liderliğindeki laboratuar grubu da RBL hücre hattı geliştirdi. Bu RBL hücreler, insan FcεRIα ifade geliştirilmiş ve protokol 4 tarafından yayınlandı. Son parçasıDeney 4-hidroksi-3 hapten hedef bir IgE değişken bölgesi için bir fare geninin aşağısında ağır zincir genini klonlayarak, bir IgE antikorlarının üretimini tarif Neuberger 26 ile kağıt pSV plazmidin gelişimi ile gelen bölgesinin -nitro-fenasetil (NP), elde edilen kimerik antikor, tam fonksiyonel. Ayrıca bazofil hücre degranülasyonu ölçmek için yararlı bir protokol verme deneyinin standardizasyon sonuçlanan RBL hücrelerinde yüzeyi reseptörüne klonlanması ise becerisi aynı hapten hedefleme IgE geliştirmektir.
Tahlil artıları ve eksileri var. Analizin artıları, bizim laboratuvar böylece insan, köpek ve at sistemleri degranülasyonunu test etmek için kullanılan olan herhangi bir memeli sistemi içinde kullanılmak üzere olan uyum ve bu basit bir organizmanın IgE sentezlenmesi ve bunun reseptörü klonlama ile elde edilebilir RBL hücrelerinde yüzeyi üzerine.
Diğer taraftan,Tahlil dezavantajları, RBL hücrelerinde bunların Aynı deney içinde degranülasyon seviyelerinin varyasyonu elde yapma, termal, mekanik ve pH değişikliklerine karşı çok duyarlı olmasıdır. Bu nedenle kuvvetli tahliller zaman, üç kez tekrar edilir ve daha sonra bir ortalama onlardan alınır tavsiye edilir. Ayrıca, RBL hücreleri kendi bakım hantal hale uzun bir zaman (> 10 haftalık) 27 doku kültürü içinde kalması durumunda olmayan serbest fenotipe doğru kayma eğilimindedir. Onlar da bir ışık mikroskobu görünmez ve hücrenin morfolojisi değişmez mikoplazma bakterilerin neden olduğu enfeksiyonların, eğilimli, ama büyük ölçüde onların degranülasyona düzeylerini değiştirmek istiyorum. Böylece düzenli mikoplazma testleri gereklidir.
Protokol
Celi Line 1) hazırlanması:
- At FcεRI α ifade RBL-2H3.1 hücre çizgisi Geliştirme:
- 28: tek tabakalı hücre hatları için temel doku kültürü teknikleri kullanılarak, at FcεRIα gen (Y18204.1 Gen Bankası) taşıyan, pEE6 plasmidi kullanılarak ebeveyn RBL-2H3.1 hücreleri transfekte. 1.2 x10 7 hücreleri mi -1 yoğunluğunda hücreler 0.8 ml 2 ug plasmid DNA ug ul -1 ekleyin. Hemen ardından 10 dakika süreyle buz üzerinde inkübe 0.4 cm'lik bir electrocuvette kullanılarak, 250 V 960 uF'de hücrelerin elektroporasyonu.
- Genetisin G418 sülfat 0.4 g içeren bir ortam kullanılarak dönüştürülmüş hücreler daha sonra da bir floresan IgE antikorları ile etiketleyerek FACS yoluyla geri kalan canlı hücreler sıralamak. Soruşturma 2, 3, at FcεRIα hücre hattı ifade edilen RBL-2H3.1 kullanın.
- Ön testi, antikor hassasiyeti:
- Hasat birleşen bir Petri kabı at FcεRIα hücrelerini ifade RBL-2H3.1. 5x10 hücre 5 mi -1 değerinde bir hücre yoğunluğu kültür ortamı içinde hücrelerin yeniden askıya yıkayın.
- , 1 ng mL -1 nihai konsantrasyona kadar süspanse hücrelerine ilgi IgE ekleyin daha sonra sütun 1-6 bir 96 kuyulu bir levha üzerine hücre, 100 ul plaka ve 37 ° C ila +% 5 CO2 ile + 90% inkübe 16 saat süre bağıl nem. İnkübasyon süresinden sonra, ve salım deneyi gerçekleştirmeden önce, iyi bir karışmaya ve hücre yapışması için bir mikroskop altında kuyu edin.
2) Salma Deneyi:
- Hücreleri Yıkama:
- Sıcak salınım tamponu 37 ° C 'de (25 mM PIPES, 120 mM sodyum klorür, 5 mM potasyum klorid, 0.04 mM magnezyum klorür, 1 mM kalsiyum klorür), nazik bir hücre yıkama için izin vermek.
- Hücre ortamı çıkarmak için plaka iterek ve sıcak 100 ul ekleyerek 3 hücreleri yıkayın7 ° C, çıkış tamponu. Iki kez tekrarlayın.
- Antigen ile karşılaşmadan:
- Antijenin bir seri seyreltme 0 ng ml -1, mililitre başına 0,1 ng mi -1, 1 ng mL -1, 10 ng mi -1, 100 ng mi -1 (NIP-HSA ve DNP-HSA), 1.000 ng ml hazırlayın -1, 10,000 ng açma tamponu mi -1 ve 37 ° C'de ısıtın.
- Ikinci hücre yıkamadan sonra, ortam atmak ve antijen çözümler 100 ul ile değiştirilir. Aynı sıradaki çukurlar (örneğin A1-6) 'ü ilave aynı antijen konsantrasyonu olduğundan emin olun.
- 0 ng ml -1 antijeni ekleyerek satır A negatif kontrol kurmak. Triton-X tamponu (% 5 Triton X-100), H sırası hücreleri içinde hücreleri lize etmek için, ardından sıra (BG) aşağı doğru artan antijen konsantrasyonu ekleme, bir pozitif kontrol olarak kullanılır. 20 dakika sonra, hücreler, kendi aracıları bırakma izin vermek için 37 ° C'de inkübe edilir.
- Birey kontrolleri ayarlama:
- İnkübasyondan sonra, levha, diğer yarısı (kuyular A1-6 kuyu A7-12 için, vs.), hücre süpernatan 50 ul transfer. Süpernatant geri kalan 50 ul atın ve sütun 1-6 hücrelerin içindeki toplam aracıların yüzdesi de sütun 7-12 her serbest aracıların niceliğin ölçülmesini sağlamak için Triton-X tampon maddesi 50 ul ile değiştirin .
- Enzim alt-tabaka:
- Β-heksosaminidaz alt-tabaka (50 mM 4-nitrofenil N-asetil-β-D-glükozaminit sitrat tamponu 0.2 M sitrik asit ve 0.2 M sodyum asetat ilave edilmesi ile 2 mM'ye kadar seyreltilir DMSO içinde hazırlanmış, pH 4.5) 50 ul ekle Tüm oyuklara β-heksosaminidaz enzim ile 4-nitrofenol için alt-tabaka dönüşümünü kolaylaştırdı. 2 saat boyunca 37 ° C'de inkübe edin.

- Reaksiyonu Sonlandırma:
- Her bir ilave 150 ul Tris tamponu (1 M Tris-HCI, pH 9) ayrıca tampon yüksek pH ile reaksiyonu durdurun reaksiyonu durdurur ve bir sarı renk içine 4-nitrofenol döner.
- Sonuçları Okuma ve analiz:
- Sarı renk içine çekmeyi ölçmek üzere 405 nm 'de bir plakalı spektrofotometresi kullanılarak, plaka okuyun. Aşağıdaki formül kullanılarak serbest β-heksosamınıdaz yüzdesi hesaplanmıştır:
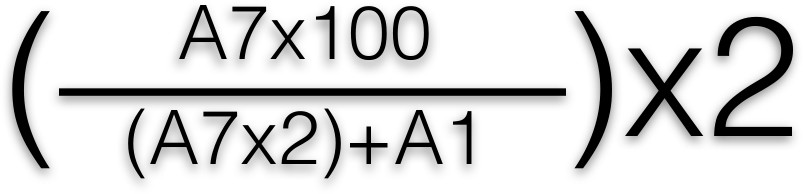
- Ortalama her satır için alınır sonra her kuyuya, bu formülü uygulayın. A1 ve A7 96 oyuklu bir plaka içerisinde kuyu konumunu temsil eder. Agai (toplam mediatör salınımı karşılık) β-heksosaminidaz salımının yüzde grafiğenst antijen konsantrasyonu 2, 3.
Sonuçlar
Ebeveyn RBL-2H3.1 hücreleri ve at FcεRIα reseptörü geni ile transfekte edilmiş olan birinci fare IgE anti-DNP-HSA ile duyarlı ve DNP-HSA antigen ile tehdit edildi. Fare IgE her iki hücre içinde endojen fare reseptörüne bağlanan ve bu nedenle mediatörler (Şekil 1 A) 'serbest bırakmak için, her iki hücre çizgilerinin salma canlılığını test etmek için bir kontrol olarak işlev görür. Bu önemli bir kontroldür ve hücre kültüründe uzatılmış (> 10 hafta) geçmesi üzer...
Tartışmalar
Özetle bu soruşturmanın sonuçları at FcεRIα ifade RBL-2H3.1 hücreleri, bir antijen tarafından at IgE ile duyarlı ve meydan, onlar içinde arabulucu toplam miktarın% 4.88 ± 36,68% bir zirve mediatör salınımını vermek olduğunu gösterdi Hücreler, RBL-2H3.1 göre ana hücreler ekuin FcεRIα ifade değildir.
Dolayısıyla, bu tahlil soruşturma ve in vitro at alerjik yanıtları incelemek için yararlı bir araç sağlar. Onun mast hücresi / bazofil soy hücreleri t...
Açıklamalar
The authors declare that they have no competing financial interests in this paper.
Teşekkürler
The authors thank Dr. Lynda Partridge for the provision of advice and laboratory facilities.
Malzemeler
| Name | Company | Catalog Number | Comments |
| RBL-2H3.1 Expressing Equine FcεRIα | - | - | Produced in the lab |
| Equine IgE anti NIP-HSA | - | - | Produced in the lab |
| 96 Well Plate | Sigma | CLS3595 | - |
| Multi Channel Pipette | Anachem | - | - |
| Incubator | Galaxy R | - | - |
| 4Hydroxy-5-iodo-3-nitrophenylacetic acid | Cambridge Research Biochemicals | N-1070-1 | NIP-OH was conjugated with Human Serum Albumin to make NIP-HSA in the lab |
| Dinitrophenyl Conjugated to Human Serum Albumin | Sigma | A6661 | Abbreviated DNP-HSA |
| Plate Spectrophotometer | Anthos Labtec HT2 | - | - |
| Pipes | Sigma | P1851 | - |
| Sodium Chloride | Sigma | S7653 | - |
| Potassium Chloride | Sigma | P9333 | - |
| Magnesium Chloride | Sigma | M2670 | - |
| Calcium Chloride | Sigma | C1016 | - |
| Triton x100 | Sigma | X100 | - |
| 4-nitrophenyl N-acetyl-β-D-glucosaminide | Sigma | N9376 | Stock solution called β-hexosaminidase substrate was 50mM prepared in DMSO |
| Dimethyl Sulfoxide | Sigma | D2650 | - |
| Citric Acid | Sigma | 251275 | - |
| Sodium Acetate | Sigma | S7670 | - |
| Tris | Sigma | T5941 | - |
Referanslar
- Taudou, G., et al. Expression of the Alpha Chain of Human FcεRI in Transfected Rat Basophilic Leukemia Cells: Functional Activation after Sensitization with Human Mite-Specific IgE. Int Arch Allergy Immunol. 100 (4), 344-350 (1993).
- Sabban, S. . Development of an in Vitro Model System for Studying the Interaction of EquuscaballusIgE with Its High-Affinity FcεRI Receptor. , (2011).
- Sabban, S., Ye, H., Helm, B. A. Development of an in Vitro Model System for Studying the Interaction of EquuscaballusIgE with Its High-Affinity Receptor FcεRI. Vet ImmunolImmunopathol. 153 (1-2), 6-10 (2013).
- Wilson, A. P. M., Pullar, C. E., Camp, A. M., Helm, B. A. Human IgE mediates stimulus secretion coupling in rat basophilic leukemia cells transfected with the a chain of the human high-affinity receptor. Eur J Immunol. 23, 240-244 (1993).
- Hunter, M. J., Vratimos, A. P., Housden, J. E. M., Helm, B. A. Generation of canine-human Fc IgE chimeric antibodies for the determination of the canine IgE domain of interaction with FcεRIα. MolImmunol. 45 (8), 2262-2268 (2008).
- Rashid, A., et al. Review: Diagnostic and therapeutic applications of rat basophilic leukemia cells. MolImmunol. 52 (3-4), 224-228 (2012).
- Cohen, S. G. Asthma in antiquity: the Ebers Papyrus. Allergy Proc. 13 (3), 147-154 (1992).
- Dudler, T., et al. A link between catalytic activity, IgE-independent mast cell activation, and allergenicity of bee venom phospholipase A2. J. Immunol. 155, 2605-2613 (1995).
- Machado, D. C., Horton, D., Harrop, R., Peachell, P. T., Helm, B. A. Potential allergens stimulate the release of mediators of the allergic response from cells of mast cell lineage in the absence of sensitization with antigen-specific IgE. Eur J Immunol. 26 (12), 2972-2980 (1996).
- Smyth, L. J., et al. Assessment of the molecular basis of pro-allergenic effects of cigarette smoke. Environ Sci Technol. 34 (7), 1370-1374 (2000).
- Okada, H., Kuhn, C., Feillet, H., Bach, J. F. The 'hygiene hypothesis' for autoimmune and allergic diseases: an update. ClinExpImmunol. 160 (1), 1-9 (2010).
- Eder, C., et al. Influence of environmental and genetic factors on allergen-specific immunoglobulin-E levels in sera from Lipizzan horses. Equine Vet J. 33 (7), 714-720 (2001).
- Cook, W. R., Rossdale, P. D. The syndrome of 'Broken Wind' in the horse. Proceedings of the Royal Society of Medicine. 56, 972-977 (1963).
- Eyre, P., Lewis, A. J. Acute systemic anaphylaxis in the horse. Br. J. Pharmacol. 48 (3), 426-437 (1973).
- Wagner, B. IgE in horses: occurrence in health and disease. Vet ImmunolImmunopathol. 132 (1), 21-23 (2009).
- Hellberg, W., et al. Equine insect bite hypersensitivity: immunoblot analysis of IgE and IgG subclass responses to Culicoidesnubeculosus salivary gland extract. Vet. Immunol. Immunopathol. 113 (1-2), 99-112 (2006).
- Schaffartzik, A., et al. Equine insect bite hypersensitivity: what do we know. Vet ImmunolImmunopathol. 147 (3-4), 113-126 (2012).
- Künzle, F., et al. IgE-bearing cells in bronchoalveolar lavage fluid and allergen-specific IgE levels in sera from RAO-affected horses. J Vet Med A PhysiolPatholClin Med. 54 (1), 40-47 (2007).
- Tahon, L., et al. In vitro allergy tests compared to intradermal testing in horses with recurrent airway obstruction. Vet ImmunolImmunopathol. (1-2), 85-93 (2009).
- Wagner, B., Radbruch, A., Rohwer, J., Leibold, W. Monoclonal anti-equine IgE antibodies with specificity for different epitopes on the immunoglobulin heavy chain of native IgE. Vet ImmunolImmunopathol. 92 (1-2), 45-60 (2003).
- Wilson, A. D., Harwood, L., Torsteinsdottir, S., Marti, E. Production of monoclonal antibodies specific for native equine IgE and their application to monitor total serum IgE responses in Icelandic and non-Icelandic horses with insect bite dermal hypersensitivity. Vet ImmunolImmunopathol. 112 (3-4), 156-170 (2006).
- McAleese, S. M., et al. Cloning and expression of the extra-cellular part of the alpha chain of the equine high-affinity IgE receptor and its use in the detection of IgE. Vet ImmunolImmunopathol. 110 (1-2), 187-191 (2006).
- Ledin, A., et al. Generation of therapeutic antibody responses against IgE in dogs, an animal species with exceptionally high plasma IgE levels. Vaccine. 24 (1), 66-74 (2006).
- Siraganian, R. P., Hook, W. A. Histamine release and assay methods for the study of human allergy. Manual of Clinical Immunology. , (1980).
- Neuberger, M. S., et al. A hapten-specific chimaericIgE antibody with human physiological effector function. Nature. 314 (6008), 268-270 (1985).
- Bingham, B. R., Monk, P. N., Helm, B. A. Defective Protein Phosphorylation and Ca2+ Mobilization in a low secreting variant of the rat basophilic leukemia cell line. The Journal of Biological Chemistry. 269 (30), 19300-19306 (1994).
- McAleese, S. M., Halliwell, R. E., Miller, H. R. Cloning and sequencing of the horse and sheep high-affinity IgE receptor alpha chain cDNA. Immunogenetics. 1 (51), 878-881 (2000).
- Hongtu, Y. Study of the structure/function relationship in canine and human IgE as the basis for the development of rational therapeutic intervention strategies in allergic disease. , (2010).
- Sabban, S., et al. Towards a pan-anti-allergy vaccine. JIBTVA. 2 (2), 15-27 (2013).
- Moran, G., Burgos, R., Araya, O., Folch, H. In vitro bioassay to detect reaginic antibodies from the serum of horses affected with recurrent airway obstruction. Vet Res Commun. 34, 91-99 (2010).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır