Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Développement d'un
Dans cet article
Résumé
The current study describes the development and applications of a genetically engineered assay system based on the transfection of rat basophilic leukemia cells with the equine FcεRIα gene. Transfected cells express a functional receptor where the release of mediators of the allergic response can be activated by IgE and antigen.
Résumé
The interaction of IgE with its high-affinity Fc receptor (FcεRI) followed by an antigenic challenge is the principal pathway in IgE mediated allergic reactions. As a consequence of the high affinity binding between IgE and FcεRI, along with the continuous production of IgE by B cells, allergies usually persist throughout life, with currently no permanent cure available. Horses, especially race horses, which are commonly inbred, are a species of mammals that are very prone to the development of hypersensitivity responses, which can seriously affect their performance. Physiological responses to allergic sensitization in horses mirror that observed in humans and dogs. In this paper we describe the development of an in situ assay system for the quantitative assessment of the release of mediators of the allergic response pertaining to the equine system. To this end, the gene encoding equine FcεRIα was transfected into and expressed onto the surface of parental Rat Basophil Leukemia (RBL-2H3.1) cells. The gene product of the transfected equine α-chain formed a functional receptor complex with the endogenous rat β- and γ-chains 1. The resultant assay system facilitated an assessment of the quantity of mediator secreted from equine FcεRIα transfected RBL-2H3.1 cells following sensitization with equine IgE and antigenic challenge using β-hexosaminidase release as a readout 2, 3. Mediator release peaked at 36.68% ± 4.88% at 100 ng ml-1 of antigen. This assay was modified from previous assays used to study human and canine allergic responses 4, 5. We have also shown that this type of assay system has multiple applications for the development of diagnostic tools and the safety assessment of potential therapeutic intervention strategies in allergic disease 6, 2, 3.
Introduction
Allergie est connue depuis des millénaires. Un traitement de l'asthme a été décrit dans le texte médical égyptien antique connu sous le papyrus Ebers (~ 1550 avant notre ère) et discuté remèdes pour traiter 7.
allergie est aujourd'hui considéré comme une réponse d'hypersensibilité de type I, où le type T cellulaire auxiliaire 2 (TH 2) du bras du système immunitaire dirige la production d'immunoglobulines E (IgE), des anticorps en réponse à des antigènes environnementaux appelés allergènes. Ce sont diverses substances qui interagissent couramment avec les cellules du système immunitaire et stimuler la synthèse et la sécrétion de cytokines pro-inflammatoires, y compris l'interleukine-4 et l'interleukine-13, 8, 9 comme ne particules dans les particules de fumée de cigarette ou diesel échappement qui augmente la synthèse des IgE 10.
La hausse des manifestations allergiques dans les pays industrialisés au cours des 50 dernières années a été attribué à une combinaison de l'effet depolluants de l'environnement et une tendance à un environnement plus aseptisé, qui se combinent pour décaler la réponse immunitaire vers un profil prédominé par Th 2 cytokines, telle que proposée par la 'hypothèse hygiénique »11.
Comme mentionné ci-dessus, l'homme ne sont pas les seuls mammifères affligés par une allergie. Notamment les chevaux et les chiens peuvent aussi développer des réactions allergiques classiques et une étude de 12 a montré que, comme chez les humains, l'allergie équin est attribuée à des facteurs génétiques et environnementaux. En conséquence, ces animaux présentent de bons modèles pour étudier l'interaction entre les facteurs génétiques et environnementaux de l'allergie, la progression de la sensibilisation à la maladie et les stratégies d'intervention possibles une fois les manifestations cliniques sont fixés dans
En 1887, Stömmer était la première personne pour décrire la similitude entre l'homme et l'asthme équine 13, l'effet de l'histamine sur le système cardio-vasculaire équine esttrès similaire à celui des humains 14. Les chevaux sont aussi la pierre angulaire de l'industrie des courses de chevaux, qui vaut 72 milliards de dollars, un chiffre d'affaires de paris de 115 milliards de dollars par an 15.
La plupart des chevaux de course contemporains sont des descendants du petit nombre de chevaux arabes élevés par Lady Anne Blunt à partir de 1878. Chevaux de course modernes sont souvent consanguins à sélectionner pour les capacités de performance. Ils sont sujets à des troubles génétiques, dont l'un est leur susceptibilité à monter des réponses allergiques. Ils ont aussi 1000 fois plus élevés que les niveaux d'IgE sériques même les êtres humains plus sévèrement allergique 16. réactions allergiques à cheval sont se manifeste habituellement par une hypersensibilité insecte morsure (IBH) 17, 18. IBH résultats dans des dermatoses dues aux piqûres d'insectes forment dans le genre Culicoides. Une autre forme de la maladie allergique équine est obstructions des voies respiratoires récurrentes (RAO), cela se manifeste dans les poumons et les voies respiratoires. Elle est caractérisée par une respiration sifflante et laboratoirerespiration ORed. RAO se produit généralement en réponse à spores de moisissures, et des niveaux élevés d'IgE spécifiques des allergènes ont été enregistrés chez les chevaux atteints de RAO dans une étude 19 mais une autre enquête n'a pas confirmé cette 20.
Des études sur l'allergie équine ont tourné autour de l'essai de contrôle et de neutraliser équine IgE par le développement d'anticorps anti-équin IgE monoclonal (mAb) 21, 22. En outre, l'étude de 23 traite de la production de domaines extracellulaires de l'α de l'équin haute affinité Fc récepteur chaîne (FcεRIα) récepteur dans le but de détecter et de quantifier le sérum équin IgE. Une étude connexe par Ledin 24 traite d'une nouvelle approche visant à neutraliser les IgE sériques en amorçant le système immunitaire en utilisant un auto / non-soi immunogène. Toutes ces études, cependant, manquait un dosage efficace pour tester l'innocuité et l'efficacité de leurs protocoles. Dans cet article, nous présentons un tel sys d'essaisystème applicable à l'étude des stratégies diagnostiques et thérapeutiques pertinentes pour le système équin, où β-hexosaminidase libération, comme un indicateur de médiateur de la dégranulation cellulaire, a été évaluée sur des cellules RBL-2H3.1 exprimant FcεRIα équine. Ce protocole est basé sur des publications antérieures 25, 4, 5, 2, 3, décrivant l'ingénierie de cellules RBL transfectées avec le gène codant le domaine de liaison du récepteur IgE de haute affinité pour les IgE provenant d'espèces différentes. Le protocole explique comment effectuer un test de libération de β-hexosaminidase, dont les résultats sont présentés en moyenne ± écart-type d'expériences en triple.
Le dosage de la libération a été développé par Siraganian et le crochet 25 pour étudier allergie humaine. Le groupe de laboratoire dirigé par le Dr Reuben Siraganian également développé la lignée cellulaire RBL. Ces cellules RBL ont été développés pour exprimer la FcεRIα humain et le protocole a été publié par 4. La dernière piècedu dosage fournie avec le développement du plasmide pSV dans le papier par Neuberger 26 qui décrit la production d'un anticorps IgE par clonage de son gène de chaîne lourde en aval d'un gène de la souris pour une région variable d'IgE qui cible l'haptène 4-hydroxy-3 nitro-phénacétyle (NP), l'anticorps chimérique résultant était pleinement fonctionnel. La possibilité de développer tout IgE ciblant le même haptène, tout en clonant son récepteur sur la surface des cellules RBL abouti à la normalisation du dosage qui en fait un protocole utile pour mesurer la dégranulation des basophiles.
Le test a des avantages et des inconvénients. Les avantages du dosage est son adaptabilité à être utilisé dans un système de mammifère, notre laboratoire a ainsi utilisé pour tester la dégranulation dans les systèmes humains, canins, équins, ce qui est réalisable simplement par synthèse d'IgE de l'organisme et le clonage de son récepteur sur la surface des cellules RBL.
D'autre part,les inconvénients de l'essai est que les cellules RBL sont très sensibles aux variations thermiques, mécaniques et PH, ce qui leur donne une variation des niveaux de dégranulation au sein de la même dosage. Il est donc fortement conseillé que les essais sont toujours répétées en triple, puis en prenant la moyenne de leur part. En outre, les cellules RBL ont tendance à se déplacer vers un phénotype non-libération si elles sont laissées en culture de tissu pendant des périodes prolongées (> 10 semaines) 27, ce qui rend leur entretien lourd. Elles sont également sujettes à des infections par des bactéries de mycoplasmes, qui ne sont pas visibles à partir d'un microscope optique et ne modifient pas la morphologie de la cellule, mais cela changerait radicalement leurs niveaux de dégranulation. Ainsi des tests réguliers de mycoplasmes sont nécessaires.
Protocole
1) Préparation de la lignée cellulaire:
- Le développement de la lignée de cellules RBL-de 2H3.1 exprimer équins α FceRI:
- En utilisant des techniques de base de culture de tissus de lignées de cellules en monocouche, transfecter des cellules RBL-2H3.1 parentales en utilisant le plasmide pEE6, portant le gène équine FcεRIα (GenBank: Y18204.1) 28. Ajouter 2 ul -1 pg de l'ADN plasmidique de 0,8 ml de cellules à une densité de 1,2 x 10 7 cellules ml -1. L'électroporation des cellules à 250 V 960 pF en utilisant un 0,4 cm electrocuvette puis incuber immédiatement sur la glace pendant 10 min.
- Sélectionnez les cellules transformées en utilisant les médias contenant 0,4 g de sulfate de généticine G418, puis trier les cellules vivantes restantes par FACS en les étiquetant avec un anticorps fluorescent IgE. Utilisez le RBL-2H3.1 résultant lignée cellulaire exprimant FcεRIα équine de l'enquête 2, 3.
- Pré-test anticorps sensibilisation:
- Récolte la RBL-2H3.1 cellules exprimant FcεRIα d'équidés en provenance d'une boîte de Pétri de confluence. Laver ensuite remettre en suspension les cellules dans un milieu de culture à une densité cellulaire de 5x10 5 cellules ml-1.
- Ajouter l'IgE de l'intérêt pour les cellules en suspension à une concentration finale de 1 ng ml-1, puis la plaque 100 pl de cellules sur une plaque à 96 puits à colonnes 1-6 et incuber à 37 ° C + 5% de CO 2 + 90% humidité relative pendant 16 heures. Après le temps d'incubation, et avant d'effectuer le test de libération, vérifier les puits sous un microscope pour bien confluence et l'adhérence des cellules.
2) Dosage de libération:
- Lavage des cellules:
- Un tampon de sortie chaud (25 mM de PIPES, du chlorure de sodium 120 mM, 5 mM de chlorure de potassium, 0,04 mM de chlorure de magnésium et 1 mM de chlorure de calcium) à 37 ° C pour permettre le lavage des cellules en douceur.
- Laver les cellules en tapotant la plaque pour enlever médias cellulaires et ajouter 100 ul chaud, 37 ° C, tampon de sortie. Répéter deux fois.
- Défi antigène:
- Préparer une série de dilutions de l'antigène (NIP-HSA ou DNP-HSA) de 0 ng ml -1, 0,1 ng ml -1, 1 ng ml -1, 10 ng ml -1, 100 ng ml -1, 1 000 ng ml -1, 10 000 ng ml -1 dans le tampon de sortie et chaud à 37 ° C.
- Après le second lavage de cellules, éliminer les médias et remplacé par 100 ul de la solution d'antigène. Veiller à ce que les puits dans la même rangée (A1-6, par exemple) ont la même concentration ajoutée à leur antigène.
- Mettre en place un contrôle négatif à la ligne A en ajoutant 0 antigène -1 ml ng. Ajouter augmentation de la concentration de l'antigène dans les rangées (BG), suivie par triton x-tampon (5% de Triton X-100) dans les cellules de rangées H à lyser les cellules pour être utilisé en tant que contrôle positif. Incuber à 37 ° C pendant 20 min pour permettre aux cellules de libérer ses médiateurs.
- Configuration du contrôle de puits individuels:
- Après l'incubation, transférer 50 pi de surnageant de cellules à l'autre moitié de la plaque (A1-6 puits à puits A7-12, etc.). Jeter les 50 ul de surnageant restant et le remplacer par 50 ul de Triton X-tampon pour permettre la mesure de la quantité de médiateurs libérés à chaque puits dans les colonnes 7 à 12 en pourcentage du total des médiateurs à l'intérieur des cellules dans la colonne 1-6 .
- Substrat enzymatique:
- Ajouter 50 ul de substrat de β-hexosaminidase (mM 4-nitrophényl N-acétyl-β-D-de glucosaminide préparé dans du DMSO dilué jusqu'à 2 mM en l'ajoutant à un tampon de citrate 0,2 M d'acide citrique et 0,2 M d'acétate de sodium, pH 4,5 à 50) dans tous les puits de la facilité de conversion du substrat de 4-nitrophénol par l'enzyme β-hexosaminidase. Incuber les plaques à 37 ° C pendant 2 heures.

- Mettre fin à la réaction:
- Arrêter la réaction par l'ajout de 150 ul de tampon Tris (1 M de Tris-HCl, pH 9) à chaque puits comme le pH élevé de la mémoire tampon arrête la réaction et le transforme en 4-nitrophénol de couleur jaune.
- La lecture et l'analyse des résultats:
- Lire la plaque à l'aide d'un spectrophotomètre de plaque à 405 nm pour mesurer l'absorbance de la couleur jaune. Calculé le pourcentage de β-hexosaminidase libéré en utilisant la formule suivante:
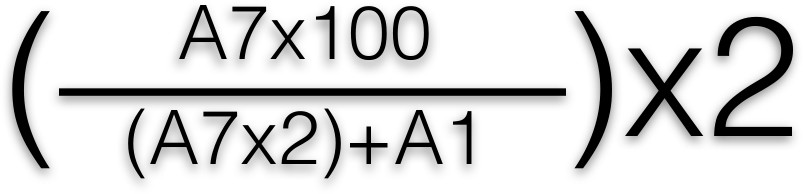
- Appliquer cette formule à chaque puits, après quoi une moyenne est calculée pour chaque ligne. A1 et A7 représentent la position des puits dans la plaque à 96 puits. Tracer la courbe de pourcentage de β-hexosaminidase de presse (qui correspond à la libération totale du médiateur) contantigène NST de concentration 2, 3.
Résultats
Les cellules RBL-2H3.1 parentales et celles transfectées avec le gène du récepteur de FcεRIα équine ont d'abord été sensibilisées avec des IgE de souris anti- DNP-HSA et la provocation avec l'antigène DNP-HSA. IgE de souris se lie au récepteur de rat endogène dans les deux lignées cellulaires et agit comme un contrôle pour tester la viabilité de la libération de deux lignées cellulaires pour libérer des médiateurs (figure 1 A) ainsi. Ceci est un test important et doit être ef...
Discussion
En résumé, les résultats de cette enquête ont montré que lorsque les cellules RBL-2H3.1 exprimant FcεRIα équins sont sensibilisées avec équine IgE et remis en cause par un antigène, ils donnent un pic de libération de médiateur de 36,68% ± 4,88% du montant total de médiateur à l'intérieur du cellules, par rapport à la RBL-2H3.1 cellules parentales non exprimant équine FcεRIα.
Ainsi, ce test fournit un outil utile pour étudier et étudier les réponses allergiques é...
Déclarations de divulgation
The authors declare that they have no competing financial interests in this paper.
Remerciements
The authors thank Dr. Lynda Partridge for the provision of advice and laboratory facilities.
matériels
| Name | Company | Catalog Number | Comments |
| RBL-2H3.1 Expressing Equine FcεRIα | - | - | Produced in the lab |
| Equine IgE anti NIP-HSA | - | - | Produced in the lab |
| 96 Well Plate | Sigma | CLS3595 | - |
| Multi Channel Pipette | Anachem | - | - |
| Incubator | Galaxy R | - | - |
| 4Hydroxy-5-iodo-3-nitrophenylacetic acid | Cambridge Research Biochemicals | N-1070-1 | NIP-OH was conjugated with Human Serum Albumin to make NIP-HSA in the lab |
| Dinitrophenyl Conjugated to Human Serum Albumin | Sigma | A6661 | Abbreviated DNP-HSA |
| Plate Spectrophotometer | Anthos Labtec HT2 | - | - |
| Pipes | Sigma | P1851 | - |
| Sodium Chloride | Sigma | S7653 | - |
| Potassium Chloride | Sigma | P9333 | - |
| Magnesium Chloride | Sigma | M2670 | - |
| Calcium Chloride | Sigma | C1016 | - |
| Triton x100 | Sigma | X100 | - |
| 4-nitrophenyl N-acetyl-β-D-glucosaminide | Sigma | N9376 | Stock solution called β-hexosaminidase substrate was 50mM prepared in DMSO |
| Dimethyl Sulfoxide | Sigma | D2650 | - |
| Citric Acid | Sigma | 251275 | - |
| Sodium Acetate | Sigma | S7670 | - |
| Tris | Sigma | T5941 | - |
Références
- Taudou, G., et al. Expression of the Alpha Chain of Human FcεRI in Transfected Rat Basophilic Leukemia Cells: Functional Activation after Sensitization with Human Mite-Specific IgE. Int Arch Allergy Immunol. 100 (4), 344-350 (1993).
- Sabban, S. . Development of an in Vitro Model System for Studying the Interaction of EquuscaballusIgE with Its High-Affinity FcεRI Receptor. , (2011).
- Sabban, S., Ye, H., Helm, B. A. Development of an in Vitro Model System for Studying the Interaction of EquuscaballusIgE with Its High-Affinity Receptor FcεRI. Vet ImmunolImmunopathol. 153 (1-2), 6-10 (2013).
- Wilson, A. P. M., Pullar, C. E., Camp, A. M., Helm, B. A. Human IgE mediates stimulus secretion coupling in rat basophilic leukemia cells transfected with the a chain of the human high-affinity receptor. Eur J Immunol. 23, 240-244 (1993).
- Hunter, M. J., Vratimos, A. P., Housden, J. E. M., Helm, B. A. Generation of canine-human Fc IgE chimeric antibodies for the determination of the canine IgE domain of interaction with FcεRIα. MolImmunol. 45 (8), 2262-2268 (2008).
- Rashid, A., et al. Review: Diagnostic and therapeutic applications of rat basophilic leukemia cells. MolImmunol. 52 (3-4), 224-228 (2012).
- Cohen, S. G. Asthma in antiquity: the Ebers Papyrus. Allergy Proc. 13 (3), 147-154 (1992).
- Dudler, T., et al. A link between catalytic activity, IgE-independent mast cell activation, and allergenicity of bee venom phospholipase A2. J. Immunol. 155, 2605-2613 (1995).
- Machado, D. C., Horton, D., Harrop, R., Peachell, P. T., Helm, B. A. Potential allergens stimulate the release of mediators of the allergic response from cells of mast cell lineage in the absence of sensitization with antigen-specific IgE. Eur J Immunol. 26 (12), 2972-2980 (1996).
- Smyth, L. J., et al. Assessment of the molecular basis of pro-allergenic effects of cigarette smoke. Environ Sci Technol. 34 (7), 1370-1374 (2000).
- Okada, H., Kuhn, C., Feillet, H., Bach, J. F. The 'hygiene hypothesis' for autoimmune and allergic diseases: an update. ClinExpImmunol. 160 (1), 1-9 (2010).
- Eder, C., et al. Influence of environmental and genetic factors on allergen-specific immunoglobulin-E levels in sera from Lipizzan horses. Equine Vet J. 33 (7), 714-720 (2001).
- Cook, W. R., Rossdale, P. D. The syndrome of 'Broken Wind' in the horse. Proceedings of the Royal Society of Medicine. 56, 972-977 (1963).
- Eyre, P., Lewis, A. J. Acute systemic anaphylaxis in the horse. Br. J. Pharmacol. 48 (3), 426-437 (1973).
- Wagner, B. IgE in horses: occurrence in health and disease. Vet ImmunolImmunopathol. 132 (1), 21-23 (2009).
- Hellberg, W., et al. Equine insect bite hypersensitivity: immunoblot analysis of IgE and IgG subclass responses to Culicoidesnubeculosus salivary gland extract. Vet. Immunol. Immunopathol. 113 (1-2), 99-112 (2006).
- Schaffartzik, A., et al. Equine insect bite hypersensitivity: what do we know. Vet ImmunolImmunopathol. 147 (3-4), 113-126 (2012).
- Künzle, F., et al. IgE-bearing cells in bronchoalveolar lavage fluid and allergen-specific IgE levels in sera from RAO-affected horses. J Vet Med A PhysiolPatholClin Med. 54 (1), 40-47 (2007).
- Tahon, L., et al. In vitro allergy tests compared to intradermal testing in horses with recurrent airway obstruction. Vet ImmunolImmunopathol. (1-2), 85-93 (2009).
- Wagner, B., Radbruch, A., Rohwer, J., Leibold, W. Monoclonal anti-equine IgE antibodies with specificity for different epitopes on the immunoglobulin heavy chain of native IgE. Vet ImmunolImmunopathol. 92 (1-2), 45-60 (2003).
- Wilson, A. D., Harwood, L., Torsteinsdottir, S., Marti, E. Production of monoclonal antibodies specific for native equine IgE and their application to monitor total serum IgE responses in Icelandic and non-Icelandic horses with insect bite dermal hypersensitivity. Vet ImmunolImmunopathol. 112 (3-4), 156-170 (2006).
- McAleese, S. M., et al. Cloning and expression of the extra-cellular part of the alpha chain of the equine high-affinity IgE receptor and its use in the detection of IgE. Vet ImmunolImmunopathol. 110 (1-2), 187-191 (2006).
- Ledin, A., et al. Generation of therapeutic antibody responses against IgE in dogs, an animal species with exceptionally high plasma IgE levels. Vaccine. 24 (1), 66-74 (2006).
- Siraganian, R. P., Hook, W. A. Histamine release and assay methods for the study of human allergy. Manual of Clinical Immunology. , (1980).
- Neuberger, M. S., et al. A hapten-specific chimaericIgE antibody with human physiological effector function. Nature. 314 (6008), 268-270 (1985).
- Bingham, B. R., Monk, P. N., Helm, B. A. Defective Protein Phosphorylation and Ca2+ Mobilization in a low secreting variant of the rat basophilic leukemia cell line. The Journal of Biological Chemistry. 269 (30), 19300-19306 (1994).
- McAleese, S. M., Halliwell, R. E., Miller, H. R. Cloning and sequencing of the horse and sheep high-affinity IgE receptor alpha chain cDNA. Immunogenetics. 1 (51), 878-881 (2000).
- Hongtu, Y. Study of the structure/function relationship in canine and human IgE as the basis for the development of rational therapeutic intervention strategies in allergic disease. , (2010).
- Sabban, S., et al. Towards a pan-anti-allergy vaccine. JIBTVA. 2 (2), 15-27 (2013).
- Moran, G., Burgos, R., Araya, O., Folch, H. In vitro bioassay to detect reaginic antibodies from the serum of horses affected with recurrent airway obstruction. Vet Res Commun. 34, 91-99 (2010).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon