É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Desenvolvimento de um
Neste Artigo
Resumo
The current study describes the development and applications of a genetically engineered assay system based on the transfection of rat basophilic leukemia cells with the equine FcεRIα gene. Transfected cells express a functional receptor where the release of mediators of the allergic response can be activated by IgE and antigen.
Resumo
The interaction of IgE with its high-affinity Fc receptor (FcεRI) followed by an antigenic challenge is the principal pathway in IgE mediated allergic reactions. As a consequence of the high affinity binding between IgE and FcεRI, along with the continuous production of IgE by B cells, allergies usually persist throughout life, with currently no permanent cure available. Horses, especially race horses, which are commonly inbred, are a species of mammals that are very prone to the development of hypersensitivity responses, which can seriously affect their performance. Physiological responses to allergic sensitization in horses mirror that observed in humans and dogs. In this paper we describe the development of an in situ assay system for the quantitative assessment of the release of mediators of the allergic response pertaining to the equine system. To this end, the gene encoding equine FcεRIα was transfected into and expressed onto the surface of parental Rat Basophil Leukemia (RBL-2H3.1) cells. The gene product of the transfected equine α-chain formed a functional receptor complex with the endogenous rat β- and γ-chains 1. The resultant assay system facilitated an assessment of the quantity of mediator secreted from equine FcεRIα transfected RBL-2H3.1 cells following sensitization with equine IgE and antigenic challenge using β-hexosaminidase release as a readout 2, 3. Mediator release peaked at 36.68% ± 4.88% at 100 ng ml-1 of antigen. This assay was modified from previous assays used to study human and canine allergic responses 4, 5. We have also shown that this type of assay system has multiple applications for the development of diagnostic tools and the safety assessment of potential therapeutic intervention strategies in allergic disease 6, 2, 3.
Introdução
Alergia é conhecida há milênios. Um tratamento da asma foi descrita no texto médico egípcio antigo conhecido como o Papiro de Ebers (~ 1.550 aC) e discutido ervas remédios para tratá-la 7.
Hoje alergia é classificada como uma resposta de hipersensibilidade do tipo I, em que o tipo de célula T helper 2 (TH 2) o braço do sistema imunitário dirige a produção de (IgE) anticorpos imunoglobulina E em resposta a antigénios ambientais chamados alérgenos. Estes são diversas substâncias que normalmente interagem com as células do sistema imunológico e estimular a síntese e secreção de citocinas pró-inflamatórias, incluindo a interleucina-4 e interleucina-13 8, 9, conforme se em partículas do fumo do cigarro ou do escape de diesel de partículas que aumentam a síntese de IgE 10.
O aumento nas manifestações alérgicas em países industrializados nos últimos 50 anos, tem sido atribuída a uma combinação do efeito depoluentes ambientais e uma tendência para um ambiente mais higienizado, que combinam a mudar a resposta imunológica para um perfil predominou por TH duas citocinas, tal como proposto pelo "Hipótese da Higiene" 11.
Como mencionado acima, os seres humanos não são os únicos mamíferos afetados por alergia. Notavelmente cavalos e cães também podem desenvolver reações alérgicas clássicos e um estudo de 12 mostrou que, como nos seres humanos, a alergia eqüina é atribuída a fatores genéticos e ambientais. Como consequência, esses animais apresentam bons modelos para o estudo da interação entre causas genéticas e ambientais de alergia, a sua progressão de sensibilização para a doença, e as possíveis estratégias de intervenção uma vez que as manifestações clínicas definidas em
Em 1887, Stömmer foi a primeira pessoa a descrever a semelhança entre o ser humano e asma equina 13, o efeito da histamina sobre o sistema cardiovascular é equinamuito semelhante à dos seres humanos 14. Cavalos também são a pedra angular da indústria de corridas a cavalo, que vale US $ 72 bilhões, com um volume de apostas de US $ 115 bilhões por ano 15.
A maioria dos cavalos de corrida contemporâneos são descendentes do pequeno número de cavalos árabes criados por Lady Anne Blunt de 1878 em diante. Cavalos de corrida modernos são comumente pura a escolha de habilidades de desempenho. Eles são propensas a doenças genéticas, uma das quais é a sua susceptibilidade para montar respostas alérgicas. Eles também têm mil vezes mais altos níveis séricos de IgE do que até mesmo os mais severamente alérgica seres humanos 16. Respostas alérgicas cavalo são geralmente se manifesta como hipersensibilidade picada de inseto (IBH) 17, 18. Resultados IBH na dermatite devido a picadas de insetos formam no gênero Culicoides. Outra forma de doença alérgica eqüina é obstruções das vias respiratórias recorrentes (RAO), isso se manifesta nos pulmões e vias respiratórias. É caracterizada por chiado e laboratóriorespiração ORed. RAO comumente ocorre em resposta a esporos, e altos níveis de IgE alérgeno-específicos foram registrados em cavalos que sofrem de RAO em um estudo de 19, embora outra investigação não confirmou esta 20.
Estudos sobre alergia equina girado em torno da tentativa de controlar e neutralizar equina IgE através do desenvolvimento de anticorpos monoclonais anti-IgE equino (mAbs) 21, 22. Além disso, o estudo de 23 discute a produção dos domínios extracelulares de α o de elevada afinidade do receptor de Fc equina cadeia (FceRIa) receptor, na tentativa de detectar e quantificar soro eqüino IgE. Um estudo relacionado por Ledin 24 discute uma nova abordagem visando neutralizar IgE soro por priming do sistema imunológico através de um auto / não-auto imunógeno. Todos estes estudos, no entanto, faltava um ensaio eficaz para testar a segurança e eficácia dos seus protocolos. Neste artigo, vamos agora apresentar tal sys ensaiotempe aplicável ao estudo de estratégias de diagnóstico e terapêuticos relevantes para o sistema equina, onde libertação β-hexosaminidase, como um indicador de mediador de células desgranulação, foi avaliada em células RBL-2H3.1 expressam equina FceRIa. Este protocolo baseia-se em publicações anteriores 25, 4, 5, 2, 3 descrevem a engenharia de células RBL transfectadas com o gene que codifica o domínio de ligação do receptor de IgE de alta afinidade para IgE a partir de espécies diferentes. O protocolo explica como realizar um ensaio de libertação de β-hexosaminidase, cujos resultados são apresentados como a média ± desvio padrão de experiências em triplicado.
O ensaio de liberação foi desenvolvido pela primeira vez por Siraganian e Gancho 25 para estudar alergia humano. O grupo de laboratório liderado pelo Dr. Reuben Siraganian também desenvolveu a linha de células RBL. Estas células RBL foram desenvolvidos para expressar o FceRIa humana e o protocolo foi publicada por 4. A peça finaldo ensaio de veio com o desenvolvimento do plasmídeo pSV no papel por Neuberger 26, que descreveu a produção de anticorpos IgE por uma clonagem do seu gene de cadeia pesada a jusante de um gene de rato para uma região variável de IgE que tem como alvo o hapteno 4-hidroxi-3 -nitro-fenacetilo (NP), o anticorpo quimérico resultante era totalmente funcional. A capacidade de desenvolver qualquer IgE direccionamento do mesmo hapteno, ao mesmo tempo, a clonagem do seu receptor na superfície das células RBL resultaram na padronização do ensaio tornando-se um protocolo útil para medir a desgranulação de basófilos.
O ensaio tem prós e contras. As vantagens do ensaio é a sua adaptabilidade para ser utilizado em qualquer sistema de mamífero, o nosso laboratório tem, assim, usou-o para testar para a desgranulação nos sistemas humanos, caninos e equinos, e isso pode ser conseguido simplesmente através da síntese de IgE do organismo e a clonagem do seu receptor sobre a superfície das células RBL.
Por outro lado,os contras do ensaio é que as células RBL são muito sensíveis a alterações térmicas, mecânicas e de PH, tornando-os dão uma variação de níveis de degranulação dentro do mesmo ensaio. É, portanto, altamente recomendável que os ensaios são sempre repetidas em triplicata e, em seguida, uma média é tomada a partir delas. Além disso, as células RBL tendem a deslocar para um fenótipo de não desprendimento, se forem deixados em cultura de tecidos durante tempos prolongados (> 10 semanas) 27, tornando complicada a sua manutenção. Eles também são propensos a infecções por micoplasma, bactérias que não são visíveis a partir de um microscópio de luz e não modificam a morfologia da célula, mas iria alterar drasticamente os seus níveis de degranulação. Assim, são necessários testes de micoplasma regulares.
Protocolo
1) Preparação de Linha de Células:
- O desenvolvimento da linha celular RBL-2H3.1 expressando α FcsRI eqüinos:
- Usando técnicas básicas de cultura de tecidos para linhas de células em monocamada, transfectar células RBL-2H3.1 parental usando o plasmídeo pEE6, que transporta o gene equina FceRIa (GenBank: Y18204.1) 28. Adicionar 2 ug -1 ul do DNA de plasmídeo a 0,8 ml de células a uma densidade de 1,2 x 10 7 células mL @ 1. Electroporate as células a 250 V, 960 uF utilizando um 0,4 centímetros electrocuvette depois incubar imediatamente em gelo durante 10 min.
- Selecione as células transformadas utilizando meios contendo 0,4 g de sulfato de geneticina G418, em seguida, classificar as restantes células vivas através FACS por marcá-los com um anticorpo IgE fluorescente. Use o RBL-2H3.1 resultando expressar eqüinos linha celular FceRIa para a investigação 2, 3.
- Pré-ensaio de anticorpo de sensibilização:
- Colheita da RBL-2H3.1 expressando células eqüinos FceRIa de um confluente placa de Petri. Lavar em seguida, re-suspender as células em meio de cultura a uma densidade celular de 5x10 5 células ml -1.
- Adicionar a IgE de interesse para as células suspensas a uma concentração final de 1 ng mL-1, em seguida, a placa 100 ul de células numa placa de 96 poços em colunas 1-6 e incubar a 37 ° C + 5% de CO 2 + 90% humidade relativa durante 16 horas. Após o tempo de incubação, e antes de realizar o ensaio de libertação, verificar os poços sob um microscópio para o bem de confluência e aderência celular.
2) Lançamento de Ensaio:
- Lavar as células:
- Tampão de libertação Quente (PIPES 25 mM, cloreto de sódio 120 mM, cloreto de potássio 5 mM, cloreto de magnésio 0,04 mM e 1 mM de cloreto de cálcio) a 37 ° C para permitir uma lavagem das células suavemente.
- Lave as células sacudindo a placa para remover a mídia de células e adicionar 100 ml quente, 37 ° C, tampão de libertação. Repita duas vezes.
- Desafio Antígeno:
- Prepara-se uma diluição em série do antigénio (NIP-HSA ou DNP-HSA) de 0 ng ml -1, 0,1 ng ml -1, 1 ng ml-1, 10 ng mL-1, 100 ng ml -1, 1.000 ng ml -1, 10.000 ng ml-1 em tampão de liberação e quente a 37 ° C.
- Após a segunda lavagem das células, os meios de descarte e substituído por 100 ul das soluções de antigénio. Certifique-se de que os poços de uma mesma fila (A1-6 por exemplo) têm a mesma concentração de antigénio adicionados a eles.
- Configurar um controle negativo na linha A, adicionando 0 ng antígeno -1 ml. Adicionar o aumento da concentração de antigénio para baixo as linhas (BG), seguido de triton x-tampão (5% de Triton X-100) H em células de linha para lisar as células a serem utilizadas como um controlo positivo. Incubar a 37 ° C durante 20 minutos para permitir que as células de libertar os seus mediadores.
- Configurar controles bem individuais:
- Após a incubação, transferir 50 ul de sobrenadante de célula para a outra metade dos poços (placa de poços A1-6 A7-12, etc). Descartar as restantes 50 ul de sobrenadante e substituir com 50 ul de Triton-x tampão para permitir a medição da quantidade de mediadores libertados em cada cavidade nas colunas 7-12 como uma percentagem do total de mediadores no interior das células na coluna 1-6 .
- O substrato enzimático:
- Adicionar 50 ul de substrato β-hexosaminidase (50 mM de 4-nitrofenilo N-acetil-β-D-glucosaminida preparado em DMSO diluídos até 2 mM, adicionando-o ao tampão de citrato ácido cítrico 0,2 M e 0,2 M de acetato de sódio, pH 4,5) a todos os poços para facilitar a conversão do substrato a 4-nitrofenol pela enzima β-hexosaminidase. Incubar as placas a 37 ° C durante 2 horas.

- Encerrando a reação:
- Parar a reacção pela adição de 150 ul de tampão Tris (1 M Tris-HCl, pH 9) a cada poço como o elevado pH do tampão de pára a reacção e transforma o 4-nitrofenol em uma cor amarela.
- Lendo e analisando os resultados:
- Ler a placa utilizando uma placa espectrofotómetro a 405 nm para medir a absorvência da cor amarela. Calculado a percentagem de β-hexosaminidase libertada utilizando a seguinte fórmula:
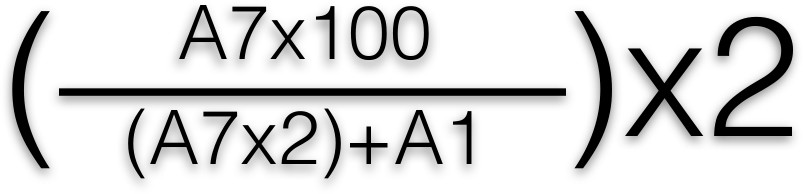
- Aplicar esta fórmula para cada poço, após o que é feita uma média para cada linha. A1 e A7 representam a localização dos poços da placa de 96 poços. Traçar uma curva de porcentagem de liberação β-hexosaminidase (o que corresponde a total liberação de mediador) açaíantígeno nst concentração 2, 3.
Resultados
As células RBL-2H3.1 parentais e as transfectadas com o gene do receptor de FceRIa equino foram sensibilizados primeiro com IgE de murganho anti DNP-HSA e desafiados com o antigénio DNP-HSA. Rato IgE se liga ao receptor endógeno de rato em ambas as linhas de células e, assim, actua como um controlo para testar a viabilidade de libertação de ambas as linhas celulares para libertar mediadores (Figura 1 A). Esta é uma verificação importante e deve ser levada a cabo rotineiramente desde cima prolon...
Discussão
Em resumo, os resultados desta investigação mostraram que, quando as células RBL-2H3.1 expressando FceRIa eqüinos são sensibilizados com IgE eqüinos e desafiado por um antígeno, eles dão um pico de liberação mediador de 36,68% ± 4,88% do montante total de mediador dentro do As células, em comparação com o RBL-2H3.1 células parentais não expressam eqüinos FceRIa.
Assim, este ensaio fornece uma ferramenta útil para investigar e estudar respostas alérgicas eqüinos in vit...
Divulgações
The authors declare that they have no competing financial interests in this paper.
Agradecimentos
The authors thank Dr. Lynda Partridge for the provision of advice and laboratory facilities.
Materiais
| Name | Company | Catalog Number | Comments |
| RBL-2H3.1 Expressing Equine FcεRIα | - | - | Produced in the lab |
| Equine IgE anti NIP-HSA | - | - | Produced in the lab |
| 96 Well Plate | Sigma | CLS3595 | - |
| Multi Channel Pipette | Anachem | - | - |
| Incubator | Galaxy R | - | - |
| 4Hydroxy-5-iodo-3-nitrophenylacetic acid | Cambridge Research Biochemicals | N-1070-1 | NIP-OH was conjugated with Human Serum Albumin to make NIP-HSA in the lab |
| Dinitrophenyl Conjugated to Human Serum Albumin | Sigma | A6661 | Abbreviated DNP-HSA |
| Plate Spectrophotometer | Anthos Labtec HT2 | - | - |
| Pipes | Sigma | P1851 | - |
| Sodium Chloride | Sigma | S7653 | - |
| Potassium Chloride | Sigma | P9333 | - |
| Magnesium Chloride | Sigma | M2670 | - |
| Calcium Chloride | Sigma | C1016 | - |
| Triton x100 | Sigma | X100 | - |
| 4-nitrophenyl N-acetyl-β-D-glucosaminide | Sigma | N9376 | Stock solution called β-hexosaminidase substrate was 50mM prepared in DMSO |
| Dimethyl Sulfoxide | Sigma | D2650 | - |
| Citric Acid | Sigma | 251275 | - |
| Sodium Acetate | Sigma | S7670 | - |
| Tris | Sigma | T5941 | - |
Referências
- Taudou, G., et al. Expression of the Alpha Chain of Human FcεRI in Transfected Rat Basophilic Leukemia Cells: Functional Activation after Sensitization with Human Mite-Specific IgE. Int Arch Allergy Immunol. 100 (4), 344-350 (1993).
- Sabban, S. . Development of an in Vitro Model System for Studying the Interaction of EquuscaballusIgE with Its High-Affinity FcεRI Receptor. , (2011).
- Sabban, S., Ye, H., Helm, B. A. Development of an in Vitro Model System for Studying the Interaction of EquuscaballusIgE with Its High-Affinity Receptor FcεRI. Vet ImmunolImmunopathol. 153 (1-2), 6-10 (2013).
- Wilson, A. P. M., Pullar, C. E., Camp, A. M., Helm, B. A. Human IgE mediates stimulus secretion coupling in rat basophilic leukemia cells transfected with the a chain of the human high-affinity receptor. Eur J Immunol. 23, 240-244 (1993).
- Hunter, M. J., Vratimos, A. P., Housden, J. E. M., Helm, B. A. Generation of canine-human Fc IgE chimeric antibodies for the determination of the canine IgE domain of interaction with FcεRIα. MolImmunol. 45 (8), 2262-2268 (2008).
- Rashid, A., et al. Review: Diagnostic and therapeutic applications of rat basophilic leukemia cells. MolImmunol. 52 (3-4), 224-228 (2012).
- Cohen, S. G. Asthma in antiquity: the Ebers Papyrus. Allergy Proc. 13 (3), 147-154 (1992).
- Dudler, T., et al. A link between catalytic activity, IgE-independent mast cell activation, and allergenicity of bee venom phospholipase A2. J. Immunol. 155, 2605-2613 (1995).
- Machado, D. C., Horton, D., Harrop, R., Peachell, P. T., Helm, B. A. Potential allergens stimulate the release of mediators of the allergic response from cells of mast cell lineage in the absence of sensitization with antigen-specific IgE. Eur J Immunol. 26 (12), 2972-2980 (1996).
- Smyth, L. J., et al. Assessment of the molecular basis of pro-allergenic effects of cigarette smoke. Environ Sci Technol. 34 (7), 1370-1374 (2000).
- Okada, H., Kuhn, C., Feillet, H., Bach, J. F. The 'hygiene hypothesis' for autoimmune and allergic diseases: an update. ClinExpImmunol. 160 (1), 1-9 (2010).
- Eder, C., et al. Influence of environmental and genetic factors on allergen-specific immunoglobulin-E levels in sera from Lipizzan horses. Equine Vet J. 33 (7), 714-720 (2001).
- Cook, W. R., Rossdale, P. D. The syndrome of 'Broken Wind' in the horse. Proceedings of the Royal Society of Medicine. 56, 972-977 (1963).
- Eyre, P., Lewis, A. J. Acute systemic anaphylaxis in the horse. Br. J. Pharmacol. 48 (3), 426-437 (1973).
- Wagner, B. IgE in horses: occurrence in health and disease. Vet ImmunolImmunopathol. 132 (1), 21-23 (2009).
- Hellberg, W., et al. Equine insect bite hypersensitivity: immunoblot analysis of IgE and IgG subclass responses to Culicoidesnubeculosus salivary gland extract. Vet. Immunol. Immunopathol. 113 (1-2), 99-112 (2006).
- Schaffartzik, A., et al. Equine insect bite hypersensitivity: what do we know. Vet ImmunolImmunopathol. 147 (3-4), 113-126 (2012).
- Künzle, F., et al. IgE-bearing cells in bronchoalveolar lavage fluid and allergen-specific IgE levels in sera from RAO-affected horses. J Vet Med A PhysiolPatholClin Med. 54 (1), 40-47 (2007).
- Tahon, L., et al. In vitro allergy tests compared to intradermal testing in horses with recurrent airway obstruction. Vet ImmunolImmunopathol. (1-2), 85-93 (2009).
- Wagner, B., Radbruch, A., Rohwer, J., Leibold, W. Monoclonal anti-equine IgE antibodies with specificity for different epitopes on the immunoglobulin heavy chain of native IgE. Vet ImmunolImmunopathol. 92 (1-2), 45-60 (2003).
- Wilson, A. D., Harwood, L., Torsteinsdottir, S., Marti, E. Production of monoclonal antibodies specific for native equine IgE and their application to monitor total serum IgE responses in Icelandic and non-Icelandic horses with insect bite dermal hypersensitivity. Vet ImmunolImmunopathol. 112 (3-4), 156-170 (2006).
- McAleese, S. M., et al. Cloning and expression of the extra-cellular part of the alpha chain of the equine high-affinity IgE receptor and its use in the detection of IgE. Vet ImmunolImmunopathol. 110 (1-2), 187-191 (2006).
- Ledin, A., et al. Generation of therapeutic antibody responses against IgE in dogs, an animal species with exceptionally high plasma IgE levels. Vaccine. 24 (1), 66-74 (2006).
- Siraganian, R. P., Hook, W. A. Histamine release and assay methods for the study of human allergy. Manual of Clinical Immunology. , (1980).
- Neuberger, M. S., et al. A hapten-specific chimaericIgE antibody with human physiological effector function. Nature. 314 (6008), 268-270 (1985).
- Bingham, B. R., Monk, P. N., Helm, B. A. Defective Protein Phosphorylation and Ca2+ Mobilization in a low secreting variant of the rat basophilic leukemia cell line. The Journal of Biological Chemistry. 269 (30), 19300-19306 (1994).
- McAleese, S. M., Halliwell, R. E., Miller, H. R. Cloning and sequencing of the horse and sheep high-affinity IgE receptor alpha chain cDNA. Immunogenetics. 1 (51), 878-881 (2000).
- Hongtu, Y. Study of the structure/function relationship in canine and human IgE as the basis for the development of rational therapeutic intervention strategies in allergic disease. , (2010).
- Sabban, S., et al. Towards a pan-anti-allergy vaccine. JIBTVA. 2 (2), 15-27 (2013).
- Moran, G., Burgos, R., Araya, O., Folch, H. In vitro bioassay to detect reaginic antibodies from the serum of horses affected with recurrent airway obstruction. Vet Res Commun. 34, 91-99 (2010).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados