Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Görünür-Işık Aydınlatması Altında Plazmonik Kataliz için Gümüş-Paladyum Alaşımlı Nanopartiküllerin Hazırlanması
Bu Makalede
Özet
Burada sunulan ZrO 2 (Ag-Pd/ZrO2)üzerinde desteklenen gümüş-paladyum (Ag-Pd) alaşımlı nanopartiküllerin(NPs) sentezi için bir protokoldür. Bu sistem, moleküler dönüşümleri hızlandırmak ve kontrol etmek için görünür ışık ışınlamadan enerji toplanmasına izin verir. Bu, Ag-Pd/ZrO2 NPs tarafından katalİze edilen ışık ışınlama altında nitrobenzen azaltma ile gösterilmiştir.
Özet
Plazmon nanopartiküllerde (NP) lokalize yüzey plazmon rezonansı (LSPR) çeşitli moleküler dönüşümlerin seçiciliğini hızlandırabilir ve kontrol edebilir. Bu, bu aralıklarda LSPR ekscitasyonunu destekleyen plazmonik nanopartiküller katalizör olarak kullanılırken reaksiyonları yönlendirmek ve kontrol etmek için sürdürülebilir bir girdi olarak görünür veya neredeyse IR ışığının kullanılması için olanaklar sunar. Ne yazık ki, paladyum (Pd) gibi birkaç katalitik metal için durum böyle değildir. Bu sınırlamayı aşmak için bir strateji plazmonik ve katalitik metaller içeren bimetalik NP'ler istihdam etmektir. Bu durumda, plazmonik metaldeki LSPR çıkarılması, katalitik bileşen tarafından yönlendirilen dönüşümleri hızlandırmaya ve kontrol etmeye katkıda bulunabilir. Burada bildirilen yöntem, plazmonik katalitik bir sistem görevi gören ZrO2'de (Ag-Pd/ZrO2)desteklenen bimetalik gümüş-paladyum (Ag-Pd) NP'lerin sentezine odaklanmaktadır. NP'ler, ZrO 2 desteğine karşılık gelen metal öncüllerinin birlikte emprenye edilmesi ve ardından doğrudan ZrO2 desteğinde bimetalik NP'lerin oluşumuna yol açan eşzamanlı azaltma ile hazırlanmıştır. Ag-Pd/ZrO2 NP'ler daha sonra LED lambalar tarafından 425 nm aydınlatmanın altındaki nitrobenzenin azaltılması için plazmonik katalizörler olarak kullanıldı. Gaz kromatografisi (GC) kullanılarak, plazmonik olmayan Pd'yi plazmonik metal Ag ile alaşımladıktan sonra LSPR uyarımı altında gelişmiş katalitik performans ve seçicilik kontrolünü gösteren, karanlık ve açık ışınlama koşulları altında azaltma reaksiyonunun dönüşümü ve seçiciliği izlenebilir. Bu teknik, çok çeşitli moleküler dönüşümlere ve NPs kompozisyonlarına uyarlanabilir, bu da farklı kataliz türlerinin plazmonik katalitik aktivitesinin dönüşüm ve seçicilik açısından karakterizasyonu için yararlı hale getirir.
Giriş
Metal nanopartiküllerin (NPs) çeşitli uygulamaları arasında, kataliz özel ilgiyi hak eder. Kataliz, sürdürülebilir bir gelecekte merkezi bir rol oynar, daha az enerji tüketimine, hammaddelerin daha iyi kullanılmasına katkıda bulunan ve daha temiz reaksiyon koşulları sağlayan1,2,3,4. Bu nedenle, katalizdeki ilerleme, kimyasal proseslerin atomik verimliliğini artırmak için araçlar sağlayabilir, bu da onları daha temiz, ekonomik olarak daha uygulanabilir ve daha çevre dostu hale getirebilir. Gümüş (Ag), altın (Au) veya bakırı (Cu) kapsayan metal NP'ler, bu sistemlerin yerelleştirilmiş yüzey plazmon rezonansı (LSPR) eksize etme 5 ,6,7,8aracılığıyla nano ölçekte ışıkla etkileşime girmelerinin benzersiz yolundan kaynaklanan görünür aralıkta ilginç optik özellikler görüntüleyebilir. Plazmonik NP'ler olarak adlandırılan bu NP'lerde LSPR, 5 ,6,7,8elektronlarının kolektif hareketiyle olay fotonları (gelen bir elektromanyetik dalgadan) arasındaki rezonans etkileşimini içerir. Bu fenomen, ortamın büyüklüğüne, şekline, bileşimine ve dielektrik sabitine bağlı karakteristik bir frekansta gerçekleşir9,10,11. Örneğin, Ag, Au ve Cu için, bu frekanslar görünürden yakın IR'ye kadar değişebilir ve LSPR 5 , 6 ,7,8,12,13'üheyecanlandırmak için güneş enerjisinin kullanımı için olanaklar açabilir.
Son zamanlarda, plazmonik NP'lerdeki LSPR ekscitasyonunun oranları hızlandırmaya ve moleküler dönüşümlerin seçiciliğini kontrol etmeye katkıda bulunabileceği gösterilmiştir5,14,15,16,17,18,19. Bu, kimyasal dönüşümleri hızlandırmak, sürmek ve / veya kontrol etmek için ışıktan enerji kullanmaya odaklanan plazmonik kataliz adı verilen bir alan doğurdu5,14,15,16,17,18,19. Bu bağlamda, plazmonik NP'lerdeki LSPR ekscitasyonunun, LSPR heyecanlı sıcak taşıyıcılar olarak adlandırılan enerjik sıcak elektronların ve deliklerin oluşumuna yol açabileceği tespit edilmiştir. Bu taşıyıcılar elektronik veya titreşimsel aktivasyon yoluyla adsorbe türlerle etkileşime girebilir15,16. Artan reaksiyon oranlarına ek olarak, bu işlem ayrıca geleneksel termokimyasal tahrikli süreçler aracılığıyla erişilemeyen alternatif reaksiyon yolları sağlayabilir ve reaksiyon seçiciliği üzerinde kontrol için yeni yollar açabilir20,21,22,23,24,25. Daha da önemlisi, plazmon çürümesinin termal dağmaya da yol açabileceğini ve NP'lerin çevresinde sıcaklık artışına yol açabileceğini ve reaksiyon oranlarını hızlandırmaya da katkıda bulunabileceğini belirtmek gerekir15,16.
Bu ilginç özellikler nedeniyle, plazmonik kataliz çeşitli moleküler dönüşümlere doğru başarıyla18. Bununla birlikte, önemli bir zorluk devam ediyor. Ag ve Au gibi plazmonik NP'ler görünür ve IR'ye yakın aralıklarda mükemmel optik özellikler gösterirken, katalitik özellikleri dönüşümlerin kapsamı açısından sınırlıdır. Başka bir deyişle, birkaç dönüşüm için iyi katalitik özellikler göstermezler. Ayrıca, paladyum (Pd) ve platin (Pt) gibi katalizörde önemli olan metaller, görünür veya IR'ye yakın aralıklarda LSPR ekscitasyonunu desteklemez. Bu boşluğu kapatmak için, plazmonik ve katalitik metal içeren bimetalik NP'ler etkili bir stratejiyi temsil eder20,26,27,28,29. Bu sistemlerde, plazmonik metal, daha sonra katalitik metaldeki moleküler dönüşümleri sürmek, hızlandırmak ve kontrol etmek için kullanılan LSPR aracılığıyla ışık ekscitasyonundan enerji toplamak için bir anten olarak kullanılabilir. Bu nedenle, bu strateji plazmonik katalizini geleneksel plazmonik metalNPs 20 , 26,27,28,29'un ötesine uzatmamızı sağlar.
Bu protokol, plazyonik kataliz için plazmonik katalitik bir sistem görevi görebilen ZrO2'de (Ag-Pd/ZrO2)desteklenen bimetalik gümüş-paladyum (Ag-Pd) alaşımlı NP'lerin fasile sentezini açıklar. Ag-Pd/ZrO2 NP'ler, ZrO2 desteğindeki ilgili metal öncüllerinin eşzamanlı olarak emprenye edilmesi ve ardından eşzamanlı azaltma30ile hazırlanmıştır. Bu yaklaşım, ZrO 2 desteğinin yüzeyinde yaklaşık 10 nm büyüklüğünde (çap) bimetalikNP'lerin oluşmasına yol açtı. NP'ler, ortaya çıkan Ag-Pd NP'lerin optik özelliklerini en üst düzeye çıkarırken katalitik metalin kullanımını en aza indirmek için Pd'nin% 1'inden oluşuyordu. Nitrobenzenin azaltılması için plazmonik katalizde Ag-Pd/ZrO2 NPs uygulamasına ilişkin bir protokol gösterilmiştir. LSPR excitation için 425 nm LED aydınlatma istihdam ettik. Karanlık ve açık ışınlama koşullarında azalma reaksiyonunun dönüşümünü ve seçiciliğini izlemek için gaz kromatografisi yapıldı. LSPR ekscitasyonu, Ag-Pd/ZrO2 NP'lerde tamamen termal tahrikli koşullara göre katalitik performansın artmasına ve seçicilik üzerinde kontrole yol açtı. Bu protokolde açıklanan yöntem, gaz kromatografisi ile birleştirilmiş basit bir fotokatalitik reaksiyon kurulumuna dayanmaktadır ve çok çeşitli moleküler dönüşümlere ve NP kompozisyonlarına uyarlanabilir. Bu nedenle, bu yöntem fotokatalitik aktivitenin, dönüşüm ve reaksiyon seçiciliği açısından, farklı NP'lerin ve sayısız sıvı fazlı dönüşüm için karakterizeini mümkün kılar. Bu makalenin hem yeni gelenlere hem de alanında daha deneyimli bilim insanlarına önemli yönergeler ve içgörüler sağlayacağına inanıyoruz.
Access restricted. Please log in or start a trial to view this content.
Protokol
1. Ag-Pd/ZrO2 NPs Sentezi
NOT: Bu prosedürde, Ag-Pd'deki Pd mol% 1'e ve ZrO2'deki Ag-Pd yüklemesi 3 wt.% 'ye karşılık geldi.
- 250 mL'lik bir kabın içine1 g ZrO 2 tozu yerleştirin.
- Oda sıcaklığında güçlü manyetik karıştırma (500 rpm) altında behere 50 mL AgNO3 (aq)(0,0059mol/L) ve 9,71 mL K 2 PdCl4 (aq) (0,00031 mol/L) çözeltisi ekleyin.
- 10 mL lizin (0,53 M) sulu çözelti ekleyin.
- Karışımı 20 dakika boyunca kuvvetli karıştırma (500 rpm) altında tutun.
- 20 dakika sonra, süspansiyona yeni hazırlanmış bir NaBH 4 (aq)(0.035 M) çözeltisinin 10 mL'lik süspansiyonu damla yönünde, 1 mL / dak hızında eklemek için bir pipet kullanın. Süspansiyonu işlem boyunca karıştırma (500 rpm) altında tutun.
- Karışımı oda sıcaklığında 30 dakika karıştırın.
2. Katalizörün ayrılması ve saflaştırılması
- Süspansiyonu santrifüj tüplerine aktarın ve katıları 10 dakika boyunca 3.260 x g'da santrifüjleme ile karışımdan ayırın.
- Sıvı fazı bir pipetle dikkatlice çıkarın ve tüplere 15 mL deiyonize su ekleyin.
- Katının dağılımı elde edilene kadar kuvvetlice çalkalayın. İyi dağılım sağlanamazsa, tüpleri 5 dakika boyunca ultrasonik bir banyoya yerleştirin.
- Dispersiyon 10 dakika boyunca 3.260 x g'da santrifüj.
- Yıkama adımlarını (2.2. ila 2.2.2.) iki kez daha iyonize su kullanarak, ardından su yerine etanol kullanarak tekrarlayın.
- Etanolleri çıkarın ve katıyı 60 °C'de bir fırında 12 saat kurutun.
- Hazırlanan Ag-Pd/ZrO2 NP'leri çeşitli mikroskopi, elementel ve spektroskopik tekniklerle karakterize edin.
3. Ag/ZrO2 NPs Sentezi
NOT: Bu prosedürde, ZrO2'ye Ag yüklemesi 3 wt.% 'ye karşılık gelir.
- 250 mL'lik bir kabın içine1 g ZrO 2 tozu yerleştirin.
- Oda sıcaklığında kuvvetli manyetik karıştırma (500 rpm) altında behere 50 mL AgNO3 (aq) (0.0059 mol/L) çözeltisi ekleyin.
- 10 mL lizin (0,53 M) sulu çözelti ekleyin.
- Karışımı 20 dakika boyunca kuvvetli karıştırma (500 rpm) altında tutun.
- 20 dakika sonra, süspansiyona yeni hazırlanmış bir NaBH 4 (aq)(0.035 M) çözeltisinin 10 mL'lik süspansiyonu damla yönünde, 1 mL / dak hızında eklemek için bir pipet kullanın. Süspansiyonu işlem boyunca karıştırma (500 rpm) altında tutun.
- Karışımı oda sıcaklığında 30 dakika karıştırın.
4. Katalizörün ayrılması ve saflaştırılması
- Süspansiyonu santrifüj tüplerine aktarın ve katıları 10 dakika boyunca 3.260 x g'da santrifüjleme ile karışımdan ayırın.
- Sıvı fazı bir pipetle dikkatlice çıkarın ve tüplere 15 mL deiyonize su ekleyin.
- Katının dağılımı gözlenene kadar kuvvetlice çalkalayın. İyi dağılım sağlanamazsa, tüpleri 5 dakika boyunca ultrasonik bir banyoya yerleştirin.
- Dispersiyon 10 dakika boyunca 3.260 x g'da santrifüj.
- Yıkama adımlarını (4.2. ila 4.2.2.) iki kez daha iyonize su kullanarak, ardından su yerine etanol kullanarak tekrarlayın.
- Etanolleri çıkarın ve katıyı 60 °C'de bir fırında 12 saat kurutun.
- Hazırlanan Ag/ZrO2 NP'ler daha sonra çeşitli mikroskopi, elementel ve spektroskopik tekniklerle karakterize edilebilir.
5. LSPR uyarımı (ışık aydınlatması) altında nitrobenzen azaltma yönünde plazmonik katalitik performansın araştırılması
- Manyetik karıştırma çubuğu ile birlikte 25 mL yuvarlak tabanlı bir şişeye 30 mg katalizör yerleştirin.
- Reaktöre izopropil alkolde (IPA) 5 mL nitrobenzen çözeltisi (0,03 mol/L) ekleyin.
- Ardından, 11.22 mg KOH tozu (0.0002 mol) ekleyin.
- Süspansiyonu 1 dakika boyunca argon akışı ile köpürterek reaktörü arındırın. Temizledikten hemen sonra şişeyi kapatın.
- Reaktörü sıcaklık kontrollü manyetik karıştırıcının (500 rpm) üzerinde 70 °C'de ısıtılmış bir yağ banyosuna yerleştirin.
- Işık kaynağı olarak dalga boyu 425 nm olan 4 LED lamba ve 0,5 W/cm2ışık yoğunluğu ile tüpü ışınlayın. Lambalardan reaksiyon şişesine olan mesafe 7 cm olmalıdır.
- Reaksiyonun kuvvetli manyetik karıştırma (500 rpm) altında 70 °C'de 2,5 saat devam etmesine izin verin.
- Ardından, ışığı kapatın, reaktörü açın ve 1 mL'lik bir örnek toplamak için bir şırınga ve bir iğne kullanın. Katalizör partiküllerini çıkarmak için 0,45 μm filtreden geçirerek bir gaz kromatografi şişesine filtreleyin.
6. LSPR ekscitasyonunun yokluğunda reaksiyon (karanlık koşullar)
- 5'te açıklanan adımları izleyin, ancak ışık ışınlama olmadan. Işığa maruz kalmayı önlemek için reaksiyon tüpünü alüminyum folyo ile sarın.
7. Gaz kromatografisi (GC) analiz hazırlığı
- Yaklaşık 30 mmol/L nitrobenzen (NB), 30 mmol/L anilin (AN) ve 30 mmol/L azobenzen (AB) içeren bir IPA çözeltisi hazırlayın.
- Uygun bir yöntem kullanarak çözümün GC analizini çalıştırın. Kolon sıcaklığı ve gaz akış programları değiştirilerek farklı yöntemler test edilebilir. Seçilen yöntem, IPA, NB, AN ve AB'ye karşılık gelen tepeleri minimum saklama süresi içinde ayırabilmelidir.
- Yöntem seçildikten sonra, IPA'da 50 mM, 25 mM, 10 mM, 5 mM ve 2,5 mM NB'lik bir çözüm seti ve aynı konsantrasyonlarda IPA'da başka bir AN ve AB çözümleri seti hazırlayın.
- Hazırlanan çözümlerin GC analizini çalıştırın. Her kromatogram 2 tepe noktası sunmalıdır: daha yüksek olan IPA'ya ve daha düşük olanı NB, AN veya AB'ye karşılık gelir. Her kromatogram için, tüm tepelerin tutma süresini ve tepe alanını not edin.
- Her numunenin yoğun alanına karşı konsantrasyonu çizerek NB, AN ve AB kalibrasyon eğrilerini takip edin.
8. GC analizi
- 5. adımlarda toplanan örnekler üzerinde bir GC analizi çalıştırın. ve 6. 7.2 adımları için kullanılan yöntemle. ve 7.4.
- Her kromatogram için saklama süresini ve tepe alanını not edin ve numunelerdeki NB, AN ve AB konsantrasyonunu belirlemek için daha önce çizilen kalibrasyon eğrilerini kullanın.
- Denklemleri kullanarak nitrobenzen dönüşümünün yanı sıra anilin ve azobenzen seçiciliğini hesaplayın:
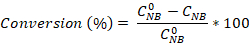
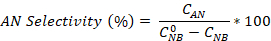
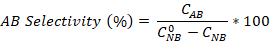
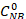 GC analizinin 2,5 saatlik reaksiyonu sonrasında ilk NBkonsantrasyonu (0,03 mol/L) ve C NB , C AN , C AB sırasıyla NB, AN ve AB konsantrasyonlarına karşılık gelir.
GC analizinin 2,5 saatlik reaksiyonu sonrasında ilk NBkonsantrasyonu (0,03 mol/L) ve C NB , C AN , C AB sırasıyla NB, AN ve AB konsantrasyonlarına karşılık gelir.
Access restricted. Please log in or start a trial to view this content.
Sonuçlar
Şekil 1A, saf ZrO 2 oksit (solda) ve Ag-Pd/ZrO 2 NPs (sağda) içeren katı örneklerin dijital fotoğraflarını göstermektedir. Beyazdan (ZrO2'de)kahverengiye (Ag-Pd/ZrO2)olan bu renk değişimi, Ag-Pd NP'lerin ZrO2 yüzeyindeki birikmesine ilişkin ilk nitel kanıtları sağlar. Şekil 1B, Ag-Pd/ZrO 2 NP'lerin (mavi iz) yanı sıra ZrO2 (siyah iz) ve Ag/ZrO2 NP'lerden (kırmızı i...
Access restricted. Please log in or start a trial to view this content.
Tartışmalar
Bu yöntemde açıklanan bulgular, Pd'nin (veya diğer katalitik ancak plazmonik metalin değil) içsel katalitik aktivitesinin, bimetalik alaşımlıNPs 35'tegörünür ışık ışınlama yoluyla LSPR ekscitasyonu ile önemli ölçüde artırılabileceğini göstermektedir. Bu durumda, Ag (veya başka bir plazmonik metal), LSPR ekscitasyonu yoluyla görünür ışık ışınlamasından enerji toplama yeteneğine sahiptir. LSPR eksitasyonu, sıcak yük taşıyıcılarının (sıcak elektronlar ve...
Access restricted. Please log in or start a trial to view this content.
Açıklamalar
Yazarların açıklayacak bir şeyi yok.
Teşekkürler
Bu çalışma Helsinki Üniversitesi ve Jane ve Aatos Erkko Vakfı tarafından desteklendi. S.H. burs için Erasmus+ AB fonlarına teşekkür ediyor.
Access restricted. Please log in or start a trial to view this content.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 2-Propanol (anhydrous, 99.5%) | Sigma-Aldrich | 278475 | CAS Number 67-63-0 |
| Aniline (for synthesis) | Sigma-Aldrich | 8.22256 | CAS Number 62-53-3 |
| Azobenzene (98%) | Sigma-Aldrich | 424633 | CAS Number 103-33-3 |
| Ethanol | Honeywell | 32221 | CAS Number 64-17-5 |
| Hydrochloric acid (37%) | VWR | PRLSMC310066 | CAS Number 7647-01-0 |
| L-Lysine (crystallized, ≥98.0% (NT)) | Sigma-Aldrich | 62840 | CAS Number 56-87-1 |
| Nitric acid (65%) | Merck | 100456 | CAS Number 7697-37-2 |
| Nitrobenzene | Sigma-Aldrich | 8.06770 | CAS Number 98-95-3 |
| Potassium hydroxide | Fisher | 10448990 | CAS Number 1310-58-3 |
| Potassium tetrachloropalladate (II) (98%) | Sigma-Aldrich | 205796 | CAS Number 10025-98-6 |
| Silver nitrate (ACS reagent, ≥99.0%) | Sigma-Aldrich | 209139 | CAS Number 7761-88-8 |
| Sodium borohydride (fine granular for synthesis) | Sigma-Aldrich | 8.06373 | CAS Number 16940-66-2 |
| Zirconium (IV) oxide (nanopowder, <100 nm particle size (TEM)) | Sigma-Aldrich | 544760 | CAS Number 1314-23-4 |
Referanslar
- Dunn, P. J., Hii, K. K., Krische, M. J., Williams, M. T. Sustainable Catalysis: Challenges and Pratices for the Pharmaceutical and Fine Chemical Industries. , Wiley-Blackwell. (2013).
- Tzouras, N. V., Stamatopoulos, I. K., Papastavrou, A. T., Liori, A. A., Vougioukalakis, G. C. Sustainable metal catalysis in C-H activation. Coordination Chemistry Reviews. 343, 25(2017).
- Polshettiwar, V., Varma, R. S. Green chemistry by nano-catalysis. Green Chemistry. 12 (5), 743(2010).
- Rodrigues, T. S., da Silva, A. G. M., Camargo, P. H. C. Nanocatalysis by noble metal nanoparticles: controlled synthesis for the optimization and understanding of activities. Journal of Materials Chemistry A. 7 (11), 5857-5874 (2019).
- Linic, S., Christopher, P., Ingram, D. B. Plasmonic-metal nanostructures for efficient conversion of solar to chemical energy. Nature Materials. 10 (12), 911-921 (2011).
- Nam, J. M., Liz-Marzán, L., Halas, N. Chemical Nanoplasmonics: Emerging Interdisciplinary Research Field at Crossroads between Nanoscale Chemistry and Plasmonics. Accounts of Chemical Research. 52 (11), 2995-2996 (2019).
- Brongersma, M. L., Halas, N. J., Nordlander, P. Plasmon-induced hot carrier science and technology. Nature Nanotechnology. 10 (1), 25-34 (2015).
- Smith, J. G., Faucheaux, J. A., Jain, P. K. Plasmon resonances for solar energy harvesting: A mechanistic outlook. Nano Today. 10 (1), 67-80 (2015).
- Hartland, G. V. Optical studies of dynamics in noble metal nanostructures. Chemical Reviews. 111 (6), 3858-3887 (2011).
- Kelly, K. L., Coronado, E., Zhao, L. L., Schatz, G. C. The optical properties of metal nanoparticles: The influence of size, shape, and dielectric environment. Journal of Physical Chemistry B. 107 (3), 668-677 (2003).
- Hermoso, W., et al. Triangular metal nanoprisms of Ag, Au, and Cu: Modeling the influence of size, composition, and excitation wavelength on the optical properties. Chemical Physics. 423, 142-150 (2013).
- Kumar, A., et al. Rational Design and Development of Lanthanide-Doped NaYF4@CdS-Au-RGO as Quaternary Plasmonic Photocatalysts for Harnessing Visible-Near-Infrared Broadband Spectrum. ACS Applied Materials and Interfaces. 10 (18), 15565-15581 (2018).
- Reddy, K. L., Kumar, S., Kumar, A., Krishnan, V. Wide spectrum photocatalytic activity in lanthanide-doped upconversion nanophosphors coated with porous TiO2 and Ag-Cu bimetallic nanoparticles. Journal of Hazardous Materials. 367, 694-705 (2019).
- Ingram, D. B., Linic, S. Water splitting on composite plasmonic-metal/semiconductor photoelectrodes: Evidence for selective plasmon-induced formation of charge carriers near the semiconductor surface. Journal of the American Chemical Society. 133 (14), 5202-5205 (2011).
- Linic, S., Aslam, U., Boerigter, C., Morabito, M. Photochemical transformations on plasmonic metal nanoparticles. Nature Materials. 14 (6), 567-576 (2015).
- Aslam, U., Rao, V. G., Chavez, S., Linic, S. Catalytic conversion of solar to chemical energy on plasmonic metal nanostructures. Nature Catalyst. 1, 656-665 (2018).
- Araujo, T. P., Quiroz, J., Barbosa, E. C. M., Camargo, P. H. C. Understanding plasmonic catalysis with controlled nanomaterials based on catalytic and plasmonic metals. Current Opinion in Colloid and Interface Science. 39, 110-122 (2019).
- Gellé, A., et al. Applications of plasmon-enhanced nanocatalysis to organic transformations. Chemical Reviews. , 986-1041 (2020).
- Shaik, F., Peer, I., Jain, P. K., Amirav, L. Plasmon-Enhanced Multicarrier Photocatalysis. Nano Letters. 18 (7), 4370-4376 (2018).
- Quiroz, J., et al. Controlling Reaction Selectivity over Hybrid Plasmonic Nanocatalysts. Nano Letters. 18, 7289-7297 (2018).
- Peiris, E., et al. Plasmonic Switching of the Reaction Pathway: Visible-Light Irradiation Varies the Reactant Concentration at the Solid-Solution Interface of a Gold-Cobalt Catalyst. Angewandte Chemie - International Edition. 58 (35), 12032-12036 (2019).
- Yu, S., Wilson, A. J., Heo, J., Jain, P. K. Plasmonic Control of Multi-Electron Transfer and C-C Coupling in Visible-Light-Driven CO2 Reduction on Au Nanoparticles. Nano Letters. 18 (4), 2189-2194 (2018).
- Yu, S., Jain, P. K. Plasmonic photosynthesis of C 1 -C 3 hydrocarbons from carbon dioxide assisted by an ionic liquid. Nature Communications. 10, 2022(2019).
- Zhang, X., et al. Product selectivity in plasmonic photocatalysis for carbon dioxide hydrogenation. Nature Communications. 8, 1-9 (2017).
- Cortés, E. Efficiency and Bond Selectivity in Plasmon-Induced Photochemistry. Advanced Optical Materials. 5 (15), 1700191(2017).
- de Freitas, I. C., et al. Design-controlled synthesis of IrO 2 sub-monolayers on Au nanoflowers: marrying plasmonic and electrocatalytic properties. Nanoscale. , 23-27 (2020).
- Zhang, C., et al. Al-Pd Nanodisk Heterodimers as Antenna-Reactor Photocatalysts. Nano Letters. 16 (10), 6677-6682 (2016).
- Zhou, L., et al. Light-driven methane dry reforming with single atomic site antenna-reactor plasmonic photocatalysts. Nature Energy. 5, 61-70 (2020).
- Swearer, D. F., et al. Heterometallic antenna-reactor complexes for photocatalysis. Proceedings of the National Academy of Sciences. 113 (32), 8916-8920 (2016).
- Peiris, S., Sarina, S., Han, C., Xiao, Q., Zhu, H. -Y. Silver and palladium alloy nanoparticle catalysts: reductive coupling of nitrobenzene through light irradiation. Dalton Transactions. 46 (32), 10665-10672 (2017).
- Rahm, J. M., et al. A Library of Late Transition Metal Alloy Dielectric Functions for Nanophotonic Applications. Advanced Functional Materials. 2002122, 02122(2020).
- Zhang, C., Chen, B. Q., Li, Z. Y., Xia, Y., Chen, Y. G. Surface Plasmon Resonance in Bimetallic Core-Shell Nanoparticles. Journal of Physical Chemistry C. 119 (29), 16836-16845 (2015).
- Liu, Z., Huang, Y., Xiao, Q., Zhu, H. Selective reduction of nitroaromatics to azoxy compounds on supported Ag-Cu alloy nanoparticles through visible light irradiation. Green Chemistry. 18 (3), 817-825 (2016).
- Chaiseeda, K., Nishimura, S., Ebitani, K. Gold nanoparticles supported on alumina as a catalyst for surface plasmon-enhanced selective reductions of nitrobenzene. ACS Omega. 2 (10), 7066-7070 (2017).
- Peiris, S., et al. Metal nanoparticle photocatalysts: emerging processes for green organic synthesis. Catalysis Science and Technology. 6 (2), 320-338 (2016).
- García-García, I., et al. Silver-Based Plasmonic Catalysts for Carbon Dioxide Reduction. ACS Sustainable Chemistry and Engineering. 8 (4), 1879-1887 (2020).
- Agrawal, A., Johns, R. W., Milliron, D. J. Control of Localized Surface Plasmon Resonances in Metal Oxide Nanocrystals. Annual Review of Materials Research. 47 (1), 1-31 (2017).
- Lounis, S. D., Runnerstrom, E. L., Llordés, A., Milliron, D. J. Defect chemistry and Plasmon physics of colloidal metal oxide Nanocrystals. Journal of Physical Chemistry Letters. 5 (9), 1564-1574 (2014).
- Rej, S., et al. Determining Plasmonic Hot Electrons and Photothermal Effects during H2 Evolution with TiN-Pt Nanohybrids. ACS Catalysis. 10 (9), 5261-5271 (2020).
- Barragan, A. A., et al. Photochemistry of Plasmonic Titanium Nitride Nanocrystals. The Journal of Physical Chemistry C. 123 (35), 21796-21804 (2019).
Access restricted. Please log in or start a trial to view this content.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır