È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Preparazione di nanoparticelle in lega di palladio d'argento per la catalisi plasmonica sotto illuminazione a luce visibile
In questo articolo
Riepilogo
Presentato qui un protocollo per la sintesi delle nanoparticelle in lega argento-palladio (Ag-Pd) (NPs) supportate su ZrO2 (Ag-Pd/ZrO2). Questo sistema consente di raccogliere energia dall'irradiazione della luce visibile per accelerare e controllare le trasformazioni molecolari. Lo dimostra la riduzione del nitrobenzene sotto irradiazione leggera catalizzata dai PNP Ag-Pd/ZrO2.
Abstract
La risonanza localizzata del plasmone superficiale (LSPR) nelle nanoparticelle plasmoniche (NP) può accelerare e controllare la selettività di una varietà di trasformazioni molecolari. Ciò apre possibilità per l'uso della luce visibile o quasi IR come input sostenibile per guidare e controllare le reazioni quando le nanoparticelle plasmoniche che supportano l'eccitazione LSPR in queste gamme sono utilizzate come catalizzatori. Purtroppo non è così per diversi metalli catalitici come il palladio (Pd). Una strategia per superare questa limitazione è quella di impiegare NP bimetallici contenenti metalli plasmonici e catalitici. In questo caso, l'eccitazione LSPR nel metallo plasmonico può contribuire ad accelerare e controllare le trasformazioni guidate dalla componente catalitica. Il metodo riportato nel presente documento si concentra sulla sintesi dei NP bimetallici argento-palladio (Ag-Pd) supportati su ZrO2 (Ag-Pd/ZrO2)che agisce come sistema plasmonico-catalitico. I PNP sono stati preparati mediante coimpregnazione dei corrispondenti precursori metallici sul supporto ZrO2, seguita da una riduzione simultanea che ha portato alla formazione di NP bimetallici direttamente sul supporto ZrO2. Gli NP Ag-Pd/ZrO2 sono stati quindi utilizzati come catalizzatori plasmonici per la riduzione dell'illuminazione nitrobenzene inferiore a 425 nm da lampade a LED. Utilizzando la gascromatografia (GC), è possibile monitorare la conversione e la selettività della reazione di riduzione nelle condizioni di irradiazione oscura e luminosa, dimostrando le migliori prestazioni catalitiche e il controllo sulla selettività sotto eccitazione LSPR dopo aver legato pd non plasmonico con metallo plasmonico Ag. Questa tecnica può essere adattata ad una vasta gamma di trasformazioni molecolari e composizioni di NPs, rendendola utile per la caratterizzazione dell'attività catalitica plasmonica di diversi tipi di catalisi in termini di conversione e selettività.
Introduzione
Tra le diverse applicazioni delle nanoparticelle metalliche (NP), la catalisi merita un'attenzione particolare. La catalisi svolge un ruolo centrale in un futuro sostenibile, contribuendo a ridurre il consumo energetico, a utilizzare meglio le materie prime e a consentire condizioni di reazione piùpulite 1,2,3,4. Pertanto, i progressi nella catalisi possono fornire strumenti per migliorare l'efficienza atomica dei processi chimici, rendendoli più puliti, economicamente sostenibili e più rispettosi dell'ambiente. I NP metallici che comprendono argento (Ag), oro (Au) o rame (Cu) possono visualizzare interessanti proprietà ottiche nella gamma visibile che derivano dal modo unico in cui questi sistemi interagiscono con la luce su scala nanometrica attraverso l'eccitazione localizzata della risonanza plasmonica superficiale (LSPR)5,6,7,8. In questi NP, indicati come NP plasmonici, l'LSPR comprende l'interazione risonante tra i fotoni incidenti (da un'onda elettromagnetica in arrivo) con il moto collettivodegli elettroni 5,6,7,8. Questo fenomeno si svolge ad una frequenza caratteristica che dipende dalle dimensioni, dalla forma, dalla composizione e dalla costante dielettricadell'ambiente 9,10,11. Ad esempio, per Ag, Au e Cu, queste frequenze possono variare dal visibile al vicino-IR, aprendo possibilità per l'utilizzo dell'energia solare per eccitare il loro LSPR5,6,7,8,12,13.
Recentemente, è stato dimostrato che l'eccitazione LSPR nei PN plasmonici può contribuire ad accelerare i tassi e controllare la selettività delle trasformazionimolecolari 5,14,15,16,17,18,19. Questo ha dato vita a un campo chiamato catalisi plasmonica, che si concentra sull'uso dell'energia dalla luce per accelerare, guidare e / o controllare le trasformazionichimiche 5,14,15,16,17,18,19. In questo contesto, è stato stabilito che l'eccitazione LSPR nei PN plasmonici può portare alla formazione di elettroni e buchi caldi energetici, indicati come portatori caldi eccitati dall'LSPR. Questi portatori possono interagire con specie adsorbiti attraverso l'attivazione elettronica ovibrazionale 15,16. Oltre all'aumento delle velocità di reazione, questo processo può anche fornire percorsi di reazione alternativi non accessibili tramite i tradizionali processi termochimici, aprendo nuove strade per il controllo della selettivitàdella reazione 20,21,22,23,24,25. È importante notare che il decadimento del plasmone può anche portare a dissipazione termica, portando a un aumento della temperatura nelle vicinanze dei PN che può anche contribuire ad accelerare i tassi direazione 15,16.
A causa di queste caratteristiche interessanti, la catalisi plasmonica è stata impiegata con successo per una varietà di trasformazionimolecolari 18. Tuttavia, rimane una sfida importante. Mentre i PNP plasmonici come Ag e Au mostrano eccellenti proprietà ottiche negli intervalli visibile e vicino all'IR, le loro proprietà catalitiche sono limitate in termini di portata delle trasformazioni. In altre parole, non mostrano buone proprietà catalitiche per molte trasformazioni. Inoltre, i metalli importanti nella catalisi, come il palladio (Pd) e il platino (Pt), non supportano l'eccitazione LSPR negli intervalli visibili o quasi IR. Per colmare questo divario, i PNP bimetallici contenenti un metallo plasmonico e catalitico rappresentano una strategiaefficace 20,26,27,28,29. In questi sistemi, il metallo plasmonico può essere utilizzato come antenna per raccogliere energia dall'eccitazione della luce attraverso l'LSPR, che viene quindi utilizzato per guidare, accelerare e controllare le trasformazioni molecolari al metallo catalitico. Pertanto, questa strategia ci consente di estendere la catalisi plasmonica oltre i tradizionali NP metallici plasmonici20,26,27,28,29.
Questo protocollo descrive la facile sintesi dei NP in lega bimetallico argento-palladio (Ag-Pd) supportati su ZrO2 (Ag-Pd/ZrO2)che possono agire come sistema plasmonico-catalitico per la catalisi plasmonica. I PNP Ag-Pd/ZrO2 sono stati preparati con la coimpregnazione dei corrispondenti precursori metallici sul supporto ZrO2 seguito da una riduzione simultanea30. Questo approccio ha portato alla formazione di NP bimetallici di circa 10 nm di dimensioni (diametro) direttamente sulla superficie del supporto ZrO2. I PNP erano composti dall'1% di Pd per minimizzare l'utilizzo del metallo catalitico massimizzando al contempo le proprietà ottiche dei nsp Ag-Pd risultanti. È stato dimostrato un protocollo per l'applicazione dei PNP Ag-Pd/ZrO2 nella catalisi plasmonica per la riduzione del nitrobenzene. Abbiamo utilizzato l'illuminazione LED a 425 nm per l'eccitazione LSPR. La gascromatografia è stata eseguita per monitorare la conversione e la selettività della reazione di riduzione nelle condizioni di irradiazione oscura e luminosa. L'eccitazione LSPR ha portato a maggiori prestazioni catalitiche e al controllo della selettività nei PN Ag-Pd/ZrO2 rispetto alle condizioni puramente guidate termicamente. Il metodo descritto in questo protocollo si basa su una semplice configurazione di reazione fotocatalitica accoppiata con gascromatografia e può essere adattato a una vasta gamma di trasformazioni molecolari e composizioni di NPs. Pertanto, questo metodo rende possibile la caratterizzazione dell'attività fotocatalitica, in termini di selettività di conversione e reazione, di diversi NP e per una miriade di trasformazioni in fase liquida. Crediamo che questo articolo fornirà importanti linee guida e approfondimenti sia ai nuovi arrivati che agli scienziati più esperti sul campo.
Access restricted. Please log in or start a trial to view this content.
Protocollo
1. Sintesi di Ag-Pd/ZrO2 NPs
NOTA: In questa procedura, il mol% del Pd in Ag-Pd corrispondeva all'1%, e il carico Ag-Pd su ZrO2 corrispondeva al 3%.
- Mettere 1 g di polvere ZrO2 in un bicchiere da 250 mL.
- Aggiungere 50 mL di un AgNO3 (aq) (0,0059 mol/L) e 9,71 mL di un K2PdCl4 (aq) (0,00031 mol/L) al becher sotto agitazione magnetica vigorosa (500 giri/min) a temperatura ambiente.
- Aggiungere 10 mL di soluzione acquosa di lysine (0,53 M).
- Mantenere la miscela sotto agitazione vigorosa (500 giri/min) per 20 minuti.
- Dopo 20 minuti, utilizzare una pipetta per aggiungere alla sospensione 10 mL di una soluzione NaBH4 (aq) (0,035 M) preparata al momento, ad una velocità di 1 mL/min. Mantenere la sospensione sotto agitazione (500 giri/min) durante tutto il processo.
- Lasciare mescolare la miscela per 30 minuti a temperatura ambiente.
2. Separazione e purificazione del catalizzatore
- Trasferire la sospensione in tubi di centrifugazione e separare i solidi dalla miscela mediante centrifugazione a 3.260 x g per 10 min.
- Rimuovere con cura la fase liquida con una pipetta e aggiungere acqua deionizzata da 15 ml ai tubi.
- Agitare vigorosamente fino a ottenere la dispersione del solido. Se non si ottiene una buona dispersione, posizionare i tubi in un bagno ad ultrasuoni per 5 minuti.
- Centrifugare la dispersione a 3.260 x g per 10 min.
- Ripetere i passaggi di lavaggio (da 2.2. a 2.2.2.) altre due volte utilizzando acqua deionizzata, quindi una volta usando l'etanolo al posto dell'acqua.
- Rimuovere l'etanolo e asciugare il solido in forno a 60 °C per 12 ore.
- Caratterizzare i PN Ag-Pd/ZrO2 preparati con una varietà di tecniche microscopie, elementali e spettroscopiche.
3. Sintesi di Ag/ZrO2 NPs
NOTA: In questa procedura, il carico Ag su ZrO2 corrispondeva al 3 wt.%.
- Mettere 1 g di polvere ZrO2 in un bicchiere da 250 mL.
- Aggiungere 50 mL di una soluzione AgNO3 (aq) (0,0059 mol/L) al becher sotto vigorosa agitazione magnetica (500 giri/min) a temperatura ambiente.
- Aggiungere 10 mL di soluzione acquosa di lysine (0,53 M).
- Mantenere la miscela sotto agitazione vigorosa (500 giri/min) per 20 minuti.
- Dopo 20 minuti, utilizzare una pipetta per aggiungere alla sospensione 10 mL di una soluzione NaBH4 (aq) (0,035 M) preparata al momento, ad una velocità di 1 mL/min. Mantenere la sospensione sotto agitazione (500 giri/min) durante tutto il processo.
- Lasciare mescolare la miscela per 30 minuti a temperatura ambiente.
4. Separazione e purificazione del catalizzatore
- Trasferire la sospensione in tubi di centrifugazione e separare i solidi dalla miscela mediante centrifugazione a 3.260 x g per 10 min.
- Rimuovere con cura la fase liquida con una pipetta e aggiungere acqua deionizzata da 15 ml ai tubi.
- Agitare vigorosamente fino a quando non si osserva la dispersione del solido. Se non si ottiene una buona dispersione, posizionare i tubi in un bagno ad ultrasuoni per 5 minuti.
- Centrifugare la dispersione a 3.260 x g per 10 min.
- Ripetere i passaggi di lavaggio (da 4.2. a 4.2.2.) altre due volte utilizzando acqua deionizzata, quindi una volta usando etanolo al posto dell'acqua.
- Rimuovere l'etanolo e asciugare il solido in forno a 60 °C per 12 ore.
- I PN Ag/ZrO2 preparati possono quindi essere caratterizzati da una varietà di tecniche microscopie, elementali e spettroscopiche.
5. Studio delle prestazioni catalitiche plasmoniche verso la riduzione del nitrobenzene sotto eccitazione LSPR (illuminazione luminosa)
- Posizionare 30 mg di catalizzatore in un pallone a fondo tondo da 25 ml insieme a una barra di agitazione magnetica.
- Aggiungere 5 mL di una soluzione di nitrobenzene (0,03 mol/L) nell'alcol isopropile (IPA) al reattore.
- Quindi, aggiungere 11,22 mg di polvere di KOH (0,0002 mol).
- Spurgo il reattore gorgogliando la sospensione con un flusso di argon per 1 minuto. Immediatamente dopo l'spurgo, sigillare il pallone.
- Posizionare il reattore in un bagno d'olio riscaldato a 70 °C sopra un agitatore magnetico a temperatura controllata (500 giri/min).
- Irradiare il tubo utilizzando 4 lampade a LED con una lunghezza d'onda di 425 nm come sorgente luminosa e un'intensità luminosa di 0,5 W/cm2. La distanza dalle lampade al pallone di reazione dovrebbe essere di 7 cm.
- Lasciare procedere la reazione per 2,5 ore a 70 °C sotto vigorosa agitazione magnetica (500 giri/min).
- Quindi, spegnere la luce, aprire il reattore e utilizzare una siringa e un ago per raccogliere un campione da 1 ml. Filtrarlo attraverso un filtro da 0,45 μm, per rimuovere il particolato catalizzatore, in una fiala gascromatografica.
6. Reazione in assenza di eccitazione LSPR (condizioni di buio)
- Seguire gli stessi passaggi descritti al punto 5, ma senza irradiazione leggera. Avvolgere il tubo di reazione con un foglio di alluminio per evitare qualsiasi esposizione alla luce.
7. Preparazione dell'analisi gascromatografica (GC)
- Preparare una soluzione IPA contenente circa 30 mmol/L nitrobenzene (NB), 30 mmol/L di anilina (AN) e 30 mmol/L di azobenzene (AB).
- Eseguire un'analisi GC della soluzione utilizzando un metodo adatto. Diversi metodi possono essere testati variando la temperatura della colonna e i programmi di flusso del gas. Il metodo selezionato dovrebbe essere in grado di separare i picchi corrispondenti a IPA, NB, AN e AB nel periodo minimo di tempo di conservazione.
- Una volta selezionato il metodo, preparare una serie di soluzioni di 50 mM, 25 mM, 10 mM, 5 mM e 2,5 mM NB in IPA e un'altra serie di soluzioni di AN e AB in IPA con le stesse concentrazioni.
- Eseguire un'analisi GC delle soluzioni preparate. Ogni cromatogramma dovrebbe presentare 2 picchi: quello più alto corrisponde all'IPA e quello inferiore corrisponde a NB, AN o AB. Per ogni cromatogramma, annotare il tempo di ritenzione e l'area di picco di tutti i picchi.
- Traccia le curve di calibrazione di NB, AN e AB tracciando l'area di concentrazione rispetto a quella di picco di ogni campione.
8. Analisi GC
- Eseguire un'analisi GC sui campioni raccolti nei passaggi 5. e 6. con lo stesso metodo utilizzato per i passaggi 7.2. e 7.4.
- Per ogni cromatogramma, annotare il tempo di ritenzione e l'area di picco e utilizzare le curve di calibrazione tracciate in precedenza per determinare la concentrazione di NB, AN e AB nei campioni.
- Calcola la conversione nitrobenzene e la selettività dell'anilina e dell'azobenzene usando le equazioni:
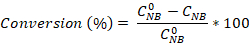
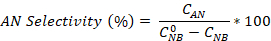
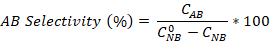
Dove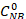 è la concentrazione iniziale di NB (0,03 mol/L) e C NB, CAN, C ABcorrispondono rispettivamente alle concentrazioni NB, AN e AB, dopo 2,5 ore di reazione da parte dell'analisi GC.
è la concentrazione iniziale di NB (0,03 mol/L) e C NB, CAN, C ABcorrispondono rispettivamente alle concentrazioni NB, AN e AB, dopo 2,5 ore di reazione da parte dell'analisi GC.
Access restricted. Please log in or start a trial to view this content.
Risultati
La figura 1A mostra le fotografie digitali dei campioni solidi contenenti l'ossido puro ZrO2 (a sinistra) e i PNA Ag-Pd/ZrO2 (a destra). Questo cambiamento di colore dal bianco (in ZrO2) al marrone (Ag-Pd/ZrO2) fornisce le prime prove qualitative sulla deposizione dei PPP Ag-Pd sulla superficie ZrO2. La figura 1B mostra gli spettri di assorbimento visibili ai raggi UV dei NP Ag-Pd/ZrO2 (traccia bl...
Access restricted. Please log in or start a trial to view this content.
Discussione
I risultati descritti in questo metodo dimostrano che l'attività catalitica intrinseca del Pd (o di altro metallo catalitico ma non plasmonico) può essere significativamente migliorata dall'eccitazione LSPR tramite irradiazione a luce visibile nei PN in lega bimetallica35. In questo caso, Ag (o un altro metallo plasmonico) è in grado di raccogliere energia dall'irradiazione a luce visibile tramite eccitazione LSPR. L'eccitazione LSPR porta alla formazione di portatori di carica calda (elettroni...
Access restricted. Please log in or start a trial to view this content.
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è stato sostenuto dall'Università di Helsinki e dalla Fondazione Jane e Aatos Erkko. S.H. ringrazia i fondi Ue Erasmus+ per la borsa di studio.
Access restricted. Please log in or start a trial to view this content.
Materiali
| Name | Company | Catalog Number | Comments |
| 2-Propanol (anhydrous, 99.5%) | Sigma-Aldrich | 278475 | CAS Number 67-63-0 |
| Aniline (for synthesis) | Sigma-Aldrich | 8.22256 | CAS Number 62-53-3 |
| Azobenzene (98%) | Sigma-Aldrich | 424633 | CAS Number 103-33-3 |
| Ethanol | Honeywell | 32221 | CAS Number 64-17-5 |
| Hydrochloric acid (37%) | VWR | PRLSMC310066 | CAS Number 7647-01-0 |
| L-Lysine (crystallized, ≥98.0% (NT)) | Sigma-Aldrich | 62840 | CAS Number 56-87-1 |
| Nitric acid (65%) | Merck | 100456 | CAS Number 7697-37-2 |
| Nitrobenzene | Sigma-Aldrich | 8.06770 | CAS Number 98-95-3 |
| Potassium hydroxide | Fisher | 10448990 | CAS Number 1310-58-3 |
| Potassium tetrachloropalladate (II) (98%) | Sigma-Aldrich | 205796 | CAS Number 10025-98-6 |
| Silver nitrate (ACS reagent, ≥99.0%) | Sigma-Aldrich | 209139 | CAS Number 7761-88-8 |
| Sodium borohydride (fine granular for synthesis) | Sigma-Aldrich | 8.06373 | CAS Number 16940-66-2 |
| Zirconium (IV) oxide (nanopowder, <100 nm particle size (TEM)) | Sigma-Aldrich | 544760 | CAS Number 1314-23-4 |
Riferimenti
- Dunn, P. J., Hii, K. K., Krische, M. J., Williams, M. T. Sustainable Catalysis: Challenges and Pratices for the Pharmaceutical and Fine Chemical Industries. , Wiley-Blackwell. (2013).
- Tzouras, N. V., Stamatopoulos, I. K., Papastavrou, A. T., Liori, A. A., Vougioukalakis, G. C. Sustainable metal catalysis in C-H activation. Coordination Chemistry Reviews. 343, 25(2017).
- Polshettiwar, V., Varma, R. S. Green chemistry by nano-catalysis. Green Chemistry. 12 (5), 743(2010).
- Rodrigues, T. S., da Silva, A. G. M., Camargo, P. H. C. Nanocatalysis by noble metal nanoparticles: controlled synthesis for the optimization and understanding of activities. Journal of Materials Chemistry A. 7 (11), 5857-5874 (2019).
- Linic, S., Christopher, P., Ingram, D. B. Plasmonic-metal nanostructures for efficient conversion of solar to chemical energy. Nature Materials. 10 (12), 911-921 (2011).
- Nam, J. M., Liz-Marzán, L., Halas, N. Chemical Nanoplasmonics: Emerging Interdisciplinary Research Field at Crossroads between Nanoscale Chemistry and Plasmonics. Accounts of Chemical Research. 52 (11), 2995-2996 (2019).
- Brongersma, M. L., Halas, N. J., Nordlander, P. Plasmon-induced hot carrier science and technology. Nature Nanotechnology. 10 (1), 25-34 (2015).
- Smith, J. G., Faucheaux, J. A., Jain, P. K. Plasmon resonances for solar energy harvesting: A mechanistic outlook. Nano Today. 10 (1), 67-80 (2015).
- Hartland, G. V. Optical studies of dynamics in noble metal nanostructures. Chemical Reviews. 111 (6), 3858-3887 (2011).
- Kelly, K. L., Coronado, E., Zhao, L. L., Schatz, G. C. The optical properties of metal nanoparticles: The influence of size, shape, and dielectric environment. Journal of Physical Chemistry B. 107 (3), 668-677 (2003).
- Hermoso, W., et al. Triangular metal nanoprisms of Ag, Au, and Cu: Modeling the influence of size, composition, and excitation wavelength on the optical properties. Chemical Physics. 423, 142-150 (2013).
- Kumar, A., et al. Rational Design and Development of Lanthanide-Doped NaYF4@CdS-Au-RGO as Quaternary Plasmonic Photocatalysts for Harnessing Visible-Near-Infrared Broadband Spectrum. ACS Applied Materials and Interfaces. 10 (18), 15565-15581 (2018).
- Reddy, K. L., Kumar, S., Kumar, A., Krishnan, V. Wide spectrum photocatalytic activity in lanthanide-doped upconversion nanophosphors coated with porous TiO2 and Ag-Cu bimetallic nanoparticles. Journal of Hazardous Materials. 367, 694-705 (2019).
- Ingram, D. B., Linic, S. Water splitting on composite plasmonic-metal/semiconductor photoelectrodes: Evidence for selective plasmon-induced formation of charge carriers near the semiconductor surface. Journal of the American Chemical Society. 133 (14), 5202-5205 (2011).
- Linic, S., Aslam, U., Boerigter, C., Morabito, M. Photochemical transformations on plasmonic metal nanoparticles. Nature Materials. 14 (6), 567-576 (2015).
- Aslam, U., Rao, V. G., Chavez, S., Linic, S. Catalytic conversion of solar to chemical energy on plasmonic metal nanostructures. Nature Catalyst. 1, 656-665 (2018).
- Araujo, T. P., Quiroz, J., Barbosa, E. C. M., Camargo, P. H. C. Understanding plasmonic catalysis with controlled nanomaterials based on catalytic and plasmonic metals. Current Opinion in Colloid and Interface Science. 39, 110-122 (2019).
- Gellé, A., et al. Applications of plasmon-enhanced nanocatalysis to organic transformations. Chemical Reviews. , 986-1041 (2020).
- Shaik, F., Peer, I., Jain, P. K., Amirav, L. Plasmon-Enhanced Multicarrier Photocatalysis. Nano Letters. 18 (7), 4370-4376 (2018).
- Quiroz, J., et al. Controlling Reaction Selectivity over Hybrid Plasmonic Nanocatalysts. Nano Letters. 18, 7289-7297 (2018).
- Peiris, E., et al. Plasmonic Switching of the Reaction Pathway: Visible-Light Irradiation Varies the Reactant Concentration at the Solid-Solution Interface of a Gold-Cobalt Catalyst. Angewandte Chemie - International Edition. 58 (35), 12032-12036 (2019).
- Yu, S., Wilson, A. J., Heo, J., Jain, P. K. Plasmonic Control of Multi-Electron Transfer and C-C Coupling in Visible-Light-Driven CO2 Reduction on Au Nanoparticles. Nano Letters. 18 (4), 2189-2194 (2018).
- Yu, S., Jain, P. K. Plasmonic photosynthesis of C 1 -C 3 hydrocarbons from carbon dioxide assisted by an ionic liquid. Nature Communications. 10, 2022(2019).
- Zhang, X., et al. Product selectivity in plasmonic photocatalysis for carbon dioxide hydrogenation. Nature Communications. 8, 1-9 (2017).
- Cortés, E. Efficiency and Bond Selectivity in Plasmon-Induced Photochemistry. Advanced Optical Materials. 5 (15), 1700191(2017).
- de Freitas, I. C., et al. Design-controlled synthesis of IrO 2 sub-monolayers on Au nanoflowers: marrying plasmonic and electrocatalytic properties. Nanoscale. , 23-27 (2020).
- Zhang, C., et al. Al-Pd Nanodisk Heterodimers as Antenna-Reactor Photocatalysts. Nano Letters. 16 (10), 6677-6682 (2016).
- Zhou, L., et al. Light-driven methane dry reforming with single atomic site antenna-reactor plasmonic photocatalysts. Nature Energy. 5, 61-70 (2020).
- Swearer, D. F., et al. Heterometallic antenna-reactor complexes for photocatalysis. Proceedings of the National Academy of Sciences. 113 (32), 8916-8920 (2016).
- Peiris, S., Sarina, S., Han, C., Xiao, Q., Zhu, H. -Y. Silver and palladium alloy nanoparticle catalysts: reductive coupling of nitrobenzene through light irradiation. Dalton Transactions. 46 (32), 10665-10672 (2017).
- Rahm, J. M., et al. A Library of Late Transition Metal Alloy Dielectric Functions for Nanophotonic Applications. Advanced Functional Materials. 2002122, 02122(2020).
- Zhang, C., Chen, B. Q., Li, Z. Y., Xia, Y., Chen, Y. G. Surface Plasmon Resonance in Bimetallic Core-Shell Nanoparticles. Journal of Physical Chemistry C. 119 (29), 16836-16845 (2015).
- Liu, Z., Huang, Y., Xiao, Q., Zhu, H. Selective reduction of nitroaromatics to azoxy compounds on supported Ag-Cu alloy nanoparticles through visible light irradiation. Green Chemistry. 18 (3), 817-825 (2016).
- Chaiseeda, K., Nishimura, S., Ebitani, K. Gold nanoparticles supported on alumina as a catalyst for surface plasmon-enhanced selective reductions of nitrobenzene. ACS Omega. 2 (10), 7066-7070 (2017).
- Peiris, S., et al. Metal nanoparticle photocatalysts: emerging processes for green organic synthesis. Catalysis Science and Technology. 6 (2), 320-338 (2016).
- García-García, I., et al. Silver-Based Plasmonic Catalysts for Carbon Dioxide Reduction. ACS Sustainable Chemistry and Engineering. 8 (4), 1879-1887 (2020).
- Agrawal, A., Johns, R. W., Milliron, D. J. Control of Localized Surface Plasmon Resonances in Metal Oxide Nanocrystals. Annual Review of Materials Research. 47 (1), 1-31 (2017).
- Lounis, S. D., Runnerstrom, E. L., Llordés, A., Milliron, D. J. Defect chemistry and Plasmon physics of colloidal metal oxide Nanocrystals. Journal of Physical Chemistry Letters. 5 (9), 1564-1574 (2014).
- Rej, S., et al. Determining Plasmonic Hot Electrons and Photothermal Effects during H2 Evolution with TiN-Pt Nanohybrids. ACS Catalysis. 10 (9), 5261-5271 (2020).
- Barragan, A. A., et al. Photochemistry of Plasmonic Titanium Nitride Nanocrystals. The Journal of Physical Chemistry C. 123 (35), 21796-21804 (2019).
Access restricted. Please log in or start a trial to view this content.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon