A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
تطوير المولدة للكبريتيد الحمأة من الرواسب البحرية والحد من Trichloroethylene في غطاء المفاعل Upflow اللاهوائية الحمأة
In This Article
Summary
Microbial sulfate reduction is a process of great importance in environmental biotechnology. The success of the sulfidogenic reactors depends among other factors on the microbial composition of the sludge. Here, we present a protocol to develop sulfidogenic sludge from hydrothermal vents sediments in a UASB reactor for reductive dechlorination purposes.
Abstract
The importance of microbial sulfate reduction relies on the various applications that it offers in environmental biotechnology. Engineered sulfate reduction is used in industrial wastewater treatment to remove large concentrations of sulfate along with the chemical oxygen demand (COD) and heavy metals. The most common approach to the process is with anaerobic bioreactors in which sulfidogenic sludge is obtained through adaptation of predominantly methanogenic granular sludge to sulfidogenesis. This process may take a long time and does not always eliminate the competition for substrate due to the presence of methanogens in the sludge. In this work, we propose a novel approach to obtain sulfidogenic sludge in which hydrothermal vents sediments are the original source of microorganisms. The microbial community developed in the presence of sulfate and volatile fatty acids is wide enough to sustain sulfate reduction over a long period of time without exhibiting inhibition due to sulfide.
This protocol describes the procedure to generate the sludge from the sediments in an upflow anaerobic sludge blanket (UASB) type of reactor. Furthermore, the protocol presents the procedure to demonstrate the capability of the sludge to remove by reductive dechlorination a model of a highly toxic organic pollutant such as trichloroethylene (TCE). The protocol is divided in three stages: (1) the formation of the sludge and the determination of its sulfate reducing activity in the UASB, (2) the experiment to remove the TCE by the sludge, and (3) the identification of microorganisms in the sludge after the TCE reduction. Although in this case the sediments were taken from a site located in Mexico, the generation of a sulfidogenic sludge by using this procedure may work if a different source of sediments is taken since marine sediments are a natural pool of microorganisms that may be enriched in sulfate reducing bacteria.
Introduction
كان واحدا من أهم الإسهامات في مجال التكنولوجيا الحيوية البيئية تصميم المفاعلات الحيوية التي كانت الحمأة المستخدمة (اللقاح) قادرة على أداء تحت كبريتات الحد من الظروف. كبريتات (SR) يسمح علاج مياه الصرف التي تحتوي على تركيزات عالية من كبريتات بالإضافة إلى إزالة في وقت واحد من COD، والمعادن الثقيلة والملوثات العضوية، الأمر الذي يجعل SR صفة مرغوبة من الحمأة 1. بعض الأمثلة من النفايات السائلة الملوثة مع كبريتات تأتي من الدباغة والورق والأدوية والصناعات الكيميائية الصناعات 1. ومع ذلك، فإن معظم الأدبيات يشير إلى المولدة للكبريتيد الحمأة عندما تم تكييفها الحمأة الحبيبية الميثان إلى sulfidogenesis 2. يتم تحقيق هذا التكيف عادة عن طريق التلاعب في COD / SO 4 2- النسبة في مفاعل حيوي وإضافة مواد كيميائية لمنع methanogens في 2،3 الحمأة. بالإضافة إلى وقت طويل أن معبد المنعم يوسف تتطلب تشكيل حبيبات المولدة للكبريتيد، والمنافسة بين methanogens ومخفضات الكبريتات والتسامح من الحمأة لتركيزات عالية من كبريتيد هي بعض من المشاكل الرئيسية التي قد تنشأ إذا تم الحصول على الحمأة المولدة للكبريتيد المستخدمة في مفاعل حيوي من تطويع في الغالب الحمأة الميثان إلى كبريتات الحد من الظروف. في هذا العمل، ونحن وصف الإجراء للحصول على الحمأة في الغالب المولدة للكبريتيد من الفتحات الحرارية المائية رواسب (بونتا ميتا، ناياريت، المكسيك) في upflow اللاهوائية مفاعل الحمأة بطانية (UASB)، ثم نقيم كبريتات في الحد من النشاط مع مرور الوقت وإجراء تجربة لتقييم تطبيقه على إزالة الكلور التخفيض. وقد تم اختيار موقع الرواسب لأنه قد تم الإبلاغ عن أن في هذا الموقع هناك تشكيل كبريتيد بسبب النشاط كبريتات الحد التي أظهرتها المجتمع الميكروبي تقطن أن معين مكان 4.
هناك سيفرمزايا القاعدة في الحصول على هذه الحمأة المولدة للكبريتيد من الرواسب على التكيف مع الحمأة الحبيبية الميثان إلى sulfidogenesis. بعض من هذه المزايا هي: (1) أنه ليس من الضروري لتشكيل حبيبات للمفاعل حيوي للعمل، (2) الحمأة تتسامح مع تركيزات عالية نسبيا من كبريتيد بالمقارنة مع الآخرين UASB التي تعمل مع تكييف الحمأة الميثان، و (3) هناك لا التنافس على الركيزة مع methanogens حتى إذا تم استخدام خلات في خليط من الأحماض الدهنية الطيارة التي يتم تضمينها في مستنبت لتشجيع تشكيل الحمأة.
وأعقب هذا الإجراء إلى تعزيز sulfidogenesis بسبب الرواسب البحرية هي بركة طبيعية من مجموعة متنوعة واسعة من الكائنات الدقيقة مثل كبريتات الحد من البكتيريا، تخمر البكتيريا والجراثيم dehalogenating فقط أن أذكر بعض 5،6. نوع كونسورتيوم المتقدمة من الرواسب البحرية باستخدام هذا البروتوكول قد تظهر كفاءة في كبريتات وبالتالي، ق عالية ulfate الحد من النشاط مع مرور الوقت وزيادة التسامح لكبريتيد بتركيزات أعلى من الإبلاغ عن سامة للmethanogens وكبريتات الحد من البكتيريا. من ناحية أخرى، فمن المرجح أن القدرة dehalogenating يظهر أيضا في الرواسب باتباع البروتوكول المقترح هنا ولكن قد تعتمد على المجتمع الميكروبي الأصلي. ويتم هذا الافتراض استنادا إلى حقيقة أنه يمكن أن تحدث إزالة الكلور التخفيض إما عن طريق التنفس أو cometabolism، سواء الظروف التي يمكن الترويج لها في المجتمع الميكروبي البحري 7. وقد أجريت زراعة الرواسب للحصول على الحمأة باستخدام خليط من خلات، بروبيونات والزبدات كما الركيزة لأنه يتم استخدام هذه الأحماض الدهنية المتطايرة من قبل عدة سلالات من كبريتات الحد من البكتيريا. هذه الأحماض هي أيضا نوع من مركبات الكربون وجدت في كثير من الأحيان في الرواسب البحرية، وفقا لعدة تقارير في الأدب على المواد الكربونية في الرواسب البحرية 5،6.
محتوى "> وأخيرا، بعض من أكثر المركبات السامة التي تم العثور عليها في المياه الجوفية والمياه الهيئات الأخرى في جميع أنحاء العالم هي المذيبات المكلورة مثل ثلاثي كلور (TCE) أو الإيثيلين (PCE). هذه المركبات السامة ليس فقط للإنسان ولكن كما أن الكائنات الحية الدقيقة، وخاصة أشكال التعبير الثقافي التقليدي، الذي لا يزال يعتبر من الملوثات ذات الأولوية من قبل وكالة حماية البيئة في الولايات المتحدة (8). وفي هذا العمل اقترحنا تجربة التي يتم اختبار الحمأة المولدة للكبريتيد على قدرتها على الحد من أشكال التعبير الثقافي التقليدي بتركيزات التي هي في مجموعة أبلغ عن المركبات المكلورة التحلل الحيوي في ظل ظروف الميثان 9،10. ومن الجدير بالذكر أن معظم البحوث على تحلل من المركبات المكلورة وقد أجريت في ظل ظروف الميثان 9،10. ونحن نعتبر أن التجربة مع أشكال التعبير الثقافي التقليدي المقترحة في هذا البروتوكول هو وكان الهدف من هذه التجربة خير مثال على التطبيقات المحتملة للحمأة إلى البريدتثمين التسامح من الحمأة لأشكال التعبير الثقافي التقليدي وأشكال التعبير الثقافي التقليدي تأثير على كبريتات الحد من النشاط. مع الأخذ بعين الاعتبار أن معظم البحوث على تحلل من مركبات الكلور تتم في ظل ظروف الميثان، يوحي هذا البروتوكول تشكيل الحمأة يمكن أن تستخدم لفي وقت واحد: (1) إزالة كبريتات، (2) إزالة COD و (3) إزالة المركبات المكلورة. خطوة أخرى يمكن أن تكون لتقييم الحمأة على إزالة في وقت واحد من أشكال التعبير الثقافي التقليدي والمعادن الثقيلة (بالإضافة إلى كبريتات وCOD)، واثنين من الشروط التي لا يمكن تقييمها في ظل ظروف الميثان.Protocol

الشكل 1. مخطط للخطوات من البروتوكول. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
1. جمع الرواسب البحرية لتشكيل الحمأة
- تحديد منطقة تحت سطح البحر ودود إما قريبة من الفتحات الحرارية المائية (بسبب وجود كبريتيد، مما قد يشير إلى كبريتات النشاط الحد من أعلى) أو إلى المنطقة التي الحطام من المواد العضوية قابلة للكشف.
- لغرض هذا العمل، يستغرق حوالي 3 أو 4 كجم من الرواسب واستنزاف المياه قبالة العينات. وضع العينات في أكياس بلاستيكية داكنة. ليس هناك حاجة إلى التبريد.
- مرة واحدة في المختبر، والحفاظ على أكياس مع العينات في الثلاجة إذا لم تكن على وشك أن يستخدم على الفور. لغرض هذا العمل، عصيدةليه يمكن أن يكون في الثلاجة لمدة أسابيع أو أشهر قبل استخدامها.
- تأخذ جزءا كبيرا من العينة الرواسب (أي 1 أو 2 كلغ) واستخدام شبكة المناسبة (0.2 سم) للقضاء على من الرواسب تحت الانقاض كبيرة من المواد الكربونية التي قد تكون موجودة أو بعض الصخور التي قد تكون موجودة.
ملاحظة: في هذه الحالة تم استخدام شبكة من 0.20 سم القطر (0.0767 في) لكنها قد تكون ذات حجم مختلفة وفقا لحجم الجسيمات في العينة.- بعد اجتياز الرواسب من خلال عيون، مزيج الجزء المحدد لتعزيز هذا الجزء هو متجانس.
- خذ فصل عينات أصغر (أي 2-3 ز) لتحديد المتطايرة المواد الصلبة العالقة (VSS) محتوى باتباع الطرق القياسية 11.
ملاحظة: انظر الشكل 2 لخطوات 1،2-1،4.

الشكل 2. صور للعينات الرواسب.عينات (A) الرواسب فقط بعد نقله. العينة (B) الرواسب بعد مرورها من خلال شبكة (C) عينة أخذت وزنها قبل المواد الصلبة العالقة المتطايرة (VSS) تقرير. لا يحتاج طبق بيتري إلى أن تكون معقمة. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
2. مفاعل حيوي تعيين لأعلى
- لغرض هذا العمل، استخدام مفاعل الزجاج UASB مع حجم العمل الكلي لل3 L. بدلا من ذلك، استخدم 1 أو 2 L مفاعل الزجاج الحجم.
- بناء على محتوى VSS من الرواسب حساب كمية الرواسب لاستخدامها اللقاح للحصول على 5 غرام من VSS في 1 L.
- تأخذ في الاعتبار أنه إذا كمية الرواسب بعد حساب كبير جدا، ويجب أن احتل حجم ثم ما يقرب من 25٪ إلى 30٪ من مفاعل حيوي من الرواسب بدلا من ذلك.
- تسجيل المحتوى VSS منذسيتغير عندما يتم إثراء المجتمع الميكروبي في مفاعل حيوي. هناك حاجة إلى المحتوى VSS لحسابات سلفات خفض النشاط في مفاعل حيوي.
- تأكد من أن تركيز النهائي من المتوسط وعازلة حل القاعدية في مفاعل حيوي يشبه ذكرت من قبل غيريرو باراخاس وآخرون. (2014) 12.
- تأكد من أن كميات الأخيرة من الرواسب والمتوسطة القاعدية، حل العازلة والأحماض الدهنية الطيارة هي مساوية لحجم العمل النهائي للمفاعل. المتوسط صفة القاعدية 12 تحتوي على تركيزات مناسبة من أجل حل المعادن النزرة والفيتامينات.
- يعد حل الأسهم المتوسطة القاعدية وحل العازلة في التركيز المناسب لحجم العمل في مفاعل المستخدمة (أي، 2، 3 أو 4 أضعاف أكثر تركيزا من ذكرت في الخطوة 2.4) للتأكد من أنه عندما يتم تخفيفه، فمن في تركيز ذكرت غيريرو باراخاس وآخرون. (2014)12).
ملاحظة: الحل الأسهم على المدى المتوسط القاعدية هو من الضروري دائما، ومع ذلك، هناك حاجة فقط حل العازلة في البدء. ليس من الضروري إضافة محلول منظم بعد هذا الوقت. - إعداد محلول المخزون من الأحماض الدهنية الطيارة: خلات، بروبيونات والزبدات في 2.5: 1: 1 نسبة COD. خذ بعين الاعتبار لحسابات خلات الصوديوم المدرجة في المتوسط القاعدية. تركيز COD النهائي في المفاعل يجب أن تكون 2.7 غرام / L.
تحذير: يعد هذا الحل في غطاء الدخان. ارتداء القفازات النتريل ونظارات واقية لإعداد هذا الحل. تأخذ بعين الاعتبار رياضيات الكيمياء من ردود الفعل من كبريتات مع الأحماض الدهنية المتطايرة الذي يظهر في الشكل (3). - إعداد محلول المخزون من كبريتات الصوديوم (نا 2 SO 4) في التركيز المناسب لتسليم المفاعل تركيز النهائي من 4000 ملغم / لتر من أيون الكبريتات (SO 4 2-). بدلا من ذلك، تتضمن عشرمبلغ (ه) من كبريتات المطلوبة في المتوسط القاعدية بدلا من إضافته من حل الأسهم طالما أن كبريتات النهائية (SO 4 2-) التركيز هو الصحيح.
- ضع الرواسب في المفاعل مختلطة مع جزء من المتوسط القاعدية للتأكد من أنها تصل إلى قاع المفاعل.
- إضافة بقية المتوسطة وعازلة القاعدية حل مختلطة مع الأحماض الدهنية الطيارة الحل ومحلول كبريتات. تأكد من أن الحل من الأحماض الدهنية الطيارة يسكب السائل. ملاحظة: إجراء هذه الخطوة في غطاء الدخان.
- تعيين الاتصالات وخطوط الأنابيب من المفاعل إلى مضخة إعادة التدوير. ضبط معدل تدفق إعادة التدوير في 60 مل / دقيقة. تعيين مفاعل حيوي في غرفة درجة الحرارة إلى 34 درجة مئوية. تحقق بانتظام أن تغيرات درجة الحرارة هي صغيرة (أي 34 ± 1.7 ° C)
- تعيين الاتصالات إلى العمود النزوح الغاز.
ملاحظة: انظر الشكل 4 للخطوات 2،1-2،5.
الشكل 3. الاتحاد العنصري من كبريتات مع VFA (خلات، بروبيونات والزبدات). الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
الرقم 4. UASB المفاعل. (A) الساعة الأولي. (B) نظام مستمر بعد 300 أيام من العملية. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.3. تشغيل المفاعل في تعزيز Sulfidogenesis ونمو الكائنات الدقيقة
ملاحظة: السماح لقيحة للاستهلاك الخامسolatile الأحماض الدهنية وكبريتات. لهذا الغرض، وانتظر لمدة أسبوع لإجراء التحليل الأول للكبريتات، كبريتيد والاستهلاك COD.
- بعد أسبوع واحد من الحضانة أخذ عينة من 5-7 مل من السائل إلى إجراء تحليل لCOD، كبريتات والمحتوى كبريتيد ودرجة الحموضة في أعقاب الأساليب القياسية 11 و 13.
- تحليل كبريتيد في طيفيا السائل (في الطول الموجي (λ) من 670 نانومتر) باتباع الميثيلين الأزرق 13 طريقة.
- وضع 5 مل من محلول خلات الزنك (2٪ ث / ث) في 25 مل قارورة حجمية، إضافة بسرعة 200 ميكرولتر من العينة إلى حل خلات الزنك.
- إضافة 2.5 مل من N، N -dimethyl- ص -phenylenediamine أكسالات (DMP) حل (0.2٪ ث / ث في H 2 SO 4 20٪) و 125 ميكرولتر من الحديد (III) محلول كبريتات الأمونيوم (10٪ ث / ث في 2٪ H 2 SO 4) وكاملة مع الماء المقطر 25 مل في القارورة الحجمية. انتظر 30 دقيقة للتفاعلأن يحدث، في الوقت الذي استقر اللون الأزرق. 13.
ملاحظة: انتظر 15 دقيقة على الأقل، ولكن ليس أكثر من 60 دقيقة لاختبار العينات في معمل. إجراء القراءة من الحل النهائي الأزرق في معمل.
- تحليل كبريتات وفقا للطرق القياسية 11. هنا، تحديد كبريتات كما كبريتات الباريوم باستخدام طريقة قياس العكارة.
- وضع 5 مل من محلول تكييف (حمض الهيدروكلوريك حمض الهيدروكلوريك 1: 1) في قارورة حجمية من 25 مل، إضافة 1 مل من العينة طرد سابقا (في 11320 × ز)، واستكمال 25 مل من القارورة الحجمية مع الماء المقطر و إضافة 1 غرام من كلوريد الباريوم.
- مزيج الحل لمدة 1 دقيقة في دوامة. الانتظار لمدة 4 دقائق للكبريتات الباريوم لتشكيل وقراءة العينة في معمل في الطول الموجي (λ) من 420 نانومتر 11.
- تحليل COD وفقا للأساليب القياسية 11. بدلا من ذلك، استخدم COD determinaمجموعة نشوئها.
- قبل تحديد COD، الطرد المركزي العينة بدقة (في 11320 x ج) لإزالة كبريتيد المتبقية التي قد تتداخل في تحديد. إذا لزم الأمر، الطرد المركزي مرتين: المرة الأولى مباشرة بعد أخذ عينة والمرة الثانية تنتظر 6 أو 8 ساعات ثم إجراء التحليل COD.
- إضافة 2 مل من العينة إلى قارورة رد فعل من مجموعة تقرير COD، وختم قارورة وتجانس الخليط عن طريق الإثارة لطيف. إعداد فارغة بإضافة 2 مل من الماء المقطر لقارورة رد فعل آخر، وتجانس الخليط.
- ضع قارورة في المفاعل الهضم عند 150 درجة مئوية لمدة 2 ساعة. إزالة قارورة والسماح لهم يبرد في الظلام. أخذ القراءات من قارورة في معمل عند طول موجي 620 نانومتر ل.
- الحصول على حجم الغاز من العمود النزوح الغاز.
- تحليل كبريتيد في طيفيا السائل (في الطول الموجي (λ) من 670 نانومتر) باتباع الميثيلين الأزرق 13 طريقة.
- الانتظار لمدة تصل إلى 5-7 أيام أخرى حتى يتم استهلاك كبريتات. كبريتات وCOD يجب أن تستهلك فيpproximately 85٪ إلى 90٪ قبل بدء دفعة جديدة تغذيها.
- مرة واحدة يتم استهلاكها كبريتات (وCOD)، كرر الخطوة تماما 2،4. العرض المتوسطة الطازجة والمواد المغذية جديدة لكل دفعة.
- كرر الخطوات من 3.1 و 3.2. في هذه المرحلة يجب على كل دفعة تستمر ما بين 7 و 10 أيام.
- عندما تم الانتهاء 3-4 دفعات، كرر الخطوة 2.4 ولكن زيادة تركيز COD إلى 4 ز / L.
- كرر الخطوة 3.1 و 3.2 خطوة.
- كرر الخطوة 3.3 ولكن زيادة تركيز COD إلى 6 ز / L.
- كرر 3.6 و 3.6.1 زيادة تدريجيا تركيز COD حتى 10 جرام / لتر.
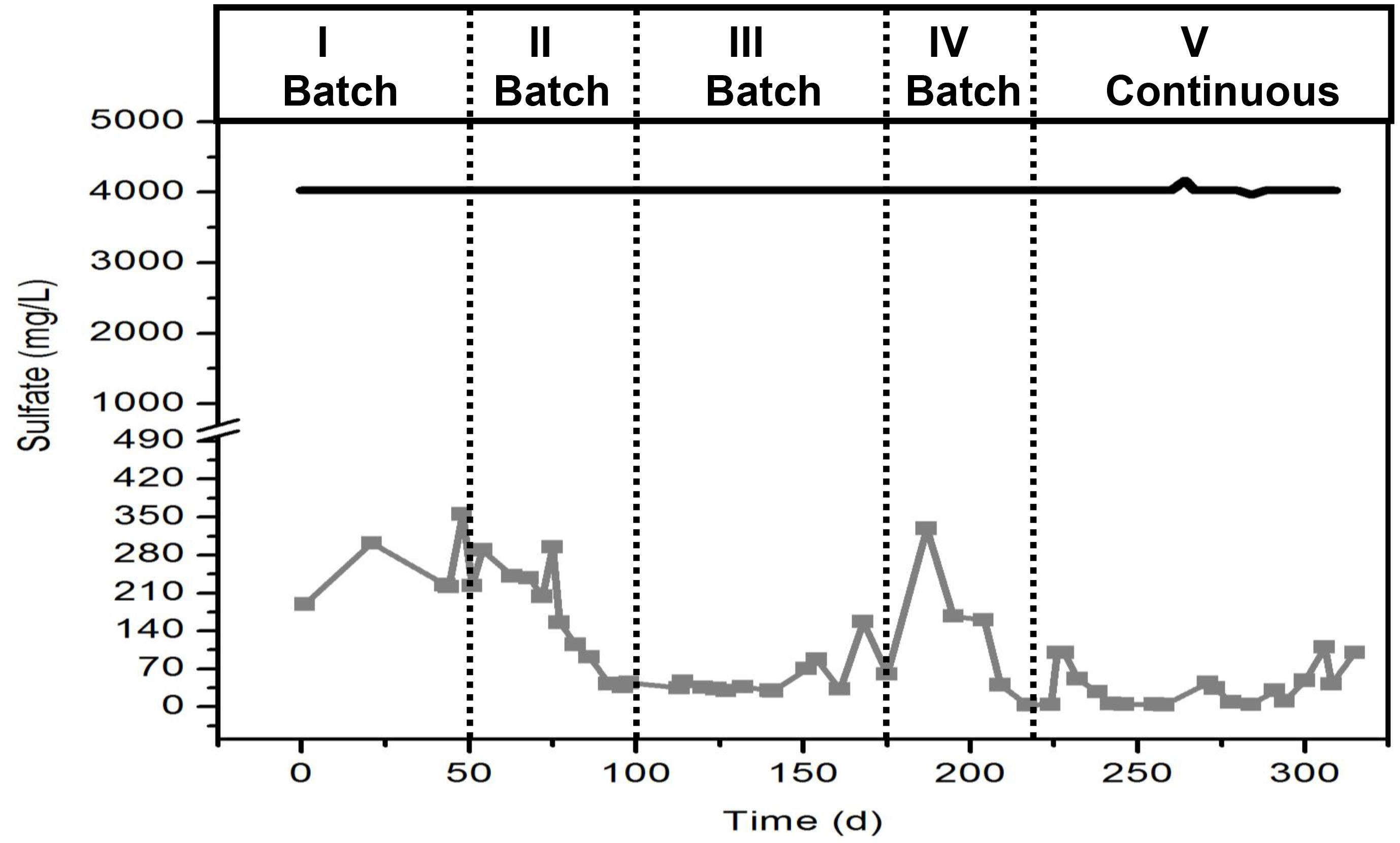
ملاحظة: جعل الرسم البياني الذي يطرح تركيز كبريتات (ملغم / لتر) في مقابل الوقت (د).
- عندما استهلاك كبريتات أكثر من 80٪ في أقل من 24 ساعة وهذا يحدث لأكثر من أسبوع واحد، والتبديل في تشغيل المفاعل إلى الوضع المستمر. لوضع مستمر ضبط الوقت الاحتفاظ الهيدروليكي (HRT) في 24 ساعة، والحفاظ على تركيز كبريتات في 4 ز / L وCODفي 10 جرام / لتر.
ملاحظة: مع مرور الوقت يجب أن يكون استهلاك كبريتات أسرع.
4. كبريتات تخفيض آخر اختبار
- قبل هذا الاختبار التأكد من أن مفاعل حيوي في ظل نظام مستمر يعرض أقل من 10٪ الاختلاف في تركيز كبريتات المتبقية.
- في أي يوم من الأيام، ووقف المفاعل بعد HRT دورة واحدة والسلوك خطوة 2.4. لخطوة 2.4.3 استخدام تركيز COD من 10 جرام / لتر.
- مرة واحدة ويتم تغذية مفاعل حيوي، واتخاذ 5-7 مل عينات من السائل وإجراء تحليل لCOD، كبريتات، كبريتيد (الخطوة 3.1) ودرجة الحموضة في كل ساعة. سجل حجم الغاز المنتج.
- حساب سلفات الحد من نشاط وفقا لأدبيات 14.

SRA = كبريتات الحد من نشاط (ملغ COD-H 2 S) / gVSS * د
م H 2 S = تركيز كبريتيد كما ملغ COD-H 2 S
VSS = متقلبة تركيز المواد الصلبة العالقة
ر = الزمن (د أو ساعة)
- جعل الرسوم البيانية المقابلة التي تظهر نسبة استهلاك كبريتات مقابل تركيز كبريتيد على مر الزمن في ملغم / لتر. جعل الرسوم البيانية التي تبين نسبة استهلاك COD بمرور الوقت. جعل الرسوم البيانية التي تظهر اختلاف درجة الحموضة مع مرور الوقت.
5. Trichloroethylene (TCE) اختبار الحد
- قبل هذا الاختبار التأكد من أن مفاعل حيوي يعمل في ظل نظام مستمر ويعرض أقل من 10٪ الاختلاف في تركيز كبريتات المتبقية. لا تبدأ هذا الاختبار إذا كبريتات في مفاعل حيوي أقل من 90٪.
- إعداد محلول المخزون من ثلاثي كلور (TCE) مع الأخذ بعين الاعتبار أن تركيز النهائي من هذا المركب في الطور السائل من مفاعل حيوي يجب أن يكون 300 ميكرومتر. النظر في حواجزنانوغرام من المجمع إلى فراغ الرأس باستخدام ثابت أبعاد القانون Henry's (H') لأشكال التعبير الثقافي التقليدي في 34 ° C. H'at 34 ° C لأشكال التعبير الثقافي التقليدي هو 0.4722.
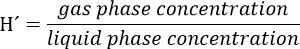
تحذير: يعد هذا الحل في fumehood وارتداء قفازات ونظارات واقية.- على سبيل المثال، عن حل الأسهم 5000 ميكرومتر، وحساب على النحو التالي:
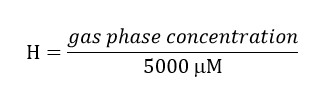
TCE تركيز الطور الغازي = (0.4722) * (5000) = 2139 ميكرومتر. يشمل هذا التركيز في إعداد محلول المخزون حيث أن هذه الكمية من أشكال التعبير الثقافي التقليدي يكون في فراغ الرأس.
ثم في السائل (الماء) من الحل المخزون، وسوف تركيز أشكال التعبير الثقافي التقليدي الفعلي على النحو التالي: 5000 + 2139 = 7139 ميكرومتر. كثافة TCE = 1.43 جم / مل. تحويل ميكرومتر 7139 إلى ملغ ثم باستخدام كثافة TCE حساب حجم أشكال التعبير الثقافي التقليدي من أجل حل الأسهم.
ملاحظة: تركيز أشكال التعبير الثقافي التقليدي حل سهم مAY يكون أقل من 5000 ميكرومتر، أي 3000 أو 1000 ميكرومتر، وهذا يتوقف على الكيفية التي يمكن أن يتم تسليم الكثير من حجم هذا الحل لمفاعل حيوي وفقا لحجمه المرحلة السائلة.
- على سبيل المثال، عن حل الأسهم 5000 ميكرومتر، وحساب على النحو التالي:
- إعداد المنحنيات القياسية في الكروماتوجرافي الغاز لأشكال التعبير الثقافي التقليدي ورابطة الدول المستقلة -1،2-dichloroethylene، عبر -1،2-dichloroethylene، كلوريد الفينيل والإيثين. إعداد رابطة الدول المستقلة -1،2-dichloroethylene وعبر -1،2-dichloroethylene منحنيات القياسية من محلول المخزون من هذه المركبات باتباع نفس الإجراء الموضح في 5.2 لحل الأسهم أشكال التعبير الثقافي التقليدي. إعداد منحنيات القياسية لكلوريد الفينيل والإيثين عن طريق تمييع تركيز كل غاز من المعايير (اسطوانات الغاز).
- إعداد منحنيات القياسية لهذه المركبات في مجموعة من 20-300 ميكرومتر. استخدم الطريقة التي أبلغ عنها غيريرو باراخاس وآخرون. (2011) 15 لتحليل هذه المركبات في الكروماتوجرافي الغاز.
تحذير: إعداد هذه الوقوفحلول ارض في fumehood وارتداء قفازات ونظارات واقية.
- إعداد منحنيات القياسية لهذه المركبات في مجموعة من 20-300 ميكرومتر. استخدم الطريقة التي أبلغ عنها غيريرو باراخاس وآخرون. (2011) 15 لتحليل هذه المركبات في الكروماتوجرافي الغاز.
- في أي يوم من الأيام، ووقف المفاعل بعد HRT دورة واحدة والسلوك خطوة 2.4. لخطوة 2.4.3 استخدام تركيز COD من 10 جرام / لتر.
- مرة واحدة ويتم تغذية مفاعل حيوي، إضافة TCE مباشرة إلى السائل في مفاعل حيوي من الحل الأوراق المالية على استعداد في 5.2، يجب أن يكون تركيز أشكال التعبير الثقافي التقليدي النهائي في المرحلة السائلة من مفاعل حيوي 300 ميكرومتر. تعيين HRT إلى 12 ساعة.
- في نهاية دورة HRT واحد أخذ عينات من السائل (500 إلى 1000 ميكرولتر) وتحليل سلوك COD، كبريتات وكبريتيد (الخطوات 3.1.1، 3.1.2 و 3.1.3). أخذ عينات من فراغ الرأس (100-250 ميكرولتر) وإجراء تحليل لأشكال التعبير الثقافي التقليدي ورابطة الدول المستقلة -1،2-dichloroethylene، عبر -1،2-dichloroethylene، كلوريد الفينيل والإيثين في الكروماتوجرافي الغاز.
- كرر الخطوة 2.4. لخطوة 2.4.3 استخدام تركيز COD من 10 جرام / لتر.
- عدم تكرار أي اختبار الحد من أشكال التعبير الثقافي التقليدي حتى يعرض مفاعل حيوي أكثر من 90٪ تخفيض كبريتات والاختلاف أقل من 10٪ في كل من، كبريتات وكبريتات المتبقية في مفاعل حيوي.
- كرر 5.4 و 5.5 و 5.6 مرتين أو ثلاث مرات أكثر.
- أخذ عينات الرواسب (0.5 غرام) لإجراء التعرف على الكائنات الحية الدقيقة بعد انتهاء اختبار الحد من أشكال التعبير الثقافي التقليدي. القيام بذلك بعد 2 أو 3 اختبارات للحد من أشكال التعبير الثقافي التقليدي.
6. كبريتات تخفيض آخر اختبار بعد تجربة لحد من أشكال التعبير الثقافي التقليدي
- كرر الخطوة 4 تماما.
7. التعرف على الكائنات الدقيقة
- أخذ عينات من الحمأة ما يقرب من 0.5 غرام لكل وإجراء استخراج الحمض النووي الريبي الإجمالي وفقا لأسلوب قياسي 12.
- تضخيم الجينات 16S الريباسي مع النسخ العكسي وإجراء تفاعل البلمرة المتسلسل (RT-PCR) والتضخيم خطوة واحدة 12.
- تصميم الاشعال لتضخيم أو استخدام كنهج أولي تلك المقترحة في الأدب 11. اتبع amplifواقترح إجراء ication في الأدب 12.
- بناء المكتبات 16S الريباسي. amplicons PCR يمكن استنساخ باستخدام الاستنساخ طقم 11. عادة، يمكن استنساخ 10 المستعمرات من كل لوحة (كل مستعمرة تمثل المنتج PCR واحد). إعداد DNA البلازميد لتسلسل وفقا للإجراءات المقترحة في الأدب 12.
- إجراء تسلسل شظايا. إعادة تضخيم ما يقرب من 1400 سنة مضت من المنتجات الخارجية PCR مع بروتوكول PCR التضخيم هو موضح سابقا (الخطوة 7.4) واستنساخ وفقا للإجراءات المقترحة في الأدب 12. عزل البلازميد المؤتلف من E. المستعمرات القولونية كما اقترحت في الأدب 12. هل إجراء الإجراء الجزئي لتسلسل مع M13 التمهيدي العالمية 12.
- إجراء تحليل متواليات. محاذاة تسلسل النوكليوتيدات باستخدام كلوستال X وضبط يدويا في محرر النصوص. إجراء عمليات بحث BLAST من databas NCBIه. (http://www.ncbi.nlm.nih.gov/BLAST/Blast.cgi) 12.
- الحصول على أرقام تسلسل النوكليوتيدات الانضمام. إيداع تسلسل النوكليوتيدات من الحيوانات المستنسخة التي تم تحديدها في تسلسل النوكليوتيدات قاعدة بيانات EMBL (جنرال بنك / EMBL / DDBJ) تحت أرقام الانضمام المقابلة (أي JQ713915eJQ713925 لمتواليات من amplicons) 12.
النتائج
ويرد السلوك النموذجي للكبريتات في مفاعل حيوي في الشكل (5). ومن المهم أن نلاحظ أنه خلال الأسابيع الأولى للحد من كبريتات العملية ستكون بطيئة. لكن بطيئة، واستهلاك أكثر من 90٪ من سلفات مع مرور الوقت إلى أن اللقاح على تطوير المجتمع الميكروبي قادرة على الحد من كبريت?...
Discussion
هناك العديد من التطبيقات من sulfidogenesis في مجال التكنولوجيا الحيوية البيئية، واحدة من التطبيقات الأكثر استخداما من عملية التمثيل الغذائي للبكتيريا الحد من الكبريتات في اتحادات مع تخمر البكتيريا في معالجة مياه الصرف الصحي. المفاعلات UASB هي من بين الأساليب الهندسية الرئ?...
Disclosures
The authors Selene Montserrat García-Solares, Claudio Garibay-Orijel and Claudia Guerrero Barajas submitted (as inventors) in 2012 the application to obtain a patent entitled: “Process for the anaerobic treatment of industrial wastewater with high content of sulfate and chlorinated compounds”. This submission has been approved to the stage of the formatting. The submission has Instituto Politécnico Nacional as the rights owner.
Acknowledgements
The authors are grateful for the financial support provided by Instituto Politécnico Nacional grants 20120110, 20130399 and 20140239 SIP and also by Instituto de Ciencia y Tecnología del Distrito Federal Mexico (PICS 08-79, ICYT-DF, 2009-2012). Thanks also to CONACYT – Mexico for the graduate scholarship (225806) awarded to Selene Montserrat García-Solares and for the financial support provided by grant 82627.
Materials
| Name | Company | Catalog Number | Comments |
| trichloroethylene | sigma Aldrich | 251402 | |
| cis-1,2-dichlorotehylene | sigma Aldrich | ||
| trans-1,2-dichloroethylene | sigma Aldrich | D-62209 | |
| vinyl chloride scotty standard | supelco | 1,000 ppm v/v in nitrogen | |
| ethene scotty standard | supelco | 99% purity | |
| pump | Masterflex | Model 7553-75 | |
| spectrophotometer | any | ||
| microcentrifuge | any | ||
| gas tight syringes | any | 100 and 200 microliters | |
| UASB glass reactor | any | under design | |
| gas chromatograph | any | FID detector | |
| capillary column SPB-624 | supelco | ||
| pH meter | any | ||
| viton tubing | Masterflex | ||
| basal medium reagents | any | ||
| trace metals reagents | any | ||
| vitamins solution reagents | any | ||
| sodium sulfate | any | ||
| volatile fatty acids | any | ||
| COD determination kit | HACH | range 0-15,000 mg/L | |
| TOPO-TA cloning kit pCR®4.0 | Invitrogen, US | ||
| S.N.A.P. TM Miniprep Kit | Invitrogen, UK | ||
| Pure link TM Quick Plasmid Miniprep kit | Invitrogen |
References
- Lens, P., Esposito, M. V. G., Zandvoort, M. Perspectives of sulfate reducing bioreactors in environmental biotechnology. ReViews Environmental Science and Biotechnology. 1 (4), 311-325 (2002).
- Omil, F., Lens, P., Hulshoff, P., Lettinga, G. Characterization of biomass from a sulfidogenic, volatile fatty acid-degrading granular sludge reactor. Enzyme and MicrobialTechnology. 20, 229-236 (1997).
- Lopes, S. I. C., Wang, X., Capela, M. I., Lens, P. N. L. Sulfate reduction during the acidification of sucrose at pH 5 under thermophilic (55 °C) conditions.II: Effect of sulfide and COD/SO4-2 ratio. Bioresource Technology. 101, 4278-4284 (2010).
- Alfonso, P., Prol-Ledesma, R. M., Canet, C., Melgarejo, J. C., Fallick, A. E. Sulfur isotope geochemistry of the submarine hydrothermal coastal vents of Punta Mita, Mexico. Journal of Geochemical Exploration. 78-79, 301-304 (2003).
- Valdemarsen, T., Kristensen, E. Degradation of dissolved organic monomers and short chain fatty acids in sandy marine sediment by fermentation and sulfate reduction. Geochimica et Cosmochimica Acta. 74, 1593-1605 (2010).
- Quistad, S. D., Valentine, D. L. Anaerobic propane oxidation in marine hydrocarbon seep sediments. Geochimica et Cosmochimica Acta. 75, 2159-2169 (2011).
- Futagami, T., Morono, Y., Terada, T., Kaksonen, A. H., Inagaki, F. Dehalogenation activities and distribution of reductive dehalogenase homologous genes in marine subsurface sediments. Applied and Environmental Microbiology. 75 (21), 6905-6909 (2009).
- U.S. Environmental Protection Agency. List of priority pollutants. Clean Water Methods. , (2014).
- Ozdemir, C., Dursun, S., Karatas, M., Sen, N., Sahinkaya, S. Removal of trichloroethylene (TCE) in upFlow anaerobic sludge blanket reactors (UASB). Biotechnology and Biotechnological Equipment. 21 (1), 107-112 (2007).
- Zhang, Y., Wang, X., Hu, M., Li, P. Effect of hydraulic retention time (HRT) on the biodegradation of trichloroethylene wastewater and anaerobic bacterial community in the UASB reactor. Applied Microbiology and Biotechnology. 99, 1977-1987 (2015).
- . . Standard Methods for the Examination of Water and Wastewater. , (1998).
- Guerrero-Barajas, C., et al. Enhanced sulfate reduction and trichloroethylene (TCE) biodegradation in a UASB reactor operated with sludge developed from hydrothermal vents sediments: process and microbial ecology. International Biodeterioration and Biodegradation. 94, 182-191 (2014).
- Trüper, H. G., Schlegel, H. G. Sulphur metabolism in Thiorhodaceae I. Quantitative measurements on growing cells of Chromatium okenii. Antoine van Leeuwenhoek. 30, 225-238 (1964).
- Gallegos-García, M. G. . Biological processes of sulfate reduction in biofilms for metals precipitation [Ph D thesis]. , (2009).
- Guerrero-Barajas, C., Garibay-Orijel, C., Rosas-Rocha, L. E. Sulfate reduction and trichloroethylene biodegradation by a marine microbial community from hydrothermal vents sediments. International Biodeterioration and Biodegradation. 65, 116-123 (2011).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved