A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
أسلوب العامة للكشف عن تكوين نيتروساميدي في الأيض في المختبر من نيتروسامينيز من الفسفرة P450s
In This Article
Summary
Α-هيدروكسيليشن نيتروسامينيز المسببة للسرطان من الفسفرة P450s هو مسار الأيض المقبولة التي تنتج المواد الوسيطة تضر بالحمض النووي، التي تتسبب في حدوث طفرات. بيد أن البيانات الجديدة تشير إلى زيادة الأكسدة إلى نيتروساميديس يمكن أن تحدث. يصف لنا عامة الأسلوب للكشف عن نيتروساميديس المنتجة من المختبر السيتوكروم P450 حفزت استقلاب نيتروسامينيز.
Abstract
ن-نيتروسامينيز هي مجموعة راسخة من المسرطنات البيئية، التي تقتضي أكسدة السيتوكروم P450 معرض النشاط. إليه مقبولة للتنشيط الأيضي ينطوي على تشكيل α-هيدروكسينيتروسامينيس التي تتحلل تلقائياً إلى وكلاء alkylating الحمض النووي. تراكم الأضرار الحمض النووي والطفرات الناتجة يمكن أن تؤدي في النهاية إلى مرض السرطان. أدلة جديدة تشير إلى أن α-هيدروكسينيتروسامينيس يمكن أن يكون كذلك تتأكسد إلى نيتروساميديس بروسيسيفيلي من الفسفرة P450s. نيتروساميديس لأن نيتروساميديس هي عموما أكثر استقرارا من α-هيدروكسينيتروسامينيس، ويمكن أيضا الكيلات الحمض النووي، قد تلعب دوراً في التسرطن. في هذا التقرير، يصف لنا بروتوكول عام لتقييم إنتاج نيتروساميدي من المختبر السيتوكروم P450 حفز الأيض نيتروسامينيز. هذا البروتوكول يستخدم نهج عام لتركيب نيتروساميديس ذات الصلة و في المختبر السيتوكروم P450 أيض مقايسة باستخدام نانوسبراي كروماتوغرافيا سائلة عالية التأين القرار جنبا إلى جنب الكتلي للكشف. هذا الأسلوب الكشف عن N′-نيتروسونوركوتينيني ك المستقلب طفيفة من N′-نيتروسونورنيكوتيني في دراسة المثال. يحتوي الأسلوب على حساسية عالية، والواجب بشكل انتقائي لدقة الكشف الشامل. تطبيق هذا الأسلوب على مجموعة متنوعة من نظم النيتروسامين-السيتوكروم P450 سيساعد في تحديد الطابع العام لهذا التحول. لأن الفسفرة P450s متعددة الأشكال وتختلف في النشاط، فهم أفضل لتشكيل نيتروساميدي يمكن أن تساعد في تقييم مخاطر السرطان الفردية.
Introduction
ن-نيتروسامينيز فئة كبيرة من المواد المسرطنة الموجودة في النظام الغذائي ومنتجات التبغ، والبيئة العامة؛ أنها يمكن أيضا أن تشكل اندوجينوسلي في جسم الإنسان1. واختبرت أكثر من 300 ن-مركبات نيتروزو و > 90% قيمت المسرطنة كما في النماذج الحيوانية2،3. يحمل على السرطنة، يجب أولاً تنشيط هذه المركبات من الفسفرة P450s1،،من23. وتبين البحوث أن الفسفرة P450s سهولة أكسدة نيتروسامينيز إلى α-هيدروكسينيتروسامينيس (الشكل 1)، ومركبات شديدة التفاعل مع إنصاف ~ 5 s قبل المتحللة تلقائياً إلى الكيلديازوهيدروكسيديس. يمكن الكيلات الأخير الحمض النووي بعد فقدان ح2س ون2. الناتجة عن ذلك الحمض النووي adducts، إذا سوائلها، يمكن أن يسبب الطفرات التي، إذا أونكو الحرجة-أو ورم المكثف الجينات، تؤدي إلى السرطان التنمية1. لهذا السبب، فقد أنفق الكثير من الجهد للحصول على فهم كامل للمسارات الأيضية، والحمض النووي adducts، والمتلقين للمعلومات من أكسدة السيتوكروم P450 نيتروسامينيز المسببة للسرطان. هذه المعرفة بإمكانية تطبيقها في تقييم مخاطر السرطان الفردية4.
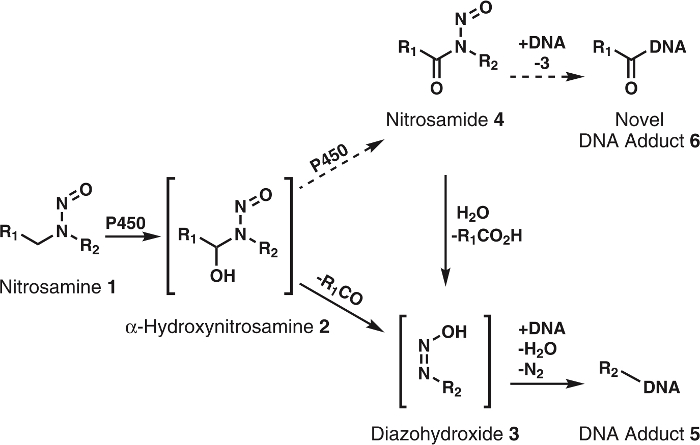
الشكل 1: العامة والتمثيل الغذائي المقترح من نيتروسامينيز.
تتأكسد نيتروسامينيز (1) من P450s إلى α-هيدروكسينيتروسامينيس (2) التي تتحلل تلقائياً إلى الكيلديازوهيدروكسيديس (3). يمكن ربط هذه المركبات للحمض النووي لتشكيل الحمض النووي adducts. هو الافتراض بأن 2 تتأكسد المزيد من P450s إلى نيتروساميديس 4. هذه مباشرة ربط الحمض النووي بشكل رواية الحمض النووي adducts أو أن تحلل إلى 3 لنموذج معروف الحمض النووي adducts. ص1 وص2 تمثل أي مجموعة الألكيل. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
على الرغم من أن الفرضية α-هيدروكسينيتروساميني قوة تدعمها البيانات واسعة النطاق، هناك بعض أوجه عدم الاتساق؛ رئيسي هو أن نصف العمر القصير α-هيدروكسينيتروسامينيس5،6. ومن المعروف أن هذه المركبات تنتج في غشاء هيولى وفي وقت لاحق الكيلاتي الحمض النووي. نظراً لحياتها لبضع ثوان، مما يبعث على الحيرة كيف هذه الوسيطة البقاء على قيد الحياة السفر المطلوبة على الرغم من سيتوسول. فرضية واحدة أن قسما من α-هيدروكسينيتروسامينيس تتأكسد بروسيسيفيلي نيتروساميديس،من78، التي هي مستقر تماما في المقارنة بين9. سوف يفترض أن يحدث هذا عن طريق الاحتفاظ α-هيدروكسينيتروسامينيس في موقع نشط السيتوكروم P450. وقد شوهد سابقة لهذا النوع من الأكسدة مع النيكوتين10، كحول11و12،الكيلنيتروسامينيس بسيطة13. بالإضافة إلى ذلك، يتم نيتروساميديس المباشر المسرطنة2،3. استناداً إلى ما مفاعليه9، يعتقد هذه المركبات لإنتاج الحمض النووي adducts مماثلة لتلك الناتجة عن α-هيدروكسينيتروسامينيس إلى جانب جديد، غير مستكشفة الحمض النووي adducts (الشكل 1). وبالتالي، يفسر هذا الافتراض ليس فقط النقل عن طريق سيتوسول، ولكن أيضا تشكيل الحمض النووي إلى تلف المنتجات.
ويرد في هذه الورقة، وبروتوكول عام لتقييم في المختبر السيتوكروم P450 بوساطة تحويل نيتروسامينيز إلى نيتروساميديس. وعرضت تحويل المبلغ عنها سابقا N′-نيتروسونورنيكوتيني (NNN) إلى N′-نيتروسونوركوتينيني (مركز التغذية الوطني) من 2A6 السيتوكروم P450 ك مثال14. تطبيق هذا البروتوكول على طائفة واسعة من نظم إنزيم الركازة سيساعد في تحديد أهمية نيتروساميديس في العام النيتروسامين الأيض.
Access restricted. Please log in or start a trial to view this content.
Protocol
1-المواد والإجراءات العامة
- Synthesize NNN كما تم وصفه سابقا 15. الحصول على نوركوتينيني، باكولوسوميس 2A6 P450 وتجديد نظام نادف، x 0.5 رد فعل المخزن المؤقت وجميع المواد الكيميائية الأخرى أو المذيبات من مصادر تجارية في الصف الكاشف.
- أطياف "الرنين المغناطيسي النووي سجل" على مطياف 500 ميغاهرتز. التحولات الكيميائية التقرير كأجزاء لكل مليون (ppm). استخدام قمم المذيبات المتبقية كمراجع داخلي ل 1 ح-الرنين المغناطيسي النووي (7.26 ppm كدكل 3) و 13 ج-الرنين المغناطيسي النووي (ppm 77.2 كدكل 3)-
ملاحظة: تقسيم ذروة استخدام المختصرات التالية: s = القميص، د = يبنوا، dd = يبنوا doublets، dt = يبنوا لثلاثة توائم، dq = يبنوا للرباعيات، ddd = يبنوا ليبنوا دوبليتس، وأم = مولتيبليت. - أداء عالية الدقة الطيف الكتلي (نظام إدارة الموارد البشرية) للمركبات المختارة على فيلوس أوربيتراب لتق وبيانات التقرير ك m/z.
- استخدام مخطط متعدد المغلفة مسبقاً لوحات هلام السليكا TLC (40 مم × 80 مم، 0.2 مم) مع 254 نانومتر مؤشر الفلورسنت لطبقة رقيقة اللوني (TLC). عن طريق تشعيع مصباح الأشعة فوق البنفسجية تصور لوحات TLC.
- تنفيذ اللوني فلاش على 60 هلام السليكا مش 70-150، استخدام عمود زجاج 1.5 سم × 15 سم.
2. إعداد المراقبة الإيجابية نيتروساميدي (N ′-نيتروسونوركوتينيني، مركز التغذية الوطني)
- الجاف، في فرن بين عشية وضحاها (ح 16، ~ 140 درجة مئوية)، 25 مل، الجولة-أسفل قارورة تحتوي على شريط إثارة مغناطيسية. في الصباح، بارد قارورة تحت تيار ن 2 أثناء استخدام bubbler نفط الحفاظ على تدفق 2 ن قي فقاعة إطار واحد في الثانية الواحدة.
ملاحظة: بعد التبريد، أية احتياطات للحفاظ على قارورة تحت ن 2 مطلوبة. - في غطاء دخان، إضافة نوركوتينيني (31.8 ملغ، ملمول 0.196)، أنهيدريد الخل (5 مل) وحامض الخليك (1 مل) إلى قارورة تبريد. يقلب هذا الخليط باستمرار أثناء التبريد إلى 0 درجة مئوية مع حمام الماء-الثلج-
تنبيه: أنهيدريد الخل وحمض الخليك، أكالة. - "نانو إضافة" 2 (33.3 ملغ، 0.483 ملمول) في أحد جزء ويقلب المخلوط ل h. 2.5 رصد رد فعل التقدم قبل TLC باستمرار (100 ٪ أتاك، R f = 0.19، راجع الخطوة 1.4).
ملاحظة: خلال هذا الوقت، الخليط سوف تصبح الأصفر يزداد مع السطح عرضية. - إخماد رد فعل بصب المخلوط في المثلج ح 2 س (18 مل). استخراج فورا محلول مائي مع مل 18 من الفصل 2 Cl 2 في قمع سيباراتوري 100 مل. استخراج الطبقة المائية على الأقل 2 مرات إضافية مع Cl 2 (9 مل في كل) الفصل 2-
- الجاف للمواد العضوية المجمعة أكثر ~ 100 مغ مجسو 4 ل 2 دقيقة تصفية والتركيز الحل بتبخر دوارة العائد من البترول الخام، والأصفر. الحرارة حمام الماء إلى 30 درجة مئوية خلال التبخر لإزالة حمض الخليك المتبقية.
ملاحظة: البروتوكول يمكن أن يكون مؤقتاً هنا في حالة فسخ المجمع في الفصل 2 Cl 2 وحل المخزنة في الظلام في 2-8 درجة مئوية.
تنقية - مجمع النفط الخام من كروماتوغرافيا العمود (راجع الخطوة 1.5) باستخدام هلام السليكا كمرحلة ثابتة و 100% أتاك ك الوينت 16.
تنبيه: مركز التغذية الوطني ونيتروساميديس ذات الصلة يجب أن تعالج الرعاية كما أنها يفترض أن تكون المواد المسببة للسرطان البشري- - حل مجمع نقية في كدكل 3 واستخدام الرنين المغناطيسي النووي (راجع الخطوة 1، 2) التأكد من الهيكل وتحديد مولاريتي لهذا الحل 17. تخزين هذا الحل في الظلام في 2-8 درجة مئوية إلى حين الحاجة.
ملاحظة: هذا الحل سوف تستخدم كعنصر التحكم الإيجابي في الفحص في المختبر (الخطوة 3، 5). أطياف الرنين المغناطيسي النووي والتحولات الكيميائية متاحة في "المعلومات الداعمة". - بحل مجلس التغذية الوطني الخالص، تأكيد دقة الأصل الجماهيري وتحديد الجماهير أيون المنتج عن طريق التسريب المباشر على مطياف كتلة عالية الدقة (نظام إدارة الموارد البشرية) تحت معلمات هو موضح في الخطوات 1-3 و 4، 3-
ملاحظة: سيتم استخدام الجماهير المنتج للكشف عن هذا المركب في في المختبر الأيض المقايسة (الخطوة 4، 3)-
3. P450 النيتروسامين مثال في المختبر حضانة
- إزالة P450 2A6 باكولوسوميس ونظام حية-نادف-تجديد 10 مم NADP + "الحل الأسهم" من ثلاجة-80 درجة مئوية، والسماح لهم بالذوبان في الجليد. متى مذاب، تضعف من باكولوسوميس والتجدد نادف النظام 1:10 و 01:50، على التوالي، في أنبوب واحد 1 مل مع 0.5 س رد فعل المخزن المؤقت. وبالمثل، إضافة 3 ميكروليتر من NADP + "الحل الأوراق المالية" إلى ميكروليتر 97 0.5 س رد فعل المخزن المؤقت-
ملاحظة: NADP + حساسة للضوء. يبقى هذا الحل يحميها الالتفاف في الحاوية في رقائق الألومنيوم. حلول إنزيم حساسة لدورات تجميد أذاب؛ يحد هذا بدوره لا يزيد عن 2. تحضير مختبرين اللازمة للتجارب المقبلة. - لكل حضانة، إضافة 50 ميكروليتر الحل إنزيم (التي تحتوي على 5 بمول P450) إلى 1 مل أنبوب ميكروليتر 40 تحتوي على 4 ميكرومترات NNN الحل مع "رد فعل المخزن المؤقت". قبل احتضان هذا الخليط الجديد لمدة 2 دقيقة عند 37 درجة مئوية باستخدام حمام مائي ثم قم بإضافة 10 ميكروليتر من المخفف NADP + الحل. تبني نظام كامل 1-30 دقيقة في 37 درجة مئوية.
ملاحظة: باستخدام فواصل زمنية دقيقة 5 مرات الحضانة (مثلاً 5، 10، 15 دقيقة، إلخ) وستوفر دورة وقت تشكيل نيتروساميدي كافية. - بعد الوقت المطلوب من الحضانة، آرو بأول ميكروليتر 10 إضافة 3.0 زنسو ن 4 وثم 10 ميكروليتر من 3.0 ن Ba(OH) 2- وسيشكل هذا الحل وترسبات بيضاء دوامة. الطرد المركزي العينة في 8000 غ س ل 4 دقيقة بيليه ترسبات.
ملاحظة: الإجراء يجب أن لا أتوقف عند هذه الخطوة كما حدت نيتروساميديس شكلت الاستقرار في المحاليل. قد يؤدي إيقاف مؤقت طويل السلبيات الكاذبة. - "الماصة؛" المادة طافية على الفور وتحليل 2 ميكروليتر اللوني السائل التأين نانوليكتروسبراي إيجابية عالية الدقة tandem الكتلي (LC-أبرز مؤشر الأمن القومي +--نظام إدارة الموارد البشرية/مرض التصلب العصبي المتعدد، خطوات 4.1-4.3).
- لمراقبة إيجابية إينكوباتيونس، تتبخر قاسمة تحتوي على 100 فمول المركب إلى حل مجلس التغذية الوطني في أنبوب 1 مل تحت تيار ن 2. هذه القنينة، إضافة إلى نظام الإنزيم الكامل من الخطوة 3.2 والمضي قدما كما هو موضح للخطوات 3.3-3.4.
- لمراقبة سلبية إينكوبيشنز، إجراء التجربة كوصف (خطوات 3.2-3.4) باستثناء استبدال 50 ميكروليتر الإنزيم الحل مع 0.5 س رد فعل المخزن المؤقت-
4. معلمات مثال للكشف عن نيتروساميدي طريق LC-أبرز مؤشر الأمن القومي +-نظام إدارة الموارد البشرية/MS
المكونات- "لقانون العمل"، تطبيق الانحدار المتعدد الخطوة التالية في الخطوة 4، 2 لنظام أوبلك باستخدام التجاري، ومعبأة اليد 18 C18 (5 ميكرومترات)، ميكرومترات 100 مم × 75، 15 ميكرومترات الفوهة عمود الشعرية.
- استخدام 5 مم NH 4 OAc بالمذيبات وميكن كمذيب ب، تحميل العينة على العمود بتشغيل نسبة 5% ب في 1 ميكروليتر/دقيقة من 0-5 دقيقة ومن ثم تباطؤ معدل التدفق إلى 0.3 ميكروليتر/دقيقة بعد ذلك. تشغيل التالية، متدرجة من 5 إلى 20% ب ما يزيد على 4 دقيقة، تليها من منحدر إلى 55% ب أكثر من 10 دقيقة، ومن ثم إعادة الموازنة إلى 5% ب
- أداء LC-أبرز مؤشر الأمن القومي +--نظام إدارة الموارد البشرية/ماجستير في أوربيتراب لتق. رصد لمركز التغذية الوطني بمسح كامل وتجزئة 2 مللي ثانية. إجراء فحص كامل بدقة تبلغ 000 60 واستخراج كتلة الأصل دقيقة (192.07670) في تسامح شامل 5 جزء في المليون. استخدام MS 2 تجزئة لعزل أيونات الأصل (2.0 اتحاد المغرب العربي) وجزء من الناجمة عن تصادم الانفصال (CID) مع طاقة اصطدام من 25 eV، القرار 15000، والمسح الضوئي الوقت للسيدة 30 استخراج الجماهير دقيقة لأيونات المنتج من مركز التغذية الوطني (m/z 192 m/z 134.04739 و 162.07874) في تسامح شامل 5 جزء في المليون-
Access restricted. Please log in or start a trial to view this content.
النتائج
استناداً إلى أعمال أبيض وآخرون. وكان 19، نوركوتينيني فينولات إلى مركز التغذية الوطني نظيفة وعالية الغلة (80-92%) لإنتاج معيار للتجربة في المختبر . حصل على الأدلة الهيكلية لرد فعل ناجح من تحليلات سبيكتروسكوبيك بما في ذلك 1ح-الرنين المغناطيسي النوو...
Access restricted. Please log in or start a trial to view this content.
Discussion
توضيح استقلاب نيتروسامينيز عنصر حاسم للتفاهم على السرطنة. منذ الفسفرة المعنية P450s والأنزيمات الاستقلابية الأخرى متعددة الأشكال، مواصلة تحديد تطبيق هذه المعارف عالية المخاطر الأفراد1،4يمكن أن يحتمل. البيانات الجديدة تشير إلى أن زيادة أكسدة α-هيدروكسينيتر?...
Access restricted. Please log in or start a trial to view this content.
Disclosures
الكتاب ليس لها علاقة بالكشف عن.
Acknowledgements
هذه الدراسة كانت تدعمها منحة لا. كاليفورنيا--81301 من معهد السرطان الوطني. ونحن نشكر بوب كارلسون للمساعدة التحريرية، الدكتور بيتر فيﻻلتا وشون مينغ للمساعدة الكتلي في "الموارد المشتركة الكيمياء الحيوية التحليلية" لمركز السرطان الماسونية، والدكتور آدم ت. زارث والدكتور ميشال ك. أنا لمناقشاتهم قيمة والمدخلات. الموارد المشتركة في الكيمياء التحليلية معتمد جزئيا من الوطنية سرطان معهد السرطان مركز دعم منحة CA-77598
Access restricted. Please log in or start a trial to view this content.
Materials
| Name | Company | Catalog Number | Comments |
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
References
- Rom, W. N., Markowitz, S. Environmental and Occupational Medicine. , 4th ed, Wolters Kluwer/Lippincott Williams & Wilkins. 1226-1239 (2007).
- Preussmann, R., Stewart, B. W. Chemical Carcinogens, ACS Monograph 182. Searle, C. E. 2, 2nd ed, American Chemical Society. 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R. Chemical Carcinogens. ACS monograph 173. Searle, C. E. , American Chemical Society. 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. ACS Symposium Series. 101, American Chemical Society. 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5'(1')iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochemistry. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N'-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N'-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).
Access restricted. Please log in or start a trial to view this content.
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved