Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Un método General para la detección de formación de Nitrosamide en el metabolismo In Vitro de nitrosaminas por Cytochrome P450s
En este artículo
Resumen
Α-hidroxilación de nitrosaminas carcinógenas por cytochrome P450s es la aceptada vía metabólica que produce intermediarios DNA-perjudiciales, causantes de mutaciones. Sin embargo, nuevos datos indican más a nitrosamidas puede oxidarse. Describimos un general método para la detección de nitrosamidas producido en vitro del citocromo P450-catalizada metabolismo de nitrosaminas.
Resumen
N-nitrosaminas son un grupo bien establecido de carcinógenos ambientales, que requieren la oxidación de la citocromo P450 que exhiben actividad. El mecanismo aceptado de activación metabólica implica la formación de α-hydroxynitrosamines que se descomponen espontáneamente a los agentes alquilantes del ADN. Acumulación de daño en el ADN y las mutaciones que en última instancia puede conducir a cáncer. Nueva evidencia indica que α-hydroxynitrosamines puede estar más oxidado a nitrosamidas processively por cytochrome P450s. Porque nitrosamidas son generalmente más estables que la α-hydroxynitrosamines y también pueden alkylate ADN, nitrosamidas pueden desempeñar un papel en la carcinogénesis. En este informe, describimos un protocolo general para la evaluación de producción de nitrosamide catalizada por la P450 metabolismo de en vitro del citocromo de nitrosaminas. Este protocolo utiliza un acercamiento general a la síntesis de las nitrosamidas pertinentes y un en vitro citocromo P450 metabolismo ensayo usando spectrometry total en tándem cromatografía líquido-nanospray ionización alta resolución para la detección. Este método detecta N′- nitrosonorcotinine como un metabolito menor de N′- nitrosonornicotine en el estudio de ejemplo. El método tiene alta sensibilidad y selectiva debido a la precisa detección de masa. Aplicación de este método a una amplia variedad de sistemas de nitrosaminas-citocromo P450 ayudará a determinar la generalidad de esta transformación. Porque cytochrome P450s son polimórficos y varían en la actividad, una mejor comprensión de la formación de nitrosamide puede ayudar en la evaluación del riesgo individual de cáncer.
Introducción
N-nitrosaminas son una gran clase de carcinógenos en la dieta, productos del tabaco y el medio ambiente en general; también puede ser formados endógenamente en el cuerpo humano1. Más de 300 N -nitroso compuestos han sido probados y > 90% fueron evaluado como carcinógeno en modelos animales de2,3. Para exhibir su carcinogenicidad, estos compuestos deben ser primero activados por cytochrome P450s1,2,3. La investigación muestra que citocromo P450s oxida fácilmente nitrosaminas a α-hydroxynitrosamines (figura 1), que son compuestos altamente reactivos con vidas medias de ~ 5 s antes de descomponerse espontáneamente a alkyldiazohydroxides. Este último puede alkylate la DNA después de la pérdida de H2O y N2. Aductores de ADN resultante, si sin reparar, puede causar mutaciones que, en caso de crítica onco - o genes supresores de tumores, cáncer desarrollo1. Por esta razón mucho esfuerzo se ha expendido para adquirir un conocimiento completo de las rutas metabólicas, aductores de ADN y aguas abajo metabolitos de la oxidación de la citocromo P450 de nitrosaminas carcinógenas. Este conocimiento tiene aplicación potencial en de evaluación de riesgo individual de cáncer4.
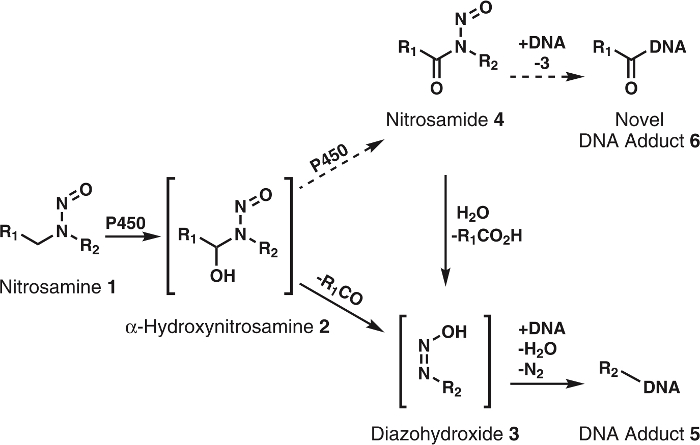
Figura 1: General y metabolismo propuesto de nitrosaminas.
Nitrosaminas (1) se oxidan por P450s a α-hydroxynitrosamines (2) que se descomponen espontáneamente a alkyldiazohydroxides (3). Estos compuestos pueden atar a la DNA para formar que aductos de ADN. Se presume que 2 más son oxidados por P450s nitrosamidas 4. Estos pueden enlazar directamente ADN para formar nuevo ADN aductos o ser hidrolizada a 3 para formar que aductos de ADN conocida. R1 y R2 representan cualquier grupo Alquilo. Haga clic aquí para ver una versión más grande de esta figura.
Aunque la hipótesis de α-hydroxynitrosamine esté solidamente apoyada por datos de amplia, hay algunas inconsistencias; uno importante es la vida media corta de α-hydroxynitrosamines5,6. Es conocido que estos compuestos se producen en la membrana del retículo endoplásmico y posteriormente alkylate la DNA nuclear. Teniendo en cuenta la vida de unos pocos segundos, es desconcertante cómo estos intermedios sobreviven el viaje requiere sin embargo el citosol. Una hipótesis es que una porción de la α-hydroxynitrosamines se processively oxidan a nitrosamidas7,8, que son bastante estables en comparación9. Esto probablemente ocurre vía retención de α-hydroxynitrosamines en el sitio de activo de citocromo P450. Precedente para este tipo de oxidación se ha visto con nicotina10, alcoholes11y12,de alkylnitrosamines simple13. Además, nitrosamidas son carcinógenos de acción directa2,3. Basado en su reactividad9, estos compuestos se creen producir ADN aductos idénticas a las derivadas de α-hydroxynitrosamines junto con el nuevo, inexplorado ADN aductos (figura 1). Así, esta hipótesis no sólo explica el transporte a través del citosol, sino también la formación de ADN dañar productos.
En este artículo se describe un protocolo general para la evaluación del en vitro del citocromo P450-mediated conversión de nitrosaminas en nitrosamidas. La conversión previamente divulgada de N′- nitrosonornicotine (NNN) N′- nitrosonorcotinine (NNC) por citocromo P450 2A6 es presentada como un ejemplo14. Aplicación del presente Protocolo para una amplia gama de sistemas de la enzima substrato ayudará a determinar la importancia de nitrosamidas en metabolismo total de nitrosamina.
Access restricted. Please log in or start a trial to view this content.
Protocolo
1. materiales y procedimientos generales de
- sintetizar NNN como describió anteriormente 15. Obtener norcotinine, P450 2A6 Baculosomes, sistema de regeneración de NADPH, tampón de reacción de 0.5 x y todos los otros productos químicos o solventes de fuentes comerciales en grado reactivo.
- Espectros de RMN de registro en un espectrómetro de 500 MHz. Cambios químicos de informe como partes por millón (ppm). Utilizar picos de solvente residual como referencias internas para 1 H-NMR (7,26 ppm CDCl 3) y 13 C-RMN (77,2 ppm CDCl 3).
Nota: Pico partir utiliza las siguientes abreviaturas: s = camiseta, d = doblete, dd = doblete de Dobletes, dt = doblete de tríos, dq = doblete de cuartetos, ddd = doblete de doblete de Dobletes y m = multiplet. - Realizar espectrometría de masas de alta resolución (HRMS) para compuestos seleccionados en un LTQ Orbitrap Velos y los datos como m/z.
- Uso polygram cubierto primero placas de Silicagel TLC (40 mm x 80 mm, 0,2 mm de espesor) con indicador fluorescente de 254 nm para cromatografía en capa fina (TLC). Visualizar las placas de TLC por la irradiación UV lámpara.
- Realizar la cromatografía flash sobre un 60 Å, gel de silicona de 70-150 mesh usando una columna de vidrio de 1,5 cm x 15 cm.
2. Preparación del control positivo de nitrosamide (N ′-nitrosonorcotinine, NNC)
- seco, en un horno durante la noche (16 h, ~ 140 ° C), 25 mL, matraz de fondo redondo que contiene una barra de agitación magnética. En la mañana, frío el matraz bajo una secuencia de N 2 mientras con un burbujeador de aceite para mantener el flujo de N 2 tarifa bajo una burbuja por segundo.
Nota: Después de enfriar, las precauciones para mantener el matraz bajo N 2 no son necesarias. - En una campana de humos, añadir norcotinine (31,8 mg, 0.196 mmol), anhídrido acético (5 mL) y ácido acético (1 mL) al matraz enfriado. Revuelva la mezcla continuamente mientras se enfría a 0 ° C con un baño de hielo de agua.
PRECAUCIÓN: Anhídrido acético y el ácido acético están corrosivos. - NaNO agregar 2 (33,3 mg, 0.483 mmol) en una porción y agitar continuamente la mezcla para monitorear el avance de la reacción por el TLC de 2,5 h. (100% EtOAc, R f = 0.19, consulte el paso 1.4).
Nota: Durante este tiempo, la mezcla se convertirá en cada vez más amarilla con burbujas ocasionales. - Calmar la reacción vertiendo la mezcla en helado de H 2 O (18 mL). Extraer inmediatamente la solución acuosa con 18 mL de CH 2 Cl 2 en un matraz de 100 mL. Extraer la capa acuosa de al menos 2 veces más con CH 2 Cl 2 (9 mL).
- Seco de la materia orgánica combinada más de ~ 100 mg MgSO 4 min 2 filtro y concentrar la solución por evaporación rotatoria para producir un aceite crudo, amarillo. El baño de agua a 30 ° C de calor durante la evaporación para eliminar el ácido acético residual.
Nota: El protocolo puede ser una pausa aquí si el compuesto se disuelve en la solución almacenada en la oscuridad a 2-8 ° C. y CH 2 Cl 2 - Purificar el crudo compuesto por cromatografía en columna (ver paso 1.5) usando gel de sílice como fase estacionaria y 100% EtOAc como eluyente 16.
PRECAUCIÓN: NNC y nitrosamidas relacionados deben ser manejados con cuidado ya que se supusieron que son carcinógenos humanos. - Disolver el compuesto puro en CDCl 3 y usar NMR (vea el paso 1.2) para confirmar la estructura y determinar la molaridad de esta solución 17. Almacenar esta solución en la oscuridad a 2-8 ° C hasta que sea necesario.
Nota: Esta solución se usará como control positivo en el ensayo en vitro (paso 3.5). Espectros de RMN y los cambios químicos están disponibles en la información de apoyo a. - Con una solución pura de NNC, confirmar la exacta masa los padres y determinar masas de productos ion por infusión directa en un espectrómetro de masas de alta resolución (HRMS) bajo los parámetros descritos en los pasos 1.3 y 4.3.
Nota: Las masas de producto se utilizarán para la detección de este compuesto en el en vitro ensayo metabolismo (paso 4.3).
3. Una nitrosamina-P450 en vitro incubación de ejemplo
- Retire P450 2A6 Baculosomes, sistema de regeneración de NADPH Vivid y 10 mM NADP + solución madre de un congelador de-80 ° C y dejarlos descongelar en el hielo. Una vez descongelado, diluir la Baculosomes y sistema de regeneración de NADPH 1:10 y 1:50, respectivamente, en un tubo solo 1 mL con 0,5 reacción X Buffer. Del mismo modo, agregar 3 μL de NADP + solución Stock a 97 μL de 0, 5 X Buffer de reacción.
Nota: NADP + es sensible a la luz. Mantener esta solución protegida envolviendo su envase en papel de aluminio. Soluciones enzimáticas son sensibles a los ciclos hielo-deshielo; Esto se limita a no más de 2 ciclos. Preparar alícuotas según sea necesario para futuros experimentos. - Para cada incubación, añada 50 μL de solución enzimática (contiene 5 pmol de P450) a un 1 mL del tubo que contiene 40 μL de solución NNN μM 4 hecho con tampón de reacción. Incubar previamente esta nueva mezcla por 2 min a 37 ° C utilizando un baño de agua y añadir 10 μL de la solución diluida de NADP +. Incubar el sistema completo para 1-30 min a 37 ° C.
Nota: Con intervalos de 5 min para tiempos de incubación (por ejemplo 5, 10, 15 minutos, etc.) le proporcionará un curso de tiempo suficiente de nitrosamide formación. - Después del tiempo de incubación deseados, apagar primero agregando 10 μl de 3.0 N ZnSO 4 y luego 10 μL de 3.0 N Ba(OH) 2. Vórtice que se forman de esta solución y un precipitado blanco. Centrifugar la muestra a 8000 x g por 4 min a pellet precipitado.
Nota: El procedimiento no debe detener en este paso como las nitrosamidas formados tienen una limitada estabilidad en soluciones acuosas. Largas pausas pueden resultar en falsos negativos. - Inmediatamente pipetear el sobrenadante y analizar 2 μL por cromatografía líquida positiva nanoelectrospray-ionización alta resolución tandem espectrometría de masas (LC-NSI +-HRMS/MS, los pasos 4.1-4.3).
- Para incubaciones de control positivo, se evapora una alícuota que contenga 100 fmol de solución NNC sintetizada en un tubo 1 mL bajo una corriente de N 2. A este frasco, agregue el sistema enzimático completo del paso 3.2 y proceder como se describe por pasos 3.3-3.4.
- Para incubaciones de control negativo, realizar el experimento descrito (pasos 3.2-3.4) excepto sustituir los 50 μL enzima solución con 0,5 X buffer de reacción.
4. Ejemplo de parámetros para la detección de nitrosamide por LC-NSI +-HRMS/MS
componente de- de la LC, el siguiente gradiente de múltiples paso en el paso 4.2 se aplican a un sistema UPLC con un comercial, repleto de mano 18 C18 (5 μm), 100 mm x 75 μm, columna capilar de 15 μm orificio.
- Usando 5 mM NH 4 OAc como A solvente y MeCN como disolvente B, carga la muestra en la columna ejecutando 5% B a 1 μL/min. de 0 - 5 min y luego desacelerando la tasa de flujo de 0,3 μL/min luego. A continuación, ejecute un gradiente de 5 a 20% B durante 4 min, seguido de una rampa hasta el 55% B más de 10 minutos y luego volver a equilibrar al 5% B.
- Realizar la LC-NSI +-HRMS/MS en un LTQ Orbitrap. Monitor para la NNC por análisis completo y MS 2 fragmentación. Realizar un análisis completo con una resolución de 60.000 y extraer la masa exacta del padre (192.07670) en una tolerancia de masa de 5 ppm. Uso MS 2 fragmentación aislar padre iones (2,0 amu) y fragmento de colisión-inducida disociación (CID) con una energía de colisión de 25 eV, resolución de 15.000, y análisis de tiempo de 30 Sra. extraer las masas exactas de los iones producto de NNC (m/z 192 m/z 134.04739 y 162.07874) en una tolerancia de masa de 5 ppm.
Access restricted. Please log in or start a trial to view this content.
Resultados
Basado en la obra de blanco et al. 19, norcotinine era nitrosados a NNC limpia y en alto rendimiento (80-92%) para producir un estándar para el experimento en vitro . Se obtuvo evidencia estructural para una reacción exitosa de análisis espectroscópico como 1H-NMR, 13C-RMN, COSY, HSQC (información de apoyo) junto con HRMS que confirmó el padre de masa [M + H]+ de 5 ppm de los valor teórico (
Access restricted. Please log in or start a trial to view this content.
Discusión
Dilucidar el metabolismo de las nitrosaminas es un elemento fundamental para entender su carcinogenicidad. Puesto que el implicado cytochrome P450s y otras enzimas metabólicas son polimórficos, aplicación de este conocimiento potencialmente podría identificar individuos de alto riesgo1,4. Nueva información indica más oxidación de α-hydroxynitrosamines, los principales metabolitos presumidos de nitrosaminas implicados en el atascamiento de la DNA, nitrosam...
Access restricted. Please log in or start a trial to view this content.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este estudio fue apoyado por subvención no. CA-81301 del Instituto Nacional de cáncer. Agradecemos a Bob Carlson para asistencia editorial, Dr. Peter Villalta y Xun Ming para asistencia de espectrometría de masas en el recurso de compartido de bioquímica analítica del centro Masónico de cáncer y el Dr. Adam T. Zarth Dr. Anna K. Michel por sus valiosos debates y de entrada. El recurso de compartido de bioquímica analítica es parcialmente apoyado por nacional cáncer Institute cáncer centro apoyo beca CA-77598
Access restricted. Please log in or start a trial to view this content.
Materiales
| Name | Company | Catalog Number | Comments |
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
Referencias
- Rom, W. N., Markowitz, S. Environmental and Occupational Medicine. , 4th ed, Wolters Kluwer/Lippincott Williams & Wilkins. 1226-1239 (2007).
- Preussmann, R., Stewart, B. W. Chemical Carcinogens, ACS Monograph 182. Searle, C. E. 2, 2nd ed, American Chemical Society. 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R. Chemical Carcinogens. ACS monograph 173. Searle, C. E. , American Chemical Society. 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. ACS Symposium Series. 101, American Chemical Society. 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5'(1')iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochemistry. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N'-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N'-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).
Access restricted. Please log in or start a trial to view this content.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados