Method Article
تصوير ATG9A ، وهو بروتين غشائي متعدد الامتدادات
In This Article
Summary
يصف هذا البروتوكول الطرق المختلفة التي يمكن أن تساعد في دراسة بيولوجيا ATG9A ، بما في ذلك التألق المناعي متبوعا بتحليل الصور ، واعتبارات التعبير المفرط العابر ، والتحقيق في حالة الغليكوزيل ATG9A باستخدام اللطخة الغربية.
Abstract
الالتهام الذاتي هو مسار محفوظ للغاية تستخدمه الخلية للحفاظ على التوازن ، وتدهور العضيات التالفة ، ومكافحة مسببات الأمراض الغازية ، والبقاء على قيد الحياة في الحالات المرضية. مجموعة من البروتينات ، تسمى بروتينات ATG ، تشتمل على آلية الالتهام الذاتي الأساسية وتعمل معا في تسلسل هرمي محدد. حسنت الدراسات في السنوات الأخيرة معرفتنا بمسار الالتهام الذاتي. في الآونة الأخيرة ، تم اقتراح أن حويصلات ATG9A تقع في قلب الالتهام الذاتي ، لأنها تتحكم في التوليف السريع من جديد لعضية تسمى البلعمة. أثبتت دراسة ATG9A أنها صعبة ، لأن ATG9A هو بروتين عبر الغشاء ، وهو موجود في مقصورات غشائية مختلفة. على هذا النحو ، فإن فهم الاتجار بها هو عنصر مهم لفهم الالتهام الذاتي. هنا ، يتم تقديم طرق مفصلة يمكن استخدامها لدراسة ATG9A ، وعلى وجه الخصوص ، توطينها باستخدام تقنيات التألق المناعي ، والتي يمكن تقييمها وقياسها. كما يتم تناول مخاطر الإفراط في التعبير العابر. يعد التوصيف الصحيح لوظيفة ATG9A وتوحيد التقنيات لتحليل الاتجار بها أمرا بالغ الأهمية لزيادة توصيف الأحداث التي تحكم بدء الالتهام الذاتي.
Introduction
ATG9A هو البروتين الوحيد عبر الغشاء لآلية الالتهام الذاتي الأساسية ويتم الاتجار به بين جولجي وحجرة حويصلة ATG9A الخلوية ، ويمر عبر المقصورة الاندوسومية1. بعد أن كان غامضا منذ فترة طويلة ، تم وصف ATG9A مؤخرا بأنه يعمل على أنه تدافع الدهون ، لأنه يوازن الدهون عبر طبقات الغشاءالثنائية 2,3. من الواضح الآن أن ATG9A يقع في الجزء العلوي من التسلسل الهرمي في تكوين البلعمة الذاتية ، وبالتالي فإن دراسته حيوية لفهم الالتهام الذاتي 4,5. على هذا النحو ، تم اقتراح حويصلات ATG9A مؤخرا على أنها "بذرة" البلعمة الذاتية 6,7. ومع ذلك ، فقد أظهرت الدراسات السابقة أن ATG9A يتفاعل بشكل عابر فقط مع البلعمة الذاتية المشكلة في خطوات مختلفة من نضجه ولا يندمج في غشاء الالتهام الذاتي6،8،9،10،11. وبالتالي ، هناك حاجة إلى مزيد من التحقيقات للكشف تماما عن الدور والوظائف المتعددة المحتملة ل ATG9A في تكوين البلعمة الذاتية. ومع ذلك ، لا يمكن حل التناقض بين النماذج الحالية والبيانات السابقة إلا من خلال التجارب المستهدفة التي تعالج الاتجار ب ATG9A باستخدام مناهج كمية تم التحقق من صحتها وعلامات داخل الخلايا.
هناك العديد من الأدوات المستخدمة لدراسة ATG9A ، ولكل منها مزايا وعيوب ، واستخدام هذه الأدوات معقد بسبب بنية ATG9A ووظيفتها الجزيئية والاتجار الخلوي2،8،12. يشكل ATG9A متجانسا ، وهو جليكوزيلاتي ، ويتم تهريبه في جميع أنحاء الخلية إلى مقصورات مثل جولجي ، والإندوسومات ، وغشاء البلازما13,14. نظرا لمسار الرحلة المعقد ، هناك العديد من التحديات في تفسير القراءات مثل تشتت ATG9A من Golgi على علاجات أو محفزات محددة (مثل المغذيات وتجويع المصل). ATG9A دينامية للغاية من حيث الاتجار الحويصلي. في الواقع ، تم تعريف الحويصلات المحتوية على ATG9A على أنها حجرة ATG9A في سياق الالتهام الذاتي الناجم عن الجوع. تتفاعل حجرة ATG9A ، التي تشكلها هذه الحويصلات الديناميكية ، بشكل عابر مع العديد من العضيات داخل الخلايا8،15،16،17. يجب أن تساعد التقنيات الموصوفة هنا ، بما في ذلك التألق المناعي والتصوير الحي ومقايسات الجليكوزيل ، في اكتشاف وفهم بيولوجيا ATG9A. على وجه الخصوص ، ستساعد الأساليب الموضحة في هذه المقالة في معالجة الأسئلة المتعلقة بالتوطين إلى مقصورات خلوية محددة والتفاعلات مع شركاء بروتين محددين و / أو مقصورات غشائية. نظرا لأن المجال الأساسي المحفوظ الكارهة للماء ATG9A (مجال PFAM PF04109) له طوبولوجيا فريدة ودورات ATG9A بين عدة مقصورات غشائية ، يجب أن يكون الباحثون على دراية ببعض المزالق والتحف عند الإفراط في التعبير عن ATG9A بشكل عابر ، بما في ذلك ، على سبيل المثال لا الحصر ، الاحتفاظ بالشبكة الإندوبلازمية (ER). قد تنشأ مشكلات محتملة أخرى بسبب اختلال البروتين ، أو التجميع الاصطناعي في ظروف النمو العادية ، أو عدم كفاية الكشف عن المقصورة الحويصلية بسبب بروتوكولات النفاذية دون المستوى الأمثل للتألق المناعي.
عند تصوير ATG9A الداخلي ، يجب توخي الحذر في إعداد العينة والحصول على الصور لضمان جودة التحليل الكمي اللاحق والتفسير الصحيح للبيانات. يجب أن يؤدي الجمع بين التقنيات الموضحة في هذه المقالة مع الأساليب الكيميائية الحيوية القياسية (مثل الترسيب المناعي أو التجارب المنسدلة غير الموصوفة هنا) إلى تحسين فهمنا لوظيفة ATG9A. تهدف مجموعة الأدوات التجريبية هذه إلى مساعدة الباحثين الجدد على التنقل في بعض المقايسات المطلوبة لتحديد وظيفة ATG9A في نظامهم البيولوجي.
Protocol
جميع الكواشف المستخدمة في هذه الدراسة متاحة تجاريا ، باستثناء تركيبات الحمض النووي ATG9A والجسم المضاد STO-215 محلي الصنع (انظر جدول المواد) ، والتي تتوفر عند الطلب. تستند أدوات التحليل الموصوفة هنا إلى برمجيات مفتوحة المصدر (FIJI/ImageJ)18.
1. ثقافة الخلية
- الحفاظ على الخلايا HEK293A في دورق T150 المعالج بزراعة الأنسجة إلى التقاء 80٪ -90٪ في DMEM عالي الجلوكوز (وسط النسر المعدل من Dulbecco) المكمل ب 10٪ FBS (مصل بقري الجنين) و 4 mM L-glutamine (انظر جدول المواد). احتضان الخلايا عند 37 درجة مئوية في حاضنة زراعة الأنسجة الرطبة عند 10٪ CO2.
ملاحظة: تستخدم الخلايا HEK293A في هذه الدراسة ، حيث تتمتع باستجابة قوية للالتهام الذاتي الكنسي عند تجويع الأحماض الأمينية ، والتي يتم اكتشافها ، على وجه الخصوص ، من خلال زيادة LC3 1،9،19 الدهنية المرتبطة بالغشاء ، وهي مناسبة للتصوير. - مرور الخلايا عن طريق استنشاق الوسط من القارورة باستخدام ماصة مصلية. اغسل الخلايا مرة واحدة ب 15 مل من 1x PBS (محلول ملحي مخزن بالفوسفات) أو محلول مشابه قبل إضافة 2 مل من محلول Trypsin-EDTA (حمض الإيثيلين ديامينيترايتيك) لفصل الخلايا. اجمع الخلايا المنفصلة التي تحتوي على 8 مل من DMEM ، وقم بإرجاع عدد من الخلايا بحيث يتم الوصول إلى التقاء 80٪ -90٪ بعد 2 أيام للتجارب الموضحة هنا.
2. تلطيخ داخلي من ATG9A
- خلايا HEK293A البذور (أو الخلايا المفضلة) على أغطية زجاجية معقمة رقم 1.5 موضوعة في صفيحة مكونة من 24 بئرا بحيث تكون ~ 80٪ متقاربة في اليوم التالي. هذا يعطي عادة 7 × 104 خلايا / بئر في 500 ميكرولتر من DMEM.
ملاحظة: بالنسبة للخلايا HEK293A أو غيرها من خطوط الخلايا غير الملتصقة بشكل فضفاض ، يجب طلاء أغطية الغطاء ببولي-د-ليسين عند 0.1 مجم / مل في ماء منزوع الأيونات. أضف 500 ميكرولتر من poly-D-lysine (انظر جدول المواد) في الجزء العلوي من أغطية الغطاء الموضوعة في الآبار لمدة 10 دقائق في درجة حرارة الغرفة (RT) ، متبوعة بثلاث غسلات بالماء منزوع الأيونات وغسلة أخيرة في DMEM. انتقل إلى بذر الخلايا بعد الطلاء ، واحرص على انتشارها بالتساوي في طبق الثقافة. - عالج الخلايا وفقا للظروف التجريبية المحددة (أي الجوع لمدة 2 ساعة في EBSS [محلول إيرل المتوازن للملح]).
ملاحظة: تركيبة EBSS هي 1 جم / لتر D-glucose ، 6.8 جم / لتر كلوريد الصوديوم ، 0.4 جم / لتر KCl ، 0.151 جم / لتر CaCl 2.2H 2 O ، 0.2 جم / لتر مللي مول MgSO 4.7H 2 O ، 0.124 جم / لتر NaH 2 HPO4.2H 2 O ، و 2.2 جم /لتر NaHCO 3 (انظر جدول المواد) مذاب في الماء المقطر. - نضح الوسط ، واستبدله بعناية ب 500 ميكرولتر من محلول الفورمالديهايد 4٪ في PBS المكمل ب 0.1 mM CaCl 2 و 0.1 mM MgCl2 لمدة 20 دقيقة في RT لإصلاح الخلايا.
- نضح محلول الفورمالديهايد 4٪ من كل بئر ، واستبدله ب 500 ميكرولتر من PBS. كرر خطوة الغسيل هذه ثلاث مرات. لا تدع أغطية الغطاء تجف أو تبقى بدون سائل.
- قم بإخماد مجموعات الألدهيد الحرة باستخدام 500 ميكرولتر من محلول 50 mM NH4Cl في PBS لمدة 10 دقائق في RT.
- نضح PBS ، واستبدله ب 500 ميكرولتر من محلول ديجيتونين 50 ميكروغرام / مل في PBS (محلول مخزون 1 مجم / مل في ماء منزوع الأيونات ، انظر جدول المواد) لمدة 5 دقائق في RT لاختراق الخلايا.
- استنشاق محلول الديجيتونين من كل بئر ، واستبدله ب 500 ميكرولتر من PBS. كرر خطوة الغسيل هذه ثلاث مرات.
- قم بشفط PBS من كل بئر ، واستبدله ب 500 ميكرولتر من محلول الحجب (5٪ BSA [ألبومين مصل الأبقار] مخفف في PBS) لمدة 30 دقيقة في RT.
- نضح محلول الحجب ، واستبدله ب 500 ميكرولتر من برنامج تلفزيوني.
- باستخدام الملقط ، اجمع أغطية الغطاء من البئر ، وقم بإزالة محلول PBS الزائد بعناية باستخدام مناديل الأنسجة الرقيقة أو ورق ترشيح السليلوز ، وضع برفق كل غطاء ، جانب الخلية لأسفل ، على قطرة 50 ميكرولتر من محلول الأجسام المضادة الأولية (على سبيل المثال ، الهامستر الأرمني 14F2 المخفف إلى 0.9 ميكروغرام / مل في محلول 1٪ BSA / PBS ، انظر جدول المواد). احتضان في غرفة مرطبة لمدة 1 ساعة في RT.
ملاحظة: لسهولة التعامل ، يمكن وضع قطرات محلول الأجسام المضادة على ورقة من فيلم اللدائن الحرارية ذاتية الختم (انظر جدول المواد) داخل حاوية أخرى بدلا من وضعها مباشرة على سطح صلب. - اجمع قسائم الغطاء باستخدام الملقط ، وبعد تصريف محلول الأجسام المضادة الأولية الزائدة برفق باستخدام مناديل الأنسجة الرقيقة ، استبدل أغطية الغطاء (جانب الخلية لأعلى) في اللوحة المكونة من 24 بئرا ، واغسلها ثلاث مرات باستخدام برنامج تلفزيوني.
- كرر الخطوة 2.10. باستخدام الملقط ، اجمع أغطية الغطاء من كل بئر ، واستنزف بعناية PBS الزائد باستخدام مناديل الأنسجة الرقيقة ، وضع برفق كل غطاء (جانب الخلية لأسفل) على قطرة 50 ميكرولتر من محلول الأجسام المضادة الثانوي المخفف 1: 1,000 في محلول BSA / PBS بنسبة 1٪ (على سبيل المثال ، Cy3 Goat Anti-Armenian Hamster IgG ، الذي يحتوي على الحد الأدنى من التفاعل المتبادل مع الأبقار والبشرية ، بروتينات مصل الفأر والأرانب والجرذان ، انظر جدول المواد). احتضان في غرفة مرطبة لمدة 1 ساعة في RT.
ملاحظة: اختياري: يمكن استخدام علامة الهيكل الخلوي بالإضافة إلى الجسم المضاد الثانوي لتحليل الصورة اللاحق (على سبيل المثال ، Alexa Fluor 647 Phalloidin المخفف 1: 1,000 ، انظر جدول المواد). لسهولة التعامل ، يمكن وضع قطرات محلول الأجسام المضادة على ورقة من فيلم مانع للتسرب داخل حاوية أخرى بدلا من وضعها مباشرة على سطح صلب. - اجمع قسائم الغطاء باستخدام الملقط ، وبعد تصريف محلول الأجسام المضادة الثانوي الزائد ، ضع أغطية الغطاء في لوحة 24 بئرا (جانب الخلية لأعلى) واغسلها ثلاث مرات باستخدام 500 ميكرولتر PBS.
- باستخدام الملقط ، اجمع قسائم الغطاء ، واستنزف بعناية PBS الزائد باستخدام مناديل الأنسجة الرقيقة ، وضع برفق كل غطاء (جانب الخلية لأسفل) على قطرة 50 ميكرولتر من محلول Hoechst 1: 4,000 (Hoechst 33342) في PBS. احتضان في غرفة الرطوبة لمدة 5 دقائق في RT.
ملاحظة: لسهولة التعامل ، يمكن وضع قطرات محلول الأجسام المضادة على ورقة من فيلم مانع للتسرب داخل حاوية أخرى بدلا من وضعها مباشرة على سطح صلب. - اجمع أغطية الغطاء باستخدام الملقط ، وبعد تصريف محلول Hoechst الزائد برفق باستخدام مناديل الأنسجة الرقيقة ، استبدل أغطية الغطاء في اللوحة المكونة من 24 بئرا ، واغسلها ثلاث مرات باستخدام PBS ومرة واحدة بالماء غير المتأين (500 ميكرولتر لكل غسلة).
- قم بتصريف الماء الزائد منزوع الأيونات بعناية باستخدام مناديل الأنسجة الرقيقة ، وضع برفق كل غطاء (جانب الخلية لأسفل) على قطرة 10-20 ميكرولتر من محلول التركيب (انظر جدول المواد) المرقط على شريحة مجهرية للتألق المناعي ، وتجنب تكوين فقاعات الهواء.
ملاحظة: يحتوي وسيط التركيب المستخدم هنا على نفس معامل الانكسار مثل زيت الغمر ويتصلب بعد بضع ساعات عند RT أو طوال الليل عند 4 درجات مئوية. يمكن استخدام حلول التثبيت غير المتصلبة ، ولكن يجب توخي الحذر لإغلاق غطاء الغطاء بطلاء الأظافر. - قم بإزالة محلول التثبيت الزائد عن طريق الشفط ، واترك العينات تجف أثناء الاستلقاء بشكل مسطح في RT طوال الليل في الظلام ، إما في حامل منزلق أو مغطى بورق الألمنيوم.
3. الحصول على الصور
- قم بتشغيل المجهر متحد البؤر. افتح برنامج التصوير (انظر جدول المواد) لبدء إعداد التقاط الصور.
- في علامة التبويب الوظيفة ، حدد العدسة الموضوعية Plan-Apochromat 63x/1.4 Oil DIC M27 لالتقاط الصور لتحليلها.
- في علامة التبويب وظيفة الاكتساب ، قم بتشغيل أشعة الليزر المناسبة في منطقة الليزر في لوحة التحكم (الأرجون ، الصمام الثنائي - 405-30 ، DPSS 561-10 ، و HeNe633).
- في منطقة إعداد التصوير في لوحة التحكم، قم بإنشاء أربعة مسارات، مع كل مسار يتوافق مع قناة واحدة، لإجراء اكتساب متسلسل.
- اضبط الدقة المناسبة للصور في نافذة وضع الاستحواذ . اضبط الدقة على 1024 × 1024 (حجم الإطار)، وحدد عمق بت 16 بت.
- لكل قناة ، اضبط طاقة الليزر وكسبها للحصول على إشارة جيدة بدون وحدات بكسل مشبعة ، مما قد يعيق تحليل كثافة الصورة. باستخدام الزر Live ، اضبط مستوى إخراج الليزر والكسب (رئيسي).
ملاحظة: يوصى باستخدام خيار مؤشر النطاق لاكتشاف وحدات البكسل المشبعة. حافظ على طاقة الليزر بين 1٪ و 10٪ والكسب (الرئيسي) أقل من 850 لتجنب ضوضاء الخلفية. - في منطقة القنوات في لوحة التحكم ، اضبط نفس فتحة الثقب لكل قناة ، مع مراعاة 1 وحدة تهوية (AU) للقناة ذات الطول الموجي الأعلى.
- احصل على 10 حقول عشوائية تحتوي على كميات مماثلة من الخلايا (20-30 خلية لكل حقل). سيوفر الحصول على 100-200 خلية لكل حالة قوة جيدة لتحليل الصور لاحقا.
4. تحليل صورة تشتت ATG9A
- قم بتنزيل برنامج فيجي من الإنترنت (انظر جدول المواد). افتح الصورة باستخدام FIJI بالنقر فوق المكونات الإضافية > التنسيقات الحيوية > BioFormat Importer.
- انقر فوق تحليل > تعيين القياسات ، وحدد متوسط القيمة الرمادية في نافذة القياسات لتحليل الكثافة.
- انقر فوق > الصورة Color > Split Channels ، وافصل القنوات إلى ثلاث صور (علامة Golgi ، الهيكل الخلوي ، إشارة ATG9A).
- انتقل إلى Image > ضبط عتبة > ، وحدد عتبة في القناة المقابلة لعلامة Golgi.
- انقر فوق تحرير > التحديد > إنشاء تحديد ، وقم بإنشاء تحديد من الصورة الثنائية.
- انتقل إلى تحرير > التحديد > إضافة إلى المدير > إعادة تسمية (Golgi) ، واحفظ التحديد في مدير عائد الاستثمار ، وأعد تسميته إلى Golgi.
- انقر فوق Image > ضبط عتبة > ، وحدد عتبة في القناة المقابلة لعلامة الهيكل الخلوي لتحديد محيط الخلية.
- انتقل إلى تحرير > التحديد > إنشاء تحديد، وإنشاء تحديد من الصورة الثنائية.
- انقر فوق تحرير > التحديد > إضافة إلى المدير > إعادة تسمية (الإجمالي) ، واحفظ التحديد في مدير عائد الاستثمار ، وأعد تسميته الإجمالي.
- حدد الصورة المقابلة لتلطيخ ATG9A.
- في تحليل > القياس ، قم بتطبيق عائد الاستثمار Golgi بالنقر فوقه ، وقم بقياس شدة منطقة Golgi .
- انقر فوق تحليل > قياس ، وقم بتطبيق إجمالي عائد الاستثمار بالنقر فوقه ، وقم بقياس شدة المنطقة الإجمالية.
- كرر الإجراء في جميع الصور ، واحفظ النتائج كملفات .csv ، وقم بمعالجة البيانات باستخدام الصيغة التالية:
معدل تشتت ATG9A = كثافة جولجي / الكثافة الكلية
5. تصوير الخلايا الحية لتركيبات ATG9A
- HEK293A الخلايا (أو الخلايا المفضلة) في 2 مل من الوسط في طبق زراعة الأنسجة 60 مم بحيث تصل إلى ~ 65٪ -70٪ التقاء في اليوم التالي ؛ هذا يعطي عادة 1 × 10 6-2 × 106 خلايا.
- في اليوم التالي ، قم بإعداد Lipofectamine: يمزج الحمض النووي (أو كاشف نقل الحمض النووي البديل المناسب ، انظر جدول المواد) على النحو التالي:
- اعتمادا على كفاءة التعبير الإنشائي ، قم بتخفيف 0.5-2 ميكروغرام من الحمض النووي البلازميد إلى 100 ميكرولتر من وسط مناسب خال من المصل ، واخلط المحلول برفق عن طريق السحب لأعلى ولأسفل. احتضان الخليط لمدة 5 دقائق في RT.
ملاحظة: بنية الحمض النووي البلازميد خاصة بالتجربة. يمكن للباحثين إما الاستنساخ بأنفسهم أو الحصول على من المؤلفين عند الطلب. - تمييع كاشف نقل Lipofectamine 2000 بنسبة 3: 1 Lipofectamine: DNA إلى 100 ميكرولتر من وسط مناسب خال من المصل واخلط المحلول برفق عن طريق السحب لأعلى ولأسفل. احتضن هذا المزيج لمدة 5 دقائق في RT.
- امزج كلا الحلين معا عن طريق سحب الإصبع برفق لأعلى ولأسفل والحضانة لمدة 20 دقيقة في RT.
- اعتمادا على كفاءة التعبير الإنشائي ، قم بتخفيف 0.5-2 ميكروغرام من الحمض النووي البلازميد إلى 100 ميكرولتر من وسط مناسب خال من المصل ، واخلط المحلول برفق عن طريق السحب لأعلى ولأسفل. احتضان الخليط لمدة 5 دقائق في RT.
- أضف مزيج Lipofectamine: DNA إلى كل لوحة زراعة خلية تحتوي على 4 مل من وسط النمو ، وقم بهز اللوحة برفق ذهابا وإيابا لتوزيع المزيج بالتساوي. احتضان الخلايا عند 37 درجة مئوية في حاضنة زراعة الخلايا الرطبة بنسبة 10٪ CO2.
- استبدل الوسط بوسط نمو جديد بعد 4 ساعات من النقل ، واحتضان الخلايا عند 37 درجة مئوية في حاضنة زراعة الخلايا الرطبة عند 10٪ CO2 طوال الليل.
- في اليوم التالي ، قم بالتنقيب ، عد ، وإعادة زرع الخلايا على أطباق مستنبتة مناسبة للفحص المجهري للخلايا الحية (أطباق الاستزراع مع غطاء زجاجي رقم 1.5 ، انظر جدول المواد). البذور 0.4 × 10 6-0.7 × 106 خلايا على الأطباق للوصول إلى ~ 60٪ -75٪ التقاء على غطاء في وقت التصوير.
ملاحظة: يوصى بالطلاء باستخدام poly-D-lysine ، كما هو موضح في الخطوة 2.1 ، للخلايا HEK293A. - في اليوم التالي (48 ساعة بعد النقل) ، صور الخلايا.
6. التحقيق في حالة الجليكوزيل ل ATG9A
- HEK293A البذور الخلايا (أو الخلايا المفضلة) في طبق زراعة الأنسجة 10 سم بحيث تصل إلى ~ 80٪ التقاء في اليوم التالي إذا كنت تخطط للتحقيق في ATG9A الداخلي ، والذي يعطي عادة 1.5 × 10 6-2.5 × 106 خلايا في 10 مل. بدلا من ذلك ، قم بزرع الخلايا بحيث تصل إلى ~ 65٪ -70٪ التقاء إذا تم نقل تركيبات ATG9A ، والتي تعطي عادة 1 × 10 6-1.5 × 106 خلايا في 10 مل.
- عالج الخلايا ب 100 ميكروغرام / مل سيكلوهيكساميد (CHX ، انظر جدول المواد) أو السيارة في اليوم التالي. احتضان لمدة 24 ساعة (أو حتى نقطة زمنية مطلوبة).
- قم بإزالة الخلايا من الحاضنة ، واستنشق الوسط ، وضعها على الجليد. استبدله ب 5 مل من الثلج البارد 1x PBS. افصل الخلايا فعليا عن الطبق باستخدام مكشطة خلوية ، وقم بامتصاص محلول خلية PBS في أنبوب مخروطي القاع سعة 15 مل. جهاز طرد مركزي عند 800 × جم لمدة 5 دقائق عند 4 درجات مئوية لتكوير الخلايا.
- نضح المادة الطافية ، وإعادة تعليق الخلايا في ~ 100 ميكرولتر (اعتمادا على حجم حبيبات الخلية) من محلول تحلل TNTE المثلج البارد (1٪ Triton ، 150 mM NaCl ، 20 mM Tris-HCl ، pH 7.4 ، 0.5 mM EDTA) تستكمل بأقراص كوكتيل مثبطات الأنزيم البروتيني (انظر جدول المواد) ، ونقلها إلى أنبوب طرد مركزي دقيق 1.5 مل.
- احتضان المحللة على الثلج لمدة 15 دقيقة. بعد ذلك ، يقوم جهاز الطرد المركزي بتحليل 20000 × جم لمدة 10 دقائق عند 4 درجات مئوية لترسب النوى والحطام غير القابل للذوبان ، ونقل المادة الطافية إلى أنبوب طرد مركزي دقيق جديد.
- حدد تركيز البروتين في المحللة باستخدام طريقة برادفورد20 ومقياس الطيف الضوئي الذي يمكنه القياس بطول موجي 595 نانومتر.
- تطبيع كميات البروتين ، والجمع بين 16 ميكرولتر من المحللة (التي لا تحتوي على أكثر من 100 ميكروغرام من البروتين في المجموع) مع 5x PNGase F (الببتيد: N-glycosidase F) العازلة وفقا لتعليمات الشركة المصنعة قبل إضافة 1 ميكرولتر من إنزيم PNGase F (انظر جدول المواد). احتضان وفقا لتعليمات الشركة المصنعة PNGase F.
- أضف حجما من 3x Laemmli عينة عازلة لتحقيق تركيز 1x ، واحتضانها عند 65 درجة مئوية لمدة 5 دقائق قبل التحميل للرحلان الكهربائي باستخدام جل Tris-acetate لزيادة فصل البروتينات. نقل البروتينات من الجل إلى غشاء مناسب (أي PVDF [بولي فينيليدين ثنائي فلوريد]) باستخدام بروتوكولات اللطخة الغربية القياسية21 (انظر جدول المواد).
ملاحظة: سيؤدي غلي العينات عند 95 درجة مئوية إلى تجميع ATG9A ، مما يقلل من اكتشاف ATG9A. - قم بإجراء اللطخة الغربية باستخدام أجسام مضادة محددة ل ATG9A (الجسم المضاد STO-215 ، المنتج داخليا1) (انظر جدول المواد). اترك قسم الوزن الجزيئي الأعلى للغشاء غير مقطوع لتصور الأنواع ذات الوزن الجزيئي الأعلى ATG9A.
النتائج
ATG9A هو بروتين عبر الغشاء مرتبط بالعديد من مقصورات الغشاء داخل الخلايا8،17،22،23،24. في الظروف القاعدية ، يتم توطين ATG9A بشكل أساسي في شبكة Trans-Golgi (TGN) ، كما يتضح من التألق المناعي للبروتين الداخلي والتداخل مع GM130 ، علامة cis-Golgi (الشكل 1A) ، وكذلك في الحويصلات الصغيرة التي تتداخل جزئيا مع حجرة إعادة التدوير الداخلية (ERC) 23. يمكن الكشف عن توطين ATG9A في Golgi باستخدام بروتوكولات التألق المناعي المختلفة. ومع ذلك ، فإن الجزء الحويصلي من ATG9A ، وكذلك تغييره في التوطين ، ولا سيما الزيادة في التجمع الحويصلي ، استجابة لمحفزات محددة مثل المغذيات وتجويع المصل ، يمكن أن يكون متغيرا تماما في شدته ويصعب تصوره باستخدام أساليب التصوير التقليدية. تسمى النسبة بين ATG9A المترجمة في Golgi و ATG9A المترجمة إلى جزء حويصلي معدل تشتت ATG9A. للكشف عن التغيرات في معدل تشتت ATG9A ، على سبيل المثال عند علاج EBSS ، والذي يستخدم لاستنفاد كل من المصل والأحماض الأمينية ، فإن علامة Golgi مثل GM130 أو TGN46 وعلامة الهيكل الخلوي مثل Phaloidin ، التي تلطخ محيط الخلية25 ، مفيدة لتحديد تشتت ATG9A بسهولة (الشكل 1B). الأهم من ذلك ، لا يمكن تفسير تحليل متوسط نسبة التألق إلا على أنه مقياس مقارن بين الظروف وليس كمعدل ثابت للانتشار. تعتمد النسبة بين المقصورات بشكل كبير على العوامل البيولوجية وغير البيولوجية مثل خط الخلية المستخدم أو جودة التلوين أو طرق العتبة المطبقة (الشكل 1 ب). لهذا السبب ، يحتاج الباحث إلى إعداد خط أنابيب قادر على اكتشاف تخصيب ATG9A Golgi في ظروفه التجريبية المحددة ثم توسيع التحليل بنفس المعلمات ليشمل جميع الصور في المجموعة المراد تحليلها. يتم عرض الصور الثنائية التمثيلية والمناطق المختارة لتحليل متوسط مضان ATG9A كدليل في الشكل 1B.
يحتوي ATG9A على العديد من المجالات عبر الغشاء محاطة بمجالين طرفيين N- و C مرنين نسبيا وغير منظمين ، يشمل تسلسل C-terminal ما يقرب من نصف البروتين12. الأهم من ذلك ، يمكن أن يتأثر نمط توطين ATG9A المفرط التعبير بنهاية البروتين التي يتم تمييزها (الشكل 2A). على وجه الخصوص ، عند استخدام أنظمة التعبير العابر ووضع علامات على ATG9A مباشرة على نهايته N بعلامة فلورية (على سبيل المثال ، eGFP أو mRFP أو مشتقاتها) ، يمكن اختراق توطين Golgi جزئيا ، مع رؤية إثراء أقل في الظروف القاعدية (أي التغذية) ، بينما لا تزال حويصلات ATG9A مرئية بسهولة (الشكل 2A). يبدو أن وضع علامات على ATG9A على نهايته C يحفز قليلا مجموعات إيجابية أكبر من GFP يمكن تجميعها. أخيرا ، تظهر نسخة أحادية من mRFP-ATG9A أيضا مجموعات فلورية مماثلة من الحويصلات وتلطيخ جولجي الصغير في الخلايا المفرطة التعبير (الشكل 2 أ).
يطوى ATG9A في غشاء ER قبل أن يتم تهريبه إلى حويصلات Golgi و ATG9A. أثناء إقامته في ER ، يتم تعديل ATG9A بواسطة جليكان مرتبط ب N على Asparagine 99 ، ثم عند الوصول إلى Golgi ، يكتسب جليكان معقد وناضج مرتبط بN 1,14. يمكن الكشف عن هذا التعديل عن طريق الجليكوزيل من خلال اللطخة الغربية من خلال ظهور شريط مزدوج14. تمشيا مع توطينه داخل الخلايا ، فإن معظم ATG9A الداخلي يؤوي جليكان معقد مرتبط ب N ، وبالتالي ، فإن نطاق الوزن الجزيئي الأعلى هو السائد ، مع وجود نطاق ضعيف منخفض الوزن الجزيئي مرئي أيضا (الشكل 2B). يمكن رؤية وجود نطاق مزدوج بسهولة عند استخدام المواد الهلامية Tris-acetate لتحسين دقة البروتينات ذات الوزن الجزيئي العالي (الشكل 2B ، التحكم ، t = 0). عندما يخضع البروتين الداخلي لعلاج PNGase F (الببتيد: N-glycosidase F) ، والذي يزيل معظم الجليكان المعقد المرتبط ب N ، يعمل البروتين كشريط واحد (الشكل 2B ، PNGase F ، t = 0). لذلك ، يمكن استخدام حالة الجليكوزيل المرتبطة ب N ل ATG9A كوكيل لمراقبة خروج ATG9A من ER إلى Golgi ، وهو ما ينعكس في النسبة النسبية بين النطاقين.
عندما يتراكم نقل mRFP-ATG9A بشكل عابر ، يتراكم البروتين المفرط التعبير في البداية في ER ، ربما لأن آلية الاتجار غير قادرة على طي وحركة كل ATG9A ، ويكون نطاق الوزن الجزيئي المنخفض هو السائد (الشكل 2C ، التحكم t = 0). والجدير بالذكر أنه بعد 24 ساعة من التعبير عن mRFP-ATG9A ، هناك توزيع متساو تقريبا بين النطاقين العلوي والسفلي ، مما يشير إلى أن تجمع mRFP-ATG9A ينتقل إلى Golgi (الشكل 2C ، التحكم ، t = 24). إذا تم التعامل مع الخلايا مع cycloheximide (CHX) ، الذي يمنع تخليق البروتين دي نوفو 26 ، يمكن توضيح طي وخروج ATG9A من ER. نظرا لأن البروتين الداخلي مطوي ، وجليكوزيلاتي ، ومقيم في جولجي ، فإن العلاج باستخدام CHX لا يغير بشكل كبير نسبة نطاقات الوزن الجزيئي الأدنى والأعلى (الشكل 2 ب ، التحكم). ومع ذلك ، باستخدام التعبير العابر ل mRFP-ATG9A ، يعزز علاج CHX تراكم نطاق الوزن الجزيئي الأعلى (الشكل 2C ، التحكم ، CHX t = 24). ينهار نطاق mRFP-ATG9A ذو الوزن الجزيئي الأعلى في النطاق السفلي بعد العلاج باستخدام PNGase F (الشكل 2C ، PNGase F ، t = 24). تظهر هذه البيانات أن البروتين الداخلي يكتسب بسرعة الجليكان الناضج ، كما ينعكس في غلبة نطاق الوزن الجزيئي الأعلى ، ولا تؤثر مطاردة CHX على نسبة النطاقات المزدوجة (الشكل 2 ب). في حالة mRFP-ATG9A بشكل عابر ، تحفز معالجة CHX تراكم النطاق العلوي ، مما يشير إلى أنه يتم الحصول على جليكان أكثر نضجا عندما يطوى تجمع ER ويخرج من ER إلى Golgi (الشكل 2C).
يمكن أن تكون إضافة رابط بين تسلسل ATG9A وعلامات الفلورسنت مفيدة في تعزيز توطين فسيولوجي أكثر وتهريب البروتين. يساعد دمج تسلسل 3x-FLAG (24 حمضا أمينيا) بين فلوروفور N-terminal و ATG9A البروتين المفرط التعبير على التصرف بشكل مشابه للبروتين الداخلي (الشكل 3). في الواقع ، يتزامن mCherry-3xFLAG-ATG9A مع علامة Golgi GM130 في ظروف التغذية (الشكل 3A). الأهم من ذلك ، يتم الحفاظ على هذا التوطين والمقصورة الحويصلية ATG9A بمرور الوقت ، مما يسمح بالدراسة الزمانية المكانية للاتجار ب ATG9A (الشكل 3B).
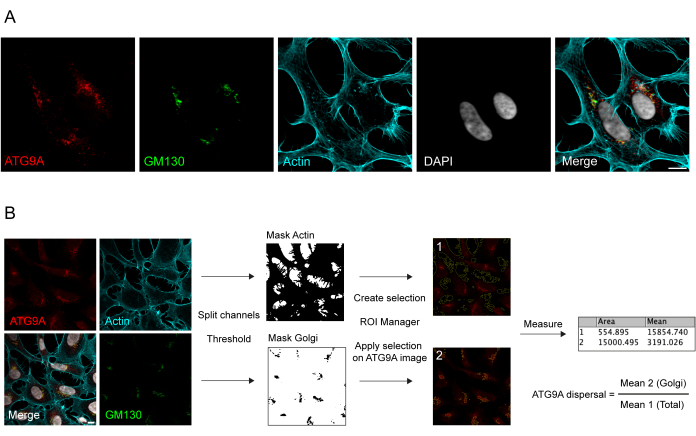
الشكل 1: تحليل الصورة لتوطين ATG9A الداخلي. (أ) صورة التألق المناعي التمثيلي ل ATG9A الداخلي (أحمر) ، GM130 كعلامة جولجي (أخضر) ، و Phalloidin لتصور الهيكل الخلوي للأكتين (سماوي). شريط المقياس = 10 ميكرومتر. (ب) سير عمل تحليل الصورة لتحديد جزء ATG9A الداخلي المنشأ الذي يتمركز في منطقة جولجي. شريط المقياس = 10 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
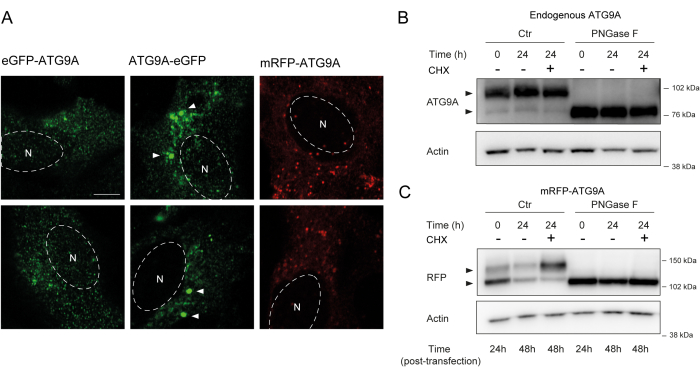
الشكل 2: تحليل تركيبات ATG9A الموسومة بالفلورسنت عن طريق التوطين والجليكوزيل. (أ) eGFP N-taged ATG9A أقل تموقعا في جولجي ويتواجد بشكل أساسي في الحويصلات. يعرض eGFP C الموسوم طرفيا ATG9A المجاميع داخل الخلية (يتم تمييز بعض الأمثلة برؤوس أسهم بيضاء ؛ eGFP-ATG9A و ATG9A-eGFP باللون الأخضر). mRFP N-taged ATG9A أقل موضعية في جولجي ويتواجد بشكل أساسي في الحويصلات. يشير N إلى الموقع التقريبي لنواة الخلية ، ويكون mRFP-ATG9A باللون الأحمر. شريط المقياس = 5 ميكرومتر. (B) يظهر ATG9A الداخلي المنشأ كشريطين عند تحليلهما بواسطة اللطخة الغربية (رؤوس الأسهم): شريط علوي (جليكان معقد مرتبط ب N) وشريط سفلي (لا يوجد جليكان ناضج مرتبط ب N). لا يؤثر العلاج بالسيكلوهيكساميد (CHX) على النسبة بين النطاقين العلوي والسفلي. العلاج مع PNGase F يسبب اختفاء الشريط العلوي. (ج) بعد الانتقال العابر ل ATG9A الموسوم ب mRFP في خلايا HEK293A ، يظهر شريطان بارزان على اللطخة الغربية (رؤوس الأسهم). العلاج مع PNGase F يسبب اختفاء الشريط العلوي. يؤدي العلاج باستخدام CHX بعد النقل إلى زيادة الجليكوزيل حيث يتم تهريب مجموعة ATG9A المنقولة من ER إلى Golgi. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
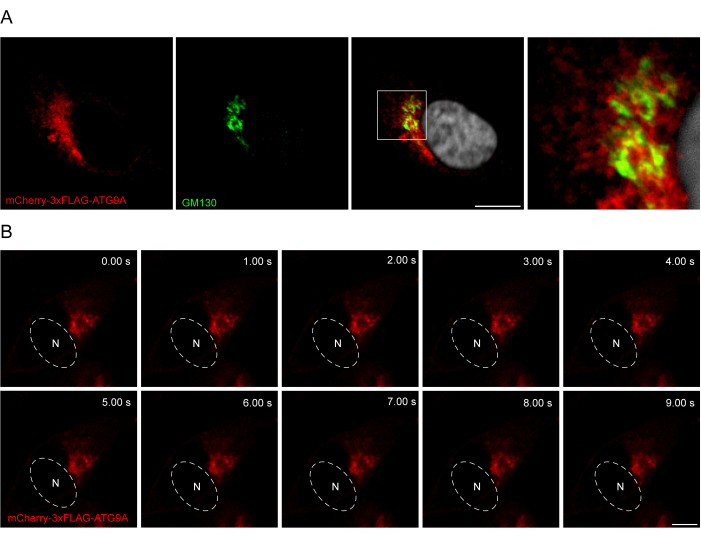
الشكل 3: تحليل توطين mCherry-3xFLAG-ATG9A عن طريق التألق المناعي والتصوير الحي. (أ) تجارب التألق المناعي لخلايا HEK293A التي تفرط في التعبير العابر عن mCherry-3xFLAG-ATG9A وملطخة بعلامة جولجي GM130. شريط المقياس = 10 ميكرومتر. mCherry-3xFLAG-ATG9A باللون الأحمر ، وعلامة GM130 Golgi باللون الأخضر. ب: المونتاج من تجارب التصوير الحي في خلايا HEK293A التي تفرط في التعبير العابر عن mCherry-3xFLAG-ATG9A. يشير N إلى الموقع التقريبي للنواة. الإطار الزمني = 1 إطارا في الثانية. شريط المقياس = 10 ميكرومتر. mCherry-3xFLAG-ATG9A باللون الأحمر. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
Discussion
توضح هذه الدراسة الأدوات المختلفة التي يمكن استخدامها للتحقيق في توطين ATG9A. أولا ، تصف هذه الدراسة كيف يمكن تصور ATG9A عن طريق التألق المناعي وكيف يمكن قياس ذلك. ثانيا ، تتم مقارنة الاستراتيجيات التي يمكن استخدامها لوضع علامة ATG9A بعلامة الفلورسنت للتصور في الخلايا الثابتة أو الحية. أخيرا ، يصف هذا العمل كيفية التحقيق في حالة الغليكوزيل الخاصة ب ATG9A واستخدامها لتحديد ما إذا كان ATG9A قد خرج من ER وتم الاتجار به عبر Golgi.
فيما يتعلق بتوصيف توطين ATG9A الداخلي عن طريق التألق المناعي ، يجب توخي الحذر مع طرق التثبيت والنفاذية المستخدمة في التجربة. وفقا للإجراءات القياسية الموصوفة هنا ، يعد تثبيت بارافورمالدهيد إلى جانب نفاذية الديجيتونين ظروفا جيدة لتصور كل من الحويصلات الإيجابية ATG9A المرتبطة بجولجي و ATG9A7. جنبا إلى جنب مع التثبيت والنفاذية ، فإن توقيت الحضانة مع حل الأجسام المضادة الأولية أمر بالغ الأهمية أيضا. لقد لاحظنا ، ولكن لم يتم توثيقه ، أن التركيزات الأعلى من محلول الأجسام المضادة الأولية وأوقات الحضانة الأطول يمكن أن تؤدي إلى زيادة تحريف في تلطيخ جولجي ل ATG9A ، مما يضر في النهاية باكتشاف إعادة توزيع ATG9A إلى مقصورات الغشاء الأخرى. بالإضافة إلى ذلك ، نظرا لوجود ATG9A في العديد من المقصورات داخل الخلايا1،13،17،22،23،24،27،28 ، فمن المهم استخدام علامات غشاء محددة ، جنبا إلى جنب مع ATG9A ، لتحديد مكان وجود ATG9A. تم استخدام العديد من الأساليب في الماضي لتحديد توطين ATG9A ، بما في ذلك معامل ارتباط بيرسون للتمركزالمشترك 29. ومع ذلك ، فإن التداخل الجزئي ل ATG9A مع Golgi والمقصورة الحويصلية المميزة يؤدي إلى عدد كبير من القيم المتطرفة للبكسل ، مما قد يؤدي إلى تحيز تفسير معامل الارتباط. لهذا السبب ، يفضل اتباع نهج أكثر بساطة يعتمد على نسبة متوسط التألق في الجزأين المراد تحليلهما ، وهذا النهج أقل حساسية لتباين كل خلية على حدة. لمزيد من المعلومات حول تحليل الصور من خلال الفحص المجهري ، يتم توجيه القراء إلى هذا الكتاب الفصل30.
عند التحقيق في حالة الجليكوزيل ل ATG9A ، من المهم اختيار المواد الهلامية لتشغيل البقع الغربية. بالنسبة لهذا البروتوكول ، يفضل استخدام 3٪ -8٪ من المواد الهلامية Tris-acetate لأنها توفر أعلى دقة للبروتينات الأكبر ، ولكن يمكن أيضا استخدام تركيبات هلام بديلة أو مخازن مؤقتة توفر فصلا جيدا للبروتينات عالية الوزن الجزيئي. يمكن للمجرب ضمان الفصل الأقصى للبروتينات عن طريق زيادة وقت الرحلان الكهربائي.
عند تحضير العينات لتصور ATG9A على اللطخة الغربية ، يجب الحرص على عدم غلي العينات بعد إضافة المخزن المؤقت Laemmli ؛ يؤدي الغليان عند 95 درجة مئوية إلى تكوين مجاميع ATG9A ، وبالتالي ، لا يهاجر ATG9A بكفاءة إلى الجل1. يوصى بتسخين العينات عند 65 درجة مئوية لمدة 5 دقائق27.
عادة ما تؤدي المستويات العالية من النقل إلى تراكم أعلى ل ATG9A في غرفة الطوارئ ، بينما تساعد مستويات التعبير المعتدلة على التوطين الفسيولوجي للبروتين. من الناحية القصصية ، غالبا ما تساعد أوقات الحضانة البالغة 72 ساعة بدلا من 48 ساعة في تقليل عناصر توطين ER. والجدير بالذكر أن mRFP-ATG9A يمكنه الإبلاغ بدقة عن الاتجار ب ATG9A ووظيفته إذا تم التحكم في المستويات من خلال مستويات التعبير أو باستخدام خطوط خلوية مستقرة8،9،22،27.
يمكن استخدام فشل مجموعة من ATG9A المبالغة في التعبير في الحصول على جليكان ناضج مرتبط ب N كقراءة للاتجار ب ATG9A المضطرب. عند تحور أو حذف مناطق معينة من ATG9A ، هناك خطر زيادة الاحتفاظ ب ER ، مما قد يؤدي إلى الفشل في الحصول على جليكان ناضج مرتبط ب N ، وبالتالي ، نطاق ATG9A أسرع هجرة على اللطخة الغربية. يجب على الباحثين الذين يعملون مع تركيبات ATG9A المقطوعة التحقق من الاحتفاظ ب ER وحالات الجليكوزيل وتوطين Golgi.
بالنسبة لتصوير الخلايا الحية ل ATG9A ، يوفر مجهر Airyscan ، الذي يعتمد على وظيفة Airyscan السريعة ، دقة مثالية تبلغ عادة حوالي 120 نانومتر. للحصول على دقة التعريب ، تكون معدلات الإطارات التي تبلغ حوالي 1-2 إطار في الثانية (fps) في وضع الدقة الفائقة مثالية اعتمادا على عدد القنوات التي يتم تصويرها. يمكن أيضا استخدام المجاهر متحدة البؤر المماثلة التي يمكنها التصوير بسرعة عالية لتصوير حويصلات ATG9A. ومع ذلك ، تجدر الإشارة إلى أن سرعة التصوير يمكن أن تؤثر بشكل مباشر على اكتشاف الأحداث ، وبالتالي تؤثر على تفسير البيانات.
باختصار ، تصف البروتوكولات المقدمة طرقا لتحديد وتوصيف توطين ATG9A عن طريق التألق المناعي ، والفحص المجهري للخلايا الحية ، وحالة الجليكوزيل الخاصة به. يمكن أن تساعد هذه البروتوكولات الباحثين الذين يعملون مع ATG9A وتساعد في تجنب بعض المزالق.
Disclosures
تعمل S.A.T. في المجلس الاستشاري العلمي لشركة Casma Therapeutics.
Acknowledgements
يشكر المؤلفون روكو دانتونو على التدقيق اللغوي لجوانب المخطوطة ، وكذلك جميع الأعضاء الحاليين والسابقين في مختبر بيولوجيا الخلية الجزيئية للالتهام الذاتي (MCBA) على المناقشات التي أدت إلى تحسين هذه البروتوكولات. تم دعم A. V.V. ، S.D.T. ، E.A. ، S.A.T ، من قبل معهد فرانسيس كريك الذي يتلقى تمويله الأساسي من أبحاث السرطان في المملكة المتحدة (CC2134) ، ومجلس البحوث الطبية في المملكة المتحدة (CC2134). تم تمويل هذا البحث كليا أو جزئيا من قبل Wellcome Trust (CC2134). لغرض الوصول المفتوح ، قام المؤلف بتطبيق ترخيص حقوق الطبع والنشر العام CC BY على أي نسخة مخطوطة مقبولة من المؤلف تنشأ عن هذا التقديم.
Materials
| Name | Company | Catalog Number | Comments |
| 24 multiwell plates | Falcon | 353047 | For tissue culture |
| 35 mm Dish | No. 1.5 Coverslip | 14 mm Glass Diameter | Uncoated | MATTEK | P35G-1.5-14-C | Cell culture dish for live-cell microscopy |
| 4x Laemmli Sample Buffer | Bio-Rad | 1610747 | |
| 60 mm tissue culture dish | Thermofisher Scientific | 10099170 | For tissue culture |
| Alexa Fluor 647 Phalloidin | Thermofisher Scientific | A22287 | Actin stain |
| anti-ATG9A antibody | home made | STO-215 | Rabbit anti N-terminal peptide ATG9A |
| anti-Rabbit IgG, peroxidase-linked | Invitrogen | 10794347/NA934-1ml | Secondary antibody for rabbit polyclonal STO-215 |
| anti-RFP antibody | Evrogen | AB233 | for Western Blot |
| ATG9A Monoclonal Antibody (14F2 8B1), Invitrogen | Invitrogen | 15232826 | Antibody for immunofluorescence |
| ATG9A-eGFP | home made | Construct which expresses tagged ATG9A | |
| Bemis Parafilm | Thermofisher Scientific | 11747487 | self-sealing thermoplastic film |
| Bio-Rad Protein Assay Dye Reagent Concentrate | Bio-Rad | 5000006 | For determining protein concentration |
| Bovine serum albumin (BSA) | Merck | 10735086001 | For blocking non-specific labelling |
| CaCl2.2H2O | / | For PBS and EBSS | |
| cOmplete Protease Inhibitor Cocktail | Roche | 11697498001 | Supplement in lysis buffer to prevent protein degradation |
| Cy3 AffiniPure Goat Anti-Armenian Hamster IgG | Jackson ImmunoResearch | 127-165-099 | Secondary antibody for i14F2 8B1 antibody for mmunofluorescence |
| Cyclohexamide | Sigma Aldrich | 66-81-9 | To stop protein translation |
| D-Glucose | / | For EBSS | |
| Digitonin | Merck | 300410 | For permeabilizing cells |
| DMEM | Merck | D6546-6x500ml | For tissue culture |
| eGFP-ATG9A | home made | Construct which expresses tagged ATG9A | |
| Fetal Bovine Serum | Gibco | 10270-106 | Supplement for DMEM for cell culture |
| FIJI (ImageJ) | / | https:/fiji.sc/ | Open source image analysis software |
| Hoechst | Thermofisher Scientific | H3570 | Stains the nucleus |
| KCl | / | For EBSS | |
| L-glutamine | Sigma | 67513 | For tissue culture |
| Lipofectamine 2000 | Invitrogen | 11668-019 | For Cell Transfection |
| LSM880 Airyscan microscope | Zeiss | / | Confocal microscopy |
| MgCl2 | / | For PBS | |
| MgSO4.7H2O | / | For EBSS | |
| Mowiol mounting solution | Millipore | 475904 | for permanent mounting glass coverslips |
| NaCl | / | For EBSS | |
| NaH2PO4.2H2O | / | For EBSS | |
| NaHCO3 | / | For EBSS | |
| NuPAGE 3 to 8%, Tris-Acetate, 1.5 mm, Mini Protein Gels | Thermofisher Scientific | EA0378BOX | for Western Blotting |
| NuPAGE MES SDS Running Buffer (20x) | Life Tech | NP0002 | for Western Blotting |
| Opti-MEM I Reduced Serum Medium | Thermofisher Scientific | 31985062 | For Cell Transfection |
| Paraformaldehyde | Agar Scientific | R1026 | For fixing cells |
| pcDNA3.1-mCherry-3xFlag-ATG9A | home made | Construct which expresses tagged ATG9A | |
| Phosphate Buffered Saline (PBS) | / | For tissue culture | |
| PNGaseF | NEB | P0710S | To remove N-linked glycans |
| Poly-D-lysine hydrobromide mol wt 70,000-150,000 | Merck | P0899 | For coating coverslips |
| Rapid PNGase F enzyme | NEB | P07105 | To remove N-linked glycans |
| RFP-ATG9A | home made | Construct which expresses tagged ATG9A | |
| Triton X-100 | Thermofisher Scientific | 13454259 | Detergent for Cell lysis |
| Trypsin-EDTA solution | Sigma | T4049 | For tissue culture |
| Whatman Filter Paper | Merck | WHA1001325 | For Western Blot and IF |
| XCell SureLock Mini-Cell Electrophoresis System | Invitrogen | EI0001 | For Western Blotting |
| Zen Black edition | Zeiss | / | Used to operate the LSM 880 |
References
- Young, A. R., et al. Starvation and ULK1-dependent cycling of mammalian Atg9 between the TGN and endosomes. Journal of Cell Science. 119, 3888-3900 (2006).
- Maeda, S., et al. lipid scrambling activity and role in autophagosome formation of ATG9A. Nature Structural & Molecular Biology. 27 (12), 1194-1201 (2020).
- Matoba, K., et al. Atg9 is a lipid scramblase that mediates autophagosomal membrane expansion. Nature Structural & Molecular Biology. 27 (12), 1185-1193 (2020).
- Mercer, T. J., Gubas, A., Tooze, S. A. A molecular perspective of mammalian autophagosome biogenesis. Journal of Biological Chemistry. 293 (15), 5386-5395 (2018).
- Yamamoto, H., Zhang, S., Mizushima, N. Autophagy genes in biology and disease. Nature Reviews: Genetics. , (2023).
- Sawa-Makarska, J., et al. Reconstitution of autophagosome nucleation defines Atg9 vesicles as seeds for membrane formation. Science. 369 (6508), (2020).
- Melia, T. J., Lystad, A. H., Simonsen, A. Autophagosome biogenesis: From membrane growth to closure. Journal of Cell Biology. 219 (6), 202002085 (2020).
- Orsi, A., et al. Dynamic and transient interactions of Atg9 with autophagosomes, but not membrane integration, are required for autophagy. Molecular Biology of the Cell. 23 (10), 1860-1873 (2012).
- Judith, D., et al. ATG9A shapes the forming autophagosome through Arfaptin 2 and phosphatidylinositol 4-kinase IIIbeta. Journal of Cell Biology. 218 (5), 1634-1652 (2019).
- Karanasios, E., et al. Autophagy initiation by ULK complex assembly on ER tubulovesicular regions marked by ATG9 vesicles. Nature Communications. 7, 12420 (2016).
- Koyama-Honda, I., Itakura, E., Fujiwara, T. K., Mizushima, N. Temporal analysis of recruitment of mammalian ATG proteins to the autophagosome formation site. Autophagy. 9 (10), 1491-1499 (2013).
- Guardia, C. M., et al. Structure of human ATG9A, the only transmembrane protein of the core autophagy machinery. Cell Reports. 31 (13), 107837 (2020).
- Soreng, K., et al. SNX18 regulates ATG9A trafficking from recycling endosomes by recruiting Dynamin-2. EMBO Reports. 19 (4), e44837 (2018).
- Staudt, C., Gilis, F., Boonen, M., Jadot, M. Molecular determinants that mediate the sorting of human ATG9A from the endoplasmic reticulum. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1863 (9), 2299-2310 (2016).
- Knaevelsrud, H., Carlsson, S. R., Simonsen, A. SNX18 tubulates recycling endosomes for autophagosome biogenesis. Autophagy. 9 (10), 1639-1641 (2013).
- Takahashi, Y., et al. The Bif-1-Dynamin 2 membrane fission machinery regulates Atg9-containing vesicle generation at the Rab11-positive reservoirs. Oncotarget. 7 (15), 20855-20868 (2016).
- Imai, K., et al. Atg9A trafficking through the recycling endosomes is required for autophagosome formation. Journal of Cell Science. 129 (20), 3781-3791 (2016).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- van Vliet, A. R., et al. ATG9A and ATG2A form a heteromeric complex essential for autophagosome formation. Molecular Cell. 82 (22), 4324-4339 (2022).
- Kielkopf, C. L., Bauer, W., Urbatsch, I. L. Bradford assay for determining protein concentration. Cold Spring Harbor Protocols. 2020 (4), 102269 (2020).
- Kurien, B. T., Scofield, R. H. Validating antibody specificities for immunohistochemistry by protein blotting. Methods in Molecular Biology. 2593, 21-33 (2023).
- Lamb, C. A., et al. TBC1D14 regulates autophagy via the TRAPP complex and ATG9 traffic. EMBO Journal. 35 (3), 281-301 (2016).
- Longatti, A., et al. TBC1D14 regulates autophagosome formation via Rab11- and ULK1-positive recycling endosomes. Journal of Cell Biology. 197 (5), 659-675 (2012).
- Ravussin, A., Brech, A., Tooze, S. A., Stenmark, H. The phosphatidylinositol 3-phosphate-binding protein SNX4 controls ATG9A recycling and autophagy. Journal of Cell Science. 134 (3), (2021).
- DesMarais, V., Eddy, R. J., Sharma, V. P., Stone, O., Condeelis, J. S. Optimizing leading edge F-actin labeling using multiple actin probes, fixation methods and imaging modalities. BioTechniques. 66 (3), 113-119 (2019).
- Ennis, H. L., Lubin, M. Cycloheximide: Aspects of inhibition of protein synthesis in mammalian cells. Science. 146 (3650), 1474-1476 (1964).
- Webber, J. L., Tooze, S. A. Coordinated regulation of autophagy by p38alpha MAPK through mAtg9 and p38IP. EMBO Journal. 29 (1), 27-40 (2010).
- Claude-Taupin, A., et al. ATG9A protects the plasma membrane from programmed and incidental permeabilization. Nature Cell Biology. 23 (8), 846-858 (2021).
- Aaron, J. S., Taylor, A. B., Chew, T. L. Image co-localization - Co-occurrence versus correlation. Journal of Cell Science. 131 (3), 211847 (2018).
- D'Antuono, R., Nechyporuk-Zloy, V. Basic digital image acquisition, design, processing, analysis, management, and presentation. Principles of Light Microscopy: From Basic to Advanced. , 77-104 (2022).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved