A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
إنشاء سرطان الكبد في الفئران BALB / c-nu والتحقيق في التأثير العلاجي لصيغة Sanleng Jiashen
In This Article
Summary
هنا ، نقدم البروتوكول خطوة بخطوة للتحقيق في التأثيرات العلاجية والمثبطة للأوعية الدموية لتركيبة Sanleng Jiashen على الفئران BALB / c-nu المصابة بسرطان الخلايا الكبدية تقويم العظام.
Abstract
أجبرت فتاكة سرطان الكبد ومقاومة الأدوية الكيميائية على البحث عن وصفات طبية فعالة للأعشاب التقليدية لسرطان الكبد. النماذج الحيوانية القابلة للتكرار وسهلة التلاعب وتحاكي بشكل كبير العمليات الفيزيولوجية المرضية لسرطان الكبد هي الشرط الأساسي للفحص الناجح للأدوية الفعالة المرشحة. وفي الوقت نفسه ، فإن مؤشرات ووسائل تقييم فعالية الأدوية الموثوقة هي أيضا ضمان البحث والتطوير للأدوية المضادة لسرطان الكبد.
صيغة Sanleng Jiashen ، وصفة طبية تمثيلية للطب الصيني التقليدي تحتوي على Sparganium stoloni erum ، Buch. -لحم الخنزير. (سانلينغ) ، باناكس الجينسنغ سي إيه مي. (الجينسنغ) ، Rheum officinale Baill. (الراوند) ، و Ligusticum chuanxiong Hort. (Chuanxiong) ، يوصف لتغذية الكبد وإزالة الحرارة وإزالة السموم وتعزيز الدورة الدموية لعلاج سرطان الكبد. يصف هذا البروتوكول التجريبي تحضير تركيبة Sanleng Jiashen المجففة بالتجميد وعملية إنشاء سرطان الكبد في الموقع في فئران BALB / c-nu. تم استخدام التلوين النسيجي المرضي ، والكشف الكيميائي المناعي لعلامات السرطان ، والتصوير في الجسم الحي للفئران ، واختبار الغشاء المشيمي لجنين الكتاكيت لاستكشاف تأثير التثبيط والمضاد لتكوين الأوعية لتركيبة Sanleng Jiashen على التكاثر الخبيث لأنسجة سرطان الكبد. تظهر البيانات أن تركيبة Sanleng Jiashen يمكن أن تقاوم بشكل فعال التكاثر الخبيث لأنسجة سرطان الكبد ، والذي يتجلى في انخفاض حجم كتلة الورم ، وتحسين الضرر المرضي ، وانخفاض مستويات علامة السرطان ki67.
يشير التثبيط المتفوق لتكوين الأوعية الدموية أيضا إلى أن صيغة Sanleng Jiashen قد يكون لها القدرة على علاج ومنع تطور وتدهور سرطان الكبد. يظهر المخطط التجريبي بأكمله عملية شاملة لمكونات الطب الصيني التقليدي في علاج سرطان الكبد الفأر ، والتي توفر مرجعا لإنشاء وتحسين نموذج سرطان الكبد ، بالإضافة إلى البحث والتطوير للأدوية للوقاية من سرطان الكبد وعلاجه.
Introduction
سرطان الكبد هو سرطان قاتل ينشأ في الكبد وهو ثاني أكثر الأسباب شيوعا للوفاة المرتبطة بالسرطان في جميع أنحاءالعالم 1. تظهر معدلات أمراض الكبد في الولايات المتحدة وبعض البلدان النامية مستويات عالية ، ويمكن أن يكون هناك أكثر من مليون حالة إصابة بسرطان الكبد في جميع أنحاء العالم بحلول عام 20302. بسبب العادات المعيشية غير الصحية مثل التدخين والسمنة وشرب الكحول ، وويلات التهاب الكبد B والتهاب الكبد C والفيروسات الأخرى ، زاد معدل الإصابة والوفيات بسرطان الكبد بشكل ملحوظ عاما بعد عام3. باعتباره ورما خبيثا غير متجانس مع سمات نسيجية مختلفة وتشخيص ضعيف ، فإن سرطان الكبد له مجموعة واسعة جدا من الحالات ، بما في ذلك سرطان الخلايا الكبدية ، وسرطان القنوات الصفراوية داخل الكبد ، وسرطان الكبد الليفي4. غالبا ما يتم تشخيص سرطان الكبد في مرحلة متقدمة ، والعديد من المرضى المتقدمين ليسوا مرشحين للعلاجالإشعاعي 5. مثبط مولتيكيناز سورافينيب هو دواء مقبول للغاية للمرضى الذين يعانون من سرطان الكبد المتقدم ، لكن المرضى غالبا ما يطورون مقاومة كبيرة خلال فترة قصيرة6. في الوقت الحاضر ، أحرزت مثبطات نقاط التفتيش المناعية PD-1 و PD-L1 جنبا إلى جنب مع سورافينيب بعض التقدم في السيطرة على تطور سرطان الكبد ، لكن التأثير العلاجي لا يزال مثيرا للجدل7.
سرطان الكبد تقويم العظام هو نوع مبكر من سرطان الكبد: لم تنتشر الخلايا السرطانية حول أنسجة الكبد أو تحدث ورم خبيث بين الأعضاء ، ولا تتأثر وظيفة الكبد بشكل كبير8. نظرا لأن سرطان الكبد تقويم العظام لا يظهر بشكل عام أعراض عدم الراحة الواضحة ، فقد يعاني بعض المرضى من آلام خفيفة في الكبد والتعب وأعراض أخرى9. في الممارسة السريرية ، يمكن للتصوير بالموجات فوق الصوتية دوبلر الملون للكبد وفحص التصوير المقطعي المحوسب المعزز تشخيص آفات كبيرة تشغل مساحة في الكبد10. على الرغم من أن سرطان الكبد الموضعي الذي لم ينتشر وينتقل يمكن إزالته عن طريق الجراحة ، إلا أن هناك بعض المخاطر الجراحية والعبء النفسي الحتمي للمرضى11. يمكن أن يقتل العلاج الكيميائي الإشعاعي كل خلايا سرطان الكبد أو جزء منها ، وقد يؤثر تثبيط المناعة على المدى الطويل لدى المرضى الذين يعانون من الأدوية على فعالية العلاج ويزيد من خطر الإصابة بأمراض أخرى12. لذلك ، فإن البحث عن علاج دوائي آمن وفعال للوقاية المبكرة من سرطان الكبد وعلاجه هو المفتاح للحد من تطور سرطان الكبد وتدهوره.
يعتمد مبدأ الطب الصيني في علاج سرطان الكبد على مفهوم التوازن والانسجام داخل الجسم. ينظر الطب الصيني إلى سرطان الكبد على أنه خلل أو تنافر في طاقة الجسم ، والمعروف باسم Qi ، والذي يؤثر على الكبد13. يتضمن علاج الطب الصيني لسرطان الكبد طرقا مختلفة ، بما في ذلك الأدوية العشبية والوخز بالإبر والعلاج الغذائي وتوصيات نمط الحياة. المبدأ هو استعادة توازن Qi ، وتقوية آليات دفاع الجسم ، وتعزيز قدرة الجسم على شفاءنفسه 14،15. ينتمي سرطان الكبد في الطب الصيني التقليدي إلى فئة "طبلة الأذن" و "تراكم الكبد". في وقت مبكر من "الشريعة الداخلية لهوانغدي" لديها سجل مفصل لأعراضه ، يحدث سرطان الكبد بسبب ركود الدم ونقص Zhengqi ويتم علاجه عن طريق إزالة ركود الدم ، والقضاء على طبلة الأذن ، وتقوية مقاومة الجسم لتوحيد الدستور13. نشأت حبوب Sanleng من كتاب "Weisheng Baojian" الذي كتبه لوه تياني ، وهو طبيب مشهور في عهد أسرة يوان. يتكون من ثلاثة أنواع من الأدوية: Sparganium stoloni erum ، Buch. -لحم الخنزير. (سانلينغ) ، Ligusticum chuanxiong Hort. (Chuanxiong) ، و Rheum officinale Baill. (راوند). يمكن أن تدخل هذه الأنواع الثلاثة من الأدوية إلى خط الزوال الكبد ولها قيمة علاجية لعلاج سرطانالكبد 14. تتكون صيغة Sanleng Jiashen من 16 جم من Sanleng و 16 جم من Panax ginseng C.A.Mey. (الجينسنغ) ، 8 جم من الراوند ، و 2 جم من Chuanxiong (الشكل 1) ، والذي يوصف لتنغيم الكبد ، وإزالة الحرارة ، والقضاء على السموم ، وتعزيز الدورة الدموية. يعتقد أن هذه الأعشاب لها خصائص مضادة للسرطان وتساعد في تقليل نمو الورم وتخفيف الأعراض وتحسين الرفاهية العامة. في التجارب المختبرية السابقة ، يمكن لصيغة Sanleng Jiashen أن تمنع تكاثر خلايا سرطان الكبد15. ومع ذلك ، كيف يتم تقييم التأثير المثبط للمركبات العشبية الصينية على سرطان الكبد بكفاءة ومعقولة؟ من خلال إنشاء نموذج سرطان الكبد في الموقع BALB / c-nu ، تم التحقيق في التأثير المثبط لصيغة Sanleng Jiashen على سرطان الكبد وتكوين الأوعية بشكل أساسي من خلال التصوير الحي للحيوانات الصغيرة واختبار الغشاء المشيمي لجنين الكتاكيت.
Protocol
تم تغذية ذكور الفئران العارية BALB / c-nu التي كانت خالية من مسببات الأمراض ، وعمر 5 أسابيع ، ووزنها 18-22 جم في المركز التجريبي الحيواني لكلية الطب التحويلية بجامعة جيلين. كانت ظروف التغذية 22 درجة مئوية -24 درجة مئوية مع رطوبة نسبية 40٪ -60٪. رقم ترخيص التجارب هو SYXK (Ji) 2018-0006 ، وتتوافق العملية التجريبية مع قواعد ولوائح لجنة الأخلاقيات بجامعة جيلين ، ورقم الموافقة على أخلاقيات هو 20221228-01.
1. تحضير تركيبة Sanleng Jiashen المجففة بالتجميد15
- ضع 16 جم من Sanleng و 16 جم من الجينسنغ و 8 جم من الراوند و 2 جم من Chuanxiong في وعاء ديكوت ذكي (انظر جدول المواد) وانقع في 294 مل من الماء منزوع الأيونات في درجة حرارة الغرفة لمدة 30 دقيقة. بعد التسخين والغليان ، استمر في الطهي لمدة 30 دقيقة عند 100 درجة مئوية ، وقم بتصفية السائل من خلال شاش طبي مزدوج (انظر جدول المواد). أضف 252 مل من الماء منزوع الأيونات إلى البقايا ، واطهيه لمدة 30 دقيقة عند 100 درجة مئوية ، وقم بتصفية السائل بشاش مزدوج.
- اجمع المرشح من الخطوة 1.1 في طبق نظيف من الفولاذ المقاوم للصدأ وقم بتجميده لمدة 12 ساعة عند -80 درجة مئوية (انظر جدول المواد).
- ضع تركيبة Sanleng Jiashen من الخطوة 1.2 في مجفف تجميد مفرغ من الهواء (انظر جدول المواد) (درجة حرارة المصيدة الباردة: -55 درجة مئوية) وجففها لمدة 48 ساعة للحصول على المسحوق المجفف بالتجميد لتركيبة Sanleng Jiashen.
2. بناء خط خلية HCCLM3 يعبر عن لوسيفيراز بثبات16
- أضف 1.0 مل من معلق خلية HCCLM3 في الصفيحة المكونة من 24 بئرا (انظر جدول المواد) مع 5 × 105 خلايا / بئر وزراعة في وسط كامل (10٪ مصل بقري جنيني + 1٪ محلول بنسلين ستربتومايسين + DMEM) (انظر جدول المواد) يحتوي على 3 ميكروغرام / مل بورومايسين لمدة 72 ساعة في حاضنة خلية (37 درجة مئوية ، 5٪ ثاني أكسيدالكربون 2 ، انظر جدول المواد).
- تخلص من المادة الطافية للخلية في الخطوة 2.1 ، وأضف 100 ميكرولتر من محلول التربسين 0.25٪ لهضم الخلايا في حاضنة الخلية لمدة دقيقة واحدة (انظر جدول المواد). أضف 300 ميكرولتر من الوسط الكامل واستخدم ماصة لتحرير الخلايا الملتصقة وإنهاء عملية الهضم. اجمع جميع معلقات الخلايا وضعها في أنبوب طرد مركزي سعة 15 مل في درجة حرارة الغرفة عند 1,000 × جم لمدة 5 دقائق. بعد التخلص من المادة الطافية ، أضف 1 مل من الوسط الكامل واخلطها عن طريق سحب العينات.
- أضف 100 ميكرولتر من معلق الخلية من 4 × 103 خلايا HCCLM3 / بئر من الخطوة 2.2 إلى صفيحة 96 بئرا وزراعتها في حاضنة خلية لمدة 24 ساعة (37 درجة مئوية ، 5٪ ثاني أكسيدالكربون 2 ، انظر جدول المواد).
- أضف 0.27 ميكرولتر من فيروس العدسات GFP إلى الألواح المكونة من 96 بئرا في الخطوة 2.3 والزراعة في حاضنة خلية لمدة 15 ساعة (37 درجة مئوية ، 5٪ ثاني أكسيد الكربون2 ، انظر جدول المواد). تخلص من المادة الطافية للخلية ، وأضف 100 ميكرولتر من وسط الثقافة الكامل ، واحصل على صور باستخدام مجهر مضان عند الطول الموجي للإثارة البالغ 488 نانومتر والطول الموجي للانبعاث 507 نانومتر (انظر جدول المواد).
- استبدل 2 مل من فيروس العدسات GFP واستمر في الاستزراع لمدة 24 ساعة. استبدل 2 مل من وسط المزرعة الكامل بدون فيروس العدسات GFP لمدة 24 ساعة أخرى.
ملاحظة: كانت كفاءة تعداء فيروس العدسات GFP إلى خلايا HCCLM3 80٪ كما رأينا تحت المجهر الفلوري المقلوب. - أضف 5 مل من 2 × 10 5 خلايا معلقة من الخطوة 2.1 إلى طبق بتري 60 مم وزراعته في حاضنة خلية لمدة 24 ساعة. أضف 64.5 ميكرولتر من اللوسيفيراز ، واستمر في الزراعة في حاضنة خلية لمدة 15 ساعة (37 درجة مئوية ، 5٪ ثاني أكسيدالكربون 2 ، انظر جدول المواد).
- تخلص من المادة الطافية وأضف 5 مل من الوسط الكامل لمواصلة الزراعة حتى تصبح الخلايا متجانسة بنسبة 90٪ في طبق بتري. تخلص من المادة الطافية للخلية ، واغسلها ب 2 × 1 مل من PBS ، وأضف 1 مل من محلول التربسين 0.25٪ لهضم الخلايا في حاضنة الخلية لمدة دقيقة واحدة (37 درجة مئوية ، 5٪ ثاني أكسيد الكربون2 ، انظر جدول المواد). أضف 3 مل من الوسط الكامل والماصة لأعلى ولأسفل لتحرير الخلايا الملتصقة وإنهاء عملية الهضم. اجمع كل معلقات الخلايا لحقن الفأر لاحقا.
ملاحظة: للحصول على عدد كاف من الخلايا ، تم تمرير الخلايا وزراعتها باستمرار.
3. إنشاء نموذج الفئران العارية BALB / c-nu لسرطان الكبد في الموقع والعلاج15
- أضف 100 ميكرولتر من 1 × 107 خلايا HCCLM3 المنقولة باللوسيفيراز في الخطوة 2.7 و 100 ميكرولتر من غراء المصفوفة (انظر جدول المواد) في أنبوب طرد مركزي سعة 1.5 مل (انظر جدول المواد) ، واخلطه برفق مع ماصة سعة 1 مل (انظر جدول المواد).
ملاحظة: يجب أن تتم العملية الكاملة لتحضير المحلول على الجليد لمنع غراء المصفوفة من المعالجة. - تطهير الإبطين الأيسر والأيمن للفئران العارية BALB / c-nu باليودوبين (انظر جدول المواد) وإزالة اليود بالكحول (انظر جدول المواد).
- قم بحقن 100 ميكرولتر ببطء من خليط خلايا HCCLM3 وغراء المصفوفة من الخطوة 3.1 في الإبطين الأيسر والأيمن للفئران العارية BALB / c-nu باستخدام حقنة يمكن التخلص منها 1 مل.
ملاحظة: بعد حوالي 10 أيام ، طورت الفئران العارية BALB / c-nu كتلة ورم تبلغ حوالي 0.5 سم3 في موقع حقن الإبط الثنائي. - تخدير الفئران العارية BALB / c-nu في الخطوة 3.3 عن طريق الحقن داخل الصفاق بنسبة 1٪ ، 50 مجم / كجم بنتوباربيتال الصوديوم. قم بقص جلد كلا الإبطين بمقص وملاقط للعيون (انظر جدول المواد) ، وقشر كتلة الورم تحت الجلد برفق لوضعها في طبق زراعة الخلايا (انظر جدول المواد) الذي يحتوي على مخزن مؤقت PBS مبرد مسبقا (انظر جدول المواد) ، وقم بتقطيعه إلى 1 مم3 قطع بمشرط (انظر جدول المواد).
ملاحظة: يجب حصاد كتلة الورم تحت الإبط للفئران العارية BALB / c-nu على الجليد في غضون 0.5 ساعة للحفاظ على نشاط الخلايا السرطانية وزيادة معدل نجاح النموذج. في نهاية أخذ العينات ، قتلت الفئران عن طريق إزالة فقرات عنق الرحم. إذا كان هناك جزء من الورم ، فيجب إزالته ، مع ترك الورم الأبيض السمكة فقط لمنع العدوى أثناء زراعة سرطان تقويم العظام. - تخدير الفئران العارية BALB / c-nu بنسبة 1٪ ، 50 مجم / كجم من البنتوباربيتال الصوديوم داخل الصفاق (انظر جدول المواد) ، وتطهير البطن باليود (انظر جدول المواد) ، وإزالة اليود بالكحول (انظر جدول المواد).
- استخدم مقص وملاقط للعيون (انظر جدول المواد) لقطع شق جراحي بزاوية 45 درجة حوالي 1 سم في موضع 0.5 سم أسفل عملية الخنجري لكشف الكبد ، والضغط برفق على الكبد للضغط على أنسجة الكبد ، وإصلاح الكبد بورق الوزن.
ملاحظة: يمكن وضع مسحات أو أعواد قطنية تحت أضلاع الفئران لفضح الكبد بشكل فعال. - خذ قطعة صغيرة من أنسجة الورم في الخطوة 3.4 بإبرة حقن يمكن التخلص منها 10 مل ، وزرع كتلة الورم في الكبد على بعد حوالي 0.5 سم بالتوازي مع الكبد لإصلاحها تحت كبسولة الكبد وسحب الإبرة ببطء.
ملاحظة: استخدم حقنة يمكن التخلص منها سعة 1 مل لإسقاط قطرتين من غراء المصفوفة الذائبة ، ومراقبة كتلة الورم دون أي زلات عرضية وبدون نزيف ، ثم خياطة الشق الجراحي. - أغلق الشق الجراحي بإبرة 12 سم تحمل ملقط و6-0 خيوط جراحية (انظر جدول المواد). ضع مرهم العين الإريثروميسين (انظر جدول المواد) على موقع الجراحة لمنع العدوى. ضع الفئران على وسادة ساخنة (انظر جدول المواد) واحتفظ بها في أقفاص منفصلة بعد الاستيقاظ.
- بدءا من اليوم الأول بعد النمذجة ، قم بإعطاء 7.5 مجم / كجم من سورافينيب وتركيبة Sanleng Jiashen (7.8 جم / كجم و 15.6 جم / كجم و 31.2 جم / كجم) عن طريق التزقيم للفئران من الخطوة 3.8 لمدة 14 يوما ، مرة واحدة في اليوم. قم بإعطاء كمية متساوية من المحلول الملحي العادي للفئران في المجموعة النموذجية.
4. تقييم التصوير في الجسم الحي
ملاحظة: في اليوم 14 ، تم إجراء التصوير الحي بعد ساعة واحدة من انتهاء الإعطاء.
- قم بتشغيل الكمبيوتر وأداة التصوير في الجسم الحي (انظر جدول المواد). انقر نقرا مزدوجا فوق أيقونة الصورة الحية على سطح المكتب لتشغيل البرنامج. انقر فوق تهيئة نظام IVIS في لوحة التحكم لبدء تشغيل نظام IVIS بالكامل.
ملاحظة: بعد أن يكمل الجهاز الاختبار الذاتي، يكون ضوء حالة درجة الحرارة في لوحة التحكم أحمر. انتظر حوالي 5-10 دقائق بعد أن تنخفض درجة الحرارة ويتحول الضوء إلى اللون الأخضر ، ويمكن إجراء الحصول على الصورة. - تطهير بطن الفئران بالكحول وحقن 10 ميكرولتر D-luciferin داخل الصفاق لكل غرام من وزن الجسم (انظر جدول المواد) بحقنة يمكن التخلص منها. تخدير الفئران عن طريق الحقن داخل الصفاق بنسبة 1٪ ، 50 مجم / كجم بنتوباربيتال الصوديوم.
ملاحظة: تم تخفيف D-luciferin باستخدام PBS معقم إلى 15 مجم / مل. - ضع الفئران المخدرة في الخطوة 4.3 في صندوق المراقبة وأغلق الباب ، واضبط وقت التعرض على 30 ثانية في لوحة التحكم: تحديد الوضع: حدد الإضاءة وفقا لنوع العينة ، وحدد البرنامج التلقائي افتراضيا ، واضغط على اكتساب للحصول على الصور.
- انقر فوق حفظ بيانات الصورة الحية ، وحدد جميع ملفات بيانات الصور الحية ، واحفظها على سطح مكتب الكمبيوتر.
- انقر فوق الخروج في الصورة الحية على الشاشة الرئيسية. قم بإيقاف تشغيل طاقة الكاميرا وطاقة جهاز التصوير وطاقة الكمبيوتر بدورها.
- بعد التصوير ، القتل الرحيم للفئران المخدرة (الحقن داخل الصفاق بنسبة 1٪ ، 50 مجم / كجم بنتوباربيتال الصوديوم) عن طريق خلع فقرات عنق الرحم.
5. تلطيخ الهيماتوكسيلين - اليوزين17
- قم بإصلاح أنسجة الكبد الطازجة للفئران من الخطوة 4.7 في 4٪ بارافورمالدهيد لمدة 48 ساعة ، ثم اشطفها بالماء الجاري 3 مرات لمدة 5 دقائق في كل مرة لغسل بارافورمالدهايد (انظر جدول المواد).
- تجفيف أنسجة الكبد في الخطوة 5.1 في 30٪ إيثانول ، 50٪ إيثانول ، 70٪ إيثانول ، 95٪ إيثانول
 ، 95٪ إيثانول ، وإيثانول
، 95٪ إيثانول ، وإيثانول  95٪ ، والإيثانول اللامائي لمدة ساعة واحدة بدوره (انظر جدول المواد).
95٪ ، والإيثانول اللامائي لمدة ساعة واحدة بدوره (انظر جدول المواد). - ضع أنسجة الكبد المجففة في الخطوة 5.2 إلى 50٪ من الإيثانول و 50٪ الزيلين والزيلين
 والزيلين
والزيلين 
 بالتتابع لجعلها شفافة لمدة ساعة واحدة (انظر جدول المواد).
بالتتابع لجعلها شفافة لمدة ساعة واحدة (انظر جدول المواد).
ملاحظة: الزيلين متطاير وسام ، ويتم تنفيذ هذه الخطوة في غطاء الدخان. - قم بإذابة شمع البارافين والحفاظ على درجة الحرارة عند حوالي 55 درجة مئوية. ضع كتل أنسجة الكبد في الخطوة 5.3 في آلة تضمين البارافين (انظر جدول المواد) مملوءة بمحلول الشمع للتضمين.
- قم بتثبيت كتلة الشمع المدمجة في أنسجة كبد الفئران في الخطوة 5.4 على آلة تقطيع البارافين (انظر جدول المواد) ، وقم بتقطيعها إلى شرائح بسمك 5 ميكرومتر ، ووضع الشرائح بشكل مسطح تماما في ماء 50 درجة مئوية ، ثم اغرفها بشريحة. أخيرا ، ضعها في آلة خبز المناديل البيولوجية للتجفيف لمدة 20 دقيقة عند 70 درجة مئوية (انظر جدول المواد).
- انقع الأقسام التي يبلغ حجمها 5 ميكرومتر في الخطوة 5.5 في الزيلين
 والزيلين
والزيلين  والإيثانول
والإيثانول  اللامائي والإيثانول
اللامائي والإيثانول  اللامائي لمدة 10 دقائق على التوالي ، ثم انقعها في 95٪ إيثانول ، 90٪ إيثانول ، 80٪ إيثانول ، و 70٪ إيثانول لمدة 5 دقائق على التوالي ، وأخيرا اغسلها بالماء المقطر لمعالجة إزالة الشمع (انظر جدول المواد).
اللامائي لمدة 10 دقائق على التوالي ، ثم انقعها في 95٪ إيثانول ، 90٪ إيثانول ، 80٪ إيثانول ، و 70٪ إيثانول لمدة 5 دقائق على التوالي ، وأخيرا اغسلها بالماء المقطر لمعالجة إزالة الشمع (انظر جدول المواد). - صبغ أقسام أنسجة الكبد الشمعية المجففة بسمك 5 ميكرومتر بالهيماتوكسيلين لمدة 8 دقائق ، ثم اشطفها بالماء الجاري.
- تفريق في محلول حمض الهيدروكلوريك 1٪ لمدة 10 ثوان ، واشطفها بالماء الجاري لمدة 30 دقيقة (انظر جدول المواد).
- صبغ بمحلول يوزين 0.5٪ لمدة 1 دقيقة (انظر جدول المواد).
- ضع الشرائح في 95٪ كحول
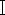 ، 95٪ كحول
، 95٪ كحول 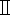 ، إيثانول
، إيثانول 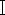 لامائي ، إيثانول
لامائي ، إيثانول 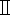 لامائي ، زيلين
لامائي ، زيلين 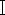 ، وزيلين
، وزيلين 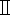 لمدة 5 دقائق لكل منهما لتجفيفها (انظر جدول المواد).
لمدة 5 دقائق لكل منهما لتجفيفها (انظر جدول المواد). - ختم بالعلكة المحايدة ، والتقط صورا تحت مجهر ضوئي مقلوب (انظر جدول المواد).
6. تلطيخ كيميائي مناعي18
- قم بإسقاط 1.5٪ H2O2 على أقسام 5 ميكرومتر من كبد الفأر في الخطوة 5.6 واحتضانها في درجة حرارة الغرفة لمدة 10 دقائق ، ثم اغسلها باستخدام PBS لمدة 2 × 5 دقائق (انظر جدول المواد).
- قم بإصلاح الأنسجة بمحلول حامض الستريك (انظر جدول المواد) لمدة 5 دقائق واغسلها باستخدام PBS لمدة 3 × 5 دقائق.
- احتضن مع 0.2٪ triton X-100 (انظر جدول المواد) في درجة حرارة الغرفة لمدة 4 دقائق ، ثم احتضن بنسبة 0.5٪ triton X-100 في درجة حرارة الغرفة لمدة 4 دقائق ، واغسلها باستخدام PBS.
- أضف مصل الماعز (انظر جدول المواد) لإغلاقه لمدة 15 دقيقة ، ثم أضف الجسم المضاد الأساسي ki67 (انظر جدول المواد) المخفف ب PBS (1: 300) للاحتضان عند 4 درجات مئوية بين عشية وضحاها. يغسل باستخدام PBS لمدة 3 × 5 دقائق.
- احتضن بجسم مضاد ثانوي مخفف ب PBS (1: 200) في درجة حرارة الغرفة لمدة ساعة واحدة ، واغسله باستخدام PBS لمدة 3 × 5 دقائق (انظر جدول المواد).
- وصمة عار بالمحلول النامي لمدة 5 دقائق واشطفها بالماء المقطر المزدوج (انظر جدول المواد).
- أعد تلطيخ الهيماتوكسيلين لمدة دقيقتين ، وقم بتمييزه في محلول حمض الهيدروكلوريك بنسبة 1٪ لمدة 10 ثوان ، ثم اشطفه بالماء الجاري لمدة 30 دقيقة (انظر جدول المواد).
- ضع الشرائح في 95٪ كحول
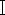 ، 95٪ كحول
، 95٪ كحول 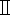 ، إيثانول
، إيثانول  لامائي ، إيثانول
لامائي ، إيثانول  لامائي ، زيلين
لامائي ، زيلين  ، وزيلين
، وزيلين  لمدة 5 دقائق لكل منهما لتجفيفها (انظر جدول المواد).
لمدة 5 دقائق لكل منهما لتجفيفها (انظر جدول المواد). - ختم بالعلكة المحايدة والتقط صورا تحت مجهر ضوئي مقلوب (انظر جدول المواد).
7. اختبار الغشاء المشيمي لجنين الفرخ19
- اترك بيض الدجاج ذو الريش الأبيض (انظر جدول المواد) في درجة حرارة الغرفة لمدة ساعتين ورشه بالكحول للتطهير. احفر حفرة في غرفة الهواء باستخدام مثقاب جمجمة (انظر جدول المواد) ، واحتضان البيض مع غرفة الهواء لأعلى لمدة 7 أيام (درجة حرارة الحضانة 37.8-38.2 درجة مئوية والرطوبة النسبية 65٪).
ملاحظة: خلال الأيام الثلاثة الأولى من الحضانة ، يتم تشغيل زر تقليب البيض التلقائي لمنع غشاء جنين الفرخ المشيمي من الالتصاق بالقشرة وإنشاء غرفة هواء زائفة. - تخلص من البويضات الضعيفة / غير المخصبة في مصباح البويضة (انظر جدول المواد). انزع نافذة مقاس 1 × 1 سم بعناية باستخدام ملاقط العين (انظر جدول المواد) بعد حفر ثقب في غرفة الهواء المزيفة باستخدام مثقاب الجمجمة (انظر جدول المواد).
ملاحظة: يرجى ملاحظة أن قشر البيض يجب ألا يقع في غشاء المشيمة التركي لجنين الكتكوت. - في اليوم الثامن من الحضانة ، أضف 100 ميكرولتر من تعليق الخلايا السرطانية (1 × 106 خلايا) إلى كل بيضة من غرفة الهواء المزيفة باستثناء المجموعة الضابطة. في مجموعات الأدوية ، أضف 100 ميكرولتر من محلول سورافينيب وصيغة Sanleng Jiashen. في مجموعات التحكم والنموذج ، أضف 100 ميكرولتر من PBS.
ملاحظة: يتكون تعليق الخلايا السرطانية من خلايا HCCLM3 وغراء مصفوفة بحجم متساو. يتم تعيين تركيز الدواء على النحو التالي: 7.5 مجم / كجم سورافينيب وتركيبة سانلينغ جياشين (7.8 جم / كجم ، 15.6 جم / كجم ، و 31.2 جم / كجم). - قم بتغطية النافذة بضمادة شفافة (انظر جدول المواد) وقم بتطهيرها برذاذ الكحول (انظر جدول المواد). بعد 7 أيام من الحضانة ، قم بإزالة الضمادة الشفافة ، وأضف 1 مل من المثبت (الميثانول: الأسيتون = 1: 1) (انظر جدول المواد) من غرفة الهواء المزيفة لتثبيت لمدة 30 دقيقة.
- تخلص من المثبت باستخدام حقنة سعة 1 مل. قم بقص غشاء المشيمة ~ 5 × 5 سم في غرفة الهواء المزيفة بمقص العيون وضعه في طبق بتري 60 مم.
ملاحظة: بالنسبة للغشاء المشيمي لجنين الكتاكيت بالدم ، اشطفه باستخدام PBS. بالنسبة لغشاء جنين الفرخ المشيمي المرتبط بالأنسجة ، افصل بمقص العيون. - ضع الغشاء المشيمي من الخطوة 7.5 تحت المجهر البصري وقم بتصوير الأوعية (انظر جدول المواد).
النتائج
كما هو موضح في الشكل 2 أ ، أنشأنا نموذجا لسرطان الكبد في الموقع لفئران BALB / c-nu وقمنا بتقييم التأثير المضاد للأورام لصيغة Sanleng Jiashen. يوضح الشكل 2 ب أن تركيبة Sanleng Jiashen يمكن أن تمنع بشكل كبير نمو أورام الكبد. أشارت النتائج المرضية إلى أنه با?...
Discussion
أكدت كمية كبيرة من الأدلة أن Sanleng و ginseng و rauarb و Chuanxiong في صيغة Sanleng Jiashen لها تأثيرات دوائية على علاج سرطان الكبد. أظهرت الدراسات أن Sanleng يمكن أن يمنع بشكل كبير تكاثر الخلايا السرطانية ونموها لمنع غزو الخلايا السرطانية والورم الخبيث ، والحث على موت الخلايا المبرمج للخلايا ، ?...
Disclosures
المؤلفون ليس لديهم ما يكشفون عنه.
Acknowledgements
تم دعم هذا العمل من قبل مؤسسة الفلسفة والعلوم الاجتماعية في الصين (20VYJ070) ، ومشروع إدارة التعليم بمقاطعة جيلين (JJKH20230963KJ) ، والدفعة الثانية من مشروع هندسة علماء Xinglin في جامعة Changchun للطب الصيني (QNKXJ2-2021 + ZR25).
Materials
| Name | Company | Catalog Number | Comments |
| 0.25% trypsin solution | HyClone, America | SH30042.01B | |
| 1 mL disposable syringe | Mingankang Medical Equipment Co., Ltd., China | RWSB | |
| 1% Penicillin & streptomycin solution | Hyclone, America | SV30010 | |
| 1.5 mL centrifuge tube | Corning, America | MCT-150-C-S | |
| 12 cm needle forceps | Hesdick, China | HKQS-211 | |
| 6-0 surgical sutures | Shanghai Jinhuan Medical Equipment Co., Ltd., Shanghai, China | CR631 | |
| 75% alcohol | Sichuan Youbang Enterprise Co., Ltd., Sichuan, China | 1.00009E+11 | |
| 96-well plates | NEST, China | 701001 | |
| Acetone | Tianjin Dingfu Chemical General Plant, Tianjin, China | GB686-89 | |
| BALB/c-nu male nude mice | Beijing Weitonglihua Experimental Animal Technology Co., Ltd., Beijing, China | SYXK(Ji) 2018-0006 | |
| Biological tissue baking machine | Leica, Germany | Leica HI1220 | |
| Cell culture dish | NEST, China | NEST.706001 | |
| Citric acid solution | Wuhan Canos Technology Co., Ltd., Wuhan, China | sj1074 | |
| D-luciferin | Gold Biotechnology®, Inc., China | LUCK-100 | |
| DMEM | Hyclone, America | SH30243.01 | |
| Egg illuminator | Shandong Weizhen Incubation Equipment Company, Shandong, China | WZSDT | |
| Eosin staining solution | Hunan BKMAM Biotechnology Co., Ltd., Hunan, China | 110703061 | |
| Erythromycin eye ointment | Cisen Pharmaceutical Co., Ltd., Shanghai, China | H37022025 | |
| Fetal bovine serum | Clark, America | FB25015 | |
| Fully automatic intelligent chick incubator | Shandong Weizhen Incubation Equipment Company, Shandong, China | 29538 | |
| GFP lentivirus solution | Suzhou GenePharma Co.,Ltd., Suzhou, China | F22AZ | |
| Goat serum | Shenyang Wanlei Biotechnology Co., Ltd., Shengyang, China | WLA067 | |
| Hand-held mouse skull drill | STRONGWT, China | 190 | |
| HCCLM3 cell line | WheLab, Shanghai, China | C1010 | |
| Heating pad | Zhongke Life Technology Co., Ltd., Hangzhou, China | GEJRD-10W | |
| Hematoxylin | Hunan BKMAM Biotechnology Co., Ltd., Hunan, China | B-YH250-1 | |
| Intelligent decoction pot | Hangzhou Jiuyang living Appliance Co., Ltd., Hangzhou, China | 3003BQ | |
| Inverted fluorescence microscope | Olympus, Japan | IX73 | |
| ki67 primary antibody | Wuhan Servicebio Technology Co., Ltd., Wuhan, China | GB121141-100 | |
| Lodophor disinfectant | Cofoe Medical Technology Co.,Ltd., Hunan, China | 202110073 | |
| Luciferase | Suzhou GenePharma Co.,Ltd., Suzhou, China | E26JZ | |
| Matrix glue | Corning, America | 356234 | |
| Medical gauze | Yunnan Chenye Biotechnology Co., Ltd., Yunnan, China | 71712049971 | |
| Methanol | Guangdong Guanghua Sci-Tech Co., Ltd., Guangdong, China | 1.17001.023 | |
| Ophthalmic scissor | Hesdick, China | HKQS-209 | |
| Ophthalmic tweezer | Hesdick, China | HKCL-20 | |
| Paraffin embedding machine | Leica, Germany | EG1150H | |
| Paraffin slicing machine | Leica, Germany | Leica CM1950 | |
| Paraformaldehyde | Biosharp, China | BL539A | |
| PBS buffer | Wuhan Servicebio Technology Co., Ltd., Wuhan, China | G2156-1L | |
| Puromycin | Beijing Solarbio Science & Technology Co., Ltd., Beijing, China | P8230 | |
| Refrigerator | Thermo Scientific, America | TDE40086FV-ULTS | |
| Scalpel | Hesdick, China | HKCL-93 | |
| Secondary antibody | Wuhan Servicebio Technology Co., Ltd., Wuhan, China | GB23301 | |
| Small animal live imaging system | Caliper Life Sciences, America | IVIS Lumina XR | |
| Sorafenib | Shanghai Aladdin Biochemical Technology Co., Ltd., Shanghai, China | 284461-73-0 | |
| Transparent dressing | 3M, America | 9534HP | |
| Triton X-100 | Beijing Solarbio Science & Technology Co., Ltd., Beijing, China | T8200 | |
| Vacuum freeze dryer | Ningbo Xinzhi Biotechnology Co., Ltd., Ningbo, China | sz-10N | |
| White feather chicken eggs | Shandong Haotai Experimental Animal Breeding Co., Ltd., Shandong, China | SCXK(Lu) 20180004 | |
| Xylene | Sigma-Aldrich, , America | 534056 |
References
- Sia, D., Villanueva, A., Friedman, S. L., Llovet, J. M. Liver cancer cell of origin, molecular class, and effects on patient prognosis. Gastroenterology. 152 (4), 745-761 (2017).
- Starley, B. Q., Calcagno, C. J., Harrison, S. A. Nonalcoholic fatty liver disease and hepatocellular carcinoma: a weighty connection. Hepatology. 51 (5), 1820-1832 (2010).
- Siegel, R. L., Miller, K. D., Wagle, N. S., Jemal, A. Cancer statistics. CA-A Cancer J. Clin. 73 (1), 17-48 (2023).
- Lozano, R., et al. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet. 380 (9859), 2095-2128 (2012).
- Verslype, C., et al. The management of hepatocellular carcinoma. Current expert opinion and recommendations derived from the 10th World Congress on Gastrointestinal Cancer, Barcelona, 2008. Ann. Oncol. , (2009).
- Greten, T. F., et al. Biomarkers for immunotherapy of hepatocellular carcinoma. Nat. Rev. Clin. Oncol. 20 (11), 780-798 (2023).
- Rimassa, L., Finn, R. S., Sangro, B. Combination immunotherapy for hepatocellular carcinoma. J. Hepatol. 79 (2), 506-515 (2023).
- Wu, Z. H., et al. A terrylene-anthraquinone dyad as a chromophore for photothermal therapy in the NIR-II window. J. Am. Chem. Soc. 145 (48), 26487-26493 (2023).
- Pawlik, T. M. Hepatocellular carcinoma. Sure. Oncol. Clin. N. Am. 33 (1), (2024).
- Schwarze, V., et al. Diagnostic value of contrast-enhanced ultrasound versus computed tomography for hepatocellular carcinoma: a retrospective, single-center evaluation of 234 patients. J. Int. Med. Res. 48 (6), 1-10 (2020).
- Maki, H., Hasegawa, K. Advances in the surgical treatment of liver cancer. Biosci. Trends. 16 (3), 178-188 (2022).
- Pepe, A., et al. Medical radiology: current progress. Diagnostics. 13 (14), 2439 (2023).
- Li, Y., Zhang, C. Significance of 'harmonious' thinking in Inner Canon of Huangdi on the prevention and treatment of primary liver cancer. China Journal of Traditional Chinese Medicine and Pharmacy. 28 (02), 305-308 (2013).
- Luo, T. . Wishing Baojian (M). , (2019).
- Li, Y. . Effect and mechanism of Sanlengjiashen Decoction on hepatocellular carcinoma by JAK2/STAT3 signaling pathway [D]. , (2022).
- Wang, P., et al. BTF3 promotes proliferation and glycolysis in hepatocellular carcinoma by regulating GLUT1. Cancer Biol. Ther. 24 (1), 2225884 (2023).
- Xie, N., et al. Rhodiola crenulate alleviates hypobaric hypoxia-induced brain injury via adjusting NF-κB/NLRP3-mediated inflammation. Phytomedicine. 103, 154240 (2022).
- Wang, X., et al. Rhodiola crenulata attenuates apoptosis and mitochondrial energy metabolism disorder in rats with hypobaric hypoxia-induced brain injury by regulating the HIF-1α/microRNA210/ISCU1/2 (COX10) signaling pathway. J. Ethnopharmacol. 241, 111801 (2019).
- Guerrieri, A. N., et al. A novel patient-derived immortalised cell line of myxofibrosarcoma: a tool for preclinical drugs testing and the generation of near-patient models. BMC Cancer. 23 (1), 1194 (2023).
- Li, Y., Zhao, J., Zhao, H., Yu, C. Research progress of Sparganium Stoloniferum. Journal of Liaoning University of Traditional Chinese Medicine. 20 (09), 92-94 (2018).
- Kim, T. W., Lee, S. Y., Kim, M., Cheon, C., Ko, S. G. Kaempferol induces autophagic cell death via IRE1-JNK-CHOP pathway and inhibition of G9a in gastric cancer cells. Cell Death Dis. 9 (9), 875 (2018).
- Lee, M. J., et al. Kaempferol alleviates mitochondrial damage by reducing mitochondrial reactive oxygen species production in lipopolysaccharide-induced prostate organoids. Foods. 12 (20), 3836 (2023).
- Zhang, Q., et al. Molecular docking and in vitro experiments verified that kaempferol induced apoptosis and inhibited human HepG2 cell proliferation by targeting BAX, CDK1, and JUN. Mol. Cell. Biochem. 478 (4), 767-780 (2023).
- Kumar, S., et al. Myricetin: a potential plant-derived anticancer bioactive compound-an updated overview. N-S Arch. Pharmacol. 396 (10), 2179-2196 (2023).
- Wang, M., et al. Myricetin reverses epithelial-endothelial transition and inhibits vasculogenic mimicry and angiogenesis of hepatocellular carcinoma by directly targeting PAR1. Phytother. Res. 36 (4), 1807-1821 (2022).
- Li, J., Li, F., Jin, D. Ginsenosides are promising medicine for tumor and inflammation: A review. Am. J. Chinese Med. 51 (4), 883-908 (2023).
- Guo, X., Hu, N., Sun, G., Li, M., Zhang, P. Shenyi capsule plus chemotherapy versus chemotherapy for non-small cell lung cancer:A systematic review of overlapping meta-analyses. Chinese Journal of Integrative Medicine. 24 (3), 227-231 (2018).
- Zhang, R., et al. Network Meta-analysis of oral Chinese patent medicine for adjuvant treatment of primary liver cancer. China Journal of Chinese Materia Medica. 46 (09), 2333-2343 (2021).
- Oh, H. M., Cho, C. K., Son, C. G. Experimental evidence for the anti-metastatic action of ginsenoside Rg3: A systematic review. Int. J. Mol. Sci. 23 (16), 9077 (2022).
- Nowak-Perlak, M., Ziółkowski, P., Woźniak, M. A promising natural anthraquinones mediated by photodynamic therapy for anti-cancer therapy. Phytomedicine. 119, 155035 (2023).
- Bai, J., et al. Emodin, a natural anthraquinone, suppresses liver cancer in vitro and in vivo by regulating VEGFR and miR-34a. Invest. New Drug. 38 (2), 229-245 (2020).
- Cheng, G., et al. Cell metabolomics reveals the potential mechanism of aloe emodin and emodin inhibiting breast cancer metastasis. Int. J. Mol. Sci. 23 (22), 13738 (2022).
- Wang, X., et al. Inhibition of tetramethylpyrazine on P-gp, MRP2, MRP3 and MRP5 in multidrug resistant human hepatocellular carcinoma cells. Oncol. Rep. 23 (1), 211-215 (2010).
- Hu, J., et al. Ultrasonic extraction, antioxidant and anticancer activities of novel polysaccharides from Chuanxiong rhizome. Int. J. Biol. Macromol. 85, 277-284 (2016).
- Zhong, C., et al. Physicochemical properties of polysaccharides from Ligusticum chuanxiong and analysis of their anti-tumor potential through immunoregulation. Food Funct. 12 (4), 1719-1731 (2021).
- Hou, Y., et al. Salidroside intensifies mitochondrial function of CoCl2-damaged HT22 cells by stimulating PI3K-AKT-MAPK signaling pathway. Phytomedicine. 109, 154568 (2023).
- Wang, X., et al. Salidroside, a phenyl ethanol glycoside from Rhodiola crenulata, orchestrates hypoxic mitochondrial dynamics homeostasis by stimulating Sirt1/p53/Drp1 signaling. J. Ethnopharmacol. 293, 115278 (2022).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved