Method Article
引物的适体的选择,使用一个随机DNA文库
摘要
SELEX协议包括多轮选拔,其中每一个需要结合的配体,这反过来又需要固定的引物序列,侧翼的随机库地区的再生。这些固定的引物序列,可以干扰与选择过程(误报和底片)。在这里,我们目前无底漆的协议。
摘要
适配是高度结构化的寡核苷酸(DNA或RNA),可以结合与亲和力与抗体 1的目标。他们发现通过体外筛选过程称为指数富集的配体(SELEX) 的系统演化,识别目标的种类繁多,从小分子蛋白质和2-4等大分子物质。适配,以及适合在体内诊断和/或治疗应用的属性:除了良好的特异性和亲和力,他们很容易合成,更严格的加工条件下生存,他们是不良的免疫原性,其规模相对较小,可能会导致在轻便渗透组织。
通过标准SELEX过程中确定的适配通常包括〜80个核苷酸(NT),因为它们通常是从〜40 nt的随机地区,再加上每边固定引物位点的〜20 NT的核酸库中选择。固定引物序列,从而可以由近〜50%的库序列,因此可能会产生积极或消极的妥协,在遴选过程中 3适配识别,生物信息学方法虽然建议的固定序列,不作出重大贡献后, 选择 5到适体的结构。为了解决这些潜在的问题,引物序列互补的寡核苷酸被封锁或交换在SELEX 6轮中途不同的序列,或已修整至新台币7,8 6-9。温家宝和灰色9设计了引物基因组SELEX方法,其中引物序列完全不同于前选择库中删除,然后再生,让选定的基因组片段的扩增。然而,聘请技术,一个独特的基因组库将建造,拥有有限的多样性,和轮筛选后的再生依赖线性reamplification步骤。另外,努力规避固定序列的引物,使用高效率的分区造成的问题,会见了 PCR扩增10的问题。
我们已经开发出一个引物(PF)的选择方法,大大简化了SELEX程序,并有效地消除了引物干扰问题,11,12 。协议工作在一个简单的方式。中央库中随机地区是没有多余的侧翼序列和纯化绑定到一个合适的目标(例如纯化的蛋白质或复杂的混合物,如细胞株)。绑定序列得到侧翼序列团聚,并重新放大,生成选定的子库。作为一个例子,在这里我们选择适配S100B蛋白,黑色素瘤的蛋白标记。结合实验显示,在10 -7 Kd的小号- 10 -8 M系列选择了几个回合后 ,我们表明,适配功能有效三明治约束力格式。
研究方案
1。底漆自由选择协议简介
使用相应的寡核苷酸(图1和2,步骤a),其中包含30 NT随机域中央两侧由两个引物区域,PCR构建一个双链DNA库。两种略为不同的“引无”(PF)的协议。在双链DNA库,5' -区域包含内切酶“刻痕”内切酶Nt.BstNBI网站;,这种酶识别双链DNA,但切割DNA底物只有一个链。 3' -地区的双链DNA库包含的内切酶Nt.BbvCI的另一个“刻痕”网站,识别双链DNA,但劈开只有一个链,留在3'end(功率因数为1), 以及作为BspMI完工内切酶酶切位点,其中切割股只剩下3'没有额外的核苷酸(PF 2 )。我们通常采用功率因数为1协议最初(因为它更容易在遴选过程中产生的独立片段,见下文),然后采用PF 2随后的几轮选择协议。
5' - pN30 - CC - 3“的片段(32 +片段指定)和5' - pN30 - 3”片段(30 +片段)30 NT 32 NT Nt.BbvCI / NT分别产生BstNBI或BspMI / Nt.BstNBI卵裂的双链DNA库,凝胶净化。 32 +片段包含30 NT随机域,与CC在3' -末端侧翼序列(功率因数为1)。 30 +片段(PF 2)只包含30个随机NT域序列。凝胶净化(Nt.BbvCI或Nt.BstNBI削减只有上部的“+”链)获得“自我桥”66 - 片段(含5'和3'侧翼序列的随机N30地区)。获得这种自我的桥梁,直接在PF 1协议,或可以生成和分离,切割后的 PF 2协议(图1和2,步骤b)只有NtBbv.CI或Nt.BstNBI DNA库。 32 + - 32 +片段与纯化蛋白质或培养的黑色素瘤细胞共孵育允许的片段结合的蛋白质或细胞,未绑定的碎片被大水冲走(图1和2,步骤c)。约束或选定的片段用于底漆地区重新生成。
杂交/结扎反应,产生自我的桥梁和纯化在同一时间为32 + - 30 +片段纯化; 5'端引物库的建设和3' -末端的引物,取代相同相匹配的引物,还包含一个额外的SP6在3' -末端的转录子(图1和2,步骤d)。杂交/结扎反应的产品,然后用于在体外 RNA转录(图1和2,步骤e)。 RNA的转录,结扎的DNA(包括未被选中的自我桥的DNA片段),由DNA酶消化,我以消除干扰的背景序列。反转录(RT)- PCR数据表明,产品的再生底漆有效reamplified,构成一个“圆”的选择(图1和2,步骤f)。背景在没有实时控制PCR扩增循环次数高,可以完全去除额外的DNA酶I消化后没有检测到较低的周期数字,我们经常聘请。
经过7轮的选择,适体结合特性进行了表征。 Kd值均在10-7 10-8 M的范围(图3)。在结合分析,对各种适配表明添加剂具有约束力,表明他们的目标S100B蛋白上的不同地点。因此,我们在“三明治”结合试验测试适配对,无论在玻璃芯片,采用荧光标记的第二个适配(Codelink幻灯片),第二适配衍生的黄金加上50纳米的黄金纳米粒子(纳米金;图3)纳米线。在这两种情况下,结合特异性高:在Codelink芯片,无夹心约束力适配没有表现出添加剂Kd的裁决具有约束力。随着衍生的纳米线,我们观察到对非目标蛋白质几乎没有任何约束力,适体耦合的纳米金(图3)可以通过观察和个人夹心复合物。
2。材料
2.1。生成的PF的束缚片段的DNA文库和Reamplification
详细的描述在2009年泛和克劳森;潘等人,2008年。2.2。纯化的蛋白质基础的选择
- 20毫米的Tris - HCl,pH值7.4
- 32 +片段和30 +片段
- 选择缓冲区(氯化钙2 2.5毫米,5毫米MgCl 2的 1X磷酸盐缓冲液,pH值7.4,GIBCO)
- 镍NTA琼脂糖珠(QIAGEN)
- 聚丙烯列(QIAGEN)
- 结合缓冲液(50毫米的Na 2 HPO 4 -的NaH 2 PO 4,PH7.2,150 mM氯化钠)
- 表达,纯化S100B蛋白结合缓冲液(5微克/μL)
- 酚:氯仿:IAA(pH值7.9,Ambion公司)
- 3 M醋酸钠,pH值5.2
- 100%,70%的乙醇
2.3。 TOPO克隆和测序分析选定的双链DNA库
- 第 7 次轮选中的PCR产物(可以进行额外的轮继续优化适配子具有约束力)
- pCR2.1 - TOPO载体(Invitrogen公司)
- DH5α,组成电池(Invitrogen公司)
- 质粒试剂盒(QIAGEN)
- M13正向引物
- Informax的Vector NTI公司(Invitrogen公司)
2.4。结合特性的适配
- 适体和控制的寡核苷酸(N 30 CC和N 30,IDT)
- T4多聚核苷酸激酶(New England Biolabs公司)
- γ- 32 P - ATP(3000次/毫摩尔; 10μCi/毫升)
- 纯净S100B的结合缓冲液(5μg/μL的)
2.5。纯净S100B蛋白和选择适配的“三明治”结合试验
- 第一届适体耦合要么A.)Codelink芯片幻灯片或B)金的纳米线。
- 纯化的S100B蛋白,为稀释或者0.125μM70μL)或1μM50μL为B)。
- 第二届适体要么与A标记)Alexafluor 546 Codelink阵列幻灯片,或B),加上50 nm的纳米金与衍生金纳米线的研究。
3。方法
3.1。 PF DNA文库的生成
克劳森和潘,2009年Pan 等人 ,2008年中可以找到详细的方法和适体选择的协议。
3.2。核酸适体的选择使用纯净S100B蛋白
人力S100钙结合蛋白B(S100B.基因ID#6285)被用来作为一个目标。 6标签的他S100B蛋白(98个氨基酸)的表达和纯化使用的QIAexpressionist系统。 (QIAGEN公司)。如果需要的话或表示,他的6个标记酶可以去除。在两轮选拔的,从每一步的1μL样品保存液体闪烁计数来确定整体的结合效率。
3.2.1。 PF的图书馆DNA片段的制备
- 再暂停40μL20毫米的Tris - HCl,pH值7.4的32 +和30 +的片段。
- 热3分钟在85 ° C,并降温至37℃,3分钟孵化器在37 ° C。
- 选择缓冲液添加760μL(氯化钙2.5毫米,5毫米MgCl 2的1X磷酸盐缓冲液,pH值7.4,GIBCO公司)和3分钟37 ° C,然后在室温(RT),保持10分钟。
- 穿过一列载镍NTA琼脂糖珠(QIAGEN公司),选择缓冲区预洗,然后在室温下使用,直到。
3.2.2。镍NTA琼脂糖珠约束S100B在室温下制备
- 离心3秒400μL镍NTA琼脂糖珠,弃上清。
- 400μL结合缓冲液(50毫米的Na 2 HPO 4的NaH 2 PO 4,PH7.2,氯化钠150毫米)轻轻吹打5次,然后降速和上清液冲洗珠。
- 重复步骤2的两倍。
- 加入400μL纯化S100B(5微克/μL结合缓冲液中悬浮),轻轻地吸液管5次,每3分钟共15分钟。
- 降速和上清液。
- 洗净珠约束S100B的400μL结合缓冲液轻轻吹打3倍,然后降速和上清液。
- 重复步骤6两次。
3.2.3。选择的S100B的绑定适配
- 转让32 + - +碎片3.2.1和30珠约束S100B。
- 孵育15分钟,轻轻混匀,轻轻吹打,每3分钟。
- 洗净S100B蛋白- DNA复合物,用800μL结合缓冲液轻轻吹打,然后降速和上清液。
- 重复步骤3两次。
3.2.4。 S100B选择适配的恢复
- 加入200微升20毫米的Tris -盐酸,加热3时85分钟(PH7.4)° C,涡旋混合1分钟和自旋向下,然后将上清转移到一个新的管。
- 一次重复步骤1,并结合上清液。
- 9-12从以前的出版物(11,12)每步净化所选的DNA片段。
3.2.5。 TOPO克隆和测序鉴定的共识适体序列分析
- 克隆选择PCR产物我的第 10轮不pCR2.1 - TOPO载体(Invitrogen公司)。可以做额外的克隆,进行进一步的选择。
- 序列M13正向引物(我们使用的Hershey医疗中心的分子遗传学研究核心设施)40-50单菌落。
- 使用Informax的Vector NTI公司(Invitrogen)的对齐选择的序列。
- 确定的路线为基础的共识序列。
- 从综合的DNA技术共识适配,然后购买。
3.3。对选择适配的“三明治”结合试验
3.3.1。芯片格式 使用荧光标记的第二适配。
- 1共识ST适配合成5' - amineC6基团。他们在打印缓冲区的终浓度为15微米的悬浮到Codelink激活幻灯片使用一个Apogent发现微网Arrayer在DNA芯片的设施电源,大学园区(GE医疗/生物科技公司Amersham公司)发现),以下Codelink推荐的协议。每张幻灯片都印有12阵列。
- 在一个2 × 8格式的芯片杂交纸盒(数组,TeleChem国际)进行杂交。芯片盒是密封的使用无核酸粘接密封箔(AlumaSeal二,研究产品国际),以防止水分蒸发。
- S100B蛋白在PBS稀释到适当的浓度在70μL,并应用到芯片盒井。绑定Codelink幻灯片上印的适配是在室温下1小时。录像带井,然后单独洗涤3X用PBS + 5毫米氯化镁2(PBSM),多余的缓冲液洗被抹杀。 PBSM在70μL0.125微米稀释荧光标记的适配,然后加热到85℃,3分钟,3分钟就冰。适配应用的芯片卡式的井,并在室温下1小时孵育。韦尔斯再次单独洗涤PBSM 3X。录像带,然后拆开,广告PBSM冲洗整个幻灯片。离心的幻灯片,然后彻底干燥,并使用一个扫描惠普生物科技ScanArray 4000XL(Perkin Elmer公司)扫描。
3.3.2。衍生物纳米线的格式,使用2次,再加上50 nm的纳米金适配
黄金NWS(〜5微米的长度,直径在320纳米)的合成在多孔氧化铝膜的恒电按照先前公布的协议(13,14)。纳米线多孔膜解散后,悬浮于1 mL无水乙醇。
如上所述,DNA是从综合的DNA技术购买。纳米金(50纳米)均购自特德佩拉。硫醇盐的DNA切割100毫米0.1 M磷酸钠pH值8.3一小时的数码地面电视,然后在离心旋转10柱纯化。
黄金纳米线和纳米粒子的核酸适体附件
一位50μLAu的纳米线等分放入0.5 mL的不粘离心管中,并冲洗成10 mM的磷酸盐缓冲液,300毫米氯化钠,pH值7.4。在5'端(在5 10吨间隔“结束)硫醇盐的DNA是在终浓度为0.4μM电线。该样本是振荡30分钟,然后冲洗三次离心(8100克)与10毫米的磷酸盐缓冲液,300毫米氯化钠,pH 7.4和50毫米5毫米氯化镁 2,pH值7.2的磷酸盐缓冲液,三次。悬浮于100μL的缓冲稀释一半的DNA涂层的电线。
衍生的DNA -金纳米粒子的制备,加入50μL100毫米第二届适体(一个10吨的5' -端的间隔)至1 mL,50 nm的金纳米粒子,并加热,在37 °为一小时彗星。加热后,增加了10毫米磷酸钠缓冲液,1M氯化钠,pH值7.4(100μL,150μL和128μL25μL两次)每隔0.5小时。共轭左37 ° C过夜,使用前加热块上。样品50毫米5毫米氯化镁2,pH值7.2的磷酸盐缓冲液,冲洗3次。偶联物悬浮于120μL的缓冲区。
对纳米线的夹心杂交
DNA包覆线,1μL的稀释,添加到缓冲区的PCR管。 S100B蛋白或HtrA1控制的蛋白(1μg/μL的)加入终浓度为50μL缓冲(〜10-12每平方纳米Au的纳米线表面的蛋白质分子添加)1微米。样品振荡1〜2小时。电线50毫米5毫米氯化镁2,pH值7.2的磷酸盐缓冲液,离心(8100克)冲洗三次,分别重悬于20μL金纳米粒子/ DNA的结合物。振荡在2小时的结合物,电线,然后冲洗,离心(1300克)的5倍,5毫米MgCl 2的50 mM磷酸盐缓冲液, pH值7.2除去多余的纳米粒子。对样品进行了重悬于20μL缓冲和干金FE - SEM分析涂层的硅片上。
纳米线的FE - SEM图像,获得使用狮子座1530场发射扫描电子显微镜在5.00千伏工作电压的肖特基场发射电子源。
4。代表性的成果
图1。 5' -引物(功率因数为1), 引物(PF 2)协议。
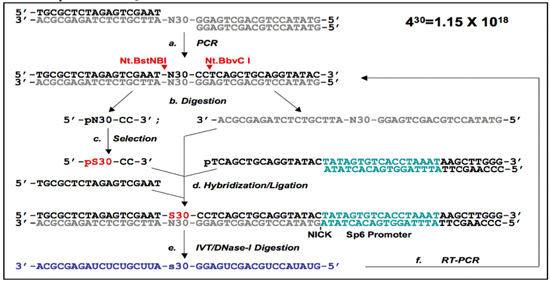
(一)功率因数为1的DNA适配子选择协议。库寡核苷酸退火在一起,并受到PCR扩增产生一个双链DNA库(A)。 5'端引无(功率因数为1)从PF的单链DNA库随机地区准备Nt.BstNBI / Nt.BbvCI消化(用红色箭头标记的切割位点)和凝胶纯化,并自凝胶净化(二)桥(黑色箭头)是孤立的。 (三)选择后,选定的序列(PS30 - CC)杂交及其相应的低聚物和自我桥结扎重新生成以前删除的底漆地区。在这个阶段,引物引入包含在3' -末端的SP6启动子(D)。这是包含选定区域(E)用于转录的RNA。最后,RNA是完全重新扩增(模板DNA消化)用RT - PCR技术(F),和选定的子库,准备下一轮的选择。
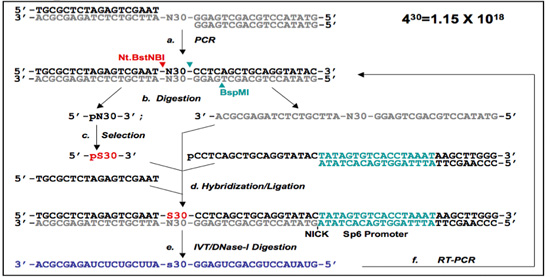
(二)的PF 2的DNA适配子选择协议。库寡核苷酸退火和PCR扩增产生一个双链DNA库(A)。无底漆(PF 2)从PF的单链DNA库随机地区准备Nt.BstNBI / BspMI消化(削减网站用箭头表示)和凝胶净化。自我桥是孤立的,无论是从功率因数为1协议和/或开始Nt.BstNBI(二)库单消化,加上凝胶净化。 (三)选择后,选定的序列(指定PS30)杂交及其相应的低聚物和自我的桥梁,并结扎再生先前删除的底漆地区。在功率因数为1,引物引入包含3' -末端的SP6启动子(D )。这是包含选定区域(E)用于转录的RNA。那么,RNA是专门reamplified用RT - PCR(F),和选定的子库,准备下一轮的选择。
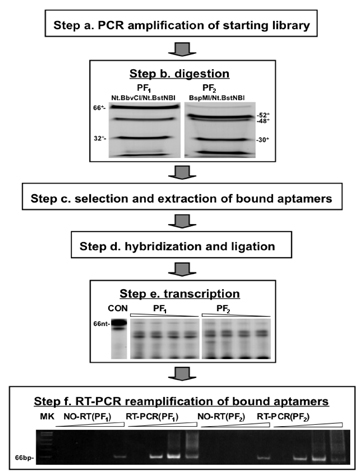
图2。示意图和实验结果/减少到实践的PF选择协议。指定步骤如图1所示的对应。 PCR扩增(步骤一)与限制性内切酶(如表示)兴建的PF库后的消化,消化产品10%的凝胶上分离变性条件下逐页。与PF 1 PF 2选择协议获得相应片段(步骤b)所示。 (步骤三)选择后,势必适配杂交与其相应的低聚物和自我桥,连接再生先前删除的底漆地区。 3' -末端,引物引入包含SP6启动子3' -末端(步骤d)。32 P标记的RNA转录使用结扎产品1,0.5,0.25,0.125 5μL反应液,并6%凝胶上分离变性条件下(步骤e)逐页。笔录,然后用DNase处理,以消除未被选中的随机DNA区域,反转录成cDNA,然后为7,14,21或28个PCR循环reamplified。 8%非变性条件下凝胶的产品是按页分开。 66 NT片段全长的产品,包含选定的PS30 - CC和PS30序列的5'和3'侧翼序列内重新嵌入。迁移PhiX174/HinfI标记显示在左边(步骤六)。控制包括遗漏的反转录(RT)加强。一个少量的产品在这些样品中可以看出在高循环次数;这大概可以完全与第二个(或长期)的DNA酶消化步骤消除。
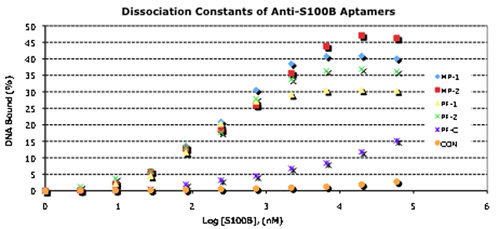
图3。选择适配和其配对使用夹心格式的结合特性 。
A.浓度属32个P -适体结合Kd值测定。使用G - 32的P - ATP(3000Ci /适配是5' -结束标记〜10 MCI)和T4多聚核苷酸激酶(New England Biolabs公司),并具有约束力的毫摩尔,被确定为。
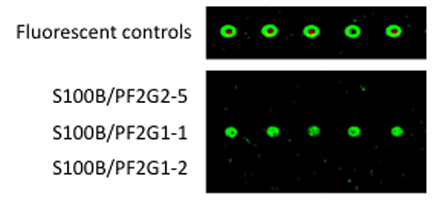
B. 5' -胺衍生物1 ST适配加上Codelink芯片。纯净S100B蛋白势必会第一届适体,幻灯片彻底冲洗,并AlexaFluor546标记, 第二届适体是必然第一届适体:S100B蛋白复合物。通过冲洗后,荧光定量使用ScanArray扫描仪。

C. 5' -巯基衍生物第一适配加上金纳米线的使用标准硫醇化学。 第二适配被耦合到50 nm的金纳米粒子以相同的方式。纯净S100B蛋白(左)或纯化HtrA1控制蛋白质(右),那么势必首先衍生的纳米线。彻底冲洗后, 第二届适体的50 nm的金纳米粒子随后被绑定1 日 ,适体纳米线:S100B蛋白复合物。经过清洗后,势必夹心复合物使用场发射扫描电子显微镜的可视化。比例尺= 1微米。
披露声明
致谢
我们感谢克雷格保罗在他的帮助芯片的核心设施。这项工作得到了NIH / NCI的津贴#CA118591的iMAT计划。民主左翼联盟也承认一个宾夕法尼亚州的财政支持空间格兰特财团奖学金。本刊物是由美国宾夕法尼亚州立大学材料研究所纳米加工网络和美国国家科学基金会合作协议0335765号,国家纳米技术基础设施网络,与美国康乃尔大学的支持。
材料
| Name | Company | Catalog Number | Comments |
| Tris-HCl | |||
| HotMaster TAQ DNA Polymerase | 5 PRIME | ||
| dNTP Mix | Sigma-Aldrich | ||
| Acrylamide | Fisher Scientific | ||
| UltraPure 10X TBE Buffer | Invitrogen | ||
| Ammonium Persulfate | Bio-Rad | ||
| TEMED | Fisher Scientific | ||
| PhiX174 DNA/Hinf I DNA Marker | Promega Corp. | ||
| Ethidium Bromide | |||
| α-32P-dCTP | |||
| Phenol:ChCl3:IAA | Ambion | ||
| NaCl | |||
| Ethanol | |||
| Restriction Enzymes | New England Biolabs | ||
| Urea | Fisher Scientific | ||
| Photographic Film | ECE Scientific | ||
| PBS | GIBCO, by Life Technologies | ||
| CaCl2 | GIBCO, by Life Technologies | ||
| MgCl2 | GIBCO, by Life Technologies | ||
| Ni-NTA Agarose Beads | Qiagen | ||
| Polypropylene Column | Qiagen | ||
| NaHPO4 | |||
| NaAc | |||
| Detroit-551 cells | |||
| SK-MEL-31 cells | |||
| MEM | |||
| TrypLE Express | GIBCO, by Life Technologies | ||
| T4 DNA Ligase | New England Biolabs | ||
| Dimethyl Sulfoxide | Promega Corp. | ||
| Sp6 RNA Polymerase | Promega Corp. | ||
| RNase-Free DNase I | Promega Corp. | ||
| RNase Inhibitor | Promega Corp. | ||
| SensiScript Reverse Transcriptase | Qiagen | ||
| pCR-2.1-TOPO Vector | Invitrogen | ||
| DH5α Compotent Cells | Invitrogen | ||
| Plasmid Mini Kit | Qiagen | ||
| Vector NTI | Invitrogen | ||
| T4 Polynucleotide Kinase | New England Biolabs | ||
| γ-32P-ATP |
参考文献
- Kulbachinskiy, A. V. Methods for selection of aptamers to protein targets. Biochemistry (Moscow). 72, 1505-1518 (2006).
- Mairal, T. Aptamers: molecular tools for analytical applications. Anal Bioanal Chem. 390, 989-1007 (2008).
- Stoltenburg, R., Reinemann, C., Strehlitz, B. SELEX -- A (r)evolutionary method to generate high-affinity nucleic acid ligands. Biomolec Engineering. 24, 381-403 (2007).
- Que-Gewirth, N. S., Sullenger, B. A. Gene therapy progress and prospects: RNA aptamers. Gene Ther. 14, 283-2891 (2007).
- Cowperthwaite, M. C., Ellington, A. D. Bioinformatic analysis of the contribution of primer sequences to aptamer structures. J Mol Evol. 67, 95-102 (2008).
- Shtatland, T., Gill, S. C., Javornik, B. E. Interactions of Escherichia coli RNA with bacteriophage MS2 coat protein: genomic SELEX. Nucleic Acids Res. 28, E93-E93 (2000).
- Jarosch, F., Buchner, K., Klussmann, S. In vitro selection using a dual RNA library that allows primerless selection. Nucleic Acids Res. 34, E86-E86 (2006).
- Vater, A., Jarosch, F., Buchner, K., Klussmann, S. Short bioactive Spiegelmers to migraine-associated calcitonin gene-related peptide rapidly identified by a novel approach: tailored-SELEX. Nucleic Acids Res. 31, E130-E130 (2003).
- Wen, J. D., Gray, D. M. Selection of genomic sequences that bind tightly to Ff gene 5 protein: primer-free genomic SELEX. Nucleic Acids Res. 32, E182-E182 (2004).
- Musheev, M. U., Krylov, S. N. Selection of aptamers by systematic evolution of ligands by exponential enrichment: addressing the polymerase chain reaction issue. Anal Chim Acta. 564, 91-916 (2006).
- Pan, W. H., Clawson, G. A. Primer-free aptamer selection using a random DNA library. Methods Mol Biol. , (2009).
- Pan, W., Xin, P., Clawson, G. A. Minimal-Primer and Primer-Free SELEX Protocols for Selection of Aptamers from Random DNA Libraries. BioTechniques. 44, 351-360 (2008).
- Nicewarner-Pena, S., Freeman, G., Reiss, B. Submicrometer metallic barcodes. Science. 294, 137-141 (2001).
- JC, H. u. l. t. e. e. n., CR, M. a. r. t. i. n. A general template-based method for the preparation of nanomaterials. J Materials Chem. 7, 1075-1087 (1997).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。