需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
成像免疫突触动力学内皮平面细胞模型
摘要
Adaptive immunity is controlled by dynamic 'immunological synapses' formed between T cells and antigen presenting cells. This protocol describes methods for investigating endothelial cells both as understudied physiologic APCs and as a novel type of 'planar cellular APC model'.
摘要
适应性免疫是通过T细胞和抗原呈递细胞('的APC')之间动态相互作用调节被称为"免疫突触'。在这些贴心的细胞与细胞间的接口MHC /银TCR,F-肌动蛋白,粘连分离亚细胞簇和信号分子形成和重塑迅速。这些动力被认为是双方的效率和发展的免疫应答的质量的关键因素,因此,保护与病理性免疫。免疫突触生理装甲运兵车的当前的理解是可获得的成像分辨率不足的限制。尽管人造材料模型 (例如,平面脂质双层)提供了出色的分辨率和一直非常有价值的工具,它们是固有的非生理性和过于简单。血管和淋巴管内皮细胞已经成为"半职业的一个重要的外周组织(或基质)隔人装甲运兵车"。这些装甲运兵车(其中表达最专业的装甲运兵车的分子机器)都形成几乎平坦的细胞表面的独特的功能,且很容易转染的(例如,用荧光蛋白记者)。本文将描述一个基本的方法来实现的内皮细胞作为一种新颖的和生理'平面蜂窝APC模式"为改进的成像和基本的抗原性信令过程的询问。
引言
T淋巴细胞是其特征在于,以有效地识别肽抗原(Ag)材料的能力适应性免疫系统势必主要组织相容性复合体(MHC)的一个分支分子通过它们的T细胞受体(TCR)1。幼稚淋巴细胞组成迁移和扫描的专业抗原呈递细胞"(的APC;例如,树突细胞)的淋巴结内,而记忆/效应T细胞需要能够有效地测量极其广泛外周组织内APC和潜在的靶细胞。
在下面的APC的初始确认同源Ag的分,淋巴细胞逮捕他们的迁移,并开始形成一个专门的亲密细胞间的接口称为"免疫突触"(IS)。持续(即,30-60分钟)IS触点需要以扩增和维持信令2-7。新兴的研究确定了IS内,它是在连续的形成和快速řemodeling离散的亚细胞信号传导的微群 (例如,含有MHC /银TCR,F-肌动蛋白,黏附和信号分子)确定的强度和产生的免疫反应2-7质量。然而,动态信息这一过程和调控机制不完全理解8,9。这在很大程度上源于与APC的表面不规则拓扑和细胞-细胞相互作用平面的控制不良取向,问题的深刻限制所需时空成像相关联的技术挑战接近8-10(Figure1A)。
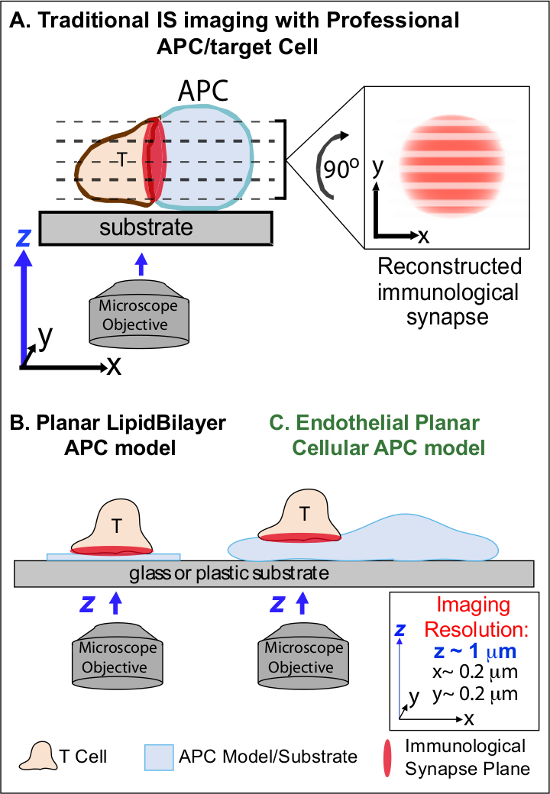
图1.生理平面成像免疫突触动力电池APC模型。该图说明免疫突触的T细胞和professio之间的传统影像最终APC(A)和T细胞与传统的平面脂双层APC模型(B)相比,这种新型内皮平面APC模式(C)。专职APC提供生理免疫突触,但提供取向不良的细胞-细胞接口(即相对于该最佳的xy成像平面;分辨率〜0.2微米),这显着地损害了空间(Z成象平面分辨率〜1微米)和时间(即由于需要通过所有的z成像平面)成像的分辨率反复扫描。双层车型有平面拓扑结构,提供最佳的时空成像分辨率,而且还高度简化,非生理性和刚性。这种内皮细胞模型结合脂质双层的平面拓扑与经典的APC的生理基板于生理环境提供最佳的空间和时间分辨率的成像。M /文件/ ftp_upload / 53288 / 53288fig1large.jpg"目标="_空白">点击此处查看该图的放大版本。
以前的工作已部分规避这些障碍通过开发平面衬底的模型(即,脂双层和抗体包被的表面上)提供最佳的时空分辨率(即,经由T细胞活化表面固定到一个单一的计划,是平行于最佳的xy成像平面)11-15日 (图1B)。这些模式促进了重要的见解控制抗原信号的T细胞,包括动态肌动蛋白/ TCR信号微群7,11-14的发现的亚细胞/分子动力学。然而,这种模型被固有地过于简化,以及刚性(排除的三维拓扑特征的发展/研究)( 图1B)。因此,尚不能确定如何与这样的调查结果PHYsiologic细胞与细胞免疫监视。
虽然仍然充分研究,血管及淋巴管内皮细胞正在成为一个大的( 即 ,更大数量比所有专业的装甲运兵车,由〜1000倍)的"半专业"的APC 16-18周边室。这些细胞表达MHC-I-,MHC-II-和多种共刺激分子(例如,CD40,LFA3,ICOSL,4-1BB,OX40L,TL1A,PD-L1,但不是CD80和CD86),并在战略上是位于血液组织界面,他们成为专业的定点功能16-18。以往的研究表明,内皮细胞可以有效地重新刺激效应/记忆,但不幼稚,T细胞19-25。因此,血管内皮细胞有可能在周围组织内的适应性免疫反应,如对T细胞的活化,分 化,存储器和公差16,17,26局部影响的效应阶段发挥独特的APC的作用。 CRI的角度讲,当在体外生长的细胞,内皮细胞形成几乎平坦的细胞表面,且很容易转染的(例如,用荧光蛋白记者)。这些特性非常适合拓扑动态过程中细胞间的相互作用19,27的高时空分辨率的成像。因此,内皮细胞可作为生理"平面细胞APC"的模式明显适合于驱动抗原识别和调节反应( 图1C)19,20的亚细胞/分子重塑机制的研究。
先前建立互补的成像技术(包括内皮细胞的细胞膜和胞浆内的荧光蛋白制造商的转染),用于粘附和跨内皮迁移27期间学习白细胞-内皮相互作用的细节,显示,白细胞由动态主动探测内皮的表面插入的亚微米级的D-回缩,肌动蛋白富圆柱形突起(〜在直径和深度200-1,000纳米)称为invadosome状突起(即,'ILPS')27,28。这些成像方法已被进一步扩大以及创造的协议采取的内皮APC功能优势,开发的第一个方法为T细胞与内皮细胞免疫突触的高时空分辨率成像报告19,20和进一步说明在此。从这个新的平面细胞APC模型推导出一个核心发现是,T细胞ILPS无论是在推动初期银检测和维持后续信号功能。事实上,多个ILPS(被稳定和应计响应初始钙通量)显示富集TCR和分子暗示的积极信号,例如PKC-Q,ZAP-70,磷酸和HS1的阵列。因此,ILPS似乎代表一个三维生理等效于TCR的信令微集群出现在平面双层模型。这种做法,因此,敏感地揭示/报道分子和建筑(以及隐含的生物力学)动力学没有其他检测。
本文所描述的方法应是有益的桥连专职APC和人工APC的基底模型之间的间隙,以提高我们的询问适应性免疫应答的基本机制的能力。而这里的重点是对CD4 + Th1型效应/记忆细胞的活化,这基本的方法可以容易地修改,以研究各种T细胞类型和AGS,如下面所讨论。
研究方案
在这个协议中描述的所有实验都与原代人T细胞和市售的初级人内皮细胞(皮肤或肺微血管内皮细胞)涉及人类受试者的。任何研究方案必须通过机构审查委员会的批准,并签署知情同意书必须从规定进行每个献血者。使用此协议进行的实验批准了贝斯以色列女执事医疗中心的内部评级法。
1.准备人CD4 +的Th1效应/记忆T细胞
- 应用止血带捐赠者的手臂,擦拭静脉用酒精,并插入针。慢慢地画将15ml血液进入使用EDTA抗凝真空采血管。当血已经绘就,取出针前解开止血带。马上施加压力,伤口用无菌纱布时针取出。
- 转移到血液50ml管。添加的RPMI-1640在室温在1:1稀释(最终体积30ml)中。小心地覆盖稀ð血到含有15 ml的预过滤的淋巴细胞分离培养基如菲可 - 帕克在RT两个50ml试管。
- 离心在RT梯度30分钟,在1200×g离心在吊桶式转子。而离心制备的T细胞培养基(500毫升的RPMI-1640的50毫升的FCS,5 ml青霉素/链霉素)。
- 在除去50毫升管从离心机中,观察四层:红细胞粒料在底部,帕确,一层细胞含有白血细胞(包括淋巴细胞)和血浆。小心去除白血细胞层用巴斯德吸管和转印在50ml Falcon管中。
- 通过加入RT的RPMI-1460(最多20毫升)中,并在室温在1200×g下离心5分钟,洗白血细胞层。重悬在1ml的T细胞培养基的白血细胞。加入5微升1 ml的细胞悬浮液以250μl的T细胞的培养基在1.5ml离心管中,轻轻混匀上下通过吸管。
- 加入25微升稀释ð细胞悬液,以25微升0.4%台盼蓝。加10μl混合物中,一个标准血细胞计数器的每一侧。
- 将血细胞计数器在低功耗光学显微镜。使用10X物镜计数活已排除了锥虫蓝染料和存在于血球的两面的中间正方形细胞的数目。
- 为了计算细胞浓度,乘以的2格通过100(稀释因子)的平均值,然后乘以10 4,得到的细胞/ ml的数量。
- 调整最终浓度为0.5×10 6个细胞/ T细胞培养基毫升。加1微克的终浓度/ ml的每种细菌超抗原葡萄球菌肠毒素B(SEB)和中毒性休克综合征毒素1(TSST)与细胞的。培养72小时(37℃,5%CO 2)以展开的 CD4 + T细胞群。
- 粒料T细胞(1200×g离心,5分钟),重悬在0.5×10 6个细胞/ T细胞培养基毫升与加入人IL-15(20毫微克/毫升)。淋巴细胞转移至T150烧瓶中。继续扩大/拆分单元格中的全中IL-15每24-48小时根据需要(基于媒体的颜色;也就是说,当媒体变成由粉红色至淡黄色)之后。保持所得到的淋巴细胞群体长达15天。
注:按照设计,这个协议将激活和扩大具体的 CD4 + T细胞是反应性的,以SEB和TSST的子集,然后开车送他们向Th1细胞样效应/记忆表型。其它白血细胞不能存活并在这些条件下生长,使得由步骤1.10的细胞将是至少95% 的 CD4 +,CD45RO + T细胞 19,如可以很容易地通过流式细胞术评估。如果需要,进一步的纯化可容易地通过商购的抗体/磁珠基于阳性或阴性选择的试剂盒来实现的。
2.启动小学的人内皮细胞培养
- 外套T25培养瓶中用纤连蛋白(FN)20微克/毫升在PBS中在无菌条件下。留在RT 30-60分钟。删除FN加入5 ml完全培养基(内皮基础培养基(EBM-2)培养基中添加内皮生长培养基(EGM-2)singlequots)。预温育在37 ℃的细胞培养孵化器中至少30分钟。
- 在37℃水浴解冻冷冻人肺或皮肤微血管内皮细胞(HLMVECs或HDMVECs)的小瓶偶尔轻轻摇动〜2-3分钟。立即细胞转移到含有预热的媒体的T25烧瓶。轻轻转动并放入培养箱中,在37℃。
- 后〜4-6小时更换介质。继续改变媒体大约每48小时(或当媒体变成微黄色),直到板达到〜90-95%汇合。
3.一般拆分和扩展内皮细胞
- 生长细胞〜90-95汇合。这可能需要2-5天。对于拆分,删除媒体和冲洗用PBS。除去PBS,换上新鲜的1X胰蛋白酶最小体积(0.5毫升T25或1.5毫升T75)。轻轻旋转,以覆盖所有表面的胰蛋白酶。在37 °下〜5分钟。监视来自板使用低功率光学显微镜的细胞的分离。
- 当大多数细胞出现圆形或分离,添加5体积(即,相对于加入的胰蛋白酶体积)预热完成的EGM-2培养基中,并轻轻地吸取在烧瓶的表面上以分离所有的细胞。
- 如在1.6-1.7中所述计数内皮细胞用血细胞计数器。沉淀细胞通过离心(5分钟,1200×g离心)。去除上清。加入预热完整的EGM-2 MV媒体调整浓度为每毫升50万细胞。
- 转移的细胞的等分试样到适当的FN-包被的培养皿或培养瓶中以进行维护。轻轻转动并放置在孵化器。在6-12小时镀更改媒体。媒体笑ULD改变大约此后每48小时。
4.内皮细胞转染
注:主内皮细胞难治转由最常见的化学和电穿孔的方法。下面描述的核转染的基于方法允许相对高的转染效率(〜50-70%)。一个有效的替代方法是使用感染的适当病毒载体(见材料表注释)。
- 制备T25或T75烧瓶HLMVECs或HDMVECs的(如需要),以90-95%的confluency.Coat用纤连蛋白(FN)20微克/毫升在PBS中在无菌条件下任显微镜培养皿如德尔塔-T的板的最终密度(对于步骤5)或12毫米的圆形盖玻片放置在24孔细胞培养板(用于步骤6的孔)与上述(2.1),为描述的。
- 加入1毫升完整的EGM-2培养基,以显微镜文化platesor0.5毫升每24井和平衡板的湿度37℃/ 5%CO 2培养箱。
- 收获并计数内皮细胞与步骤3.1-3.3.Centrifuge细胞所需的体积(每个样品0.5百万个细胞),在1200×g离心5分钟,室温。在每个样品100微升RT核转染溶液小心地重悬细胞沉淀。
- 结合100微升细胞悬浮液与1-5微克的DNA。转移细胞/ DNA悬液注入认证的比色皿;样品必须覆盖的反应杯的底部没有气泡。
注 :靶向YFP或红色荧光蛋白在细胞膜上(通过neuromodulin的N-末端20个氨基酸,其中包含翻译后棕榈酰化的信号)构建单独被用来(膜-YFP单独或膜DsRed的单独)或共转染了细胞质体积的标记(例如,膜 -YFP和DsRed的水溶性)。的荧光蛋白标记物的许多排列都可以使用。 - 关闭比色皿盖。将与比色皿细胞/ DNA悬液注入的电穿孔的试管架,并应用电项目S-005。取试管进出该支座一旦程序结束。
- 添加〜500微升预平衡培养基的试管轻柔地从使用在核转染试剂盒中提供的塑料移液管试管取出细胞悬浮液。
- 对于使用显微镜培养板的实验从一个反应划分细胞悬液之间含有预热媒体(步骤4.2-4.3)两个菜一样。对于使用24孔/板,隔板3口井各占一个反应实验。
- 孵育细胞在加湿37℃/ 5%CO 2培养箱和改变介质4-6小时,并再一次在12日至16小时后转染。
5.活细胞成像与分析
- 准备内皮
- 第0天:经由nucleofe共同转染与膜YFP和DsRed的水溶性主HLMVECsction技术作为在步骤4和平板描述到活细胞成像培养板。
- 1天:更换培养基与含有的IFN-γ(100毫微克/毫升)来诱导的MHC-II表达的新鲜培养基。第2天,通过加入20毫微克/毫升的TNF-α到现有媒体刺激转染的细胞。
- 在第3天,孵育内皮用1微克/每细菌超抗原的ML葡萄球菌肠毒素B(SEB)和中毒性休克综合征毒素1(TSST)在37 °下紧接实验30-60分钟。省略了" - 银"控制条件这一步。
- 准备淋巴细胞
- 在与步骤5.1.3平行,制备缓冲液A(无酚红的HBSS),补充有20mM HEPES,pH为7.4和0.5%体积/体积的人血清白蛋白预加热到37 C。取培养的淋巴细胞的样品,并确定所述密度通过用血细胞计数器(步骤1.12-1.17)计数。
- 离心机200万美元的样品池1,200×g离心5分钟,在室温在15ml锥形管中。吸媒体和在2毫升缓冲液轻轻悬浮细胞沉淀A使得无细胞簇依然存在。
- 除去的Fura-2的染料钙,重悬新鲜等分试样在DMSO中,制成原料浓度为1mM。
- 加入2微升的Fura-2原液到T细胞悬浮液(2μM终浓度),盖上管并通过反转所述管,以确保均匀分散染料的立即混合。在37 °下进行30分钟。
- 离心如在步骤5.2.2。吸缓冲区A和20-40微升新鲜缓冲-A温柔而彻底悬浮淋巴细胞。
- 活细胞成像设置和获取
注:各种各样的系统可被用于活细胞成像的直立和倒置的光学显微镜。基本要求包括一个荧光光源和过滤器,CCD照相机,电动滤波器开关和百叶窗,加热的阶段(或microscOPE-安装加热腔室)和软件进行自动图像采集。此协议高数值孔径,高倍率(即,40X,63X)浸油透镜需要以达到必要的空间分辨率。特别必须注意选择合适的荧光光源和镜头的Fura-2型钙成像,因为不是所有都具有必要三百八十零分之三百四十〇纳米的激发波长兼容。另一种方法(与标准的绿色和红色荧光过滤器组兼容)可以与非ratiomentic钙敏感染料中使用(例如,将Fluo-4,RHOD-3),尽管这些不能准确地定量钙流和仅提供一个相对的/定量的读数。- 打开显微镜系统(PC进行操作,显微镜,CCD摄像头,滤光轮和氙灯)。
- 打开指定的软件。
- 设置显微镜/软件自动多通道时间推移成像。包括分步收购的广告。微分干涉对比(DIC),标准的绿色荧光,标准的红色发出荧光和标准的340和380 nm激发的Fura-2图像。设置时间间隔采集10-30秒和20-60〜分的总时间。
- 为的Fura-2影像设置曝光时间。
- 加入新的目标,石油和加载包含只有0.5 1ml缓冲液-A的上加热阶段适配器显微镜菜,并立即打开平衡至37 °C(将于〜2-3分钟)。
- 添加使用20微升吸管休息Fura2装淋巴细胞安装的显微镜菜室。
- 打开亮场成像。选择光路目镜。使用粗调旋钮,使目标与miscoscope盘的底部接触。使用目镜和精细调焦旋钮专注于T细胞在培养皿底部的解决。
- 使用XY工作台控制选择含有至少10个细胞的一个字段。避免过度拥挤的领域和细胞团块,因为这些会造成图像伪影。
- 从明场切换到荧光光源。从目镜成像切换到CCD照相机。设置采集参数 (例如,曝光时间,探测器增益和分档)。使用软件获取静止Fura2-340和Fura2-380图像(从相同的曝光时间为每个,通常在〜200-1,000毫秒的范围内)。
- 使用步骤5.4.1计算Fura2-340 / Fura2-380为每个淋巴细胞描述的方法。执行调整Fura2-340和Fura2-380曝光时间,获取图像并计算比率,直到平均值接近1的重复迭代。
- 为MEM-YFP和红色荧光蛋白设置曝光时间。
- 更换步骤5.3.3.1与miscroscope菜用显微镜菜含有转染,激活或松弛处理(或未经处理;控制)HLMVECs或HDMVECs从细胞培养孵化器(步骤4.5。1)。使用的一次性移液管迅速取出介质,通过加入1〜ml的预热的缓冲液A的冲洗一次。吸,然后加入0.5 1ml缓冲液-A的。
- 确定在明亮的荧光阳性转染血管内皮细胞的存在和出现的健康与良好的细胞间连接领域。
- 调整采集参数(例如,曝光时间,探测器增益和分档)的MEM-YFP和红色荧光蛋白。可以肯定,在每个信道的平均荧光信号强度在25%和检测器的动态范围的75%下降。
- 为的Fura-2影像设置曝光时间。
- 开展活细胞成像实验。
- 使用自动化的软件,开始图像采集和捕获多个间隔的图像,以建立基线。
- 在采集期间申请〜5微升浓的Fura-2-加载淋巴细胞(从步骤5.2),以在显微镜菜摄像视场的中心的通过插入小体积(P-5的手指或P-20)移液管进入媒体靠近物镜和喷射慢慢的中心。
- 淋巴细胞下沉到摄像视场,使得在焦点的微调,以确保T细胞 - 内皮细胞接口(免疫突触)被保持在焦平面上。随着40和63X客观的,〜每场10-20细胞是最佳的。如果较少的细胞在成像领域的重复步骤5.3.4.2观察。
- 后实验所需的观察间隔竞争,继续成像和立即吸管洛诺霉素直接进入miscoscope菜(使用技术如5.3.4.2)至2微米的最终浓度以诱导最大钙通量/的Fura-2信号的信号(即,校准的一种手段,见分析5.4。)。
- 作为替代5.3.4.4after实验所需的观察间隔竞争,立即吸出缓冲液A和它与以0.5ml固定液(在PBS中3.7%的甲醛)5分钟替换室温,随后漂洗三次,用PBS。然后继续第6步。
- 活细胞成像分析
注:保存获取的文件后,它们可直接分析或通过各种各样的脱线的图像分析软件应用导出进行分析。 ImageJ的是一个特别有价值的,高度灵活的包是免费提供,并与几乎每一个采集软件兼容。在步骤5.1-5.3中描述的成像实验的设计将产生的淋巴细胞和内皮的APC在缺乏和同源超抗原的存在之间的相互作用的高空间和时间分辨率动态。几乎是无限的分析处理的细胞形态/信令动态影像数据时是可能的。在这个特殊的议定书中所描述的具体目标是协调量化淋巴细胞迁移和信令(即,动力学和细胞内钙离子通量水平)以及动态人改变了免疫突触结构,重点是特定功能( 即 ILPS / PODO印痕)。独立的标准和非标准下面是例子( 即 ,这些实验/问题而开发的)分析。- 测量淋巴细胞钙通量
- 选择加法淋巴细胞前获得的初始Fura2-340(340nm处的EX-510 nm的 EM)和Fura2-380(380nm处的EX-510 nm的 EM)的图像。使用这些作为背景图象和数字化从所有时间序列中的每个相应信道的图像的相减。
- 对于每个时间点创建扣除背景的Fura2-340和扣除背景Fura2-380图像(即,340nm处的EX-510 nm的 EM-背景/ 380nm处的EX-510 nm的 EM-背景)的数字比图像。
- 选择合适的软件绘图工具。点击屏幕上绘制我一个圆形区域nterest(ROI)围绕每个细胞。这些将产生为每个淋巴细胞和时间帧的像素平均比率值。
- 绘制所计算的比值作为时间使用适当的软件应用程序(例如,电子表格程序)的功能。通过累加所有每场的淋巴细胞的比率值,并除以该值乘以淋巴细胞的总数为每个时间点计算平均钙通量实验
- 开展lympocyte迁移的跟踪分析。
- 通过使用从每个视频的DIC通道合适的细胞追踪软件应用程序(例如,ImageJ的)分析细胞T细胞的迁移。使用ImageJ细胞示踪插件,手动通过点击它在每个逐行帧识别在每帧中每个电池单元的质心。
- 使用产生的串行XY坐标( 即迁移路径痕迹)来计算平均速度(总距离迁移/总间隔Ø˚F成像)和曲折(总距离迁移/在第一和最后的图像的单元格位置之间的线性端至端的距离)。
- 上的细胞通过细胞基础互相关这些参数与钙通量(5.4.1)动力学。
- 评估距离PODO打印/ ILP密度
- 伯爵ILP形成在每个T细胞总数为定义的时间间隔( 如5分钟后添加T细胞)。这些可识别的离散微米级荧光膜YFP环与黑眼圈的内皮APC共定位于细胞质红色荧光蛋白在细胞粘连的部位。
- 在细胞通过细胞的基础上交叉关联所产生的"ILP指标"与钙通量(5.4.1)的动态。
- 测量PODO打印/ ILP寿命。
- 对于每个PODO打印/ ILP在一个给定的就是计算其寿命的最后时间点的ILP是明显的 - 该时间点时PODO打印/ ILP网络首先出现了。平均ILP使用寿命期每两个IS。
- 上的细胞通过细胞基础互相关这些寿命与钙通量(5.4.1)动力学。
- 评估初始ILP形成和钙流之间的时间关系。
- 对于每一个细胞识别的时间点(帧),在该钙第一高于基准19。
- 对于每个淋巴细胞识别第一PODO打印/ ILP出现时的时间点。
- 对于每一个细胞计算的"偏移时间"从初始PODO打印/ ILP中减去初始钙流出的时间点。平均的值字段中所有的淋巴细胞。正值表示ILP形成之前的钙流,而负数表示相反。
注意:这些实验可以很容易地在生理学相关层剪切流使用市售的平行壁血流图室如1进行9。
- 测量淋巴细胞钙通量
6.修正细胞成像与分析
- 固定终点的T细胞,内皮细胞在形成和染色
- 制备T细胞在1中描述制备内皮细胞( - / + SAG)如步骤5.1(转染,步骤5.1.1是可选的)。取培养的淋巴细胞的样品,并确定所述密度通过用血细胞计数器(第1)计数。
- 转移淋巴细胞培养体积相当于至少3×10 5个淋巴细胞/样品到15ml锥形管中并离心,在200×g离心3分钟。去除上清,悬浮颗粒淋巴细胞在缓冲-A(步骤5.2.1)的6×10 5淋巴细胞/ ml的浓度。
- 从细胞培养孵化器中取出的内皮细胞和(前进一个采样时间)依次抽吸培养基并添加0.5淋巴细胞悬浮液(3×10 5淋巴细胞/样品)中的溶液,并更换至37 °C Incubator。
- 经过适当的温育时间,如上所述,从孔中吸出培养基,并添加足够的固色剂溶液(在PBS中3.7%的甲醛),以完全覆盖样品(例如,在24孔板〜300-500微升)。在室温下孵育5-10分钟。
- 冲洗样品3次用PBS。通过在室温下加入第一抗体60分钟染色(见名单)。如果主抗体针对细胞内蛋白质,附加的透步骤需要由加入足够通透溶液(0.01%的TritonX-100的PBS),以完全覆盖样品在室温1分钟进行的。冲洗样品3次用PBS。添加适当的二级抗体(在某些情况下,伴随荧光鬼笔环肽),用于在室温60分钟。
- 安装在成像幻灯片上的圆形玻璃盖玻片。固定终点的T细胞,内皮细胞在形成和染色。首先成像位置成像幻灯片包含在显微镜舞台上的样品,并选择63X油目的。应用新的浸油。
- 使用明视场成像模式和眼用透镜定位焦平面。切换到萤光并通过眼用透镜检查样品。选择感兴趣的领域。切换到激光扫描方式。
- 使用快速扫描模式和在最宽的领域可能个别地调整激光功率和每个信道的增益,以优化信号,使得,理想的是,所述特定信号强度达到工作至少〜25%,动态范围的不超过75%的的探测器。
- 使用手动聚焦控制,快速通过Z轴扫描,并确定切片的上限和下限(通常所有的信息应包含的厚度为〜15微米的范围内)。选择在〜0.2-1.0微米的范围内的Z轴部厚度。
- 最后,缩放/裁剪成像领域的兴趣,并进行扫描的特定区域。除了具有非常光明的,特异性荧光SIgnal样品中,获取高分辨率三维成像需要扫描和调整,以采集参数的迭代。的目的是获得最大的xy和z轴分辨率,而没有明显的光致漂白。
- 定性通过合适的软件应用程序(例如,图像J),进行所得到的光学切片的数字三维重建分析了IS的三维拓扑的拓扑。通过类似的应用定量评估的荧光信号分布( 如 Pearson的合作,本地化和相关的荧光强度线扫描分析和正交观看)。
结果
使用内皮细胞和结合生理复杂性和专职APC变形的平面脂双层模型的分辨率优点的新型成像方法被开发(图1)。图2提供了典型的迁移,钙流和拓扑动力学与此观察的例子做法。在内皮上没有凹陷,超抗原特异性的 CD4 + Th1细胞淋巴细胞迅速蔓延,极化和横向上内皮表面(图2A)迁移,而熔合钙(未示出)。在〜5-10分...
讨论
总体而言,这一协议描述方法研究内皮细胞作为一)充分研究生理装甲运兵车和ii)作为"平面细胞APC模式"一种新的类型。相对于前者,它已成为日益认识到,非造血外围设备(或"基质")的APCs发挥关键的,非冗余的作用(即,相比于造血的APC)在成形适应性免疫应答16-18。在这样的"半专业"装甲运兵车,血管及淋巴管内皮细胞(这远多于专业装甲运兵车)均名列前茅赞赏16-18。
披露声明
The authors have nothing to disclose.
致谢
We thank Dr. Peter T. Sage for his assistance in generating some of the representative images. This work was supported by an NIH R01 grant to C.V.C. (HL104006).
材料
| Name | Company | Catalog Number | Comments |
| BD Vacutainer stretch latex free tourniquet | BD Biosciences | 367203 | |
| BD alcohol swabs | BD Biosciences | 326895 | |
| BD Vacutainer Safety-Lok | BD Biosciences | 367861 | K2 EDTA |
| BD Vacutainer Push Button Blood Collection Set | BD Biosciences | 367335 | |
| RPMI-1640 | Sigma-Aldrich | R8758-1L | |
| Ficoll-Paque | Sigma-Aldrich | GE17-1440-02 | Bring to RT before use |
| FCS-Optima | Atlanta Biologics | s12450 | Heat inactivated |
| Penicillin-Streptomycin | Sigma-Aldrich | P4458-100ML | |
| Trypan blue | Sigma-Aldrich | T8154-20ML | |
| staphylococcal enterotoxin B | Toxin Technology | BT202RED | Stock solution 1mg/ml in PBS |
| toxic shock syndrome toxin 1 | Toxin Technology | TT606RED | Stock solution 1mg/ml in PBS |
| human IL-15 | R&D Systems | 247-IL-025 | Stock solution 50ug/ml in PBS |
| PBS | Life Technologies | 10010-049 | |
| Fibronectin | Life Technologies | 33016-015 | Stock solution 1mg/ml in H20 |
| HMVEC-d Ad-Dermal MV Endo Cells | Lonza | CC-2543 | Other Human Microvascular ECs can be used, i.e. HLMVECs |
| EGM-2 MV bullet kit | Lonza | CC-3202 | |
| Trypsin-EDTA | Sigma-Aldrich | T-4174 | Stock solution 10x, dilute in PBS |
| amaxa-HMVEC-L Nucleofector Kit | Lonza | vpb1003 | Required Kit for step 4 |
| IFN-g | Sigma-Aldrich | I3265 | Stock solution 1mg/ml in H20 |
| TNF-alpha 10ug, human | Life Technologies | PHC3015 | Stock solution 1mg/ml in H20 |
| phenol Red-free HBSS | Life Technologies | 14175-103 | |
| Hepes | Fisher Scientific | BP299-100 | |
| Calcium Chloride | Sigma-Aldrich | C1016-100G | Stock solution 1M in H20 |
| Magnesium chloride | Sigma-Aldrich | 208337 | Stock solution 1M in H20 |
| Human Serum albumin | Sigma-Aldrich | A6909-10ml | |
| Immersol 518 F fluorescence free Immersion oil | Fisher Scientific | 12-624-66A | |
| Fura-2 AM 20x50ug | Life Technologies | F1221 | Stock solution 1mM in DMSO |
| pEYFP-Mem (Mem-YFP) | Clontech | 6917-1 | |
| pDsRed-Monomer (Soluble Cytoplasmic DsRed) | Clontech | 632466 | |
| pDsRed-Monomer Membrane (Mem-DsRed) | Clontech | 632512 | |
| pEGFP-Actin | Clontech | 6116-1 | |
| Alexa Fluor 488 Phalloidin | Life Technologies | A12379 | |
| Formaldehyde solution 37% | Fisher Scientific | BP531-500 | Toxic, use fumehood |
| Triton X-100 | Sigma-Aldrich | X100-5ML | |
| Falcon 15mL Conical Centrifuge Tubes | Fisher Scientific | 14-959-70C | |
| Falcon 50mL Conical Centrifuge Tubes | Fisher Scientific | 14-959-49A | |
| Falcon Tissue Culture Treated Flasks T25 | Fisher Scientific | 10-126-9 | |
| Falcon Tissue Culture Treated Flasks T75 | Fisher Scientific | 13-680-65 | |
| Corning Cell Culture Treated T175 | Fisher Scientific | 10-126-61 | |
| Glass coverslips | Fisher Scientific | 12-545-85 | 12 mm diameter |
| Falcon Tissue Culture Plates 24-well | Fisher Scientific | 08-772-1 | |
| Delta-T plates | Bioptechs | 04200415B | |
| Wheaton Disposable Pasteur Pipets | Fisher Scientific | 13-678-8D | |
| 1.5 ml Eppendorf tube | Fisher Scientific | 05-402-25 | |
| ICAM1 mouse anti-human | BD Biosciences | 555509 | |
| HS1 mouse anti-human | BD Biosciences | 610541 | |
| Anti-Human CD11a (LFA-1alpha) Purified | ebioscience | BMS102 | |
| Anti-Human CD3 Alexa Fluor® 488 | ebioscience | 53-0037-41 | |
| Anti-MHC Class II antibody | Abcam | ab55152 | |
| Anti-Talin 1 antibody | Abcam | ab71333 | |
| Anti-PKC theta antibody | Abcam | ab109481 | |
| phosphotyrosine (4G10 Platinum) | Millipore | 50-171-463 | |
| Nucleofector II | Amaxa Biosystems | Required electroporator for step 4 | |
| Zeiss Axiovert | Carl Zeiss MicroImaging | ||
| Zeiss LSM510 | Carl Zeiss MicroImaging | ||
| Zeiss Axiovison Software | Carl Zeiss MicroImaging | ||
| NU-425 (Series 60) Biological Safety Cabinet | NuAIRE | Nu-425-600 | |
| Forma STRCYCLE 37 °C, 5% CO2 Cell culture Incubator | Fisher Scientific | 202370 | |
| Centrifuge 5810 | Eppendorf | EW-02570-02 | |
| Hemocytometer | Sigma-Aldrich | Z359629 | Bright-Line Hemocytometer |
| Isotemp Waterbath model 202 | Fisher Scientific | 15-462-2 |
参考文献
- von Andrian, U. H., Mackay, C. R. T-cell function and migration. Two sides of the same coin. N. Engl. J. Med. 343 (14), 1020-1034 (2000).
- Springer, T. A. Adhesion receptors of the immune system. Nature. 346 (6283), 425-434 (1990).
- Shaw, A. S., Dustin, M. L. Making the T cell receptor go the distance: a topological view of T cell activation. Immunity. 6 (4), 361-369 (1997).
- Monks, C. R., Freiberg, B. A., Kupfer, H., Sciaky, N., Kupfer, A. Three-dimensional segregation of supramolecular activation clusters in T cells. Nature. 395 (6697), 82-86 (1998).
- Delon, J., Stoll, S., Germain, R. N. Imaging of T-cell interactions with antigen presenting cells in culture and in intact lymphoid tissue. Immunol Rev. 189, 51-63 (2002).
- Brossard, C., et al. Multifocal structure of the T cell - dendritic cell synapse. Eur J Immunol. 35 (6), 1741-1753 (2005).
- Dustin, M. L. The cellular context of T cell signaling. Immunity. 30 (4), 482-492 (2009).
- Balagopalan, L., Sherman, E., Barr, V. A., Samelson, L. E. Imaging techniques for assaying lymphocyte activation in action. Nat Rev Immunol. 11 (1), 21-33 (2011).
- Cebecauer, M., Spitaler, M., Serge, A., Magee, A. I. Signalling complexes and clusters: functional advantages and methodological hurdles. J Cell Sci. 123, 309-320 (2010).
- Oddos, S., et al. High-speed high-resolution imaging of intercellular immune synapses using optical tweezers. Biophys J. 95 (10), L66-L68 (2008).
- Grakoui, A., et al. The immunological synapse: a molecular machine controlling T cell activation. Science. 285 (5425), 221-227 (1999).
- Bunnell, S. C., et al. T cell receptor ligation induces the formation of dynamically regulated signaling assemblies. J Cell Biol. 158 (7), 1263-1275 (2002).
- Yokosuka, T., et al. Newly generated T cell receptor microclusters initiate and sustain T cell activation by recruitment of Zap70 and SLP-76. Nat Immunol. 6 (12), 1253-1262 (2005).
- Seminario, M. C., Bunnell, S. C. Signal initiation in T-cell receptor microclusters. Immunol Rev. 221, 90-106 (2008).
- Dustin, M. L. Supported bilayers at the vanguard of immune cell activation studies. J Struct Biol. 168 (1), 152-160 (2009).
- Martinelli, R., Carman, C. V., Bradshaw, R. A., Stahl, P. Lymphocyte Endothelilal Interactions. Encyclopedia of Cell Biology. , (2015).
- Choi, J., Enis, D. R., Koh, K. P., Shiao, S. L., Pober, J. S. T lymphocyte-endothelial cell interactions. Annu Rev Immunol. 22, 683-709 (2004).
- Marelli-Berg, F. M., Jarmin, S. J. Antigen presentation by the endothelium: a green light for antigen-specific T cell trafficking?. Immunol Lett. 93 (2-3), 109-113 (2004).
- Sage, P. T., et al. Antigen recognition is facilitated by invadosome-like protrusions formed by memory/effector T cells. J Immunol. 188 (8), 3686-3699 (2012).
- Kumari, S., et al. Actin foci facilitate activation of the phospholipase C-gama in primary T lymphocytes via the WASP pathway . eLife. , (2015).
- Marelli-Berg, F. M., et al. Major histocompatibility complex class II-expressing endothelial cells induce allospecific nonresponsiveness in naive T cells. J Exp Med. 183 (4), 1603-1612 (1996).
- Ma, W., Pober, J. S. Human endothelial cells effectively costimulate cytokine production by, but not differentiation of, naive CD4+ T cells. J Immunol. 161 (5), 2158-2167 (1998).
- Perez, V. L., Henault, L., Lichtman, A. H. Endothelial antigen presentation: stimulation of previously activated but not naive TCR-transgenic mouse T cells. Cell Immunol. 189 (1), 31-40 (1998).
- Epperson, D. E., Pober, J. S. Antigen-presenting function of human endothelial cells. Direct activation of resting CD8 T cells. J Immunol. 153 (12), 5402-5412 (1994).
- Shiao, S. L., et al. Human effector memory CD4+ T cells directly recognize allogeneic endothelial cells in vitro and in vivo. J Immunol. 179 (7), 4397-4404 (2007).
- Marelli-Berg, F. M., Okkenhaug, K., Mirenda, V. A two-signal model for T cell trafficking. Trends Immunol. 28 (6), 267-273 (2007).
- Carman, C. V., et al. Transcellular diapedesis is initiated by invasive podosomes. Immunity. 26 (6), 784-797 (2007).
- Carman, C. V. Mechanisms for transcellular diapedesis: probing and pathfinding by 'invadosome-like protrusions'. J Cell Sci. 122 ((Pt 17)), 3025-3035 (2009).
- Dustin, M. L., Tseng, S. Y., Varma, R., Campi, G. T. T cell-dendritic cell immunological synapses. Curr Opin Immunol. 18 (4), 512-516 (2006).
- Saito, T., Yokosuka, T. Immunological synapse and microclusters: the site for recognition and activation of T cells. Curr Opin Immunol. 18 (3), 305-313 (2006).
- Gomez, T. S., et al. HS1 functions as an essential actin-regulatory adaptor protein at the immune synapse. Immunity. 24 (6), 741-752 (2006).
- Burbach, B. J., Medeiros, R. B., Mueller, K. L., Shimizu, Y. T-cell receptor signaling to integrins. Immunol Rev. 218, 65-81 (2007).
- Vicente-Manzanares, M., Sanchez-Madrid, F. Role of the cytoskeleton during leukocyte responses. Nat Rev Immunol. 4 (2), 110-122 (2004).
- Ma, Z., Janmey, P. A., Finkel, T. H. The receptor deformation model of TCR triggering. Faseb J. 22 (4), 1002-1008 (2008).
- Ma, Z., Sharp, K. A., Janmey, P. A., Finkel, T. H. Surface-anchored monomeric agonist pMHCs alone trigger TCR with high sensitivity. PLoS Biol. 6 (2), e43 (2008).
- Groves, J. T. Bending mechanics and molecular organization in biological membranes. Annu Rev Phys Chem. 58, 697-717 (2007).
- Xu, C., et al. Regulation of T cell receptor activation by dynamic membrane binding of the CD3epsilon cytoplasmic tyrosine-based motif. Cell. 135 (4), 702-713 (2008).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。