Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Schnelle Ein-Schritt-enzymatische Synthese und All-wässrige Reinigung von Trehalose Analogen
In diesem Artikel
Zusammenfassung
Trehalose analogues are emerging as important molecules for bio(techno)logical and biomedical applications. We describe an optimized protocol for enzymatically synthesizing and purifying trehalose analogues that is simple, efficient, fast, and environmentally friendly. Its application to the rapid production and administration of a probe for the detection of mycobacteria is demonstrated.
Zusammenfassung
Chemisch-Versionen von Trehalose modifiziert oder Trehalose-Analoga, haben Anwendungen in der Biologie, Biotechnologie und der pharmazeutischen Wissenschaft, unter anderen Bereichen. Zum Beispiel haben Trehalose - Analoga Lager nachweisbar Tags verwendet worden Mycobacterium tuberculosis zu erkennen und können Anwendungen wie Tuberkulose diagnostische Bildgebungsmittel haben. Hydrolysestabile Versionen von Trehalose sind auch für die Verwendung als nicht-kalorische Süßstoffe und biologische Schutzmittel aufgrund ihres Potentials verfolgt. Trotz der Attraktivität dieser Klasse von Verbindungen für verschiedene Anwendungen, bleibt ihr Potenzial unerfüllt aufgrund des Fehlens eines robusten Weg zu ihrer Herstellung. Hier berichten wir ein detailliertes Protokoll für den schnellen und effizienten Ein-Schritt-biokatalytische Synthese von Trehalose-Analoga, die die Probleme im Zusammenhang mit der chemischen Synthese umgeht. Durch die Verwendung der thermo Trehalose - Synthase (Tret) Enzym aus Thermoproteus Tenax, Trehalose - Analoga können generat seined in einem einzigen Schritt aus Glucose-Analoga und Glucose Uridindiphosphat in hoher Ausbeute (bis zu Umsatz) in 15-60 min. Eine einfache und schnelle nicht-chromatographischen Reinigungsprotokoll, das von Spindialyse und Ionenaustausch besteht, können viele Trehalose Analoga bekannter Konzentration in wässriger Lösung in weniger als 45 min zu liefern. In Fällen, in denen nicht umgesetzten Glucoseanalog noch chromatographische Reinigung des Trehalose analogen Produkt verbleibt, kann durchgeführt werden. Insgesamt bietet dieses Verfahren eine "grüne" biokatalytische Plattform für die beschleunigte Synthese und Reinigung von Trehalose-Analoga, die auf nicht-Chemiker effizienter und leichter zugänglich ist. Um die Anwendbarkeit dieses Verfahrens veranschaulichen, beschreiben wir ein Protokoll für die Synthese, die alle wässrigen Reinigung und Verwaltung eines Trehalose-basierten Klick-Chemie-Sonde Mycobakterien, von denen alle dauerte weniger als 1 Stunde und ermöglicht Fluoreszenzdetektion von Mykobakterien. In Zukunft stellen wir uns, dass unter OTHer Anwendungen kann dieses Protokoll zur schnellen Synthese von Trehalose-basierte Sonden für Tuberkulose-Diagnostik eingesetzt werden. Zum Beispiel kurzlebigen Radionuklid-modifizierte Trehalose - Analoga (zB 18 F-modifizierte Trehalose) könnte für fortgeschrittene klinische Bildgebungsverfahren wie die Positronen - Emissions - Tomographie-Computertomographie (PET-CT) eingesetzt werden.
Einleitung
Trehalose ist ein symmetrisches nicht reduzierenden Disaccharid , bestehend aus zwei Glucose - Einheiten, die von einem 1,1-α, α-glycosidische Bindung (1A) verbunden sind. Während Trehalose von Menschen und anderen Säugetieren nicht vorhanden ist, ist es häufig in Bakterien, Pilzen, Pflanzen und wirbellosen Tieren 1 gefunden. Die primäre Rolle von Trehalose in den meisten Organismen ist gegen Umwelteinflüsse zu schützen, wie Austrocknungs 1. Darüber hinaus erfordern einige menschliche Pathogene Trehalose für die Virulenz, einschließlich der Tuberkulose verursachende Mycobacterium tuberculosis, die für den Bau von immunmodulatorischen Glycolipide 2 Trehalose als Mediator der Zellhülle Biosynthese und als Baustein verwendet.
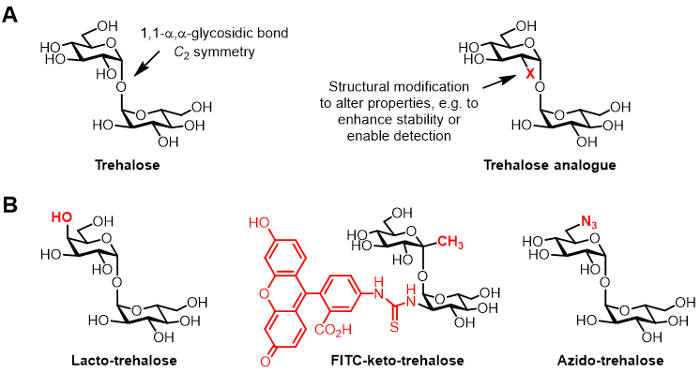
Abbildung 1: Trehalose Trehalose und Analoga. (A) Strukturen der natürlichen Trehalose und eine unnatürliche Trehalose-Analogon, wobei X eine strukturelle Modifikation ist. (B) Beispiele für Trehalose - Analoga in der Literatur berichtet , dass mögliche Anwendungen in Biokonservierung und bioimaging haben.
Aufgrund seiner einzigartigen Struktur und physiologischen Funktionen hat Trehalose 3 große Aufmerksamkeit für den Einsatz in Bio (techno) logischer und biomedizinische Anwendungen gezogen. Die schützenden Eigenschaften von Trehalose beobachtet in natur- zB seine auffällige Fähigkeit in "Auferstehung" Pflanzen Leben erhalten zu helfen , die extreme Austrocknung 4 -Haben spornte seine umfangreichen Einsatz in Biokonservierung Anwendungen unterzogen wurden. Trehalose wurde 3 eine Vielzahl von biologischen Proben, wie Nukleinsäuren, Proteine, Zellen und Gewebe zu erhalten , verwendet. So wird beispielsweise Trehalose als Stabilisierungszusatz in einer Reihe von Arzneimitteln verwendet tHut auf dem Markt sind , darunter mehrere Anti-Krebs - monoklonalen Antikörpern 3. Wie gut, Trehalose als Süßstoff in der Lebensmittelindustrie verwendet werden, und es ausgiebig für Produktschutz sowohl in der Lebensmittel- und Kosmetikindustrie verwendet wird. Die Annahme von Trehalose für diese Arten von kommerziellen Anwendungen wurde zunächst durch die Unfähigkeit beschränkt auf größere Mengen von reinem Trehalose, die aus natürlichen Quellen oder durch Synthese erhalten. Jedoch hat ein effizientes enzymatisches Verfahren zur wirtschaftlichen Herstellung von Trehalose aus Stärke vor kurzem entwickelt worden, die ihre weit verbreitete kommerzielle Nutzung angespornt hat 5.
Chemisch Derivate von Trehalose modifiziert, die hierin als Trehalose Analoga bezeichnet werden , gewonnen haben zunehmende Aufmerksamkeit für verschiedene Anwendungen (generische Struktur gezeigt in 1A; spezifische Beispiele für Trehalose - Analoga in 1B gezeigt) 6. Beispielsweise Lacto-Trehalose ist ein Trehalose-Analogon mit einem seiner Glucose-Einheiten mit Galactose ersetzt, wodurch seine 4-Stellung eine Hydroxylgruppe hat eine invertierte stereochemische Konfiguration. Lacto-Trehalose hat die gleichen Eigenschaften wie Stabilisierungs Trehalose ist jedoch beständig gegenüber Abbau durch Verdauungsenzyme, wodurch es attraktiv als nicht-kalorischen Lebensmittelzusatzstoff 6, 7.
Unsere Gruppe Interesse an Trehalose-Analoga bezieht sich in erster Linie auf ihren Wert als Mykobakterien-spezifischen Sonden und Inhibitoren. Die Barry und Davis Gruppen entwickelten ein Fluorescein-konjugiertes keto-Trehalose - Analogon, genannt FITC-keto-Trehalose, die metabolisch gezeigt wurde , die Zellwand von lebenden M. tuberculosis beschriften, so dass seine Detektion durch Fluoreszenzmikroskopie 8. Das Bertozzi Labor entwickelte kleinere Azido-Trehalose (TreAz) Analoga, die metabolisch die Zellwand bezeichnen könnte und anschließend det seinektiert mit Klick - Chemie und Fluoreszenzanalyse 9. Diese Fortschritte weisen auf die Möglichkeit der Verwendung von Trehalose-basierten Sonden als diagnostische Bildgebungsmittel für Tuberkulose. Trehalose - Analoga wurden auch als Inhibitoren von M. tuberculosis aufgrund ihres Potentials zu stören Wege in dem Bakterium verfolgt worden , die mit 10 für die Lebensfähigkeit und Virulenz wesentlich sind, 11, 12.
Bisher ist das Haupthindernis für Trehalose-Analoga bio (Techno) logisch und biomedizinische Anwendungen zu entwickeln, ist der Mangel an effizienten Synthesemethoden. Die beiden traditionellen Routen zu produzieren Trehalose - Analoga verlassen sich auf die chemische Synthese (Abbildung 2). Ein Weg beinhaltet Desymmetrisierung / Modifizierung von natürlichen Trehalose, während die andere beinhaltet mit geeignet funktionalisierten Monosaccharid-Bausteine Starten und Durchführen der chemischen Glykosylierungschmieden, um die 1,1-α, α-Glykosid-Bindung. Diese Ansätze, die vor kurzem in Übersichtsartikeln diskutiert 13, 14, haben sich als nützlich erwiesen , für die Erfüllung mehrstufige Synthese kleiner Mengen komplexer Trehalose haltige Naturprodukte, wie Sulfolipids-1 von M. tuberculosis 15. Allerdings sind beide Ansätze im allgemeinen ineffizient, zeitaufwendig, unzugänglich nicht-Chemiker, und zusätzlich werden nicht als umweltfreundlich angesehen. So sind bestimmte Arten von Trehalose-Analoga zu synthetisieren, sind diese Strategien nicht ideal.
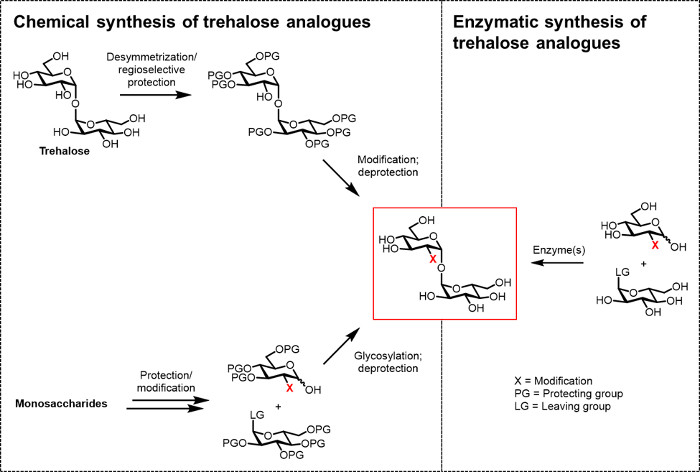
Abbildung 2: Ansätze zur Trehalose analoge Synthese. Chemische Ansätze zur Trehalose analoge Synthese, auf der linken Seite gezeigt, verwenden mehrstufige Verfahren, die schwer protec beinhaltention / Entschützen Desymmetrisierungen und / oder Glykosylierungsschritte. Die enzymatische Synthese, auf der rechten Seite gezeigt, verwendet Enzym (en) zu konvertieren stereoselektiv einfache, ungeschützte Substrate Analoga in wässriger Lösung zu Trehalose. Die enzymatische Protokoll berichtet hierin verwendet eine Trehalose-Synthase (t Ret) Enzym Glucose-Analoga und UDP-Glucose in Trehalose-Analoga in einem einzigen Schritt zu konvertieren. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.
Eine effiziente biokatalytische Route zu Trehalose-Analoga würde die Produktion, Auswertung und Anwendung dieser vielversprechenden Klasse von Molekülen ermöglichen. Während die kommerzielle enzymatisches Verfahren zur Herstellung von Trehalose 5 bis Synthetisieren Analoga nicht anpassungsfähig ist , weil es Stärke als Substrat nutzt, gibt es andere biosynthetische WegWege in der Natur, die für Trehalose analoge Synthese ausgenutzt werden kann. Die Forschung in diesem Bereich, die vor kurzem 6 überprüft wurde, begrenzt. Ein Bericht über ein Verfahren , durch das coli Trehalose Biosyntheseweg Escherichia inspiriert eine einzige Fluor-Trehalose zuzugreifen analog aus den entsprechenden Fluor-Glucose. Allerdings erfordert dieser Ansatz ein Drei-Enzym - System , das die Effizienz und Allgemeinheit 8 begrenzt ist. Ein weiterer Ansatz, der untersucht worden ist , ist zu Trehalose - Phosphorylase (TREp) in der umgekehrten Richtung zu verwenden, die im Prinzip erlaubt die einstufige Synthese von Trehalose Analoga von Glucose - Analogen und Glucose-1-phosphat 6, 16, 17. Obwohl dieser Ansatz künftig Versprechen haben kann, beide Invertierung und Halte TREP noch Nachteile für analoge Synthese. Zum Beispiel haben invertierende TREP einen prohibitiv expensive Donatormolekül (β-D-Glucose-1-Phosphat) und Halte TREP schlechte Enzym Expressionsausbeuten / Stabilität und begrenzte Substratpromiskuität. Signifikante Verbesserungen (zB über Enzym - Engineering) werden vor dem Trep-vermittelte analoge Synthese benötigt werden , ist praktisch.
Derzeit ist die praktischste Vorgehensweise für die enzymatische Synthese von Trehalose - Analoga ist eine Trehalose - Synthase (t Ret) Enzym zu verwenden, die Glucose umwandelt und Uridindiphosphat (UDP) -Glucose in Trehalose in einem einzigen Schritt 6. Wir berichteten vor kurzem die Verwendung von Thermoproteus tenax Tret-und einer thermostabilen Enzyms unidirektionale 18 -bis Trehalose Analoga von Glucose - Analoga und UDP-Glukose (Abbildung 3) 19 synthetisieren. Dieses Enzym wirkt nur in der synthetischen Richtung und vermeidet das Problem von Trehalose Abbau im Trep System nicht gefunden. Dieses einstufige Reaktions could in 1 Stunde abgeschlossen werden, und eine Vielzahl von Trehalose - Analoga wurden in hoher Ausbeute zugänglich aus leicht verfügbaren Glucoseanalog Substrate (siehe Tabelle 1 in den Repräsentative Ergebnisse (bis wie durch Hochleistungs - Flüssigkeitschromatographie (HPLC) bestimmt> 99%) Abschnitt).
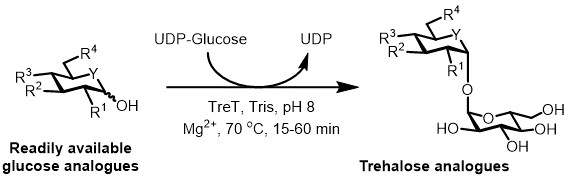
Abbildung 3: t Ret-katalysierte Ein-Schritt - Synthese von Trehalose - Analoga. Der Tret - Enzym von T. tenax stereoselektiv beitreten leicht verfügbar Glukose - Analoga und UDP-Glucose Trehalose - Analoga in einem Schritt zu bilden. R 1 -R 4 = Variable strukturelle Modifikation, beispielsweise Azido-, Fluoro-, Deoxy-, Thio- stereochemischen oder Isotopenmarkierung Modifikationen; Y = variable Heteroatom, beispielsweise Sauerstoff oder Schwefel, oder isotopenmarkierten Heteroatom.
Hier bieten wir adETAILLIERTE Protokoll für den Tret - Syntheseverfahren, einschließlich der Expression und Reinigung von t Ret von E. coli, optimierte Tret Reaktionsbedingungen und ein verbessertes Reinigungsverfahren , die vollständig in der wäßrigen Phase durchgeführt wird. Dieses modifizierte Protokoll ermöglicht die zweckmäßige und effiziente Synthese und Reinigung von Trehalose verschiedenen Analoga auf einer semi-präparativen Maßstab (10-100 mg). Wir zeigen auch die Verwendung dieses Protokolls für die Zubereitung und eine Trehalose-basierenden Sonde mit Mycobakterien in weniger als 1 Stunde verabreicht, die die schnelle Fluoreszenzdetektion von mykobakteriellen Zellen aktiviert.
Protokoll
1. Expression und Reinigung von t Ret von E. coli Top10
HINWEIS: Bitte beachten Sie die Autoren Kontakt mit dem Tret-exprimierenden E. coli - Stamm zu verlangen (pBAD Tret - Plasmid, enthaltend das T. tenax tret - Gen unter der Kontrolle des AraC Protein, verwandelt in Top10 E. coli - 19) und die dazugehörige Materialübertragungsvereinbarung . Das folgende Protokoll gibt typischerweise eine Proteinausbeute von etwa 4 mg / L.
- Bereiten Sie eine 3 ml Übernachtkultur von Tret-exprimierenden E. coli.
- Streak Top10 E. coli , transformiert mit pBAD-Tret - Expressionsvektor auf einem LB-Medium (LB) Agarplatten enthaltend 100 ug / ml Ampicillin.
- Inkubieren der Platte bei 37 ° C für etwa 48 Stunden.
- Wählen Sie eine einzelne Kolonie von der Platte und Beimpfen von 3 ml LB-Flüssigmedium, enthaltend 100 ug / ml Ampicillin in einem Kulturröhrchen.
- Das Röhrchen wird in einem Schüttelinkubator bei 37 & #176; C x über Nacht 175 Umdrehungen pro Minute.
- Induce Proteinexpression in Tret-exprimierenden E. coli.
- Hinzufügen 750 ml Terrific Broth mit 100 ug / ml Ampicillin zu einer 2.800 mL Fernbach-Kulturkolben ergänzt. 1 ml Brühe aus dem Kolben in eine Küvette für die spätere Verwendung als Rohling.
- Fügen Sie die 3 ml über Nacht Kultur erzeugt in Schritt 1.1.4 an die Kulturflasche, dann wird der Kolben in einem Inkubator und schütteln bei 37 ° C x 200 Umdrehungen pro Minute. Prüfen Sie regelmäßig die Absorption der Kultur bei 600 nm im Vergleich zu dem Rohling in Schritt 1.2.1 gesammelt.
- Sobald die Absorption bei 600 nm zwischen 0,5-1,0 erreicht, veran Tret-Expression durch Zugabe von 750 ul 1 M Arabinose-Lösung (1 mM Endkonzentration) zu der Kultur. Bringen Sie den Kolben in den Inkubator und schütteln über Nacht bei 37 ° C x 200 Umdrehungen pro Minute.
- Pellet und die t Ret-exprimierenden E. coli - Zellen zu lysieren.
- Übertragen, um die Kultur zu einem Polypropylen-bottle und zentrifugieren für 15 min bei 4000 × g bei 4 ° C.
- Überstand verwerfen und resuspendiere das Pellet in 15 ml phosphatgepufferter Salzlösung (PBS).
- Übertragen die Zellsuspension in ein 50 ml konisches Röhrchen und zentrifugieren für 15 min bei 4.000 × g bei 4 ° C. Überstand verwerfen und entweder gehen Lyse (Schritt 1.3.4) oder lagern Sie das Pellet auf unbestimmte Zeit bei -80 ° C zu Zelle.
- Man löst 1 Protease - Inhibitor Minitablette in 20 ml Waschpuffer (50 mM NaH 2 PO 4, 500 mM NaCl, 20 mM Imidazol, pH 8,0) in einem 50 ml konischen Röhrchen.
- Übertragung der Protease-Inhibitor enthaltenden Waschpuffer zu dem konischen Rohr, das Pellet enthält. Vortexen, bis das Pellet resuspendiert.
- Übertragen resuspendierten Zellen in ein 100 ml Becherglas gegeben und lysieren die Zellen durch Beschallung (Impulsfolge von 45 Sekunden, 45 Sekunden aus mit einer Laufzeit von 2 min und 15 Sekunden bei einer Amplitude von 75 Prozent).
- Transfer des Lysats in ein 50 ml konisches Metallrohrund zentrifugieren für 60 min bei 15.000 × g bei 4 ° C.
- Klärung des Lysats durch Hindurchleiten durch einen 0,2-0,45 & mgr; m-Spritzenfilter in ein konisches 50 ml-Röhrchen.
HINWEIS: Die typische Konzentration von Lysat erhalten wird, 100 mg / mL.
- Reinige Tret aus E. coli Zelllysat unter Verwendung von Fast - Protein - Flüssigchromatographie (FPLC).
- Stellen Sie die FPLC mit einer Nickel-Affinitätssäule nach oben (5 ml Bettvolumen). Die Säule wird mit 10 ml entionisiertem Wasser oder bis die Kolonne sauber von Verunreinigungen. Äquilibrieren der Säule unter Verwendung von 20 ml Waschpuffer (50 mM NaH 2 PO 4, 500 mM NaCl, 20 mM Imidazol, pH 8,0) bei einer Fließgeschwindigkeit von 1 ml / min.
- Legen Sie das Lysat (20 ml), erhalten aus Schritt 1.3.8 auf die Säule und Eluieren unmarkierte Proteine mit Waschpuffer bei einer Flussrate von 1 mL / min, bis die Extinktion Hintergrundwerte erreicht (typischerweise 80-100 ml Waschpuffer erforderlich) .
- Eluieren His-markierte Tret durch einen linearen g unter Verwendung vonradient Elutionspuffer (50 mM NaH 2 PO 4, 500 mM NaCl, 250 mM Imidazol, pH 8,0) , 1 bis 100% über 60 min bei einer Fließgeschwindigkeit von 1 ml / min. Sammeln Sie 4 ml-Fraktionen bis Tret eluiert wurde und die Absorption erreicht Basisniveau.
HINWEIS: In der Regel werden 60 ml Elutionspuffer sind erforderlich, um das Protein zu eluieren, und das Protein eluiert im 60-100% Elutionspuffer Bereich. Etwa 10-15 ml reinem Tret in Elutionspuffer erhalten. - Bestimme die Konzentration von t Ret durch Extinktion bei 280 nm gegen einen Elutionspuffer blank messen.
- Austausch Tret in Tris (hydroxymethyl) aminomethan (Tris) -Puffer durch Dialyse.
- Nach dem Dialyseschlauch Herstellung gemäß den Anweisungen des Herstellers, es prime durch Spülen mit deionisiertem Wasser und dann Tris-Puffer (50 mM Tris, 300 mM NaCl, pH 8,0).
- Laden Sie die Tret Probe in den Dialyseschlauch mit einer Spritze und stumpfe Nadel. Dialysiere über Nacht eingainst 2 l Tris-Puffer.
- Bestimme die Konzentration von t Ret durch Extinktion bei 280 nm gegen eine Blindprobe von der Dialyse Waschen gesammelt messen.
- Übertragen Sie die Tret-Lösung zu einem 50 ml konischen Röhrchen und fahren Sie mit Trehalose analoge Synthese (Schritt 2) oder lagern Sie das Enzym bei 4 ° C.
HINWEIS: Tret ist ein thermo Protein. Der Tret wurde in Tris-Puffer bei 4 ° C mehrere Monate gelagert, ohne signifikanten Aktivitätsverlust zu beobachten.
2. Eine einstufige Synthese von Trehalose Analogues Verwendung Tret Enzyme
HINWEIS: Das Protokoll unten beschreibt eine Reaktionsskala basierend auf 4 ml Volumen, das etwa 15 bis 30 mg Trehalose analog liefern kann je nach Reaktionseffizienz und das Molekulargewicht des Produkts. Die Reaktionskomponenten können skaliert werden, um mehr oder weniger Trehalose analog zu erhalten, falls gewünscht.
- Zugeben von Glukose Analogon (0,080 mmol, Masse wird von dem Molekulargewicht abhängen), UDP-Glucose (0.160 mmol, 97,6 mg) und MgCl 2 (0,080 mmol, 16,3 mg) in ein 15 ml konischen Röhrchen. Die Endkonzentrationen dieser Komponenten wird 20 mM, 40 mM und 20 mM betragen, respectively.
- Hinzufügen Tret in Tris-Puffer (erhalten aus Schritt 1.5.4), und, falls erforderlich, ein geeignetes Volumen von Tris-Puffer (50 mM Tris, 300 mM NaCl, pH 8,0), um eine endgültige Enzymkonzentration von 300 & mgr; g / mL und einem letzten zu erreichen Volumen von 4 mL. Pipettieren das Gemisch nach oben und unten sanft oder das Rohr invertieren die Feststoffe zu lösen.
- Inkubieren der Reaktion bei 70 ° C mit bei 300 Upm für 1 Stunde Schütteln, dann das Reagenzglas auf Eis zu kühlen.
3. Reinigung von Trehalose-Analoga aus Roh-enzymatische Reaktionsgemisch
- Vorspülen eine Zentrifugal-Filtereinheit (Nennmolekulargewichtsgrenze (NWML) 10 kDa) durch Zugabe von 3 ml entionisiertem Wasser zu der Zentrifugenfiltereinheit und Zentrifugieren bei 3.000 xg trace Glycerin in der Membran zu entfernen, bis die gesamte Flüssigkeit durch den Filter passiertin das Rohr (ca. 20 min). Wiederholen Sie zwei weitere Male. Führen Sie diesen Schritt unmittelbar vor oder während der Reaktion (Schritt 2.3).
- Nach dem Abkühlen der enzymatischen Reaktionsmischung (aus Schritt 2.3) erhaltenen, überträgt es auf die vorgespült Zentrifugalfiltereinheit. Spülen Sie das Reaktionsrohr mit 1 ml deionisiertem Wasser und Transfer zum Zentrifugalfiltereinheit. Wiederholen Spülen des Reaktionsrohres für eine maximale Rückgewinnung des Produkts.
- Zentrifugieren der Zentrifugalfiltereinheit bei 3000 xg, bis die gesamte Flüssigkeit durch den Filter in das Rohr (ca. 20 min). Spülen Sie die obere Kammer des Zentrifugenfiltereinheit mit 3 mL entionisiertem Wasser und Zentrifuge bei 3000 xg, bis die gesamte Flüssigkeit den Filter in das Rohr durchläuft (ungefähr 20 min). Wiederholen Sie dies für eine maximale Rückgewinnung von Produkt zu spülen.
- Entsorgen Sie die obere Kammer des Zentrifugenfiltereinheit. Hinzufügen Mischbett-Ionenaustauschharz (3 g) zu dem Filtrat am Boden des Röhrchens (typisch Filtrat volume ist 8-15 mL auf die Anzahl der Spülgänge abhängig). Rühre bei Raumtemperatur 1 Stunde lang mit einem magnetischen Rührstab mit einer Geschwindigkeit ausreichend, um die Harzkügelchen in der Lösung suspendiert zu halten.
- Dekantiert den Überstand und filtern sie das Harz zu entfernen. 5 ml entionisiertes Wasser, um das restliche Harz zu spülen. Dekantiert den Überstand und filtern sie es mit der Produktlösung aus der ersten Dekantierung kombiniert. Wiederholen Spülen des Harzes für eine maximale Rückgewinnung des Produkts.
- Analyse der Reaktion durch Dünnschichtchromatographie (TLC) oder HPLC, um zu bestimmen, ob eine vollständige Umwandlung des Glucoseanalogausgangsmaterial zur Trehalose analogen Produkt erzielt wurde. Siehe Schritt 4.1 für DC-Analyse und Schritt 4.2 für die HPLC-Analyse.
- Entfernung von Wasser durch Gefriertrocknung oder Rotationsverdampfung des getrockneten Produkts. Wenn kein nicht umgesetzten Glucoseanalog während TLC oder HPLC-Analyse, Reinigung durch Chromatographie beobachtet wurde, ist nicht erforderlich. Wiegen Sie das Produkt der Reaktion yie zu erhaltenld und führen Kernspinresonanz (NMR) Spektroskopie-Analyse (Schritt 4.3) Produktstruktur und Reinheit zu bestätigen.
- Wenn nicht umgesetzten Glucose-Analogon während die DC-Analyse beobachtet wurde, trennen es vom Trehalose-Analogon mit einer Größenausschluss-Spalte.
- Bereiten Sie eine 1 x 100 cm Säule mit entsalztem Wasser gesättigt, extrafein P2 Polyacrylamid Wulstgröße Ausschluss Medien gemäß den Anweisungen des Herstellers.
HINWEIS: Die Größenausschluss-Säule kann nach dem Waschen mit deionisiertem Wasser wiederverwendet werden. - Wieder aufzulösen das getrocknete enzymatische Reaktionsprodukt (erhalten aus Schritt 3.7) in 0,5 ml entionisiertem Wasser. Tragen Sie die Produktlösung auf die Größenausschlusssäule manuell oder durch einen Säulenfluss-Adapter. Spülen Sie das Fläschchen, die das Rohprodukt mit weiteren 0,5 ml entsalztes Wasser enthalten ist, und laden Sie es in die Größenausschlusssäule.
- Eluieren das Produkt mit entionisiertem Wasser durch Schwerkraftfluss und sammeln Fraktionen von ca. 2 mL Volumen.
- Analysieren Sie die Fraktionen durch TLC (Schritt 4.1). Pool der Fraktionen, die reines Trehalose-Analogon.
- Entfernung von Wasser durch Gefriertrocknung oder Rotationsverdampfung des getrockneten Produkts. Wiegen Sie das Produkt die Reaktionsausbeute und gehen Sie auf die NMR-Analyse zu erhalten (siehe Schritt 4.3).
- Bereiten Sie eine 1 x 100 cm Säule mit entsalztem Wasser gesättigt, extrafein P2 Polyacrylamid Wulstgröße Ausschluss Medien gemäß den Anweisungen des Herstellers.
4. Analyse von Trehalose Analoge Produkte
- Führen Sie Dünnschichtchromatographie (TLC) Analyse von Tret - Reaktion.
Hinweis: Dieses Verfahren kann auch verwendet werden, um Grßenausschlusssäule Fraktionen zu analysieren. Es kann notwendig sein, die Reaktionsmischung oder Säulenfraktionen vor der TLC-Analyse zu konzentrieren Verbindung Färbung auf der DC-Platte zu beobachten.- Mark Spuren auf der Oberfläche DC-Platte mit einem Bleistift und anwenden Analyt (en) und relevanten Norm (en) auf die entsprechenden Spuren, einschließlich der Glucoseanalog Standard, der Trehalose analogen Standard (falls vorhanden), dem Reaktionsgemisch (oder Fraktionen gesammelt aus Größe exclusion Säulenreinigung), und ein Co-Spot. jede Probe auf die DC-Platte Nach dem Auftragen kann der Platte zu trocknen.
HINWEIS: Bei Reaktionsanalyse, typischerweise 2 & mgr; l der Probe auf die DC-Platte aufgebracht wird. - Entwickeln Sie die DC - Platte unter Verwendung von n - Butanol / Ethanol / VE - Wasser (5: 3: 2).
- Trocknen Sie die entwickelte DC - Platte, dann tauchen sie in 5% H 2 SO 4 in Ethanol (Zucker - Färbung) und Hitze auf einer heißen Platte auf hohe Einstellung , bis zuckerhaltigen Flecken können ( in der Regel 5 min) sichtbar gemacht werden.
- Mark Spuren auf der Oberfläche DC-Platte mit einem Bleistift und anwenden Analyt (en) und relevanten Norm (en) auf die entsprechenden Spuren, einschließlich der Glucoseanalog Standard, der Trehalose analogen Standard (falls vorhanden), dem Reaktionsgemisch (oder Fraktionen gesammelt aus Größe exclusion Säulenreinigung), und ein Co-Spot. jede Probe auf die DC-Platte Nach dem Auftragen kann der Platte zu trocknen.
- Führen HPLC - Analyse von Tret Reaktionsgemische unter Verwendung einer beliebigen HPLC System, das zur Trennung und Detektion Kohlenhydrate. Dieses Protokoll beinhaltet Kohlenhydrat Trennung eine aminopropyl - HPLC - Säule und Detektion unter Verwendung von Brechungsindex verwendet wird .
- Bringen Sie Aminopropyl-Säule (4,6 x 250 mm) mit einer Vorsäule Guard zur HPLC enthält.
- Aminopropyl-Säule mit 80% Acetonitril in deionisiertem Wasser mit einer Strömungsgeschwindigkeit von 0,4 äquilibrierenml / min.
- Laden Sie die Lösung des Reaktionsprodukts (oder Standard) auf die aminopropyl Spalte.
- Eluieren des Produkts (oder Standard) mit 80% Acetonitril in deionisiertem Wasser mit einer Strömungsgeschwindigkeit von 0,4 ml / min und einer Säulentemperatur von 50 ° C. Üblicherweise werden die Laufzeit beträgt 40 min.
HINWEIS: Sowohl die Glucoseanalogausgangsmaterial und die Trehalose analogen Produkt kann durch Brechungsindex nachgewiesen werden, obwohl andere Verfahren wie beispielsweise Verdampfungslichtstreuungsdetektion (ELSD) verwendet werden könnten. Unter Verwendung der beschriebenen Bedingungen, Glucose-Analoga typischerweise eluieren zwischen 10-15 Minuten und Trehalose Analoga zwischen 15-25 min eluieren.
- NMR - Analyse des gereinigten Trehalose Analoga.
- Man löst gereinigte Trehalose - Analogon in D 2 O (700 & mgr; l) und die Lösung in einem NMR - Röhrchen.
- Erwerben 1 H und 13 C NMR - Spektren gemäß entsprechenden NMR Anlage Protokollen.
5. Anwendung des Tret-synthetisierte Trehalose Analogues zum Nachweis von Mykobakterien
- Synthesize, zu reinigen und zu verwalten , 6-TreAz auf M. smegmatis (Msmeg).
- Liste 6-Azido-6-deoxy glucopyranose (6-GlcAz, 0,020 mmol, 4,1 mg), UDP-Glucose (0,040 mmol, 24,4 mg) und MgCl 2 (0,020 mmol, 4,1 mg) in ein 15 ml konischen Röhrchen.
- Hinzufügen Tret in Tris-Puffer (erhalten aus Schritt 1.5.4) eine endgültige Enzymkonzentration von 300 & mgr; g / ml und einem Endvolumen von 1 ml zu erreichen. Pipettieren das Gemisch nach oben und unten sanft oder das Rohr invertieren die Feststoffe zu lösen.
- Inkubieren der Reaktion bei 70 ° C mit 15 min schütteln.
- Verdünne die enzymatische Reaktionsmischung mit 3 ml entionisiertem Wasser und überträgt es auf einen vorgewaschenen Zentrifugalfiltereinheit (NMWL 10 kDa). Zentrifugieren der Filtereinheit bei 3.000 xg bis der größte Teil der Flüssigkeit durch den Filter in das Rohr, etwa 10 min.
- Verwerfen the obere Kammer des Zentrifugenfiltereinheit. Hinzufügen Mischbett-Ionenaustauscher-Harz (0,75 g) in das Röhrchen und umrühren / schütteln bei Raumtemperatur für 25 min. Dekantiert den Überstand und filtern sie das Harz zu entfernen.
Hinweis: Die Schritte 5.1.1-5.1.5 liefern eine wässrige Lösung von 6-Azido-Trehalose (6-TreAz) bei etwa 5 mM Konzentration in weniger als 1 Stunde. Die 5 mM-Konzentration wird basierend auf der quantitativen Umwandlung von Substrat zu Produkt und dem Verdünnungs geschätzt, dass Orte während der Reinigungsschritte erfolgt unter der Annahme, minimalen Verlust an Produkt während dieser Schritte. Die Lösung kann steril filtrierten vor der Zugabe zu einer biologischen Probe sein, falls gewünscht. - Füge das entsprechende Volumen von 6-TreAz Produktlösung zu einer log-Phasen - Kultur von M. smegmatis (Msmeg), typischerweise eine endgültige Kulturvolumen von 100-1000 & mgr; l zu erreichen , und eine endgültige 6-TreAz Konzentration von ~ 25 uM. Inkubieren der Zellen bei 37 ° C für die gewünschte Zeitdauer, in der Regel 60 min.
- Führen Chemie klicken , um ein Fluorophor an Azid-markierte Zellen zu konjugieren. In diesem Protokoll verwenden , Cu-katalysierte Azid-Alkin - Cycloaddition (CuAAC) ein Fluorophor an Zelloberflächen Aziden in Msmeg zu liefern.
- Zentrifugieren der Zellen bei 3.900 × g für 5 min und anschließend Waschen der Zellen mit PBS 0,5% Rinderserumalbumin enthält. Wiederholen Sie zweimal.
- Re-suspend die pelletierten Zellen in 4% para-Formaldehyd in PBS, sie zu beheben. Nach Inkubation für 10 min, wiederholen Sie Schritt 5.2.1 um die Zellen zu waschen.
- Re-suspend pelletierten Zellen in 138 & mgr; l PBS.
- In 3 ul einer 1 mM Stammlösung von Alkin-Carboxyrhodamin 110 (Alkin-488) in DMSO.
- Werden 3 & mgr; l einer frisch hergestellten 60 mM Stammlösung von Natriumascorbat in deionisiertem Wasser.
- Werden 3 ul einer 6,4 mM Stammlösung von Tris [(1-benzyl-1H-1,2,3-triazol-4-yl) methyl] amin (TBTA) in tert - Butanol / Dimethylsulfoxid (DMSO) 4: 1.
- In 3 & #956; l einer 50 mM Stammlösung von CuSO 4 in entmineralisiertem Wasser.
- Pipettieren die Suspension bis Zelle und ab, dann für 30 Minuten im Dunkeln bei Raumtemperatur inkubiert.
- Wiederholen Sie Schritt 5.2.1, um die Zellen zu waschen. Wieder die Zellen in 150 & mgr; l PBS.
- Führen zelluläre Fluoreszenzanalyse. In diesem Protokoll verwenden , Fluoreszenzmikroskopie zelluläre Fluoreszenz von markiertem Msmeg zu visualisieren.
- In 10 ul bakterieller in PBS suspendierten Zellen auf einen Objektträger und leicht die Flüssigkeit in einer dünnen Schicht ausgebreitet den Rand eines Deck verwenden. Lassen Sie im Dunkeln an der Luft trocknen.
- In 10 ul Eindeckmedium über die getrocknete Probe, dann legen Abdeckung gleitet über die Probe und den Klebstoff (zB Nagellack) zu immobilisieren.
- Bild die Folien ein Fluoreszenzmikroskop bei 100-facher Vergrößerung verwendet wird.
Ergebnisse
T. tenax Tret wurde aus E. coli in einer Ausbeute von etwa 4 mg / L unter Verwendung von Standard - Proteinexpression und Reinigungstechniken erhalten. Eine einzelne Nickel - Affinitätschromatographie Schritt war ausreichend Tret aus E. coli - Lysat (a repräsentativen FPLC trace gezeigt in 4) zu reinigen. Wie in unserer ersten Veröffentlichung auf dem Syntheseverfahren Tret gegründet, ist rekombinantes T. tenax Tret der Lage , eine...
Diskussion
Trehalose - Analoga haben das Potenzial , verschiedene Felder zu beeinflussen, von Konservierung von Lebensmitteln und Arzneimitteln zur Diagnose und Behandlung von mikrobiellen Infektionen 6. Bestehenden vielstufige chemische Syntheseverfahren sind nützlich für komplexe Trehalose Analoga mit mehreren Standorten Modifikations Herstellung (beispielsweise natürlich vorkommende komplexe mykobakterielle Glykolipide). Jedoch sind diese Verfahren immer langwierig und ineffizient, auch wenn ...
Offenlegungen
The authors have nothing to disclose.
Danksagungen
This work was funded by a grant from the National Institutes of Health (R15 AI117670) to B.M.S and P.J.W, as well as a Cottrell College Scholar Award from the Research Corporation (20185) to P.J.W. L.M.M. was supported by a Provost's Fellowship from CMU.
Materialien
| Name | Company | Catalog Number | Comments |
| LB agar | Research Products International | L24021 | |
| Ampicillin sodium salt | Sigma Aldrich | A9518 | |
| Luria broth | Research Products International | L24045 | |
| Terrific Broth | Research Products International | T15050 | |
| L-(+)-Arabinose | Sigma Aldrich | A3256 | |
| Phosphate-buffered Saline | GE Healthcare | SH30256 | |
| Imidazole | Sigma Aldrich | I5513 | |
| Sodium chloride | BDH | BDH9286 | |
| Sodium phosphate, | Fisher Scientific | S374 | |
| monobasic | |||
| Syringe filter, 0.45 µm | Fisher Scientific | 09719D | |
| Protease Inhibitor mini-tablets, EDTA-free | Thermo Scientific | 88666 | |
| HisTrap HP nickel affinity column, 5 mL | GE Healthcare | 17-5248-02 | |
| TRIS base ultrapure | Research Products International | T60040 | |
| Dialysis tubing, MWCO 12–14,000 | Fisher Scientific | 21-152-16 | |
| Glucose analogues | CarboSynth, | Examples of vendors that offer numerous glucose analogues | |
| Sigma Aldrich, | |||
| Santa Cruz Biotechnology, American Radiolabeled Chemicals | |||
| 6-Azido-6-deoxy glucopyranose (6-GlcAz) | CarboSynth | MA02620 | |
| UDP-Glucose | abcam Biochemicals | ab120384 | |
| Magnesium chloride hexahydrate | Fisher Scientific | M33 | |
| Amicon Ultra-15 centrifugal filter unit | EMD Millipore | UFC901008 | |
| Bio-Rex RG 501-X8 mixed-bed ion-exchange resin | Bio-Rad | 444-9999 | |
| Extra-Fine Bio-Gel P2 media | Bio-Rad | 150-4118 | |
| Glass-backed silica gel thin-layer chromatography plates | EMD Millipore | 1056280001 | |
| n-Butanol | Fisher Scientific | A399 | |
| Ethanol | Fisher Scientific | S25310A | |
| Sulfuric acid | Fisher Scientific | A300 | |
| Acetonitrile | EMD Millipore | AX0145 | |
| Deuterium oxide, 99.8% | Acros Organics | 351430075 | |
| Aminopropyl HPLC column | Sigma Aldrich | 58338 | |
| Bovine serum albumin | Sigma Aldrich | 5470 | |
| Para-formaldehyde | Ted Pella | 18505 | |
| Alkyne-488 | Sigma Aldrich | 761621 | |
| Sodium ascorbate | Sigma Aldrich | A7631 | |
| Tris[(1-benzyl-1H-1,2,3-triazol-4-yl)methyl]amine (TBTA) | Click Chemistry Tools | 1061 | |
| tert-Butanol | Sigma Aldrich | 360538 | |
| Dimethylsulfoxide | Sigma Aldrich | W387520 | |
| Copper(II) sulfate | Sigma Aldrich | C1297 | |
| Fluoromount-G mounting medium | Southern Biotechnology | 10001 |
Referenzen
- Elbein, A. D., Pan, Y. T., Pastuszak, I., Carroll, D. New insights on trehalose: a multifunctional molecule. Glycobiology. 13, 17-27 (2003).
- Tournu, H., Fiori, A., Van Dijck, P. Relevance of trehalose in pathogenicity: some general rules, yet many exceptions. PLoS Pathog. 9, 1003447 (2013).
- Ohtake, S., Wang, Y. J. Trehalose: Current use and future applications. J. Pharm. Sci. 100, 2020-2053 (2011).
- Adams, R. P., Kendall, E., Kartha, K. K. Comparison of free sugars in growing and desiccated plants of Selaginella lepidophylla. Biochem. Syst. Ecol. 18, 107-110 (1990).
- Kubota, M., Ohnishi, M. . Glycoenzymes. , (2000).
- Walmagh, M., Zhao, R., Desmet, T. Trehalose analogues: latest insights in properties and biocatalytic production. Int. J. Mol. Sci. 16, 13729-13745 (2015).
- Kim, H. -. M., Chang, Y. -. K., Ryu, S. -. I., Moon, S. -. G., Lee, S. -. B. Enzymatic synthesis of a galactose-containing trehalose analogue disaccharide by Pyrococcus horikoshii trehalose-synthesizing glycosyltransferase: Inhibitory effects on several disaccharidase activities. J. Mol. Catal. B: Enzym. 49, 98-103 (2007).
- Backus, K. M., et al. Uptake of unnatural trehalose analogs as a reporter for Mycobacterium tuberculosis. Nat. Chem. Biol. 7, 228-235 (2011).
- Swarts, B. M., et al. Probing the mycobacterial trehalome with bioorthogonal chemistry. J. Am. Chem. Soc. 134, 16123-16126 (2012).
- Rose, J. D., et al. Synthesis and biological evaluation of trehalose analogs as potential inhibitors of mycobacterial cell wall biosynthesis. Carbohydr. Res. 337, 105-120 (2002).
- Wang, J., et al. Synthesis of trehalose-based compounds and their inhibitory activities against Mycobacterium smegmatis. Bioorg. Med. Chem. 12, 6397-6413 (2004).
- Gobec, S., et al. Design, synthesis, biochemical evaluation and antimycobacterial action of phosphonate inhibitors of antigen 85C, a crucial enzyme involved in biosynthesis of the mycobacterial cell wall. Eur. J. Med. Chem. 42, 54-63 (2007).
- Sarpe, V. A., Kulkarni, S. S. Regioselective protection and functionalization of trehalose. Trends in Carbohydr. Res. 5, 8-33 (2013).
- Chaube, M. A., Kulkarni, S. S. Stereoselective construction of 1,1-alpha,alpha-glycosidic bonds. Trends in Carbohydr. Res. 4, 1-19 (2013).
- Leigh, C. D., Bertozzi, C. R. Synthetic studies toward Mycobacterium tuberculosis sulfolipid-I. J. Org. Chem. 73, 1008-1017 (2008).
- Chaen, H., et al. Efficient enzymatic synthesis of disaccharide, alpha-D-galactosyl-alpha-D-glucoside, by trehalose phosphorylase from Thermoanaerobacter brockii. J. Appl. Glycosci. 48, 135-137 (2001).
- Vander Borght, J., Soetaert, W., Desmet, T. Engineering the acceptor specificity of trehalose phosphorylase for the production of trehalose analogs. Biotechnol. Progr. 28, 1257-1262 (2012).
- Kouril, T., Zaparty, M., Marrero, J., Brinkmann, H., Siebers, B. A novel trehalose synthesizing pathway in the hyperthermophilic Crenarchaeon Thermoproteus tenax: the unidirectional TreT pathway. Arch. Microbiol. 190, 355-369 (2008).
- Urbanek, B. L., et al. Chemoenzymatic synthesis of trehalose analogues: rapid access to chemical probes for investigating mycobacteria. ChemBioChem. 15, 2066-2070 (2014).
- Rostovtsev, V. V., Green, L. G., Fokin, V. V., Sharpless, K. B. A stepwise Huisgen cycloaddition process: copper(I)-catalyzed regioselective "ligation" of azides and terminal alkynes. Angew. Chem. Int. Ed. 41, 2596-2599 (2002).
- Tornøe, C. W., Christensen, C., Meldal, M. Peptidotriazoles on solid phase: [1,2,3]-triazoles by regiospecific copper(I)-catalyzed 1,3-dipolar cycloadditions of terminal alkynes to azides. J. Org. Chem. 67, 3057-3064 (2002).
- Kalscheuer, R., Weinrick, B., Veeraraghavan, U., Besra, G. S., Jacobs, W. R. Trehalose-recycling ABC transporter LpqY-SugA-SugB-SugC is essential for virulence of Mycobacterium tuberculosis. Proc. Natl. Acad. Sci. U. S. A. 107, 21761-21766 (2010).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten