Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Methionin funktionalisierte biokompatible Blockcopolymere für gezielte Plasmid-DNA-Lieferung
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Zusammenfassung
Diese Arbeit stellt die Herstellung von Methionin funktionalisierten biokompatiblen Blockcopolymeren (mBG) über das reversible Additions-Fragmentierungs-Kettentransfer-Verfahren (RAFT) vor. Die Plasmid-DNA-Komplexierungsfähigkeit des erhaltenen mBG und ihre Transfektionseffizienz wurden ebenfalls untersucht. Die RAFT-Methode ist sehr vorteilhaft für die Polymerisation von Monomeren, die spezielle funktionelle Gruppen enthalten.
Zusammenfassung
Die reversible Additions-Fragmentierungs-Kettenübertragung (RAFT)-Polymerisation integriert die Vorteile der Radikalpolymerisation und der lebenden Polymerisation. Diese Arbeit stellt die Herstellung von Methionin funktionalisierten biokompatiblen Blockcopolymeren über RAFT-Polymerisation vor. Erstens wurde N,N-Bis(2-Hydroxyethyl)methacrylamid-b-N-(3-aminopropyl)methacrylamid (BNHEMA-b-APMA, BA) mittels RAFT-Polymerisation mit 4,4'-Azobis(4-Cyanovalersäure) (ACVA) als Initiierungsmittel und 4-Cyanopentanosäure Dithiobenzoat (CTP) als Kettentransfermittel. Anschließend wurde N,N-bis(2-Hydroxyethyl)Methacrylamid-b-(3-guanidinopropyl)methacrylamid (Methionin transplantiert BNHEMA-b-GPMA, mBG) durch Modifizieren von Amingruppen in APMA mit Methionin und Guanidin hergestellt. Gruppen. Drei Arten von Blockpolymeren, mBG1, mBG2 und mBG3, wurden zum Vergleich synthetisiert. Eine Ninhydrin-Reaktion wurde verwendet, um den APMA-Gehalt zu quantifizieren; mBG1, mBG2 und mBG3 hatten 21 %, 37 % bzw. 52 % aPMA. Die Ergebnisse der Gelpermeationschromatographie (GPC) zeigten, dass BA-Copolymere Molekulargewichte von 16.200 (BA1), 20.900(BA2) und 27.200(BA3) g/mol besitzen. Die Plasmid-DNA-Komplexierungsfähigkeit der erhaltenen Blockcopolymer-Genträger wurde ebenfalls untersucht. Die Ladungsverhältnisse (N/P) waren 8, 16 und 4, wenn pDNA vollständig mit mBG1, mBG2, mBG3 komplexiert wurde. Wenn das N/P-Verhältnis von mBG/pDNA-Polyplexen höher als 1 war, war das Zeta-Potenzial von mBG positiv. Bei einem N/P-Verhältnis zwischen 16 und 32 lag die durchschnittliche Partikelgröße von mBG/pDNA-Polyplexen zwischen 100-200 nm. Insgesamt veranschaulicht diese Arbeit ein einfaches und bequemes Protokoll für die Blockcopolymer-Trägersynthese.
Einleitung
In den letzten Jahren hat sich die Gentherapie für die therapeutische Abgabe von Nukleinsäuren als Medikamente zur Behandlung aller Arten vonKrankheiten1 herausgebildet. Die Entwicklung von Genmedikamenten einschließlich Plasmid-DNA (pDNA) und kleiner störender RNA (siRNA) beruht auf der Stabilität und Effizienz des Arzneimittelabgabesystems (DDS)2. Unter allen DDS haben kationische Polymerträger die Vorteile einer guten Stabilität, geringen Immunogenität und einfachen Vorbereitung und Modifikation, die kationischen Polymerträgern breite Anwendungsperspektiven geben3,4. Für praktische Anwendungen in der Biomedizin müssen Forscher einen kationischen Polymerträger mit hoher Effizienz, geringer Toxizität und guter Targeting-Fähigkeit finden5. Unter allen Polymerträgern sind Blockcopolymere eines der am häufigsten verwendeten Arzneimittelabgabesysteme. Blockcopolymere werden intensiv auf ihre Selbstmontageeigenschaften und Fähigkeiten zur Bildung von Mizellen, Mikrosphären und Nanopartikeln in der Wirkstoffabgabeuntersucht 5. Blockcopolymere können über lebende Polymerisation oder Klickchemiemethoden synthetisiert werden.
1956 sprachen Szwarc et al. das Thema der lebenden Polymerisation an und definierten es als Reaktion ohne kettenbrechende Reaktionen6,7. Seitdem wurden mehrere Techniken entwickelt, um Polymere mit dieser Methode zu synthetisieren; Daher wird die lebende Polymerisation als Meilenstein der Polymerwissenschaft8angesehen. Lebende Polymerisation kann in lebende anionische Polymerisation, lebende kationische Polymerisation und reversible Deaktivierung sradikalpolymerisation (RDRP)9klassifiziert werden. Lebende anionische/kationische Polymerisationen haben aufgrund ihrer strengen Reaktionsbedingungen einen begrenzten Anwendungsbereich10. Die kontrollierte/lebende Radikalpolymerisation (CRP) hat milde Reaktionsbedingungen, eine bequeme Disposition und eine gute Ausbeute und war damit in den letzten Jahren ein schwerpunktweise11. In CRP werden aktive Ausbreitungsketten reversibel zu ruhenden passiviert, um die Konzentration freier Radikale zu reduzieren und die bimolekulare Reaktion von sich ausbreitenden Kettenradikalen zu vermeiden. Die Additionspolymerisation kann nur fortgesetzt werden, wenn die inaktiven ruhenden Vermehrungsketten reversibel zu Kettenradikalen animiert werden. Als eine der vielversprechendsten Formen der lebenden Radikalpolymerisation ist die reversible Additions-Fragmentierungs-Kettentransfer-Polymerisation (RAFT) ein Verfahren, das zur Ausbeute von Blockpolymeren mit kontrolliertem Molekulargewicht und Struktur, schmalem Molekulargewicht Verteilung und das Tragen von Funktionsgruppen12. Der Schlüssel zu einer erfolgreichen RAFT-Polymerisation ist die Wirkung von Kettentransfermitteln, meist Dithioeten, die eine sehr hohe Kettentransferkonstante besitzen.
In diesem Papier wurde ein RAFT-Polymerisationsverfahren entwickelt, um BNHEMA-b-APMA-Blockpolymer zu zubereiten, wobei 4,4'-Azobis(4-Cyanovalersäure) (ACVA) als Initiierungsmittel und 4-Cyanopentanosäure-Dithiobenzoat (CTP) als Kettentransfermittel verwendet werden. Die RAFT-Polymerisation wurde zweimal verwendet, um BNHEMA in die kationischen Polymerträger einzuführen. Anschließend wurden die Amingruppen in der APMA-Kette mit Methionin und dem Guanidaylierungsreagenz 1-Amidinopyzolhydrochlorid modifiziert. Durch die Verwendung der positiven Ladungen des Guanidalylierungsreagenzes und der Methacrylamid-Polymerskelettstruktur wurde die zelluläre Aufnahmeeffizienz der erhaltenen Blockpolymerträger verbessert.
Protokoll
1. Synthese von BNHEMA-Polymer (PBNHEMA)
- 1,87 g N, N-Bis(2-Hydroxyethyl)Methacrylamid (BNHEMA) in 1 ml destilliertem Wasser in einer Polymerisationsflasche auflösen.
HINWEIS: Die Polymerisationsflasche ist ein rund-Boden-Kolben mit einem Gummistopfen und einem Magnetrührer. - 0,03 g 4-Cyanopentanosäure-Dithiobenzoat (CTP) und 0,02 g 4,4'-Azobis (4-Cyanovalericacid) (ACVA) in 0,5 ml 1,4-Dioxan in einem 5 ml Becher auflösen. Fügen Sie dann die CTP- und ACVA-Lösung der Polymerisationsflasche ab Schritt 1.1 hinzu.
- Belüften Sie das Reaktionssystem in der Polymerisationsflasche mit Stickstoff über drei Gefrier-Pumpen-Tau-Zyklen.
- Im Detail die Lösung in der Polymerisationsflasche mit einer Kondensatfalle einfrieren, die Polymerisationsflasche an der Eisenstütze fixieren und Stickstoff über einen mit einer Nadel gekippten Schlauch (#9 Nadel, Innendurchmesser 0,65 mm, Außendurchmesser 0,9 mm). Versiegeln Sie die Polymerisationsflasche und tauen Sie die Lösung bei Raumtemperatur für 30 min auf.
- Wiederholen Sie die Gefrier-Pumpen-Tau-Zyklen dreimal.
- Die Polymerisationsflasche in ein 70 °C Ölbad geben und die Lösung 24 h unter der Stickstoffatmosphäre reagieren lassen.
- Kühlen Sie die Polymerisationsflasche bei 0 °C und öffnen Sie den Gummistopfen, um den Polymerisationsprozess zu beenden.
- Aceton in einem -20 °C-Kühlschrank für 2 h vorkühlen und dann mit der Reaktionslösung schritt 1.5 bei 50:1 (v/v) mischen. Danach zentrifugieren Sie bei 8.200 x g für 10 min, um Aceton zu entfernen und den Niederschlag zu sammeln.
- Um das synthetisierte PBNHEMA zu reinigen, lösen Sie den gesammelten Niederschlag in 2 ml reinem Wasser auf und mischen Sie ihn dann mit 100 ml vorgekühltem Aceton im Verhältnis 1:50 (v/v). Zentrifugieren Sie die Lösung bei 8.200 x g für 10 min und sammeln Sie den Niederschlag. Wiederholen Sie diesen Vorgang dreimal.
- Trocknen Sie den produzierten PBNHEMA mit einem 50 °C Vakuumtrockner. Nach dem Trocknen das Pulver mit einem Gleichgewicht wiegen. Berechnen Sie die Ausbeute gemäß Gleichung 1.
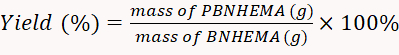 (1)
(1)
HINWEIS: In diesem Experiment betrug die erzielte Ausbeute 77,2%.
2. Synthese von BNHEMA-b-APMA-Polymer (BA)
- 0,96 g N-(3-Aminopropyl)Methacrylamidhydrochlorid (APMA) und 0,93 g PBNHEMA in 5 ml destilliertem Wasser in einem 10 ml Becher auflösen.
- 0,01 g 4,4'-Azobis (4-Cyanovalersäure) (ACVA) in 0,5 ml 1,4-Dioxan auflösen und mit der APMA-PBNHEMA-Lösung aus Teil 2.1 mischen.
- Das Gemisch in eine Polymerisationsflasche geben und mit trockenem Stickstoff 1 h belüften.
- Die Polymerisationsflasche in ein 70 °C Ölbad geben und 24 H unter der Stickstoffatmosphäre reagieren lassen.
- Kühlen Sie die Polymerisationsflasche bei 0 °C und öffnen Sie den Gummistopfen, um den Polymerisationsprozess zu beenden.
- Die Lösung ab Schritt 1.6 auf das gekühlte Aceton übertragen und dann bei 8.200 x g für 10 min zentrifugieren, um den BA auszufällen.
- Den BA in 2 ml destilliertem Wasser auflösen und das Polymer in gekühltem Aceton ausfällen. Wiederholen Sie dies dreimal.
- Trocknen Sie den produzierten BA in einem 50 °C-Vakuumtrockner und wiegen Sie das erhaltene Pulver. Berechnen Sie die Ausbeute nach Gleichung 2.
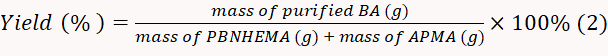
HINWEIS: In diesem Experiment wurde die Ausbeute auf 82,0 % berechnet.
3. Bestimmen Sie den Mol-Prozent-Anteil von APMA in BA-Copolymer über die Ninhydrin-Methode
HINWEIS: Spektrophotometrie wird verwendet, um den Inhalt von Mehrkomponenten-Aminosäuren zu bestimmen. Das Prinzip ist eine Farbreaktion von Ninhydrin und Aminosäure, bei der die Absorption bis zu einem gewissen Grad mit dem Aminosäuregehalt13,14korreliert.
- 5 g Ninhydrin in 125 ml kochendem destilliertem Wasser auflösen. Lösen Sie außerdem 5 g Vitamin C in 250 ml warmem destilliertem Wasser auf. Fügen Sie die 250 ml Vitamin-C-Lösung tropfenweise in die Ninhydrinlösung unter magnetischem Rühren ein. 15 min weiter rühren und dann die Reaktionslösung in einem 4 °C-Kühlschrank abkühlen lassen.
- Nehmen Sie die Lösung aus dem Kühlschrank und filtern Sie durch Absaugen mit einem Buchner-Trichter, um reduziertes Ninhydrin zu erhalten. Sammeln Sie den Niederschlag und bewahren Sie ihn in einem Phosphorpentoxid-Dehydrator auf.
- 85 mg Ninhydrin und 15 mg reduziertes Ninhydrin in 10 ml Ethylenglykolmonomethylether auflösen, um die Ninhydrin-Färbungslösung vorzubereiten.
HINWEIS: Die Ninhydrin-Färbungslösung kann mit dem APMA-Amino reagieren und eine violette Verbindung mit einer Struktur bilden, wie in einer früheren Studiebeschrieben 15. - 1 ml 0, 1, 10, 100, 1.000 mg/ml APMA-Monomerlösungen mit 1 ml Acetatpuffer (2 M, pH 5,4) verdünnen und dann 1 ml Ninhydrin-Färbungslösung hinzufügen.
- Erhitzen Sie die Mischungen 15 min in einem kochenden Wasserbad und kühlen Sie sie dann mit fließendem Wasser ab. Lassen Sie die Lösungen 5-10 min sitzen und verdünnen Sie sie mit 3 ml 60% Ethylalkohol und mischen Sie sie gründlich. Messen Sie die Absorption bei 570 nm mit einem Spektralphotometer und zeichnen Sie die Standardkurve (Gleichung 3).
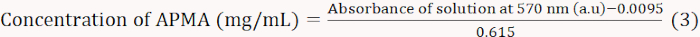
ANMERKUNG: Gleichung 3 wurde von der linearen Anpassung der Absorption bei 570 nm im Vergleich zur APMA-Konzentration abgeleitet. - 0,01 g BA in 1 ml destilliertem Wasser auflösen; 1 ml Acetatpuffer (2 M, pH 5,4) und 1 ml Ninhydrin-Färbungslösung hinzufügen. Berechnen Sie den Molgehalt von APMA entsprechend der Absorption bei 570 nm.

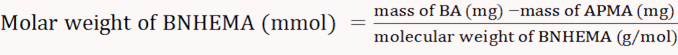 (5)
(5)
HINWEIS: Die Berechnungsformeln sind wie folgt (Gleichungen 3-6).
4. Synthese von Methionin-gepfropftem BA-Polymer (mBA)
- 8,9 mg Fomc-Methionin in 5 ml DMSO in einem Rückgewinnungskolben auflösen.
- 6,92 mg 1-Ethyl-3-(3-Dimethylaminopropyl) Carbodiimidhydrochlorid (EDCl) und 4,86 mg 1-Hydroxybenzotriazol (HOBT) in den Rückgewinnungskolben geben und bei 0 °C für 0,5 h reagieren.
- 2,59 g BA in 5 ml DMSO-Lösung auflösen und dann 50 l Trimethylamin hinzufügen; Fügen Sie diese Lösung tropfenweise in den Rückgewinnungskolben (Schritt 4.2) und lassen Sie die Lösung für 0,5 h bei Raumtemperatur reagieren.
- Dialyse, um DMSO und Trimethylamin aus der BA-Lösung in Schritt 4.3 mit einem Dialysebeutel (MWCO 10 kDa) in einem 2 L Becher für 24 h zu entfernen; das entionisierte Wasser alle 6 h ersetzen.
- Gefriertrocken den erhaltenen mBA und wiegen, um die Ausbeute rate nach Gleichung 7zu berechnen.
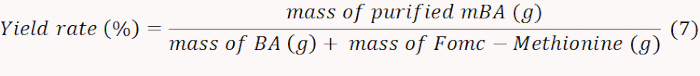
HINWEIS: In diesem Fall wurde die Rendite auf 71 % festgelegt. - Quantifizieren Sie das NH 2, das mBA enthält, indem Sie die Absorption bei 570 nm messen, um die Menge an gepfropftem Methionin zu berechnen. Berechnen Sie den Molgehalt von Methionin gemäß Gleichung 8.

5. Synthese von guanidiniertem und Methionin konjugiertem BNHEMA- b-APMA-Polymer (mBG)
HINWEIS: Drei verschiedene mBA1-, mBA2- und mBA3-Copolymere wurden synthetisiert. mBA3-Copolymer wird in den folgenden Schritten als Beispiel verwendet.
- Lösen Sie mBA3 mit 60 mol Aminogruppe in 5 ml reinem Wasser auf.
HINWEIS: Der Aminogruppengehalt wurde mit der in Schritt 3.5 beschriebenen Ninhydrinmethode quantifiziert. - 40,6 mg Guanidinylierungsreagenz 1-Amidinopyzolhydrochlorid in mBA-Lösungen auflösen.
- Stellen Sie den pH-Wert mit der gesättigten Natriumcarbonatlösung auf 9,0 ein und lassen Sie ihn bei Raumtemperatur 24 h stabilisieren.
- Dialysieren Sie das mBG-Produkt mit entionisiertem Wasser in einem Dialysebeutel in einem Becher (MWCO 10 kDa, 2 L) und bewahren Sie es in Form eines gefriergetrockneten Pulvers auf.
Der Ertragsprozentsatz wurde über Gleichung 8auf 85 % berechnet.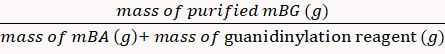 (8)
(8) - MBG-Pulver in D2O in den NMR-Röhren auflösen und mit 1H Kernspinresonanzspektroskopie (1H NMR)16charakterisieren.
6. Vorbereitung und Charakterisierung von mBG/pDNA Polyplexen
- Lösen Sie 50 g pDNA in 50 l RNase/DNase-freiem Wasser auf.
- 1 mg mBG-Copolymere in 1 ml RNase/DNase-freiem Wasser auflösen.
- Fügen Sie die mBG-Copolymerlösung direkt in die pDNA-Lösung nach unterschiedlichen Zuführverhältnissen, d.h. unterschiedlichen N/P-Verhältnissen (1:1, 4:1, 8:1, 16:1 und 32:1) ein.
HINWEIS: Das N/P-Verhältnis ist definiert als das Molverhältnis der Guanidingruppe in der Polymer- und der Phosphatgruppe in pDNA, nämlich das Molverhältnis der GPMA-Kette im Polymer und das Mononukleotid in pDNA. Das N/P-Verhältnis wird nach den Molekulargewichten von Aminostickstoff (N) in mBG und Phosphatgruppe (P) in pDNA berechnet. - Mischen Sie die Lösungen mit einem Wirbelmischer und lassen Sie sie für 30 min bei Raumtemperatur stehen. Danach das Gemisch in Phosphatpufferlösung (PBS, pH 7.4) dispergieren und die erhaltenen mBG/pDNA-Polyplexe bei 4 °C für die Folgeexperimente aufbewahren.
HINWEIS: Die durchschnittliche Partikelgröße und das Zeta-Potenzial von mBG und die Komplexe wurden mithilfe der dynamischen Lichtstreuung (DLS)17erkannt. - Verdünnen Sie 10 l der mBG/pDNA Polyplex-Lösungen mit 1 ml PBS (pH 7.4) in den DLS- und Zeta-potenzialen Probenzellen.
HINWEIS: Partikelgröße und Zeta-Potenzialdetektion wurden dreimal durchgeführt und ein Durchschnitt der drei Werte wurde genommen.
7. Elektrophoretische Retardierungsexperiment von mBG/pDNA-Polyplexen
HINWEIS: Zur Bestimmung des Mindestladeverhältnisses wurde ein elektrophoretisches Retardierungsexperiment durchgeführt.
- Nehmen Sie fünf Gruppen der mBG/pDNA-Polyplexe mit unterschiedlichen N/P-Verhältnissen (1:1, 4:1, 8:1, 16:1 und 32:1), die 50 g pDNA enthalten.
- Den mBG/pDNA Polyplexproben 6x Ladepuffer zu einer Endkonzentration von 1x hinzufügen.
- Fügen Sie die Lösungen zu den 1,5% Agarose Gelen hinzu und führen Sie das Gel bei 90 mV für 15 min, mit pDNA als Kontrolle .
- Nehmen Sie Fotos der Gele mit einem Gel-Imager auf.
8. Zytotoxizität von mBG/pDNA-Polyplexen
- Saat MCF-7-Zellen in die 96-Well-Platten mit einer Dichte von 104 Zellen pro Brunnen. Dann kulturieren Sie die Zellen für 12 h mit DMEM Medium (10% FBS und 1% Antibiotikum) in einem befeuchteten 37 °C Inkubator mit 5%CO2geliefert.
- Ersetzen Sie das Kulturmedium durch antibiotikafreie DMEM-Kulturmedien, die 10% fetales Rinderserum (FBS) und mBG/pDNA-Polyplexe mit unterschiedlichen Ladungsverhältnissen (N/P 4, 8, 16 und 32, n=6) für 6 h enthalten und Zellen mit gleichen Mengen PBS-Lösung als Kontrolle verwenden. Dann ersetzen Sie das Kulturmedium durch 150 l frisches 1640 Medium und weiter Kultur die Zellen für 24 h.
- 5 mg/ml 3-(4,5-Dimethylthiazol-2-yl)-2,5-Diphenyltetrazoliumbromid (MTT) Lösung (20 l/well) zu den 96-Well-Platten hinzufügen und die Zellen für 4 h weiter ankulturieren.
- Entfernen Sie die Lösung und fügen Sie jedem Brunnen 150 L DMSO hinzu und schütteln Sie die 96-Well-Platten 30 Sek.
- Messen Sie die optische Dichte (OD) bei 490 nm mit einem Mikroplattenleser, um die Zelllebensfähigkeit zu zeigen. Berechnen Sie den Prozentsatz der Zelllebensfähigkeit gemäß Gleichung 9.
Zelllebensfähigkeit % = (9)
% = (9)
9. Transfektionswirkungseffizienz von mBG/ GFP-pDNA Polyplexen
- Lösen Sie 50 g pDNA mit dem Reportergen grünes fluoreszierendes Protein (GFP) pDNA (GFP-pDNA) in 50 l RNase/DNase-freiem Wasser auf. Dann 1 mg mBG-Copolymere in 1 ml RNase/DNase-freiem Wasser auflösen. Mischen Sie pDNA und mBG Lösung mit einem Ladeverhältnis (N/P) von 1:1, 4:1, 8:1, 16:1 und 32:1 und brüten für 30 min bei Raumtemperatur. Dispergieren Sie die Lösung mBG/GFP-pDNA Polyplexes mit Ultraschallwellen (30 s) und lagern Sie sie bei 4 °C für die Folgeexperimente.
HINWEIS: Das N/P-Verhältnis wird nach den Molekulargewichten von Aminostickstoff (N) in mBG und Phosphatgruppe (P) in pDNA berechnet. - Saat MCF-7-Zellen mit einer Dichte von 2 x 105 Zellen pro Brunnen in einer 6-Well-Platte und kulturieren sie bei 37 °C und 5% CO2 in einem befeuchteten Inkubator für 12 h.
- Ersetzen Sie das Kulturmedium durch das frische Kulturmedium, das mBG/GFP-pDNA-Polyplexe unterschiedlicher N/P-Verhältnisse (4, 8, 16 und 32) für 6 h enthält.
- Ersetzen Sie das Medium durch 2 ml frisches RPMI1640 Medium und Kultur für 48 h.
- Sammeln Sie die Zellen und erkennen Sie die grüne Fluoreszenz mit einem Durchflusszytometer.
Ergebnisse
BNHEMA wurde nach dem in Tabelle 1angegebenen objektiven Polymerisationsgrad gefüttert; das Syntheseverfahren von mBG ist in Abbildung 1dargestellt. Zunächst wurde BNHEMA Homopolymer über das reversible Additions-Fragmentierungs-Kettentransfer-Verfahren (RAFT) im Wasser-Dioxan-System unter Verwendung von 4-Cyanopentanosäure-Dithiobenzoat als Kettentransfermittel hergestellt. Zweitens wurde PBNHEMA als Kettentransfermittel zur Herstellung von BNHEMA-b-APMA-Blockp...
Diskussion
Diese Studie führte eine Reihe von BNHEMA-b-APMA Block polymeren Genträgern ein. Diese Blockpolymere wurden über das reversible Additions-Fragmentierungs-Kettentransferverfahren (RAFT) synthetisiert. Das hydrophile Segment BNHEMA wurde eingeführt, um die Löslichkeit zu verbessern. Methionin- und Guanidingruppen wurden modifiziert, um die Zielfähigkeit und Transfektionseffizienz zu verbessern5. Der APMA-Kettengehalt erhöhte sich und die Guanidinylierung im mBG-Copolymer reduzierte die Partik...
Offenlegungen
Die Autoren bescheinigen, dass es keinen Interessenkonflikt mit einer Finanzorganisation in Bezug auf das in diesem Artikel diskutierte Material gibt.
Danksagungen
Diese Forschung wurde unterstützt durch das National Key Research and Development Program of China (Nr. 2016YFC0905900), National Natural Science Foundation of China (Nos. 81801827, 81872365), Basic Research Program of Jiangsu Province (Natural Science Foundation, No. BK20181086) und Jiangsu Cancer Hospital Scientific Research Fund (Nr. ZK201605).
Materialien
| Name | Company | Catalog Number | Comments |
| 1-hydroxybenzotriazole | Macklin Biochemical Co., Ltd,China | H810970 | ≥97.0% |
| 1,4-dioxane | Sinopharm chemical reagent Co., Ltd, China | 10008918 | AR |
| 1-amidinopyrazole Hydrochloride | Aladdin Co., Ltd., China | A107935 | 98% |
| 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride | Aladdin Co., Ltd., China | E106172 | AR |
| 4,4’-azobis(4-cyanovaleric acid) | Aladdin Co., Ltd., China | A106307 | Analytical reagent (AR) |
| 4-cyano-4-(phenylcarbonothioylthio)pentanoic Acid | Aladdin Co., Ltd., China | C132316 | >97%(HPLC) |
| Acetate | Sinopharm chemical reagent Co., Ltd, China | 81014818 | AR |
| Acetone | Sinopharm chemical reagent Co., Ltd, China | 10000418 | AR |
| Agarose | Aladdin Co., Ltd., China | A118881 | High resolution |
| Ascorbic acid | Aladdin Co., Ltd., China | A103533 | AR |
| DMSO | Aladdin Co., Ltd., China | D103272 | AR |
| Ethylene glycol | Aladdin Co., Ltd., China | E103319 | AR |
| N-(3-aminopropyl)methacrylamide hydrochloride | Aladdin Co., Ltd., China | N129096 | ≥98.0%(HPLC) |
| N,N-bis(2-hydroxyethyl)methacrylamide | ZaiQi Bio-Tech Co.,Ltd, China | CF259748 | ≥98.0%(HPLC) |
| Ninhydrin | Aladdin Co., Ltd., China | N105629 | AR |
| PBS buffer | Aladdin Co., Ltd., China | P196986 | pH 7.4 |
| Plasmid DNA | BIOGOT Co., Ltd, China | pDNA-EGFP | pDNA-EGFP |
| Plasmid DNA | BIOGOT Co., Ltd, China | Pdna | pDNA |
| Sodium carbonate decahydrate | Aladdin Co., Ltd., China | S112589 | AR |
| Trimethylamine | Aladdin Co., Ltd., China | T103285 | AR |
Referenzen
- Flotte, T. R. Gene and Cell Therapy in 2018: A Look Ahead. Human Gene Therapy. 29, 1-1 (2018).
- Huang, W., et al. Nanomedicine-based combination anticancer therapy between nucleic acids and small-molecular drugs. Advanced Drug Delivery Reviews. 115, 82-97 (2017).
- Wu, Y., et al. Reversing of multidrug resistance breast cancer by co-delivery of P-gp siRNA and doxorubicin via folic acid-modified core-shell nanomicelles. Colloids & Surfaces B Biointerfaces. 138, 60-69 (2016).
- Quader, S., Kataoka, K. Nanomaterial-Enabled Cancer Therapy. Molecular Therapy. 25, 1501-1513 (2017).
- Wu, Y., et al. Multivalent methionine-functionalized biocompatible block copolymers for targeted siRNA delivery and subsequent reversal effect on adriamycin resistance in human breast cancer cell line MCF-7/ADR. Journal of Gene Medicine. 19, e2969 (2017).
- Szwarc, M. ‘Living’ Polymers. Nature. 178, 168-169 (1956).
- Szwarc, M., Rembaum, A. Polymerization of methyl methacrylate initiated by an electron transfer to the monomer. Journal of Polymer Science. 22 (100), 189-191 (1956).
- Mukhopadhyay, R. D., Ajayaghosh, A. Living supramolecular polymerization. Science. 349, 241 (2015).
- Ozkose, U. U., Altinkok, C., Yilmaz, O., Alpturk, O., Tasdelen, M. A. In-situ preparation of poly(2-ethyl-2-oxazoline)/clay nanocomposites via living cationic ring-opening polymerization. European Polymer Journal. 88, 586-593 (2017).
- Wu, W., Wang, W., Li, J. Star polymers: Advances in biomedical applications. Progress in Polymer Science. 46, 55-85 (2015).
- Boyer, C., et al. Copper-Mediated Living Radical Polymerization (Atom Transfer Radical Polymerization and Copper(0) Mediated Polymerization): From Fundamentals to Bioapplications. Chemical Reviews. 116, 1803-1949 (2016).
- Keddie, D. J. A guide to the synthesis of block copolymers using reversible-addition fragmentation chain transfer (RAFT) polymerization. Chemical Society Reviews. 43, 496-505 (2014).
- Wu, Y., et al. Guanidinylated 3-gluconamidopropyl methacrylamide-s-3-aminopropyl methacrylamide copolymer as siRNA carriers for inhibiting human telomerase reverse transcriptase expression. Drug Delivery. 20, 296-305 (2013).
- Qin, Z., Liu, W., Guo, L., Li, X. Studies on Guanidinated N-3-Aminopropyl Methacrylamide-N-2-Hydroxypropyl Methacrylamide Co-polymers as Gene Delivery Carrier. Journal of Biomaterials Science, Polymer Edition. 23, 1-4 (2012).
- Friedman, M. Applications of the Ninhydrin Reaction for Analysis of Amino Acids, Peptides, and Proteins to Agricultural and Biomedical Sciences. Journal of Agricultural and Food Chemistry. 52, 385-406 (2004).
- Habuchi, S., Yamamoto, T., Tezuka, Y. Synthesis of Cyclic Polymers and Characterization of Their Diffusive Motion in the Melt State at the Single Molecule Level. Journal of Visualized Experiments. (115), 1-9 (2016).
- Rao, D. A., Nguyen, D. X., Mishra, G. P., Doddapaneni, B. S., Alani, A. W. Preparation and Characterization of Individual and Multi-drug Loaded Physically Entrapped Polymeric Micelles. Journal of Visualized Experiments. 102, 1-5 (2015).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten