Method Article
Schnelle Charakterisierung genetischer Teile mit zellfreien Systemen
In diesem Artikel
Zusammenfassung
Gut charakterisierte genetische Teile sind für das Design neuartiger genetischer Schaltkreise notwendig. Hier beschreiben wir eine kostengünstige Hochdurchsatzmethode zur schnellen Charakterisierung genetischer Teile. Unsere Methode reduziert Kosten und Zeit durch die Kombination von zellfreien Lysaten, linearer DNA zur Vermeidung von Klonen und akustischem Flüssigkeitshandling, um den Durchsatz zu erhöhen und das Reaktionsvolumen zu reduzieren.
Zusammenfassung
Die Charakterisierung und Katalogisierung genetischer Teile ist entscheidend für das Design nützlicher genetischer Schaltkreise. Gut charakterisierte Teile ermöglichen die Feinabstimmung genetischer Schaltkreise, so dass ihre Funktion zu vorhersagbaren Ergebnissen führt. Mit dem Wachstum der synthetischen Biologie als Feld gab es eine Explosion von genetischen Schaltkreisen, die in Mikroben implementiert wurden, um Funktionen im Zusammenhang mit Sensorik, metabolischer Veränderung und zellulärem Computing auszuführen. Hier zeigen wir eine schnelle und kostengünstige Methode zur Charakterisierung genetischer Teile. Unsere Methode verwendet zellfreies Lysat, das im eigenen Haus hergestellt wird, als Medium, um Teile über die Expression eines Reporterproteins zu bewerten. Template-DNA wird durch PCR-Amplifikation unter Verwendung kostengünstiger Primer hergestellt, um dem Reporter-Gen Variantenteile hinzuzufügen, und die Template wird der Reaktion als lineare DNA ohne Klonierung hinzugefügt. Zu den Teilen, die auf diese Weise hinzugefügt werden können, gehören Promotoren, Operatoren, Ribosomenbindungsstellen, Isolatoren und Terminatoren. Dieser Ansatz, kombiniert mit der Integration eines akustischen Liquid Handlers und 384-Well-Platten, ermöglicht es dem Benutzer, Hochdurchsatz-Auswertungen von genetischen Teilen an einem einzigen Tag durchzuführen. Im Vergleich dazu erfordern zellbasierte Screening-Ansätze ein zeitaufwändiges Klonen und längere Testzeiten aufgrund von Nachtkultur- und Kulturdichtenormalisierungsschritten. Darüber hinaus ermöglicht die Arbeit mit zellfreiem Lysat dem Benutzer eine genauere Kontrolle der Expressionsbedingungen durch die Zugabe von exogenen Komponenten und DNA in präzisen Konzentrationen. Die Ergebnisse des zellfreien Screenings können direkt in Anwendungen zellfreier Systeme oder in einigen Fällen zur Vorhersage der Funktion ganzer Zellen verwendet werden.
Einleitung
Eine Kernanstrengung der synthetischen Biologie ist die Entwicklung genetischer Werkzeugkits mit gut charakterisierten Teilen, die verwendet werden können, um genetische Schaltkreise1 zu konstruieren, die nützliche Funktionen erfüllen, wenn sie in Mikroben oder zellfreien Lysaten eingesetzt werden. Bereiche, in denen solche genetischen Schaltkreise an Bedeutung gewonnen haben, sind die Sensorik 2,3,4, die menschliche Leistungsfähigkeit5,6, Biokraftstoffe7,8, die Materialproduktion 9,10 und das zelluläre Computing 11. Register für standardisierte genetische Teile wurdeneingerichtet 12, um neue und bestehende Teile in Kategorien wie Promotoren, Operatoren, kodierende Sequenzen und Terminatoren zu katalogisieren, um nur einige zu nennen. Bemühungen wie der iGEM-Wettbewerb (International Genetically Engineered Machines)13 haben maßgeblich dazu beigetragen, diese genetischen Teile zu charakterisieren und zu katalogisieren. Es wurden viele Methoden entwickelt, um den schnellen Zusammenbau dieser Teile zu nützlichen genetischen Schaltkreisen zu erleichtern14,15. Es wurde sogar Software entwickelt, um die Zusammensetzung von gut charakterisierten Teilen zu Schaltkreisen zu automatisieren, die eine gewünschte Funktion erreichen16. Die Zusammenstellung nützlicher genetischer Schaltkreise mit vorhersagbaren Funktionen beruht jedoch auf der Annahme, dass die genetischen Werkzeugkästen gut charakterisierte genetische Teile enthalten. Aufgrund der Notwendigkeit dieser Toolkits für die Weiterentwicklung der synthetischen Biologie wurden zahlreiche Bemühungen zur besseren Katalogisierung von Schaltkreisen und Teilen mit geeigneten Charakterisierungsdaten beschrieben 17,18,19,20,21.
Ein Ansatz zur Charakterisierung genetischer Komponenten nutzt zellfreie Proteinsynthesesysteme (CFPS), die zelluläre Funktionen wie Transkription und Translation ex vivorekonstruieren 22. Mehrere Studien haben das Potenzial von CFPS für das Prototyping genetischer Komponenten23, 24, 25, 26, 27, 28, 29, 30, 31, 32 gezeigt, sei es für direkte Anwendungen in zellfreien Systemen oder zur Vorhersage der Funktion genetischer Konstrukte in Zellen, wie z. B. der relativen Aktivität von Teilen innerhalb einer Bibliothek 29 , Optimierung des Stoffwechselwegs27 und zelluläre Belastung30. Zu den Vorteilen des Prototypings von CFPS im Vergleich zu Zellen, die in diesen Studien hervorgehoben wurden, gehören die Vermeidung von zeitaufwändigem Klonen, die präzise Kontrolle über die Konzentration von DNA und anderen Reaktionskomponenten sowie die Fähigkeit, mehrere DNA-Konstrukte einfach zu mischen und aufeinander abzustimmen. Der Vorteil der Vermeidung von Klonen zeigt sich besonders bei der Verwendung linearer DNA-Vorlagen, die es ermöglichen, neue Konstrukte durch In-vitro-Methoden zusammenzusetzen, die Stunden statt33 Tage dauern. Die Möglichkeit, die Konzentration von DNA-Konstrukten und anderen Komponenten einfach durch Pipettieren zu manipulieren, macht den Ansatz noch attraktiver, indem es Hochdurchsatzexperimente ermöglicht, die von Liquid-Handling-Robotern angetrieben werden34,35. Während Erfolge mit CFPS für das Prototyping berichtet wurden, ist es wichtig zu beachten, dass es abzuwarten bleibt, in welchen Kontexten CFPS-Ergebnisse die Funktionalität in Zellen zuverlässig vorhersagen können.
Hier stellen wir eine Methode für das CFPS-Prototyping vor, die die Vorteile in Bezug auf Geschwindigkeit, Durchsatz und Kosten im Vergleich zu herkömmlichen zellbasierten Ansätzen hervorhebt. Der Ansatz leitet sich von unserer früheren Arbeit ab, in der wir CFPS verwendeten, um eine Bibliothek von T7-Promotorvarianten, die durch den Transkriptionsfaktor TetR32 reguliert werden, schnell zu charakterisieren, was die kleine Handvoll regulierter T7-Promotorvarianten, die zu dieser Zeit in der Literatur verfügbar waren, signifikant erweitert36,37. Andere haben seither die Palette solcher Promotoren weiter ausgebaut38. In unserer Methode wird der Aufbau genetischer Konstrukte durch die Verwendung von PCR beschleunigt, um Template-DNA über Primer zu amplifizieren, die einem Reportergen verschiedene genetische Teile hinzufügen. Die akustische Handhabung von Flüssigkeiten in 384-Well-Platten wird verwendet, um den Durchsatz zu erhöhen und das erforderliche Materialvolumen zu verringern. Frühere Arbeiten haben den erfolgreichen Einsatz von akustischem Liquid Handling bei signifikant niedrigeren Volumina39,40 mit einer Variabilität gezeigt, die mit dem manuellen Pipettieren größerer Volumina vergleichbarist 41. Neben der Methode bieten wir Informationen zur Fehlerbehebung und eine Bewertung möglicher Kosten- und Zeiteinsparungen. Beachten Sie, dass wir hier zwar ein Protokoll zur Herstellung von zellfreien Lysaten auf Basis von Sun et al.42 enthalten, aber zahlreiche andere kommerzielle Kits und Protokolle43,44 ebenfalls funktionieren sollten. Während wir die Methode zur Charakterisierung von Promotorvarianten32 demonstrieren, können andere Teile durch PCR-Amplifikation ausgetauscht werden, wie z.B. Riboregulatoren, Ribosomenbindungsstellen (RBS), Isolatoren, Proteinmarkierungen und Terminatoren. Wir hoffen, dass diese Methodik der Gemeinschaft der synthetischen Biologie helfen kann, die Anzahl der charakterisierten Teile für den Aufbau vorhersagbarer genetischer Schaltkreise mit nützlicher Funktion weiter zu erhöhen.
Protokoll
1. Herstellung von Zellextrakt
- Aufbereitung von Medien
- Für 2xYT-Medien: 16 g Trypton, 10 g Hefeextrakt und 5 g NaCl zu 900 ml entionisiertem Wasser geben und den pH-Wert mit 5 M NaOH auf 7,0 einstellen. Erhöhen Sie das Lösungsvolumen mit entionisiertem Wasser auf 1 l und sterilisieren Sie es im Autoklaven oder Filter. Alternativ können Sie 2xYT-Medien erwerben.
- Für S30B-Puffer: Bereiten Sie eine Lösung aus 14 mM Mg-Glutamat, 60 mM K-Glutamat und 5 mM Tris in 2 l entionisiertem Wasser vor. Verwenden Sie 2 M Tris, um den pH-Wert auf 8,2 einzustellen, autoklavieren und bei 4 °C lagern. Ergänzen Sie die Lösung durch Zugabe von Dithiothreitol (DTT) zu einer Endkonzentration von 1 mM kurz vor der Verwendung.
- Präparation von Zellen
- Escherichia coli BL21(DE3) Rosetta2-Zellen oder eine andere Zelllinie der Wahl (siehe Cole et al.44 für eine kürzlich durchgeführte umfassende Übersichtsarbeit) auf eine LB (Lysogeny Bouillon) Agarplatte streifen und bei 37 °C für 10-14 h inkubieren.
- Verwenden Sie eine einzelne E. coli-Kolonie , um 3 ml 2xYT-Medium in einem 10-ml-Kulturröhrchen zu impfen. Dieses Röhrchen wird bei 37 °C unter Schütteln bei 250 U/min für 8 h inkubiert.
- Verwenden Sie 50 μl aus der 3-ml-Kultur, um 50 ml 2xYT-Medium in einem 500-ml-Kolben zu impfen. Der Kolben wird bei 37 °C unter Schütteln bei 250 U/min 8 h lang inkubiert.
- Verwenden Sie 7,5 ml aus der 50-ml-Kultur, um jeden der vier 4-L-Prallkolben mit 0,75 l 2xYT-Medium zu impfen. Diese Kolben werden bei 37 °C unter Schütteln bei 220 U/min inkubiert, bis sie nach etwa 3-4 h bei 600 nm eine optische Dichte von 2 bis 4 erreicht haben.
- Die Zellen werden aus jedem Kolben entnommen, indem sie in 1-Liter-Behälter umgefüllt und 12 min bei 4 °C bei 5.000 x g zentrifugiert werden. Entsorgen Sie den Überstand, indem Sie ihn in einen Abfallbehälter umfüllen.
- Waschen Sie jedes Zellpellet mit 150 ml eiskaltem S30B-Puffer, indem Sie es mit einer Pipette vollständig resuspendieren, um die Zellmasse aufzubrechen, und sammeln Sie die Zellen dann durch Zentrifugation bei 5.000 x g für 12 Minuten wieder ein. Entsorgen Sie den Überstand.
- Waschen Sie jedes Zellpellet erneut in 40 ml eiskaltem S30B-Puffer, indem Sie es vollständig resuspendieren und die Zellmasse mit einer Pipette aufbrechen. Die Zellen werden in vorgewogene 50 ml konische Röhrchen übergeben und durch Zentrifugation bei 2.000 x g für 8 min bei 4 °C wieder gesammelt. Verwerfen Sie den Überstand durch Dekantieren.
- Wiegen Sie die Nasszellenpellets. Die Zellpellets schockgefrieren, indem Sie die Röhrchen direkt in flüssigen Stickstoff legen und bei -80 °C lagern.
- Zelllyse
- Tauen Sie die Zellpellets auf Eis auf.
- Resuspendieren Sie jedes Zellpellet in 1,4 ml S30B-Puffer pro 1 g des Zellpellets durch Vortexen.
- Die Zellen werden mit einer französischen Druckzelle bei 640 psi bei 4 °C lysiert. Das Lysat wird in Mikrozentrifugenröhrchen auf Eis gesammelt und unmittelbar nach der Lyse 3 μL 1 M DTT pro 1 ml Lysat zugegeben.
HINWEIS: Es ist am besten, das französische Druckentlastungsventil mit einer kleinen Metallstange anzuklopfen, um einen gleichmäßigen Druck aufrechtzuerhalten und plötzliche Druckabfälle zu vermeiden. - Das Lysat wird durch Zentrifugieren bei 30.000 x g für 30 min bei 4 °C gereinigt und das Pellet nach dem Pipettieren des Überstands in ein neues eiskaltes Mikrozentrifugenröhrchen entsorgt, wobei darauf zu achten ist, dass das Pellet nicht zerstört wird.
- Der Überstand wird ein zweites Mal bei 30.000 x g für 30 min bei 4 °C zentrifugiert. Pipettieren Sie den resultierenden Überstand in ein eiskaltes Mikrozentrifugenröhrchen. Entsorgen Sie das Pellet.
- Der Überstand wird in einem 37 °C warmen Wasserbad für 1 h inkubiert.
- Der Überstand wird durch Zentrifugieren bei 15.000 x g für 15 min bei 4 °C gereinigt und der resultierende Überstand in ein eiskaltes Mikrozentrifugenröhrchen überführt, wobei darauf zu achten ist, dass das Pellet nicht zerstört wird.
- Der Überstand wird ein zweites Mal bei 15.000 x g für 15 min bei 4 °C zentrifugiert und der resultierende Überstand in ein eiskaltes Mikrozentrifugenröhrchen überführt, wobei darauf zu achten ist, dass keine verbleibenden Pellets zerstört werden.
- Verteilen Sie den Überstand in 100 μL-Aliquoten in 1,5-ml-Mikrozentrifugenröhrchen und gefrieren Sie sie durch direktes Einlegen in flüssigen Stickstoff. Lagern Sie den Überstand bei -80 °C.
2. Lineare Schablonenvorbereitung
- Primer-Design
- Wählen Sie eine Kernsequenz als PCR-Schablone. Fügen Sie mindestens eine Reportersequenz hinzu, z. B. sfGFP (Superfolder Green Fluorescent Protein), LacZ oder Spinat-Aptamer. Fügen Sie andere Teile hinzu, die über abgeschirmte Varianten hinweg fixiert werden, z. B. Terminatoren, Promotoren oder RBSs, je nach Design.
HINWEIS: Der Einschluss eines Terminators ist nicht immer für die Expression von linearer DNA in zellfreien Systemen erforderlich. - Wählen Sie für die Vorwärtsprimer ein Minimum von 20 bp, das dem 5-Ende der Kernsequenz als 3-Ende des Primers entspricht. Wenn Sie Teile zum 5'-Ende des Konstrukts hinzufügen, entwerfen Sie den Rest des 5'-Endes des Primers, um die genetischen Teile von Interesse durch PCR-Amplifikation zur Kernsequenz hinzuzufügen (Abbildung 1A und Abbildung 2).
HINWEIS: Da Primer über ~ 60 bp häufig dramatisch in den Kosten steigen, können mehrere überlappende Primer entworfen werden, um längere Sequenzen oder mehrere Teile hinzuzufügen. Während mehrere Primer in einer einzigen PCR-Reaktion verwendet werden können, wird empfohlen, mehrere PCR-Runden durchzuführen. - Wählen Sie für die Reverse-Primer ein Minimum von 20 bp, um dem 3'-Ende der Kernsequenz als 3'-Ende des Primers zu entsprechen. Wenn Sie Teile zum 3'-Ende des Konstrukts hinzufügen, entwerfen Sie den Rest des 5'-Endes des Primers, um die genetischen Teile von Interesse durch PCR-Amplifikation zur Kernsequenz hinzuzufügen (Abbildung 1A und Abbildung 2). Stellen Sie sicher, dass die Glühtemperatur des Reverse-Primers innerhalb von 5 °C von der Glühtemperatur des gesamten Forward-Primers abweicht.
- Wählen Sie eine Kernsequenz als PCR-Schablone. Fügen Sie mindestens eine Reportersequenz hinzu, z. B. sfGFP (Superfolder Green Fluorescent Protein), LacZ oder Spinat-Aptamer. Fügen Sie andere Teile hinzu, die über abgeschirmte Varianten hinweg fixiert werden, z. B. Terminatoren, Promotoren oder RBSs, je nach Design.
- Lineare Schablonenverstärkung
- Bestimmen Sie die Anzahl der durchzuführenden PCR-Reaktionen basierend auf der Anzahl der Kernsequenzen und berechnen Sie die Menge der einzelnen erforderlichen Komponenten anhand von Tabelle 1.
- Bereiten Sie die Mastermischung gemäß Tabelle 1 vor und lagern Sie sie auf Eis. Aliquot 30 oder 40 μL (siehe Tabelle 1) des Masters in die bestimmte Anzahl von PCR-Röhrchen geben und 10 μL jedes variablen Primers (d. h. Primer, die für eine Teiländerung kodieren, siehe Tabelle 1) bei 5 μM zu entsprechend markierten PCR-Röhrchen hinzufügen.
- Legen Sie die PCR-Röhrchen in den Thermocycler und führen Sie das folgende PCR-Programm durch: 98 °C für 3 min; 30 Zyklen von 98 °C für 15 s, XX °C für 20 s, 72 °C für YY min; Endverlängerung bei 72 °C für 10 min. Halten Sie dann die Reaktion bei 4 °C.
Dabei steht XX für die Glühtemperatur des Primers mit der niedrigeren Glühtemperatur und YY für die Verlängerungszeit, die für die Länge des Amplikons berechnet wurde, basierend auf den Empfehlungen des Herstellers für die verwendete High-Fidelity-Polymerase. Optimieren Sie diese Bedingungen nach Bedarf für verschiedene Primer und/oder Vorlagen. - (Optional) Fügen Sie 1 μL des DpnI-Restriktionsenzyms hinzu, um die ursprüngliche Vorlage zu verdauen. Die Reaktion wird bei 37 °C für 1 h inkubiert. Führen Sie diesen Schritt nur aus, wenn es sich bei der ursprünglichen Vorlage um Plasmid-DNA handelt.
- Analysieren Sie 5 μL jedes PCR-Produkts durch Gelelektrophorese. Trennen Sie das Produkt mit einem 1%igen Agarosegel bei 180 V für 20 Minuten. Überprüfen Sie die richtige Bandgröße, die mit der gewählten Kernsequenz und der Länge der hinzugefügten Teile variiert.
- Reinigen Sie die lineare Schablone mit einem handelsüblichen PCR-Aufreinigungskits oder mit der bevorzugten PCR-Aufreinigungsmethode. Wenn mehrere Banden durch Gelelektrophorese-Analyse vorhanden waren, optimieren Sie entweder die PCR-Bedingungen oder reinigen Sie die richtigen Molekulargewichtsbanden mit einem handelsüblichen Gel-Extraktionskit gemäß der Empfehlung des Herstellers.
- Quantifizieren Sie jede DNA-Vorlage mit einem Spektralphotometer. Beurteilen Sie die Qualität der DNA-Vorlage, indem Sie überprüfen, ob das Verhältnis von 260 nm/280 nm ungefähr 1,8 beträgt.
- (Optional) Trennen Sie erneut einen Teil der DNA-Vorlage mit einem 1%igen Agarose-Gel bei 180 V für 20 Minuten und stellen Sie sicher, dass alle unerwünschten Banden während der Vorlagenreinigung entfernt wurden.
- Gereinigte DNA-Templates sofort verwenden oder bei -20 °C lagern.
3. Gereinigte Proteinzubereitung
- Protein-Expression
- Für jedes Protein, das exprimiert werden soll, stellen Sie ein geeignetes Expressionskonstrukt zusammen. Codon-Optimierung des Gens für die Expression in E. coli. Das Gen wird über die bevorzugte Plasmid-Assemblierungsmethode in einen pET-22b-Expressionsvektor oder einen anderen geeigneten Expressionsvektor eingefügt. Das Expressionsplasmid wird in BL21(DE3)-Rosetta2-Expressionszellen oder eine andere geeignete Zelllinie transformiert.
- Verwenden Sie für jedes Protein eine einzelne Kolonie, um 3 ml LB-Medium in einem 10-ml-Kulturröhrchen zu impfen. Diese Röhrchen werden bei 37 °C inkubiert und über Nacht bei 250 U/min geschüttelt.
- Ein 2-Liter-Kolben mit 750 ml LB-Medium wird mit 1 ml der Nachtkultur beimpft. Diese Kolben werden bei 37 °C unter Schütteln bei 250 U/min inkubiert, bis sie einen OD600 von 0,6-1,0 erreichen.
- Die Proteinexpression wird induziert, indem man jedem Kolben 0,75 ml 1 M Isopropyl-β-D-1-thiogalactopyranosid (IPTG) in Wasser zugibt und diese Kolben bei 37 °C unter Schütteln bei 250 U/min 4 h lang inkubiert.
- Die Zellen aus jedem Kolben werden mit einer 1-Liter-Zentrifugenflasche 12 Minuten lang bei 5.000 x g zentrifugiert. Entsorgen Sie den Überstand.
- Die Pellets in ein konisches 50-ml-Röhrchen geben und jedes Pellet wiegen. Die Zellen werden in flüssigem Stickstoff schockgefroren und bei -80 °C gelagert oder mit Schritt 3.2 fortgefahren.
HINWEIS: Es wird erwartet, dass 2-5 g Zellen pro 0,75 ml aus diesem Schritt resultieren.
- Proteinreinigung durch Nickel-Affinitätssäulenchromatographie
- Bereiten Sie den Lysepuffer vor, indem Sie 50 mM Tris-Cl, 500 mM NaCl und 5 mM Imidazol kombinieren. Auf pH 8,0 einstellen.
- Bereiten Sie den Waschpuffer vor, indem Sie 50 mM Tris-Cl, 500 mM NaCl und 25 mM Imidazol kombinieren. Auf pH 8,0 einstellen.
- Bereiten Sie den Elutionspuffer vor, indem Sie 50 mM Tris-Cl, 500 mM NaCl und 250 mM Imidazol kombinieren. Auf pH 8,0 einstellen.
- Bereiten Sie den Dialysepuffer vor, indem Sie 50 mM NaHPO4, 100 mM NaCl und 2% DMSO kombinieren. Auf pH 7,5 einstellen.
- Tauen Sie die Zellpellets auf, indem Sie die Röhrchen in Wasser bei Raumtemperatur legen. Man fügt 5 ml des Lysepuffers pro 1 g des Zellpellets hinzu und resuspendiert durch Vortexing.
- Lysieren Sie die Zellen durch Beschallung. Trennen Sie das Zellhomogenat so, dass nicht mehr als 30 ml pro konischem 50-ml-Röhrchen vorhanden sind, und halten Sie jedes Röhrchen auf Eis. Die Zellen werden mit einem Ultraschallgerät mit einer Sonde mit einem Durchmesser von 0,16 cm in 15 s Runden mit 30 s Pausen 10 Mal lysiert.
HINWEIS: Vermeiden Sie Schaumbildung, da dies das Protein denaturiert. Die Bildung von Schaum kann vermieden werden, indem die Ultraschallspitze während des Betriebs mindestens 2/3 in das Lysat eingetaucht bleibt. Neben der Ultraschallbehandlung sind auch andere Verfahren der Zelllyse möglich44. - Das Lysat wird durch Zentrifugation bei 15.000 x g für 30 min bei 4 °C geklärt und der Überstand in ein neues konisches 50-ml-Röhrchen gegeben.
- Fügen Sie 1 ml Nickel-Nitrilotriessigsäure (Ni-NTA)-Harz pro 5 ml Überstand hinzu. Teilen Sie die Zelllysat/Ni-NTA-Aufschlämmung so auf, dass nicht mehr als 36 ml pro 50 ml konischem Röhrchen vorhanden sind. Inkubieren bei 4 °C auf einem Rohrrotator bei 10 U/min für 1 h.
- Laden Sie das Harz ein, indem Sie die Zelllysat/Ni-NTA-Aufschlämmung in eine 2-ml-Bettvolumen-Chromatographiesäule dekantieren und das Elutionsmittel bei Bedarf für weitere Analysen auffangen, andernfalls entsorgen. Waschen Sie das Harz mit 10 Harzbettvolumen Waschpuffer.
- Sammeln Sie das Protein, indem Sie drei Harzbettvolumina des Elutionspuffers in die Säule geben und das Volumen auf 1,5 ml konzentrieren, indem Sie einen Zentrifugalkonzentrator mit der entsprechenden Molekulargewichts-Cut-off-Membran für jedes Protein verwenden.
- Das Protein wird gegen 2 l Dialysepuffer bei 4 °C für 1 h dialysiert. Dialysieren Sie das Protein erneut gegen 2 L Dialysepuffer über Nacht bei 4 °C.
- Quantifizieren Sie das Protein mit seinem molaren Extinktionskoeffizienten und der Absorption bei 280 nm. Analysieren Sie das Protein auf Reinheit, indem Sie es mit Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese (SDS-PAGE) trennen. Lagern Sie das Protein bei -80 °C.
4. Zellfreie Proteinsynthese
- Herstellung des CFPS-Reaktionsgemisches
- Bereiten Sie die Ergänzungsmischung vor, indem Sie die Schritte Aminosäurelösungsvorbereitung, Energielösungsvorbereitung und Puffervorbereitung in Sun et al.42 befolgen. Einzeln oder kombiniert bei -80 °C in Aliquots lagern. Stellen Sie sicher, dass die Endkonzentrationen mit denen übereinstimmen, die in Sun et al.42 im Abschnitt "Experimentelle Ausführung einer TX-TL-Reaktion" beschrieben sind.
- Bereiten Sie ein Additiv vor, um lineare DNA vor dem Abbau zu schützen. Wenn Sie GamS33,45 verwenden, bereiten Sie sich über die Schritte in Abschnitt 3 oben vor oder beziehen Sie sie von einem kommerziellen Anbieter. Für andere Ansätze siehe die entsprechende Literatur46,47,48. Alternativ kann ein CFPS-System verwendet werden, das keine Zusatzstoffe49 benötigt.
- Bereiten Sie T7-Polymerase, Repressorproteine und andere Zusatzstoffe unter Verwendung der in Abschnitt 3 beschriebenen Schritte vor oder beziehen Sie sie von einem kommerziellen Anbieter.
- Bestimmen Sie die Anzahl der durchzuführenden CFPS-Reaktionen und berechnen Sie die erforderliche Menge jeder Komponente anhand von Tabelle 2. Modifizieren Sie die Konzentrationen der Komponenten, einschließlich des Hinzufügens oder Entfernens von Komponenten nach Bedarf, und stellen Sie die Wassermenge so ein, dass das Endvolumen jedes Reaktionsgemisches immer 10 μL beträgt. Modifizieren Sie in ähnlicher Weise den Master-Mix, um das Dosieren anderer Komponenten durch akustisches Liquid Handling wie gewünscht zu erleichtern (siehe Abschnitt Diskussion ).
- Tauen Sie alle Komponenten auf Eis auf und bereiten Sie eine Mastermischung vor, indem Sie jede Komponente wie oben berechnet mischen. Mischen Sie alle Komponenten gründlich per Pipette. Achten Sie sorgfältig darauf, Ausfällungen zu vermeiden, insbesondere bei der Aminosäuremischung. Halten Sie den Master-Mix auf Eis.
- Kühlen Sie eine 384-Well-Platte auf Eis und verteilen Sie die Mastermischung in 9-μL-Aliquots in jede Vertiefung.
HINWEIS: Es ist möglich, diese Komponenten durch akustisches Liquid Handling zu verteilen, obwohl darauf geachtet werden sollte, dass eine ordnungsgemäße Dosierung sichergestellt wird (siehe Abschnitt "Diskussion " zur Fehlerbehebung).
- Verteilung von Zusatzkomponenten durch akustisches Liquid Handling
- Berechnen Sie die Menge an Repressorprotein (und anderen optionalen Komponenten), die für alle CFPS-Reaktionen erforderlich ist.
- Tauen Sie das Repressorprotein auf Eis auf und verteilen Sie es in einer akustischen Liquid-Handling-Quellplatte oder einer anderen geeigneten Platte. Stellen Sie sicher, dass die für den Typ der verwendeten Quellenplatte erforderliche Menge an Totvolumen angegeben ist.
- Verteilen Sie das Repressorprotein in 1 μL Volumen über den Liquid Handler in die entsprechenden Vertiefungen. Weitere Informationen zur Fehlerbehebung bei der Verteilung finden Sie im Abschnitt Diskussion .
- Standardkurven
- Um einen Vergleich der Ergebnisse mit anderen Studien und anderen Laboratorien zu ermöglichen, ist eine serielle Verdünnung des gereinigten Reporters (siehe Abschnitt 3 zur Proteinreinigung)41 oder des entsprechenden chemischen Standards50 auf die Platte aufzubringen. Wählen Sie einen Konzentrationsbereich, der für den verwendeten Reporter und den erwarteten Ausdrucksbereich der Experimente geeignet ist.
- Ausführen von CFPS-Reaktionen
- Den Plattenleser auf 30 °C vorheizen. Stellen Sie das Plattenlesegerät so ein, dass es mit den Einstellungen liest, die für den in der Kernsequenz verwendeten Reporter geeignet sind, ohne die Schritte zu schütteln.
HINWEIS: Während hier 30 °C verwendet wird, werden auch 29 °C und 37 °C häufig verwendet und funktionieren gut mit diesem Protokoll. Andere Temperaturen können für alternative zellfreie Reaktionspräparate bevorzugt werden. Für Leseintervalle sind 10 Minuten ausreichend, um eine gute Auflösung für die hier dargestellten repräsentativen Daten zu erreichen; Andere Auflösungen können jedoch besser sein, abhängig vom Reporterprotein und dem jeweiligen CFPS-Rezept. - (Optional) Führen Sie zuerst eine Testreaktion durch, um die entsprechende Verstärkungs- oder Empfindlichkeitseinstellung festzulegen, um die Änderung der Fluoreszenz ohne Signalüberlauf zu erfassen.
- Versiegeln Sie die 384-Well-Platte mit einem undurchlässigen, verschließbaren Kunststoffdeckel, um eine Verdunstung zu verhindern. Stellen Sie nach Möglichkeit am Gerät einen vertikalen Temperaturgradienten von 1 °C ein, um die Kondensation auf der Dichtung zu begrenzen. Legen Sie die 384-Well-Platte auf den Plattenhalter und beginnen Sie mit dem Lesen.
- Den Plattenleser auf 30 °C vorheizen. Stellen Sie das Plattenlesegerät so ein, dass es mit den Einstellungen liest, die für den in der Kernsequenz verwendeten Reporter geeignet sind, ohne die Schritte zu schütteln.
Ergebnisse
Um den Nutzen unserer Methoden zu demonstrieren, präsentieren wir Ergebnisse, die die Auswirkungen der Nähe der tetO-Sequenz zum T7-Promotor auf die Regulation der T7-RNAP-gesteuerten Expression beschreiben. Die vollständigen Ergebnisse und ihre Implikationen finden sich in der Arbeit von McManus et al.32. Der Workflow wird in Abbildung 1 beschrieben. Fünfzehn lineare Templates, die sich nur im Abstand des T7-Promotors relativ zur tetO-Sequenz unterschieden, wurden durch PCR-Amplifikation des sfGFP-Reporters mit Primern hergestellt, die dazu bestimmt waren, jede Promotorvariante (Abbildung 2) hinzuzufügen, wie in Abschnitt 2 des Protokolls beschrieben. CFPS-Reaktionskomponenten und Reaktionen wurden nach dem Protokoll hergestellt. Die Expression von sfGFP wurde von jedem Template mit einer Titration von 12 verschiedenen Konzentrationen des TetR-Proteins in dreifacher Ausführung unter Verwendung eines akustischen Liquid Handlers gemessen. Bei 36 CFPS-Reaktionen pro Template und 15 Templates wurden insgesamt 540 Reaktionen für den gesamten Satz von T7-tetO-Kombinationen durchgeführt. Die gesamte Auswertung wurde auf zwei Platten in zwei Plattenlesern durchgeführt. Die Analyse dieser Daten zeigte, dass die T7-RNAP die T7-gesteuerte Expression gleichmäßig bis 13 bp stromabwärts vom Beginn des T7-Transkripts herunterreguliert (Abbildung 3). Dieses Ergebnis hat Implikationen für das zukünftige Design von regulierbaren T7-gesteuerten Genschaltkreisen, indem es ein vermeintliches Fenster für eine effektive Unterdrückung von T7 durch andere Repressoren beschreibt. Der Vergleich der Ergebnisse des hier beschriebenen Protokolls mit DNA, die durch traditionelles Klonen hergestellt wurde, ergab einen kleinen, aber statistisch signifikanten Unterschied im Grad der TetR-Repression zwischen den Formaten. Wir stellten die Hypothese auf, dass die unspezifische Bindung von TetR an die Vektor-DNA den beobachteten Unterschied erklären könnte. Experimentelle Ergebnisse zeigten, dass die Zugabe von linearer Vektor-DNA zu Reaktionen mit linearer Template-DNA die Differenz zu nicht-statistischer Signifikanz reduzierte, obwohl sie Beiträge anderer Faktoren nicht ausschloss, wie z.B. Unterschiede in der Periodizität der DNA-Helix für lineare vs. zirkuläre Formate, die wiederum die TetR-Bindung beeinflussen könnten. Je nach Anwendung kann die Verwendung einer linearen Schablone eine zusätzliche Validierung erfordern.
Darüber hinaus beziehen wir repräsentative Daten zu potenziellen Problemen bei der genauen Dosierung mit akustischem Liquid Handling ein (Abbildung 4). Eine Lösung von 1x phosphatgepufferter Kochsalzlösung (PBS) mit einem pH-Wert von 7,4, die 0,25 mM Tartrazinfarbstoff enthielt, wurde verwendet, um zwei Methoden zur Programmierung eines akustischen Liquid Handlers zur Dosierung von Volumina >1 μL zu evaluieren. Nach der Flüssigkeitsdosierung wurde die Zielplatte versiegelt und bei 1.500 x g für 1 min zentrifugiert und die Extinktion bei 425 nm mit einem Plattenleser gemessen. Repräsentative Ergebnisse von neun Experimenten werden gezeigt und zeigen eine konsistentere Dosierung über die Serie von acht Zielbohrungen, wenn der 5-μL-Transfer in separate 1-μL-Dosen aufgeteilt wird. Basierend auf diesen Beobachtungen wird empfohlen, Transfers >1 μL in mehrere Transfers von ≤1 μL zu zerlegen. Weitere Informationen zur Fehlerbehebung bei diesem wichtigen Aspekt des Protokolls finden Sie im Abschnitt Diskussion .
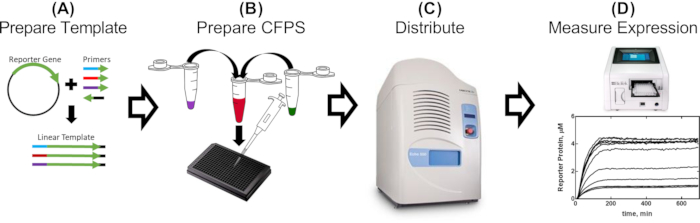
Abbildung 1: Eintägiger Arbeitsablauf zur Bewertung von Promotorteilen in zellfreiem Extrakt. (A) Ein Reporter wird PCR-amplifiziert unter Verwendung von Primern, die genetische Teile enthalten, die ausgewertet werden sollen (2-5 h). (B) Das zellfreie Reaktionsgemisch wird wie im Protokoll beschrieben hergestellt und in eine 384-Well-Platte mit den PCR-amplifizierten Schablonen (30 min) verteilt. (C) Akustisches Liquid Handling wird verwendet, um zusätzliche Komponenten zu verteilen, die Repressorproteine, Effektormoleküle und andere bedingte Effektoren umfassen können (10 min). (D) Die Expression des Reporterproteins aus jeder Reaktion wird in einem Plattenleser gemessen (2-16 h, abhängig von der CFPS-Rezeptur und dem Konstrukt). Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
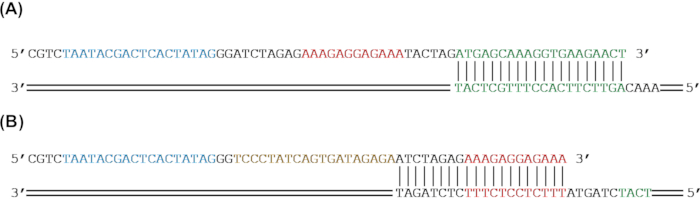
Abbildung 2: Primer-Design für das Hinzufügen genetischer Teile zu einem Reportergen durch PCR-Amplifikation . (A) Das sfGFP-Reporter-Gen (grün) wird durch PCR amplifiziert, um einen RBS (rot) und einen T7-Promotor (blau) hinzuzufügen. (B) Das sfGFP (grün) und ein RBS (rot) werden durch PCR amplifiziert, um eine tetO-Sequenz (gold) und einen T7-Promotor (blau) hinzuzufügen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
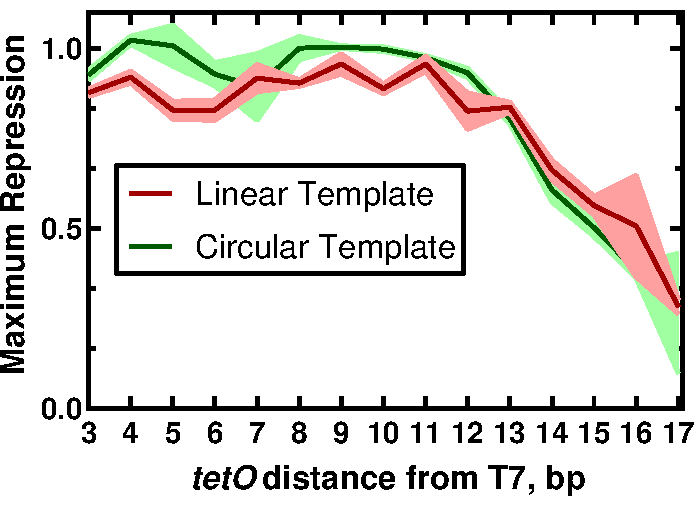
Abbildung 3: Der Einfluss der tetO-Position auf die Regulation einer T7-gesteuerten Expression. Normalisierte maximale Repressionswerte für lineare und kreisförmige Schablonen als Funktion der tetO-Position . Leiterbahnen stellen den Mittelwert und die Standardabweichungen für drei Replikate dar. Diese Abbildung wurde von McManus et al.32 unter einer Creative Commons CC-BY-Lizenz modifiziert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
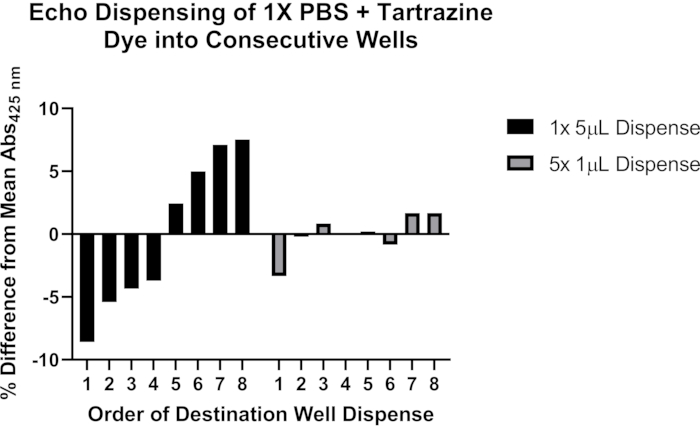
Abbildung 4: Verwendung von Tartrazinfarbstoff zur Validierung der Flüssigkeitsdosierung mit einem akustischen Liquid Handler. Schwarze Balken zeigen an, dass 5 μl Tartrazinlösung aus einer einzigen Quelle mit einem einzigen Programmierbefehl in jedes der acht aufeinanderfolgenden Zielwellen einer 384-Well-Platte abgegeben werden. Graue Balken zeigen an, dass 1 μL aus einer einzigen Quelle mit einem einzigen Programmierbefehl in jedes der acht aufeinanderfolgenden Zielbohrungen abgegeben und dieser Schritt dann viermal wiederholt wird, um insgesamt 5 μl in jedem Zielbohrloch zu dosieren. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
| Name der Komponente | Volumen für 1 Reaktion (μL) | Volumen für 110% von X Anzahl der Reaktionen (μL) |
| Q5 PCR Premix | 25 | |
| Wasser | 4 | |
| Schablone (1–3 ng/μL) | 1 | |
| (falls fixiert1) Forward Primer (5 μM) | 0 oder 10 | |
| (falls fixiert1) Reverse Primer (5 μM) | 0 oder 10 | |
| Master Mix Gesamt: | 30 oder 40 | |
| (beiVariable 1) Forward Primer (5 μM) | 0 oder 10 | |
| (beiVariable 1) Reverse Primer (5 μM) | 0 oder 10 |
Tabelle 1: Arbeitsblatt zur Herstellung von Reagenzien für PCR-Reaktionen. Die Werte in der rechten Spalte können von Benutzern in Abhängigkeit von der beabsichtigten Anzahl der Reaktionen ausgefüllt werden. 1 Variable Primer enthalten einen bestimmten Teil, der in der PCR-Reaktion hinzugefügt wird, und können der Vorwärtsprimer, der Reverse-Primer oder beides sein. Feste Primer fügen kein Teil hinzu und können der Vorwärtsprimer oder der Reverse-Primer sein, aber nicht beides.
| Name der Komponente | Volumen für 1 Reaktion (μL) | Volumen für 110% von X Anzahl der Reaktionen (μL) |
| Zell-Extrakt | 4.2 | |
| Ergänzungs-Mix | 3.3 | |
| GamS-Protein (207 μM) | 0.15 | |
| Template-DNA (20 nM) | 1 | |
| T7-Polymerase (13 mg/ml) | 0.12 | |
| Wasser | 0.73 (diese Zahl kann variieren) | |
| Master Mix Gesamt: | 9 | |
| Repressor-Protein: | 1 |
Tabelle 2: Arbeitsblatt für die Herstellung von Reagenzien für CFPS-Reaktionen. Die Werte in der rechten Spalte können von Benutzern in Abhängigkeit von der beabsichtigten Anzahl der Reaktionen ausgefüllt werden.
Ergänzende Tabelle. Bitte klicken Sie hier, um diese Tabelle herunterzuladen.
Diskussion
Die hier beschriebenen Protokolle bieten eine kostengünstige und schnelle Möglichkeit, genetische Teile durch die Expression eines Reporterproteins durch CFPS zu screenen. Gut charakterisierte genetische Teile sind entscheidend für das Design vorhersagbarer genetischer Schaltkreise mit nützlicher Funktion. Diese Methodik erhöht den Durchsatz und verringert die Zeit, die für das Screening neuer genetischer Teile benötigt wird, indem die Notwendigkeit, in lebenden Zellen zu arbeiten, beseitigt wird, während die Funktionalität erhalten bleibt, die die zelluläre Umgebung widerspiegelt, indem der metabolische Prozess der Proteinexpression im Zelllysat beibehalten wird. Unser Protokoll kann in 1 Tag nach Erhalt der Primer durchgeführt werden (~ 2,5-6 h für die Reaktionsvorbereitung, 2-16 h für die CFPS-Reaktion; Abbildung 1), verglichen mit mindestens 3 Tagen für das traditionelle Klonen (jeweils 1 Tag für den Aufbau und die Transformation des Konstrukts, die Sequenzüberprüfung von Klonen und die Kultivierung von Zellen zur Bewertung). Wir schätzen weiter, dass die Kosten pro Konstrukt mit linearer DNA etwa ein Drittel des traditionellen Klonens betragen (78 US-Dollar gegenüber 237 US-Dollar; Ergänzende Tabelle 1) Methodik. Kommerzielle Synthesedienste bieten derzeit je nach Größe mindestens 4 Werktage an, obwohl sie ähnliche Kosten wie unsere Methode verursachen würden, wenn lineare Fragmente direkt in CFPS gescreent werden (78 US-Dollar gegenüber 91 US-Dollar). Wir haben diesen Ansatz nicht überprüft. Die Kosten für die Bewertung eines Teils mit CFPS sind im Vergleich zur Generierung der Template-DNA gering (0,05 $ / Reaktion22 vs. 78 $ pro Template), obwohl zu beachten ist, dass die Anlaufkosten für Bulk-Reagenzien und Lysegeräte mindestens mehrere tausend Dollar betragen. Der Einsatz eines akustischen Liquid Handlers verbessert die Kosten nur geringfügig, da kleinere Volumina bis zu 0,5 μL40 möglich sind. Der bedeutendere Vorteil ist die Verkürzung der Zeit für die Vorbereitung von Reaktionen (~ 10 min vs. bis zu 1 h, abhängig von der Anzahl der Reaktionen), insbesondere wenn die Vorbereitung einer großen Anzahl von Reaktionen Bedenken hinsichtlich der vorbereiteten Reaktion für längere Zeit vor der Inkubation aufwirft.
Obwohl es schnell und kostengünstig ist, bleiben die Einschränkungen, wann das CFPS-Prototyping die In-vivo-Funktion angemessen vorhersagt, abzuwarten. Zum Beispiel wird eine Kreuzreaktivität mit genomischer DNA nicht erkannt, da das Wirtsgenom während der Produktion des CFPS-Systems entfernt wird. Außerdem können die Komponentenkonzentrationen in CFPS um 1-2 Größenordnungen niedriger sein als in Zellen51, was wahrscheinlich das Verhalten einiger Teile als Folge unterschiedlicher makromolekularer Crowding-Bedingungen beeinflusst. Darüber hinaus kann die Fähigkeit der linearen DNA, die In-vivo-Funktion vorherzusagen, eingeschränkt sein, beispielsweise wenn die DNA-Sekundärstruktur eine wichtige Rolle spielt. Eine letzte Einschränkung besteht darin, dass Konstrukte vor dem Testen auf Funktionen nicht sequenzverifiziert werden. Es kann Fälle geben, in denen der charakterisierte Teil nicht wirklich mit der beabsichtigten theoretischen Reihenfolge übereinstimmt. All diese Einschränkungen können gemildert werden, indem eine Teilmenge der Teile, die mit dieser Methode in der beabsichtigten In-vivo-Anwendung gesiebt wurden, validiert wird.
Wir haben diese Methodik ursprünglich entwickelt, um die Auswirkungen einer Änderung der Bedienerposition auf hybride T7-tetO-Promotoren zu untersuchen 32. Wir haben die Protokolle hier in einem allgemeineren Format vorgestellt, so dass sie auf Promotoren, Operatoren, Ribosomenbindungssequenzen, Isolatoren und Terminatoren angewendet werden können. Diese genetischen Teile können durch PCR unter Verwendung von Primern für jedes Design an das 5- oder 3ʹ-Ende des Reportergens angefügt werden, wodurch die Notwendigkeit einer Synthese oder Klonierung jeder zu testenden Variante entfällt. Die resultierenden PCR-Produkte dienen als Template-DNA für die Auswertung über die Expression eines Reporterproteins. In unserer Arbeit wurde das hier bereitgestellte Affinitätsreinigungsprotokoll für TetR und GamS verwendet. Das gleiche Verfahren kann für die Expression und Reinigung anderer Repressoren, Aktivatoren, Polymerasen, Sigma-Faktoren und anderer Proteine verwendet werden, die mit einem genetischen Teil von Interesse verwandt sind, obwohl Modifikationen erforderlich sein können, damit das gewünschte Protein exprimiert wird. Die Aufreinigung und Titration dieser Proteine in CFPS-Reaktionen ermöglicht eine detailliertere Charakterisierung eines bestimmten genetischen Teils. Schließlich gibt es zahlreiche alternative CFPS-Protokolle, von denen jedes für den Teile-Screening-Teil der Methodik geeignet sein sollte. Als Beispiel nehmen wir keinen Dialyseschritt in dieses Protokoll auf, den andere als wichtig für die Expression von nativen bakteriellen Promotoren erachtet haben22. Es ist auch möglich, die Konzentrationen der zugrunde liegenden Bestandteile der GFPS zu variieren. Der Einsatz von Liquid Handling verbessert die Fähigkeit, die unzähligen Bedingungen zu testen, indem der Durchsatz erhöht und der Materialbedarf verringertwird 34,35.
Ein Bereich, der eine erhebliche Fehlersuche erfordern kann, ist die Optimierung des akustischen Liquid Handlers. Die Dosierung von Acoustic Liquid Handlern sollte für jede zu übertragende Komponente optimiert werden, und es wird dringend empfohlen, Kontrollen durchzuführen, um die ordnungsgemäße Verteilung und Reproduzierbarkeit vor der Datenerfassung zu überprüfen. Der ideale Quellplattentyp und die Einstellung der Flüssigkeitsklasse hängen von der zu dosierenden Flüssigkeit und ihren Bestandteilen ab. Es wird nicht empfohlen, aminbeschichtete Platten zum Dosieren von DNA zu verwenden, da die Aminbeschichtung mit der DNA interagieren kann. Es sollte auch beachtet werden, dass die Fähigkeit, höhere Konzentrationen bestimmter Komponenten abzugeben, vom akustischen Liquid-Handler-Modell abhängen kann. Ein Testflüssigkeitstransfer kann durch Dosieren auf eine Folienplattendichtung durchgeführt werden, um eine erfolgreiche Tröpfchenbildung sichtbar zu machen; Dieser Test liefert jedoch nur begrenzte Informationen, und Tröpfchen aus verschiedenen Einstellungen können identisch erscheinen. Die Verwendung eines wasserlöslichen Farbstoffs, wie z. B. Tartrazin, kann verwendet werden, um genauer zu überprüfen, ob das richtige Volumen bei einer bestimmten Einstellung oder einem bestimmten Arbeitsablauf abgegeben wird (siehe Repräsentative Ergebnisse). Eine optimale Programmierung von Flüssigkeitstransfers kann auch die Genauigkeit und Konsistenz der generierten Daten beeinflussen. Für Transfers >1 μL von einem Quellbohrloch zu einem Zielbohrloch haben wir festgestellt, dass sequentielle Transfers von ≤1 μL programmiert werden sollten, um die systematische Well-to-Well-Variabilität zu reduzieren (Abbildung 4). Schließlich können die theoretischen und tatsächlichen Volumina der Quelle je nach Art der Quellplatte, der Flüssigkeitsklasseneinstellung und den Komponenten der spezifischen Flüssigkeit dramatisch variieren. Die Verwendung der Acoustic Liquid Handler Survey-Funktion zur Beurteilung des Bohrlochvolumens vor dem Ausführen eines Programms kann dazu beitragen, zu beurteilen, wie genau das Gerät in der Lage ist, eine bestimmte Flüssigkeit zu messen.
Die CFPS-Reaktionsleistung kann variieren, wenn die Ergebnisse zwischen verschiedenen Anwendern, Materialchargen, Plattenlesern und Laboratorien verglichenwerden 41. Für Fälle, in denen solche Vergleiche beim Prototyping genetischer Schaltkreise erforderlich sind, empfehlen wir, interne Kontrollreaktionen mit standardmäßigen konstitutiven Promotoren in jede Reaktionsplatte aufzunehmen, um die Ergebnisse über Versuchsaufbauten hinweg zu normalisieren. Die Methode der DNA-Präparation kann auch wesentlich zur CFPS-Aktivität beitragen. Die Einbeziehung eines Ethanol-Fällungsschritts wird empfohlen. Darüber hinaus kann die optimale Reaktionszusammensetzung durch die Charge des Extrakts34 variieren. Es hat sich gezeigt, dass insbesondere die optimalen Konzentrationen von Magnesiumglutamat und Kaliumglutamat je nach Charge42 oder mit dem verwendeten Promotor- oder Reporterprotein24 variieren. Die Konzentrationen dieser Komponenten sollten optimiert werden, indem mehrere Konzentrationen jeder Komponente pro genetischem Konstrukt und pro Zellextraktpräparat untersucht werden, um die optimalen Bedingungen für die Proteinexpression zu bestimmen. Zu den Best Practices für eine konsistente CFPS-Reaktionsleistung gehören gründliches Mischen, sorgfältiges Pipettieren und Konsistenz bei der Herstellung jeder Reagenzkomponente.
Über die Charakterisierung einzelner Teile hinaus kann das gleiche Verfahren verwendet werden, um Kombinationen von Teilen zu untersuchen, die komplexe Schaltkreise bilden, wie z.B. Logikschaltungen16 oder Oszillatoren52,53. Diese Methode kann auch zum Screening und zur Optimierung von Biosensoren für Anwendungen in der epidemiologischen Diagnostik54, 55, 56, 57 oder zur Gefahrenerkennung und -quantifizierung3, 58, 59 angewendet werden. Die Anwendung von KI-gesteuerten Techniken wie aktivem Lernen34 kann auch mit dem Hochdurchsatzcharakter dieser Methode kombiniert werden, um die schnelle Erkundung komplexer biologischer Designräume voranzutreiben. Letztendlich stellen wir uns vor, dass dieser Ansatz beschleunigte Entwicklungszeiten für neue genetische Designs in der synthetischen Biologie unterstützt.
Offenlegungen
RMM ist finanziell an Tierra Biosciences beteiligt, einem privaten Unternehmen, das zellfreie Technologien wie die in diesem Artikel beschriebenen für die Proteinexpression und das Screening einsetzt.
Die anderen Autoren haben nichts offenzulegen.
Danksagungen
Diese Arbeit wurde durch das Programm "Angewandte Forschung für die Förderung von Wissenschafts- und Technologieprioritäten" des Büros des Verteidigungsministers ermöglicht. Wir danken Scott Walper (Naval Research Laboratory) für die Bereitstellung des Bestandes an verwendetem sfGFP und Zachary Sun und Abel Chiao (Tierra Biosciences) für fruchtbare Diskussionen im Zusammenhang mit dem Prototyping mit zellfreien Systemen und der damit verbundenen Fehlerbehebung des akustischen Liquid Handlings.
Materialien
| Name | Company | Catalog Number | Comments |
| 2x YT medium | Sigma-Aldrich | Y2377-250G | Alternative to making 2xYT media |
| Agar | Bacto | 214010 | For plating cells |
| Chromatography column (5 cm diameter) | BIO-RAD | 731-1550 | Used for protein purification. |
| Destination plate | Thermo Scientific Nunc plate | 142761 | For CFPS reactions |
| DMSO | Sigma-Aldrich | D2650 | For dialysis buffer |
| DpnI | NEB | R0176L | For digestion of plasmid templates |
| DTT | Roche | 20871723 | S30 Buffer B |
| E. coli BL21(DE3) Rosetta2 | Novagen | 70954 | Cell line used for production of lysate and purified proteins |
| Echo acoustic liquid handler | Labcyte | 525 | Acoustic liquid handler |
| French pressure cell | Thermo Spectronic | FA-078 | For lysing cells for CFPS |
| Imidazole | Sigma-Aldrich | 56750 | For buffers |
| Impermeable plastic sealable lid | Thermo | 232702 | Plate seal |
| IPTG | RPI | I56000-25.0 | Used for protein induction. |
| K-Glu | Sigma-Aldrich | g1501-500G | S30 Buffer B |
| Labcyte Echo source plate | Labcyte | PL-05525 | For use with Echo acoustic liquid handler |
| Mg-Glu | Sigma-Aldrich | 49605-250G | S30 Buffer B |
| NaCl | Sigma-Aldrich | S7653-250G | For buffers |
| NaHPO4 | Sigma-Aldrich | 71505 | For dialysis buffer |
| NaOH | Mallinckrodt Chemicals | 7708-10 | For making 2xYT media. Currently not produced by Mallinckrodt. Alternate: Sigma-Aldrich S0899 |
| Ni-NTA resin | Invitrogen | R901-15 | For production of purified proteins |
| PCR H2O | Ambion | AM9937 | PCR of linear templates |
| Plate Reader | BioTek | H10 | Plate reader used |
| Q5 PCR Master Mix | NEB | M0494S | PCR of linear templates |
| QIAquick Gel Extraction Kit | Qiagen | 28606 | PCR of linear templates |
| QIAquick PCR Purification Kit | Qiagen | 28004 | PCR of linear templates |
| QSonica Ultrasonic Processor | Qsonica | Q700 | Cell disruption during protein purification |
| RTS Amino Acid Sampler | biotechrabbit | BR1401801 | Updated supplier from Sun et al. |
| Tris | MP | 819623 | S30 Buffer B |
| Tris-Cl | Sigma-Aldrich | T5941 | For buffers |
| Tryptone | Fluka | T7293 | For making 2xYT media |
| Yeast Extract | Bacto | 212750 | For making 2xYT media |
Referenzen
- Purnick, P. E. M., Weiss, R. The second wave of synthetic biology: from modules to systems. Nature Reviews. Molecular Cell Biology. 10 (6), 410-422 (2009).
- Saltepe, B., Kehribar, E. Ş, Su Yirmibeşoǧlu, S. S., Şafak Şeker, U. Ö Cellular biosensors with engineered genetic circuits. ACS Sensors. 3 (1), 13-26 (2018).
- Bereza-Malcolm, L. T., Mann, G., Franks, A. E. Environmental sensing of heavy metals through whole cell microbial biosensors: A synthetic biology approach. ACS Synthetic Biology. 4 (5), 535-546 (2015).
- Mimee, M., et al. An ingestible bacterial-electronic system to monitor gastrointestinal health. Science. 360 (6391), 915-918 (2018).
- Isabella, V. M., et al. Development of a synthetic live bacterial therapeutic for the human metabolic disease phenylketonuria. Nature Biotechnology. 36 (9), 857-867 (2018).
- Healy, C. P., Deans, T. L. Genetic circuits to engineer tissues with alternative functions. Journal of Biological Engineering. 13, 39(2019).
- Kaushik, A., Tiwari, S., Dev Jayant, R., Marty, A., Nair, M. Towards detection and diagnosis of Ebola virus disease at point-of-care. Biosensors and Bioelectronics. 75, 254-272 (2016).
- Jagadevan, S., et al. Recent developments in synthetic biology and metabolic engineering in microalgae towards biofuel production. Biotechnology for Biofuels. 11, 185(2018).
- Keating, K. W., Young, E. M. Synthetic biology for bio-derived structural materials. Current Opinion in Chemical Engineering. 24, 107-114 (2019).
- Smanski, M. J., et al. Synthetic biology to access and expand nature's chemical diversity. Nature Reviews Microbiology. 14 (3), 135-149 (2016).
- Xiang, Y., Dalchau, N., Wang, B. Scaling up genetic circuit design for cellular computing: advances and prospects. Natural Computing. 17 (4), 833-853 (2018).
- Galdzicki, M., Rodriguez, C., Chandran, D., Sauro, H. M., Gennari, J. H. Standard biological parts knowledgebase. PLoS One. 6 (2), 17005(2011).
- Kelwick, R., Bowater, L., Yeoman, K. H., Bowater, R. P. Promoting microbiology education through the iGEM synthetic biology competition. FEMS Microbiology Letters. 362 (16), (2015).
- Torella, J. P., et al. Unique nucleotide sequence-guided assembly of repetitive DNA parts for synthetic biology applications. Nature Protocols. 9 (9), 2075-2089 (2014).
- Halleran, A. D., Swaminathan, A., Murray, R. M. Single day construction of multigene circuits with 3G assembly. ACS Synthetic Biology. 7 (5), 1477-1480 (2018).
- Nielsen, A. K., et al. Genetic circuit design automation. Science. 352 (6281), (2016).
- Canton, B., Labno, A., Endy, D. Refinement and standardization of synthetic biological parts and devices. Nature Biotechnology. 26 (7), 787-793 (2008).
- Boehm, C. R., Bock, R. Recent advances and current challenges in synthetic biology of the plastid genetic system and metabolism. Plant Physiology. 179 (3), 794-802 (2019).
- Takahashi, M. K., et al. Characterizing and prototyping genetic networks with cell-free transcription-translation reactions. Methods. 86, 60-72 (2015).
- Chappell, J., Watters, K. E., Takahashi, M. K., Lucks, J. B. A renaissance in RNA synthetic biology: New mechanisms, applications and tools for the future. Current Opinion in Chemical Biology. 28, 47-56 (2015).
- Endy, D. Foundations for engineering biology. Nature. 438 (7067), 449-453 (2005).
- Silverman, A. D., Karim, A. S., Jewett, M. C. Cell-free gene expression: an expanded repertoire of applications. Nat. Reviews. Genetics. 21 (3), 151-170 (2020).
- Dopp, J. L., Rothstein, S. M., Mansell, T. J., Reuel, N. F. Rapid prototyping of proteins: Mail order gene fragments to assayable proteins within 24 hours. Biotechnology and Bioengineering. 116 (3), 667-676 (2019).
- Garamella, J., Marshall, R., Rustad, M., Noireaux, V. The all E. coli TX-TL toolbox 2.0: A platform for cell-free synthetic biology. ACS Synthetic Biology. 5 (4), 344-355 (2016).
- Kopniczky, M. B., et al. Cell-free protein synthesis as a prototyping platform for mammalian synthetic biology. ACS Synthetic Biology. 9 (1), 144-156 (2020).
- Kelwick, R., et al. Cell-free prototyping strategies for enhancing the sustainable production of polyhydroxyalkanoates bioplastics. Synthetic Biology. 3 (1), (2018).
- Karim, A. S., et al. In vitro prototyping and rapid optimization of biosynthetic enzymes for cell design. Nature Chemical Biology. 16 (8), 912-919 (2020).
- Takahashi, M. K., et al. Rapidly characterizing the fast dynamics of RNA genetic circuitry with cell-free Transcription-Translation (TX-TL) systems. ACS Synthetic Biology. 4 (5), 503-515 (2015).
- Chappell, J., Jensen, K., Freemont, P. S. Validation of an entirely in vitro approach for rapid prototyping of DNA regulatory elements for synthetic biology. Nucleic Acids Research. 41 (5), 3471-3481 (2013).
- Borkowski, O., et al. Cell-free prediction of protein expression costs for growing cells. Nature Communications. 9 (1), 1457(2018).
- Dudley, Q. M., Karim, A. S., Nash, C. J., Jewett, M. C. In vitro prototyping of limonene biosynthesis using cell-free protein synthesis. Metabolic Engineering. 61, 251-260 (2020).
- McManus, J. B., Emanuel, P. A., Murray, R. M., Lux, M. W. A method for cost-effective and rapid characterization of engineered T7-based transcription factors by cell-free protein synthesis reveals insights into the regulation of T7 RNA polymerase-driven expression. Archives of Biochemistry and Biophysics. 674, 108045(2019).
- Sun, Z. Z., Yeung, E., Hayes, C. A., Noireaux, V., Murray, R. M. Linear DNA for rapid prototyping of synthetic biological circuits in an escherichia coli based TX-TL cell-free system. ACS Synthetic Biology. 3 (6), 387-397 (2014).
- Borkowski, O., et al. Large scale active-learning-guided exploration for in vitro protein production optimization. Nature Communications. 11 (1), 1872(2020).
- Caschera, F., et al. High-throughput optimization cycle of a cell-free ribosome assembly and protein synthesis system. ACS Synthetic Biology. 7 (12), 2841-2853 (2018).
- Iyer, S., Karig, D. K., Norred, S. E., Simpson, M. L., Doktycz, M. J. Multi-input regulation and logic with T7 promoters in cells and cell-free systems. PLoS One. 8 (10), 78442(2013).
- Karig, D. K., Iyer, S., Simpson, M. L., Doktycz, M. J. Expression optimization and synthetic gene networks in cell-free systems. Nucleic Acids Research. 40 (8), 3763-3774 (2012).
- Jung, J. K., et al. Cell-free biosensors for rapid detection of water contaminants. Nature Biotechnology. 38 (12), 1451-1459 (2020).
- Bailey, J., Eggenstein, E., Lesnick, J. Miniaturization and rapid processing of TXTL reactions using acoustic liquid handling. Labcyte Technical Note. , 1-12 (2018).
- Marshall, R., Garamella, J., Noireaux, V., Pierson, A. High-throughput microliter-sized cell-free transcription-translation reactions for synthetic biology applications using the echo 550 liquid handler. Labcyte Application Note. , 1-6 (2018).
- Cole, S. D., et al. Quantification of interlaboratory cell-free protein synthesis variability. ACS Synthetic Biology. 8 (9), 2080-2091 (2019).
- Sun, Z. Z., et al. Protocols for implementing an Escherichia coli based TX-TL cell-free expression system for synthetic biology. Journal of Visualized Experiments: JoVE. (79), e50762(2013).
- Dopp, J. L., Tamiev, D. D., Reuel, N. F. Cell-free supplement mixtures: Elucidating the history and biochemical utility of additives used to support in vitro protein synthesis in E. coli extract. Biotechnology Advances. 37 (1), 246-258 (2019).
- Cole, S. D., Miklos, A. E., Chiao, A. C., Sun, Z. Z., Lux, M. W. Methodologies for preparation of prokaryotic extracts for cell-free expression systems. Synthetic and Systems Biotechnology. 5 (4), 252-267 (2020).
- Sitaraman, K., et al. A novel cell-free protein synthesis system. Journal of Biotechnology. 110 (3), 257-263 (2004).
- Marshall, R., Maxwell, C. S., Collins, S. P., Beisel, C. L., Noireaux, V. Short DNA containing χ sites enhances DNA stability and gene expression in E. coli cell-free transcription-translation systems. Biotechnology and Bioengineering. 114 (9), 2137-2141 (2017).
- Yim, S. S., Johns, N. I., Noireaux, V., Wang, H. H. Protecting linear DNA templates in cell-free expression systems from diverse bacteria. ACS Synthetic Biology. 9 (10), 2851-2855 (2020).
- Zhu, B., et al. Increasing cell-free gene expression yields from linear templates in Escherichia coli and Vibrio natriegens extracts by using DNA-binding proteins. Biotechnology and Bioengineering. 117 (12), 3849-3857 (2020).
- Tuckey, C., Asahara, H., Zhou, Y., Chong, S. Protein synthesis using a reconstituted cell-free system. Current Protocols in Molecular Biology. 108, 1-22 (2014).
- Hoffman, R. A., Wang, L., Bigos, M., Nolan, J. P. NIST/ISAC standardization study: Variability in assignment of intensity values to fluorescence standard beads and in cross calibration of standard beads to hard dyed beads. Cytometry. Part A. 81 (9), 785-796 (2012).
- Karzbrun, E., Shin, J., Bar-Ziv, R. H., Noireaux, V. Coarse-grained dynamics of protein synthesis in a cell-free system. Physical Review Letters. 106 (4), 048104(2011).
- Rossi, N. A., Dunlop, M. J. Making waves with synthetic oscillators. Cell Systems. 6 (4), 406-407 (2018).
- Niederholtmeyer, H., et al. Rapid cell-free forward engineering of novel genetic ring oscillators. eLife. 4, 09771(2015).
- Chang, H., Voyvodic, P. L., Structurale, C. D. B. Microbially derived biosensors for diagnosis, monitoring and epidemiology. Microbial Biotechnology. 10 (5), 1031-1035 (2017).
- Pardee, K., et al. low-cost detection of Zika virus using programmable biomolecular components. Cell. 165 (5), 1255-1266 (2016).
- Pardee, K., et al. Portable, on-demand biomolecular manufacturing. Cell. 167 (1), 248-259 (2016).
- Pardee, K., et al. Paper-based synthetic gene networks. Cell. 159 (4), 940-954 (2014).
- Liu, X., Germaine, K. J., Ryan, D., Dowling, D. N. Whole-cell fluorescent biosensors for bioavailability and biodegradation of polychlorinated biphenyls. Sensors. 10 (2), 1377-1398 (2010).
- Gautam, P., Suniti, S., Amrita, K., Madathil, D., Nair, B. A Review on Recent Advances in Biosensors for Detection of Water Contamination. International Journal of Environmental Sciences. 2 (3), 1565-1574 (2012).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten