Method Article
Células Progenitoras de aislamiento Mesangiogenic (PSM) de Humana de Médula Ósea
* Estos autores han contribuido por igual
En este artículo
Resumen
Here we describe an optimized, highly reproducible protocol to isolate Mesodermal Progenitor Cells (MPCs) from human bone marrow (hBM). MPCs were characterized by flow cytometry and nestin expression. They showed the ability to give rise to exponentially growing MSC-like cell cultures while retaining their angiogenic potential.
Resumen
In a research study aimed to isolate human bone marrow (hBM)-derived Mesenchymal Stromal Cells (MSCs) for clinical applications, we identified a novel cell population specifically selected for growth in human serum supplemented medium. These cells are characterized by morphological, phenotypic, and molecular features distinct from MSCs and we named them Mesodermal Progenitor Cells (MPCs). MPCs are round, with a thick highly refringent core region; they show strong, trypsin resistant adherence to plastic. Failure to expand MPCs directly revealed that they are slow in cycling. This is as also suggested by Ki-67 negativity. On the other hand, culturing MPCs in standard medium designed for MSC expansion, gave rise to a population of exponentially growing MSC-like cells. Besides showing mesenchymal differentiation capacity MPCs retained angiogenic potential, confirming their multiple lineage progenitor nature. Here we describe an optimized highly reproducible protocol to isolate and characterize hBM-MPCs by flow cytometry (CD73, CD90, CD31, and CD45), nestin expression, and F-actin organization. Protocols for mesengenic and angiogenic differentiation of MPCs are also provided. Here we also suggest a more appropriate nomenclature for these cells, which has been re-named as "Mesangiogenic Progenitor Cells".
Introducción
Las células estromales mesenquimales (MSC) son de valor clínico relevante por su capacidad de diferenciación multi-linaje y su capacidad para soportar la hemopoyesis, para secretar factores de crecimiento / citoquinas, así como de desempeñar un papel en la inmunorregulación 1. En la definición de la producción de células terapias basadas en el MSC y la aplicación han sido objeto de una amplia investigación clínica y preclínica 2, con especial atención a la regulación internacional específico para la seguridad y eficacia de la célula de productos medicinales (CBMP) 3 tratamientos a base. MSCs humanas son ampliamente cultivadas en medios que contienen suplementos y reactivos de origen animal, tales como suero fetal bovino (FBS) y tripsina bovina. Por lo tanto, junto con los riesgos de infección asociados a la manipulación de células, los pacientes también se enfrentan a la exposición del prión, así como los riesgos inmunológicos vinculados a las proteínas, péptidos u otras biomoléculas de origen animal que podrían persistir después de la recolección de células y transplantación 4.
Para evitar el problema, cultivamos la médula ósea humana (HBM) -derivado MSC en medio libre de animales, en sustitución de FBS con agrupada humana de tipo AB suero (Phab). En estas condiciones, junto con MSCs crecientes hemos identificado un nuevo población celular. Estas células fueron morfológicamente y fenotípicamente diferentes de las MSC y mostró un perfil de expresión de genes distintivos, así como propiedades características de crecimiento / de adhesión. Se conservan las dos células mesodérmicas Progenitoras mesengenic y el potencial angiogénicos y por lo tanto fueron nombrados (PSM) 5. Posteriormente, hemos sido capaces de definir las condiciones de cultivo selectivas y reproducibles para generar PSM con alto grado de pureza 6.
Además, investigó las propiedades morfológicas y biológicas de los PSM. Los PSM mostraron ser nestina positivas, lento en el ciclismo, Ki-67-negativo, y con los cromosomas que se caracterizan por largos telómeros 5. Expresaron plurLos factores de transcripción asociados ipotency-MSC maestros reguladores Runx2 y Sox9 7 Oct-4 y Nanog en lugar de. Fenotípicamente, PSM expresó endoglina (CD105) en el nivel más bajo que las MSC mientras que carecen de marcadores mesenquimales CD73, CD90, CD166. PSM también mostró un patrón distintivo de moléculas de adhesión que se caracterizan por la expresión coherente de PECAM (CD31), integrinas αL (CD11a), αM (CD11b), αX (CD11c), así como la integrina β2 (CD18) que sustenta específicamente estructuras podosome-como 8 . En los medios de expansión MSC estándar, PSM diferenciarse rápidamente en las MSC a través de una etapa intermedia que ofrece la activación de Wnt5 / calmodulina de señalización 9 de la célula. PSM también retuvo propiedades angiogénicas, como se ha demostrado por su capacidad de brotar de esferoides en la matriz extracelular (ECM) cultivos 3D de proteínas murinas. El potencial angiogénico se pierde rápidamente después de la diferenciación MPC lo largo del linaje mesengenic.
Aquí presentamos Proprotocolos optimizados para aislar y caracterizar los PSM altamente purificadas de las muestras de sangre HBM. También se describen los protocolos reproducibles para MPC mesengenic y diferenciación angiogénico.
Protocolo
NOTA: Después de consentimiento por escrito, se obtuvieron muestras de HBM durante la cirugía ortopédica de reemplazo de cadera. Inmediatamente después de la osteotomía del cuello femoral y antes femoral escariado una jeringa de 20 ml que contiene 500 UI de heparina, se utilizó para aspirar BM fresco. El protocolo debe ser considerado ampliamente aplicable a cualquier fuente BM.
1. Aislamiento del hueso humano células de la médula mononucleares (MNC HBM-)
- Diluir 5 - 10 ml de BM fresco a 50 ml, la aplicación de solución salina tamponada con fosfato de Dulbecco (D-PBS) y se mezcla por inversión. Igualmente distribuir 25 ml en dos nuevos tubos de 50 ml cónicos, añadir 25 ml de D-PBS a cada tubo y mezclar por inversión.
- Permitir que los tubos en reposo durante 10 min a temperatura ambiente, para la separación de fragmentos de hueso minerales y grasa de la solución.
- Retirar con cuidado la grasa flotante con una suspensión de células pipeta Pasteur y el filtro estéril a través de filtros de 70 micras sin perturbar el sedimento fragmento de hueso mineral.
- Establecer cuatro tubos de 50 ml con 15 ml de medio de centrifugación en gradiente de densidad discontinuo (1,077 g / ml). Asegúrese de que este medio es a temperatura ambiente.
- Coloque con cuidado 20 - 25 ml de BM diluida en la parte superior del medio de gradiente de densidad. Realice esta operación con cuidado, dejando goteo suspensión de células en las paredes del tubo para evitar que las capas de mezcla.
- Llevar a cabo la centrifugación en gradiente de densidad a 400 xg durante 30 min a temperatura ambiente con frenado está desactivado.
- Recoger el anillo blanquecino de células situadas entre las dos fases utilizando una pipeta Pasteur estéril y la transfiere a un nuevo tubo de 50 ml.
- Lavar las células con medio de cultivo fresco: libre de rojo fenol, nivel bajo de glucosa (1000 mg / l) de Eagle modificado por Dulbecco (DMEM), 10% (v / v) agrupado tipo AB de suero humano (Phab), 2 mM L-glutamina y antibióticos (DMEM / 10% Phab). Centrifugar a 400 xg durante 5 min.
- Aspirar el sobrenadante y resuspender en pellets de 5 - 10 ml de DMEM fresco / 10% Phab.
- Continúe con el recuento de células.Determinar el número de células blancas de la sangre por 1: 1 de dilución en tripano. Aplicar esto a la hemocitómetro, y observar con un microscopio de contraste de fase. Excluir eritrocitos pequeños y perfectamente redondeados y las células muertas teñidas de azul desde el recuento de células.
NOTA: Se recomienda Phab pantalla lotes por su rendimiento en la recuperación de MPC. Phab de fuentes USA han dado mejores resultados mientras que la mayoría de los sueros de origen diferente resultó en culturas MPC con porcentajes más altos de células MSC-como.
2. Aislamiento del PSM de HBM-MNC
- Conjunto hidrófobos matraces T-75 con 15 ml de DMEM / 10% Phab y dejar que el pH y la temperatura se equilibran por pre-incubación a 37 ° C en 5% de CO2 durante 30 min.
- Semilla 4 - 6 x 10 7 HBM-MNC por matraz y se incuba a 37 ° C en 5% de CO2 durante 48 horas.
- Aspirar y desechar las células medianas y no adherentes de los matraces. Añadir 15 ml de DMEM / 10% Phab y se incuba a 37 ° Cen 5% de CO 2. Mantener los cultivos durante 6 - 8 días, cambiando el medio cada 48 horas.
OPCIONAL: Para aumentar el rendimiento MPC, las células no adherentes de 2.3 podrían ser re-chapada en un nuevo frasco de cultivo y se mantienen como se describe para los cultivos primarios. - Aspirar y descartar medio de los matraces, lavar con DMEM fresco y añadir 2 ml de solución de animales proteasa libre de desprendimiento. Se incuba a 37 ° C durante 5 - 15 min (evitar la incubación prolongada).
- Añadir 10 ml de DMEM fresco / 10% Phab, aspirar la suspensión de células y se centrifuga a 400 xg durante 5 min
- Aspirar y desechar el sobrenadante y volver a suspender sedimento en 1 - 2 ml de DMEM fresco / 10% Phab. Continúe con el recuento de células como se describe en el paso 1.10.
NOTA: No utilice tripsina / EDTA como reactivo de desprendimiento. PSM son la tripsina resistentes. detección morfológica de las culturas, antes de la recolección de células, es muy recomendable con el fin de evaluar la presencia de células MSC-como en forma de huso. En caso considerable cantidad de células MSC-como son detected, aumentar la pureza del producto de células por la eliminación selectiva de las células contaminadas. Para ello, la digestión con tripsina se puede llevar a cabo antes de la recolección MPC, mediante la adición de 2 ml de tripsina / EDTA 0,05% durante 2 min. culturas de lavado dos veces con 5 ml de DMEM / 10% Phab, a continuación, proceder al tratamiento con proteasas que el anterior.
3. Caracterización de la célula
- Citometría de flujo
- Configurar las muestras duplicadas de 10 5 células recién desprendidas en la solución de lavado: D-PBS suplementado con 0,5% (v / v) de albúmina de suero bovino (BSA) y 0,02% (w / v) de azida de sodio. Centrifugar a 400 xg durante 5 min.
PRECAUCIÓN: La azida sódica es tóxica. - Vuelva a suspender gránulos en 200 l de solución de lavado y añadir anti-CD90, anti-CD45, anti-CD73 y anti-CD31 anticuerpos conjugados con colorantes fluorescentes ( "test"); en paralelo configurar los controles de isotipo ( "CTRL").
NOTA: Las cantidades de tinción de anticuerpos deben determinarse mediante titulación o According con las instrucciones del fabricante. - Incubar las muestras a 4 ° C durante 30 min.
- Centrifugar a 400 xg durante 5 min. Vuelva a suspender las células en 500 l de solución de lavado y adquirir al menos 5 x 10 4 eventos en el flujo multicolor citómetro 7 9 10.
- Analizar los resultados de dot-parcelas y utilizar "CTRL" eventos registrados para establecer cuadrantes.
NOTA: Con el fin de definir la cultura como la cultura MPC el porcentaje de CD73 CD90 neg neg células CD31 + CD45 + debe ser superior al 95%. Para algunas aplicaciones específicas, es decir, el análisis de la expresión génica, la recuperación de corte tiene que ser aumentado a 97-98%.
- Configurar las muestras duplicadas de 10 5 células recién desprendidas en la solución de lavado: D-PBS suplementado con 0,5% (v / v) de albúmina de suero bovino (BSA) y 0,02% (w / v) de azida de sodio. Centrifugar a 400 xg durante 5 min.
- la detección y el análisis de la organización nestin F-actina
- Placa recién aisladas PSM en portaobjetos de cámara de cultivo (20.000 / cm2). Permitir que las células se adhieren por incubación durante la noche a 37 ° C en 5% de CO 2.
- Lavar las células en la solución de lavado y fix en 4% (w / v) para-formaldehído a temperatura ambiente durante 15 min. Para retirar el fijador, añadir la solución de lavado, se incuba durante 2 minutos y se vierte.
- Repetir el lavado dos veces.
- Permeabilizar células en D-PBS suplementado con 0,05% (v / v) de Triton X-100 durante 15 min a RT.
- Se interrumpe la reacción por la proteína potenciador libre de señal (30 min a RT) o solución de bloqueo estándar (D-PBS suplementado con 3% (w / v) BSA).
- Retire mejorador de señal / solución de bloqueo.
- Añadir 7 g / ml (w / v) de anticuerpo primario anti-nestina humano y se incuba a 4 ° C durante la noche en una cámara humidificada. Al mismo tiempo, utilizar anticuerpos de control isotıpicos para evaluar las señales de fluorescencia no específicos.
- Lavado de los portaobjetos mediante la adición de D-PBS, dejar durante 2 minutos y se vierte. Repetir dos veces.
- Añadir 2 g / ml (w / v) de colorante fluorescente anticuerpo secundario conjugado y se incuba a 4 ° C durante 1 hora en la oscuridad.
- Lavar los portaobjetos que el anterior.
- Añadir faloidina fluorescente (5 UI / ml), dejar a temperatura ambiente durante 30 men en la oscuridad y lavar 3 veces en D-PBS.
- Retire las paredes de la cámara y montar diapositivas en medio de montaje acuoso suplementado con antifade reactivo y 4 ', 6-diamidino-2-fenilindol (DAPI) para la detección de núcleos. Proceder a la formación de imágenes 7 9 10.
4. Diferenciación de Mesengenic PSM
- Placa de 2 x 10 4 / cm2 PSM recién aisladas en frascos de cultivo T75 tratadas con TC y dejar que las células se adhieran durante la noche en DMEM / 10% Phab a 37 ° C en 5% de CO 2.
- Reemplazar DMEM / 10% Phab con medio de suero reducido estándar, alrededor de 200 l / cm 2, diseñado para la expansión de células mesenquimales del estroma (medio MSC-RS). Se cultivan las células hasta confluencia (P1-MSC), normalmente de 7 a 10 días después de la inducción. Refrescar el medio cada 2 días.
- Aspirar y descartar medio de los matraces, lavar con medio MSC-RS fresco y añadir 2 ml de solución de animales proteasa libre de desprendimiento. Incubar a 3776; C durante 5 - 15 min (evitar la incubación prolongada).
- Añadir 10 ml de medio de MSC-RS fresco, aspirar la suspensión de células y se centrifuga a 400 xg durante 5 min
- Aspirar el sobrenadante y resuspender pellet en 1 - 2 ml de medio MSC-RS fresco. Continúe con el recuento de células como se describe en el paso 1.10
- Proceder a la sub-cultura de ellos mediante la siembra de 3 - 5 de 10 x 3 células / cm2. Se cultivan las células a confluencia (P2-MSC).
- Las células de la cosecha por la digestión de la proteasa como se describe en el paso 4.3 al paso 4.5 y proceder a la caracterización como se describe en la sección 3.
NOTA: Un porcentaje de células CD31 neg neg CD73 + CD90 + CD45 menor que 95% indicaría solamente la diferenciación parcial y requieren de un paso de cultivo más. - Placa P2-MSC a 2 x 10 4 / cm2 en placas de seis pocillos tratados con TC y crecer hasta la confluencia en medio MSC-RS.
- Marque dos pozos como "No Dif" y refrescar medio MSC-RS.
- Marca de los dos, asís como "Osteo" y reemplazar medio con 200 l / cm 2 de medio osteogénico estándar, diseñado específicamente para la diferenciación de MSC.
- Marque dos pozos como "Adipo" y reemplazar medio con 200 l / cm2 de medio adipogénico estándar, diseñado específicamente para la diferenciación de MSC.
- Mantener los cultivos a 37 ° C en 5% de CO 2 al cambiar el conjunto de los medios de comunicación cada 48 horas.
NOTA: Se recomienda utilizar los medios diferenciadores estándar disponibles comercialmente para la reproducibilidad de los ensayos. Después de 2/3 semanas bajo condiciones de diferenciación, los depósitos de calcio aparecen en las culturas osteogénicas inducida, mientras que la acumulación de lípidos intracelulares gotitas es evidente en las células adipogénicas inducida. - Aspirar y descartar los medios de cultivo y luego se lavan con D-PBS.
- Fijar los cultivos mediante la adición de 1 ml de 4% (w / v) para-formaldehído durante 15 min a temperatura ambiente.
- Para retirar el fijador añadir D-PBS, se incuban durante 2 minutos y se vierte. Repetir el lavadodos veces.
- Manchar uno "Sin Dif", junto con los dos "Osteo" marcó pozos en solución fluorescente específica hidroxiapatita y uno "Sin Dif", junto con los dos "Adipo" marcó pozos en 200 nM solución de Rojo Nilo. Incubar durante 30 minutos a temperatura ambiente 11,12.
- Retire las soluciones de tinción y lavar en D-PBS dos veces.
- Eliminar D-PBS, añadir D-PBS suplementado con 50% (v / v) de glicerina y proceder a la imagen 7 9 10.
5. MPC esferoide del brote Ensayo
- Para producir esferoides 3D, coloque 20 gotas l de suspensión recién aisladas MPC (1,5 x 10 4 células / gota) en la superficie interna de una tapa de placa de Petri.
NOTA: Como gotas de manipulación podría conducir a su ruptura, es altamente recomendable para ponerlas en exceso. - Con cuidado, usar la tapa para recapitular una placa de Petri que contiene D-PBS para evitar la evaporación cae colgante. Incubar a 37 ° C en 5% de CO 2durante la noche para permitir que las células se agregan en esferoides 3D.
- Establecer un gel espeso de las proteínas murinas matriz extracelular (ECM) mediante la adición de 300 ml de alícuotas de proteínas ECM estándar en una placa de cultivo de pre-refrigerada de 24 pocillos, y se incuba a 37 ° C durante 30 minutos.
- incline con cuidado sobre la tapa placa de Petri y suavemente recoger los esferoides utilizando una pipeta Pasteur estéril.
- Coloque esferoides en el gel de proteínas ECM, añadir 700 ml de alícuotas de medio de crecimiento de células endoteliales VEGF-rica estándar e incubar a 37 ° C en 5% de CO 2.
- Después de 24 horas ya los 7 días de cultivo, tomar fotografías de las culturas 3D en una potencia de magnificación 4X. Evaluar la brotación de esferoides que aplican el software de análisis de imágenes mediante la medición de la distancia radial entre la última célula invasora y el borde esferoide. Repetir las medidas a lo largo de al menos 20 direcciones diferentes. La media distancia se considera como positiva cuando 50 micras o más.
Resultados
Las condiciones de cultivo selectivos descritos aquí han permitido el aislamiento de una población de células adherentes y casi monomórfica novela como 1,0% de la HBM-MNCs (0,5 a 2,0 x 10 6 HBM-MNCs a partir de 5 - 10 ml de las muestras de BM frescas) 5,6 . Se identificaron estos grandes (40 - 60 micras de diámetro), redondeado, células en reposo, Ki-67-negativos como PSM 5. Morfológicamente, se caracterizan por una forma de huevo frito distintivo con una región de núcleo de espesor, rodeado de una periferia plana delgada que muestra porciones de filopodios en mayor energía de la ampliación (flechas blancas en la Figura 1 A.1). Polar elongación del límite exterior de la célula se observa con frecuencia (flechas negras en la Figura 1 A.1). Tal morfología es claramente diferente de la apariencia típica en forma de huso-mesenquimal de células estromales reportado en cultivos de MSC estándar. La citometría de flujo mostró que más del 95% de los PSM recién aisladas para expresar CD31 y CD45, mientras que mesenchymal marcadores asociados CD90 y CD73 13 fueron indetectables (Figura 1 A.2). Consideramos que este conjunto restringido de cuatro antígenos como indicativo para los PSM. Otras características distintivas de PSM son la distribución de puntos F-actina revelando un número de estructuras podosome-como (rojo en la Figura 1 A.3) e intensa expresión de nestina (verde en la Figura 1 A.3), que no se detecta en las células tiñeron con anticuerpo de control isotípico (datos no mostrados).
PSM cultivo en medio estándar RS diseñados para MSC resultados de expansión en rápida diferenciación en células en crecimiento exponencial MSC-como (Figura 1) B.1. Después de dos pasajes células finalmente cambian su fenotipo de CD73 CD90 neg neg CD45 + CD31 + CD73 + CD90 al CD45 + CD31 neg neg (Figura 1 B.2). En el proceso, PSM re-organize F-actina en las fibras de estrés mientras que la expresión de nestina queda confinada a unas pocas células raras (Figura 1) B.3. MPC diferenciación en un fenotipo mesengenic MSC-como definitivo se produce a través de dos pasos distintos revelados por diferentes morfologías celulares. Después de una semana en un medio MSC RS una población residual de células MPC-como todavía se puede detectar una capa confluente de células multi-ramificados poligonales plano (P1-MSC en la Figura 2 A). Se requiere un paso más para obtener un cultivo casi monomórfica de células en forma de huso-MSC-como (P2-MSC en la Figura 2 A). Estas células de crecimiento exponencial se pueden diferenciar fácilmente en osteoblastos o adipocitos cuando se transfiere en medio selectivo durante al menos 2 semanas, lo que confirma su naturaleza MSC. En las culturas osteogénicas inducida, depósitos de calcio se pueden detectar por cualquiera de las colorimétrico mancha alizarina-S o colorantes fluorescentes específicos (verde en la Figura 2 B). Después las células de inducción adipogénicosmostrar la acumulación de gotas de lípidos según lo revelado por cualquiera colorimétrico Rojo Aceite o fluorescente tinción con Rojo Nilo (rojo en la Figura 2 B).
MPC tipificación fue confirmada por brotación ensayo de angiogénesis. PSM mostraron su capacidad de invadir (más de 50 micras) en gel de proteínas ECM murino de esferoides 3D después de 24 horas de VEGF-estímulo (Figura 2 C). Después se detectaron células invasoras de una semana a 300 - 600 Distancia al micras. Por el contrario, la capacidad de invasión se perdió en P2-MSC después de la diferenciación mesengenic (Figura 2 D).
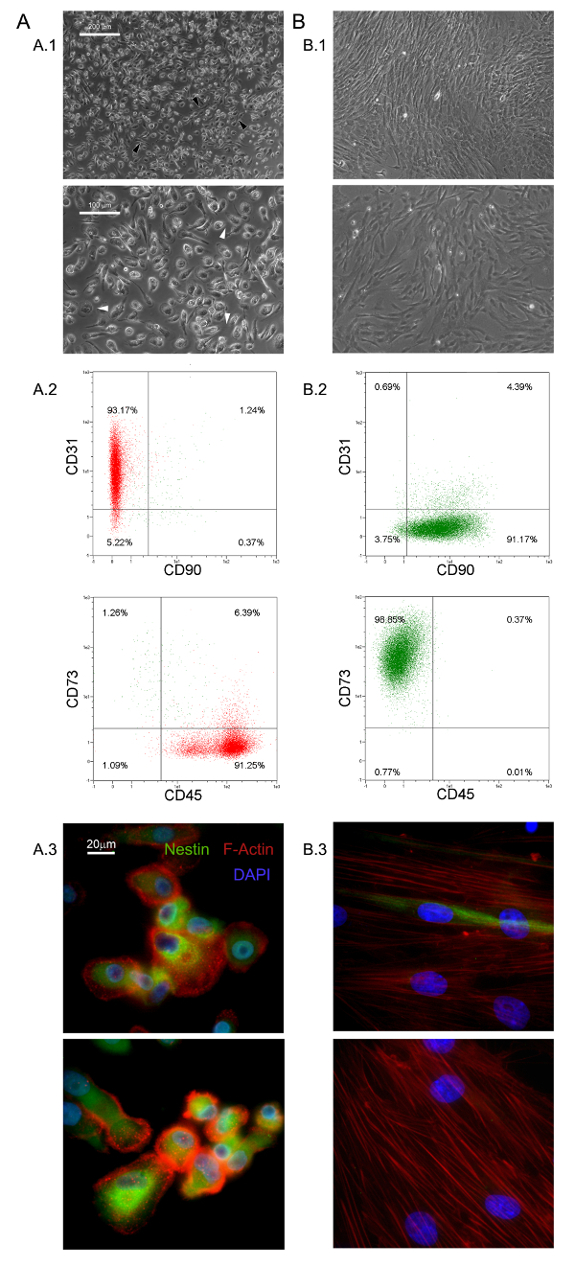
Figura 1. PSM recién aisladas tienen características distintivas. El cultivo HBM-MNC en DMEM / 10% Phab durante siete días da lugar a una población de PSM en reposo (A) fácilmente distinguibles de las MSC (B) en términos de morfología (A.1, B.1, barras de escala = 100 micras), el fenotipo (A.2, B.2), F-actina de distribución (rojo en A.3, B.3), y nestin expresión (verde en A.3, B.3, barras de escala = 20 micras). Haga clic aquí para ver una versión más grande de esta figura.
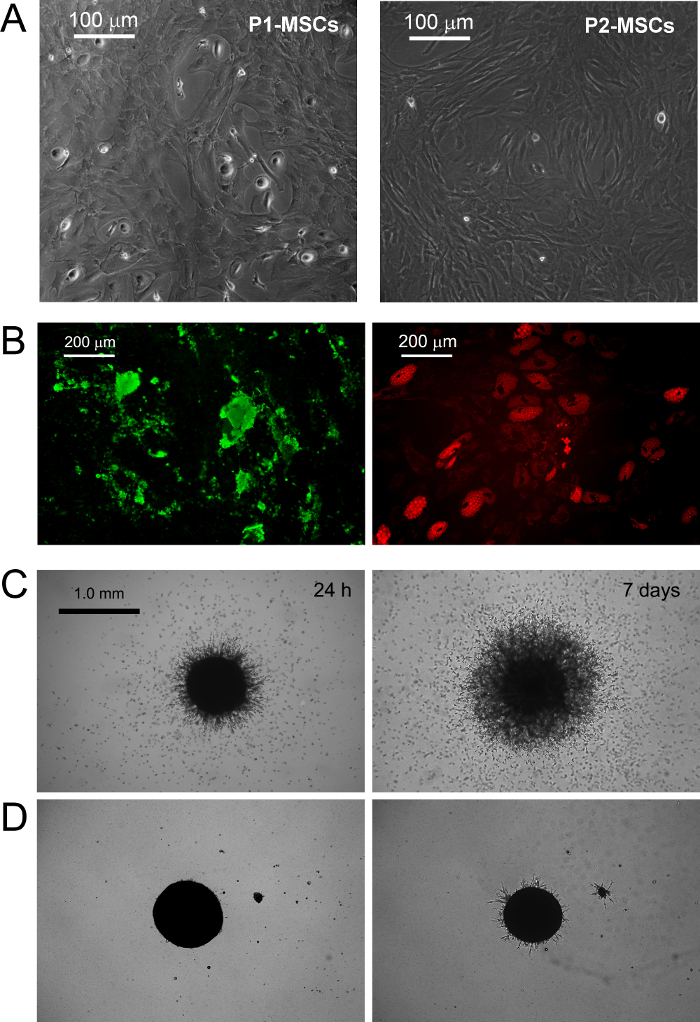
Figura 2. PSM diferenciarse en MSC estándar y Mostrar Brote angiogénesis in vitro. La sustitución de DMEM / Phab con RS disponibles en el mercado medio diseñado para la expansión de MSC desencadena la inducción mesengenic del PSM. Después de una semana en cultivo unos PSM residuales son todavía detectable (P1-MSC), mientras que un paso más en medio MSC-RS conduce a una población de células confluentes MSC-como (P2-MSC, a barras de escala = 100 m). PAG2-MSC diferenciar terminal en osteocitos o adipocitos bajo estímulos apropiados según lo revelado por la deposición de calcio (verde en B) y la acumulación de gotas de lípidos (rojo en B, barras de escala = 200 m), respectivamente. PSM muestran surgimiento constante de esferoides en gel de proteínas ECM murino (C) a una diferencia con P2-MSC (D, barras de escala = 1,0 mm). Por favor, haga clic aquí para ver una versión más grande de esta figura.
Discusión
In the last decades, MSCs have been extensively researched and pre-clinically evaluated for possible application in the treatment of various bone/articular, immunological, neurological, cardiovascular, gastrointestinal and hematological disorders14,15. The easy and inexpensive isolation of multipotent MSCs, from many different tissues, together with their lack of significant immunogenicity16, contribute to make these cells one of the most interesting cell population to be applied in cell based therapies. Nonetheless, the very low frequency in the tissue of origin represents a great limitation to the MSCs application in clinics, forcing the expansion of these cells, in vitro, before the infusion or transplantation.
Expanded MSC cultures have revealed high grades of heterogeneity and variability17-19 making it difficult to reach a consensus about MSC production and characterization protocols. Moreover, recent investigations suggested the presence of multiple in vivo MSC ancestors in a wide range of tissues, which contribute to culture heterogeneity10,20. In fact, it has been proposed that particular culture conditions possibly select or simply promote specific sub-populations of MSCs progenitors present, in various percentages, in "crude" and unprocessed samples like bone marrow (hBM-MNCs) or adipose tissues (stromal vascular fraction)2. Thus, the variability in MSC-initiating cell populations together with the great number of different enrichment/isolation and culture protocols applied, represent a great obstacle to the definition of feasible MSC-based therapies.
A crucial factor affecting heterogeneity of MSC cultures is serum supplementation21. In our hands replacement of FBS with PhABS in primary cultures from hBM-MNCs, combined with high density seeding on hydrophobic plastics, led to the isolation of a novel highly adherent cell population with distinct biological features named MPCs5,6. We observed that the addition of small percentages of PhABS to FBS primary cultures also allowed MPC isolation, suggesting the presence of MPC inducing agents in the human serum6. At the moment, the MPC isolation/characterization protocol is a unique method available to obtain almost pure MPCs. The protocol has been carefully adjusted and it is highly reproducible for quality screening of MPC preparations before further applications.
MPCs could be used as a source for MSC production, thus limiting the variability introduced by use of unfractionated starting material. The precise definition of the multiple steps characterizing MPC mesengenic differentiation reported9 would allow synchronized mesenchymal cell expansion. Nonetheless, this latest condition could be realized exclusively applying highly purified MPC population, as a consequence the characterization of the cell products obtained by the protocol described here, results of crucial importance. This isolating method has been reported allowing MPC recovery with purity generally around 95%. However, donor/patient variability together with the variability related to the different batches of human pooled serum applied, could lead to a significant percentage of MSC-like cells co-isolated together with MPCs, under selective conditions.
It is not clear if these "contaminating" MSC-like cells could arise from the other different in vivo progenitors described in bone marrow22 or from uncontrolled and spontaneous MPC differentiation. In any case, a consistent percentage of MSC-like cells in the MPC products nullify the possibility to applying these cells as homogeneous starting material for the MSC expansion. Thus, here it has been suggested a simple and inexpensive method, based on the MPC resistance to trypsin digestion, increasing the purity of the MPC products. Similar or even better results in purifying MPC cultures could be achieved by fluorescent or magnetic cell sorting performing CD73 and/or CD90 depletion, but significantly prolonging the process time and increasing the costs.
Moreover, MPCs showed expression of pluripotency-associated markers and Nestin, all rapidly lost during mesengenic differentiation7. Sprouting assay revealed MPC ability to invade murine ECM protein gel. Taken together these results indicate that MPCs have to be considered a more immature progenitor, retaining angiogenic potential. Nonetheless, the initial enthusiasm about mesodermal differentiation potential of MPCs is actually waning. In fact, after more than 7 years of studies on MPCs, mesengenic and angiogenic potential have been extensively described5-9, but differentiation toward any other cells of mesodermal origin is still lacking. Thus, here we propose a new, and more rigorous, definition of these cells as "Mesangiogenic Progenitor Cells", maintaining the acronym MPCs.
We also believe that most controversies about MSC angiogenic potential could be related to the heterogeneous composition of expanded cultures consisting of sub-populations of MPCs and MSCs in variable percentages23.
Finally, MPCs could also play a crucial role for the implementation of CBMPs applicable for tissue reconstruction, as these cells could also support the neo-vascularization. In fact, future studies on regeneration should take in consideration that the newly formed tissue growth should be supported by concomitant neo-angiogenesis. The co-existence of mesengenic and angiogenic potential in MPCs could significantly improve the regeneration potential of new therapeutic approaches that involve these interesting cells.
Divulgaciones
The authors have no competing financial interests or other conflicts of interest.
Agradecimientos
Los autores desean agradecer especialmente a Dr. Paolo Parchi, Departamento de Cirugía, Medicina y Patología Molecular y la Medicina de la Universidad de Pisa, para proporcionar muestras de médula ósea y su experiencia en la osteo-progenitores humanos
Materiales
| Name | Company | Catalog Number | Comments |
| Matrigel Basement Membrane Matrix | BD Bioscience (San Jose, CA-USA) | 354230 | Murine ECM proteins Stock Concentration: 100% (9 - 12 mg/ml) Final Concentration: 100% |
| Dulbecco's Phosphate-Buffered Saline (D-PBS) | Sigma (St. Louis, MO, USA) | D8537 | |
| 70 μm Filters | Miltenyi Biotec (BergischGladbach, Germany) | 130-095-823 | |
| Ficoll-Paque PREMIUM | GE Healthcare (Uppsala, Sweden) | 17-5442-03 | medium for discontinuos density gradient centrifugation |
| Pooled human AB type serum (PhABS) | LONZA (Walkersville MD-USA) | 14-490E | Final Concentration: 10% |
| Glutamax-I | ThermoFisher (Waltham, MA USA) | 35050-038 | Stabilized L-Glutamine Stock Concentration: 100x Final Concentration: 2 mM |
| Bovine Serum Albumin (BSA) | Sigma (St. Louis, MO, USA) | A8412 | Stock Concentration: 7.5% Final Concentration: 0.5% |
| Sodium Azide | Sigma (St. Louis, MO, USA) | S8032 | Final Concentration: 0.02% |
| Penicillin/Streptomycin (Pen Strep) | Gibco (Grand Island, NY, USA) | 15070-063 | Antibiotics Stock Concentration: 5,000 UI/ml penicillin, 5,000 μg/ml Streptomycin Final Concentration: 50 UI/ml penicillin, 50 μg/ml Streptomycin |
| T-75 culture flask for suspension cultures | Greiner Bio-one (Frickenhausen, Germany) | 658 190 | |
| T-75 culture flask TC treated | Greiner Bio-one (Frickenhausen, Germany) | 658170 | |
| TrypLE Select | ThermoFisher (Waltham, MA USA) | 12563-011 | Animal-free proteases detaching solution Stock Concentration: 1x Final Concentration: 1x |
| Trypsin/EDTA | ThermoFisher (Waltham, MA USA) | 15400-054 | Phenol red free Stock Concentration: 0.5% Final Concentration: 0.25% |
| anti-CD90 APC antibody (CD90) | MiltenyiBiotec (BergischGladbach, Germany) | 130-095-402 | Final Concentration: 1:40 |
| anti-CD45 APC-Vio770 antibody (CD45) | MiltenyiBiotec (BergischGladbach, Germany) | 130-096-609 | Final Concentration: 1:40 |
| anti-CD73 PE antibody (CD73) | MiltenyiBiotec (BergischGladbach, Germany) | 130-095-182 | Final Concentration: 1:40 |
| anti-CD31 PE Vio-770 antibody (CD31) | MiltenyiBiotec (BergischGladbach, Germany) | 130-105-260 | Final Concentration: 1:40 |
| Mouse IgG1 APC antibody | MiltenyiBiotec (BergischGladbach, Germany) | 130-098-846 | Final Concentration: 1:40 |
| Mouse IgG2a APC Vio770 antibody | MiltenyiBiotec (BergischGladbach, Germany) | 130-096-637 | Final Concentration: 1:40 |
| Mouse IgG1 PE antibody | MiltenyiBiotec (BergischGladbach, Germany) | 130-098-845 | Final Concentration: 1:40 |
| Mouse IgG1 PE Vio-770 antibody | MiltenyiBiotec (BergischGladbach, Germany) | 130-098-563 | Final Concentration: 1:40 |
| Low Glucose Dulbecco's Modified Eagle Medium (DMEM) | ThermoFisher (Waltham, MA USA) | 13-1331-82 | Phenol red-free minimal essential medium Stock Concentration: 1,000 mg/L glucose |
| Fetal Bovine Serum (FBS) | ThermoFisher (Waltham, MA USA) | 10500 | Stock Concentration:0.2 mg/ml Final Concentration: 2 μg/ml |
| Prolong Gold antifade reagent with 4’,6-diamidino-2-phenylindole | Invitrogen (Waltham, MA, USA) | P-36931 | Aqueous mounting medium + DAPI Final Concentration: 1x |
| Paraformaldehyde | Sigma (St. Louis, MO, USA) | P6148 | Fixative Final Concentration: 4% |
| LAB-TEK two-well chamber slides | Sigma (St. Louis, MO, USA) | C6682 | |
| Anti-Nestin antibody [clone 10C2] | Abcam (Cambridge, UK) | ab2035 | Stock Concentration: 1 mg/ml Final Concentration: 7 μg/ml |
| Alexa Fluor 555 Phalloidin | ThermoFisher (Waltham, MA USA) | A34055 | Stock Concentration: 200 UI/ml Final Concentration: 5 UI/ml |
| Triton X-100 | Euroclone (Milan, Italy) | EMR237500 | Final Concentration: 0.05% |
| MesenPRO RS Medium (MSC-RS medium) | ThermoFisher (Waltham, MA USA) | 12746-012 | |
| Alexa Fluor 488 anti-mouse SFX kit | ThermoFisher (Waltham, MA USA) | A31619 | Goat anti-mouse secondary antibody + Signal enhancer Stock Concentration: 2 mg/ml Final Concentration: 2 μg/ml |
| Pasteur Pipette | Kartell Labware (Noviglio (MI), ITALY ) | 329 | |
| StemMACS AdipoDiff Media | MiltenyiBiotec (BergischGladbach, Germany) | 130-091-679 | |
| StemMACS OsteoDiff Media | MiltenyiBiotec (BergischGladbach, Germany) | 130-091-678 | |
| Osteoimage Bone mineralization Assay | LONZA (Walkersville MD-USA) | PA-1503 | Hydroxyapatite specific fluorescent staining solution |
| 50 ml Polystyrene conical tube | Greiner bio-one (Kremsmünster Austria) | 227261 | |
| Nile Red | ThermoFisher (Waltham, MA USA) | N1142 | Fluorescent staining solution for lipids Stock Concentration: 100 mM Final Concentration: 200 Nm |
| Glycerin | Sigma (St. Louis, MO, USA) | G2289 | Final Concentration: 50% |
| Polistirene Petri dishes | Sigma (St. Louis, MO, USA) | P5606 | |
| 24-well plates TC-treated | Greiner Bio-one GmbH (Frickenhausen, Germany) | 662160 | |
| Endothelial Growth Medium, EGM-2 BulletKit (EGM-2) | LONZA (Walkersville MD-USA) | CC-3162 | VEGF-rich endothelial cell growth medium |
| Leica Qwin Image Analisys Software | Leica (Wetzlar, Germany) | Image analysis software |
Referencias
- Stoltz, J. F., et al. Stem Cells and Regenerative Medicine: Myth or Reality of the 21th Century. Stem Cells Int. 2015, 734731 (2015).
- Pacini, S. Deterministic and stochastic approaches in the clinical application of mesenchymal stromal cells (MSCs). Front Cell Dev Biol. 2, 50 (2014).
- Galvez, P., Clares, B., Hmadcha, A., Ruiz, A., Soria, B. Development of a cell-based medicinal product: regulatory structures in the European Union. Br Med Bull. 105, 85-105 (2013).
- Herberts, C. A., Kwa, M. S., Hermsen, H. P. Risk factors in the development of stem cell therapy. J Transl Med. 9, 29 (2011).
- Petrini, M., et al. Identification and purification of mesodermal progenitor cells from human adult bone marrow. Stem Cells Dev. 18 (6), 857-866 (2009).
- Trombi, L., et al. Selective culture of mesodermal progenitor cells. Stem Cells Dev. 18 (8), 1227-1234 (2009).
- Pacini, S., et al. Constitutive expression of pluripotency-associated genes in mesodermal progenitor cells (MPCs). PLoS One. 5 (3), 9861 (2010).
- Pacini, S., et al. Specific integrin expression is associated with podosome-like structures on mesodermal progenitor cells. Stem Cells Dev. 22 (12), 1830-1838 (2013).
- Fazzi, R., et al. Mesodermal progenitor cells (MPCs) differentiate into mesenchymal stromal cells (MSCs) by activation of Wnt5/calmodulin signalling pathway. PLoS One. 6 (9), 25600 (2011).
- Tormin, A., et al. CD146 expression on primary nonhematopoietic bone marrow stem cells is correlated with in situ localization. Blood. 117 (19), 5067-5077 (2011).
- Greenspan, P., Mayer, E. P., Fowler, S. D. Nile red: a selective fluorescent stain for intracellular lipid droplets. J Cell Biol. 100 (3), 965-973 (1985).
- Wang, Y. H., Liu, Y., Maye, P., Rowe, D. W. Examination of mineralized nodule formation in living osteoblastic cultures using fluorescent dyes. Biotechnol Prog. 22 (6), 1697-1701 (2006).
- Horwitz, E. M., et al. Clarification of the nomenclature for MSC: The International Society for Cellular Therapy position statement. Cytotherapy. 7 (5), 393-395 (2005).
- Wang, S., Qu, X., Zhao, R. C. Clinical applications of mesenchymal stem cells. J Hematol Oncol. 5, 19 (2012).
- Si, Y. L., Zhao, Y. L., Hao, H. J., Fu, X. B., Han, W. D. MSCs: Biological characteristics, clinical applications and their outstanding concerns. Ageing Res Rev. 10 (1), 93-103 (2011).
- Le Blanc, K., Tammik, C., Rosendahl, K., Zetterberg, E., Ringden, O. HLA expression and immunologic properties of differentiated and undifferentiated mesenchymal stem cells. Exp Hematol. 31 (10), 890-896 (2003).
- Phinney, D. G. Biochemical heterogeneity of mesenchymal stem cell populations: clues to their therapeutic efficacy. Cell Cycle. 6 (23), 2884-2889 (2007).
- Phinney, D. G. Functional heterogeneity of mesenchymal stem cells: implications for cell therapy. J Cell Biochem. 113 (9), 2806-2812 (2012).
- Tolar, J., Le Blanc, K., Keating, A., Blazar, B. R. Concise review: hitting the right spot with mesenchymal stromal cells. Stem Cells. 28 (8), 1446-1455 (2010).
- Corselli, M., et al. The tunica adventitia of human arteries and veins as a source of mesenchymal stem cells. Stem Cells Dev. 21 (8), 1299-1308 (2012).
- Bieback, K., et al. Human alternatives to fetal bovine serum for the expansion of mesenchymal stromal cells from bone marrow. Stem Cells. 27 (9), 2331-2341 (2009).
- Watson, L., Elliman, S. J., Coleman, C. M. From isolation to implantation: a concise review of mesenchymal stem cell therapy in bone fracture repair. Stem Cell Res Ther. 5 (2), 51 (2014).
- Pacini, S., Petrini, I. Are MSCs angiogenic cells? New insights on human nestin-positive bone marrow-derived multipotent cells. Front Cell Dev Biol. 2, 20 (2014).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados