Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Reduciendo la emisión de combustible de madera de sauce por microondas de baja temperatura asistida por carbonización hidrotérmica
En este artículo
Resumen
Se presenta un protocolo para el agotamiento de precursores de emisiones de biomasa de baja calidad mediante un tratamiento de carbonización hidrotermal asistido por microondas de baja temperatura. Este protocolo incluye los parámetros de microondas y el análisis del producto Biocoal y el agua de proceso.
Resumen
La biomasa es un combustible sostenible, ya que sus emisiones de CO2 se reintegran en el crecimiento de la biomasa. Sin embargo, los precursores inorgánicos en la biomasa causan un impacto ambiental negativo y la formación de escoria. La madera de sauce del coppice de rotación corta (SRC) seleccionada tiene un alto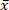 contenido de ceniza (= 1,96%) y, por lo tanto, un alto contenido de emisiones y precursores de escoria. Por lo tanto, se investiga la reducción de minerales de madera de sauce SRC por microondas de baja temperatura asistida por carbonización hidrotérmica (MAHC) a 150 ° c, 170 ° c y 185 ° c. Una ventaja de MAHC sobre los reactores convencionales es una conductancia de temperatura incluso en el medio de reacción, ya que las microondas penetran todo el volumen del reactor. Esto permite un mejor control de la temperatura y un enfriamiento más rápido. Por lo tanto, se puede analizar eficazmente una sucesión de reacciones de despolimerización, transformación y repolimerización. En este estudio, el análisis de la pérdida de masa, el contenido de ceniza y la composición, los valores de calentamiento y las proporciones de O/C molar y H/C de la madera de sauce de SCR tratada y no tratada mostraron que el contenido mineral del carbón MAHC se redujo y aumentó el valor de calentamiento. El agua del proceso mostró un pH decreciente y contenía furfural y 5-Metilfurfural. Una temperatura de proceso de 170 ° c mostró la mejor combinación de entrada de energía y reducción de componentes de ceniza. El MAHC permite una mejor comprensión del proceso de carbonización hidrotérmica, mientras que una aplicación industrial a gran escala es improbable debido a los altos costos de inversión.
contenido de ceniza (= 1,96%) y, por lo tanto, un alto contenido de emisiones y precursores de escoria. Por lo tanto, se investiga la reducción de minerales de madera de sauce SRC por microondas de baja temperatura asistida por carbonización hidrotérmica (MAHC) a 150 ° c, 170 ° c y 185 ° c. Una ventaja de MAHC sobre los reactores convencionales es una conductancia de temperatura incluso en el medio de reacción, ya que las microondas penetran todo el volumen del reactor. Esto permite un mejor control de la temperatura y un enfriamiento más rápido. Por lo tanto, se puede analizar eficazmente una sucesión de reacciones de despolimerización, transformación y repolimerización. En este estudio, el análisis de la pérdida de masa, el contenido de ceniza y la composición, los valores de calentamiento y las proporciones de O/C molar y H/C de la madera de sauce de SCR tratada y no tratada mostraron que el contenido mineral del carbón MAHC se redujo y aumentó el valor de calentamiento. El agua del proceso mostró un pH decreciente y contenía furfural y 5-Metilfurfural. Una temperatura de proceso de 170 ° c mostró la mejor combinación de entrada de energía y reducción de componentes de ceniza. El MAHC permite una mejor comprensión del proceso de carbonización hidrotérmica, mientras que una aplicación industrial a gran escala es improbable debido a los altos costos de inversión.
Introducción
La aplicación de microondas para la carbonización hidrotérmica (MAHC) se utilizó para la transformación termoquímica de compuestos modelo de biomasa como fructosa, glucosa1,2 o celulosa3, y para sustratos orgánicos, preferiblemente residuos de material4,5,6,7,8,9,10. La utilización de microondas es ventajosa ya que permite un calentamiento incluso de la biomasa tratada2,10 principalmente a través de las pérdidas térmicas de un disolvente dieléctrico11,12, aunque las microondas hacen no transfiera suficiente energía para romper directamente los enlaces químicos e inducir reacciones13. Las microondas penetran todo el volumen de reacción del recipiente del reactor HTC y transfieren la energía directamente al material, lo que no es posible con un reactor convencional que muestra una tasa de calentamiento más lenta debido a la alta capacidad de calentamiento del manto de acero y el muestra en sí14. La excitación incluso de las moléculas de agua de la muestra por microondas permite un mejor control del proceso, ya que la temperatura en el reactor de microondas se distribuye uniformemente11,14,15 y el tiempo de reutilización después de la reacción es mucho más rápida. Además, los reactores convencionales se calientan mucho más despacio y las reacciones químicas que ocurren durante la calefacción pueden sesgar los resultados que normalmente se asignan a la temperatura final. El control mejorado del proceso en un reactor MAHC permite una elaboración precisa de la dependencia de temperatura de las reacciones de HTC seleccionadas (p. ej., deshidratación o descarboxilación). Otra ventaja de la distribución uniforme de la temperatura en el volumen del HTC-reactor es la menor adherencia de las partículas inmovilizadas y completamente carbonizadas en la pared del reactor interno2. Sin embargo, el agua es sólo un disolvente de absorción de microondas promedio que incluso muestra la disminución de la absorbancia de microondas a temperaturas más altas, lo que limita la temperatura máxima alcanzable. Este efecto negativo se compensa cuando se producen ácidos durante el proceso de HTC o se añaden catalizadores (especies iónicas o polares) antes del tratamiento. Las reacciones inducidas por microondas muestran un mayor rendimiento del producto en general11,15 y específicamente de 5-hidroximetilfurfural (5-HMF) de fructosa en comparación con las reacciones catalizada de lecho de arena12. También tienen un balance energético mucho mejor que los métodos de calentamiento convencionales15,16.
El concepto químico fundamental de la carbonización hidrotérmica es la degradación y la polimerización sucesiva de la biomasa. En el transcurso de estas complejas reacciones de interacción el tejido se agota de oxígeno, lo que aumenta el valor de calentamiento. Al principio, los polímeros hemicelulosa y celulosa se hidrolizan a los monómeros de azúcar17, aunque las bajas temperaturas afectan principalmente a la hemicellulosa18,19,20,21. En esta etapa temprana de las reacciones de HTC, los ácidos orgánicos se forman a partir de la transformación de los aldehídos de azúcar y la deacetilación de hemicellulosa. Estos ácidos pueden ser acético, láctico, levulínico, acrílico o ácido fórmico20,21,22 y disminuyen el pH del agua de reacción en el reactor. Debido a la disociación, forman iones negativos libres que aumentan el producto de iones en el agua de proceso. El creciente producto de iones permite la resolución de cationes, que son los principales constituyentes de la ceniza en la biomasa. Por este mecanismo, el tejido se agota de precursores de emisiones y formadores de escoria (por ejemplo, potasio, sodio, calcio, cloro y metales pesados)23,24.
Los ácidos orgánicos formados pueden apoyar la deshidratación de los monómeros de azúcar a los furanos. Un producto común de deshidratación de azúcar es furfural y 5-hidroximetilfurfural, que son productos factibles para la industria química, ya que sirven como productos de plataforma (por ejemplo, para la síntesis de biopolímeros). 5-Metilfurfural puede ser formado por reacciones catalizada de celulosa25,26 o 5-hidroximetilfurfural27. Mientras que la síntesis de biopolímero es una repolimerización artificial bajo condiciones controladas, los furanos también pueden condensar, polimerizar y formar estructuras aromáticas de alto peso molecular en el complejo entorno químico del reactor MAHC. La interacción de los compuestos orgánicos e inorgánicos solubilizados con la matriz de células de madera modificada se suman a la complejidad del sistema de reacción20. Las vías de reacción de polimerización furana emplean condensación de aldólica o deshidratación intermoleculares18,20 y producen partículas de hydrochar con una cáscara hidrófoba y un núcleo más hidrófilo28. Aún no se ha revelado si las partículas de biomasa están completamente descompuestas y luego repolimerizadas o si las partículas de biomasa sirven como una plantilla para la carbonización. Sin embargo, las reacciones de degradación y repolimerización comprenden la deshidratación y las reacciones de descarboxilación, así como29,30, lo que induce la caída en el diagrama de van Krevelen hacia las proporciones de O/c y H/c del carbono negro.
Mientras que otros estudios demostraron el efecto reductor de minerales del tratamiento hidrotermal a base de reactor convencional31, de un lavado de agua con lixiviación mecánica combinada32 o agua/acetato de amonio/lavado de ácido clorhídrico33, nuestro estudios investigan la lixiviación mineral durante la carbonización a baja temperatura con microondas por primera vez. Como este estudio se enfoca en la lixiviación de precursores de emisiones para la mejora de combustible, investiga el destino de potasio, sodio, magnesio, calcio, cloro, azufre, nitrógeno y metales pesados. Los precursores de polvo fino forman sales volátiles (p. ej., KCl o K2so4) a temperaturas elevadas en la fase gaseosa. Cuando estas sales se acumulan en los gases de combustión, metales pesados como el zinc pueden compactarlos como partículas de nucleación, lo que conduce a una reacción en cadena de crecimiento de partículas. A bajas temperaturas de los gases de combustión, la condensación de sal desencadena aún más el crecimiento de las partículas y produce una emisión cancerógena de polvo fino de la chimenea. Estas emisiones son, en la actualidad, el principal factor que compromete la sostenibilidad de los combustibles de biomasa. Un suministro energético sostenible se basa en su reducción por filtros costosos o su reducción de los combustibles (por ejemplo, por MAHC). Como este estudio sigue un enfoque práctico, la madera de sauce de coppice de rotación corta (SRC) fue elegida como una materia prima de bioenergía potencial con altas tasas de crecimiento. Puede ser cultivada por los agricultores en sus campos para una fuente de alimentación autosustentable por gasificación, pero también para la generación de calor por combustión directa. Una desventaja de la SRC de sauce es su alto contenido de corteza debido a un tallo bajo: relación de corteza en etapa madura. La corteza contiene una gran cantidad de minerales en comparación con la madera34,35,36,37 y produce mayores cantidades de gases o emisiones de partículas38. El HTC de baja temperatura puede mejorar las propiedades de combustión de la madera de sauce de SRC y, de este modo, contribuir a un calor y una fuente de alimentación sostenibles. Otro parámetro importante del Biocoal de HTC investigado en este estudio es su densidad de energía, su temperatura de combustión inicial más alta y su temperatura de combustión final más alta39.
Protocolo
1. preparación del material de muestra
- Cosecha de sauce de cinco años, tipo clon "Tordes" ([Salix schwerinii x s. viminalis] x s. vim.), con una altura de 12 − 14 m y un diámetro de pecho de aproximadamente 15 cm.
- Astillar la madera y secar las virutas en un secador de horno durante 24 h a 105 ° c.
- Cortar los chips de madera con un molino de corte y moler con un molino centrífugo a un tamaño de partícula de 0,12 mm.
2. la carbonización hidrotérmica asistida por microondas
- Utilice un horno de microondas con 850 W y una frecuencia de magnetrón de 2.455 MHz.
- Colocar 500 mg de materia prima del paso 1,3 en un recipiente de reacción de politetrafluoroetileno (PTFE) de 50 mL con una espátula. Añadir 10 mL de agua desmineralizada. Atornille la tapa del recipiente de reacción para que la válvula de presión en la tapa esté en el mismo nivel que el borde del tapón.
- Para cada temperatura de tratamiento, coloque doce recipientes de reacción con materias primas en el horno de microondas y cierre el horno.
- Configurar tres programas de temperatura, con el microondas para las tres temperaturas: 150 ° c (rampa + 12,5 ° c min-1, mantener 60 min, potencia pico 50%), 170 ° c (rampa + 9,6 ° c min-1, Hold 60 min, potencia pico 80%), y 185 ° c (rampa + 5,3 ° c min-1 , sostenga 30 min, rampa-1,1 ° c min-1 a 150 ° c, potencia pico 100%). Inicie el horno de microondas, para cada programa individual.
- Una vez finalizado el programa, retire los recipientes de reacción, permita que se enfríen y reactiven. A continuación, ábralos bajo un armario de humos después de soltar la presión en el interior.
- Añadir 35 mL de agua destilada dos veces a cada recipiente de reacción. Vierta la solución en cada recipiente en un cilindro centrífugo y centrifugue a 1.714 x g durante 10 min.
- El agua de proceso se drena en otro tubo y se almacena congelado a-5 ° c para el análisis de pH y cromatografía de gases y espectrometría de masas (GC-MS).
- Congelar el cilindro centrífugo con el resto de pellets de biocarbón a-5 ° c. A continuación, sacar el pellet de biocarbón y secarlo a 105 ° c durante 24 h. pesar el pellet de biocarbón y calcular la pérdida de peso inducida por el tratamiento con MAHC.
- Repita los pasos 2.2 − 2.8 cuatro veces por temperatura (48 recipientes de reacción por temperatura) para producir suficiente biocarbón (aproximadamente 22 g) para el análisis posterior.
3. determinación del contenido de ceniza
- Pesar 20 platos de cerámica vacíos individualmente. Añadir en cada 1 g de muestra (5 x 1 g de materia prima, y 5 x 1 g de biocarbón de cada tratamiento de temperatura).
Nota: debido a que los platos no pueden etiquetarse, se debe trazar un plan para la disposición de los recipientes en el horno. - Coloque los platos de cerámica abiertos en un horno de mufla y cierre el horno.
- Programar un programa de temperatura para el horno de mufla (+ 6 ° c min-1 de 25 ° c a 250 ° c, sostener 60 min, + 10 ° c min-1 a 550 ° c, sostener 120 min) e iniciar el programa.
- Una vez finalizado el programa, deje enfriar el horno de mufla hasta 105 ° c. A continuación, abra el horno y sacar los platos de cerámica.
- Colocar los platos de cerámica en un extractor (tabla de materiales) lleno de un agente de secado que consiste en gel de sílice. Cierre el desecador y seque al vacío con la ayuda de una bomba de vacío.
- Sacar los platos de cerámica después de 24 h de enfriamiento. Pesar el plato de cerámica que contiene la ceniza y calcular el peso de la ceniza restando el peso de la placa de cerámica vacía.
- Determine el contenido de ceniza en porcentaje dividiendo el peso de ceniza por la masa seca de la materia prima o el biocarbón.
4. determinación de los valores de calentamiento superiores e inferiores
- Activar la bomba de agua del calorímetro y abrir la válvula de oxígeno para suministrar 99,5% de oxígeno al calorímetro.
- Pesar 1 g de glucosa y colocarlo en una bolsa plástica de muestra con un valor calorífico definido de 46.479 J/g. Coloque la bolsa de muestra en el crisol de combustión de una bomba de calorímetro.
- Añadir 5 mL de agua doblemente desionizada en la parte inferior de la bomba y atornillar la bomba. Pon la bomba en el calorímetro y cierra el calorímetro.
- Introduzca el peso de la muestra y cambie la configuración al método de la bolsa de muestra. Arranca el calorímetro.
- Una vez completada la medición, saca la bomba, dale la vuelta y agítalo lentamente durante 1 min.
- Desenrosque la bomba, extraiga 5 mL de agua desmineralizada dos veces y guárdela en un recipiente de tapón de tornillo para el análisis posterior de la cromatografía de iones.
- Repita los pasos 4.2 − 4.6 tres veces para obtener el estándar de calibración.
- Repita los pasos 4.2 − 4.6 cinco veces con cada Biocoal MAHC (150 ° c, 170 ° c, 185 ° c) y la materia prima.
- Calcule el valor de calentamiento inferior utilizando la siguiente ecuación40:
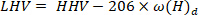
donde el LHV es el valor de calentamiento más bajo, el HHV es el valor de calentamiento más alto obtenido del calorímetro en el paso 4,4,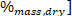 y ω es el contenido de hidrógeno [obtenido del análisis elemental.
y ω es el contenido de hidrógeno [obtenido del análisis elemental.
5. cromatografía de iones para la cuantificación de cloro
Nota: Compruebe la calibración del cromatógrafo de iones antes del análisis.
- Sacar los 5 mL de solución del paso 4,8 y añadir 45 mL de agua desmineralizada dos veces en una mascarilla volumétrica de 50 mL.
- Inserte el tubo de aspiración de muestra en un recipiente de muestra y dibuje aproximadamente 3 mL de la muestra con una jeringa en la precolumna. Inicie la ejecución del análisis.
- Realice las mediciones de acuerdo con las instrucciones del fabricante.
- Repita los pasos 5,2 y 5,3 para cada muestra preparada en la sección 4.
6. análisis elemental para la determinación de las relaciones O/C y H/C
- Seleccione un método apropiado en el manual del instrumento para medir las muestras.
- Haga todos los estándares de 20 mg de sulfonamida y los espacios en blanco requeridos para calibrar el dispositivo.
- Para preparar una muestra de material, poner 20 mg de muestra en papel de aluminio en el micro balance. Pese la muestra en la lámina de estaño, cierre la lámina alrededor de la muestra y presione el envase para contener el menor aire posible. Luego repite este 5x para cada muestra.
Nota: para poder analizar las muestras de biochar, se debe añadir la misma cantidad de trióxido de tungsteno que la cantidad de la muestra en una proporción de 1:1. Esto es necesario para compensar el oxígeno que falta en el biochar para asegurar la combustión completa en el Analizador elemental. - Inserte las muestras preparadas en el muestreador automático del Analizador elemental.
- Abra la válvula de oxígeno y helio para la cámara de combustión del Analizador elemental.
- Inicie el análisis cuando el dispositivo haya alcanzado la temperatura especificada por el dispositivo. En este caso, espere hasta que la temperatura llegue a 900 ° c.
- Calcular los lunares de cada elemento en el estándar de sulfonamida por el peso estándar de sulfonamida (paso 6,2), y el peso de 1 mol del elemento respectivo.
- Calcular la relación entre los lunares de C, H, S y N en sulfonamida, obtenida del paso 6,7, y las respectivas áreas pico.
- Reste el contenido de ceniza de muestra, obtenido del paso 3,7, del peso total de la muestra.
- Compare el área de pico del elemento respectivo en el estándar de sulfonamida y la muestra, y multiplique por el topo de cada elemento en sulfonamida para obtener el topo del elemento en la muestra.
- Calcule el peso de C, H, S y N en la muestra multiplicando el topo del elemento, obtenido del paso 6,10, con la masa molar respectiva del elemento de la tabla periódica.
- Calcule el peso del oxígeno en la muestra utilizando la masa de muestra libre de cenizas, obtenida del paso 6,9, y restando el peso de C, H, N y S, obtenido del paso 6,11.
- Calcule las relaciones molar H/C y O/C en la materia prima y las muestras de biocarbón MAHC.
7. Espectroscopía de emisión óptica de plasma acoplado inducida
- Pesar 400 mg de materia prima seca o biocarbón MAHC y ponerlo en un recipiente de reacción de PTFE de 50 mL con una espátula. Añadir 3 mL de ácido nítrico al 69% y 9 mL de ácido clorhídrico al 35%.
- Atornille la tapa del recipiente de reacción para que la válvula de presión en la tapa esté en el mismo nivel que el borde del tapón.
- Coloque los recipientes de reacción de las muestras que se analizarán en el horno de microondas y cierre el horno.
- Programar el programa de temperatura para la degradación completa del material orgánico: rampa + 15,5 ° c min-1 a 200 ° c, sostener 30 min, enfriar hasta 180 ° c, sostener durante 5 min. Inicie el horno microondas.
- Una vez finalizado el programa, retire los recipientes de reacción, permita que se enfríen y reactiven. A continuación, abra los recipientes debajo de un armario de humos después de soltar la presión en el interior.
- Vierta las muestras en un cilindro de bombilla de 50 mL. A continuación, enjuague el recipiente de reacción minuciosamente con agua doblemente desionizada y transfiérala al cilindro del bulbo. Rellenable el cilindro a la marca de 50 mL con agua doblemente desionizada para asegurar la dilución de todas las muestras.
- Filtre la muestra del paso 7,6 con papel de filtro de malla de 150 μm. Llene el filtrado en tubos de centrífuga cónica de 50 mL.
- Ponga las muestras estándar en el autoinyector del ICP-OES. Las muestras estándar son de las concentraciones conocidas (0,0001 ppm, 0,001 ppm, 0,1 ppm, 1 ppm 10 ppm, 20 ppm, 50 ppm) de los elementos a cuantificar (CA, as, B, be, fe, se, Zn, AG, al, BA, BI, CD, Co, CR, Cu, GA, K, Li , Mg, MN, MO, na, ni, PB, RB, Sr, te, TL, V).
- Poner las muestras en el autoinyector del ICP-OES y ejecutar el análisis ICP-OES con los mismos parámetros.
- Después del análisis ICP-OES, obtener la concentración elemental del software, calculado automáticamente en mg/kg, basado en las curvas de calibración obtenidas de muestras estándar en el paso 7,8.
- Calcular la reducción de la concentración elemental en el biocarbón producido:
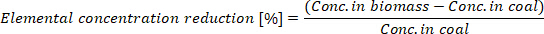
donde la Conc. en la biomasa es la concentración elemental en la biomasa y la Conc. En el carbón está la concentración elemental en el biocarbón.
8. medir el pH del agua del proceso de HTC
- Llene cada fracción líquida del tratamiento MAHC (paso 2,7) de la materia prima y los tres biocarbales en cuatro vasos respectivos.
- Calibre la sonda de pH con soluciones estándar.
- Mida el pH de la fracción líquida de la materia prima y los tres biocoals MAHC.
9. cromatografía de gases-espectrometría de masas
- Filtre las fracciones líquidas del tratamiento MAHC (paso 2,7) con papel de filtro de malla de 150 μm. Añadir 20 mL de metanol a 1 mL de las fracciones líquidas filtradas.
- Transfiera 200 μL a un vial de muestreador automático GC-MS y coloque el vial en el muestreador automático GC-MS.
- Diluir los estándares puros de furfural y 5-Metilfurfural (grado analítico) hasta 10-2, 10-3, 10-4, y 10-5 con metanol.
- Ponga los estándares en el muestreador automático GC-MS y analícelos con los parámetros: 1 μL de volumen de inyección a 230 ° c de temperatura del inyector y 1:40 Split; 5MS columna no polar (tabla de materiales) con 15 m de longitud y 0,25 mm de espesor de película; Programa de temperatura 30 ° c, sostenga 2 min, rampa de + 40 ° c/min a 250 ° c, sostenga 2 min; ionización con 70 mV y detector de MS en el modo de escaneo con un rango m/z de 35 − 400, cada escaneo en 0,3 s.
- Establecer curvas de calibración por el área de pico total de iones (TIC) y la concentración compuesta.
- Ejecute las muestras de fase líquida de biocarbón de HTC preparadas con los mismos parámetros analíticos e identifique el furfural y el 5-Metilfurfural por medio del tiempo de retención del estándar y del espectro que coinciden en una biblioteca de espectros.
- Determine las concentraciones de furfural y 5-Metilfurfural utilizando la curva de calibración calculada (paso 9,6) e insertando las áreas de pico de muestra de furfural y 5-Metilfurfural.
10. estadísticas
- Analice los datos con la prueba de Shapiro Wilks para una distribución normal.
- Utilice la prueba U de Mann-Whitney para conjuntos de datos no distribuidos normalmente y la prueba t para conjuntos de datos distribuidos normalmente para encontrar diferencias significativas entre conjuntos de datos.
Nota: Si un conjunto de datos se distribuye normalmente y el otro no, utilice la prueba U de Mann-Whitney.
Resultados
Los resultados del análisis elemental revelaron diferencias entre la relación O/C-H/C de la madera de sauce y los biocoals del MAHC (figura 1). La materia prima muestra mayores ratios de O/C-H/C y una mayor variación de los valores. El tratamiento con MAHC redujo la variación del valor debido a la homogeneización en el reactor de microondas. La precisión del reactor de microondas permitió la diferenciación de tres etapas de degradación. La relación ...
Discusión
El MAHC permite diferenciar los pasos de la degradación química aplicando diferentes intensidades de tratamiento térmico. Por lo tanto, es posible evaluar las interacciones entre la pérdida de masa, la relación O/C-H/C, el valor de calentamiento, la reducción del componente de ceniza, el aumento del pH del agua de proceso y la acumulación de furanos en el agua de proceso. La ventaja del método MAHC sobre el método convencional del reactor HTC se basa en la conducción térmica a través de microondas que penetra...
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
A los autores les gusta agradecer a Christoph Warth, Michael Russ, Carola Lepski, Julian Tejada y el Dr. Rainer Kirchhof por su apoyo técnico. El estudio fue financiado por el BMBF (proyecto BiCoLim-bio-combustibles limpios) bajo el número de subvención 01DN16036.
Materiales
| Name | Company | Catalog Number | Comments |
| 5MS non-polar cloumn | Thermo Fisher Scientific,Waltham, USA | TraceGOLD SQC | GCMS |
| 9µm polyvinylalcohol particle column | Methrom AG, Filderstadt, Germany | Metrosep A Supp 4 -250/4.0 | Ion chromatography |
| argon | Westfalen AG, Münster, Germany | UN 1006 | ICP-OES |
| calorimeter | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C6000 | higher and lower heating value |
| centrifuge | Andreas Hettich GmbH & Co.KG, Germany | Rotofix 32 A | |
| centrifuge mill | Retsch Technology GmbH, Haan, Germany | ZM 200 | |
| ceramic dishes | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | XX83.1 | Ash content |
| cutting mill | Fritsch GmbH, Markt Einersheim, Germany | pulverisette 19 | |
| D(+) Glucose | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | X997.1 | higher and lower heating value |
| elemental analyzer | elementar Analysesysteme GmbH, Langenselbold, Germany | varioMACRO cube | elemental analysis |
| exicator | DWK Life Sciences GmbH, Wertheim, Germany | DURAN DN300 | Ash content |
| GC-MS system | Thermo Fisher Scientific,Waltham, USA | Trace 1300 | GCMS |
| hydrochloric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | HN53.3 | ICP-OES |
| ICP OES | Spectro Analytical Instruments GmbH, Kleve, Germany | Spectro Blue-EOP- TI | ICP-OES |
| Ion chromatograph | Methrom GmbH&Co.KG, Filderstadt, Germany | 833 Basic IC plus | Ion chromatography |
| kiln dryer | Schellinger KG, Weingarten, Germany | ||
| kiln dryer | Schellinger KG, Weingarten, Germany | Ash content | |
| mesh filter paper | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | L874.1 | ICP-OES |
| microwave oven | Anton Paar GmbH, Graz, Austria | Multiwave Go | |
| muffel furnance | Carbolite Gero GmbH &Co.KG, Neuhausen, Germany | AAF 1100 | Ash content |
| nitric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | 4989.1 | ICP-OES |
| oxygen | Westfalen AG, Münster, Germany | UN 1072 | higher and lower heating value |
| pH-meter | ylem Analytics Germany Sales GmbH & Co. KG, Weilheim,Germany | pH 3310 | pH |
| sample bag | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C12a | higher and lower heating value |
| Standard Laboratory Vessels and Instruments | |||
| standard samples | Bernd Kraft GmbH, Duisburg, Germany | ICP-OES | |
| sulfonamite | elementar Analysesysteme GmbH, Langenselbold, Germany | SLBS4782 | elemental analysis |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | ICP-OES |
| tin foil | elementar Analysesysteme GmbH, Langenselbold, Germany | S12.01-0032 | elemental analysis |
| tungstenVIoxide | elementar Analysesysteme GmbH, Langenselbold, Germany | 11.02-0024 | elemental analysis |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ||
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | higher and lower heating value | |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ICP-OES |
Referencias
- Li, C., Zhao, Z. K., Cai, H., Wang, A., Zhang, T. Microwave-promoted conversion of concentrated fructose into 5-hydroxymethylfurfural in ionic liquids in the absence of catalysts. Biomass and Bioenergy. 35 (5), 2013-2017 (2011).
- Möller, M., Harnisch, F., Schröder, U. Microwave-assisted hydrothermal degradation of fructose and glucose in subcritical water. Biomass and Bioenergy. 39, 389-398 (2012).
- Guiotoku, M., Rambo, C. R., Hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. 63 (30), 2707-2709 (2009).
- Guiotoku, M., Rambo, C. R., hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. (63), 2707-2709 (2009).
- Kannan, S., Gariepy, Y., Raghavan, G. S. V. Optimization and characterization of hydrochar produced from microwave hydrothermal cabonization of fish waste. Waste Management. , 159-168 (2017).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted and conventional hydrothermal carbonization of lignocellulosic waste material: Comparison of the chemical and structural properties of the hydrochars. Journal of Analytical and Applied Pyrolysis. 118, 1-8 (2016).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted hydrothermal carbonization of rapeseed husk: A strategy for improving its solid fuel properties. Fuel Processing Technology. 149, 305-312 (2016).
- Chen, W. -. H., Ye, S. -. C., Sheen, H. -. K. Hydrothermal carbonization of sugarcane bagasse via wet torrefaction in association with microwave heating. Bioresource technology. 118, 195-203 (2012).
- Nizamuddin, S., et al. Upgradation of chemical, fuel, thermal, and structural properties of rice husk through microwave-assisted hydrothermal carbonization. Environmental science and pollution research international. 25 (18), 17529-17539 (2018).
- Nizamuddin, S., et al. An overview of microwave hydrothermal carbonization and microwave pyrolysis of biomass. Reviews in Environmental Science and Bio/Technology. 17 (4), 813-837 (2018).
- Dallinger, D., Kappe, C. O. Microwave-assisted synthesis in water as solvent. Chemical reviews. 107 (6), 2563-2591 (2007).
- Qi, X., Watanabe, M., Aida, T. M., Smith, J. R. L. Catalytic dehydration of fructose into 5-hydroxymethylfurfural by ion-exchange resin in mixed-aqueous system by microwave heating. Green Chemistry. 10 (7), 799 (2008).
- Nüchter, M., Ondruschka, B., Bonrath, W., Gum, A. Microwave assisted synthesis - a critical technology overview. Green Chem. 6 (3), 128-141 (2004).
- Schanche, J. -. S. Microwave synthesis solutions from personal chemistry. Molecular Diversity. 7 (2-4), 291-298 (2003).
- Kappe, C. O. Controlled microwave heating in modern organic synthesis. Angewandte Chemie (International ed. in English). 43 (46), 6250-6284 (2004).
- Gronnow, M. J., White, R. J., Clark, J. H., Macquarrie, D. J. Energy Efficiency in Chemical Reactions: A Comparative Study of Different Reaction Techniques. Organic Process Research & Development. 9 (4), 516-518 (2005).
- Kruse, A., Dahmen, N. Hydrothermal biomass conversion: Quo vadis?. The Journal of Supercritical Fluids. 134, 114-123 (2018).
- Reza, M. T., et al. Hydrothermal Carbonization of Biomass for Energy and Crop Production. Applied Bioenergy. 1 (1), (2014).
- Libra, J. A., et al. Hydrothermal carbonization of biomass residuals: a comparative review of the chemistry, processes and applications of wet and dry pyrolysis. Biofuels. 2 (1), 71-106 (2011).
- Reza, M. T., Uddin, M. H., Lynam, J. G., Hoekman, S. K., Coronella, C. J. Hydrothermal carbonization of loblolly pine: reaction chemistry and water balance. Biomass Conversion and Biorefinery. 4 (4), 311-321 (2014).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. 4 (2), 160-177 (2010).
- Kruse, A., Funke, A., Titirici, M. -. M. Hydrothermal conversion of biomass to fuels and energetic materials. Current opinion in chemical biology. 17 (3), 515-521 (2013).
- Reza, M. T., Lynam, J. G., Uddin, M. H., Coronella, C. J. Hydrothermal carbonization: Fate of inorganics. Biomass and Bioenergy. 49, 86-94 (2013).
- Zhang, D., et al. Comparison study on fuel properties of hydrochars produced from corn stalk and corn stalk digestate. Energy. 165, 527-536 (2018).
- Huang, Y. -. B., Yang, Z., Dai, J. -. J., Guo, Q. -. X., Fu, Y. Production of high quality fuels from lignocellulose-derived chemicals: a convenient C-C bond formation of furfural, 5-methylfurfural and aromatic aldehyde. RSC Advances. 2 (30), 11211 (2012).
- Van de Vyver, S., Geboers, J., Jacobs, P. A., Sels, B. F. Recent Advances in the Catalytic Conversion of Cellulose. ChemCatChem. 3 (1), 82-94 (2011).
- Delidovich, I., Leonhard, K., Palkovits, R. Cellulose and hemicellulose valorisation: an integrated challenge of catalysis and reaction engineering. Energy & Environmental Science. 7 (9), 2803 (2014).
- Sevilla, M., Fuertes, A. B. The production of carbon materials by hydrothermal carbonization of cellulose. Carbon. 47 (9), 2281-2289 (2009).
- Yao, Z., Ma, X. Characteristics of co-hydrothermal carbonization on polyvinyl chloride wastes with bamboo. Bioresource technology. 247, 302-309 (2018).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. (4), 160-177 (2010).
- Liu, Z., Balasubramanian, R. Upgrading of waste biomass by hydrothermal carbonization (HTC) and low temperature pyrolysis (LTP): A comparative evaluation. Applied Energy. 114, 857-864 (2014).
- Khalsa, J., Döhling, F., Berger, F. Foliage and Grass as Fuel Pellets-Small Scale Combustion of Washed and Mechanically Leached Biomass. Energies. 9 (5), 361 (2016).
- Saddawi, A., Jones, J. M., Williams, A., Le Coeur, C. Commodity Fuels from Biomass through Pretreatment and Torrefaction: Effects of Mineral Content on Torrefied Fuel Characteristics and Quality. Energy & Fuels. 26 (11), 6466-6474 (2012).
- Kaltschmitt, M., Hartmann, H., Hofbauer, H. . Energie aus Biomasse: Grundlagen, Techniken und Verfahren. , (2016).
- Fengel, D., Wegener, G. . Wood: Chemistry, Ultrastructure, Reactions. , (1989).
- Obernberger, I., Thek, G. Physical characterisation and chemical composition of densified biomass fuels with regard to their combustion behaviour. Biomass and Bioenergy. 27 (6), 653-669 (2004).
- Kenney, W. A., Sennerby-Forsse, L., Layton, P. A review of biomass quality research relevant to the use of poplar and willow for energy conversion. Biomass. 21 (3), 163-188 (1990).
- Tharakan, P. J., Volk, T. A., Abrahamson, L. P., White, E. H. Energy feedstock characteristics of willow and hybrid poplar clones at harvest age. Biomass and Bioenergy. 25 (6), 571-580 (2003).
- Liu, Z., Quek, A., Balasubramanian, R. Preparation and characterization of fuel pellets from woody biomass, agro-residues and their corresponding hydrochars. Applied Energy. , 1315-1322 (2014).
- Technischen Komitee ISO/TC 238. . "Solid biofuels" und Technisches Komitee CEN/TC 335 "Biogene Festbrennstoffe" Solid biofuels - Determination of calorific value (ISO 18125:2017); German version EN ISO 18125:2017. , (2017).
- Kambo, H. S., Dutta, A. A comparative review of biochar and hydrochar in terms of production, physico-chemical properties and applications. Renewable and Sustainable Energy Reviews. 45, 359-378 (2015).
- Knappe, V., et al. Low temperature microwave assisted hydrothermal carbonization (MAHC) reduces combustion emission precursors in short rotation coppice willow wood. Journal of Analytical and Applied Pyrolysis. 134, 162-166 (2018).
- Liu, Z., Quek, A., Kent Hoekman, S., Balasubramanian, R. Production of solid biochar fuel from waste biomass by hydrothermal carbonization. Fuel. 103, 943-949 (2013).
- Hoekman, S. K., Broch, A., Robbins, C., Zielinska, B., Felix, L. Hydrothermal carbonization (HTC) of selected woody and herbaceous biomass feedstocks. Biomass Conversion and Biorefinery. 3 (2), 113-126 (2013).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados