JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
저온 마이크로파 보조 열 량 화에의 한 버드 나무 연료 방출 감소
요약
저온 마이크로파 보조 열가 탄 화 처리에 의해 저급 바이오 매스 로부터 고갈 된 방출 전 구체를 위한 프로토콜이 제시 된다. 이 프로토콜은 마이크로파 매개 변수와 바이오 석탄 제품 및 공정 수의 분석을 포함 한다.
초록
바이오 매스는 CO2 배출량이 바이오 매스 성장 에 다시 통합 되기 때문에 지속 가능한 연료입니다. 그러나, 바이오 매스 내의 무기 전 구체는 부정적인 환경적 영향과 슬 래그 형성을 야기 한다. 선택 된 짧은 회전 코피스 (SRC) 버드 나무는 높은 회분 함량 (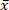 = 1.96%) 그리고, 따라서, 방출 및 슬 래그 전 구체의 함량이 높다. 따라서, 150 ° c, 170 ° c, 및 185 ° c에서 저온 마이크로파 보조 열 수가 (MAHC)에 의해 SRC 버드 나무에서 미네랄의 감소가 조사 된다. 기존 반응 기에 걸친 MAHC의 이점은 반응 매체에서 균일 한 온도 전도도 이며, 마이크로파가 전체 원자로 체적을 관통 합니다. 이것은 더 나은 온도 제어 및 빠른 재사용 대기 시간을 허용 합니다. 따라서, 중 합, 형질 전환 및 중 합 반응의 연속은 효과적으로 분석 될 수 있다. 본 연구에서, 처리 된 SCR 버드 나무의 질량 손실, 회분 함량 및 조성 물,가 열 값 및 몰 O/c 및 H/C 비율의 분석 결과는 MAHC 석탄의 광물 함량이 감소 하 고가 열 값이 증가 하는 것으로 나타났다. 공정 수는 pH를 감소 하 고 퍼 푸 랄과 5-메 틸 푸 르를 함유 하였다. 170 ° c의 공정 온도는 에너지 입력과 회분 성분 감소의 최상의 조합을 보였다. MAHC는 수 열 탄소 화 공정의 더 나은 이해를 가능 하 게 하며 대규모 산업 응용은 높은 투자 비용으로 인해 거의 불가능 합니다.
= 1.96%) 그리고, 따라서, 방출 및 슬 래그 전 구체의 함량이 높다. 따라서, 150 ° c, 170 ° c, 및 185 ° c에서 저온 마이크로파 보조 열 수가 (MAHC)에 의해 SRC 버드 나무에서 미네랄의 감소가 조사 된다. 기존 반응 기에 걸친 MAHC의 이점은 반응 매체에서 균일 한 온도 전도도 이며, 마이크로파가 전체 원자로 체적을 관통 합니다. 이것은 더 나은 온도 제어 및 빠른 재사용 대기 시간을 허용 합니다. 따라서, 중 합, 형질 전환 및 중 합 반응의 연속은 효과적으로 분석 될 수 있다. 본 연구에서, 처리 된 SCR 버드 나무의 질량 손실, 회분 함량 및 조성 물,가 열 값 및 몰 O/c 및 H/C 비율의 분석 결과는 MAHC 석탄의 광물 함량이 감소 하 고가 열 값이 증가 하는 것으로 나타났다. 공정 수는 pH를 감소 하 고 퍼 푸 랄과 5-메 틸 푸 르를 함유 하였다. 170 ° c의 공정 온도는 에너지 입력과 회분 성분 감소의 최상의 조합을 보였다. MAHC는 수 열 탄소 화 공정의 더 나은 이해를 가능 하 게 하며 대규모 산업 응용은 높은 투자 비용으로 인해 거의 불가능 합니다.
서문
열가 탄 화를 위한 마이크로파의 적용 (mahc)은과 당, 포도 당1,2 또는 셀 룰로 오 스와 같은 바이오매스 모델 화합물의 열 화학적 형질 전환 및 유기 기질을 위해 사용 되었다 바람직하게는 폐기물4,5,6,8,10. 마이크로파의 활용은 주로 유전 용 매 (11)의 열 손실을 통해 처리 된 바이오 매스2,10 의 균일 한가 열을 가능 하 게 하기 때문에, 마이크로파는 비록 직접 화학 결합을 중단 하 고 반응을 유도 하기 위해 충분 한 에너지를 전달 하지13. 마이크로파는 HTC 반응 기 용기의 전체 반응 체적을 관통 하 고 에너지를 재료에 직접 전달 하며,이는 종래의 반응 기로는 철강 맨 틀의 높은가 열 용량으로 인 한 느린가 열 속도를 나타내는 것이 불가능 하 고 샘플 자체14. 마이크로파에의 한 시료의 물 분자의 고른 흥분은 마이크로웨이브 반응 기의 온도가11,14,15 로 균등 하 게 분배 되 고 이후 재사용 대기 시간이 단축 됨에 따라 개선 된 공정 제어를 가능 하 게 합니다. 반응은 훨씬 빠릅니다. 더욱이, 종래의 반응 기는 발열 시 발생 하는 화학적 반응이 훨씬 느리고, 일반적으로 최종 온도에 할당 되는 결과를 바이어스 할 수 있다. MAHC 반응 기의 개선 된 공정 제어는 선택 된 HTC 반응 (예: 탈수 또는 탈 탄산)의 온도 의존성을 정밀 하 게 구체화 합니다. HTC 반응 기 부피에서 균등 한 온도 분포의 또 다른 이점은 내부 반응 기 벽 (2) 상에 서 고 정화 및 완전히 탄 화 된 입자의 접착력이 낮아진 것 이다. 그러나 물만이 평균 마이크로파 흡수 용 제로 서, 높은 온도에서 마이크로파 흡 광도를 감소 시키는 것을 보여주고,이는 달성 가능한 최대 온도를 제한 합니다. 이 부정적인 영향은 처리 전에 추가 된 HTC 공정 또는 촉매 (이온 또는 극성 종) 중에 산이 생성 될 때 보상 됩니다. 마이크로파 유도 반응은 일반적으로11,15 에서 더 높은 제품 수율과과 당에서 5-하이드 록 시 메 틸 푸 르 팔 (5-hmf)을 표시 모래 침대 촉매 반응에 비해12. 그들은 또한 기존의가 열 방법15,16다음 훨씬 더 나은 에너지 균형을가지고 있다.
열가 탄 화의 근본적인 화학 개념은 바이오 매스의 분해 및 연속적인 중 합 이다. 이러한 복잡 한 상호작용 반응의 과정에서 조직은 산소를 고갈 시켜가 열 값을 증가 시킵니다. 우선, 헤 미 및 셀 룰로 오 스는 당 단량체17로 가수분해 되 고, 저온은 주로 헤 미18,20,21에 영향을 미친다. HTC 반응의 초기 단계에서 유기 산은 설탕 알 데히드와 헤 미 셀 루 deacetylation의 변형으로 형성 됩니다. 이들 산은 아세트산, 락 트, 레 불린, 아크릴 또는 포 름 산20,21,22 일 수 있으며 반응 기 내에서의 물의 pH를 감소 시켰다. 해리로 인해 공정 수에서 이온 생성 물을 증가 시키는 자유 음이온을 형성 합니다. 증가 하는 이온 제품은 바이오 매스에 있는 회분의 주요 성분 인 양이온의 해결을 가능 하 게 합니다. 이 메커니즘에 의해, 조직은 방출 전 구체 및 슬 래그 포 머 (예: 칼륨, 나트륨, 칼슘, 염소 및 중 금속) 로부터고갈 된다24.
형성 된 유기 산은 퓨 란에 당 단량체의 탈수를 지원할 수 있다. 일반적인 당 탈수 제품은 플랫폼 제품 (예: 바이오 폴리머의 합성) 역할을 하기 때문에 화학 산업에 적합 한 제품 인 소량의과 5-하이드 록 시 메 틸 푸 르 푸 르입니다. 5-메 틸 퓨 푸 랄은 셀 룰로 오 스25,26 또는 5 하이드 록 시 메 틸 푸 르27에서 촉매 반응에 의해 형성 될 수 있습니다. 생체 고분자 합성은 통제 된 조건 하에서 인위적인 재 중 합을 하는 반면, 퓨 란는 또한 mahc 반응 기의 복잡 한 화학 환경에서 고 분자량 방향족 구조를 응축, 중 합 및 형성할 수 있습니다. 상기 가용 화 된 유기 및 무기 화합물과 변형 된 우드 셀 매트릭스의 상호작용은 반응 계 (20)의 복잡도를 더 한다. 퓨 란 중 합 반응 경로는 알 돌 응축 또는 분 자간 탈수18,20 및 소수 성 쉘과 더 친수성 코어 (28)를 갖는 하이드로 차르 입자를 사용 한다. 아직 바이오 매스 입자가 완전히 분해 된 다음 재 중 합 되었는지 또는 바이오 매스 입자가 탄소 화를 위한 템플릿으로 작용할 지 여부는 밝혀지지 않았습니다. 그러나, 분해 및 재 중 합 반응은 탈 탄산 및 블랙 카본의 H/c 비율을 향하여 밴 크 레 덴 다이어그램에서 강하를 유도 하는29,30과 같이 탈수 및 반응 반응을 포함 한다.
다른 연구는 종래의 반응 기 기반 수 열 처리 (31)의 광물 환 원 효과를 입증 하는 반면, 결합 된 기계 침 출32 또는 물/암모늄 아세테이트/염 산 세척33으로 물 세척 하는 것은, 우리의 연구는 처음으로 마이크로파를 가진 저온 탄 화 도중 무기물 침 출을 조사 합니다. 이 연구는 연료 업그레이드를 위한 방출 전 구체 침 출에 초점을 맞추고 있으므로 칼륨, 나트륨, 마그네슘, 칼슘, 염소, 황, 질소 및 중 금속의 운명을 조사 합니다. 미세 먼지 전 구체는 기체 상태의 고온에서 휘발성 염 (예: KCl또는 kca3.1)을 형성 합니다. 이러한 염이 연도 가스에 축적 되 면 아연과 같은 중 금속은 입자 성장 연쇄 반응으로 이어지는 핵 생성 입자로 청소할 수 있습니다. 낮은 연도 가스 온도에서 염 응축은 입자의 성장을 유발 하 고 굴뚝에서 cancerogenous 미세한 먼지 배출을 초래 합니다. 이러한 배출량은 현재 바이오 매스 연료의 지속 가능성을 손상 시키는 주요 요인이 되 고 있습니다. 지속 가능한 에너지 공급은 고가의 필터 또는 연료의 감소 (예: MAHC)에의 한 감소에 의존 합니다. 이 연구는 실용적인 접근법을 따르며, 짧은 회전 코피스 (SRC) 윌 로우 우드는 높은 성장률을 가진 잠재적인 바이오 에너지 공급 원료로 선정 되었습니다. 그것은 가스 화에 의해 자체 지속 가능한 전원 공급 장치에 대 한 자신의 분야에 농민에 의해 성장할 수 있습니다, 뿐만 아니라 직접 연소에의 한 열 발생에 대 한. 버드 나무 SRC의 단점은 낮은 줄기로 인 한 높은 수 피 함량이 며 성숙 단계에서의 나무 껍질 비율입니다. 나무 껍질은 목재34,35,36,37 와 비교 하 여 많은 미네랄을 포함 하 고 가스 또는 입자 방출38의 높은 수량을 산출 합니다. 저온 HTC는 SRC 윌 로우 우드의 연소 특성을 향상 시키고,이로 인해 지속 가능한 열 및 전원 공급에 기여할 수 있습니다. 이 연구에서 조사 된 HTC 바이오 석탄의 또 다른 중요 한 매개 변수는 에너지 밀도, 높은 초기 연소 온도 및 높은 최종 연소 온도39입니다.
프로토콜
1. 샘플 재료의 제조
- 수확 5 년 된 버드 나무, 클론 형 「 Tordes (살 릭 스schwerinii x s. viminalis) 」의 높이가 12 − 14 m, 유 방 지름 약 15cm.
- 목재를 칩 하 고 105 ° c에서 24 시간 동안가 마 건조 기에 칩을 건조 한다.
- 절단 분쇄기로 목재 칩을 절단 하 고 원심 분쇄기로 분쇄 하 여 0.12 mm의 입자 크기를 냅니다.
2. 마이크로파 보조 열로 탄 화
- 850 W의 전자 렌지와 2455 MHz의 마 그 네트 론 주파수를 사용 하십시오.
- 1.3 단계에서 원료 500 mg을 주걱으로 50 mL 에틸렌 (PTFE) 반응 용기에 넣습니다. 탈 염 수 10ml를 첨가 합니다. 캡의 압력 밸브가 캡 테두리와 동일한 수준에 있도록 반응 용기 캡을 조이십시오.
- 각 처리 온도에 대해, 전자 렌지에 원료를 12 개의 반응 용기에 넣고 오븐을 닫습니다.
- 3 온도 프로그램을 설정 합니다: 150 ° c (램프 + 12.5 ° c 분-1을 유지 60 분, 피크 전력 50%), 170 ° c (램프 + 9.6 ° c 분) 및60 ° c (램프 + 80 ° c 분-1 을 유지 30 분, 램프-1.1을 150 ° c , 최대 전력 100%)를 유지 합니다. 각 단일 프로그램에 대해 전자 렌지를 시작 하십시오.
- 프로그램이 완료 되 면 반응 용기를 제거 하 고 냉각 및 재 활성화를 허용 합니다. 그런 다음 내부 압력을 방출 한 후 연기 찬 장 아래에서 엽 니.
- 각 반응 용기에 증류수 2 회 35 mL를 추가 합니다. 각 용기의 용액을 원심 분리기 실린더에 붓고 10 분 동안 1714 x g 에서 원심 분리 합니다.
- 공정 수는 다른 튜브로 배출 되 고 pH 및 기체 크로마토그래피 질량 분 광 법 (GC-MS) 분석을 위해-5°c에서 냉동 보관 됩니다.
- 원심 분리기 실린더를-5°c에서 남아 있는 바이오 석탄 펠 릿으로 고정 합니다. 그런 다음 바이오 석탄 펠 렛을 꺼내 24 시간 동안 105 ° c에서 건조 시키십시오. 바이오 석탄 펠 릿을 계량 하 고 MAHC 처리에 의해 유도 된 체중 감량을 계산 합니다.
- 2.2 ~ 2.8 단계를 반복 하 여 온도 당 4 회 (48 반응 용기)를 생성 하 여 후속 분석을 위한 충분 한 바이오 석탄 (약 22g)을 생산 합니다.
3. 회분 함량 측정
- 20 개의 빈 세라믹 요리를 개별적으로 계량 합니다. 각 1g의 시료 (원 재료 5g× 1 g, 각 온도 처리에서 생 석탄 5g× 1g)를 추가 합니다.
참고: 요리에 레이블을 지정할 수 없기 때문에 오븐에 있는 용기의 배열에 대 한 계획을 그려야 합니다. - 오픈 세라믹 요리를 머 플로 넣고 용광로를 닫습니다.
- 상기 머 플로 (+ 6°c)에서 25°c 내지 250 ° c 에서 60 분, + 10°c에서 550 ° c까지 유지 하 고, 120 분 을 홀드 하 여 프로그램을 시작 하는 온도 프로그램을 프로그램 한다.
- 프로그램이 완료 되 면, 105 ° c로 냉각로 머 플을 보자. 그런 다음 노를 열고 세라믹 요리를 꺼내.
- 실리 카겔로 구성 된 건조제로 채워진 추출기 (재료 표)에 세라믹 접시를 놓습니다. 진공 펌프의 도움으로 건조제를 닫고 진공 건조 하십시오.
- 24 시간 냉각 후 세라믹 요리를 꺼내 세요. 재가 들어 있는 세라믹 접시를 계량 하 고 빈 세라믹 접시의 무게를 빼서 회분 중량을 계산 합니다.
- 회분의 중량을 원료 또는 바이오 석탄의 건조 질량으로 나누어 재 함량을 퍼센트로 결정 한다.
4. 더 높고 낮은가 열 값의 결정
- 열 량 계의 워터 펌프를 활성화 하 고 산소 밸브를 열어 칼로리 미터에 99.5%의 산소를 공급 합니다.
- 포도 당의 1g을 계량 하 여 46479 J/g의 열 량 값이 있는 플라스틱 샘플 봉지에 넣으십시오. 샘플 봉지를 열 량 계 폭탄의 연소 도가니에 넣으십시오.
- 폭탄 바닥에 탈 이온 수 5 mL를 넣고 폭탄을 조입니다. 열 량 계에 폭탄을 넣고 칼로리 미터를 닫습니다.
- 샘플의 무게를 입력 하 고 설정을 샘플 백 방법으로 변경 합니다. 칼로리 미터를 시작 합니다.
- 측정이 완료 되 면 폭탄을 꺼내 거꾸로 돌려 1 분간 천천히 흔들어 줍니다.
- 폭탄을 풀고 2 회 탈 염 수 5 mL를 제거 하 고 후속 이온 크로마토그래피 분석을 위해 스크류 캡 용기에 보관 하십시오.
- 4.2-4.6 단계를 반복 하 여 교정 표준을 얻습니다.
- 각 MAHC 바이오 석탄 (150 ° c, 170 ° c, 185 ° c) 및 원료를 사용 하 여 4.2-4.6 단계를 5 회 반복 하십시오.
- 다음 방정식40을 사용 하 여 낮은가 열 값을 계산 합니다.
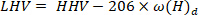
LHV가가 열 값이 낮을수록 HHV는 4.4 단계에서 열 량 계 로부터 얻어진 발열량이 높고, ω은 원소 분석 으로부터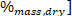 얻어진 수소 함유량 이다.
얻어진 수소 함유량 이다.
5. 염소의 정량화를 위한 이온 크로마토그래피
참고: 분석 전에 이온 크로마 토 그래프의 교정을 확인 하십시오.
- 4.8 단계에서 5 mL 용액을 꺼내 50 mL 볼륨 측정 마스크에 2 회 탈 염 수의 45 mL를 추가 합니다.
- 샘플 흡입 튜브를 샘플 용기에 넣고 주사기를 사용 하 여 샘플 약 3ml을 프리 칼럼에 그립니다. 분석 실행을 시작 합니다.
- 제조업체의 지침에 따라 측정을 수행 합니다.
- 섹션 4에서 준비한 각 샘플에 대해 5.2 및 5.3 단계를 반복 합니다.
6. O/C 및 H/C 비율 측정을 위한 원소 분석
- 측정할 샘플에 대해서는 계측기 설명서에서 적절 한 방법을 선택 하십시오.
- 장치를 교정 하는 데 필요한 모든 20 mg 미드 표준과 공백을 만드십시오.
- 재료 샘플을 준비 하려면 마이크로 저울에 샘플 20 mg을 주석 호 일에 넣으십시오. 주석 호 일의 샘플을 계량 하 고 샘플 주위의 호 박을 닫은 다음 패키지를 눌러 가능한 한 적은 공기를 포함 시킵니다. 그런 다음 각 샘플에 대해이 5 배를 반복 합니다.
참고: biochar 샘플을 분석할 수 있으려면, 샘플의 양과 동일한 양의 삼산화 텅스텐을 1:1의 비율로 첨가 해야 합니다. 이는 원소 분석기에서 완전 연소를 보장 하기 위해 biochar에서 누락 된 산소를 보상 하기 위해 필요 합니다. - 준비 된 샘플을 원소 분석기의 오토 샘플러에 삽입 합니다.
- 원소 분석기의 연 소실에 대 한 산소 및 헬륨 밸브를 엽니다.
- 장치가 장치에서 지정한 온도에 도달 하면 해석을 시작 합니다. 이 경우, 온도가 900 ° c에 도달할 때까지 기다리십시오.
- 미드 표준 무게 (단계 6.2) 및 각 원소의 1 몰의 중량에 의해 미드 표준에서 각 원소의 몰수를 계산 한다.
- 6.7 단계에서 얻은 미드에서 C, H, S 및 N의 두더지와 각각의 피크 영역 사이의 관계를 계산 합니다.
- 총 샘플 중량에서 3.7 단계에서 얻은 샘플 회분 함량을 뺍니다.
- 미드 표준 및 샘플의 각 요소 피크 영역을 비교 하 고, 미드의 각 요소에 대 한 몰을 곱하여 샘플에서 요소의 몰 수를 구합니다.
- 6.10 단계에서 얻어진 원소의 몰을 주기율표의 각각의 몰 질량과 곱하여 시료에서 C, H, S 및 N의 중량을 계산 한다.
- 6.9 단계에서 얻어진 애쉬 프리 샘플 덩어리를 이용 하 여 시료에서 산소의 중량을 계산 하 고, 6.11 단계에서 얻어진 C, H, N 및 S의 중량을 뺀 다.
- 원료 및 MAHC 바이오 석탄 샘플에서의 몰 H/C 및 O/C 비율을 계산 합니다.
7. 유도 결합 플라즈마 광 방출 분 광 법
- 말린 원료 또는 MAHC 바이오 석탄 400 mg을 계량 하 여 50 mL PTFE 반응 용기에 넣어 주걱으로 넣습니다. 69%의 질 산과 35% 염 산 9 mL의 3 mL를 추가 합니다.
- 캡의 압력 밸브가 캡 테두리와 동일한 수준에 있도록 반응 용기 캡을 조이십시오.
- 분석 하고자 하는 시료의 반응 용기를 전자 렌지에 넣고 오븐을 닫으십시오.
- 유기 재료의 완전 한 분해를 위한 온도 프로그램을 프로그래밍: 램프 + 15.5 ° c 분- 200 ° c, 30 분을 유지 하 고 180 ° c까지 냉각 하 여 5 분간 유지 합니다. 전자 렌지를 시작 합니다.
- 프로그램이 완료 되 면 반응 용기를 제거 하 고 냉각 및 재 활성화를 허용 합니다. 그런 다음 내부 압력을 방출 한 후 연기 찬 장 아래에서 용기를 엽니다.
- 샘플을 50 mL 벌브 실린더에 붓 습니다. 이어서 반응 용기를 2 회 탈 이온 수로 철저히 헹 구 고이를 벌브 실린더에 전달 한다. 모든 시료의 희석도를 보장 하기 위해 실린더를 50 mL 마크에 두 번 탈 이온 수로 올려 보세요.
- 150 µm 메쉬 필터 종이로 7.6 단계에서 샘플을 필터링 합니다. 여과 액을 50 mL 원추형 원심 분리기 튜브에 채우십시오.
- ICP의 자동 인젝터에 표준 샘플을 넣습니다. 상기 표준 시료는 알려진 농도 (0.0001 ppm, 0.001 ppm, 0.1 ppm, 1ppm 10ppm, 20ppm 50, 5Ppm)(b)로 정량화 되는 원소로 서, Fe,이 세, Zn, Ag, 알루미늄, 구리, 이를 통해, 밀리 그램, 미네소타, 모에 나, 니켈, Rb 및
- ICP의 자동 인젝터에 샘플을 넣고 동일한 파라미터로 ICP 분석을 실행 합니다.
- ICP 분석 후 7.8 단계에서 표준 샘플에서 얻은 교정 곡선을 기반으로 밀리 그램/kg으로 자동 계산 되는 소프트웨어에서 원소 농도를 구합니다.
- 생산 된 바이오 석탄의 원소 농도 감소를 계산:
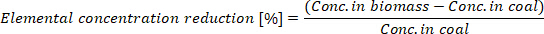
여기서 Conc. 바이오 매스는 바이오 매스와 Conc의 원소 농도 이다. 석탄에는 바이오 석탄의 원소 농도가 있습니다.
8. HTC 공정 수의 pH 측정
- 원 재료의 MAHC 처리 (단계 2.7)에서 각 액체 분 획을 각각의 비 커에 있는 3 개의 생물 석탄으로 채우십시오.
- 표준 솔루션으로 pH 프로브를 교정 합니다.
- 원료의 액체 분 획과 3 개의 MAHC 바이오 석탄의 pH를 측정 합니다.
9. 가스 크로마토그래피-질량 분석기
- 150 µm 메시 여과 지를 가진 MAHC 처리 (단계 2.7)에서 액체 분 획을 여과 하십시오. 20 mL의 메탄올을 여과 된 액체 분 획의 1Ml에 첨가 한다.
- 200 µ L을 GC-MS 오토 샘플러 바이 알에 전달 하 고, 바이 알을 GC-MS 오토 샘플러에 넣는다.
- 푸 르 푸 랄과 5-메 틸 푸 르 푸 랄 (분석적 등급)의 순수한 표준에 메탄올을 사용 하여 10 ~2, 10, 10 ~5 까지 희석 하십시오.
- GC-MS 자동 샘플러에 표준을 넣고 매개 변수를 사용 하 여 분석 하십시오: 230 ° c에서 1 µ L 사출 체적 인젝터 온도 및 1:40 분할; 5MS 비 극성 열 (재료의 테이블) 길이 15 m 및 0.25 mm 필름 두께; 온도 프로그램 30°c, 2 분, + 40 ° c/분의 램프를 250 ° c로 유지 하 고 2 분간 유지 합니다. 0.3의 각 스캔 35-1400의 m/z 범위의 스캔 모드에서 70 mV 및 MS 검출기로 이온화 합니다.
- 총 이온 수 (TIC) 피크 영역과 복합 농도에 따라 보정 곡선을 설정 합니다.
- 동일한 분석 매개 변수를 사용 하 여 준비 된 HTC 바이오 석탄 액체 상 샘플을 실행 하 고 스펙 트 라 라이브러리의 표준 및 스펙트럼 일치의 보존 시간에 따라 소량의 및 5-메 틸 푸 르 팔을 식별 합니다.
- 계산 된 교정 곡선 (단계 9.6)을 사용 하 고 푸 르 푸 랄 및 5-메 틸 푸 르의 샘플 피크 영역을 삽입 하 여 소량의 및 5-메 틸 푸 랄의 농도를 확인 합니다.
10. 통계
- 정규 분포를 테스트 하 여 데이터를 분석 합니다.
- 비 통상적으로 분산 된 데이터 세트에 대 한만-휘트니 U 테스트를 사용 하 고 데이터 세트 간의 중요 한 차이를 찾기 위해 일반적으로 분산 된 데이터 세트에 대 한 t-검정을 이용 하십시오.
참고: 하나의 데이터 세트가 일반적으로 배포 되 고 다른 데이터가 아닌 경우에는만-휘트니 U 테스트를 사용 하십시오.
결과
원소 분석의 결과는 버드 나무와 MAHC 바이오 석탄의 O/C-H/C 비율의 차이를 밝혀 주었다 (그림 1). 원료는 더 높은 O/C-H/C 비율과 값의 높은 편차를 보여줍니다. MAHC 처리는 마이크로파 반응 기에서 균질 화에의 한 값 변동을 감소 시켰습니다. 마이크로파 반응 기의 정밀도는 3 단계의 분해의 분화를 허용 하였다. H/C 비율이 150 ° c에서 감소 하였으며, H/c 및...
토론
MAHC는 열 처리의 상이한 강도를 적용 하 여 화학적 분해 단계의 분화를 허용 한다. 따라서, 공정 수 중의 질량 손실, O/C-H/C 비율,가 열 값, 회분 성분 환 원, 공정 수의 pH 증가 및 퓨 란의 축적 간의 상호작용을 평가할 수 있다. 종래의 HTC 반응 기에 걸친 MAHC 방법의 이점은 전체 반응 기 부피를 관통 하는 마이크로파를 통한 열전도를 기반으로 하 고 거시적 층에 의해 반응 기 부피를가 열 하는 것이 아...
공개
저자는 공개 할 것이 없습니다.
감사의 말
저자는 크리스토프 Warth, 마이클 러 스, Carola 렙 스키, 줄리안 테 하다 및 박사 Rainer 키 르 호프의 기술 지원을 부탁 드립니다. 이 연구는 보조금 번호 01DN16036에서 BMBF (프로젝트 BiCoLim-가연성 Limpios)에 의해 자금을 지원 하였다.
자료
| Name | Company | Catalog Number | Comments |
| 5MS non-polar cloumn | Thermo Fisher Scientific,Waltham, USA | TraceGOLD SQC | GCMS |
| 9µm polyvinylalcohol particle column | Methrom AG, Filderstadt, Germany | Metrosep A Supp 4 -250/4.0 | Ion chromatography |
| argon | Westfalen AG, Münster, Germany | UN 1006 | ICP-OES |
| calorimeter | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C6000 | higher and lower heating value |
| centrifuge | Andreas Hettich GmbH & Co.KG, Germany | Rotofix 32 A | |
| centrifuge mill | Retsch Technology GmbH, Haan, Germany | ZM 200 | |
| ceramic dishes | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | XX83.1 | Ash content |
| cutting mill | Fritsch GmbH, Markt Einersheim, Germany | pulverisette 19 | |
| D(+) Glucose | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | X997.1 | higher and lower heating value |
| elemental analyzer | elementar Analysesysteme GmbH, Langenselbold, Germany | varioMACRO cube | elemental analysis |
| exicator | DWK Life Sciences GmbH, Wertheim, Germany | DURAN DN300 | Ash content |
| GC-MS system | Thermo Fisher Scientific,Waltham, USA | Trace 1300 | GCMS |
| hydrochloric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | HN53.3 | ICP-OES |
| ICP OES | Spectro Analytical Instruments GmbH, Kleve, Germany | Spectro Blue-EOP- TI | ICP-OES |
| Ion chromatograph | Methrom GmbH&Co.KG, Filderstadt, Germany | 833 Basic IC plus | Ion chromatography |
| kiln dryer | Schellinger KG, Weingarten, Germany | ||
| kiln dryer | Schellinger KG, Weingarten, Germany | Ash content | |
| mesh filter paper | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | L874.1 | ICP-OES |
| microwave oven | Anton Paar GmbH, Graz, Austria | Multiwave Go | |
| muffel furnance | Carbolite Gero GmbH &Co.KG, Neuhausen, Germany | AAF 1100 | Ash content |
| nitric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | 4989.1 | ICP-OES |
| oxygen | Westfalen AG, Münster, Germany | UN 1072 | higher and lower heating value |
| pH-meter | ylem Analytics Germany Sales GmbH & Co. KG, Weilheim,Germany | pH 3310 | pH |
| sample bag | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C12a | higher and lower heating value |
| Standard Laboratory Vessels and Instruments | |||
| standard samples | Bernd Kraft GmbH, Duisburg, Germany | ICP-OES | |
| sulfonamite | elementar Analysesysteme GmbH, Langenselbold, Germany | SLBS4782 | elemental analysis |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | ICP-OES |
| tin foil | elementar Analysesysteme GmbH, Langenselbold, Germany | S12.01-0032 | elemental analysis |
| tungstenVIoxide | elementar Analysesysteme GmbH, Langenselbold, Germany | 11.02-0024 | elemental analysis |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ||
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | higher and lower heating value | |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ICP-OES |
참고문헌
- Li, C., Zhao, Z. K., Cai, H., Wang, A., Zhang, T. Microwave-promoted conversion of concentrated fructose into 5-hydroxymethylfurfural in ionic liquids in the absence of catalysts. Biomass and Bioenergy. 35 (5), 2013-2017 (2011).
- Möller, M., Harnisch, F., Schröder, U. Microwave-assisted hydrothermal degradation of fructose and glucose in subcritical water. Biomass and Bioenergy. 39, 389-398 (2012).
- Guiotoku, M., Rambo, C. R., Hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. 63 (30), 2707-2709 (2009).
- Guiotoku, M., Rambo, C. R., hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. (63), 2707-2709 (2009).
- Kannan, S., Gariepy, Y., Raghavan, G. S. V. Optimization and characterization of hydrochar produced from microwave hydrothermal cabonization of fish waste. Waste Management. , 159-168 (2017).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted and conventional hydrothermal carbonization of lignocellulosic waste material: Comparison of the chemical and structural properties of the hydrochars. Journal of Analytical and Applied Pyrolysis. 118, 1-8 (2016).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted hydrothermal carbonization of rapeseed husk: A strategy for improving its solid fuel properties. Fuel Processing Technology. 149, 305-312 (2016).
- Chen, W. -. H., Ye, S. -. C., Sheen, H. -. K. Hydrothermal carbonization of sugarcane bagasse via wet torrefaction in association with microwave heating. Bioresource technology. 118, 195-203 (2012).
- Nizamuddin, S., et al. Upgradation of chemical, fuel, thermal, and structural properties of rice husk through microwave-assisted hydrothermal carbonization. Environmental science and pollution research international. 25 (18), 17529-17539 (2018).
- Nizamuddin, S., et al. An overview of microwave hydrothermal carbonization and microwave pyrolysis of biomass. Reviews in Environmental Science and Bio/Technology. 17 (4), 813-837 (2018).
- Dallinger, D., Kappe, C. O. Microwave-assisted synthesis in water as solvent. Chemical reviews. 107 (6), 2563-2591 (2007).
- Qi, X., Watanabe, M., Aida, T. M., Smith, J. R. L. Catalytic dehydration of fructose into 5-hydroxymethylfurfural by ion-exchange resin in mixed-aqueous system by microwave heating. Green Chemistry. 10 (7), 799 (2008).
- Nüchter, M., Ondruschka, B., Bonrath, W., Gum, A. Microwave assisted synthesis - a critical technology overview. Green Chem. 6 (3), 128-141 (2004).
- Schanche, J. -. S. Microwave synthesis solutions from personal chemistry. Molecular Diversity. 7 (2-4), 291-298 (2003).
- Kappe, C. O. Controlled microwave heating in modern organic synthesis. Angewandte Chemie (International ed. in English). 43 (46), 6250-6284 (2004).
- Gronnow, M. J., White, R. J., Clark, J. H., Macquarrie, D. J. Energy Efficiency in Chemical Reactions: A Comparative Study of Different Reaction Techniques. Organic Process Research & Development. 9 (4), 516-518 (2005).
- Kruse, A., Dahmen, N. Hydrothermal biomass conversion: Quo vadis?. The Journal of Supercritical Fluids. 134, 114-123 (2018).
- Reza, M. T., et al. Hydrothermal Carbonization of Biomass for Energy and Crop Production. Applied Bioenergy. 1 (1), (2014).
- Libra, J. A., et al. Hydrothermal carbonization of biomass residuals: a comparative review of the chemistry, processes and applications of wet and dry pyrolysis. Biofuels. 2 (1), 71-106 (2011).
- Reza, M. T., Uddin, M. H., Lynam, J. G., Hoekman, S. K., Coronella, C. J. Hydrothermal carbonization of loblolly pine: reaction chemistry and water balance. Biomass Conversion and Biorefinery. 4 (4), 311-321 (2014).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. 4 (2), 160-177 (2010).
- Kruse, A., Funke, A., Titirici, M. -. M. Hydrothermal conversion of biomass to fuels and energetic materials. Current opinion in chemical biology. 17 (3), 515-521 (2013).
- Reza, M. T., Lynam, J. G., Uddin, M. H., Coronella, C. J. Hydrothermal carbonization: Fate of inorganics. Biomass and Bioenergy. 49, 86-94 (2013).
- Zhang, D., et al. Comparison study on fuel properties of hydrochars produced from corn stalk and corn stalk digestate. Energy. 165, 527-536 (2018).
- Huang, Y. -. B., Yang, Z., Dai, J. -. J., Guo, Q. -. X., Fu, Y. Production of high quality fuels from lignocellulose-derived chemicals: a convenient C-C bond formation of furfural, 5-methylfurfural and aromatic aldehyde. RSC Advances. 2 (30), 11211 (2012).
- Van de Vyver, S., Geboers, J., Jacobs, P. A., Sels, B. F. Recent Advances in the Catalytic Conversion of Cellulose. ChemCatChem. 3 (1), 82-94 (2011).
- Delidovich, I., Leonhard, K., Palkovits, R. Cellulose and hemicellulose valorisation: an integrated challenge of catalysis and reaction engineering. Energy & Environmental Science. 7 (9), 2803 (2014).
- Sevilla, M., Fuertes, A. B. The production of carbon materials by hydrothermal carbonization of cellulose. Carbon. 47 (9), 2281-2289 (2009).
- Yao, Z., Ma, X. Characteristics of co-hydrothermal carbonization on polyvinyl chloride wastes with bamboo. Bioresource technology. 247, 302-309 (2018).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. (4), 160-177 (2010).
- Liu, Z., Balasubramanian, R. Upgrading of waste biomass by hydrothermal carbonization (HTC) and low temperature pyrolysis (LTP): A comparative evaluation. Applied Energy. 114, 857-864 (2014).
- Khalsa, J., Döhling, F., Berger, F. Foliage and Grass as Fuel Pellets-Small Scale Combustion of Washed and Mechanically Leached Biomass. Energies. 9 (5), 361 (2016).
- Saddawi, A., Jones, J. M., Williams, A., Le Coeur, C. Commodity Fuels from Biomass through Pretreatment and Torrefaction: Effects of Mineral Content on Torrefied Fuel Characteristics and Quality. Energy & Fuels. 26 (11), 6466-6474 (2012).
- Kaltschmitt, M., Hartmann, H., Hofbauer, H. . Energie aus Biomasse: Grundlagen, Techniken und Verfahren. , (2016).
- Fengel, D., Wegener, G. . Wood: Chemistry, Ultrastructure, Reactions. , (1989).
- Obernberger, I., Thek, G. Physical characterisation and chemical composition of densified biomass fuels with regard to their combustion behaviour. Biomass and Bioenergy. 27 (6), 653-669 (2004).
- Kenney, W. A., Sennerby-Forsse, L., Layton, P. A review of biomass quality research relevant to the use of poplar and willow for energy conversion. Biomass. 21 (3), 163-188 (1990).
- Tharakan, P. J., Volk, T. A., Abrahamson, L. P., White, E. H. Energy feedstock characteristics of willow and hybrid poplar clones at harvest age. Biomass and Bioenergy. 25 (6), 571-580 (2003).
- Liu, Z., Quek, A., Balasubramanian, R. Preparation and characterization of fuel pellets from woody biomass, agro-residues and their corresponding hydrochars. Applied Energy. , 1315-1322 (2014).
- Technischen Komitee ISO/TC 238. . "Solid biofuels" und Technisches Komitee CEN/TC 335 "Biogene Festbrennstoffe" Solid biofuels - Determination of calorific value (ISO 18125:2017); German version EN ISO 18125:2017. , (2017).
- Kambo, H. S., Dutta, A. A comparative review of biochar and hydrochar in terms of production, physico-chemical properties and applications. Renewable and Sustainable Energy Reviews. 45, 359-378 (2015).
- Knappe, V., et al. Low temperature microwave assisted hydrothermal carbonization (MAHC) reduces combustion emission precursors in short rotation coppice willow wood. Journal of Analytical and Applied Pyrolysis. 134, 162-166 (2018).
- Liu, Z., Quek, A., Kent Hoekman, S., Balasubramanian, R. Production of solid biochar fuel from waste biomass by hydrothermal carbonization. Fuel. 103, 943-949 (2013).
- Hoekman, S. K., Broch, A., Robbins, C., Zielinska, B., Felix, L. Hydrothermal carbonization (HTC) of selected woody and herbaceous biomass feedstocks. Biomass Conversion and Biorefinery. 3 (2), 113-126 (2013).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유