È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Ridurre l'emissione di combustibile di salice a bassa temperatura a microonde assistito carbonizzazione Idrotermica
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Viene presentato un protocollo per la deplezione dei precursori delle emissioni da biomassa di bassa qualità mediante trattamento di carbonizzazione idrotermale assistito da microonde a bassa temperatura. Questo protocollo include i parametri del microonde e l'analisi del prodotto biocarbone e dell'acqua di processo.
Abstract
La biomassa è un combustibile sostenibile, poiché le sue emissioni di CO2 sono reintegrate nella crescita della biomassa. Tuttavia, i precursori inorganici nella biomassa causano un impatto ambientale negativo e la formazione di scorie. Il legno di salice (SRC) a rotazione corta selezionata ha un elevato tenore di ceneri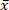 (= 1,96%) e, pertanto, un elevato contenuto di precursori delle emissioni e delle scorie. Pertanto, la riduzione dei minerali dal legno di salice SRC mediante la carbonizzazione Idrotermica assistita a microonde a bassa temperatura (MAHC) a 150 ° c, 170 ° c e 185 ° c è studiata. Un vantaggio del MAHC rispetto ai reattori convenzionali è una conduttanza di temperatura uniforme nel mezzo di reazione, poiché le microonde penetrano nell'intero volume del reattore. Questo permette un migliore controllo della temperatura e un tempo di recupero più veloce. Pertanto, una successione di reazioni di depolimerizzazione, trasformazione e repolimerizzazione può essere analizzata efficacemente. In questo studio, l'analisi della perdita di massa, del contenuto di ceneri e della composizione, dei valori di riscaldamento e dei rapporti molari di O/C e H/C del legno di salice SCR trattato e non trattato ha mostrato che il contenuto minerale del carbone MAHC è stato ridotto e il valore di riscaldamento è aumentato. L'acqua di processo ha mostrato un pH decrescente e conteneva furfurale e 5-metilfurfural. Una temperatura di processo di 170 ° c ha mostrato la migliore combinazione di energia assorbita e riduzione dei componenti in cenere. Il MAHC permette una migliore comprensione del processo di carbonizzazione idrotermale, mentre un'applicazione industriale su larga scala è improbabile a causa degli elevati costi di investimento.
(= 1,96%) e, pertanto, un elevato contenuto di precursori delle emissioni e delle scorie. Pertanto, la riduzione dei minerali dal legno di salice SRC mediante la carbonizzazione Idrotermica assistita a microonde a bassa temperatura (MAHC) a 150 ° c, 170 ° c e 185 ° c è studiata. Un vantaggio del MAHC rispetto ai reattori convenzionali è una conduttanza di temperatura uniforme nel mezzo di reazione, poiché le microonde penetrano nell'intero volume del reattore. Questo permette un migliore controllo della temperatura e un tempo di recupero più veloce. Pertanto, una successione di reazioni di depolimerizzazione, trasformazione e repolimerizzazione può essere analizzata efficacemente. In questo studio, l'analisi della perdita di massa, del contenuto di ceneri e della composizione, dei valori di riscaldamento e dei rapporti molari di O/C e H/C del legno di salice SCR trattato e non trattato ha mostrato che il contenuto minerale del carbone MAHC è stato ridotto e il valore di riscaldamento è aumentato. L'acqua di processo ha mostrato un pH decrescente e conteneva furfurale e 5-metilfurfural. Una temperatura di processo di 170 ° c ha mostrato la migliore combinazione di energia assorbita e riduzione dei componenti in cenere. Il MAHC permette una migliore comprensione del processo di carbonizzazione idrotermale, mentre un'applicazione industriale su larga scala è improbabile a causa degli elevati costi di investimento.
Introduzione
L'applicazione di forni a microonde per la carbonizzazione Idrotermica (mahc) è stata utilizzata per la trasformazione termochimica di composti del modello di biomassa come fruttosio, glucosio1,2 o cellulosa3, e per substrati organici, preferibilmente materiali di scarto4,5,6,7,8,9,10. L'utilizzo delle microonde è vantaggioso in quanto consente un riscaldamento uniforme della biomassa trattata2,10 principalmente attraverso perdite termiche di un solvente dielettrico11,12, anche se le microonde fanno non trasferire abbastanza energia per rompere direttamente legami chimici e indurre reazioni13. Le microonde penetrano l'intero volume di reazione della nave del reattore HTC e trasferiscono l'energia direttamente al materiale, che non è possibile con un reattore convenzionale che mostra una velocità di riscaldamento più lenta a causa dell'elevata capacità di riscaldamento del mantello d'acciaio e della campione stesso14. L'eccitazione uniforme delle molecole d'acqua del campione mediante microonde consente un migliore controllo del processo, poiché la temperatura nel reattore a microonde è distribuita uniformemente11,14,15 e il tempo di recupero dopo la reazione è molto più veloce. Inoltre, i reattori convenzionali riscaldano molto più lentamente e le reazioni chimiche che si verificano durante il riscaldamento possono polarare i risultati che vengono solitamente assegnati alla temperatura finale. Il miglioramento del controllo di processo in un reattore MAHC consente una precisa elaborazione della dipendenza della temperatura dalle reazioni HTC selezionate (ad es. disidratazione o decarbossilazione). Un altro vantaggio della distribuzione uniforme della temperatura nel volume del reattore HTC è la minore adesione di particelle immobilizzate e completamente carbonizzate sulla parete interna del reattore2. Tuttavia, l'acqua è solo un solvente medio che assorbe il microonde che mostra anche diminuire l'assorbanza a microonde a temperature più elevate, che limita la temperatura massima raggiungibile. Questo effetto negativo viene compensato quando gli acidi vengono prodotti durante il processo HTC o catalizzatori (specie ioniche o polari) vengono aggiunti prima del trattamento. Le reazioni causate da microonde mostrano rendimenti di prodotto più elevati in generale11,15 e in particolare di 5-idrossimetil Furfural (5-HMF) dal fruttosio rispetto alle reazioni catalizzate a letto di sabbia12. Hanno anche un bilancio energetico molto migliore poi metodi di riscaldamento convenzionali15,16.
Il concetto chimico fondamentale di carbonizzazione idrotermale è il degrado e la successiva polimerizzazione della biomassa. Nel corso di queste complesse reazioni interagenti il tessuto è impoverito di ossigeno, che aumenta il valore di riscaldamento. In un primo momento, i polimeri emicellulosa e cellulosa sono idrolizzati ai monomeri di zucchero17, anche se le basse temperature colpiscono principalmente l'emicellulosa18,19,20,21. In questa fase iniziale delle reazioni di HTC, gli acidi organici sono formati dalla trasformazione delle aldeidi di zucchero e dalla deacetilazione dell'emicellulosa. Questi acidi possono essere acetico, lattico, levulinico, acrilico o acido formico20,21,22 e diminuiscono il pH dell'acqua di reazione nel reattore. A causa della dissociazione, formano ioni negativi liberi che aumentano il prodotto ionico nell'acqua di processo. Il crescente prodotto ionico consente la risoluzione delle cationi, che sono i principali costituenti della cenere nella biomassa. Con questo meccanismo, il tessuto è impoverito dai precursori delle emissioni e dalle matrici di scorie (ad esempio potassio, sodio, calcio, cloro e metalli pesanti)23,24.
Gli acidi organici formati possono sostenere la disidratazione dei monomeri di zucchero ai furani. Un prodotto comune di disidratazione dello zucchero è il furfurale e il 5-idrossimetil furfurale, che sono prodotti realizzabili per l'industria chimica, in quanto servono come prodotti di piattaforma (ad esempio, per la sintesi di biopolimeri). 5-methylfurfural può essere formata da reazioni catalizzate da25,26 o 5-idrossimetil Furfural27di cellulosa. Mentre la sintesi biopolimerizzante è una repolimerizzazione artificiale in condizioni controllate, i furani possono anche condensare, polimerizzare e formare strutture aromatiche ad alto peso molecolare nel complesso ambiente chimico del reattore MAHC. L'interazione dei composti organici e inorganici solubilizzati con la matrice di cellule di legno modificata aggiunge alla complessità del sistema di reazione20. Le vie di reazione di polimerizzazione del furano impiegano la condensazione aldolica o/e la disidratazione intermolecolare18,20 e producono particelle di hydrochar con un guscio idrofobico e un nucleo più idrofilo28. Non si è ancora rivelato se le particelle di biomassa siano completamente decomposte e poi repolimerizzate o se le particelle di biomassa fungono da modello per la carbonizzazione. Tuttavia, le reazioni di degradazione e repolimerizzazione comprendono le reazioni di disidratazione e decarbossilazione, così29,30, che induce il calo nel diagramma van krevelen verso i rapporti O/c e H/c di carbonio nero.
Mentre altri studi hanno dimostrato l'effetto di riduzione minerale del convenzionale trattamento idrotermale a base di reattore31, di un lavaggio dell'acqua con lisciviazione meccanica combinata32 o acqua/ammonio acetato/Acido cloridrico lavaggio33, il nostro studi studiano la lisciviazione minerale durante la carbonizzazione a bassa temperatura con le microonde per la prima volta. Poiché questo studio si concentra sulla lisciviazione dei precursori delle emissioni per l'aggiornamento del combustibile, indica il destino di potassio, sodio, magnesio, calcio, cloro, zolfo, azoto e metalli pesanti. I precursori di polveri sottili formano sali volatili (ad esempio, KCl o K2so4) a temperature elevate nella fase gassosa. Quando questi sali si accumulano nel gas di combustione, i metalli pesanti come lo zinco possono dispergarli come particelle di nucleazione, il che porta ad una reazione a catena di crescita delle particelle. A temperature del gas di combustione inferiori, la condensazione del sale innesca ulteriormente la crescita delle particelle e provoca un'emissione di polveri sottili cancerogene dal camino. Queste emissioni sono attualmente il fattore principale che compromette la sostenibilità dei combustibili da biomassa. Un approvvigionamento energetico sostenibile si basa sulla loro riduzione con filtri costosi o la loro riduzione dei combustibili (ad esempio, da MAHC). Poiché questo studio segue un approccio pratico, il legno di salice a rotazione corta (SRC) è stato scelto come una potenziale materia prima di bioenergia con alti tassi di crescita. Può essere coltivato dagli agricoltori sui loro campi per un approvvigionamento di energia auto-sostenibile dalla gassificazione, ma anche per la generazione di calore mediante combustione diretta. Uno svantaggio di salice SRC è il suo alto contenuto di corteccia a causa di un basso stelo: rapporto di corteccia a stadio maturo. La corteccia contiene un sacco di minerali rispetto al legno34,35,36,37 e produce maggiori quantità di emissioni gassose o particellari38. La bassa temperatura HTC può migliorare le proprietà di combustione del legno di salice SRC e, in tal modo, contribuire a un calore e un alimentatore sostenibili. Un altro importante parametro del biocarbone HTC indagato in questo studio è la sua densità di energia, la sua maggiore temperatura di combustione iniziale e la sua maggiore temperatura di combustione finale39.
Protocollo
1. preparazione del materiale del campione
- Raccogli il salice di cinque anni, tipo clone "Tordes" ([Salix schwerinii x s. viminalis] x s. vim.), con un'altezza di 12 − 14 m e un diametro del seno di circa 15 cm.
- Scheggia il legno e asciuga le patatine in un essiccatoio per 24 ore a 105 ° c.
- Tagliare i trucioli di legno con un mulino da taglio e macinare con un mulino centrifugo ad una granulometria di 0,12 mm.
2. carbonizzazione idrotermale assistita a microonde
- Utilizzare un forno a microonde con 850 W e una frequenza di magnetron di 2.455 MHz.
- Posizionare 500 mg di materia prima dal punto 1,3 in un vaso di reazione in politetrafluoroetilene (PTFE) da 50 mL con una spatola. Aggiungere 10 mL di acqua demineralizzata. Avvitare il tappo del recipiente di reazione in modo che la valvola di pressione nel tappo sia sullo stesso livello della tesa del tappo.
- Per ogni temperatura di trattamento, mettere dodici vasi di reazione con materie prime nel forno a microonde e chiudere il forno.
- Impostare tre programmi di temperatura, con il forno a microonde per le tre temperature: 150 ° c (rampa + 12,5 ° c min-1, tenere 60 min, potenza di picco 50%), 170 ° c (rampa + 9,6 ° c min-1, tenere 60 min, potenza di picco 80%) e 185 ° c (rampa + 5,3 ° c min-1 , tenere 30 min, rampa-1,1 ° c min-1 a 150 ° c, potenza di picco 100%). Avviare il forno a microonde, per ogni singolo programma.
- Una volta completato il programma, rimuovere i vasi di reazione, consentire loro di raffreddare e riattivare. Poi aprirli sotto un armadietto dei fumi dopo aver rilasciato la pressione all'interno.
- Aggiungere 35 mL di acqua distillata due volte a ciascun recipiente di reazione. Versare la soluzione in ogni recipiente in un cilindro centrifugo e centrifugare a 1.714 x g per 10 min.
- L'acqua di processo viene scaricata in un altro tubo e conservata congelata a-5 ° c per l'analisi di pH e gascromatografia-spettrometria di massa (GC-MS).
- Congelare il cilindro centrifugo con il restante pellet di biocarbone a-5 ° c. Poi estrarre il pellet di biocarbone e asciugarlo a 105 ° c per 24 h. pesare il pellet di biocarbone e calcolare la perdita di peso indotta dal trattamento MAHC.
- Ripetere i passaggi 2.2 − 2.8 quattro volte per temperatura (48 serbatoi di reazione per temperatura) per produrre abbastanza biocarbone (circa 22 g) per l'analisi successiva.
3. determinazione del contenuto di ceneri
- Pesare 20 piatti di ceramica vuoti singolarmente. Aggiungere ogni 1 g di campione (5 x 1 g di materia prima e 5 x 1 g di biocarbone per ogni trattamento di temperatura).
Nota: poiché i piatti non possono essere etichettati, un piano deve essere disegnato per la disposizione dei vasi nel forno. - Collocare i piatti in ceramica aperta in un forno a muffola e chiudere il forno.
- Programmare un programma di temperatura per il forno a muffola (+ 6 ° c min-1 da 25 ° c a 250 ° c, tenere 60 min, + 10 ° c min-1 a 550 ° c, tenere 120 min) e avviare il programma.
- Una volta completato il programma, lasciare raffreddare il forno a muffola fino a 105 ° c. Quindi aprire il forno e togliere i piatti di ceramica.
- Collocare i piatti di ceramica in un estrattore (tabella dei materiali) riempito con un agente di essiccazione costituito da gel di silice. Chiudere l'essiccatore e asciugare sottovuoto con l'ausilio di una pompa per vuoto.
- Togliere i piatti di ceramica dopo 24 h di raffreddamento. Pesare il piatto di ceramica contenente la cenere e calcolare il peso della cenere sottraendo il peso del piatto di ceramica vuoto.
- Determinare il tenore di ceneri in percentuale dividendo il peso della cenere per la massa secca della materia prima o del biocarbone.
4. determinazione dei valori di riscaldamento superiori e inferiori
- Attivare la pompa dell'acqua del calorimetro e aprire la valvola dell'ossigeno per fornire 99,5% di ossigeno al calorimetro.
- Pesare 1 g di glucosio e metterlo in un sacchetto di plastica campione con un valore calorico definito di 46.479 J/g. Metti il sacchetto del campione nel crogiolo di combustione di una bomba calorimetro.
- Aggiungere 5 mL di acqua due volte deionizzata nella parte inferiore della bomba e avvitare la bomba. Metti la bomba nel calorimetro e Chiudi il calorimetro.
- Immettere il peso del campione e modificare le impostazioni per il metodo del sacchetto di campionamento. Avviare il calorimetro.
- Dopo la misurazione è completata, togliere la bomba, capovolgerla e scuotere lentamente per 1 min.
- Svitare la bomba, rimuovere 5 mL di acqua due volte demineralizzata e conservarla in un contenitore di tappo a vite per l'analisi di cromatografia ionica successiva.
- Ripetere i passaggi 4.2 − 4.6 tre volte per ottenere lo standard di calibrazione.
- Ripetere i passaggi 4.2 − 4.6 cinque volte con ogni biocarbone MAHC (150 ° c, 170 ° c, 185 ° c) e la materia prima.
- Calcolare il valore di riscaldamento inferiore utilizzando la seguente equazione40:
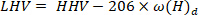
dove LHV è il valore di riscaldamento più basso, HHV è il valore di riscaldamento più elevato ottenuto dal calorimetro nel passaggio 4,4 e ω è il contenuto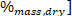 di idrogeno [ottenuto dall'analisi elementare.
di idrogeno [ottenuto dall'analisi elementare.
5. cromatografia ionica per la quantificazione del cloro
Nota: controllare la calibrazione del cromatografo ionico prima dell'analisi.
- Estrarre i 5 mL di soluzione dal passo 4,8 e aggiungere 45 mL di acqua due volte demineralizzata in una maschera volumetrica da 50 mL.
- Inserire il tubo di aspirazione del campione in un contenitore campione e prelevare circa 3 mL del campione con una siringa nella pre-colonna. Avviare l'esecuzione dell'analisi.
- Eseguire le misurazioni secondo le istruzioni del fabbricante.
- Ripetere i passaggi 5,2 e 5,3 per ogni campione preparato nel paragrafo 4.
6. analisi elementale per la determinazione dei rapporti O/C e H/C
- Selezionare un metodo appropriato dal manuale dello strumento per i campioni da misurare.
- Fare tutti gli standard di 20 mg sulfonamide e spazi vuoti necessari per calibrare il dispositivo.
- Per preparare un campione di materiale, mettere 20 mg di campione in lamina di stagno sul micro equilibrio. Pesare il campione sulla lamina di stagno, chiudere il foglio intorno al campione e premere il pacchetto per contenere il meno possibile l'aria. Successivamente ripetere questo 5x per ogni campione.
Nota: al fine di essere in grado di analizzare i campioni di biochar, la stessa quantità di triossido di tungsteno come la quantità del campione deve essere aggiunto in un rapporto di 1:1. Questo è necessario per compensare l'ossigeno mancante nel biochar per garantire la completa combustione nell'analizzatore elementare. - Inserire i campioni preparati nel campionatore automatico dell'analizzatore elementare.
- Aprire la valvola dell'ossigeno e dell'elio per la camera di combustione dell'analizzatore elementare.
- Avviare l'analisi quando il dispositivo ha raggiunto la temperatura specificata dal dispositivo. In questo caso, attendere fino a raggiungere la temperatura di 900 ° c.
- Calcolare le talpe di ogni elemento nello standard sulfonamide dal peso standard sulfonamide (passo 6,2), e il peso di 1 mole del rispettivo elemento.
- Calcolare la relazione tra le talee di C, H, S e N in sulfonamide, ottenuta dal passo 6,7 e le rispettive aree di picco.
- Sottrarre il contenuto di ceneri campione, ottenuto dal passaggio 3,7, dal peso totale del campione.
- Confrontare la rispettiva area di picco dell'elemento nello standard sulfonamide e il campione, e moltiplicare per la mole di ogni elemento in sulfonamide per ottenere la mole dell'elemento nel campione.
- Calcolare il peso di C, H, S e N nel campione moltiplicando la mole dell'elemento, ottenuta dal passo 6,10, con la rispettiva massa molare dell'elemento dalla tavola periodica.
- Calcolare il peso di ossigeno nel campione utilizzando la massa del campione privo di ceneri, ottenuta dal passo 6,9, e sottraendo il peso di C, H, N e S, ottenuto dal passaggio 6,11.
- Calcolare i rapporti molari H/C e O/C nella materia prima e nei campioni di biocarbone MAHC.
7. spettroscopia di emissione ottica a plasma accoppiato indotta
- Pesare 400 mg di materia prima secca o biocarbone MAHC e metterlo in un vaso di reazione di PTFE 50 mL con una spatola. Aggiungere 3 mL di 69% di acido nitrico e 9 mL di acido cloridrico 35%.
- Avvitare il tappo del recipiente di reazione in modo che la valvola di pressione nel tappo sia sullo stesso livello della tesa del tappo.
- Mettere i vasi di reazione dei campioni da analizzare nel forno a microonde e chiudere il forno.
- Programmare il programma di temperatura per la degradazione completa del materiale organico: rampa + 15,5 ° c min-1 a 200 ° c, tenere 30 min, raffreddare fino a 180 ° c, tenere premuto per 5 min. avviare il forno a microonde.
- Una volta completato il programma, rimuovere i vasi di reazione, consentire loro di raffreddare e riattivare. Quindi aprire i vasi sotto un armadio fumi dopo aver rilasciato la pressione all'interno.
- Versare i campioni in un cilindro a bulbo da 50 mL. Quindi sciacquare accuratamente il recipiente di reazione con acqua deionizzata due volte e trasferirla al cilindro della lampadina. Rifinire il cilindro al contrassegno 50 mL con acqua deionizzata due volte per garantire anche la diluizione di tutti i campioni.
- Filtrare il campione dal passaggio 7,6 con carta filtrante a maglie da 150 μm. Riempire il filtrato in provette centrifughe coniche da 50 mL.
- Inserire i campioni standard nell'autoiniettore dell'ICP-OES. I campioni standard sono delle concentrazioni conosciute (0,0001 ppm, 0,001 PPM, 0,1 ppm, 1 ppm 10 ppm, 20 ppm, 50 ppm) degli elementi da quantificare (CA, As, B, be, Fe, se, Zn, AG, al, BA, bi, CD, Co, CR, cu, GA, K, li , Mg, MN, MO, na, NI, PB, RB, SR, te, TL, V).
- Inserire i campioni nell'autoiniettore dell'ICP-OES ed eseguire l'analisi ICP-OES con gli stessi parametri.
- Dopo l'analisi ICP-OES, ottenere la concentrazione elementare dal software, calcolata automaticamente in mg/kg, in base alle curve di calibrazione ottenute da campioni standard nel passaggio 7,8.
- Calcolare la riduzione della concentrazione elementare nel biocarbone prodotto:
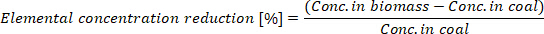
dove conc. in biomassa è la concentrazione elementare nella biomassa e conc. Nel carbone è la concentrazione elementare nel biocarbone.
8. misurare il pH dell'acqua di processo HTC
- Riempire ogni frazione liquida dal trattamento MAHC (fase 2,7) della materia prima e i tre biocarboni in quattro rispettivi Becher.
- Calibrare la sonda di pH con soluzioni standard.
- Misurare il pH della frazione liquida della materia prima e i tre biocarboni MAHC.
9. gascromatografia-spettrometria di massa
- Filtrare le frazioni liquide dal trattamento MAHC (passo 2,7) con 150 μm di carta filtrante mesh. Aggiungere 20 mL di metanolo a 1 mL delle frazioni liquide filtrate.
- Trasferire 200 μL in un flaconcino del campionatore automatico GC-MS e inserire il flaconcino nel campionatore automatico GC-MS.
- Diluire gli standard puri di furfurale e 5-methylfurfural (grado analitico) fino a 10-2, 10-3, 10-4, e 10-5 con metanolo.
- Inserire gli standard nel campionatore automatico GC-MS e analizzarli con i parametri: 1 μL di volume di iniezione a 230 ° c temperatura dell'iniettore e 1:40 Split; 5MS colonna non polare (tabella dei materiali) con lunghezza 15 m e spessore del film 0,25 mm; programma di temperatura 30 ° c, tenere 2 min, rampa di + 40 ° c/min a 250 ° c, tenere premuto 2 min; ionizzazione con 70 mV e MS detector in modalità di scansione con una gamma m/z di 35 − 400, ogni scansione in 0,3 s.
- Stabilire le curve di calibrazione per l'area di picco totale (TIC) e la concentrazione composta.
- Eseguire i campioni di fase liquida di HTC Biocoal preparati con gli stessi parametri analitici e identificare furfurale e 5-methylfurfural per mezzo del tempo di ritenzione dello standard e della corrispondenza dello spettro in una libreria di spettri.
- Determinare le concentrazioni di furfurale e 5-methylfurfural utilizzando la curva di calibrazione calcolata (passo 9,6) e inserendo le aree di picco del campione di furfurale e 5-metilfurfural.
10. statistiche
- Analizzare i dati con il test di Shapiro Wilks per la distribuzione normale.
- Utilizzare il test U Mann-Whitney per set di dati non distribuiti normalmente e il test t per insiemi di dati normalmente distribuiti per trovare differenze significative tra insiemi di dati.
Nota: se un set di dati è normalmente distribuito e l'altro no, utilizzare il test Mann-Whitney U.
Risultati
I risultati dell'analisi elementare hanno rivelato differenze tra il rapporto O/C-H/C del legno di salice e i biocarboni MAHC (Figura 1). La materia prima mostra rapporti O/C-H/C più elevati e una maggiore variazione dei valori. Il trattamento MAHC ha ridotto la variazione di valore dovuta all'omogeneizzazione nel reattore a microonde. La precisione del reattore a microonde ha permesso la differenziazione di tre stadi di degradazione. Il rapporto H/C è stat...
Discussione
Il MAHC permette la differenziazione delle fasi della degradazione chimica applicando diverse intensità di trattamento termico. Pertanto, è possibile valutare le interazioni tra la perdita di massa, il rapporto O/C-H/C, il valore di riscaldamento, la riduzione dei componenti in cenere, l'aumento del pH dell'acqua di processo e l'accumulo di furani nell'acqua di processo. Il vantaggio del metodo MAHC rispetto al metodo convenzionale del reattore HTC si basa sulla conduzione termica tramite microonde che penetrano l'inte...
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Gli autori amano ringraziare Christoph Warth, Michael Russ, Carola Lepski, Julian Tejada e il dottor Rainer Kirchhof per il loro supporto tecnico. Lo studio è stato finanziato dal BMBF (progetto BiCoLim-bio-combustibles limpios) con il numero di sovvenzione 01DN16036.
Materiali
| Name | Company | Catalog Number | Comments |
| 5MS non-polar cloumn | Thermo Fisher Scientific,Waltham, USA | TraceGOLD SQC | GCMS |
| 9µm polyvinylalcohol particle column | Methrom AG, Filderstadt, Germany | Metrosep A Supp 4 -250/4.0 | Ion chromatography |
| argon | Westfalen AG, Münster, Germany | UN 1006 | ICP-OES |
| calorimeter | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C6000 | higher and lower heating value |
| centrifuge | Andreas Hettich GmbH & Co.KG, Germany | Rotofix 32 A | |
| centrifuge mill | Retsch Technology GmbH, Haan, Germany | ZM 200 | |
| ceramic dishes | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | XX83.1 | Ash content |
| cutting mill | Fritsch GmbH, Markt Einersheim, Germany | pulverisette 19 | |
| D(+) Glucose | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | X997.1 | higher and lower heating value |
| elemental analyzer | elementar Analysesysteme GmbH, Langenselbold, Germany | varioMACRO cube | elemental analysis |
| exicator | DWK Life Sciences GmbH, Wertheim, Germany | DURAN DN300 | Ash content |
| GC-MS system | Thermo Fisher Scientific,Waltham, USA | Trace 1300 | GCMS |
| hydrochloric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | HN53.3 | ICP-OES |
| ICP OES | Spectro Analytical Instruments GmbH, Kleve, Germany | Spectro Blue-EOP- TI | ICP-OES |
| Ion chromatograph | Methrom GmbH&Co.KG, Filderstadt, Germany | 833 Basic IC plus | Ion chromatography |
| kiln dryer | Schellinger KG, Weingarten, Germany | ||
| kiln dryer | Schellinger KG, Weingarten, Germany | Ash content | |
| mesh filter paper | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | L874.1 | ICP-OES |
| microwave oven | Anton Paar GmbH, Graz, Austria | Multiwave Go | |
| muffel furnance | Carbolite Gero GmbH &Co.KG, Neuhausen, Germany | AAF 1100 | Ash content |
| nitric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | 4989.1 | ICP-OES |
| oxygen | Westfalen AG, Münster, Germany | UN 1072 | higher and lower heating value |
| pH-meter | ylem Analytics Germany Sales GmbH & Co. KG, Weilheim,Germany | pH 3310 | pH |
| sample bag | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C12a | higher and lower heating value |
| Standard Laboratory Vessels and Instruments | |||
| standard samples | Bernd Kraft GmbH, Duisburg, Germany | ICP-OES | |
| sulfonamite | elementar Analysesysteme GmbH, Langenselbold, Germany | SLBS4782 | elemental analysis |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | ICP-OES |
| tin foil | elementar Analysesysteme GmbH, Langenselbold, Germany | S12.01-0032 | elemental analysis |
| tungstenVIoxide | elementar Analysesysteme GmbH, Langenselbold, Germany | 11.02-0024 | elemental analysis |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ||
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | higher and lower heating value | |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ICP-OES |
Riferimenti
- Li, C., Zhao, Z. K., Cai, H., Wang, A., Zhang, T. Microwave-promoted conversion of concentrated fructose into 5-hydroxymethylfurfural in ionic liquids in the absence of catalysts. Biomass and Bioenergy. 35 (5), 2013-2017 (2011).
- Möller, M., Harnisch, F., Schröder, U. Microwave-assisted hydrothermal degradation of fructose and glucose in subcritical water. Biomass and Bioenergy. 39, 389-398 (2012).
- Guiotoku, M., Rambo, C. R., Hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. 63 (30), 2707-2709 (2009).
- Guiotoku, M., Rambo, C. R., hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. (63), 2707-2709 (2009).
- Kannan, S., Gariepy, Y., Raghavan, G. S. V. Optimization and characterization of hydrochar produced from microwave hydrothermal cabonization of fish waste. Waste Management. , 159-168 (2017).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted and conventional hydrothermal carbonization of lignocellulosic waste material: Comparison of the chemical and structural properties of the hydrochars. Journal of Analytical and Applied Pyrolysis. 118, 1-8 (2016).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted hydrothermal carbonization of rapeseed husk: A strategy for improving its solid fuel properties. Fuel Processing Technology. 149, 305-312 (2016).
- Chen, W. -. H., Ye, S. -. C., Sheen, H. -. K. Hydrothermal carbonization of sugarcane bagasse via wet torrefaction in association with microwave heating. Bioresource technology. 118, 195-203 (2012).
- Nizamuddin, S., et al. Upgradation of chemical, fuel, thermal, and structural properties of rice husk through microwave-assisted hydrothermal carbonization. Environmental science and pollution research international. 25 (18), 17529-17539 (2018).
- Nizamuddin, S., et al. An overview of microwave hydrothermal carbonization and microwave pyrolysis of biomass. Reviews in Environmental Science and Bio/Technology. 17 (4), 813-837 (2018).
- Dallinger, D., Kappe, C. O. Microwave-assisted synthesis in water as solvent. Chemical reviews. 107 (6), 2563-2591 (2007).
- Qi, X., Watanabe, M., Aida, T. M., Smith, J. R. L. Catalytic dehydration of fructose into 5-hydroxymethylfurfural by ion-exchange resin in mixed-aqueous system by microwave heating. Green Chemistry. 10 (7), 799 (2008).
- Nüchter, M., Ondruschka, B., Bonrath, W., Gum, A. Microwave assisted synthesis - a critical technology overview. Green Chem. 6 (3), 128-141 (2004).
- Schanche, J. -. S. Microwave synthesis solutions from personal chemistry. Molecular Diversity. 7 (2-4), 291-298 (2003).
- Kappe, C. O. Controlled microwave heating in modern organic synthesis. Angewandte Chemie (International ed. in English). 43 (46), 6250-6284 (2004).
- Gronnow, M. J., White, R. J., Clark, J. H., Macquarrie, D. J. Energy Efficiency in Chemical Reactions: A Comparative Study of Different Reaction Techniques. Organic Process Research & Development. 9 (4), 516-518 (2005).
- Kruse, A., Dahmen, N. Hydrothermal biomass conversion: Quo vadis?. The Journal of Supercritical Fluids. 134, 114-123 (2018).
- Reza, M. T., et al. Hydrothermal Carbonization of Biomass for Energy and Crop Production. Applied Bioenergy. 1 (1), (2014).
- Libra, J. A., et al. Hydrothermal carbonization of biomass residuals: a comparative review of the chemistry, processes and applications of wet and dry pyrolysis. Biofuels. 2 (1), 71-106 (2011).
- Reza, M. T., Uddin, M. H., Lynam, J. G., Hoekman, S. K., Coronella, C. J. Hydrothermal carbonization of loblolly pine: reaction chemistry and water balance. Biomass Conversion and Biorefinery. 4 (4), 311-321 (2014).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. 4 (2), 160-177 (2010).
- Kruse, A., Funke, A., Titirici, M. -. M. Hydrothermal conversion of biomass to fuels and energetic materials. Current opinion in chemical biology. 17 (3), 515-521 (2013).
- Reza, M. T., Lynam, J. G., Uddin, M. H., Coronella, C. J. Hydrothermal carbonization: Fate of inorganics. Biomass and Bioenergy. 49, 86-94 (2013).
- Zhang, D., et al. Comparison study on fuel properties of hydrochars produced from corn stalk and corn stalk digestate. Energy. 165, 527-536 (2018).
- Huang, Y. -. B., Yang, Z., Dai, J. -. J., Guo, Q. -. X., Fu, Y. Production of high quality fuels from lignocellulose-derived chemicals: a convenient C-C bond formation of furfural, 5-methylfurfural and aromatic aldehyde. RSC Advances. 2 (30), 11211 (2012).
- Van de Vyver, S., Geboers, J., Jacobs, P. A., Sels, B. F. Recent Advances in the Catalytic Conversion of Cellulose. ChemCatChem. 3 (1), 82-94 (2011).
- Delidovich, I., Leonhard, K., Palkovits, R. Cellulose and hemicellulose valorisation: an integrated challenge of catalysis and reaction engineering. Energy & Environmental Science. 7 (9), 2803 (2014).
- Sevilla, M., Fuertes, A. B. The production of carbon materials by hydrothermal carbonization of cellulose. Carbon. 47 (9), 2281-2289 (2009).
- Yao, Z., Ma, X. Characteristics of co-hydrothermal carbonization on polyvinyl chloride wastes with bamboo. Bioresource technology. 247, 302-309 (2018).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. (4), 160-177 (2010).
- Liu, Z., Balasubramanian, R. Upgrading of waste biomass by hydrothermal carbonization (HTC) and low temperature pyrolysis (LTP): A comparative evaluation. Applied Energy. 114, 857-864 (2014).
- Khalsa, J., Döhling, F., Berger, F. Foliage and Grass as Fuel Pellets-Small Scale Combustion of Washed and Mechanically Leached Biomass. Energies. 9 (5), 361 (2016).
- Saddawi, A., Jones, J. M., Williams, A., Le Coeur, C. Commodity Fuels from Biomass through Pretreatment and Torrefaction: Effects of Mineral Content on Torrefied Fuel Characteristics and Quality. Energy & Fuels. 26 (11), 6466-6474 (2012).
- Kaltschmitt, M., Hartmann, H., Hofbauer, H. . Energie aus Biomasse: Grundlagen, Techniken und Verfahren. , (2016).
- Fengel, D., Wegener, G. . Wood: Chemistry, Ultrastructure, Reactions. , (1989).
- Obernberger, I., Thek, G. Physical characterisation and chemical composition of densified biomass fuels with regard to their combustion behaviour. Biomass and Bioenergy. 27 (6), 653-669 (2004).
- Kenney, W. A., Sennerby-Forsse, L., Layton, P. A review of biomass quality research relevant to the use of poplar and willow for energy conversion. Biomass. 21 (3), 163-188 (1990).
- Tharakan, P. J., Volk, T. A., Abrahamson, L. P., White, E. H. Energy feedstock characteristics of willow and hybrid poplar clones at harvest age. Biomass and Bioenergy. 25 (6), 571-580 (2003).
- Liu, Z., Quek, A., Balasubramanian, R. Preparation and characterization of fuel pellets from woody biomass, agro-residues and their corresponding hydrochars. Applied Energy. , 1315-1322 (2014).
- Technischen Komitee ISO/TC 238. . "Solid biofuels" und Technisches Komitee CEN/TC 335 "Biogene Festbrennstoffe" Solid biofuels - Determination of calorific value (ISO 18125:2017); German version EN ISO 18125:2017. , (2017).
- Kambo, H. S., Dutta, A. A comparative review of biochar and hydrochar in terms of production, physico-chemical properties and applications. Renewable and Sustainable Energy Reviews. 45, 359-378 (2015).
- Knappe, V., et al. Low temperature microwave assisted hydrothermal carbonization (MAHC) reduces combustion emission precursors in short rotation coppice willow wood. Journal of Analytical and Applied Pyrolysis. 134, 162-166 (2018).
- Liu, Z., Quek, A., Kent Hoekman, S., Balasubramanian, R. Production of solid biochar fuel from waste biomass by hydrothermal carbonization. Fuel. 103, 943-949 (2013).
- Hoekman, S. K., Broch, A., Robbins, C., Zielinska, B., Felix, L. Hydrothermal carbonization (HTC) of selected woody and herbaceous biomass feedstocks. Biomass Conversion and Biorefinery. 3 (2), 113-126 (2013).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon