Method Article
Caracterización de proteínas celulares con oxidación fotoquímica rápida en las células de proteínas
En este artículo
Resumen
Aquí, caracterizamos la estructura de proteínas y los sitios de interacción en células vivas utilizando una técnica de huella proteica llamada oxidación fotoquímica rápida en las células de proteínas (IC-FPOP).
Resumen
La rápida oxidación fotoquímica de proteínas (FPOP) es un método de huella de proteína sorteradical utilizado para caracterizar la estructura e interacciones proteicas. FPOP utiliza un láser excimer de 248 nm para fotolizar el peróxido de hidrógeno produciendo radicales hidroxilo. Estos radicales oxidativamente modifican las cadenas laterales expuestas solventes de 19 de los 20 aminoácidos. Recientemente, este método se ha utilizado en células vivas (IC-FPOP) para estudiar las interacciones proteicas en su entorno nativo. El estudio de proteínas en las células explica el hacinamiento intermolecular y varias interacciones proteicas que se interrumpen para los estudios in vitro. Se diseñó un sistema de flujo de celda única personalizado para reducir la agregación de celdas y la obstrucción durante IC-FPOP. Este sistema de flujo enfoca las células más allá del láser excimer individualmente, asegurando así una irradiación consistente. Al comparar el grado de oxidación producido a partir de FPOP con la accesibilidad solvente de la proteína calculada a partir de una estructura cristalina, IC-FPOP puede sondear con precisión las cadenas laterales de proteínas accesibles al disolvente.
Introducción
La huella de proteína sión de radicales hidroxilo (HRPF) es un método que sondas la accesibilidad solvente de una proteína a través de modificaciones covalentes producidas a partir de radicales hidroxilo. Cuando la estructura proteica o las interacciones proteicas cambian, alterará la exposición a disolventes de aminoácidos, alterando así el grado de modificación de los residuos. Con HRPF, las interacciones proteicas1,2,3 y los cambios de conformación proteica4,5,6 han sido interrogados con éxito in vitro. Existen varios métodos que generan radicales hidroxilo para experimentos de HRPF, uno de ellos es una rápida oxidación fotoquímica de proteínas (FPOP). FPOP fue desarrollado por Hambly y Gross en 2005 y utiliza un láser excimer de 248 nm para producir radicales hidroxilo a través de la fotólisis del peróxido de hidrógeno (H2O2)7.
Recientemente, Espino y otros ampliaron el uso de FPOP para sondear la estructura proteica en células vivas, un método llamado FPOP en células (IC-FPOP)8. A diferencia de los estudios in vitro, el estudio de las proteínas en las células explica el hacinamiento molecular junto con varias interacciones proteicas que potencialmente podrían influir en la estructura. Además, presenta la ventaja de proporcionar una instantánea del proteome completo que potencialmente proporciona información estructural de numerosos sistemas a la vez para realizar una biología estructural amplia del proteome. Además, esta técnica es ideal para proteínas que son difíciles de estudiar in vitro, como las proteínas de membrana.
Los estudios iniciales de IC-FPOP sondearon con éxito 105 proteínas que varían en abundancia de proteínas y localización celular. Para mejorar el método IC-FPOP, Rinas y otros desarrollaron un sistema de microflujo para el flujo de una sola célula9. La mejora del sistema de flujo original limita la agregación de celdas y aumenta el H2O2 disponible disponible para la irradiación. En el sistema de flujo inicial, las células que se aglutinan en el tubo de sílice dieron lugar a obstrucciones e irradiación desigual. La incorporación de dos corrientes de un tampón de vaina enfoca hidrodinámicamente las células, lo que les permite fluir individualmente más allá del láser. La incorporación de una jeringa separada para el H2O2 permite un tiempo de exposición más controlado y optimizable que permite concentraciones más altas de H2O2 sin efectos adversos. Además, limitar el tiempo de incubación limita la descomposición de H2O2 por catalasa endógena. Al incorporar este nuevo sistema de flujo, el número detectado de proteínas con una modificación FPOP aumentó 13 veces, ampliando así las capacidades de este método para sondear una multitud de proteínas en células vivas. En este protocolo se describe un experimento general IC-FPOP centrado en el montaje del sistema de flujo IC-FPOP.
Protocolo
1. Configurar el sistema de flujo IC-FPOP
- Para comenzar el montaje del sistema de flujo, corte la sílice fusionada usando una piedra de escote a medida. El sistema de flujo IC-FPOP requiere cuatro sílice fusionada de 12 cm y una de 17 cm con un diámetro interior (ID) de 450 m y diámetro exterior (OD) de 670 m, dos de 24 cm y uno de 40 cm con un ID de 75 m y un OD de 360 m , y finalmente dos 57 cm con un ID de 150 m y una DoT de 360 m.
NOTA: Al cortar el tubo de sílice, raspe suavemente el recubrimiento de poliimida y doble para obtener el corte más limpio. Compruebe que se trata de un corte recto (esto es necesario para garantizar que no se formen bloqueos o fugas). - Configure 15 conexiones con manguitos nano-apretados (0.0155" ID X 1/16" OD para tubos de sílice OD de 360 m y 0.027" ID X 1/16" OD para el tubo de sílice OD de 670 m) con tuerca súper sin brida PEEK 1/4-28 de fondo plano para 1/16" OD y hirule super flangeless w/ SST Tefzel (ETFE), 1/4-28 fondo plano, para 1/16" OD. Construir conexiones según el protocolo del fabricante(Figura 1).
- Coloque 6 imanes cilíndricos pequeños en una jeringa de 500 ml. Llene esta jeringa junto con otra jeringa de 500 ml y dos jeringas de 5 ml con tampón y retire el aire. Posición en la bomba de jeringa como se muestra en la Figura 2A.
NOTA: Las jeringas de 5 ml son más grandes que las jeringas de 500 ml, por lo que se necesita un espaciador para apretar todas las jeringas simultáneamente en su lugar(Figura 2B). - Apriete el tapón de la bomba de la jeringa para que la jeringa de la célula tenga aproximadamente 50 ml cuando el motor se detenga. Esto dejará espacio para los agitadores magnéticos. (Figura 2C-D).
ADVERTENCIA: Si la bomba de la jeringa ejerce presión sobre los imanes, atascarán la jeringa y provocarán que la jeringa se rompa. - Con un adaptador Luer, conecte una válvula manual a cada jeringa. Montar el tubo de sílice como se muestra en la Figura 3.
NOTA: Enrosque la línea con las celdas + H2O2 hasta el otro lado. A continuación, insértelo en el tubo de sílice id de 450 m. Los amortiguadores de vaina de la jeringa de 5 ml fluirán a una velocidad más rápida que las células y H2O2. Con los amortiguadores de vaina en ambos lados, las células se enfocarán hidrodinámicamente en una sola línea para la irradiación. - Sistema de flujo de posición junto al láser. Usando un encendedor, queme el recubrimiento de sílice en el tubo id de 450 m para hacer una ventana para la irradiación láser.
- Coloque un agitador magnético por encima de la jeringa celular que contiene los seis imanes.
- Ajuste la bomba de la jeringa a 492,4 l/min para un caudal final de 1.083,3 l/min. Tampón de flujo a través del sistema tres veces para vaciar el sistema y comprobar si hay fugas.
- Enfoca el láser excimer en el tubo de sílice con una lente convexa. Una vez enfocado, pruebe la ventana de irradiación colocando un pequeño pedazo de papel detrás del tubo de sílice y encienda el láser. Mida la región quemada por la irradiación. Calcule la frecuencia láser necesaria utilizando la ventana de irradiación y el caudal para obtener una fracción de exclusión de cero.
NOTA: La energía láser recomendada para un experimento IC-FPOP es de 120 mJ. Para obtener una fracción de exclusión de 0 con una ventana de irradiación de 2,58 mm y un caudal de 1083,3 l/min, la frecuencia debe ser 44. A continuación se muestran las ecuaciones necesarias para calcular la frecuencia del láser si se conoce la ventana de irradiación, el caudal y la fracción de exclusión.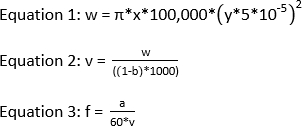
donde w es el volumen en nL, x es el ancho de punto láser en mm, y es el ID de tubo de sílice en ám, v es el volumen total en L, b es la fracción de exclusión, a es el caudal en l/min, y f es la frecuencia en Hz.
2. Haga temple y H2O2
- Hacer temple que contenga 100 mM N-tert-Butyl-alfa-fenilnitrone (PBN) y 100 mM N,N'-dimetiltiourea (DMTU). Aliquot 11 ml de temple para cada muestra en un tubo cónico de 50 ml.
- Diluir H2O2 a 200 mM. Cada muestra requiere 500 ml de H2O2.
NOTA: El temple se puede hacer el día anterior y almacenarse a 4 oC durante la noche, protegido de la luz. H2O2 debe refrescarse el día de la experimentación.
3. Recoger celdas
- Cultivar células en un matraz T175 a aproximadamente 70-90% de confluencia.
- Retire el soporte y enjuague con tampón.
NOTA: Los búferes típicos a utilizar son la solución salina con fosfato (DPBS) de grado de cultivo celular de Dulbecco o la solución salina equilibrada (HBSS) de Hank. - Separe las células usando trippsin-EDTA o con un rascador.
- Una vez desasociada resuspend en 10 mL de buffer y cuenta las celdas.
- Gire hacia abajo, quite el buffer y la trippsin-EDTA, y resuspende para hacer 2 x 106 células/mL.
- Aliquot 500 l de las células por muestra.
NOTA: Para cada condición, haga un mínimo de 3 muestras láser y 3 sin controles láser.
4. Realización de IC-FPOP
- Llene las dos jeringas de 5 ml con tampón, la jeringa de 500 ml que contiene los imanes con las células y la jeringa final de 500 ml con H2O2. Encienda el agitador magnético.
- Espiga en 220 l de dimetil sulfóxido (DMSO) a una alícuota de temple, mezcle suavemente y coloque detrás del sistema de flujo para recoger muestras irradiadas. La adición de DMSO inhibirá la sulfóxido de metionina endógena reductasa.
- Encienda el láser, espere 7 s, y luego encienda el sistema de flujo.
- Una vez que la muestra termine de fluir, apague el láser y mezcle suavemente el temple con la muestra recogida. Coloque esto a un lado durante los pasos 4.5 y 4.6.
- Llene las cuatro jeringas con el búfer en el que se suspenden las células y fluya a través del sistema de flujo.
- Después de que el sistema termine de enjuagar, repita los pasos 4.1 y 4.2. Inicie el flujo sin irradiación. Este es el no control láser para tener en cuenta la oxidación de fondo en las células.
- Mientras se ejecuta la siguiente muestra, gire hacia abajo la muestra anterior a 450-800 x g durante 5 min, retire el disolvente y vuelva a suspender en 100 l de un tampón de lisis celular como tampón de ensayo de radioinmunoprecipitación (RIPA).
- Transfiera la muestra a un tubo de microcentrífuga y congele el flash en nitrógeno líquido.
- Cuando todas las muestras hayan terminado de funcionar, desmonte el sistema de flujo para su limpieza. Deseche el tubo de sílice usado y limpie todas las demás conexiones sonicando durante 1 h en agua al 50%: 50% de metanol. Limpie las jeringas según las instrucciones del fabricante.
5. Digest
- Digerir todo el lisado celular. Comience descongelando las muestras y caliente a 95oC durante 10 min.
- Después de calentar, enfríe el lisado sobre hielo durante 15 minutos.
- Añadir 25 unidades de nucleasa para digerir EL ADN y el ARN e incubar en la habitación templada durante 15 min.
- Esgire muestras utilizando una centrífuga de mesa a 16.000 x g durante 10 min a 4 oC.
- Recoja el sobrenadante y transfiéralo a un tubo de microcentrífuga limpio.
- Compruebe la concentración de proteínas utilizando un kit de ensayo de proteínas.
- Transfiera 20-100 g de muestra a un tubo de microcentrífuga limpio y lleve a 100 ol.
- Reduzca las muestras con ditiloitotol de 20 mM (TDT) a 50 oC durante 45 min.
- Enfríe las muestras a temperatura ambiente durante 15 min.
- Alquilato con yodoacetamida de 20 mM (IAA) a temperatura ambiente durante 20 min protegido de la luz.
- Añadir acetona pre-enfriada en una proteína de proporción 1:4: acetona. Mezclar las muestras y colocar las muestras en -20 oC durante la noche.
- A la mañana siguiente, espíe muestras a 16.000 x g durante 10 min a 4oC.
- Retire el sobrenadante y agregue 50 s de acetona pre-enfriada al 90%. Mezclar las muestras y girar hacia abajo a 16.000 x g durante 5 min a 4 oC.
- Retire la acetona y deje que las muestras se sequen dejando las tapas de la microcentrífuga abiertas con una toallita libre de pelusas que cubra la parte superior. Después de que las muestras se hayan secado, resuspenda el pellet de proteína con 10 mM Tris buffer pH 8.
- Resuspenda 20 g de tripsina en 40 ml de 10 mM Tris buffer pH 8. Añadir 2 g de tripsina (masa: relación de masa de 1 trypsin: 50 muestra). Incubar muestras a 37oC durante la noche.
- A la mañana siguiente comprobar la concentración de péptidos utilizando un ensayo de péptido. Después de eliminar la muestra para el ensayo de péptidos, atemple la digestión de la trippsina añadiendo ácido fórmico a las muestras (la concentración final es del 5% de ácido fórmico).
- Una vez determinada la concentración final del péptido, transfiera 10 g de cada muestra a un tubo de microcentrífuga limpio. Esto garantiza que se analice la misma cantidad de cada muestra. Seque la muestra con una centrífuga al vacío. Una vez secado resuspend con 20 l de espectrometría de masas grado 0.1% ácido fórmico. Transfiera muestras a viales de muestreador automático.
6. Cromatografía líquida-Espectrometría de masas tándem
- Para localizar las modificaciones FPOP, analice el caso de celda digerida mediante el análisis LC-MS/MS.
- Utilizar fases móviles de ácido fórmico al 0,1% en agua (A) y 0,1% de ácido fórmico en acetonitrilo (B).
- Cargue una columna de captura de 0,5 g de muestra en una columna de captura de 180 m x 20 mm C18 (5 m y 100 o) y la muestra de lavado con 99% (A) y 1% (B) durante 15 min.
- Utilizando una columna analítica de 75 m x 30 cm C18 (5 m y 125 o), ejecute el método de separación analítica con un caudal de 0,300 l/min a partir del 3% (B) durante un minuto y, a continuación, rampa al 10% (B) de 1-2 min. Siguiente rampa a 45% (B) de 2-100 min luego 100% (B) de 100-110 min. Limpie la columna sosteniendo al 100% (B) de 110-115 min. Reacondicione la columna reduciendo a 3% (B) de 115-116 min y mantenga a 3% (B) de 116-130 min.
- Establezca el método de adquisición de MS para que tenga una resolución de 60.000 con un rango de exploración m/z de 375-1500. Establezca el objetivo de control de ganancia automático (AGC) en 5,0 x 105 con un tiempo de inyección máximo de 50 ms.
- Durante la adquisición de EM, seleccione los iones precursores con estados de carga 2-6 para el aislamiento a través de la adquisición dependiente de datos (DDA) con una ventana de aislamiento de 1,2 m/z y un tiempo de ciclo de 4 s. Seleccione los péptidos con un umbral de intensidad de 5,0 x 104 para la activación de HCD con una energía normalizada establecida en 32%. Excluir los péptidos después de la adquisición de MS/MS para 60 s. Establezca la resolución MS/MS en 15.000 con una meta AGC de 5,0 x 104 y un tiempo máximo de inyección de 35 ms.
7. Procesamiento de datos
- Busque los archivos RAW en un software de análisis de proteínas disponible contra una base de datos de proteínas relevante y la enzima de resumen relevante. Aquí, utilice la base de datos Swiss-Prot Homo Sapiens y la trippsina.
- Establezca la masa precursora para buscar entre 350 y 5.000 Da y una tolerancia de masa de 10 ppm. Puede haber como máximo 1 sitio de escote perdido con una longitud de péptido entre 6 y 144 residuos. Estas limitaciones facilitan la búsqueda de bases de datos.
- Establezca la tolerancia de masa máxima de los iones de fragmento según 0,02 Da con el carbamidometil (+57.021) como modificación estática y todas las modificaciones FPOP de 17 aminoácidos como modificación dinámica(la Figura 4 es un ejemplo del flujo de trabajo de análisis de proteínas utilizado para detectar modificaciones FPOP).
NOTA: Las modificaciones de FPOP en la serina y la trionina no se incluyen en la búsqueda debido a su menor reactividad con radicales hidroxilo. - Busque con una base de datos de señuelos con una tasa de descubrimiento falsa del 1% y el 5%.
- Una vez que los archivos han terminado de buscar, calcule la extensión de la modificación de FPOP. Abra Proteome Discoverer 2.2, secuencia de exportación, ubicaciones de modificación, adhesión de proteínas, archivo de espectro, abundancia de precursores e información de tiempo de retención. Calcular la extensión de la modificación a partir de la ecuación 4:

El área EIC modificada es el área cromatográfica de un péptido específico con una modificación de radical hidroxilo. El área EIC es el área cromatográfica total de las áreas modificadas y no modificadas de ese péptido específico. El grado de oxidación se calcula en las muestras con y sin irradiación. La muestra que omite la irradiación (control) explica cualquier oxidación de fondo que podría haber estado presente en las células antes y después de la exposición a H2O2. Los controles se restan de las muestras de irradiación para ayudar a aislar las modificaciones específicas de FPOP.
Resultados
IC-FPOP es un método de huella para interrogar las interacciones proteicas en células vivas. En el sistema de flujo IC-FPOP, el tiempo de exposición H2O2 se limita a aproximadamente 3 s, lo que garantiza concentraciones más altas de H2O2 sin consecuencias perjudiciales para las células. El sistema de flujo también incorpora dos corrientes de tampón de vaina, que enfoca hidrodinámicamente las células al centro del tubo produciendo un solo flujo de células para ser irradiadas uniformemente(Figura 5)9. Las imágenes de fluorescencia de imágenes apiladas YZ ortogonales(Figura 5A)muestran una separación clara del tampón de vaina (que contiene un fluoróforo FITC) de la solución celular (que contiene un fluoróforo TMRM). Para enfatizar esta separación, la Figura 5B y la Figura 5C muestran mapas de calor promedio tridimensionales de la solución de búfer de vaina o la solución celular, lo que ilustra una mezcla mínima de las dos soluciones.
El uso del sistema de flujo de una sola célula aumenta el número de proteínas modificadas oxidativamente en 13 veces(Figura 6A)9. En este método, las proteínas en muchos de los compartimentos celulares están etiquetadas con proteínas de membrana, proteínas citoplasmáticas y proteínas dentro del núcleo siendo el más frecuente8,9. Para garantizar que las proteínas se modificaran dentro de las células intactas, se realizaron imágenes fluorescentes de las células tratadas con CellROX tras el tratamiento y la irradiación de H2O2 (Figura 6B)8. La estabilidad de las células a lo largo del proceso de etiquetado confirma aún más la eficacia de IC-FPOP para sondear proteínas en su entorno celular nativo. Mediante el uso de espectrometría de masas tándem, estas modificaciones se pueden localizar a aminoácidos específicos en una proteína. La Figura 7 representa una modificación que tiene lugar durante IC-FPOP junto con su cromatograma iónico extraído. El desplazamiento observado en el cromatograma iónico extraído se traduce en el cambio en la hidrofobicidad causado por la metionina oxidada en el péptido modificado.
Para comprobar si la sonda de modificaciones FPOP de la sonda de accesibilidad solvente dentro de las células, en la célula se comparó la actina etiquetada en las células con un estudio de huella in vitro y varias estructuras cristalinas de actina (Figura 8)8. La actina etiquetada en la célula está representada en la Figura 8A muestra extensiones comparables de oxidación del estudio in vitro realizado por Guan et al.10 (Figura 8B),la actina final tiene una accesibilidad solvente similar para estudios tanto en la célula como en los in vitro. Para confirmar aún más que IC-FPOP estaba sondeando la accesibilidad solvente de la actina, el alcance de las modificaciones de FPOP se comparó con la accesibilidad solvente de los residuos etiquetados calculados a partir de dos estructuras cristalinas de actina(Figura 8C). Esta correlación demuestra que IC-FPOP sondea la accesibilidad solvente del pozo de proteína monomérica.

Figura 1: Cómo construir correctamente los férulos. (A) Coloque las férulas, el tubo de sílice y el manguito antes de apretar. (B) Apriete todos los componentes juntos. (C) El producto final producirá una férula que se ha apretado en el manguito. Haga clic aquí para ver una versión más grande de esta figura.

Figura 2: Configuración del sistema de flujo IC-FPOP. (A) Imagen de un sistema de flujo IC-FPOP completamente montado situado junto al láser. (B) Ejemplo de un espaciador necesario para aumentar el diámetro exterior de las jeringas de 500 ml para apretar con éxito todas las jeringas juntas. (C) Imágenes representativas que muestren el espacio necesario para los agitadores magnéticos. (D) Los taponadores son necesarios para detener la bomba de la jeringa sin romper las jeringas. Haga clic aquí para ver una versión más grande de esta figura.
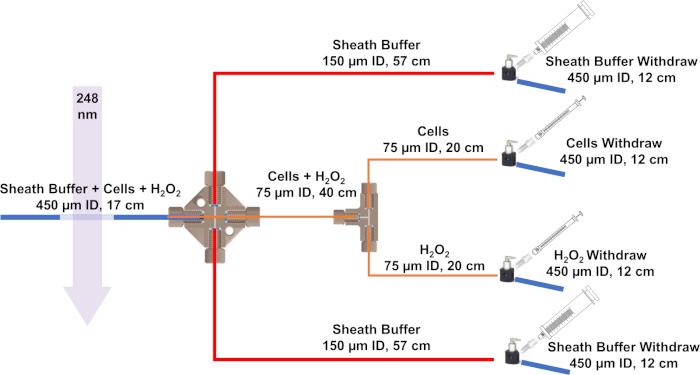
Figura 3: Esquema del sistema de flujo desarrollado para IC-FPOP. Las líneas azules representan tubos de sílice con un ID de 450 m y 670 m de DoL, las líneas rojas tienen un ID de 150 m y un OD de 360 m, y las líneas naranjas tienen un ID de 75 m y un OD de 360 m. Haga clic aquí para ver una versión más grande de esta figura.

Figura 4: Software de análisis de proteínas utilizado para detectar modificaciones FPOP. Un flujo de trabajo típico con las modificaciones correspondientes buscadas en cada nodo. Haga clic aquí para ver una versión más grande de esta figura.
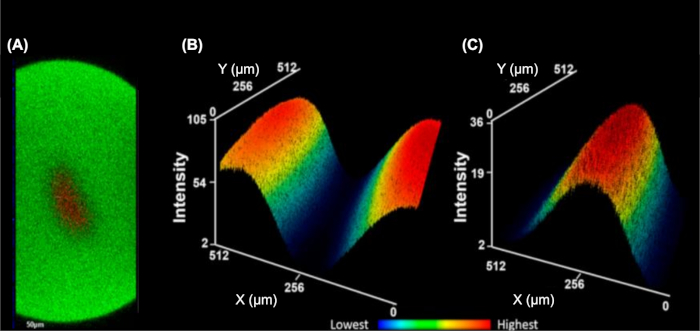
Figura 5: El sistema de flujo de una sola célula enfoca hidrodinámicamente las células en una sola corriente. (A) Pila yZ ortogonal que ilustra el enfoque 3D del analito celular (rojo, fluoróforo TMRM) rodeado por el búfer de vaina (verde, fluoróforo FITC). Mapa de calor de intensidad media tridimensional del búfer de vaina (B) y analito celular (C). Las intensidades más bajas son azules y las más altas son rojas (B-C). Esta figura ha sido modificada de Rinas et al.9Haga clic aquí para ver una versión más grande de esta figura.
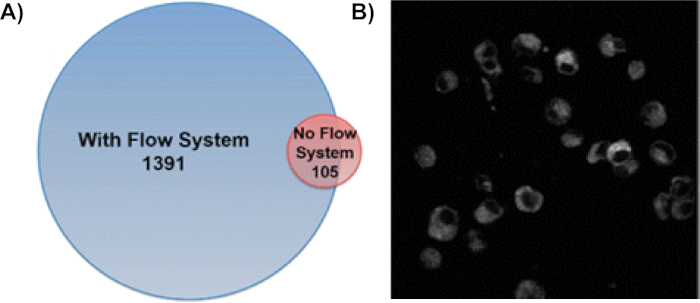
Figura 6: La utilización del sistema de flujo IC-FPOP aumenta drásticamente las proteínas modificadas por FPOP en las células de ingesta. (A) Comparación de proteínas oxidadas identificadas con y sin el sistema de flujo. El sistema de flujo identificó 1391 proteínas modificadas FPOP, mientras que sólo 105 proteínas fueron identificadas sin sistema de flujo con una superposición de 58 proteínas modificadas. Esta cifra ha sido modificada de Rinas et al.9 (B) Imágenes de fluorescencia de células tratadas con CellROX después de IC-FPOP muestran que las células siguen intactas después del etiquetado oxidativo. Las células fueron fotografiadas usando un microscopio multifota Olympus Fluoview FV1000 MPE a 665 nm. La imagen que se muestra es un solo sector. Esta figura ha sido modificada de Espino et al.8Haga clic aquí para ver una versión más grande de esta figura.

Figura 7: Ejemplos de espectros MS/MS en tándem que tienen lugar durante IC-FPOP. Espectros de iones de producto (MS/MS) de un péptido(A) no modificado y una oxidación(B)detectada en el residuo M8 encontrado en ese péptido. Un EIC representativo del péptido no modificado (C) y (D) péptido modificado. Haga clic aquí para ver una versión más grande de esta figura.

Figura 8: IC-FPOP es eficaz para sondear la accesibilidad a disolventes de proteínas. (A) Extensión de modificación de los 9 péptidos modificados oxidativamente de actina. Los valores se muestran como promedios más y menos desviación estándar (n a 3). (B) Modificación de péptidos de actina oxidados in vitro por radiolisis sincrotrón de Guan et al.10 (C) Correlación de residuos Modificaciones FPOP con SASA en los estados estrechos (triángulos, línea de tendencia discontinua) y abierto (círculos, línea de tendencia sólida) de actina. Esta figura ha sido modificada de Espino et al.8Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Se han desarrollado varias técnicas basadas en espectrometría de masas para estudiar la estructura de proteínas y los complejos de proteínas-ligand de una manera a lo ancho del proteome en células enteras o lisados celulares. Estas técnicas incluyen, entre otras, la estabilidad de las proteínas a partir de la tasa de oxidación (SPROX), el perfilado de proteome térmico (TPP), la reticulación química (XL-MS) y la huella de proteínas radicales hidroxilo (HRPF). Cada técnica tiene limitaciones y ventajas únicas en comparación entre sí, que han sido ampliamente revisadas12. Cada uno de estos métodos se han utilizado para la biología estructural amplia proteome para dilucidar la estructura de proteínas y, en última instancia, funcionar dentro del entorno celular complejo. IC-FPOP es una técnica DE HRPF que utiliza radicales hidroxilo para modificar oxidativamente las cadenas laterales expuestas a disolventes de aminoácidos, sondeando la estructura proteica y las interacciones proteína-ligand dentro de las células viables13. IC-FPOP es una mejora a la HRPF inicial en células vivas que utilizaron la química de Fenton para generar radicales en la escala de tiempo de minutos14. En este estudio, los cambios estructurales en una proteína de membrana integral en respuesta a la reducción del pH o la fuerza iónica del tampón se caracterizaron con éxito con una buena cobertura de oxidación a través de la proteína. En comparación con la química de Fenton, IC-FPOP es mucho más rápido, modificando las proteínas en la escala temporal de microsegundos, lo que permite estudiar la conformación de proteínas nativas.
Una prueba clave para IC-FPOP es confirmar la viabilidad de las células después de la exposición a H2O2. Usando una línea de mezcla de 40 cm, las células se incuban en H2O2 durante aproximadamente 3 s antes de la irradiación. Este tiempo se puede ajustar cambiando la longitud de este tubo de sílice. Cabe destacar que aunque el uso de trypan azul para probar la viabilidad celular muestra la integridad de las células se sostienen después de la incubación de H2O2, las células podrían estar bajo vías de señalización que afectan al estrés que interactúan con H2O2. Afortunadamente, el corto tiempo de incubación es más rápido que la síntesis de proteínas proporcionando confianza las proteínas presentes no son inducidas por H2O2.
El siguiente paso importante es confirmar el montaje adecuado del sistema de flujo. Una vez montado, asegúrese de que no haya fugas después de vaciar el sistema con el búfer deseado. Si hay fugas, asegúrese de que el tubo de sílice se haya cortado correctamente y esté al ras contra la férula para hacer un sello adecuado una vez apretado. Todas las piezas están apretadas a mano, por lo que no se necesarian herramientas. Durante cada experimento IC-FPOP, asegúrese de que los agitadores magnéticos de la jeringa celular permanezcan en movimiento. Esta pequeña agitación limita el número de células que se asientan en la parte inferior de la jeringa, pero no es lo suficientemente dura como para cortar las células. Después de una carrera, quedan aproximadamente 50 ml de células en la jeringa. Asegúrese siempre de diluir esto con un paso de encuadernparamiento para limitar el número de células que se transportan al siguiente experimento. Se recomienda utilizar una jeringa de células nuevas si se están comparando varios tratamientos celulares. También es importante seleccionar un búfer adecuado para las celdas que se están probando. Algunos tampones acalmtan el radical hidroxilo, lo que lleva a menos modificaciones en las proteínas. Xu y otros han demostrado que algunos buffers comúnmente utilizados disminuyen la vida útil del radical hidroxilo11. DPBS y HBSS son búferes comunes utilizados para experimentos IC-FPOP.
Siguiendo IC-FPOP, optimice el protocolo de digestión en función de los parámetros necesarios. Dado que el FPOP produce modificaciones covalentes irreversibles, hay un amplio tiempo disponible para una digestión y limpieza a fondo sin perder la cobertura de etiquetado. Pruebe y normalice siempre la concentración de proteínas para que las concentraciones uniformes de péptidos se carguen para la espectrometría de masas en tándem. Por último, tenga en cuenta que no se puede realizar una inmunoprecipitación junto con IC-FPOP. Si una modificación FPOP se dirige a la región de interacción, se reducirá la afinidad del anticuerpo. Para ayudar a aumentar la identificación de las modificaciones FPOP, los pasos de separación cromatográfica 2D han demostrado triplicar el número de péptidos oxidados detectados15.
Un desafío de cualquier experimento FPOP es el complicado nivel de análisis de datos debido a los posibles productos de oxidación que pueden surgir. Esto es cierto tanto en la célula como in vitro, pero se incrementa drásticamente con la complejidad añadida de analizar los lysates celulares. Con una mayor optimización de IC-FPOP surgen más proteínas con mayores coberturas de modificación, lo que hace que el análisis sea más arduo. La cantidad de cizallamiento de datos generados a partir de un único experimento IC-FPOP limita el uso de la validación manual, lo que hace que los investigadores dependan más del software. Debido a esto, Rinas y otros desarrollaron una estrategia de cuantificación para HRPF utilizando Proteome Discoverer (PD)16. Este método utiliza un flujo de trabajo de nodo de búsqueda múltiple en PD combinado con una plataforma cuantitativa en una hoja de cálculo. Se están realizando nuevas mejoras en la plataforma IC-FPOP para aumentar el número de péptidos identificados con modificaciones de FPOP, junto con una mayor reproducibilidad y precisión de cuantificación.
Divulgaciones
Lisa Jones es una inventora en el montaje de flujo para la patente de celdas (número de publicación: 20180079998).
Agradecimientos
Este trabajo fue apoyado por el Premio NSF CAREER (MCB1701692) para LMJ.
Materiales
| Name | Company | Catalog Number | Comments |
| 15 mL Conical Centrifuge Tubes | Fisher Scientific | 14-959-53A | any brand is sufficient |
| 5 mL Gas Tight Syringe, Removable Luer Lock | SGE Analytical Science | 008760 | |
| 50 mL Conical Centrifuge Tubes | Fisher Scientific | 14-432-22 | any brand is sufficient |
| 500 µL SGE Gastight Syringes: Fixed Luer-Lok Models | Fisher Scientific | SG-00723 | |
| Acetone, HPLC Grade | Fisher Scientific | A929-4 | 4 L quantity is not necessary |
| Acetonitrile with 0.1% Formic Acid (v/v), LC/MS Grade | Fisher Scientific | LS120-500 | |
| ACQUITY UPLC M-Class Symmetry C18 Trap Column, 100 Å, 5 µm, 180 µm x 20 mm, 2G, V/M, 1/pkg | Waters | 186007496 | |
| ACQUITY UPLC M-Class System | Waters | ACQUITY UPLC M-Class System | |
| Aluminum Foil | Fisher Scientific | 01-213-100 | any brand is sufficient |
| Aqua 5 µm C18 125 Å packing material | Phenomenex | 04A-4299 | |
| Centrifuge | Eppendorf | 022625501 | |
| Delicate Task Wipers | Fisher Scientific | 06-666A | |
| Dithiothreiotol (DTT) | AmericanBio | AB00490-00005 | |
| DMSO, Anhydrous | Invitrogen | D12345 | |
| EX350 excimer laser | GAM Laser | EX350 excimer laser | |
| FEP Tubing 1/16" OD x 0.020" ID | IDEX Health & Science | 1548L | |
| Formic Acid, LC/MS Grade | Fisher Scientific | A117-50 | |
| HV3-2 VALVE | Hamilton | 86728 | |
| Hydrogen Peroxide | Fisher Scientific | H325-100 | any 30% hydrogen peroxide is sufficient |
| Iodoacetamide (IAA) | ACROS Organics | 122270050 | |
| Legato 210 syringe pump | KD Scientific | 788212 | Any syringe pump that can hold 4, 5 mL syringes, withdraw and expel liquid, and have a way to stale the motor should work |
| Luer Adapter Female Luer to 1/4-28 Male Polypropylene | IDEX Health & Science | P-618L | |
| Methanol, LC/MS Grade | Fisher Scientific | A454SK-4 | 4 L quantity is not necessary |
| Microcentrifuge | Thermo Scientific | 75002436 | |
| N,N'-Dimethylthiourea (DMTU) | ACROS Organics | 116891000 | |
| NanoTight Sleeve Green 1/16" ID x .0155" ID x 1.6" | IDEX Health & Science | F-242X | |
| NanoTight Sleeve Yellow 1/16" OD x 0.027" ID x 1.6" | IDEX Health & Science | F-246 | |
| N-tert-Butyl-α-phenylnitrone (PBN) | ACROS Organics | 177350250 | |
| Orbitrap Fusion Lumos Tribrid Mass Spectrometer | Thermo Scientific | Orbitrap Fusion Lumos Tribrid Mass Spectrometer | other high resolution instruments (e.g. Q exactive Orbitrap or Orbitrap Fusion) can be used |
| PE50-C pyroelectric energy meter | Ophir Optronics | 7Z02936 | |
| Pierce Quantitative Colorimetric Peptide Assay | Thermo Scientific | 23275 | |
| Pierce Rapid Gold BCA Protein Assay Kit | Thermo Scientific | A53225 | |
| Pierce Trypsin Protease, MS Grade | Thermo Scientific | 90058 | |
| Pierce Universal Nuclease for Cell Lysis | Fisher Scientific | 88702 | |
| Polymicro Cleaving Stone, 1" x 1" x 1/32" | Molex | 1068680064 | any capillary tubing cutter is sufficient |
| Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 150 µm, Outer Diameter 360 µm, TSP150350 | Polymicro Technologies | 1068150024 | |
| Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 450 µm, Outer Diameter 670 µm, TSP450670 | Polymicro Technologies | 1068150025 | |
| Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 75 µm, Outer Diameter 360 µm, TSP075375 | Polymicro Technologies | 1068150019 | |
| Potassium Phosphate Monobasic | Fisher Scientific | P382-500 | |
| Proteome Discover 2.2 (bottom-up proteomics software) | Thermo Scientific | OPTON-30799 | |
| Rotary Magnetic Tumble Stirrer | V&P Scientific, Inc. | VP 710D3 | |
| Rotary Magnetic Tumble Stirrer, accessory kit for use with Syringe Pumps | V&P Scientific, Inc. | VP 710D3-4 | |
| Super Flangeless Ferrule w/SST Ring, Tefzel™ (ETFE), 1/4-28 Flat-Bottom, for 1/16" OD | IDEX Health & Science | P-259X | |
| Super Flangeless Nut PEEK 1/4-28 Flat-Bottom, for 1/16" & 1/32" OD | IDEX Health & Science | P-255X | |
| Super Tumble Stir Discs, 3.35 mm diameter, 0.61 mm thick | V&P Scientific, Inc. | VP 722F | |
| Thermo Scientific Pierce RIPA Buffer | Fisher Scientific | PI89900 | |
| Tris Base | Fisher Scientific | BP152-500 | |
| Upchurch Scientific Low-Pressure Crosses: PEEK | Fisher Scientific | 05-700-182 | |
| Upchurch Scientific Low-Pressure Tees: PEEK | Fisher Scientific | 05-700-178 | |
| UV Fused Silica Plano-Convex Spherical Lenses | THORLABS | LA4052 | |
| V&P Scientific IncSupplier Diversity Partner TUMBL STIR DISC PARYLENE 1000 | V&P Scientific, Inc. | VP724F | |
| VHP MicroTight Union for 360µm OD | IDEX Health & Science | UH-436 | |
| Water with 0.1% Formic Acid (v/v), LC/MS Grade | Fisher Scientific | LS118-500 | |
| Water, LC/MS Grade | Fisher Scientific | W6-4 |
Referencias
- Gau, B., Garai, K., Frieden, C., Gross, M. L. Mass spectrometry-based protein footprinting characterizes the structures of oligomeric apolipoprotein E2, E3, and E4. Biochemistry. 50 (38), 8117-8126 (2011).
- Li, Z., et al. High structural resolution hydroxyl radical protein footprinting reveals an extended Robo1-heparin binding interface. Journal of Biological Chemistry. 290 (17), 10729-10740 (2015).
- Zhang, H., Gau, B. C., Jones, L. M., Vidavsky, I., Gross, M. L. Fast photochemical oxidation of proteins for comparing structures of protein− ligand complexes: the calmodulin− peptide model system. Analytical Chemistry. 83 (1), 311-318 (2010).
- Jones, L. M., et al. Complementary MS methods assist conformational characterization of antibodies with altered S-S bonding networks. Journal of the American Society for Mass Spectrometry. 24 (6), 835-845 (2013).
- Kiselar, J. G., Janmey, P. A., Almo, S. C., Chance, M. R. Structural analysis of gelsolin using synchrotron protein footprinting. Molecular & Cellular Proteomic. 2 (10), 1120-1132 (2003).
- Vahidi, S., Stocks, B. B., Liaghati-Mobarhan, Y., Konermann, L. Mapping pH-induced protein structural changes under equilibrium conditions by pulsed oxidative labeling and mass spectrometry. Analytical Chemistry. 84 (21), 9124-9130 (2012).
- Hambly, D. M., Gross, M. L. Laser flash photolysis of hydrogen peroxide to oxidize protein solvent-accessible residues on the microsecond timescale. Journal of the American Society for Mass Spectrometry. 16 (12), 2057-2063 (2005).
- Espino, J. A., Mali, V. S., Jones, L. M. In cell footprinting coupled with mass spectrometry for the structural analysis of proteins in live cells. Analytical Chemistry. 87 (15), 7971-7978 (2015).
- Rinas, A., Mali, V. S., Espino, J. A., Jones, L. M. Development of a Microflow System for In-Cell Footprinting Coupled with Mass Spectrometry. Analytical Chemistry. 88 (20), 10052-10058 (2016).
- Guan, J. Q., Almo, S. C., Reisler, E., Chance, M. R. Structural Reorganization of Proteins Revealed by Radiolysis and Mass Spectrometry: G-Actin Solution Structure Is Divalent Cation Dependent. Biochemistry. 42 (41), 11992-12000 (2003).
- Xu, G., Chance, M. R. Hydroxyl radical-mediated modification of proteins as probes for structural proteomics. Chemical Reviews. 107 (8), 3514-3543 (2007).
- Kaur, U., et al. Proteome-Wide Structural Biology: An Emerging Field for the Structural Analysis of Proteins on the Proteomic Scale. Journal of Proteome Research. 17 (11), 3614-3627 (2018).
- Chea, E. E., Jones, L. M. Analyzing the structure of macromolecules in their native cellular environment using hydroxyl radical footprinting. Analyst. 143 (4), 798-807 (2018).
- Zhu, Y., et al. Elucidating in vivo structural dynamics in integral membrane protein by hydroxyl radical footprinting. Molecular & Cellular Proteomic. 8 (8), 1999-2010 (1999).
- Rinas, A., Jones, L. M. Fast photochemical oxidation of proteins coupled to multidimensional protein identification technology (MudPIT): expanding footprinting strategies to complex systems. Journal of the American Society for Mass Spectrometry. 26 (4), 540-546 (2015).
- Rinas, A., Espino, J. A., Jones, L. M. An efficient quantitation strategy for hydroxyl radical-mediated protein footprinting using Proteome Discoverer. Analytical and Bioanalytical Chemistry. 408 (11), 3021-3031 (2016).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados