Method Article
Характеристика клеточных белков с в-клеточной быстрой фотохимической окисления белков
В этой статье
Резюме
Здесь мы характеризуем структуру белка и места взаимодействия в живых клетках с помощью метода протеин-следа, называемого в клетке быстрым фотохимическим окислением белков (IC-FPOP).
Аннотация
Быстрое фотохимическое окисление белков (FPOP) является гидроксиловрадикальным протеиновым методом, используемым для характеристики структуры белка и взаимодействий. FPOP использует 248 нм эксимерный лазер для фотолизуации перекиси водорода, производящего гидроксиловые радикалы. Эти радикалы окисляют растворительные открытые боковые цепи 19 из 20 аминокислот. В последнее время этот метод был использован в живых клетках (IC-FPOP) для изучения белковых взаимодействий в их родной среде. Изучение белков в клетках объясняет межмолекулярную скученность и различные взаимодействия белков, которые нарушаются для исследований in vitro. Пользовательская система потока одной ячейки была разработана для уменьшения агрегации и засорения клеток во время IC-FPOP. Эта система потока фокусирует клетки мимо эксимерного лазера индивидуально, обеспечивая таким образом последовательное облучение. Сравнивая степень окисления, производимого из FPOP, с доступностью растворителя белка, рассчитанной из кристаллической структуры, IC-FPOP может точно исследовать растворитель доступных боковых цепей белков.
Введение
Гидроксилрадикальный протеин след (HRPF) является методом, который зондирует платежеспособность белка через ковалентные изменения, производимые из гидроксилевых радикалов. Когда структура белка или белковые взаимодействия меняются, это изменит воздействие растворителя аминокислот, тем самым изменяя степень модификации остатков. С HRPF, белковые взаимодействия1,,2,3 3и белковые конформационные изменения4,,5,,6 успешно были допрошены в пробирке. Есть несколько методов, которые генерируют гидроксиловые радикалы для HRPF экспериментов, один из которых быстро ежей фотохимического окисления белков (FPOP). FPOP был разработан Hambly и Gross в 2005 году и использует 248 нм эксимерный лазер для производства гидроксиловадных радикалов через фотолиз перекиси водорода (H2O2)7.
Недавно Espino et al. расширили использование FPOP для исследования структуры белка в живых клетках, метод, называемый в клетке FPOP (IC-FPOP)8. В отличие от исследований in vitro, изучение белков в клетках объясняет молекулярную скученность наряду с различными белковыми взаимодействиями, которые потенциально могут влиять на структуру. Кроме того, он представляет собой преимущество предоставления снимок полного протеома потенциально предоставления структурной информации многочисленных систем сразу для выполнения протеом атакжем широкой структурной биологии. Кроме того, этот метод идеально подходит для белков, которые трудно изучать в пробирке, как мембранные белки.
Первоначальные исследования IC-FPOP успешно исследовали 105 белков, начиная от изобилия белка и клеточной локализации. Для улучшения метода IC-FPOP компания Rinas et al. разработала систему микропотока для одноклеточного потока9. Улучшение первоначальной системы потока ограничивает агрегацию клеток и увеличивает доступный H2O2 для облучения. В начальной системе потока клетки, слипающиеся в трубах кремнезема, приводили к засолькам и неравномерному облучению. Включение двух потоков оболочки буфера гидродинамически фокусирует клетки, позволяя им течь индивидуально мимо лазера. Включение отдельного шприца для H2O2 позволяет более контролируемое и оптимизируемое время экспозиции, что позволяет более высокие концентрации H2O2 без побочных эффектов. Кроме того, ограничение времени инкубации ограничивает разбивку H2O2 эндогенной каталазой. Путем включения этой новой системы потока, обнаруженное количество белков с модификацией FPOP увеличилось в 13 раз, тем самым расширяя возможности этого метода для зондирования множества белков в живых клетках. В этом протоколе описан общий эксперимент IC-FPOP, посвященный сборке системы потока IC-FPOP.
протокол
1. Настройка системы потока IC-FPOP
- Чтобы начать сборку системы потока, вырежьте сливку с помощью расщепления камня по размеру. Система потока IC-FPOP требует четырех 12 см и одного 17 см сливного кремния с внутренним диаметром (ID) 450 мкм и внешним диаметром (OD) 670 мкм, 24 см и один 40 см с идентификатором 75 мкм и OD 360 мкм , и, наконец, два 57 см с ID 150 мкм и OD 360 мкм.
ПРИМЕЧАНИЕ: При резке кремнезема труб, аккуратно соскребать полиимидовое покрытие, и согнуть, чтобы получить чистый разрез. Проверьте, чтобы убедиться, что это прямой разрез (это необходимо, чтобы убедиться, что нет завалов или утечек форме). - Настройка 15 соединений с использованием нано-жесткие рукава (0.0155 "ID X 1/16" OD для 360 мкм OD силика труб и 0,027 " ID X 1/16" OD для 670 мкм OD кремния труб) с супер flangeless орех PEEK 1/4-28 плоский дно для 1/16 " Тефцель (ETFE), 1/4-28 плоское дно, для 1/16" OD. Построить соединения в рамках протокола производителя(рисунок 1).
- Поместите 6 маленьких цилиндрических магнитов в один шприц в 500 л. Заполните этот шприц вместе с еще 500 шприцев и двумя шприцев 5 мл с буфером и удалить воздух. Позиция на шприц насос, как показано на рисунке 2A.
ПРИМЕЧАНИЕ: Шприцы размером 5 мл больше, чем 500 шприцев, поэтому для затягивания всех шприцев одновременно необходим прокладка(рисунок 2B). - Затяните шприц пробка насоса так, что шприц клетки имеет примерно 50 Л слева, когда двигатель останавливается. Это оставит место для магнитных мешалки. (Рисунок 2C-D).
ВНИМАНИЕ: Если шприц насос оказывает давление на магниты, они будут варенье шприц и может привести к шприц сломать. - Используя адаптер Luer, подключите ручной клапан к каждому шприцу. Соберите силика труб, как показано на рисунке 3.
ПРИМЕЧАНИЕ: Нить линии с клетками H2O2 весь путь через крест на другую сторону. Затем вставьте его в 450 мкм ID кремнезема труб. Буферы оболочки в шприцу 5 мл будут течь быстрее, чем клетки и H2O2. С буферами оболочки с обеих сторон, клетки будут гидродинамически сосредоточены в одну линию для облучения. - Система потока позиции рядом с лазером. Используя зажигалку, сжечь кремнезема покрытие на 450 мкм ID трубки, чтобы сделать окно для лазерного облучения.
- Поместите магнитный мешалку над клеточном шприцем, содержащим шесть магнитов.
- Установите шприц насос до 492,4 л /мин для конечной скорости потока 1083,3 л / м. Поток буфера через систему в три раза, чтобы промыть систему и проверить на любые утечки.
- Сосредоточьте эксимерный лазер на кварцевые трубки с помощью выпуклой линзы. После сосредоточения, проверить облучение окно, поместив небольшой лист бумаги за кремнезема труб и включить лазер. Измерьте регион, сгоревший от облучения. Рассчитайте необходимую частоту лазера с помощью окна облучения и скорости потока, чтобы получить долю исключения нуля.
ПРИМЕЧАНИЕ: Рекомендуемая лазерная энергия для эксперимента IC-FPOP составляет 120 мДж. Чтобы получить исключенную фракцию 0 с окном облучения 2,58 мм и скоростью потока 1083,3 л/мин, частота должна быть 44. Ниже приведены уравнения, которые необходимы для расчета частоты лазера, если известно окно облучения, скорость потока и фракция исключения.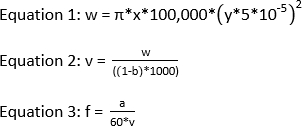
где w объем в nL, x ширина пятна лазера в mm, y будет ID tubing кремнезема в мкм, v будет полным томом в ЗЛ, b будет фракцией исключения, a будет тарифпотока потока в л/мин, и f частота в Hz.
2. Сделать утолить и H2O2
- Сделать утоление, содержащее 100 мМ N-терт-Бутил-альфа-фенилнитрон (PBN) и 100 мМ N, N'-dimethylthiourea (DMTU). Aliquot 11 мл утоления для каждого образца в 50 мл конической трубки.
- Разбавить H2O2 до 200 мМ. Каждый образец требует 500 л H2O2.
ПРИМЕЧАНИЕ: Утоление может быть сделано накануне и хранится при 4 градусах Цельсия на ночь, защищенном от света. H2O2 следует сделать свежим в день экспериментов.
3. Собирать ячейки
- Выращивайте клетки в колбе T175 примерно до 70-90% сближание.
- Удалите носители и промыть буфером.
ПРИМЕЧАНИЕ: Типичными буферами для использования являются фосфатно-буферный солевой раствор Dulbecco (DPBS) или сбалансированный соляной раствор Хэнка (HBSS). - Отсоединяйте клетки с помощью либо трипсина-ЭДТА, либо с помощью скребока.
- После того, как отдельные resuspend в 10 мл буфера и рассчитывать ячейки.
- Спин вниз, удалить буфер и trypsin-EDTA, и resuspend сделать 2 х 106 ячеек / мл.
- Aliquot 500 л клеток на образец.
ПРИМЕЧАНИЕ: Для каждого условия, сделать как минимум 3 лазерных образцов, и 3 без лазерного управления.
4. Выполнение IC-FPOP
- Заполните два шприца 5 мл с буфером, 500 л шприц, содержащий магниты с клетками, и окончательный 500 л шприц с H2O2. Включите магнитный мешалку.
- Спайк в 220 л диметилсульксида (DMSO) к одному аликто утоления, аккуратно перемешать, и место позади системы потока для сбора облученных образцов. Добавление DMSO будет препятствовать эндогенной метионин сульфодоксид редуктазы.
- Включите лазер, подождите 7 с, а затем включите систему потока.
- Как только образец заканчивается течет, выключите лазер, и аккуратно смешать утоления с собранным образцом. Поместите это в сторону во время шагов 4.5 и 4.6.
- Заполните все четыре шприца буфером, в который приостанавливаются клетки, и процвейте его через систему потока.
- После завершения промывки системы повторите шаги 4.1 и 4.2. Запустите поток без облучения. Это не лазерный контроль для учета фонового окисления в клетках.
- В то время как следующий образец работает, спина вниз предыдущий образец на 450-800 х г в течение 5 минут, удалить растворитель, и resuspend в 100 злицис буфера лиза клетки, как радиоиммунопреции анализ (RIPA) буфера.
- Перенос образца в микроцентрифуговую трубку и флэш-заморозку в жидком азоте.
- Когда все образцы закончат работу, разберите систему подачи для очистки. Откажитесь от использованных кварцевых труб и очистите все остальные соединения, соникируя на 1 ч в 50% воды: 50% метанола. Очистите шприцы в рамках инструкций производителя.
5. Дайджест
- Переварить всю клетку lysate. Начните с оттаивания образцов и нагревайте при температуре 95 градусов по Цельсию в течение 10 мин.
- После нагрева, охладить лизат на льду в течение 15 минут.
- Добавьте 25 единиц нуклеазы для переваривания ДНК и РНК и инкубировать в комнате умеренный в течение 15 минут.
- Образцы спина с помощью центрифуги столешницы при 16 000 х г в течение 10 мин при 4 градусах Цельсия.
- Соберите супернатант и перенесите его в чистую микроцентрифуговую трубку.
- Проверьте концентрацию белка с помощью набора анализ овак белка.
- Перенесите 20-100 мкг образца в чистую микроцентрифуговую трубку и доведите до 100 л.
- Уменьшите образцы с 20 мМ дитиотрейотол (DTT) при 50 градусах по Цельсию в течение 45 мин.
- Охладите образцы при комнатной температуре в течение 15 мин.
- Алкилат с 20 мМ йодоацетамидом (IAA) при комнатной температуре в течение 20 минут защищен от света.
- Добавьте предварительно охлажденный ацетон в соотношении 1:4: ацетон. Смешайте образцы и поместите в -20 градусов на ночь.
- На следующее утро, спина образцов на 16000 х г в течение 10 минут при 4 градусах Цельсия.
- Удалить супернатант и добавить 50 л 90% предварительно охлажденный ацетон. Смешайте образцы и вращайтесь при 16 000 х г в течение 5 мин при 4 градусах Цельсия.
- Удалите ацетон и дайте образцам высохнуть, оставив крышки микроцентрифуга открытыми с ворсом свободной салфеткой, покрывающей верхнюю часть. После того, как образцы высохли, resuspend протеиновые гранулы с 10 мм Tris буфер рН 8.
- Отрептить 20 мкг трипсина в 40 qL 10 мм Tris буфер рН 8. Добавьте 2 мкг трипсина (масса: соотношение массы 1 трипсина: 50 образцов). Инкубировать образцы при 37 градусах Цельсия на ночь.
- На следующее утро проверьте концентрацию пептида с помощью пептида. После того, как образец был удален для пептидного асссиса, утолить пищеварение трипсина, добавив в образцы формальную кислоту (окончательная концентрация составляет 5% для кислоты).
- Как только окончательная концентрация пептида определяется, перенесите 10 мкг каждого образца в чистую микроцентрифуговую трубку. Это гарантирует, что анализируется одинаковое количество каждого образца. Высушите образец с помощью вакуумной центрифуги. После высушивания повторно приостанавливается с 20 ЗЛ масс-спектрометрии класса 0,1% для мистовой кислоты. Передача образцов на флаконы автосэмпера.
6. Ликвидная хроматография-Тандемская масс-спектрометрия
- Для локализации модификаций FPOP анализируйте переваренный клеточный лизат с помощью анализа LC-MS/MS.
- Используйте мобильные фазы 0,1% для модной кислоты в воде (A) и 0,1% для мической кислоты в ацетонитриле (B).
- Загрузите 0,5 мкг образца на 180 мкм х 20 мм C18 (5 мкм и 100 евро) захвата колонки и мыть образец с 99% (A) и 1% (B) в течение 15 мин.
- Используя аналитическую колонку C18 (5 мкм и 125 м), запустите аналитический метод разделения с частотой потока 0,300 мл/мин, начиная с 3% (B) в течение одной минуты, затем наращивай до 10% (B) с 1-2 мин. Следующий пандус до 45% (B) от 2-100 мин, затем 100% (B) от 100-110 мин. Очистите колонну, удерживая на 100% (B) от 110-115 мин. Восстановление колонны путем ramping до 3% (B) от 115-116 мин и удерживайте на 3% (B) от 116-160 мин.
- Установите метод приобретения MS, чтобы иметь разрешение 60000 с диапазоном м /з сканирования 375-1500. Установите цель автоматического управления усилением (AGC) до 5,0 x 105 с максимальным временем впрыска 50 мс.
- Во время приобретения MS выберите ионы предшественников с состояниями заряда 2-6 для изоляции через приобретение зависимых данных (DDA) с изоляционным окном 1,2 м/з и временем цикла 4 с. Выберите пептиды с порогом интенсивности 5,0 х 104 для активации HCD с нормализованным набором энергии до 32%. Исключить пептиды после 1 MS / MS приобретения для 60 s. Установите MS / MS резолюции до 15000 с целью AGC 5,0 х 104 и максимальное время инъекции 35 мс.
7. Обработка данных
- Поиск RAW файлов на доступных программное обеспечение анализа белка против соответствующей базы данных белка и соответствующих фермента дайджеста. Здесь используйте швейцарскую базу данных Homo Sapiens и трипсин.
- Установите массу предшественника для поиска от 350 до 5000 Da и массовой допуск 10 ppm. Там может быть не более 1 пропущенного расщепления сайта с пептидной длины от 6 до 144 остатков. Эти ограничения облегчают поиск базы данных.
- Установите максимальной массоустойчивости фрагментов до 0,02 Da с карбамидоэтилом (No57.021) в качестве статической модификации и всех модификаций FPOP из 17 аминокислот в качестве динамической модификации(рисунок 4 является примером рабочего процесса анализа белка, используемого для обнаружения модификаций FPOP).
ПРИМЕЧАНИЕ: FPOP модификации на серинку и молотин не включены в поиск из-за их низкой реактивности с гидроксиловыми радикалами. - Поиск с базой данных приманки с ложной скоростью обнаружения 1% и 5%.
- После завершения поиска файлы вычисляют степень модификации FPOP. Открытый Proteome Discoverer 2.2, экспортная последовательность, места модификации, присоединение белка, файл спектра, изобилие прекурсоров и информация о времени удержания. Рассчитайте степень модификации из уравнения 4:

Измененная область EIC представляет собой хроматографическую область специфического пептида с гидроксильной радикальной модификацией. Область EIC представляет собой общую хроматографическую область как модифицированных, так и неизмененных областей этого специфического пептида. Степень окисления рассчитывается в образцах с облучением и без его облучения. Образец опускания облучения (контроля) объясняет любое фоновое окисление, которое могло присутствовать в клетках до и после воздействия H2O2. Элементы управления вычитаются из образцов облучения, чтобы помочь изолировать FPOP конкретных модификаций.
Результаты
IC-FPOP является методом следовдля взаимодействия белков в живых клетках. В системе потока IC-FPOP время воздействия H2O2 ограничено примерно 3 с, что требует более высоких концентраций H2O2 без пагубных последствий для клеток. Система потока также включает в себя два потока оболочки буфера, который гидродинамически фокусирует клетки в центре труб, производя один поток клеток, которые будут равномерно облучены (Рисунок 5)9. Флуоресценция изображения ортогоналированных Y ' сложенные изображения(Рисунок 5A) показывают четкое отделение буфера оболочки (содержащий фторфор FITC) от клеточного раствора (содержащего фторофор TMRM). Чтобы подчеркнуть это разделение, Рисунок 5B и Рисунок 5C показывают трехмерные средние карты тепла либо решения буфера оболочки или клеточного решения, иллюстрирующие минимальное смешивание двух решений.
Использование одноклеточной системы потока увеличивает количество окислительно модифицированных белков в 13 раз(рисунок 6А)9. В этом методе, белки во многих клеточных отсеках помечены мембранных белков, цитоплазматических белков и белков в ядре является наиболее распространенным8,9. Для обеспечения белки были изменены в нетронутых клеток, флуоресцентные изображения CellROX обработанных клеток были выполнены после H2O2 лечения и облучения(Рисунок 6B)8. Стабильность клеток на протяжении всего процесса маркировки еще больше подтверждает эффективность IC-FPOP для зондирования белков в их родной клеточной среде. Используя тандемно-масс-спектрометрию, эти модификации могут быть локализованы в конкретных аминокислотах на белке. Рисунок 7 представляет собой модификацию, которая происходит во время IC-FPOP вместе с извлеченной ионной хроматограммой. Сдвиг, наблюдаемый в извлеченной ионной хроматограмме, приводит к изменению гидрофобоксичности, вызванному окисленным метионином в модифицированном пептидном.
Чтобы проверить, если FPOP модификации зонда платежеспособной доступности внутри клеток, в клетке помечены актин был по сравнению как в пробирке следисследования исследования и различных кристаллических структур актина (Рисунок 8)8. В ячейке помечены актин представлен на рисунке 8показывает сопоставимые степени окисления из исследования in vitro Гуань и др.10 (Рисунок 8B), заключение актина имеет аналогичную платежеспособную доступность как для в-клеток и в пробирке исследований. Для дальнейшего подтверждения IC-FPOP зондирования платежеспособной доступности актина, степень модификаций FPOP были сопоставлены с платежеспособной доступности помеченных остатков, рассчитанных из двух кристаллических структур актина(рисунок 8C). Эта корреляция показывает, что IC-FPOP зондирует платежеспособность мономерного белка хорошо.

Рисунок 1: Как правильно построить ферули. (A) Место ferrules, кремнезем абонемента, и рукав вместе до затягивания. (B) Затяните все компоненты вместе. (C) Конечный продукт будет производить ferule, который был затянут вниз на рукаве. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 2: Настройка системы потока IC-FPOP. (A) Изображение полностью собранной системы потока IC-FPOP, расположенной рядом с лазером. (B) Пример прокладки, необходимых для увеличения внешнего диаметра 500 шприцев, чтобы успешно затянуть все шприцы вниз вместе. (C) Представитель фотографии, показывающие пространство, необходимое для магнитных мешалки. (D) Пробки необходимы, чтобы затормозить шприц насос, не нарушая шприцы. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
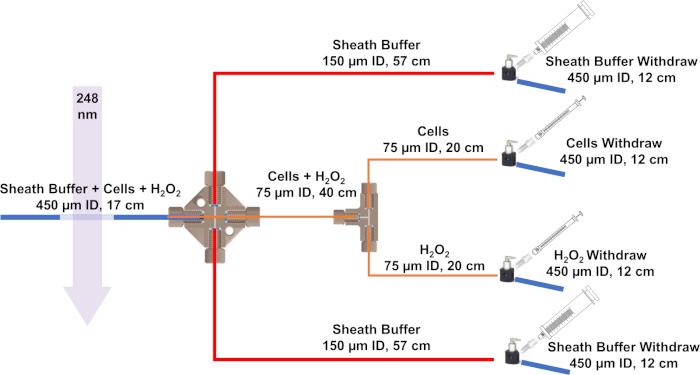
Рисунок 3: Схема системы потока, разработанная для IC-FPOP. Синие линии представляют силика труб с 450 мкм ID и 670 мкм OD, красные линии имеют 150 мкм ID и 360 мкм OD, и оранжевые линии имеют 75 мкм ID и 360 мкм OD. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 4: Программное обеспечение для анализа белка, используемое для обнаружения модификаций FPOP. Типичный рабочий процесс с соответствующими изменениями, исискалемый в каждом узлах. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
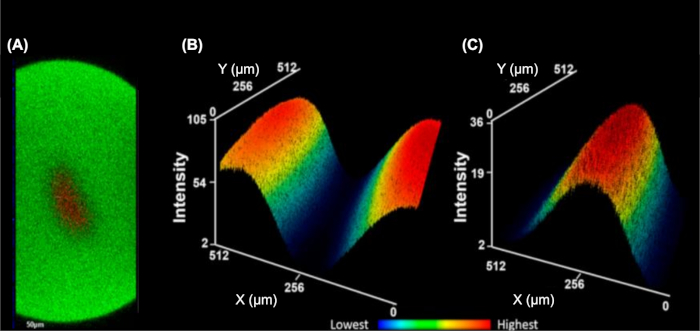
Рисунок 5: Система потока одной ячейки гидродинамически фокусирует клетки в один поток. (A) Orthogonal Y' стек иллюстрирующие 3D фокусировки клеточного аналита (красный, TMRM фторофора) в окружении оболочки буфера (зеленый, FITC фторофора). Трехмерная средняя тепловая карта тепловой оболочки буфера(B)и клеточного аналита(C). Более низкие интенсивности синие и самые высокие красные(B-C). Эта цифра была изменена от Rinas et al.9Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
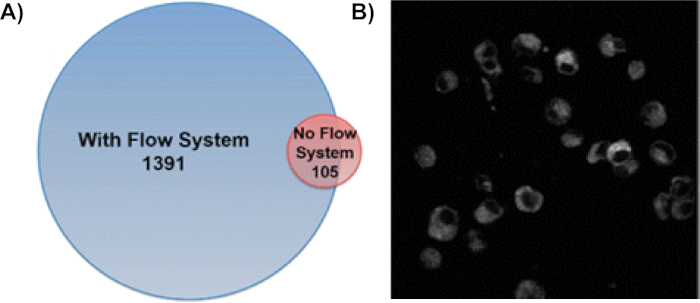
Рисунок 6: Использование системы потока IC-FPOP резко увеличивает модифицированные белки FPOP в клетках вхобовы. (A) Сравнение окисленных белков, отождествляемых с системой потока и без нее. Система потока идентифицировала 1391 FPOP модифицированных белков, в то время как только 105 белков были идентифицированы без системы потока с перекрытием 58 модифицированных белков. Эта цифра была изменена от Rinas et al.9 (B) Флуоресценция изображения клеток CellROX после IC-FPOP показать клетки по-прежнему нетронутыми после окислительной маркировки. Клетки были изображены с помощью мультифотонного микроскопа Olympus Fluoview FV1000 MPE на 665 нм. Показано изображение представляет собой один срез. Эта цифра была изменена с Espino и др.8Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 7: Примеры тандемных спектров MS/MS, которые происходят во время IC-FPOP. Продукт-ион (MS/MS) спектра (A) неизмененный пептид, и (B) окисление обнаружено на остатках M8 найдены на том пептид. Представитель EIC (C) неизмененный пептид и (D) модифицированный пептид. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 8: IC-FPOP эффективен в зондирования платежеспособности белков. (A) Масштабмодификация модификации для 9 окислительно модифицированных пептидов из актина. Значения отображаются как средние плюс и минус стандартные отклонения (n No 3). (B) Модификация актина пептиды окисляется в пробирке синхротронного радиолизотеного от Гуань и др.10 (C) Корреляция остатков FPOP модификаций с SASA в жесткой (треугольники, пунктирной линии тренда) и открытые (круги, твердая линия тренда) состояния актина. Эта цифра была изменена с Espino и др.8Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
Обсуждение
Несколько методов на основе масс-спектрометрии были разработаны для изучения структуры белка и белково-лигажных комплексов в протеоме в широком порядке в целых клетках или клеточных лисатах. Эти методы включают в себя, но не ограничиваются стабильностью белков от скорости окисления (SPROX), теплового профилирования протеома (TPP), химического перекрестного соединения (XL-MS) и гидроксильного радикального протеина (HRPF). Каждый метод имеет уникальные ограничения и преимущества по сравнению друг с другом, которые были широко рассмотрены12. Каждый из этих методов были использованы для протеома широкой структурной биологии, чтобы выяснить структуру белка и в конечном итоге функционировать в сложной клеточной среде. IC-FPOP является методhrПФ, который использует гидроксиловые радикалы окислительно модифицировать растворителя подвергаются боковые цепи аминокислот, зондирования структуры белка и белка-лиганд взаимодействия в жизнеспособных клеток13. IC-FPOP является улучшением первоначального HRPF в живых клетках, которые использовали фентон химии для создания радикалов на минутсрок14. В этом исследовании структурные изменения в интегральном белке мембраны в ответ на снижение рН или ионной силы буфера были успешно охарактеризованы с хорошим покрытием окисления по всему белку. По сравнению с химией Фентон, IC-FPOP гораздо быстрее, изменяя белки на микросекундной шкале времени, что позволяет родной конформации белка, которые будут изучены.
Ключевым испытанием для IC-FPOP является подтверждение жизнеспособности клеток после воздействия H2O2. Используя линию смешивания 40 см, клетки инкубируются в H2O2 примерно за 3 с до облучения. Это время можно отрегулировать путем изменять длину этого tubing кремнезема. Примечательно, что, хотя использование трипан синий для проверки жизнеспособности клеток показывает целостность клеток устойчивы после H2O2 инкубации, клетки могут потенциально быть под стрессом, осуществляющих сигнальные пути, которые взаимодействуют с H2O2. К счастью, короткое время инкубации быстрее, чем синтез белка, обеспечивая уверенность в том, что присутствующие белки не индуцируются H2O2.
Следующим важным шагом является подтверждение правильной сборки системы потока. После сборки убедитесь, что после промывки системы с нужным буфером нет утечек. Если утечки присутствуют, убедитесь, что кремнезем трубки был сокращен должным образом и флеш против ferrule сделать надлежащее уплотнение раз ужесточили вниз. Все детали затягиваются вручную, поэтому инструменты не требуются. Во время каждого эксперимента IC-FPOP убедитесь, что магнитные мешалки в клеточном шприцах остаются в движении. Это небольшое возбуждение ограничивает количество клеток, которые оседают в нижней части шприца, но не достаточно суровы, чтобы стрижка клеток. После одного запуска в шприче осталось примерно 50 кл. Всегда убедитесь, что разбавить это с промывки шаг, чтобы ограничить количество клеток, которые переносят на следующий эксперимент. Рекомендуется использовать свежий клеточный шприц, если сравниваются несколько клеточных процедур. Важно также выбрать подходящий буфер для тестируемых ячеек. Некоторые буферы утоляют гидроксиль-радикал, что приводит к меньшему количеству изменений в белках. Xu et al. показали, что некоторые широко используемые буферы уменьшаются гидроксиловая радикальная продолжительность жизни11. DPBS и HBSS являются общими буферами, используемыми для экспериментов IC-FPOP.
Следуя IC-FPOP, оптимизируйте протокол пищеварения на основе необходимых параметров. Поскольку FPOP производит необратимые ковалентные модификации, имеется достаточно времени для тщательного пищеварения и очистки без потери покрытия маркировки. Всегда проверяйте и нормализуйте концентрацию белка, чтобы равномерное пептидное концентрации загружалось для тандемной масс-спектрометрии. Наконец, помните, что иммунопрецит не может быть выполнена в сочетании с IC-FPOP. Если модификация FPOP нацелена на область взаимодействия, сродство антитела будет снижено. Чтобы помочь увеличить идентификацию модификаций FPOP, 2D-хроматографические шаги разделения показали более чем в три раза количество окисленных пептидов обнаружено15.
Проблема любого эксперимента FPOP является сложный уровень анализа данных из-за возможных продуктов окисления, которые могут возникнуть. Это верно как для в-клетки или in vitro, но резко увеличивается с дополнительной сложности анализа клеточных лисатов. При дальнейшей оптимизации IC-FPOP возникает больше белков с более высоким охватом модификации, что делает анализ более трудным. Объем данных, полученных в ходе одного эксперимента IC-FPOP, ограничивает использование ручной проверки, заставляя исследователей в большей степени полагаться на программное обеспечение. В связи с этим, Rinas et al. разработали стратегию количественной оценки hrPF с использованием Proteome Discoverer (PD)16. Этот метод использует рабочий процесс многопоиска на PD в сочетании с количественной платформой в электронной таблице. В настоящее время проводятся дальнейшие усовершенствования платформы IC-FPOP с целью увеличения числа выявленных пептидов с модификациями FPOP наряду с повышением воспроизводимости и точностью количественной оценки.
Раскрытие информации
Лиза Джонс является изобретателем на сборке потока для клеток патента (номер публикации: 20180079998).
Благодарности
Эта работа была поддержана NSF CAREER Award (MCB1701692) для LMJ.
Материалы
| Name | Company | Catalog Number | Comments |
| 15 mL Conical Centrifuge Tubes | Fisher Scientific | 14-959-53A | any brand is sufficient |
| 5 mL Gas Tight Syringe, Removable Luer Lock | SGE Analytical Science | 008760 | |
| 50 mL Conical Centrifuge Tubes | Fisher Scientific | 14-432-22 | any brand is sufficient |
| 500 µL SGE Gastight Syringes: Fixed Luer-Lok Models | Fisher Scientific | SG-00723 | |
| Acetone, HPLC Grade | Fisher Scientific | A929-4 | 4 L quantity is not necessary |
| Acetonitrile with 0.1% Formic Acid (v/v), LC/MS Grade | Fisher Scientific | LS120-500 | |
| ACQUITY UPLC M-Class Symmetry C18 Trap Column, 100 Å, 5 µm, 180 µm x 20 mm, 2G, V/M, 1/pkg | Waters | 186007496 | |
| ACQUITY UPLC M-Class System | Waters | ACQUITY UPLC M-Class System | |
| Aluminum Foil | Fisher Scientific | 01-213-100 | any brand is sufficient |
| Aqua 5 µm C18 125 Å packing material | Phenomenex | 04A-4299 | |
| Centrifuge | Eppendorf | 022625501 | |
| Delicate Task Wipers | Fisher Scientific | 06-666A | |
| Dithiothreiotol (DTT) | AmericanBio | AB00490-00005 | |
| DMSO, Anhydrous | Invitrogen | D12345 | |
| EX350 excimer laser | GAM Laser | EX350 excimer laser | |
| FEP Tubing 1/16" OD x 0.020" ID | IDEX Health & Science | 1548L | |
| Formic Acid, LC/MS Grade | Fisher Scientific | A117-50 | |
| HV3-2 VALVE | Hamilton | 86728 | |
| Hydrogen Peroxide | Fisher Scientific | H325-100 | any 30% hydrogen peroxide is sufficient |
| Iodoacetamide (IAA) | ACROS Organics | 122270050 | |
| Legato 210 syringe pump | KD Scientific | 788212 | Any syringe pump that can hold 4, 5 mL syringes, withdraw and expel liquid, and have a way to stale the motor should work |
| Luer Adapter Female Luer to 1/4-28 Male Polypropylene | IDEX Health & Science | P-618L | |
| Methanol, LC/MS Grade | Fisher Scientific | A454SK-4 | 4 L quantity is not necessary |
| Microcentrifuge | Thermo Scientific | 75002436 | |
| N,N'-Dimethylthiourea (DMTU) | ACROS Organics | 116891000 | |
| NanoTight Sleeve Green 1/16" ID x .0155" ID x 1.6" | IDEX Health & Science | F-242X | |
| NanoTight Sleeve Yellow 1/16" OD x 0.027" ID x 1.6" | IDEX Health & Science | F-246 | |
| N-tert-Butyl-α-phenylnitrone (PBN) | ACROS Organics | 177350250 | |
| Orbitrap Fusion Lumos Tribrid Mass Spectrometer | Thermo Scientific | Orbitrap Fusion Lumos Tribrid Mass Spectrometer | other high resolution instruments (e.g. Q exactive Orbitrap or Orbitrap Fusion) can be used |
| PE50-C pyroelectric energy meter | Ophir Optronics | 7Z02936 | |
| Pierce Quantitative Colorimetric Peptide Assay | Thermo Scientific | 23275 | |
| Pierce Rapid Gold BCA Protein Assay Kit | Thermo Scientific | A53225 | |
| Pierce Trypsin Protease, MS Grade | Thermo Scientific | 90058 | |
| Pierce Universal Nuclease for Cell Lysis | Fisher Scientific | 88702 | |
| Polymicro Cleaving Stone, 1" x 1" x 1/32" | Molex | 1068680064 | any capillary tubing cutter is sufficient |
| Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 150 µm, Outer Diameter 360 µm, TSP150350 | Polymicro Technologies | 1068150024 | |
| Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 450 µm, Outer Diameter 670 µm, TSP450670 | Polymicro Technologies | 1068150025 | |
| Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 75 µm, Outer Diameter 360 µm, TSP075375 | Polymicro Technologies | 1068150019 | |
| Potassium Phosphate Monobasic | Fisher Scientific | P382-500 | |
| Proteome Discover 2.2 (bottom-up proteomics software) | Thermo Scientific | OPTON-30799 | |
| Rotary Magnetic Tumble Stirrer | V&P Scientific, Inc. | VP 710D3 | |
| Rotary Magnetic Tumble Stirrer, accessory kit for use with Syringe Pumps | V&P Scientific, Inc. | VP 710D3-4 | |
| Super Flangeless Ferrule w/SST Ring, Tefzel™ (ETFE), 1/4-28 Flat-Bottom, for 1/16" OD | IDEX Health & Science | P-259X | |
| Super Flangeless Nut PEEK 1/4-28 Flat-Bottom, for 1/16" & 1/32" OD | IDEX Health & Science | P-255X | |
| Super Tumble Stir Discs, 3.35 mm diameter, 0.61 mm thick | V&P Scientific, Inc. | VP 722F | |
| Thermo Scientific Pierce RIPA Buffer | Fisher Scientific | PI89900 | |
| Tris Base | Fisher Scientific | BP152-500 | |
| Upchurch Scientific Low-Pressure Crosses: PEEK | Fisher Scientific | 05-700-182 | |
| Upchurch Scientific Low-Pressure Tees: PEEK | Fisher Scientific | 05-700-178 | |
| UV Fused Silica Plano-Convex Spherical Lenses | THORLABS | LA4052 | |
| V&P Scientific IncSupplier Diversity Partner TUMBL STIR DISC PARYLENE 1000 | V&P Scientific, Inc. | VP724F | |
| VHP MicroTight Union for 360µm OD | IDEX Health & Science | UH-436 | |
| Water with 0.1% Formic Acid (v/v), LC/MS Grade | Fisher Scientific | LS118-500 | |
| Water, LC/MS Grade | Fisher Scientific | W6-4 |
Ссылки
- Gau, B., Garai, K., Frieden, C., Gross, M. L. Mass spectrometry-based protein footprinting characterizes the structures of oligomeric apolipoprotein E2, E3, and E4. Biochemistry. 50 (38), 8117-8126 (2011).
- Li, Z., et al. High structural resolution hydroxyl radical protein footprinting reveals an extended Robo1-heparin binding interface. Journal of Biological Chemistry. 290 (17), 10729-10740 (2015).
- Zhang, H., Gau, B. C., Jones, L. M., Vidavsky, I., Gross, M. L. Fast photochemical oxidation of proteins for comparing structures of protein− ligand complexes: the calmodulin− peptide model system. Analytical Chemistry. 83 (1), 311-318 (2010).
- Jones, L. M., et al. Complementary MS methods assist conformational characterization of antibodies with altered S-S bonding networks. Journal of the American Society for Mass Spectrometry. 24 (6), 835-845 (2013).
- Kiselar, J. G., Janmey, P. A., Almo, S. C., Chance, M. R. Structural analysis of gelsolin using synchrotron protein footprinting. Molecular & Cellular Proteomic. 2 (10), 1120-1132 (2003).
- Vahidi, S., Stocks, B. B., Liaghati-Mobarhan, Y., Konermann, L. Mapping pH-induced protein structural changes under equilibrium conditions by pulsed oxidative labeling and mass spectrometry. Analytical Chemistry. 84 (21), 9124-9130 (2012).
- Hambly, D. M., Gross, M. L. Laser flash photolysis of hydrogen peroxide to oxidize protein solvent-accessible residues on the microsecond timescale. Journal of the American Society for Mass Spectrometry. 16 (12), 2057-2063 (2005).
- Espino, J. A., Mali, V. S., Jones, L. M. In cell footprinting coupled with mass spectrometry for the structural analysis of proteins in live cells. Analytical Chemistry. 87 (15), 7971-7978 (2015).
- Rinas, A., Mali, V. S., Espino, J. A., Jones, L. M. Development of a Microflow System for In-Cell Footprinting Coupled with Mass Spectrometry. Analytical Chemistry. 88 (20), 10052-10058 (2016).
- Guan, J. Q., Almo, S. C., Reisler, E., Chance, M. R. Structural Reorganization of Proteins Revealed by Radiolysis and Mass Spectrometry: G-Actin Solution Structure Is Divalent Cation Dependent. Biochemistry. 42 (41), 11992-12000 (2003).
- Xu, G., Chance, M. R. Hydroxyl radical-mediated modification of proteins as probes for structural proteomics. Chemical Reviews. 107 (8), 3514-3543 (2007).
- Kaur, U., et al. Proteome-Wide Structural Biology: An Emerging Field for the Structural Analysis of Proteins on the Proteomic Scale. Journal of Proteome Research. 17 (11), 3614-3627 (2018).
- Chea, E. E., Jones, L. M. Analyzing the structure of macromolecules in their native cellular environment using hydroxyl radical footprinting. Analyst. 143 (4), 798-807 (2018).
- Zhu, Y., et al. Elucidating in vivo structural dynamics in integral membrane protein by hydroxyl radical footprinting. Molecular & Cellular Proteomic. 8 (8), 1999-2010 (1999).
- Rinas, A., Jones, L. M. Fast photochemical oxidation of proteins coupled to multidimensional protein identification technology (MudPIT): expanding footprinting strategies to complex systems. Journal of the American Society for Mass Spectrometry. 26 (4), 540-546 (2015).
- Rinas, A., Espino, J. A., Jones, L. M. An efficient quantitation strategy for hydroxyl radical-mediated protein footprinting using Proteome Discoverer. Analytical and Bioanalytical Chemistry. 408 (11), 3021-3031 (2016).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены