Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Tomografía fotoacústica, ecográfica y angiográfica integrada (PAUSAT) para imágenes cerebrales completas no invasivas del accidente cerebrovascular isquémico
En este artículo
Resumen
Este trabajo demuestra el uso de una plataforma de imágenes multimodal basada en ultrasonido para imágenes no invasivas de accidentes cerebrovasculares isquémicos. Este sistema permite la cuantificación de la oxigenación de la sangre a través de imágenes fotoacústicas y la perfusión deteriorada en el cerebro a través de la angiografía acústica.
Resumen
Aquí se presenta un estudio experimental de accidente cerebrovascular isquémico utilizando nuestro sistema de imágenes no invasivo recientemente desarrollado que integra tres tecnologías de imágenes acústicas: fotoacústica, ultrasonido y tomografía angiográfica (PAUSAT). La combinación de estas tres modalidades ayuda a adquirir la tomografía fotoacústica multiespectral (PAT) de la oxigenación de la sangre cerebral, las imágenes de ultrasonido de alta frecuencia del tejido cerebral y la angiografía acústica de la perfusión sanguínea cerebral. La plataforma de imágenes multimodales permite el estudio de los cambios de perfusión cerebral y oxigenación en todo el cerebro del ratón después de un accidente cerebrovascular. Se evaluaron dos modelos de accidente cerebrovascular isquémico comúnmente utilizados: el modelo de oclusión permanente de la arteria cerebral media (pMCAO) y el modelo fototrombótico (TP). PAUSAT se utilizó para obtener imágenes de los mismos cerebros de ratón antes y después de un accidente cerebrovascular y analizar cuantitativamente ambos modelos de accidente cerebrovascular. Este sistema de imágenes fue capaz de mostrar claramente los cambios vasculares cerebrales después del accidente cerebrovascular isquémico, incluida la reducción significativa de la perfusión sanguínea y la oxigenación en la región del infarto del accidente cerebrovascular (ipsilateral) en comparación con el tejido no lesionado (contralateral). Los resultados fueron confirmados por imágenes de contraste moteado láser y tinción de cloruro de trifeniltetrazolio (TTC). Además, el volumen del infarto de accidente cerebrovascular en ambos modelos de accidente cerebrovascular se midió y validó mediante tinción TTC como la verdad fundamental. A través de este estudio, hemos demostrado que PAUSAT puede ser una herramienta poderosa en estudios preclínicos no invasivos y longitudinales de accidente cerebrovascular isquémico.
Introducción
La sangre transporta oxígeno (a través de la proteína hemoglobina) y otros nutrientes importantes a los tejidos de nuestro cuerpo. Cuando se interrumpe el flujo de sangre a través de los tejidos (isquemia), puede producirse un daño grave a los tejidos, cuyos efectos más inmediatos se deben a la falta de oxígeno (hipoxia). El accidente cerebrovascular isquémico es el resultado de un flujo sanguíneo interrumpido a cierta región del cerebro. El daño cerebral resultante de un accidente cerebrovascular isquémico puede ocurrir a los pocos minutos de la obstrucción de un vaso, y a menudo puede tener efectos debilitantes y duraderos 1,2. Una estrategia muy valiosa para evaluar la fisiopatología después del accidente cerebrovascular isquémico e identificar y probar nuevos tratamientos es el uso de modelos de animales pequeños en el laboratorio. Los tratamientos descubiertos en el laboratorio tienen como objetivo traducirse al uso clínico y mejorar la vida de los pacientes. Sin embargo, el uso de animales en la investigación biomédica debe evaluarse cuidadosamente de acuerdo con los principios de las 3R de Russell y Burch: reemplazo, reducción y refinamiento3. El objetivo del componente de reducción es reducir el número de animales sin comprometer la recopilación de datos. Con esto en mente, poder evaluar longitudinalmente la evolución de la lesión a través de imágenes no invasivas permite una gran ventaja en la reducción del número de animales requeridos, así como maximizar la información obtenida de cada animal4.
La tomografía fotoacústica (PAT) es una modalidad de imagen híbrida que combina el contraste de absorción óptica con la resolución espacial de imágenes de ultrasonido5. El mecanismo de imagen de PAT es el siguiente. Un pulso láser de excitación se ilumina en el objetivo que se está fotografiando. Suponiendo que el objetivo absorbe la luz en la longitud de onda del láser de excitación, aumentará su temperatura. Este rápido aumento de la temperatura da como resultado una expansión termoelástica del objetivo. La expansión hace que una onda de ultrasonido se propague desde el objetivo. Al detectar la onda de ultrasonido en muchas posiciones, el tiempo requerido para que la onda se propague desde el objetivo a los detectores se puede utilizar para crear una imagen a través de un algoritmo de reconstrucción. La capacidad de PAT para detectar la absorción óptica en regiones de tejido profundo diferencia PAT de la imagen de ultrasonido, que detecta límites de diferentes impedancias acústicas de los tejidos5. En los espectros visible e infrarrojo cercano, las principales biomoléculas altamente absorbentes que son abundantes en los organismos son la hemoglobina, los lípidos, la melanina y el agua7. De particular interés en el estudio del accidente cerebrovascular es la hemoglobina. Dado que la oxihemoglobina y la desoxihemoglobina tienen diferentes espectros de absorción óptica, PAT se puede usar con múltiples longitudes de onda láser de excitación para determinar la concentración relativa de los dos estados de la proteína. Esto permite cuantificar la saturación de oxígeno de la hemoglobina (sO2), u oxigenación sanguínea, dentro y fuera de la región del infarto 8,9. Esta es una medida importante en el accidente cerebrovascular isquémico, ya que puede indicar el nivel de oxígeno en el tejido cerebral dañado después de la isquemia.
La angiografía acústica (AA) es un método de imagen de ultrasonido con contraste que es particularmente útil para obtener imágenes de la morfología de la vasculatura in vivo10. El método se basa en el uso de un transductor wobbler de doble elemento (un elemento de baja frecuencia y un elemento de alta frecuencia) junto con microburbujas inyectadas en el sistema circulatorio del sujeto de imágenes. El elemento de baja frecuencia del transductor se utiliza para transmitir a la frecuencia resonante de las microburbujas (por ejemplo, 2 MHz), mientras que el elemento de alta frecuencia se utiliza para recibir las señales superarmónicas de las microburbujas (por ejemplo, 26 MHz). Cuando se excitan a una frecuencia resonante, las microburbujas tienen una fuerte respuesta no lineal, lo que resulta en la producción de señales súper armónicas que los tejidos corporales circundantes no producen11. Al recibir con un elemento de alta frecuencia, esto asegura que solo se detecten las señales de microburbujas. Dado que las microburbujas están confinadas a los vasos sanguíneos, el resultado es una imagen angiográfica de la morfología de los vasos sanguíneos. AA es un método poderoso para obtener imágenes del accidente cerebrovascular isquémico, ya que las microburbujas que fluyen a través del sistema circulatorio no pueden fluir a través de los vasos bloqueados. Esto permite que AA detecte regiones del cerebro que no están perfundidas debido a un accidente cerebrovascular isquémico, lo que indica la región del infarto.
La investigación preclínica del accidente cerebrovascular isquémico generalmente se basa en el uso de histología y pruebas conductuales para evaluar la ubicación y la gravedad del accidente cerebrovascular. La tinción con cloruro de trifeniltetrazolio (TTC) es un análisis histológico común utilizado para determinar el volumen del infarto sistólico. Sin embargo, solo puede ser utilizado en un punto final, ya que requiere que el animal sea sacrificado12. Las pruebas de comportamiento pueden ser utilizadas para determinar el deterioro de la función motora en múltiples puntos de tiempo, pero no pueden proporcionar valores anatómicos o fisiológicos cuantitativos13. La imagen biomédica proporciona un enfoque más cuantitativo para estudiar los efectos del accidente cerebrovascular isquémico de forma no invasiva y longitudinal 9,14,15. Sin embargo, las tecnologías de imagen existentes (como la resonancia magnética [MRI] de animales pequeños) pueden tener un alto costo, no pueden proporcionar información estructural y funcional concurrente o tienen una profundidad de penetración limitada (como la mayoría de las técnicas de imágenes ópticas).
Aquí, combinamos tomografía fotoacústica, ecográfica y angiográfica (PAUSAT; ver diagrama del sistema en la Figura 1), que permite información estructural y funcional complementaria de la perfusión sanguínea y la oxigenación después del accidente cerebrovascular isquémico16. Estos son dos aspectos importantes para evaluar la gravedad de la lesión y monitorear la recuperación o la respuesta a los tratamientos. El uso de estos métodos de imagen integrados puede aumentar la cantidad de información obtenida por cada animal, reduciendo el número de animales requeridos y proporcionando más información en el estudio de posibles tratamientos para el accidente cerebrovascular isquémico.
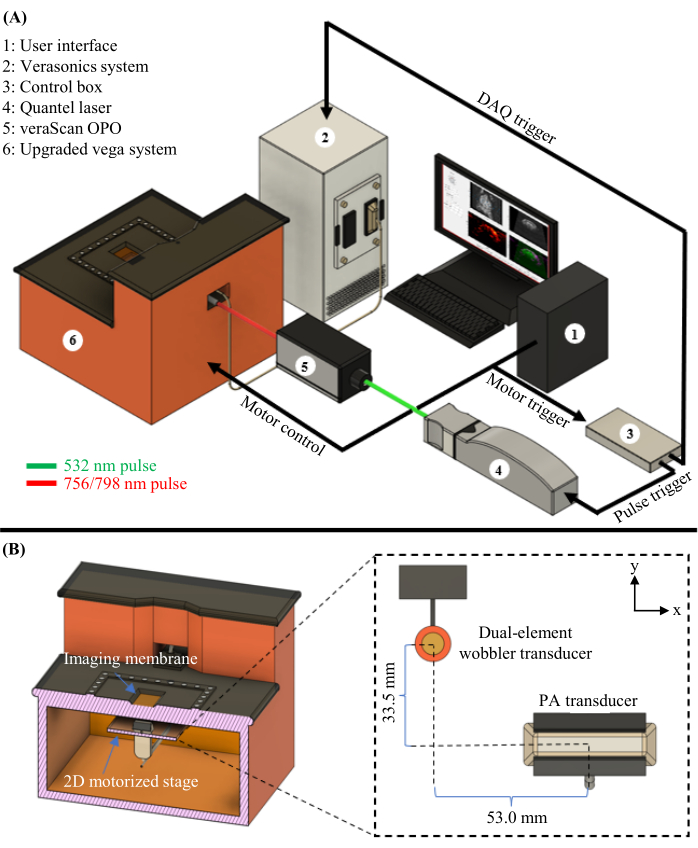
Figura 1: Diagrama PAUSAT. (A) Esquema completo del sistema PAUSAT, incluyendo el láser y el OPO utilizados para PAT. (B) Vista interior del sistema PAUSAT, incluidos dos transductores de ultrasonido. El transductor wobbler de doble elemento se utiliza tanto para ultrasonido en modo B como para AA, y el transductor de matriz lineal se utiliza para PAT. Ambos transductores están montados en la misma etapa motorizada 2D, lo que permite que el escaneo genere datos volumétricos. Esta cifra se ha modificado de16. Haga clic aquí para ver una versión más grande de esta figura.
Access restricted. Please log in or start a trial to view this content.
Protocolo
Todos los procedimientos con animales fueron aprobados por el Comité de Cuidado y Uso de Animales del Centro Médico de la Universidad de Duke y se llevaron a cabo de acuerdo con la Política sobre Cuidado Humanitario y Uso de Animales de Laboratorio del Servicio de Salud Pública de los Estados Unidos. Para estos estudios se utilizaron ratones machos y hembras C57BL/6J (ver Tabla de materiales). Se tomaron imágenes de un mínimo de tres animales por grupo modelo de accidente cerebrovascular. Consulte la figura 2 para ver el flujo de trabajo seguido en este protocolo.
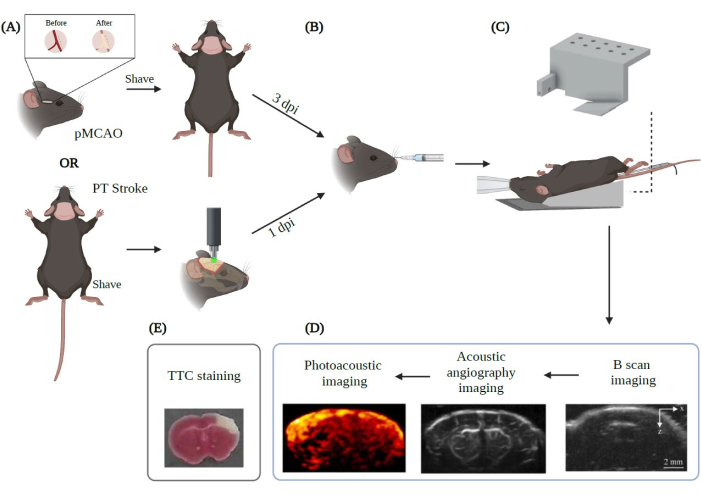
Figura 2: Resumen del procedimiento experimental para la imagen PAUSAT aplicada al ictus. Creado con Biorender.com. La figura muestra el flujo de trabajo del procedimiento de imagen a partir de (A) los dos modelos principales de accidente cerebrovascular (pMCAO y accidente cerebrovascular PT). (B) Se debe realizar una inyección retroorbitaria de las microburbujas antes de colocar al animal en la membrana PAUSAT. (C) Una máscara que proporcione anestesia continua y una almohadilla térmica para mantener estable la temperatura corporal del animal se requieren en esta configuración. El cuerpo del animal se coloca en la almohadilla térmica mientras la cabeza descansa sobre la membrana del sistema. (D) El orden de adquisición de la imagen también se muestra en la figura. (E) La tinción TTC se realiza para validar nuestros resultados en este estudio. DPI: días después de la lesión. Haga clic aquí para ver una versión más grande de esta figura.
1. Inducir el modelo de ratón de trazo
- Oclusión permanente de la arteria cerebral media (pMCAO) con ligadura de la arteria carótida común (CCA).
NOTA: Brevemente, realizar ligadura permanente del ACC derecho y electrocauterización posterior de la arteria cerebral media derecha (ACM)17. Este procedimiento limita el flujo sanguíneo cerebral en la corteza derecha del cerebro, causando un accidente cerebrovascular isquémico18.- Inducir anestesia en una cámara de inducción utilizando una mezcla inhalatoria de isoflurano al 5,0% en 30% O2/70%N2 hasta la pérdida de conciencia (reconocida como pérdida del reflejo pedal).
- Intubar al animal con un catéter de 20 G (Tabla de materiales) y conectarlo a un ventilador automático. Establezca el caudal en función del peso corporal del animal y mantenga al animal anestesiado con isoflurano al 1,5% -2,0% en 30% O 2/70% N2.
- Usando una lámpara de calentamiento y una sonda rectal conectada a un dispositivo controlador de temperatura, mantenga la temperatura corporal del animal a 37 ° C.
- Ponga una gota de ungüento lubricante para los ojos en los ojos del ratón.
- Coloque al animal en posición supina y retire el pelo del área del cuello con un recortador de pelo.
- Limpie el área de la piel usando primero un hisopo de algodón con povidona yodada y luego usando una almohadilla estéril con etanol al 70%. Realice esto tres veces.
- Verifique la profundidad de la anestesia y la ausencia de dolor pellizcando ligeramente la pata posterior del animal.
- Haga una incisión sagital de 0,8 cm en la línea media del cuello y exponga el CCA derecho.
- Prepare una sutura para la ligadura CCA disociando una sutura de seda 4-0 en hilos más delgados que componen el hilo principal. Utilice una longitud de 1,5 cm de uno de los subhilos para ligar permanentemente el CCA.
NOTA: Después de apretar el nudo, retire el exceso de hilo cortando la extensión a una distancia de 1-2 mm del nudo. - Aplique una gota de bupivacaína antes de cerrar la herida.
- Cierre la incisión con suturas quirúrgicas de seda 4-0 interrumpidas y aplique ungüento antibiótico triple en la superficie para prevenir la infección.
- Mueva el ratón para exponer el lado lateral derecho del cuerpo del animal.
-
Retire el vello en la región entre la oreja y el área de los ojos con un recortador de pelo.
-
Desinfecte el área quirúrgica con un hisopo de algodón con povidona yodada, seguido de una almohadilla estéril con etanol al 70%. Repita este paso tres veces.
-
Coloque una cortina estéril para asegurar el área quirúrgica. Luego, haga una incisión de 0,5 cm entre el ojo derecho y la oreja del animal, exponiendo la articulación entre el cráneo y el músculo temporal.
- Usando un bucle de cauterio, cauterizar el músculo para separarlo del cráneo y exponer el área del MCA.
- Perfore una ventana de 0.2 mm2 para exponer el MCA usando un taladro eléctrico, y use electrocauterio en el MCA para ocluir el flujo sanguíneo.
NOTA: Un solo pulso al 80% de intensidad de potencia es suficiente para cauterizar el MCA. - Usando una jeringa de 1 ml conectada a una aguja de 27G, aplique una gota de bupivacaína (Tabla de materiales) en el sitio quirúrgico.
- Cierre la incisión de la piel con suturas de monofilamento transparente 6-0 interrumpidas y aplique ungüento antibiótico triple en la superficie para prevenir infecciones.
- Después de completar la cirugía, transfiera el animal a una incubadora con temperatura controlada (32 ° C) y permita que el animal se recupere.
- Después de 2 h, transfiera al animal a su jaula de origen y proporcione comida y agua ad libitum.
- Accidente cerebrovascular fototrombótico (accidente cerebrovascular PT)
NOTA: Brevemente, el accidente cerebrovascular PT se realiza iluminando Rosa de Bengala dentro de los vasos en el cerebro. La Rosa de Bengala se administra por vía intraperitoneal, y una vez que se ha distribuido bien por todo el cuerpo (5 min), se ilumina con una luz verde fría, que activa la Rosa de Bengala para generar especies reactivas de oxígeno (ROS). Estas ROS dañan la membrana de las células endoteliales, creando trombos dentro de toda el área iluminada y dando lugar a la interrupción del flujo sanguíneo cerebrallocal 19.- Inducir anestesia en una cámara de inducción utilizando una mezcla inhalatoria de isoflurano al 5,0% en 30% O2/70%N2 hasta la pérdida de conciencia (reconocida como pérdida del reflejo pedal).
- Coloque al animal en un marco estereotáxico, manteniendo al animal anestesiado usando una máscara e isoflurano al 1.5% -2.0% en 30% O 2/70% N2.
- Mantener al animal a 37 °C utilizando un calentador de recirculación de agua caliente y una sonda rectal para medir la temperatura corporal del animal.
- Ponga una gota de ungüento lubricante para los ojos en los ojos del ratón.
- Afeite la cabeza del animal con un recortador de pelo.
- Limpie el área del cuero cabelludo afeitado tres veces, primero usando un hisopo de algodón con povidona yodada y luego usando una almohadilla estéril con etanol al 70%.
- Verifique la ausencia de dolor pellizcando ligeramente la pata posterior del animal.
- Haga una incisión sagital de 1,4 cm en la línea media del cuero cabelludo con un bisturí y exponga el cráneo.
- Usando un lápiz afilado, haga una marca a 1,5 mm desde el bregma hacia el lado derecho.
- Coloque un agujero circular de 2,5 mm de diámetro centrado en la marca de 1,5 mm.
NOTA: Se puede hacer un cuadrado que contiene un agujero circular utilizando cinta negra de doble cara y haciendo una abertura de 2,5 mm de diámetro en el centro utilizando una herramienta perforadora de un solo orificio del tamaño mencionado. - Coloque la luz fría verde en el agujero circular, manteniendo el espacio entre la luz y el agujero de alfiler al mínimo.
- Cubra el área con papel de aluminio para evitar la propagación de la luz.
- Una vez que la configuración esté lista, inyecte al animal por vía intraperitoneal con 10 mg / kg de Rosa de Bengala (10 mg / ml en 1x solución salina tamponada con fosfato [PBS]) y espere 5 minutos.
- Después de 5 minutos, encienda la fuente de luz fría (intensidad: 4.25) y mantenga la exposición durante 15 minutos.
- A continuación, apague la luz fría y verifique el accidente cerebrovascular a simple vista (se espera que el área sea más blanca que el área circundante) o utilizando dispositivos externos para medir el flujo sanguíneo cerebral (por ejemplo, mediante el uso de imágenes de contraste con moteado láser (Tabla de materiales; consulte el paso 5.1).
- Usando una jeringa de 1 ml conectada a una aguja de 27G, aplique una gota de bupivacaína (Tabla de materiales) en el sitio quirúrgico.
- Cierre la incisión de la piel con suturas de monofilamento transparente 6-0 interrumpidas y aplique ungüento antibiótico triple en la superficie para prevenir la infección.
- Después de completar la cirugía, transfiera el animal a una incubadora con temperatura controlada (32 ° C) y permita que el animal se recupere.
- Después de 2 h, transfiera al animal a su jaula de origen y proporcione comida y agua ad libitum.
2. Preparación de PAUSAT para imágenes
- Encienda el láser de 532 nm y déjelo encendido durante 15 minutos para calentar.
- Prepare la plataforma de imágenes para el animal anestesiado.
- Coloque una rampa personalizada (Figura 2C) unida a la etapa ajustable manualmente (Tabla de materiales) junto a la membrana de imágenes.
- Coloque un soporte para dientes de ratón con el tubo de respiración conectado a la rampa personalizada y asegure una almohadilla térmica en la superficie de la rampa.
- Después de que el láser se haya calentado, verifique que la trayectoria del láser y el acoplamiento en el haz de fibra estén bien alineados utilizando una tarjeta detectora de infrarrojo cercano (Tabla de materiales) colocando la tarjeta delante de la entrada del haz de fibra y asegurándose de que la luz láser ingrese al paquete.
NOTA: Ajuste los espejos de trayectoria láser según sea necesario para asegurarse de que la entrada láser esté centrada con la entrada del haz de fibra.
3. Preparación del animal para PAUSAT
NOTA: PAUSAT se realiza 1 día después de la cirugía de accidente cerebrovascular PT o 3 días después de la cirugía pMCAO. La preparación de PAUSAT para imágenes (paso 2) dura aproximadamente 20 minutos y debe hacerse inmediatamente antes de preparar al animal para PAUSAT.
- Inducir la anestesia en una cámara de inducción utilizando una mezcla de inhalación de isoflurano al 5% mezclado con 30% O2/70%N2 hasta la pérdida de conciencia (reconocida como una pérdida del reflejo pedal).
- Transfiera al animal a una plataforma calentada con un soporte de dientes y una máscara, y mantenga la anestesia al 1,5%-2,0% de isoflurano en 30% O2/70%N2.
- Utilice una lámpara de calentamiento y una sonda rectal conectada a un dispositivo controlador de temperatura para mantener la temperatura corporal del animal a 37 ° C.
- Recorte el pelo en la parte superior de la cabeza del animal usando una afeitadora eléctrica. Incluya la región desde cerca de los ojos hasta detrás de las orejas.
- Afeite el pelo en la parte superior de la cabeza del animal aplicando una crema depilatoria comercial para eliminar completamente el pelo corto restante. Dejar en la piel durante 5-6 minutos, luego limpiar con un hisopo de algodón frotado en agua para ayudar a eliminar completamente la crema. Repita hasta que la piel esté limpia de vello.
NOTA: Para obtener imágenes 1 día después de la cirugía, estos pasos se pueden realizar antes de comenzar la cirugía; a 1 día después del accidente cerebrovascular PT, se pueden omitir. Cuando la adquisición de imágenes PAUSAT se realiza varios días después de la cirugía, se requiere críticamente que se realice este paso. - Una vez que el animal y el sistema estén listos para la obtención de imágenes, y justo antes de transferir el animal a la plataforma del sistema, inyecte una solución de 100 μL de microburbujas en la concentración madre (Tabla de materiales) retroorbitalmente utilizando una aguja de 27 G.
NOTA: Una vez que las burbujas están en circulación en el torrente sanguíneo, hay una cantidad limitada de tiempo para obtener imágenes sin una pérdida significativa de señal (~ 10 min). - Ponga una gota de loción de protección ocular en los ojos del ratón.
NOTA: No se recomienda aplicar lubricante ocular hasta que se realice la inyección retroorbitaria para evitar que sustancias extrañas lleguen al torrente sanguíneo del animal. Por lo tanto, la aplicación de la crema depilatoria debe realizarse lenta y cuidadosamente para evitar acercarse demasiado a los ojos (pero lo suficiente como para exponer la región de interés donde se espera el trazo). La depilación de la crema se realiza con un hisopo de algodón previamente untado en agua, evitando que la crema gotea, lo que puede dañar los ojos.
4. PAUSAT Imágenes
NOTA: Esto se hace para obtener imágenes de las regiones contralaterales e ipsilaterales del cerebro después del accidente cerebrovascular
- Transfiera el ratón a la plataforma de imagen PAUSAT (Tabla de materiales) integrada, colocando el ratón en posición supina en la rampa personalizada (Figura 2C).
- Llene la ventana de imágenes con suficiente agua destilada en la superficie para el acoplamiento acústico.
NOTA: Se recomienda una rampa opcional -impresa con una impresora 3D- para evitar que el cuerpo del animal se moje durante la adquisición de la imagen y mejorar la comodidad del animal. También ayuda a mantener una temperatura corporal estable. Además, la rampa se puede conectar a una etapa manual (Tabla de materiales) para ajustar la profundidad focal del transductor wobbler de doble elemento en relación con la cabeza del ratón. El archivo de diseño de rampa personalizado está disponible a petición de los autores. - Asegure la cabeza del ratón en el soporte del diente y asegure la anestesia y el flujo de aire adecuados.
- Usando una lámpara de calentamiento y una sonda rectal conectada a un dispositivo controlador de temperatura, mantenga la temperatura corporal del animal a 37 ° C.
- Abra la aplicación de imágenes (Tabla de materiales) y navegue hasta el ultrasonido en modo B.
- Utilice la ventana de ultrasonido en vivo para ajustar manualmente la cabeza del ratón a la posición deseada.
- Utilice la ventana de ultrasonido en vivo para ajustar la altura del escenario, de modo que la profundidad focal del transductor (19 mm) esté aproximadamente en el centro del área a fotografiar.
- Imágenes con ultrasonido en modo B
- Ajuste el valor de la frecuencia de transmisión de ultrasonido en modo B (para estos estudios, use 16 MHz).
- Introduzca la información del directorio de guardado en la aplicación de imágenes.
- Utilice la caja flotante para seleccionar la región deseada para la exploración en modo B del cerebro.
- Pulse el botón Adquirir estática .
- Verifique los resultados del escaneo en la aplicación una vez que se complete la adquisición de la imagen para asegurarse de que se haya obtenido la imagen de la región deseada.
NOTA: Evite retrasos innecesarios en la adquisición de imágenes en modo B para garantizar que una concentración suficientemente alta de microburbujas permanezca en el torrente sanguíneo para el AA.
- Diagnóstico por imágenes con AA
- Volver a Adquisición de imágenes.
- Cambie al modo Angiografía acústica en la aplicación de imágenes (Tabla de materiales).
- Introduzca los parámetros del protocolo de escaneo deseados (el más importante de los cuales es el espaciado de fotogramas y el número de fotogramas por posición, que se estableció en 0,2 mm y 10, respectivamente, para estos estudios).
- Pulse el botón Adquirir estática .
NOTA: La adquisición de AA toma más tiempo que el ultrasonido de modo B. - Una vez completado el escaneo, verifique los resultados del escaneo en Análisis de imagen para asegurarse de que la calidad de la imagen sea la esperada.
NOTA: Para el modo AA, se puede adquirir un volumen de todo el cerebro más representativo repitiendo una segunda exploración a una profundidad focal diferente dentro del cerebro y luego recombinando las imágenes con el posprocesamiento adecuado (ver Figura 3).
- Imagen con tomografía fotoacústica
- Abra la aplicación del oscilador paramétrico óptico (OPO) (Tabla de materiales) y configúrela en 756 nm.
NOTA: Las OPO pueden salirse fácilmente de la calibración, por lo que antes del experimento, asegúrese de que la OPO esté calibrada correctamente utilizando un espectrómetro independiente. - Traduzca manualmente el transductor de matriz lineal a las coordenadas previamente determinadas para asegurarse de que los volúmenes wobbler y los volúmenes de matriz lineal se registran automáticamente.
NOTA: Es fundamental que se realice de antemano un experimento de registro conjunto utilizando una cuadrícula fantasma para determinar la distancia exacta necesaria para traducir la etapa, de modo que los datos resultantes de ambos transductores se registren conjuntamente en 3D. - Abra la aplicación láser y encienda el láser de 532 nm.
- Usando un medidor de potencia láser, mida la energía de la salida del láser y asegúrese de que sea la energía deseada (~ 10 mJ por pulso se utilizó para estos estudios).
- Seleccione los parámetros de escaneo deseados para PAT (tamaño de paso de 0,4 mm, longitud de escaneo de 20 mm y 10 fotogramas promediados por posición).
- Abra el programa MATLAB (Table of Materials) del sistema de adquisición de datos de ultrasonido y pulse el botón Ejecutar .
- Adquiera el escaneo PAT presionando el botón Inicio .
- Una vez finalizado el análisis, abra el programa de guardado de MATLAB. Cambie el nombre de guardar al nombre de archivo deseado y pulse el botón Ejecutar .
- Cambie la longitud de onda OPO a 798 nm y repita los pasos de 4.10.3 a 4.10.8.
NOTA: Para un estudio longitudinal, se recomienda permitir que el animal se recupere colocándolo en una incubadora y bajo observación durante unas horas (siguiendo los pasos 1.1.18 y 1.1.19). Si se desea validar el resultado, continúe con la sección 5 inmediatamente después de la obtención de imágenes PAUSAT.
- Abra la aplicación del oscilador paramétrico óptico (OPO) (Tabla de materiales) y configúrela en 756 nm.
5. Opcional: Validación de resultados
- Imágenes de contraste moteado láser (LSCI).
- Anestesiar al animal usando isoflurano al 1,5%-2,0% en 30% O2/70%N2.
- Coloque al animal en un marco estereotáxico, manteniendo al animal anestesiado con una máscara y la anestesia inhalatoria mencionada anteriormente.
- Mantener al animal a 37 °C utilizando un calentador de recirculación de agua caliente y una sonda rectal para medir la temperatura corporal del animal.
- Ponga una gota de loción de protección ocular en los ojos del ratón.
- Verifique la ausencia de dolor pellizcando ligeramente la pata posterior del animal.
- Retire el pelo del cuero cabelludo del animal con un recortador de pelo.
- Desinfecte el área quirúrgica con un hisopo de algodón con povidona yodada, seguido de una almohadilla estéril con etanol al 70%. Repita este paso tres veces.
- Haga una incisión sagital de 1,4 mm en la línea media del cuero cabelludo y exponga el cráneo. Use fórceps para sostener el cuero cabelludo y evitar que ocupe el área del cerebro para escanear.
- Aplique algunas gotas de solución salina en el cráneo y coloque el dispositivo del sistema de contraste de moteado láser (Tabla de materiales) sobre la cabeza del animal.
- En el menú Archivo , configure el dispositivo en modo en línea, incluido en el submenú Modo de trabajo.
- Seleccione la carpeta de almacenamiento de imágenes predeterminada en el menú Archivo y en el submenú Guardar configuración .
- En el menú Fuente de luz, conecte el láser guía ("Láser encendido") y la luz blanca ("Luz blanca encendida") para ubicar la ventana de imágenes en la posición correcta.
- En el menú Configuración , seleccione Configuración de ampliación, mueva el cursor manualmente a 2,5 y pulse Aplicar y Aceptar para guardar la configuración.
- Ajuste el enfoque moviendo manualmente la barra de enfoque ubicada en el submenú superior de la página principal.
- En el menú Configuración, seleccione Configuración de umbral de pseudocolor, ajuste el umbral como desee y pulse Aplicar y Aceptar para guardar la configuración.
- En el menú Fuente de luz, desconecte el láser guía ("Láser apagado") y la luz blanca ("Luz blanca apagada") antes de capturar la imagen.
- Capture la imagen seleccionando el símbolo Reproducir en el submenú superior de la página principal.
- Tinción de cloruro de trifeniltetrazolio (TTC)
- Anestesiar profundamente al animal utilizando isoflurano al 5% en 30% O2/70%N2.
- Una vez que el animal haya dejado de respirar, decapitarlo con unas tijeras afiladas.
- Retire toda la piel alrededor de la cabeza y los músculos en el área del cuello.
- Haga un corte sagital en la parte occipital del cráneo hasta que llegue al hueso parietal.
- Haga un corte horizontal (~5 mm) en el lado izquierdo y derecho debajo del vaso sanguíneo. Extraer el hueso occipital del cráneo con fórceps rectos.
- Haga un corte (~5 mm) en la sutura frontonasal del cráneo.
- Haga un corte sagital (~ 10-15 mm) en la línea media del cráneo, entre los hemisferios, y asegúrese de que estén completamente separados.
- Usando tijeras curvas de tamaño #7, retire los huesos parietales izquierdo y derecho del cráneo desde el centro hacia los lados.
- Transfiera el cerebro a un recipiente lleno con 5 ml de PBS 1x helado y manténgalo en hielo durante 10 minutos.
- Transfiera el cerebro a una matriz cerebral de acero inoxidable (secciones de 1 mm de espesor).
- Seccionar el cerebro en secciones coronales de 1 mm usando cuchillas de afeitar desechables (Tabla de materiales).
- Sosteniendo las cuchillas por sus lados, transfiéralas a un recipiente lleno de PBS helado 1x.
- Separe cuidadosamente las secciones de las cuchillas una por una.
- Transfiera las rebanadas de cerebro a una placa de Petri de 70 mm de diámetro que contenga 5 ml de TTC al 2% (Tabla de materiales, 3) en 1x PBS.
- Incubar durante 15 min en la oscuridad a temperatura ambiente (R/T).
- Después de 15 minutos, deseche el TTC, reemplácelo con 3 ml de formalina e incube en la oscuridad durante al menos 30 minutos a R/T.
- Finalmente, transfiera las rebanadas de cerebro a una película de plástico transparente y escanee las muestras, incluida una regla en la imagen de escaneo como referencia para futuras mediciones.
Access restricted. Please log in or start a trial to view this content.
Resultados
Imágenes de la morfología de los vasos sanguíneos en el cerebro
AA genera imágenes de morfología de vasos sanguíneos excitando microburbujas en el sistema circulatorio a su frecuencia resonante y recibiendo la respuesta súper armónica de las microburbujas. Mediante el uso de la rampa personalizada (Figura 2C) conectada a una etapa ajustable manualmente, podemos obtener imágenes del cerebro del ratón con modo AA a dos profundidades focales diferentes. Cuando se d...
Access restricted. Please log in or start a trial to view this content.
Discusión
Hay algunos aspectos vitales de este método que, si se hacen incorrectamente, pueden conducir a una disminución significativa de la calidad de imagen y el análisis cuantitativo. El resultado más común del error del usuario en las imágenes PAUSAT es la falta de señal o la intensidad de señal muy baja, los cuales pueden ocurrir por una variedad de razones. Una de esas razones es un problema con el acoplamiento acústico. Las grandes burbujas de aire en el agua que rodea la cabeza del ratón durante la obtención de...
Access restricted. Please log in or start a trial to view this content.
Divulgaciones
Los autores declaran no tener ningún conflicto de intereses en este trabajo.
Agradecimientos
Los autores desean agradecer al equipo de ingeniería de SonoVol Inc. por su soporte técnico. Este trabajo fue parcialmente patrocinado por el Premio de Ciencias Colaborativas de la Asociación Americana del Corazón (18CSA34080277), a J. Yao y W. Yang; Los Institutos Nacionales de Salud de los Estados Unidos (NIH) otorgan R21EB027981, R21 EB027304, RF1 NS115581 (Iniciativa BRAIN), R01 NS111039, R01 EB028143; El premio CAREER de la Fundación Nacional de Ciencias de los Estados Unidos (NSF) 2144788; la Beca de la Iniciativa Chan Zuckerberg (2020-226178), a J. Yao; y los NIH otorgan R21NS127163 y R01NS099590 a W. Yang.
Access restricted. Please log in or start a trial to view this content.
Materiales
| Name | Company | Catalog Number | Comments |
| 20 GA catheter | BD Insyte Autoguard Winged | 381534 | For mouse intubation |
| 2,3,5-Triphenyltetrazolium chloride | Sigma | T8877 | Necessary for TTC-staining brain for validation |
| 532nm Laser | Quantel | Q-smart 850 | Laser used to pump the OPO for PAT |
| Automatic Ventilator Rovent Jr. | Kent Scientific | RV-JR | To keep mice under anesthesia during surgical procedure |
| Black braided silk 4-0 USP | Surgical Specialties | SP116 | Used for sutures on the neck for pMCAO surgery |
| Bupivacaine | Hospira | 0409-1159-18 | Used prior to closing wounds during surgical procedure |
| C57BL/6 Mice | Jackson Lab | #000664 | Mice used for studying ischemic stroke (2-6 month old male/female) |
| Clear suture | Ethicon | 8606 | Used for closing wound (PT stroke and pMCAO). A clear suture won't interfere with PAT |
| Cold Light LED | Schott | KL 1600 | Needed to create PT stroke |
| Disposable Razor Blade | Accutec Blades | 74-0002 | For sectioning mouse brain |
| Electric drill | JSDA | JD-700 | Used to expose MCA during pMCAO procedure |
| Electrocauterization tool | Wet-Field | Wet-Field Bipolar-RG | Stops blood flow after drilling during pMCAO procedure |
| Hair removal gel | Veet | 8282651 | Used to remove hair from mouse prior to imaging |
| High Temperature Cautery Loop Tip | BOVIE Medical Corporation | REF AA03 | Used to avoid bleeding when separating the temporal muscle from the skull |
| IR Detector Card | Thorlabs | VRC5 | Used to ensure light path is aligned |
| Laser Power Meter | Ophir | StarBright, P/N 7Z01580 | Can be used to calibrate the laser energy prior to imaging |
| Laser Speckle Imaging System | RWD Life Science Co. | RFLSI-III | Can be used to validate stroke surgery success |
| Lubricant Eye Ointment | Soothe | AB31336 | Can be used to avoid drying of the eyes |
| Manually adjustable stage | Thorlabs | L490 | Used with custom ramp for multiple focal depth AA imaging |
| Modified Vega Imaging System | Perkin Elmer | LLA00061 | System containing both B-mode/AA and PAT transducers |
| Optical Parametric Oscillator | Quantel | versaScan-L532 | Allows for tuning of excitation wavelength in a large range |
| Programmable Ultrasound System | Verasonics | Vantage 256 | Used for PAT part of system |
| Rose Bengal | Sigma | 330000 | Necessary to induce PT stroke |
| Suture | LOOK | SP116 | Used for permanent ligation of CCA |
| Temperature Contoller | Physitemp | TCAT-2 | Used to maintain stable body temperature of mice during procedures |
| VesselVue Microbubbles | Perkin Elmer | P-4007001 | Used for acoustic angiography (2.43 × 10^9 microbubbles/mL) |
Referencias
- Durukan, A., Tatlisumak, T. Acute ischemic stroke: overview of major experimental rodent models, pathophysiology, and therapy of focal cerebral ischemia. Pharmacology Biochemistry and Behavior. 87 (1), 179-197 (2007).
- Vander Worp, H. B., van Gijn, J. Clinical Practice. Acute ischemic stroke. The New England Journal of Medicine. 357 (6), 572-579 (2007).
- Tannenbaum, J., Bennett, B. T. Russell and Burch's 3Rs then and now: the need for clarity in definition and purpose. Journal of the American Association for Laboratory Animal Science. 54 (2), 120-132 (2015).
- Hochrainer, K., Yang, W. Stroke proteomics: from discovery to diagnostic and therapeutic applications. Circulation Research. 130 (8), 1145-1166 (2022).
- Wang, L. V., Yao, J. A practical guide to photoacoustic tomography in the life sciences. Nature Methods. 13 (8), 627-638 (2016).
- Aldrich, J. E. Basic physics of ultrasound imaging. Critical Care Medicine. 35 (5), S131-S137 (2007).
- Jacques, S. L. Optical properties of biological tissues: a review. Physics in Medicine and Biology. 58 (11), R37-R61 (2013).
- Li, M., Tang, Y., Yao, J. Photoacoustic tomography of blood oxygenation: a mini review. Photoacoustics. 10, 65-73 (2018).
- Menozzi, L., Yang, W., Feng, W., Yao, J. Sound out the impaired perfusion: Photoacoustic imaging in preclinical ischemic stroke. Frontiers in Neuroscience. 16, 1055552(2022).
- Gessner, R. C., Frederick, C. B., Foster, F. S., Dayton, P. A. Acoustic angiography: a new imaging modality for assessing microvasculature architecture. International Journal of Biomedical Imaging. 2013, 936593(2013).
- Dayton, P. A., Rychak, J. J. Molecular ultrasound imaging using microbubble contrast agents. Frontiers in Bioscience. 12, 5124-5142 (2007).
- Isayama, K., Pitts, L. H., Nishimura, M. C. Evaluation of 2, 3, 5-triphenyitetrazolium chloride staining to delineate rat brain infarcts. Stroke. 22 (11), 1394-1398 (1991).
- Ruan, J., Yao, Y. Behavioral tests in rodent models of stroke. Brain Hemorrhages. 1 (4), 171-184 (2020).
- Parthasarathy, A. B., Kazmi, S. M. S., Dunn, A. K. Quantitative imaging of ischemic stroke through thinned skull in mice with Multi Exposure Speckle Imaging. Biomedical Optics Express. 1 (1), 246-259 (2010).
- Hingot, V., et al. Early ultrafast ultrasound imaging of cerebral perfusion correlates with ischemic stroke outcomes and responses to treatment in mice. Theranostics. 10 (17), 7480-7491 (2020).
- Menozzi, L., et al. Three-dimensional non-invasive brain imaging of ischemic stroke by integrated photoacoustic, ultrasound and angiographic tomography (PAUSAT). Photoacoustics. 29, 100444(2022).
- Llovera, G., Roth, S., Plesnila, N., Veltkamp, R., Liesz, A. Modeling stroke in mice: permanent coagulation of the distal middle cerebral artery. Journal of Visualized Experiments. (89), e51729(2014).
- Trotman-Lucas, M., Kelly, M. E., Janus, J., Fern, R., Gibson, C. L. An alternative surgical approach reduces variability following filament induction of experimental stroke in mice. Disease Models & Mechanisms. 10 (7), 931-938 (2017).
- Labat-Gest, V., Tomasi, S. Photothrombotic ischemia: a minimally invasive and reproducible photochemical cortical lesion model for mouse stroke studies. Journal of Visualized Experiments. (76), e50370(2013).
- Matsumoto, Y., et al. Visualising peripheral arterioles and venules through high-resolution and large-area photoacoustic imaging. Scientific Reports. 8 (1), 14930(2018).
- Xu, Y., Wang, L. V., Ambartsoumian, G., Kuchment, P. Reconstructions in limited-view thermoacoustic tomography. Medical Physics. 31 (4), 724-733 (2004).
- Yal Tang,, et al. High-fidelity deep functional photoacoustic tomography enhanced by virtual point sources. Photoacoustics. 29, 100450(2023).
- Zheng, W., Huang, C., Zhang, H., Xia, J. Slit-based photoacoustic tomography with co-planar light illumination and acoustic detection for high-resolution vascular imaging in human using a linear transducer array. Biomedical Engineering Letters. 12 (2), 125-133 (2022).
- Wang, Y., et al. Slit-enabled linear-array photoacoustic tomography with near isotropic spatial resolution in three dimensions. Optics Letters. 41 (1), 127-130 (2016).
- Vu, T., Li, M., Humayun, H., Zhou, Y., Yao, J. A generative adversarial network for artifact removal in photoacoustic computed tomography with a linear-array transducer. Experimental Biology and Medicine. 245 (7), 597-605 (2020).
- Zhang, H., et al. Deep-E: A fully-dense neural network for improving the elevation resolution in linear-array-based photoacoustic tomography. IEEE Transactions on Medical Imaging. 41 (5), 1279-1288 (2022).
- Hauptmann, A., et al. Model-based learning for accelerated, limited-view 3-D photoacoustic tomography. IEEE Transactions on Medical Imaging. 37 (6), 1382-1393 (2018).
- Li, M., et al. Three-dimensional deep-tissue functional and molecular imaging by integrated photoacoustic, ultrasound, and angiographic tomography (PAUSAT). IEEE Transactions on Medical Imaging. 41 (10), 2704-2714 (2022).
Access restricted. Please log in or start a trial to view this content.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados