Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Placage métal-composite sans bain localisé par électrostamping
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Présenté ici est un protocole d’électroplaque sans bain, où une pâte de sel métallique stagnante contenant des particules composites sont réduites pour former des composites métalliques à charge élevée. Cette méthode répond aux défis auxquels sont confrontées d’autres formes courantes d’électroplaque (jet, brosse, bain) d’intégration de particules composites dans la matrice métallique.
Résumé
Le placage composite avec des particules intégrées dans la matrice métallique peut améliorer les propriétés du revêtement métallique pour le rendre plus ou moins conductrice, dure, durable, lubrifiée ou fluorescente. Cependant, il peut être plus difficile que le placage en métal, parce que les particules composites sont soit 1) non chargées de sorte qu’ils n’ont pas une forte attraction électrostatique à la cathode, 2) sont hygroscopiques et sont bloqués par une coquille d’hydratation, ou 3) trop grand pour rester stagnant à la cathode tout en remuant. Ici, nous décrivons les détails d’une méthode de placage sans bain qui implique des plaques d’anode et de nickel cathodique en sandwich avec une pâte d’électrolyte concentrée aqueuse contenant de grandes particules phosphorescentes hygroscopiques et une membrane hydrophilique. Après l’application d’un potentiel, le nickel métal est déposé autour des particules stagnantes de phosphore, les piégeant dans le film. Les revêtements composites sont caractérisés par une microscopie optique pour la rugosité du film, l’épaisseur et la charge composite de surface. En outre, la spectroscopie de fluorescence peut être employée pour quantifier la luminosité d’illumination de ces films pour évaluer les effets de diverses densités actuelles, durée de revêtement et charge de phosphore.
Introduction
L’électroplaque traditionnelle est largement utilisée pour déposer des couches minces d’une variété de métaux, alliages et composites métalliques sur des surfaces conductrices pour les fonctionnaliser pour l’applicationprévue 1,2,3,4,5,6,7,8,9,10,11,12. Cette méthode ajoute une finition métallique aux pièces utilisées dans la fabrication d’équipements aérospatiaux, automobiles, militaires, médicaux et électroniques. L’objet à plaquer, la cathode, est immergé dans un bain aqueux contenant des précurseurs de sel métallique, qui sont réduits en métal à la surface de l’objet par l’application d’un potentiel chimique ou électrique. Les particules composites non chargées peuvent être incorporées dans le film métallique en les ajoutant au bain pendant le revêtement afin d’améliorer les propriétés du film pour une dureté accrue dans le cas des oxydes métalliques et des carbures, de la douceur avec des polymères ou de la lubrification avec des huilesliquides 12,13. Cependant, parce que ces particules n’ont pas une attirance inhérente à la cathode, le rapport de composite qui est incorporé dans le métal reste faible pour le placagede bain 13,14,15. Ceci est particulièrement problématique pour les grosses particules qui n’adsorbent pas à la cathode assez longtemps pour être incorporées par le film métallique en croissance. En outre, les particules hygroscopiques se solvent dans des solutions aqueuses et leur coquille d’hydratation agit comme une barrière physique entravant le contact avec la cathode16.
Il a été démontré que certaines méthodes prometteuses atténuent cet effet en utilisant des solvants secs non polaires pour enlever complètement la barrièred’hydratation 17,ou en décorant les particules composites de molécules chargées de surfactant16 qui perturbent la coquille d’hydratation pour permettre le contact entre la particule et la cathode. Cependant, parce que ces méthodes impliquent des matières organiques, la contamination au carbone est possible dans le film et la décomposition de ces matières organiques pourrait se produire aux électrodes. Par exemple, les solvants organiques utilisés (DMSO2 et acétamide) sont chauffés à 130 °C dans une atmosphère inerte pour un revêtement sans air; cependant, nous les avons trouvés instables pendant le revêtement dans l’air. En raison du chauffage résistant aux électrodes, les réactions de redox avec des matières organiques peuvent avoir comme conséquence des impuretés ou des emplacements pour la nucléation hétérogène et la croissance des nanoparticules métalliques18. Par conséquent, il est nécessaire d’avoir une méthode d’électroplaque aqueuse sans organique qui réponde au défi de longue date de l’adsorption particule-cathode. Jusqu’à présent, il a été démontré que le revêtement de bain métal-composite intègre des particules jusqu’à quelques micromètres dediamètre 19 et jusqu’à 15 % dechargement 16,17.
En réponse à cela, nous décrivons une méthode inorganique d’électrostamping sans bain qui force les particules composites à s’incruster dans le film à des couvertures de surface élevées malgré leur grande taille et leur nature hygroscopique20. En enlevant le bain, le processus n’implique pas de contenants de liquides de revêtement dangereux et l’objet à plaquer n’a pas besoin d’être submergé. Par conséquent, les objets gros, encombrants ou sensibles à la corrosion ou à l’eau peuvent être plaqués ou « estampillés » dans certaines zones avec le matériau composite. De plus, l’élimination de l’excès d’eau nécessite moins de nettoyage des déchets liquides dangereux.
Ici, nous démontrons cette méthode pour produire des films métalliques fluorescents lumineux en co-déposant de l’europium non toxique et stable dans l’air et du dysprosium dopé, aluminate de strontium (87 ± 30 μm) avec du nickel à des charges élevées (jusqu’à 80%). Cela contraste avec les exemples précédents qui ont été plaqués dans un bain et ont donc été limités à de petits phosphores (nanomètres à quelques micromètres)12. En outre, les films électrodeposited précédemment rapportés fluorent seulement sous la lumière UV à ondes courtes, à l’exception d’un rapport récent qui a grandi 1 - 5 cristaux luminescents d’alumine de strontium de μm dans un film d’alumine avec oxydation d’électrolyte de plasma21. Les films métalliques fluorescents pourraient avoir des applications de grande envergure dans de nombreuses industries impliquant des environnements de faible lumière, y compris l’éclairagedes panneaux routiers 21, l’emplacement de l’équipement d’entretien des aéronefset l’identification 20, décorations automobiles et de jouet, messages invisibles, authentificationdu produit 22, éclairage de sécurité, identification du stress mécanochromique10 et inspection visuelle de l’usure tribologique12,16. Malgré ces utilisations potentielles pour les surfaces métalliques brillantes, cette méthode pourrait également être élargie pour inclure d’autres particules composites grandes et/ou hygroscopiques pour produire une nouvelle variété de revêtements fonctionnels composites métalliques qui n’étaient pas possibles auparavant par électroplacage.
Protocole
1. Préparation des sels de revêtement
MISE EN GARDE : Les sels de nickel et l’acide borique sont toxiques et doivent être manipulés avec l’équipement de protection individuelle approprié comprenant des gants de nitrile, des lunettes et une couche de laboratoire. Les acides forts et les bases doivent être manipulés dans le capot des vapeurs, et tous les déchets chimiques doivent être éliminés sous forme de déchets dangereux.
- À l’aide d’un équilibre, peser les poudres suivantes dans ces rapports: 10.000 g de NiSO4·6H2O, 2.120 g de NiCl2·6H2O, 1.600 g de H3BO3 et combiner dans une fiole ensemble. Voir le tableau 1 pour les concentrations.
- Pesez 1.800 g de SrAl2O4:Eu2+, Dy3+ phosphore ou phosphore alternatif comprenant l’oxyde d’yttrium dopé à l’europium, l’aluminate de magnésium baryum dopé à l’europium, ou remplacez-le par de l’oxyde alternatif, du métal ou des matériaux composites organiques selon l’effet désiré.
REMARQUE : La quantité ajoutée ici peut varier en fonction des propriétés du matériau composite et des qualités souhaitées du film métal-composite. - À l’aide d’un mortier et d’un pilon en porcelaine, moudre la poudre composite pendant environ 10 minutes jusqu’à ce qu’elle devienne une poudre fine.
REMARQUE : Cela ne modifie pas la taille des particules, mais sépare les particules agrégées. - De même, moudre le mélange de sel de l’étape 1.1 en lots jusqu’à ce qu’il devienne une poudre fine.
- Dans un récipient pour le stockage, mélanger le phosphore moulu avec le mélange de sel moulu.
- Peser 0,188 grammes du mélange par cm2 de surface de revêtement, tel que préparé à l’étape 1.5 et ajouter à un récipient avec un dessus ouvert qui est facile d’accès.
- À cela, ajouter 40 μL d’eau par cm2 de surface de revêtement, et remuer pour dissoudre partiellement les sels formant une pâte épaisse. Mets ça de côté.
REMARQUE : Le protocole peut être mis en pause ici.
2. Préparation des électrodes
- À l’aide de ciseaux, couper l’anode à la taille et à la forme qui correspond à l’objet à plaquer. Dans cet exemple, nous préparons une feuille de nickelde 4 cm 2 à enduire, et une anode de nickelde 4 cm 2 est coupée pour correspondre à cela.
REMARQUE : D’autres objets peuvent être enduits, y compris de gros objets. Dans ce cas, sélectionnez la zone de l’objet à enduire et découpez l’anode pour correspondre à la zone de revêtement. - À l’aide d’un coton-tige ou d’un chiffon, nettoyez la surface de la feuille d’anode et de la cathode (surface de l’objet de revêtement) avec de l’hydroxyde de potassium concentré (10 M) ou de la base d’hydroxyde de sodium pour enlever les matières organiques. Ensuite, rincez les surfaces avec de l’eau pour enlever l’excès de base.
- À l’aide d’un coton-tige ou d’un chiffon, activez la surface de l’objet avec de l’acide concentré. Dans le cas du nickel, 37% vol/vol HCl est utilisé, bien que pour l’acier, 10% par volume aqueux HCl peut être plus approprié. Veuillez vous référer aux recommandations d’activation des surfaces métalliques fournies ailleurs afin de déterminer la méthode appropriée pour activer des métaux ou des alliagesspécifiques 23,24.
REMARQUE : Après cette étape, la surface métallique est réactive et la surface commencera à réagir avec de l’oxygène dans l’air pour former une couche d’oxyde. Cela provoquera l’inactivité de la surface, de sorte que les étapes suivantes (2,4 à 3,5) devraient être effectuées dans les 5 prochaines minutes; dans le cas contraire, l’étape 2.3 devrait être répétée avant de se poursuivre.
ATTENTION : Cette étape doit être effectuée dans un capot de fumée pour éviter l’exposition aux vapeurs de HCl. - Déposez rapidement la pâte de revêtement sur l’objet cathodique. Dans ce cas, la cathode est une feuille de nickel de 4 cm2 sur le banc. Couvrez la zone de l’objet à plaquer uniformément et essayez d’éviter les lacunes dans la pâte.
REMARQUE: Dans cet exemple, nous peignons sur cette pâte avec deux scoopulas, cependant, d’autres options peuvent inclure la pulvérisation, trempage ou blading médecin pour augmenter la vitesse et l’efficacité de cette étape. - À l’aide d’un coton-tige ou d’un chiffon, activez l’anode avec de l’acide concentré en trempant l’écouvillon dans l’acide et en frottant doucement la surface cathodique. Dans le cas du nickel, 70% vol/vol HNO3 peuvent être utilisés.
REMARQUE : Cependant, d’autres acides peuvent être plus appropriés pour des métaux et des alliages spécifiques. Veuillez vous référer aux recommandations fournies ailleurs pour que le réaccérable approprié active des surfaces d’anodesspécifiques 23,24.
MISE EN GARDE : Cette étape doit être effectuée dans un capot de fumée pour éviter l’exposition au NO2,un gaz brun toxique qui se forme pendant la réaction. Continuer à traiter la surface jusqu’à ce que la surface devienne grise et texturée. Après cette étape, la surface métallique est réactive et la surface commencera à réagir avec de l’oxygène dans l’air pour former une couche d’oxyde, de sorte que les étapes suivantes doivent être effectuées rapidement pour éviter l’inactivation de l’anode. - Si vous calculez l’efficacité actuelle, utilisez un équilibre analytique pour enregistrer la masse de l’anode et de la cathode.
3. Assemblage et revêtement
- Prédédez une alimentation électrique au courant désiré en mode courant constant ou en tension, si le mode tension constante est souhaité. Dans cet exemple, le mode courant constant est utilisé avec un courant de 0,1 Ampère (0,1 A pour 4 cm2 = 0,025 A/cm2).
REMARQUE : Pour les objets de forme plus grande ou irrégulière, la zone de revêtement peut être prédéterminée avec une grille ou à l’aide d’une photo avec barre d’échelle et d’un logiciel d’imagerie comme ImageJ. Le courant appliqué peut être mis à l’échelle pour offrir la même densité actuelle requise pour la zone de revêtement. - Couper un morceau de feuille de nylon (ou membrane hydrophilique alternative) à une taille plus grande que l’anode afin que l’anode n’entre pas en contact direct avec l’objet cathodique.
- Placez la feuille de nylon sur le dessus de la pâte de revêtement, puis ajoutez une petite quantité de pâte à cela.
- Ensuite, ajouter 1-2 gouttes d’eau d’une pipette pour permettre au sel de se dissoudre partiellement. Les étapes 3.2.1 – 3.3 rendent la feuille de nylon conductrice et permettent le transport de masse des ions à travers l’électrolyte, qui est nécessaire pour équilibrer la charge dans la réaction de revêtement.
- Enfin, ajoutez l’anode activée sur le dessus et attachez le plomb négatif à l’objet cathodique et le plomb positif à l’anode.
REMARQUE : Il pourrait être utile d’enregistrer ces fils de sorte que la configuration reste stationnaire, surtout si l’expérience implique de petits morceaux de papier d’aluminium. C’est moins important pour les gros objets. - Couvrez le système de plastique ou de joint pour aider à retenir l’eau, et appliquez une pression modérée (~100 g par zone de cm2), allumez l’alimentation électrique et continuez à enduire pendant la durée désirée.
- Éteignez l’alimentation électrique et exposez le système.
- Déconnecter les fils, séparer les électrodes et rincer l’objet cathodique avec de l’eau dans un récipient à déchets.
- Tremper les autres articles dans l’eau pour enlever les sels et éliminer cette solution aqueuse dans le contenant de déchets dangereux dûment étiqueté
- En portant des gants, frottez doucement l’objet cathodique à la main pour enlever les particules composites non encoées. Le revêtement est complet et prêt pour la caractérisation.
- À l’aide d’un équilibre analytique, enregistrez la masse de l’anode et de la cathode et trouvez la différence entre ces valeurs et leur masse d’origine.
- Utilisez les lois de l’électrolyse de Faraday pour calculer l’efficacité actuelle. Les grains de beauté théoriques du revêtement métallique peuvent être déterminés à l’aide de l’équation 1.
 Équation 1
Équation 1
où n est la quantité de métal déposé (unités: mol), je suis le courant appliqué, t est le temps de revêtement, F est la constante de Faraday (96485 coulombs par taupe) et z est la charge de l’ion métallique. Calculez cette valeur en fonction des paramètres expérimentaux. - Diviser la masse de dépôt déterminée expérimentalement obtenue à partir des masses de la cathode ou de l’anode (étapes 2.6 et 3.7.3) par la masse théorique perdue (anode) ou gagnée (cathode) pour calculer l’efficacité actuelle à l’aide de l’équation 2.
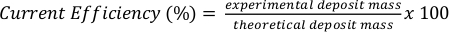 Équation 2
Équation 2
[REMARQUE : À une efficacité actuelle de 100 %, sous tension constante, on s’attend à une masse théorique de dépôt d’environ 1,095 g de nickel ou 12,3 μm de nickel par heure, compte tenu de la superficie de 0,04 A et 4 cm2. De même, sous courant constant, environ 614,6 μm de nickel déposeraient théoriquement par unité de 1 A◊cm-2 après 30 min.]
4. Caractérisation par électrochimie
- Utilisez la chronopotentiométrie pour surveiller les changements de tension sous courant constant, et la chronoampérométrie pour surveiller les changements de courant sous tension constante.
- Allumez le potentiostat et désignez la durée et le courant ou la tension appliqués.
- Répétez les étapes 3.2 – 3.5 pour préparer le revêtement.
- Utilisez un système calibré de 3 électrodes pour normaliser la tension selon une norme de référence.
- Placez une pseudo électrode de référence en fil de platine entre sur la feuille de nylon et sous l’anode. Afin de s’assurer que l’électrode de référence n’entre pas en contact direct avec l’anode, utilisez une feuille de nylon séparée (ou membrane alternative) placée au-dessus de la référence suivie de quelques gouttes d’eau, d’une petite quantité de pâte de revêtement (répéter les étapes 3.2 – 3.3) puis de l’anode.
- Connectez les conduits aux électrodes, scellez, pressez, commencez à enduire et surveillez les changements de tension ou de courant.
5. Caractérisation avec spectroscopie de fluorescence de rendement quantique
- Si le revêtement contient des particules composites fluorescentes, utilisez un fluoromètre équipé d’une sphère d’intégration pour obtenir des mesures absolues du rendement quantique.
- Placez le revêtement dans le stade du fluorure avec le revêtement fluorescent orienté à 45° de la source d’excitation et à 315° du détecteur.
- Enregistrez les spectres de fluorescence à partir d’une longueur d’onde au-dessous de la longueur d’onde d’excitation pour enregistrer les zones du pic d’excitation et du pic de fluorescence.
- Retirez l’échantillon du fluoromètre et répétez l’étape 5.1.2 pour enregistrer le pic d’excitation vierge. Calculer le rendement quantique (QY) à partir des ratios des zones des pics d’excitation et d’émission (Équation 3 et Figure 3B).
 Équation 3
Équation 3
où Aem, Aex et A osont les zones de pointe à la longueur d’onde d’émission de l’échantillon, la longueur d’onde d’excitation de l’échantillon et la longueur d’onde d’excitation du blanc, respectivement.
6. Caractérisation par microscopie optique
- Placez l’échantillon sur la scène d’un microscope optique calibré avec le côté revêtement face aux lentilles et mettre la surface au point.
- Enregistrez les images de surface aux grossissements désirés et aux sites d’échantillonnage de surface.
- À l’aide d’un logiciel d’analyse d’images (ex. ImageJ (IJ 1.46r)), calculer et tracer la couverture de surface et la taille moyenne des particules composites.
- Pour déterminer l’épaisseur du revêtement et les caractéristiques transversales, couper le papier d’aluminium cathodique à l’aide de ciseaux. Réglez le revêtement sur le côté et réajustez la mise au point. Répétez les étapes 6.2 – 6.3.
Résultats
Après avoir suivi ce protocole, une fine couche de métal doit être plaquée sur la surface cathodique et contenir les particules composites qui ont été ajoutées à la pâte de revêtement. L’incorporation de particules fluorescentes ou colorées peut être observée par inspection visuelle à la suite d’un changement d’apparence par rapport à la surface non cintrée (figure 1A1-A3). Pour étudier le pourcentage de couverture de surface des particules composites ...
Discussion
Étapes critiques de l’électrostamping. L’électrostamping sans bain partage bon nombre des mêmes étapes critiques avec l’électroplaque de bain traditionnel. Il s’agit notamment d’un nettoyage approprié des électrodes, le mélange d’ions métalliques dans l’électrolyte et l’application et externe ou chimique (placage électroless) potentiel de causer la réduction du métal sur la cathode. En outre, l’oxydation de l’anode et de la cathode doit être évitée après l’activati...
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ces travaux ont été appuyés par le Programme d’amélioration de la fiabilité et de l’entretien de l’équipement des aéronefs et le Partenariat Patuxent. Townsend a reçu l’appui d’une bourse de recherche de la Faculté de l’ONR. Les auteurs reconnaissent également le soutien général de la faculté et des étudiants du département de chimie et biochimie du SMCM, y compris le soutien de l’équipe de football du SMCM.
matériels
| Name | Company | Catalog Number | Comments |
| 37% M Hydrochloric Acid (aq) | SigmaAldrich | 320331-500ML | corrosive - handle in fume hood |
| 70% Nitric Acid (aq) | SigmaAldrich | 438073-500ML | corrosive - handle in fume hood |
| Barium magnesium aluminate, europium doped (s) | SigmaAldrich | 756512-25G | fine powder |
| Boric Acid (s) | SigmaAldrich | B6768-500G | toxic |
| Cotton Swab | Q-tips | Q-tips Cotton Swabs | |
| ImageJ | National Institutes of Health | IJ 1.46r | free software |
| Nickel (II) chloride hexahydrate (s) | SigmaAldrich | 223387-500G | toxic |
| Nickel (II) sulfate hexahydrate (s) | SigmaAldrich | 227676-500G | toxic |
| Nickel foil (s) | AliExpress | Ni99.999 | |
| Nitrile gloves | Fisher Scientific | 19-149-863B | |
| nylon membrane (s) | Tisch Scientific | RS10133 | |
| Optical Microscope equipped with FTIC filter (470 ± 20 nm) | Nikon | Eclipse 80i | |
| Plastic Wrap | Fisher Scientific | 22-305654 | |
| Porcelain Mortar | Fisher Scientific | FB961A | |
| Porcelain Pestle | Fisher Scientific | FB961K | |
| Potassium Hydroxide (s) | SigmaAldrich | 221473-25G | corrosive |
| Potentiostat with platinum wire | Gamry Instruments | 1000E | |
| Scoopula | Fisher Scientific | 14-357Q | |
| Spectrofluorometer | Photon Technology International | QM-40 | |
| Strontium aluminate, europium and dysprosium doped (s) | GloNation | 756539-25G | powder |
| Variable linear DC power supply | Tekpower | TP3005T | |
| Yttrium oxide, europium doped (s) | SigmaAldrich | 756490-25G | fine powder |
Références
- Hunt, W. H., et al. . Comprehensive Composite Materials. , (2000).
- Hovestad, A., Janssen, L. J. J. Electrochemical codeposition of inert particles in a metallic matrix. Journal of Applied Electrochemistry. 25 (6), 519-527 (1995).
- Zimmerman, A. F., Clark, D. G., Aust, K. T., Erb, U. Pulse electrodeposition of Ni-SiC nanocomposite. Materials Letters. 52 (1), 85-90 (2002).
- Devaneyan, S. P., Senthilvelan, T. Electro Co-deposition and Characterization of SiC in Nickel Metal Matrix Composite Coatings on Aluminium 7075. Procedia Engineering. 97, 1496-1505 (2014).
- Lekka, M., Kouloumbi, N., Gajo, M., Bonora, P. L. Corrosion and wear resistant electrodeposited composite coatings. Electrochimica Acta. 50 (23), 4551-4556 (2005).
- Balaraju, J. N., Sankara Narayanan, T. S. N., Seshadri, S. K. Electroless Ni-P composite coatings. Journal of Applied Electrochemistry. 33 (9), 807-816 (2003).
- Jugović, B., Stevanović, J., Maksimović, M. Electrochemically deposited Ni + WC composite coatings obtained under constant and pulsating current regimes. Journal of Applied Electrochemistry. 34 (2), 175-179 (2004).
- Hilla, F., et al. Fabrication of self-lubricating cobalt coatings on metal surfaces. Nanotechnology. 18 (11), 115703 (2007).
- Abi-Akar, H., Riley, C., Maybee, G. Electrocodeposition of Nickel-Diamond and Cobalt-Chromium Carbide in Low Gravity. Chemistry of Materials. 8 (11), 2601-2610 (1996).
- Zhang, X., Chi, Z., Zhang, Y., Liu, S., Xu, J. Recent Advances in Mechanochromic Luminescent Metal Complexes. Journal of Materials Chemistry C. 1, 3376-3390 (2013).
- Lancsek, T., Feldstein, M. Composite electroless plating. US Patent. , (2006).
- Walsh, F. C., Ponce de Leon, C. A review of the electrodeposition of metal matrix composite coatings by inclusion of particles in a metal layer: an established and diversifying technology. Transactions of the Institute of Materials Finishing. 92 (2), 83-98 (2014).
- Roos, J. R., Celis, J. P., Fransaer, J., Buelens, C. The development of composite plating for advanced materials. Journal of The Minerals, Metals and Materials Society. 42 (11), 60-63 (1990).
- Guglielmi, N. Kinetics of the Deposition of Inert Particles from Electrolytic Baths. Journal of The Electrochemical Society. 119 (8), 1009-1012 (1971).
- Celis, J. P., R, J. R., Buelens, C. A Mathematical Model for the Electrolytic Codeposition of Particles with a Metallic Matrix. Journal of The Electrochemical Society. 134 (6), 1402-1408 (1987).
- He, Y., et al. The monitoring of coating health by in situ luminescent layers. RSC Advances. 5 (53), 42965-42970 (2015).
- Ganapathi, M., et al. Electrodeposition of luminescent composite metal coatings containing rare-earth phosphor particles. Journal of Materials Chemistry. 22 (12), 5514-5522 (2012).
- Monnens, W., Deferm, C., Sniekers, J., Fransaer, J., Binnemans, K. Electrodeposition of indium from non-aqueous electrolytes. Chemical Communications. 55 (33), 4789-4792 (2019).
- Low, C. T. J., Wills, R. G. A., Walsh, F. C. Electrodeposition of composite coatings containing nanoparticles in a metal deposit. Surface and Coatings Technology. 201 (1), 371-383 (2006).
- Gerwitz, C. N., David, H. M., Yan, Y., Shaw, J. P., Townsend, T. K. Bathless Inorganic Composite Nickel Plating: Dry-Cell Stamping of Large Hygroscopic Phosphor Crystals. Advanced Materials Interfaces. 7 (4), (2020).
- Bite, I., et al. Novel method of phosphorescent strontium aluminate coating preparation on aluminum. Materials and Design. 160 (15), 794-802 (2018).
- Feldstein, M. D. Coatings with identification and authentication properties. US Patent. , (2012).
- Rose, I., Whittingham, C. . Nickel Plating Handbook. , (2014).
- Anderson, D. M., et al. . Electroplating Engineering Handbook. , (1996).
- Helle, K., Walsh, F. Electrodeposition of Composite Layers Consisting of Inert Inclusions in a Metal Matrix. Transactions of the Institute of Metal Finishing. 75 (2), 53-58 (1997).
- Kerr, C., Barker, D., Walsh, F., Archer, J. The Electrodeposition of Composite Coatings based on Metal Matrix-Included Particle Deposits. Transactions of the Institute of Metal Finishing. 78 (5), 171-178 (2000).
- Walsh, F. C., Wang, S., Zhou, N. The electrodeposition of composite coatings: Diversity, applications and challenges. Current Opinion in Electrochemistry. 20, 8-19 (2020).
- Feldstein, N. Functional coatings comprising light emitting particles. US Patent. , (1996).
- Feldstein, N. Composite plated articles having light-emitting properties. US Patent. , (1998).
- Zimmerman, E. M. Method of Jet Plating. US Patent. , (1957).
- Schwartz, B. J. Method of Electroplating. United States Patent. , (1961).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon