Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Développement d’une bande immunochromatographique à flux latéral pour la détection rapide et quantitative de composés de petites molécules
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Les bandelettes immunochromatographiques à flux latéral (CSI) à base de membrane sont des outils utiles pour l’autodiagnostic à faible coût et ont été appliquées efficacement à la détection des toxines, de l’indice physiologique et des biomarqueurs cliniques. Dans ce protocole, nous fournissons une description détaillée des étapes de développement d’un immunodosage rapide, sensible et quantitatif à flux latéral (en utilisant les AuNPs comme marqueur et les mAbs comme sonde). La procédure décrit la préparation et la caractérisation de l’or colloïdal, la synthèse du conjugué AuNP-mAb, l’assemblage de la bande immunochromatographique et l’étude méthodologique du test. Les résultats ont montré que les bandelettes finales peuvent être utilisées pour l’autodiagnostic rapide et pratique d’une petite molécule, ce qui peut fournir un outil alternatif dans l’analyse rapide et précise des indices physiologiques et biologiques.
Introduction
Les bandelettes immunochromatographiques à flux latéral (CSI) à base de membrane sont des outils utiles pour une détection rapide et à faible coût. La membrane de nitrocellulose en tant que support et l’or colloïdal en tant que marqueurs des réactifs de diagnostic rapide par chromatographie immunitaire sont la méthode POCT (point of care testing) la plus couramment utilisée, et la portée des tests du projet est plus large. Depuis leur application initiale dans la surveillance pendant la grossesse, leur utilisation a été étendue pour surveiller l’état de coagulation sanguine1,2, les lésions myocardiques3, la médecine vétérinaire4, les résidus de pesticides5, les maladies infectieuses6 et les concentrations de médicaments. D’autres types d’échantillons peuvent être évalués, y compris l’urine, la salive, le sang total, le sérum et d’autres fluides corporels7,8,9.
Au cours des dernières années, de nombreux nouveaux tests ont été développés pour détecter les biomarqueurs dans le diagnostic des troubles, y compris HPLC, UPLC, LC-MS et ELISA, qui sont sensibles et précis, crédibles et spécifiques. Cependant, ces méthodes nécessitent une instrumentation sophistiquée, un prétraitement complexe et des traitements chronophages9. Par conséquent, le développement d’une stratégie de diagnostic au point de service plus rapide et plus pratique pour la détection en temps réel et en temps réel des composés actifs médicinaux est urgent10,11.
La popularité des ICS, en particulier pour les tests courants, est motivée par leur facilité d’utilisation, car ils ne nécessitent pas de professionnels ou de configurations instrumentales élaborées12. En d’autres termes, les personnes qui n’ont pas de formation spéciale peuvent utiliser des bandelettes ou des auto-tests13. Les résultats du test peuvent être obtenus en 5 minutes, ce qui signifie qu’il peut être utilisé pour des inspections de site14. De plus, selon nos calculs, le coût des bandes pourrait être inférieur à 1 RMB15, ce qui signifie que les tests sont peu coûteux pour promouvoir16. Par conséquent, l’ICS est un appareil jetable relativement précis, simple et peu coûteux. Les ICS basés sur l’or colloïdal17,18 sont également appliqués dans la détection rapide de la COVID-19.
Le principe de l’ICS peut être divisé en ICS sandwich et ICS compétitif. La figure 1A est un diagramme schématique du SCI sandwich, qui est principalement utilisé pour détecter les substances macromoléculaires telles que les protéines, y compris les marqueurs tumoraux, les facteurs inflammatoires et la gonadotrophine chorionique humaine (HCG, antigène de grossesse précoce). Dans cette méthode, des anticorps appariés ciblant différents épitopes de l’antigène sont utilisés, et l’anticorps de capture est séché sur la membrane NC comme ligne de test. L’anticorps marqué est séché sur le tampon conjugué et l’anticorps secondaire est utilisé comme ligne de contrôle.
La figure 1B est un diagramme schématique des SCI concurrents, qui est principalement utilisé pour détecter les substances à petites molécules (MWCO < 2000 Da). L’antigène de revêtement est fixé sur la membrane NC comme ligne de test, et l’anticorps marqué est séché sur le tampon conjugué. Au cours de la détection, l’échantillon et l’anticorps marqué circulent à travers la ligne de détection sous action capillaire, et l’antigène enrobé se lie de manière compétitive à l’antigène libre dans l’échantillon et développe une couleur rouge sur la ligne de détection.
Récemment, nous avons décrit la procédure de génération d’anticorps monoclonaux contre des produits naturels19. Dans ce travail, nous avons développé un nouveau test immunologique à flux latéral basé sur l’anti-SSD mA20 préparé pour une détection rapide sur site. Les résultats indiquent que le test d’immunochromatographie est un outil indispensable et pratique pour détecter les composés naturels dérivés de produits.
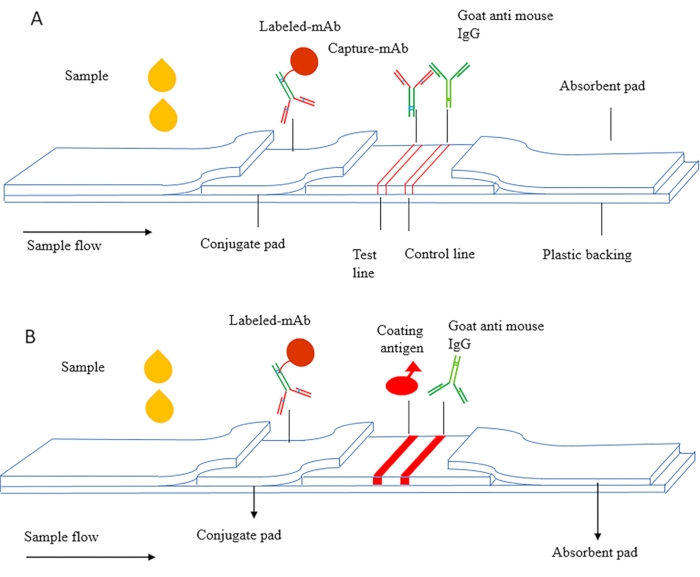
Figure 1 Schéma du test d’immunochromatographie (A) Bandelettes de test immunochromatographiques sandwich. (B) Bandelettes de test immuno chromatographiques compétitives indirectes. Ce chiffre a été modifié à partir de Zhang et al.,201821. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Protocole
Toutes les procédures effectuées dans cette étude ont été approuvées par le Comité d’éthique de l’Université de médecine chinoise de Beijing (numéro d’approbation 2017BZYYL00120).
1. Préparation et caractérisation de l’or colloïdal
REMARQUE: Pour la synthèse de l’or colloïdal, comme l’or colloïdal est facilement adsorbé sur la paroi interne du récipient et est sujet à la précipitation par les impuretés, le récipient pour la synthèse et le stockage de l’or colloïdal doit être soigneusement nettoyé et trempé dans de l’acide (40 mL d’eau distillée, 360 mL d’acide sulfurique concentré, 20 g de dichromate de potassium) ou soumis à un traitement de passivation de surface. Une méthode de réduction de l’acide citrique a été utilisée pour synthétiser l’or colloïdal.
- Allumez l’agitateur magnétique et placez la fiole (250 mL) sur le mélangeur.
- Préparer une solution d’acide de chlorure d’or à 4% et une solution de citrate de sodium à 1%, respectivement.
- Ajouter 120 mL d’eau distillée dans une fiole à fond rond et la chauffer à ébullition sur un agitateur magnétique thermostatique.
- Continuez à bouillir et ajoutez rapidement 0,5 mL d’acide chloroaurique à 4 % et 5 mL de citrate de sodium à 1 %.
- Observez la couleur de la solution. La solution d’acide chloroaurique jaune pâle rend le vin rouge en quelques minutes.
- Continuez à chauffer pendant 10 minutes, jusqu’à ce que la solution passe d’incolore à rouge vin transparent.
- Éteignez l’alimentation du mélangeur magnétique thermostatique, refroidissez à la température ambiante et déplacez le mélange dans une bouteille propre. Conservez-le à 4 °C.
- Déterminer la taille et la morphologie des AuNPs par spectroscopie ultraviolette et imagerie TEM.
REMARQUE: Différentes tailles de particules d’or colloïdaux pour diverses applications peuvent être obtenues en modifiant la proportion de citrate de sodium et d’acide chloroaurique.
2. Synthèse du conjugué AuNPs-mAb
REMARQUE: Étant donné que les anticorps se lient à l’or colloïdal par adsorption électrostatique, les charges à la surface des protéines et de l’or colloïdal affectent directement l’intensité de liaison; par conséquent, la valeur du pH tampon est un facteur important affectant la stabilité du conjugué anticorps-or colloïdal. Les mAbs SSD et anti-SSD sont utilisés comme exemples dans ce protocole.
- Évaluation du pH de couplage
- Ajouter 100 μL de solution de NaCl (10 % m/v) dans huit tubes.
- Ajuster les solutions AuNP à pH 5, 6, 7, 8, 9, 10, 11 et 12 avec 0,1 M K2CO3.
- Ajouter 100 μL de solution d’or colloïdal (pH ajusté 5-12) à huit tubes contenant du NaCl.
- Laissez les solutions reposer pendant plusieurs minutes après le mélange. Observez le changement de couleur de chaque solution de tube et enregistrez le tube qui reste rouge.
- Choisissez la valeur de pH avec le moins d’ajout deK2CO3 et la couleur de la solution stable comme valeur de pH optimale pour la préparation des conjugués AuNP-mAb.
REMARQUE: N’utilisez pas de pH-mètre car la sonde peut être détruite par les AuNPs.
- Évaluation de la quantité d’anticorps
- Ajouter 100 μL de solution de NaCl (10 % m/v) dans huit tubes.
- Ajouter 100 μL de solution d’or colloïdal avec un pH optimal à chaque tube.
- Ajouter les solutions d’anticorps monoclonaux (concentration en protéines 0,1 mg/mL-3,2 mg/mL) aux huit tubes susmentionnés.
- Laissez les solutions reposer pendant plusieurs minutes après le mélange. Observez le changement de couleur de chaque solution de tube et enregistrez le tube qui reste rouge.
- Choisissez la quantité d’anticorps avec la plus faible concentration de mAb et la couleur de la solution stable comme quantité optimale de mAb pour la préparation des conjugués AuNP-mAb.
- Préparer le tampon de resuspension : ajouter 1 M tris-HCl (pH 8,8), 1 % (p/v) BSA, 0,5 % (v/v) Tween 20 et 1 % (v/v) PEG 20000 et bien mélanger.
- Synthèse du conjugué AuNP-mAb
- Prendre 10 mL de solution d’or colloïdal et utiliser 0,1 M K2CO3 pour ajuster la solution à la valeur de pH optimale.
- Ajouter lentement les mAbs SSD à des concentrations appropriées et agiter à température ambiante pendant 30 min.
- Centrifuger le mélange à 83 x g (1 000 tr/min) pendant 10 min à 4 °C. Retirez le précipité, qui contient des impuretés ou de l’or colloïdal précipité.
- Centrifuger le mélange à 8 330 x g (10 000 tr/min) pendant 30 min à 4 °C. Jetez le surnageant, et le précipité est le conjugué colloïdal or-mAb.
- Ajouter le tampon de ressuspension pour dissocier les précipitations.
3. Assemblage de la bande
REMARQUE: Pour les immunoessais à flux ultérieur, la sélection et le prétraitement du matériau membranaire affecteront directement le test, qui doit être étudié. La bande immunochromatographique se compose d’un tampon d’échantillon, d’un tampon conjugué, d’une membrane de nitrocellulose (NC), d’un tampon absorbant et d’un panneau de PVC(Figure 1). Le matériau de la membrane doit être vérifié et évalué par stéréomicroscopie pour éliminer l’inhomogénéité.
- Collez la membrane CN sur une planche de PVC à 2 cm du bord de l’extrémité d’aspiration de la carte.
- Ajouter SSD-BSA (2 mg/mL) goutte à goutte à la membrane NC (à 2 cm du bord supérieur) comme ligne d’essai (1 mm de large), et ajouter des IgG anti-souris chèvre (1,5 mg/mL) goutte à goutte sur la membrane NC (à 2 cm du bord inférieur) comme ligne de contrôle (1 mm de large). Contrôlez la quantité de protéines ajoutées.
- Fixez le tampon absorbant à la feuille de PVC au-dessus de la membrane CN et chevauchez-le avec la membrane CN de 2 mm.
- Immergez la membrane en fibre de verre dans la solution conjuguée AuNPs-mAb. Sécher la membrane humide dans un incubateur à 37 °C.
- Coupez la membrane en fibre de verre à 5 cm de long et 2 cm de large et utilisez-la comme tampon conjugué.
- Collez le tampon conjugué prétraité sous la membrane CN. La longueur de chevauchement avec la membrane CN doit être de 0,1 cm.
REMARQUE: La membrane en fibre de verre a une forte capacité à se lier et à libérer des protéines. - Coupez la membrane fusion 3 à 1,8 cm de long et 3,5 cm de large et utilisez-la comme tampon d’échantillonnage.
- Collez le tampon d’échantillon sur la planche de PVC et chevauchez-le avec le tampon conjugué de 2 mm.
- Découpez le carton assemblé en bandes de 3,5 mm de large à l’aide d’une machine de découpe et compactez-le à l’aide d’un système de laminage par lots.
- Enfin, placez les bandelettes de test dans la coque, scellez-les dans un sac en aluminium contenant du dessiccant et rangez-les à l’abri de la lumière. Les ICS sont maintenant assemblés.
REMARQUE: Ce qui précède est la procédure de laboratoire. Dans la production, des équipements de pulvérisation d’or et des instruments à membrane croisée sont utilisés pour pulvériser de l’or et fabriquer les lignes T et C.
4. Détection quantitative
- Déposer 50 μL de solution d’échantillon sur le trou d’échantillonnage pour observer le processus de chromatographie.
REMARQUE: En raison de l’action capillaire entraînée par le tampon absorbant, la solution d’échantillon migre vers l’autre extrémité de la bandelette. Lorsque la solution d’échantillon atteint le tampon conjugué, le SSD (antigène) de l’échantillon réagit avec les AuNPs-mAb préchargés sur le tampon. Lorsque la solution migre et atteint la ligne T, les AuNPs-mAb sans SSD peuvent être capturés sélectivement par SSD-BSA (conjugué protéine porteuse d’antigène), apparaissant sous forme de couleur rouge sur la ligne T. Ensuite, la solution migre vers la ligne C, où les AuNPs-mAb sont capturés par des IgG anti-souris de chèvre dans la région, s’affichant ainsi sous forme de couleur rouge sur la ligne C. - Analysez les bandes avec un lecteur de bandes portable. La machine peut fournir le rapport de la ligne de test à la ligne de commande (T / C).
- Évaluer la spécificité, la sensibilité, la répétabilité et la stabilité du test ICS.
REMARQUE: Sous détection qualitative, une ligne rouge indique un résultat positif (ligne de contrôle). Deux lignes rouges indiquent un résultat négatif (lignes de test et de contrôle). Si la ligne de contrôle n’est pas présente, le test est considéré comme non valide.
Résultats
Caractérisation de l’or colloïdal
Les solutions d’or colloïdal préparées étaient rouge clair. Des analyses TEM ont été utilisées pour déterminer la morphologie et la forme des AuNPs (Figure 2A-D). Les figures 2A et 2B révèlent que les particules sont de forme polyédrique et uniformément réparties. Le diamètre moyen des AuNPs s’est avéré être d’environ 14 nm
Discussion
Dans ce travail, nous présentons un protocole pour la préparation de mAbs contre de petites molécules dérivées de produits naturels. Les étapes essentielles et les questions nécessitant une attention particulière dans la procédure ont été décrites, et nous avons démontré l’utilité de ce protocole en utilisant le SSD à petite molécule comme exemple. Des exemples de spectres, d’images TEM, de résultats quantitatifs et d’investigations méthodologiques sont présentés dans des données représentati...
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ce travail a été soutenu par les Fonds spéciaux pour la recherche fondamentale des établissements d’enseignement supérieur affiliés aux départements centraux. Nous apprécions le soutien de l’équipe de recherche fondamentale sur la prescription classique de l’Université de médecine chinoise de Beijing.
matériels
| Name | Company | Catalog Number | Comments |
| Chloroauric acid solution (HAuCl4) | Tianjin Fu Chen Chemical Reagents Factory | JY-SJ102 | |
| bovine serum albumin | AMRESCO | 332 | |
| centrifuge tube 15 mL | Corning | 430645 | |
| centrifuge tube 50 mL | Corning | 430828 | |
| ELISA plates, 96 well | NUNC | 655101 | |
| Filter paper | Sinopharm | H5072 | |
| Glass fibre membranes | Jieyi | XQ-Y6 | |
| goat-anti-mouse IgG antibody | applygen | C1308 | |
| Nitrocellulose membranes | Millipore | millipore 180 | |
| ovalbumin | Beijing BIODEE | 5008-25g | |
| PEG20000 | Sigma Aldrich | RNBC6325 | |
| Pipette 10mL | COSTAR | 4488 | |
| Pipette 25mL | FALCON | 357525 | |
| semi-rigid PVC sheets | Jieyi | JY-C104 | |
| Sodium citrate | Beijing Chemical Works | C1034 | |
| sodium periodate | Sinopharm Chemical | BW-G0008 | |
| Sulfo-GMBS | Perbio Science Germany | 22324 | |
| TipOne Tips 1,000 µL | Starlab | S1111-2021 | |
| Tris-HCl | Solarbio | 77-86-1 | |
| TWEEN 20 | Solarbio | 9005-64-5 |
Références
- Huang, X., et al. Membrane-based lateral flow immunochromatographic strip with nanoparticles as reporters for detection: A review. Biosensors and Bioelectronics. 75, 166-180 (2016).
- Chang, H. -. F., Wang, J. -. Q., Wang, B., Deng, A. -. P. An immune chromatographic assay for rapid and simultaneous detection of levonorgestrel and methylprednisolone in water samples. Chinese Chemical Letters. 24 (10), 937-940 (2013).
- Lai, J. J., Stayton, P. S. Improving lateral-flow immunoassay (LFIA) diagnostics via biomarker enrichment for mHealth. Methods in Molecular Biology. 1256, 71-84 (2015).
- Zhang, M. Z., et al. Development of a colloidal gold-based lateral-flow immunoassay for the rapid simultaneous detection of clenbuterol and ractopamine in swine urine. Analytical & Bioanalytical Chemistry. 395 (8), 2591-2599 (2009).
- Kranthi, K. R., et al. Development of a colloidal-gold based lateral-flow immunoassay kit for 'quality-control' assessment of pyrethroid and endosulfan formulations in a novel single strip format. Crop Protection. 28 (5), 428-434 (2009).
- Qian, K., et al. Development and evaluation of an immunochromatographic strip for rapid detection of capsid protein antigen p27 of avian leukosis virus. Journal of Virological Methods. (221), 115-118 (2015).
- Guo, H., et al. Lateral flow immunoassay devices for testing saliva and other liquid samples and methods of use of same. US Patent. , (2003).
- Miočević, O., et al. Quantitative Lateral Flow Assays for Salivary Biomarker Assessment: A Review. Frontiers in Public Health. 5, 1-13 (2017).
- Lisa, M., et al. Gold nanoparticles based dipstick immunoassay for the rapid detection of dichlorodiphenyltrichloroethane: an organochlorine pesticide. Biosensors and Bioelectronics. 25 (1), 224-227 (2009).
- Zhang, Z., et al. Monoclonal Antibody-Europium Conjugate-Based Lateral Flow Time-Resolved Fluoroimmunoassay for Quantitative Determination of T-2 Toxin in Cereals and Feed. Analytical Methods. 7 (6), 2822-2829 (2015).
- Shen, H., et al. Facile synthesis of high-quality CuInZnxS2+x core/shell nanocrystals and their application for detection of C-reactive protein. Journal of Materials Chemistry. 22 (35), 18623-18630 (2012).
- Xiang, T., et al. A novel double antibody sandwich-lateral flow immunoassay for the rapid and simple detection of hepatitis C virus. International Journal of Molecular Medicine. 30 (5), 1041-1047 (2012).
- Yang, Q., et al. Quantum dot-based immunochromatography test strip for rapid, quantitative and sensitive detection of alpha fetoprotein. Biosensors & Bioelectronics. 30 (1), 145 (2011).
- Song, L. W., et al. Rapid fluorescent lateral-flow immunoassay for hepatitis B virus genotyping. Analytical Chemistry. 87, 5173-5180 (2015).
- Zhang, Y., et al. Quantum dot-based lateral-flow immunoassay for rapid detection of rhein using specific egg yolk antibodies. Artificial Cells, Nanomedicine, and Biotechnology. 1, (2017).
- Qu, H., et al. Rapid Lateral-Flow Immunoassay for the Quantum Dot-based Detection of GsRerarin. Biosensors and Bioelectronics. 81, 358-362 (2016).
- Li, Z., et al. Development and Clinical Application of a Rapid IgM-IgG Combined Antibody Test for SARS-CoV-2 Infection Diagnosis. Journal of Medical Virology. 92 (9), (2020).
- Xiaomei, L., Jing, W., Ya, Z. The clinical application value analysis of the 2019-coronary virus disease was analyzed by the whole blood Sars-COV 2 specific antibody detection. Natural Science Edition. 42, (2020).
- Zhang, Y., et al. Generation of Monoclonal Antibodies Against Natural Products. Journal of Visualized Experiments. , e57116 (2019).
- Sai, J., et al. Development of an Enzyme-Linked Immunosorbent Assay and Immunoaffinity Column Chromatography for Saikosaponin d Using an Anti-Saikosaponin d Monoclonal Antibody. Planta Medica. 82, 432-439 (2016).
- Yue, Z., et al. A Highly Sensitive Immunochromatographic Strip Test for Rapid and Quantitative Detection of Saikosaponin d. Molecules. 23 (2), 338 (2018).
- Qu, H., et al. Rapid Lateral-Flow Immunoassay for the Quantum Dot-based Detection of Puerarin. Biosensors and Bioelectronics. 81, 358-362 (2016).
- Zhang, Y., et al. Quantum dot-based lateral-flow immunoassay for rapid detection of rhein using specific egg yolk antibodies. Artificial Cells, Nanomedicine, and Biotechnology. 1, (2017).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon