A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
Assay תקשורת צומת-המערכת יודיד-צהוב הניאון חלבון-Gap
In This Article
Summary
כאן, אנו מציגים עבור הרומן הפער צומת תקשורת המערכת assay המיועד להקרנה תפוקה גבוהה של הפער להתכוונן צומת כימיקלים גילוי תרופות רעילות הערכת פרוטוקול.
Abstract
הפער צמתים (GJs) הם ערוצי קרום התא לאפשר דיפוזיה של מולקולות קטנות יותר מאשר 1 kDa בין תאים סמוכים. כפי שהם תפקידים פיזיולוגיים ופתולוגיים, יש צורך של תפוקה גבוהה ההקרנה (HTS) מבחני לזהות GJ מאפננים במבחני גילוי של הרעלים סמים. Assay המערכת-צומת תקשורת (I-YFP-GJIC) הרומן יודיד-צהוב הניאון חלבון-gap ממלא את הצורך הזה. זה וזמינותו מבוססת תא כולל תאים מקבל ושל התורמים מתוכננים לבטא stably משתנה צהוב חלבון פלואורסצנטי (YFP), זריחה של מי הוא ברגישות מתרצה יודיד, או SLC26A4, טרנספורטר יודיד, בהתאמה. כשנוספת יודיד לתרבות מעורב מסוגי תאים שני, הם להזין את תאי התורם באמצעות המשגר SLC26A4, טשטוש לתאים סמוכים מקבל דרך GJs איפה הם להרוות את פלורסצנטיות YFP. קרינה פלואורסצנטית YFP נמדד טוב מאת טוב במצב קינטי. הקצב quenching YFP משקף פעילות GJ. וזמינותו הוא אמין ומהיר מספיק כדי לשמש עבור HTS. הפרוטוקול עבור וזמינותו אני-YFP-GJIC באמצעות תאי LN215, תאים אנושיים glioma, מתואר.
Introduction
הפער צמתים (GJs) לשמש ערוצי המערכת לאפשר פעפוע של מולקולות קטנות של < kDa 1 כגון חומרים מזינים, מטבוליטים מולקולות איתות בין תאים סמוכים. האלמנטים מהחיבור כוללים hemichannel או connexon בכל תא, ומהווה כל connexon connexins (Cxs) 61. GJs ו Cxs שימשו מבחני הרעלים של חומרים מסרטנים כגון פחמימנים ארומטיים polycyclic (הפה), אשר GJ מעכבי2,3,4. GJIC שיבשו נמצא קשור nongenotoxic carcinogenesis5,6. טיפולית כמטרה פוטנציאליים, מעורבות GJ דווחה ב תתי סוגים מסוימים של7,התקפים8, הגנה מפני הלב והמוח איסכמיה/פגיעה reperfusion פציעה9, מיגרנה עם אאורה10, שיכרון פגיעה בכבד6,11,12ריפוי הפצע. תפוקה גבוהה ההקרנה (HTS) מבחני נדרשים כדי לזהות להתכוונן GJ כימיקלים או נוגדנים לגילוי סמים, עבור מבחני רעלים, וכדי לזהות הרגולטורים הסלולר הרומן של פעילות GJ. מבחני HTS יכול לשמש גם כדי לחקור מבנה-פעילות הגומלין של GJ מאפננים2,13,14,15.
כמה מבחני GJIC כוללים העברת צבע או טכניקות מלחציים תיקון כפול. לוציפר צהוב CH (LY) ו- calcein acetoxymethyl אסתר (calcein-AM) שימשו מבחני העברת צבע. התאים אינם חדיר כדי LY, אשר הציג microinjection, מגרדים טעינה או אלקטרופורציה. פעם אחת בתוך התא, LY מתפשט לתוך השכנה תאים באמצעות GJs, פעילות GJ הוא לבדיקה על פי מידת ה-הגירה LY16. מבחני Calcein-אם כרוכים בדרך כלל הפער-זריחה התאוששות לאחר17,photobleaching18. Calcein-אם הוא צבע התא-permeant זה מומר intracellularly calcein אטום על ידי esterase מהותי. וזמינותו מחייבת מיקרוסקופ קונפוקלי להתבונן בהעברת calcein-אם בתוך תא מן הסובבים אותו בעקבות לייזר photobleaching. אם GJs פונקציונלי קיימות, calcein-אם תאים סמוכים מזין את התאים photobleached, ידי קרינה פלואורסצנטית הוא התאושש. פעילות GJ הוא לבדיקה על פי מידת פלורסצנטיות שחזור של תאי photobleached. צבע-העברת מבחני מפרך וצורכת זמן או בעלי רגישויות נמוכה. תיקון כפול מחבר חובק למעקה היא שיטת אלקטרופיזיולוגיות המודד מוליכות מהחיבור. . זה רגיש יחסית, עם תלות ישירה של מוליכות על מספר GJs פתוח19; עם זאת, כל דבר טכנית אחר, זמן רב ויקר20 הבדיקה אני-YFP-GJIC פותחה לשימוש ב- HTS.
איור 1 מדגימה את הרכיבים ואת השלבים של GJIC-YFP וזמינותו, אשר מנצל תאים מקבל ביטוי variant YFP רגיש יודיד הנושאת H148Q ו- I152L (YFPקי) ותאים התורם לבטא של טרנספורטר יודיד (SLC26A4)21 . שתי מוטציות שישאו YFPקי לאפשר שכבתה של קרינה פלואורסצנטית מאת יודיד22. Iodides מתווספים מקבל תרבותי משותף ותאים התורם; הם לא תזין את התאים מקבל, אבל שנלקחה על ידי למעליות SLC26A4 נוכח בתאי התורם. Iodides בתאי התורם מפוזרת באמצעות GJs מתפקדת לתאים סמוכים מקבל שבו הם להרוות את פלורסצנטיות YFPקי . אם GJs סגורים או נחסם על-ידי מעכבי, יודיד אין באפשרותך להזין את התאים מקבל כדי להרוות את קרינה פלואורסצנטית. הקצב quenching YFPקי משקף פעילות GJ. הנוהל וזמינותו של GJIC-YFP הוא לא מסובך ולא זמן רב. זה תואם HTS והוא יכול לשמש כדי לבדוק את ההשפעות של מספר רב של תרכובות בפעילות GJ בתקופה קצרה יחסית. זה דורש רק מקבל תאי התורם ואת שני פתרונות מלח מאוזנת. הפרוטוקול המתואר להלן מבוססת על תאים LN215 Cx העיקרי שלו הוא Cx4321. הקולטן LN215-YFPקי ואת LN215-אני תאי התורם− היו שנוצר על ידי התמרה חושית עם lentiviruses לבטא YFPקי או SLC26A421,23.
Protocol
1. דור של lentiviruses לבטא YFPקי ו- SLC26A4
- לגדל תאי הכליה עובריים אנושיים HEK293T עד 80% confluency על צלחות תרבות 100 מ מ. של Dulbecco ששינה נשר בינוני (DMEM) בתוספת 10% סרום שור עוברית פניצילין U/mL 100, סטרפטומיצין µg/mL 100 הוא המדיום תרבות בשימוש בכל רחבי הפרוטוקול כדי לשמור על HEK293T ותאים אחרים המוזכרים להלן.
- המעיל לוחות 6-ובכן תרבות על-ידי הוספת 2 מ"ל של 0.005% פולי-L-ליזין (PLL) פתרון סטרילי מכל קידוח עבור 10 דקות וארוקן את הפתרון PLL ולשטוף השטח פעמיים עם 2 מיליליטר מים סטריליים.
- לשטוף HEK293T תאים עם 10 מ"ל של פוספט buffered תמיסת מלח (PBS) מתייחסים את monolayers תא בכל מנה 100 מ מ עם 2 מ של 0.25% טריפסין-EDTA פתרון ב 37 מעלות צלזיוס במשך 3 דקות להוסיף 5 מ של תרבות בינוני ו resuspend את התאים.
- לספור התאים hemocytometer להתאים את הצפיפות של התליה תא ל 250,000 תאים למ"ל במדיום תרבות ו להוסיף תאים 500,000 2 מ של תרבות בינוני לכל מצופים ליזין טוב של צלחות 6-. טוב. דגירה התאים humidified 5% /95% CO2האוויר והאווירה במקום 37 מעלות צלזיוס במשך 24 שעות ולאחר מכן להחליף המדיום תרבות DMEM ללא פניצילין או סטרפטומיצין.
- צינור 1.5 mL, למהול 20 µL של תרביות תאים מגיב עם 500 µL של DMEM ללא סרום או אנטיביוטיקה. לערבב בעדינות על ידי pipetting ומשהים בטמפרטורת החדר 5 דקות.
- בינתיים, פיפטה 250 µL של DMEM לתוך כל אחד שני צינורות 1.5 mL ולאחר מכן להוסיף 1500 ng של pLVX-EIP-YFPקי או pLenti6P-SLC26A4, 1225 ng של psPAX2, 375 ng של pMD2.G כל אחד. שני פלסמידים lentiviral כבר שתואר לעיל21. להוסיף 250 µL של תרביות תאים מדולל ריאגנט כל שפופרת פלסמיד, לערבב בעדינות, תקופת דגירה של 20 דקות בטמפרטורת החדר.
- לאחר 20 דקות, להוסיף 500 µL של מתחמי ריאגנט של פלסמיד תרביות תאים בתוך הצינורות 1.5 mL dropwise כל צלחת תרבות גם שלב 1.4 ושילוב במוזיקת את הצלחת הלוך. דגירה תאים ב- 37 מעלות צלזיוס חממה2 CO במשך 12 שעות.
- החלף את המדיום 2.5 מ ל בינוני טריים, תקופת דגירה של h 48 נוספים. ואז מניחים את הצלחת תרבות על קרח במשך כשלוש דקות הפרסום הממוזגים המכיל lentivirus מקורר כדי לשמור על infectivity.
- הקציר שהמדיה המכילה lentiviruses, להעביר צינורות חרוט 15 מ"ל. צנטריפוגה ב x 3000 g ב 4 מעלות צלזיוס למשך 3 דקות, ואז להסיר תאים HEK293T צפה תגובת שיקוע על-ידי סינון ב- 0.4 מיקרומטר.
- חנות שהמדיה המכילה lentiviruses ב 4 ° C לשימוש תוך יומיים. לשימוש מאוחר יותר, חנות aliquots µL 200-−80 מעלות צלזיוס.
2. דור של LN215-YFPקי ו LN215-אני− תאים על-ידי התמרה חושית lentiviral
- לגדול LN215 בתאי לוחיות תרבות 100 מ מ עד 80% confluency ב DMEM בתוספת 10% סרום שור עוברית (FBS) 100 U/mL פניצילין, סטרפטומיצין µg/mL 100 כמתואר לעיל.
הערה: אם וזמינותו אני-YFP-GJIC התנהלה באמצעות שורת תאים שונים, להשתמש המדיום המתאים תרבות. LN215-YFPקי, ו LN215-אני– תאים יכולה להינתן על-ידי קרן אוניברסיטת-תעשיה, אוניברסיטת Yonsei. אנא צרו קשר עם המחבר המקביל. - יום אחד לפני התמרה חושית, תשטוף התאים פעמיים עם 10 מ"ל ל- PBS, לטפל עם 2 מ של 0.25% טריפסין-EDTA ב 37 מעלות צלזיוס במשך 3 דקות Resuspend התאים 5 מ של תרבות בינוני עם פיפטה serologic 10 מ"ל ולהתאים את צפיפות 50,000 תאים/מ. הוספת תאים 20,000 µL 400 של מדיה אל כל טוב של צלחת 24-ובכן תרבות לטיפול כמו אין שליטה וירוס, YFPקיותאים SLC26A4.
- לאחר 24 שעות של דגירה ב 37 מעלות צלזיוס, מגלי שתי בארות על-ידי החלפת המדיום תרבות µL 400 של תערובת 1:1 של pLVX-EIP-YFPקי או pLenti6P-SLC26A4 lentivirus בינוני תרבות טרי בתוספת polybrene-ריכוז סופי של 4 µg/mL. עבור פקדים לא וירוס, החלף תרבות בינוני.
- דגירה התאים ב 37 ° C עבור 15 h, תשאף המדיום המכיל lentiviruses, להוסיף בינוני תרבות טריים, דגירה את התאים עבור h 72 נוספים.
התראה: כדי למנוע זיהום של lentivirus בין בארות, השתמש עצות חדשות או pipets במשך כל כאשר אתה תשאף תרבות בינוני המכיל lentivirus או לוותר על מדיום הגידול טריים. - שטיפת שהתאים בכל טוב פעמיים 0.5 מ ל- PBS, לטפל עם 300 µL של טריפסין-EDTA עבור 3 מינימלית Resuspend התאים 2 מ של תרבות בינוני וצלחת ב 6-ובכן תרבות צלחות עם 2 puromycin µg/mL.
- התרבות התאים המדיה המכילה 2 µg/mL puromycin עד כל התאים בפקד ובכן מתים (בצורת עגול או צף כאשר שנצפתה מיקרוסקופ), אשר בדרך כלל לוקח שבוע. רענן על המדיה תרבות המכילה puromycin בכל יום במהלך תקופת הבחירה. אם LN215-YFPקי או LN215-אני– confluent תרבויות להפוך לפני הבחירה השלימה, העברת לתאים 100 מ מ צלחת ולהמשיך בחירה כמו שלב 2.5.
3. הכנת הפתרונות הנדרשים עבור וזמינותו
- הכנת 500 מ"ל של C-פתרון (10 מ מ HEPES 140 מ"מ NaCl, גלוקוז 10 מ"מ, 5 מ"מ אשלגן כלורי, 1 מ MgCl2, 1 מ"מ CaCl2) ו- 500 מ"ל של אני-פתרון (10 מ"מ HEPES, 140 מ"מ נאי, גלוקוז 10 מ"מ, 5 מ"מ אשלגן כלורי, ו 1 מ"מ CaCl2).
- להתאים את רמת החומציות של שני פתרונות 7.4 עם 1 N NaOH, לעקר את הפתרונות על ידי סינון ב- 0.4 מיקרומטר לאחסון. לאחסן ב 4 ° C עד כחודש. בדוק את ה-pH לפני השימוש.
4. ציפוי LN215-YFPקי של LN215-אני− תאים
- תרבות LN215-YFPקי ו- LN215-אני− התאים ב- 100 מ מ צלחות בנפרד במדיום תרבות להגיע האוכלוסיות הדרושות וזמינותו. LN215-YFPקי ו- LN215-אני− תאים ב-40% ו- 80% confluency ב 100 מ מ צלחות, בהתאמה, מספיקים וזמינותו 96-ובכן צלחת.
- יום אחד לפני ביצוע וזמינותו GJIC-YFP, לשטוף כל צלחת תרבות 100 מ מ עם 10 מ"ל ל- PBS. להתייחס לכל צלחת עם 2 מ של 0.25% טריפסין-EDTA פתרון, דגירה ב 37 מעלות צלזיוס במשך 5 דק Resuspend התאים בצלחת לכל ב מ 4 ל תרבות בינונית, העברת צינורות חרוט 15 מ"ל.
- גלולה התאים על ידי צנטריפוגה-1,000 x g עבור 3 מינימלית להשליך את תגובת שיקוע, resuspend כל גלולה תא עם 5 מ של תרבות בינוני. לשבור את כל הגושים תא לתוך תאים בודדים על-ידי pipetting למעלה ולמטה בערך 20 פעמים עם פיפטה סרולוגית 10 מ.
- התאים hemocytometer, ותמיד לדלל את התאים בטווח הבינוני תרבות כדי להפוך תא המתלים של LN215-YFPקי ב תאים למ"ל 80,000 ו LN215-אני− ב תאים למ"ל 160,000.
- לערבב 7 מ של LN215-YFPקי ו- 7 מ של LN215-אני− המתלים תא מאגר. להוסיף 100 µL של התערובת כל טוב של צלחת תרבות 96-ובכן התא באמצעות פיפטה רב-ערוצי.
הערה: כדי להוסיף 100 µL של התערובת היטב כל צלחת תא 96-ובכן, כ- 10 מ"ל של השעיה לתא מעורב נדרשת. מומלץ לעשות ההשעיה תא יותר מכפי הצורך. - דגירה התאים ב humidified 5% CO2/95% אוויר ב- 37 מעלות צלזיוס במשך 24 שעות ביממה. LN215-YFPקי של LN215-אני תרבית תאים−צריכה להיות 100% confluent כאשר מתנהל וזמינותו.
5. ביצוע וזמינותו GJIC -YFP
הערה: שימוש במיקרוסקופ זריחה עם 20 x הגדלה ומסנן GFP כדי לבדוק את הצלחות 96-ובכן להיות בטוח שם אין גושים של LN215-YFPקי או תאים LN215-SLC26A4 וכי התרבויות תא הם confluent באופן מלא והופץ טוב לפני ביצוע וזמינותו.
- לפחות 30 דקות לפני ביצוע וזמינותו, להפעיל את microplate והוא מוגדר כ- 37 מעלות צלזיוס.
- לשטוף את הצנרת של מזרק אוטומטי עם 3 מ"ל של 70% אתנול, 3 מ ל מים מזוקקים, ולאחר מכן מ 3 לפתרון בספיקה של 300 µL/s.
- את C-אני-פתרונות ל- C ° 37 באמבט מים חמים.
הערה: כפי µL 100 לכל פתרון יש צורך במשך כל צלחת 96-ובכן, כ- 10 מ"ל של כל פתרון נדרש עבור כל וזמינותו. נוספים 10 מ"ל של אני-הפתרון הוא נדרש עבור הטרמה כל צלחת (סה כ 20 מ ל), אוטם 25 נוספים של הפתרון C יש צורך לשטוף כל צלחת (סך של 35 מ ל). - האחות מדיום הגידול או היפוך את הצלחת לרוקן אותה; הכנע בינוני שיורית.
הערה: שיורית סרום שור העובר בתקשורת צמיחה גורם רקע זריחה ו ירידה באיכות וזמינותו. - להוסיף 200 µL של C-פתרון טוב לכל מתוך מאגר באמצעות פיפטה רב-ערוצי. האחות של C-הפתרון או היפוך לוח ריק, הכנע פתרון שיורית.
- להוסיף 50 µL µL C-פתרון, µL 1 של מניות כימי 2.5 מ מ (ראה טבלה 1) או dimethylsulfoxide (דימתיל סולפוקסיד) כרכב ולאחר מכן 50 µL µL C-פתרון כל טוב עם פיפטה רב-ערוצי.
הערה: רוב ריאגנטים בספריה כימיים הם מומס דימתיל סולפוקסיד ומותר עד 1% (v/v) מבחני מבוססת תא רוב24. דימתיל סולפוקסיד יש צפיפות גבוהה יותר מאשר מים, ריאגנטים מומס דימתיל סולפוקסיד נוטים לרדת לתחתית כאשר נוספו הבארות צלחת תרבות, שמטרידה את ריכוזי הפתרונות וזמינותו. זה יכול מצויין על-ידי הוספת µL 50 של C-פתרונות, ריאגנטים, דימתיל סולפוקסיד 50 µL C - בפתרון לפי סדר. µL 50 אחרונה של C-הפתרון הוא לערבוב. - דגירה התאים ב 37 מעלות צלזיוס באוויר, לא ב- CO 5%2. זמן הדגירה יכולה להיות שונה, אבל 10 דקות מספיקה בדרך כלל עבור תעלת יונים מאפננים לפעול.
- במהלך הדגירה, להגדיר את התוכנית קורא microplate להזריק 100 µL פתרון כדי מכל קידוח-1 s וכדי למדוד את פלורסצנטיות 10 s במרווחים s 0.4. הגדר את הקורא לקרוא פלורסצנטיות מלמטה. מהירות הזרקת המומלצת היא µL 135/סט הגל עירור 485 ננומטר, קריאה הפליטה-520 ס ננומטר.
הערה: הגדרות מפורטות עבור תוכניות קורא microplate הם כדלקמן.- לחץ על לחצן ניהול פרוטוקולים .
- לחץ על הלחצן ' חדש '. בחר את עוצמת קרינה פלואורסצנטית סעיף שיטת מדידה, ובכן מצב קריאה במצב סעיף. לאחר מכן, לחץ על הלחצן אישור . בכרטיסיה חדשה מופיע.
- בתפריט הפרמטרים הבסיסיים , להגדיר את אורך הגל של עירור 485 nm וה -520 ננומטר. בחר את התחתון אופטיים לקריאה פלורסצנטיות מלמטה. מדידה קבע זמן להיות התחלה "0 s", מספר במרווחי זמן כדי להיות "25", מספר הבזקים לכל טוב, מרווח זמן להיות "20", ואת מרווח זמן להיות "0.4 s".
- בתפריט ' פריסה ', צייר אזור של הצלחת לקריאה.
- בתפריט ' ריכוזים/אחסון/Shacking ', הגדר את הקורא microplate להחדיר µL 100-פתרון כדי מכל קידוח 135 מהירות הזרקת µL/s.
הערה: להימנע מהירויות הזרקה כי הם עלולים לגרום לניתוק של תאים. - בתפריט זמן ההזרקה , לקבוע את שעת ההתחלה הזרקת להיות 1 s. לאחר מכן, לחץ על לחצן התחל מדידה .
- לאחר דגירה, למקם את הצלחות 96-ובכן בקורא ה-microplate, להתחיל את המדידה על-ידי לחיצה על לחצן התחל מדידה שוב.
6. חישוב של פעילות GJIC
- לחשב את האחוזים YFPקי שכבתה ופעילות GJIC כמו23
YFPקי שכבתה (%) =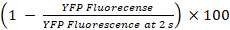
פעילות GJIC (%) =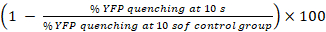
הערה: באופן עקרוני, פעילות GJIC יש לחשב נובע האחוזים של זריחה YFP בבארות עם מקבל תאים ותאים התורם, מקבל-התא המתאים רק בארות. עם זאת, כמו LN215-YFPקי תאים מראים זניח YFP שכבתה מאת יודיד אחרי 10 s, אנחנו לא מקבלים את הרקע YFP שכבתה בחשבון בעת עריכת HTS באמצעות LN215-YFPקי ו- LN215-אני– תאים.
תוצאות
עשרים ותשע 96-ובכן תרבות צלחות שימשו למסך כימיקלים, 2320 לזהות את הרומן מאפננים GJIC-YFP GJIC assay באמצעות LN215-YFPקי LN215-אני− תאים. התוצאות המתקבלות עם צלחת נציג מוצגים באיור2. האחוז של קרינה פלואורסצנטית YFP היטב כל מוצג כתרשים קווי איור 2
Discussion
הבדיקה אני-YFP-GJIC יכול לשמש עבור HTS כי זה חזקה, מהירה וזולה. Assay HTS נחשבת חזקה אם ז '-פקטור הוא מעל 0.525. מבחני לראות ג'אנג et al. לתיאור של ניתוח סטטיסטי המשמש כדי לבדוק את התאמת HTS25. כאשר תאים LN215 שימשו, ז '-גורם היה > 0.5 ללא כל אופטימיזציה וזמינותו. אם סוגי תאים אחרים משמשים וז?...
Disclosures
המחברים יש שאין ניגודי אינטרסים לחשוף.
Acknowledgements
מחקר זה נתמך על-ידי התוכנית מחקר מדעי בסיסי דרך לאומי מחקר קרן של קוריאה (ב- NRF) ממומן על ידי משרד החינוך (2011-0023701, 2016R1D1A1A02937397, ו 2018R1A6A1A03023718).
Materials
| Name | Company | Catalog Number | Comments |
| 96-well plate | SPL | 30096 | |
| Calcium chloride (CaCl2) | Sigma | C5670 | I-solution |
| D-(+)-Glucose | Sigma | G7021 | C-solution, I-solution |
| Dimethyl sulfoxide (DMSO) | sigma | 276855 | |
| HEPES | Sigma | RES6003H-B7 | C-solution, I-solution |
| Lipofectamine 2000 | Invitrogen | 11668-027 | transfection reagent |
| Magnesium chloride hexahydrate (MgCl2 6H2O) | Sigma | M2393 | C-solution |
| Microplate reader | BMG LabTech | POLARstar Omega 415-1618 | |
| pMD2.G | Addgene | #12259 | |
| Polybrene | sigma | H9268 | |
| Poly-L-lysine solution | sigma | P4707 | |
| Potassium chloride (KCl) | Sigma | P5405 | C-solution, I-solution |
| psPAX2 | Addgene | #12260 | |
| Puromycin Dihydrochloride | sigma | P8833 | |
| Sodium chloride (NaCl) | Sigma | S5886 | C-solution, I-solution |
| Sodium hyroxide (NaOH) | Sigma | S2770 | |
| Sodium Iodide (NaI) | Sigma | 383112 | I-solution |
References
- Goodenough, D. a., Goliger, J. a., Paul, D. L. Connexins, connexons, and Intercellular Communication. Annual Review of Biochemistry. 65, 475-502 (1996).
- Upham, B. L., Weis, L. M., Trosko, J. E. Modulated Gap Junctional Intercellular Communication as a Biomarker of PAH Epigenetic Toxicity: Structure-Function Relationship. Environmental Health Perspectives. 106, 975 (1998).
- U, J. E. T., Chang, C., Upham, B., Wilson, M. Epigenetic toxicology as toxicant-induced changes in intracellular signalling leading to altered gap junctional intercellular communication. Toxicology Letters. , 71-78 (1998).
- Yamasaki, H. Role of disrupted gap junctional intercellular communications in detection and characterization of carcinogens. Mutation Research - Reviews in Genetic Toxicology. , (1996).
- Yamasaki, H., et al. Gap junctional intercellular communication and cell proliferation during rat liver carcinogenesis. Environmental Health Perspectives. 101, 191-197 (1993).
- Vinken, M., et al. Gap junctional intercellular communication as a target for liver toxicity and carcinogenicity. Critical Reviews in Biochemistry and Molecular Biology. 44, 201-222 (2009).
- Fonseca, C. G., Green, C. R., Nicholson, L. F. B. Upregulation in astrocytic connexin 43 gap junction levels may exacerbate generalized seizures in mesial temporal lobe epilepsy. Brain Research. 929 (1), 105-116 (2002).
- Garbelli, R., et al. Expression of connexin 43 in the human epileptic and drug-resistant cerebral cortex. Neurology. 76 (10), 895-902 (2011).
- Schulz, R., et al. Connexin 43 is an emerging therapeutic target in ischemia/reperfusion injury, cardioprotection and neuroprotection. Pharmacology and Therapeutics. 153, 90-106 (2015).
- Sarrouilhe, D., Dejean, C., Mesnil, M. Involvement of gap junction channels in the pathophysiology of migraine with aura. Frontiers in Physiology. , (2014).
- Patel, S. J., et al. Gap junction inhibition prevents drug-induced liver toxicity and fulminant hepatic failure. Nature Biotechnology. 30 (2), 179-183 (2012).
- Kandyba, E. E., Hodgins, M. B., Martin, P. E. A murine living skin equivalent amenable to live-cell imaging: analysis of the roles of connexins in the epidermis. Journal of Investigative Dermatology. 128 (4), 1039-1049 (2008).
- Upham, B. L., et al. Differential roles of 2 , 6 , and 8 carbon ceramides on the modulation of gap junctional communication and apoptosis during carcinogenesis. Cancer Letters. 191, 27-34 (2003).
- Upham, B. L., et al. Structure-activity-dependent regulation of cell communication by perfluorinated fatty acids using in vivo and in vitro model systems. Environmental Health Perspectives. 117 (4), 545-551 (2009).
- Weis, L. M., et al. Bay or Baylike Regions of Polycyclic Aromatic Hydrocarbons Were Potent Inhibitors of Gap Intercellular Communication. Environmental Health Perspectives. 106 (1), 17-22 (1998).
- el-Fouly, M. H., Trosko, J. E., Chang, C. C. Scrape-Loading and Dye Transfer: A Rapid and Simple Technique to Study Gap Junctional Intercellular Communication. Experimental Cell Research. 168 (2), 422-430 (1987).
- Wade, M. H., Trosko, J. E., Schindler, M. Photobleaching Assay of Gap Junction- Mediated Communication Between Human Cells. Advancement of Science. 232 (4749), 525-528 (2010).
- Abbaci, M., et al. In vitro characterization of gap junctional intercellular communication by gap-FRAP technique. Proceedings of SPIE. , 585909 (2005).
- Neyton, J., Trautmann, A. Single-channel currents of an intercellular junction. Nature. 317 (6035), 331-335 (1985).
- Wilders, R., Jongsma, H. J. Limitations of the dual voltage clamp method in assaying conductance and kinetics of gap junction channels. Biophysical Journal. 63 (4), 942-953 (1992).
- Lee, J. Y., Choi, E. J., Lee, J. A new high-throughput screening-compatible gap junctional intercellular communication assay. BMC Biotechnology. 15 (1), 1-9 (2015).
- Galietta, L. J. V., Haggie, P. M., Verkman, A. S. Green fluorescent protein-based halide indicators with improved chloride and iodide affinities. FEBS Letters. 499 (3), 220-224 (2001).
- Lee, J. Y., Yoon, S. M., Choi, E. J., Lee, J. Terbinafine inhibits gap junctional intercellular communication. Toxicology and Applied Pharmacology. 307, 102-107 (2016).
- Hughes, J., Rees, S., Kalindjian, S., Philpott, K. Principles of early drug discovery. British Journal of Pharmacology. 162 (6), 1239-1249 (2011).
- Zhang, J. H., Chung, T. D. Y., Oldenburg, K. R. A simple statistical parameter for use in evaluation and validation of high throughput screening assays. Journal of Biomolecular Screening. 4 (2), 67-73 (1999).
- Upham, B. L. Role of Integrative Signaling Through Gap Junctions in Toxicology. Current Protocols in Toxicology. , (2011).
- Schalper, K. A., et al. Modulation of gap junction channels and hemichannels by growth factors. Molecular BioSystems. 8 (3), 685-698 (2012).
- Kulkarni, G. V., Mcculloch, C. A. G. Serum deprivation induces apoptotic cell death in a subset of Balb / c 3T3 fibroblasts. Journal of Cell Science. 1179, 1169-1179 (1994).
- Harris, A. L., Locke, D. Permeability of Connexin Channels. Connexins. , 165-206 (2009).
- Choi, E. J., Yeo, J. H., Yoon, S. M., Lee, J. Gambogic Acid and Its Analogs Inhibit Gap. Junctional Intercellular Communication. 9, 1-10 (2018).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved