Method Article
אבלציה לייזר מוקדי של סרטן הערמונית: הליך משרדי
In This Article
Summary
מאמר זה מציג ומתאר טיפול באשפוז לסרטן הערמונית באמצעות אבלציה לייזר מוקדי. מיקום קטטר לייזר מונחה על ידי הדמיית היתוך MRI-אולטרסאונד באופן דומה ביופסיה מחט הערמונית. הטיפול מנוטר בזמן אמת באמצעות בדיקה תרמית, הממוקמת בסמוך לסיבי הלייזר.
Abstract
במאמר זה, אנו מתארים וממחישים הליך אשפוז עבור אבלציה לייזר מוקדי (FLA) של סרטן הערמונית (PCa). ההליך דומה מבחינה רעיונית לביופסיה של היתוך ומבוצע בהרדמה מקומית במסגרת מרפאה; זמן הטיפול הוא בדרך כלל פחות משעה. החדרת לייזר מונחה על ידי אולטרסאונד; מיקוד הנגע הוא באמצעות דימות תהודה מגנטית אולטרסאונד (MRI / ארה"ב) היתוך, כמו ביופסיה הערמונית ממוקדת. ניטור אבלציה בזמן אמת מושגת ניצול בדיקה תרמית הסמוכה סיבי לייזר. הסרטון מדגים תכנון נהלים, הכנת מטופלים, שלבים שונים במהלך ההליך ומעקב אחר הטיפול. בטיחות, היתכנות ויעילות של גישה זו נקבעו במהלך ניסוי קודם. FLA אשפוז תחת הרדמה מקומית היא אופציה לניהול של סרטן הערמונית בסיכון בינוני.
Introduction
סרטן הערמונית (PCa) הוא הממאירות הפנימית הנפוצה ביותר אצל גברים בארה"ב1. כ 190,000 מקרים חדשים ו 33,000 מקרי מוות צפויים במהלך 2020, מה שהופך אותו הגורם השני בשכיחותו למוות מסרטן אצלגברים 2. רוב המקרים של PCa ניתנים לריפוי אם מטופלים בזמן מקומי הערמונית. עם זאת, זיהוי סרטן בתוך הערמונית הוא לעתים קרובות לא אפשרי עם אולטרסאונד קונבנציונלי (ארה"ב) הדמיה; לכן, הטיפול מעורב באופן מסורתי ניתוח או קרינה של הבלוטה כולה. הפרדיגמה 'בלוטה שלמה' שונתה עם כניסתה של הדמיית תהודה מגנטית (MRI), אשר, בניגוד לארה"ב, מאפשר לוקליזציה של PCa וביופסיה ממוקדת3,4,5,6. בעוד MRI סביר לזלזל multifocality של PCa7, ועלול להחמיץ נגעים קטנים8, זה יכול לזהות באופן אמין את הנגע מדד, שהוא כמעט תמיד הנהג של מחלה גרורתית9,10.
זיהוי MRI אמין של נגעים אינדקס סיפק נתיב לטיפול מוקדי של PCa (כלומר, אבלציה בלוטה חלקית (PGA)). המטרה של PGA היא להרוס את הנגע אינדקס תוך שמירה על האיבר ובכך למזער את תופעות הלוואי. אבלציה לייזר מוקד (FLA), אשר משתמשת אנרגיית אור להרוס רקמה באמצעות נמק קרישה11,12, היא צורה אחת של PGA. האפקטיביות של אנרגיית לייזר כדי ablate רקמת הערמונית הוקמה בשנת 199313, מציע את המיקום של סיבי לייזר לתוך סרטן הערמונית למטרה זו. באמצעות MRI להנחיית מיקום סיבים ותרמוגרפיה MRI לניטור טיפול (כלומר, בטיפול נשא), שיעורי הצלחה לטווח הקרוב של FLA נראים להתקרב לאלה של ניתוח אוקרינה 5,6,12,14,15,16,17,18,19. עם זאת, הליכי לייזר המבוצעים in-bore, או בתוך צינור MRI, הם לעתים קרובות מסורבלים, יקרים, זמן רב, ומשאבים אינטנסיביים. והליכים נשא מבוצעים רק על ידי רדיולוגים מאומנים תת-מומחיות.
כחלופה ל- IN-bore FLA, ההיתכנות של ביצוע FLA במסגרת מרפאה---על שימוש בהיתוך MRI / ארה"ב להדרכה ובדיקת טמפרטורה ביניים לניטור טיפול--- נמצאת תחת מחקר באוניברסיטת קליפורניה בלוס אנג'לס מאז 201419,20. הליך FLA במסגרת מרפאה הוכיח להיות דומה לזה של ביופסיה ממוקדת, החלפת סיב לייזר עבור מחט ביופסיה. בהשוואה ל- HIFU והקפאה, שהן השיטות האחרות הזמינות כיום של PGA, שיטת הלייזר המתוארת כאן היא מהירה וזולה, ללא צורך בחדר ניתוח או בהרדמה כללית.
מאמר זה נועד לתאר ולהדגים FLA אשפוז תחת הרדמה מקומית במרפאה אורולוגית. אורולוגים שמכירים את היתוך MRI/ארה"ב לביופסיה ממוקדת יעריכו את הדמיון בין FLA להליך הביופסיה. מטרות משניות כוללות תיאור אלמנטים טכניים המאפשרים קלות שימוש ותיאור היתרונות של טיפול מוקדי.
Protocol
הערה: השיטות המתוארות כאן הן אלה המשמשות ב UCLA לביצוע FLA של הערמונית. פרויקט המחקר, כולל הפרוטוקול, אושר על ידי ועדת הביקורת המוסדית של UCLA (IRB). כל החולים היו ביופסיה ממוקדת של הערמונית, שבו MRI פורש על ידי אורו רדיולוג מנוסה. נגעים הנראים ב- MRI עברו ביופסיה בתוך אזור העניין (ROI) ומחוץ להון ההשקעה באמצעות תבנית שיטתית. הביופסיות החיוביות ואזור ה-MRI של העניין משמשים לתכנון הטיפול עם אבלציה בלייזר על מנת לטפל בנגע המדד וליצור מרווח של רקמה מטופלת סביב הגידול, בהתחשב בכך ש- MRI ממעיט בגודל הגידול. 21 רק חולים עם סרטן הערמונית בסיכון בינוני (GG2-3 PSA < 20, שלב < T2), החזר על ההשקעה מדד יחיד ולא סרטן הערמונית משמעותי קלינית קונטרה נחשבים זכאים לטיפול. חולים עם דיאתזה דימום או חוסר יכולת לסבול טיפול ללא הרדמה נחשבים זכאים.
1. תכנון טיפול
- לפני הטיפול, תכננו יעדי אבלציות באמצעות קלט מקואורדינטות ה-MRI והביופסיה.
- בצע תכנון טיפול עם התוכנה המסופקת.
2. הכנת חדר פרוצדורלי
- הצג תמרור אזהרה בלייזר מחוץ לחדר הניתוח.
- מקם את תחנת העבודה לגישה נוחה.
- כוח על תחנת העבודה, מכשיר היתוך אולטרסאונד transrectal.
- הזן אישור כניסה ובחר את המטופל הרצוי מרשימת העבודה המהווה ברירת מחדל המכילה תוכניות שלא טופלו.
הערה: ניתן להוסיף תוכניות טיפול חדשות באמצעות חיבור USB או חיבור לאינטרנט כמפורט במדריך למשתמש. - לתלות שקית של מלוחים מן הוו המיועד על תחנת העבודה; שקית החזרה מלוחה פסולת מחוברת גם.
- ראש צינורות מלוחים על ידי מתן זרימת הכבידה של נוזל לפני נעילת הצינור. לאחר מכן מלוחים מחוברים למשאבה peristaltic ותלוי לשימוש מאוחר יותר במהלך ההליך.
3. הכנת בדיקה TRUS
- החל ג'לי אולטרסאונד ישירות על בדיקה TRUS נקי.
הערה: ב- UCLA, כל בדיקות TRUS מחוטאות באמצעות מערכת אוטומטית עם תמיסת מי חמצן מתאדה. - להתאים קונדום מעל ג'לי אולטרסאונד על החללית TRUS ולאבטח אותו בבסיס באמצעות גומייה.
הערה: לפי ניסיון רגיל להסיר בועות אוויר לכודים מתחת לקונדום. - מניחים מדריך רב ערוצי מעל הקונדום ולנעול אותו במקום באמצעות מהדק מתכת. קונדום שני עם ג'לי אולטרסאונד פנימי יכול להיות ממוקם מעל המדריך הרב ערוצי כדי להגדיל את נוחות המטופל.
4. הכנת המטופל
- כוון את המטופל לנקות את הכספת רקטלית שלהם עם חוקן בבוקר הביופסיה.
- ודא כי החולה השיג אנטיביוטיקה מניעתית 60 דקות לפני ההליך22.
הערה: ב UCLA, 1 גרם של Ertapenem מנוהל תוך שרירית 60 דקות לפני ההליך. החלטה זו התקבלה בהתבסס על אנטיביוגרמה UCLA ומנע פרקים ספיגה שלאחר ביופסיה על 1500 ביופסיות transrectal האחרונות. 23 בהתחשב בהצלחה זו, בחרנו גם להשתמש בו עבור אבלציה לייזר transrectal. - לספק לחולים עם Acetaminophen 1000 מ"ג PO, Ketorolac 30 IM מ ג, ובמידת האופן אך מומלץ Diazepam 10 מ"ג PO, 60 דקות לפני ההליך.
הערה: חולים עלולים לחוות רצון מתון לבטל או לחץ בפין במהלך ההליך. מניסיוננו, אין סמים מועילים. - חולים עשויים למצוא את זה שימושי להביא מוסיקה אישית ואוזניות כמו נוגדי צירים נוספים.
- מניחים את המטופל בתנוחת דקוביטוס לרוחב שמאל כמו ביופסיה transrectal.
- רשום סימנים חיוניים למטופל לפני תחילת ההליך ובמרווחים של 30 דקות.
5. ניהול של חסימת עצב הערמונית
- הכנס את הבדיקה TRUS משומנת עד מרכז הערמונית גלוי בבירור.
- לייעל את הרווח אולטרסאונד, זמן להרוויח פיצוי (מחווני TGC בצד ימין של רוב אולטרסאונד), עומק ומיקוד, כך הערמונית מרוכז בתוך צג הצפייה אולטרסאונד.
הערה: הרווח האופטימלי גורם לתמונה בצבע אפור בינוני בתוך האזור ההיקפי. המחוונים TGC מוגדרים בצורה הטובה ביותר בזווית משופעת בהדרגה כדי לפצות על הנחתת גל של רקמות רחוקות. עומק אולטרסאונד ומיקוד יהיה תלוי בגודל הערמונית. יש להגדיר את המוקד לאזור ההיקפי כדי למטב את ההדמיה של סמנים אקוסטיים על צנתר הלייזר. - הפעל את מדריך הביופסיה על המסך והנח מחט עמוד שדרה 22 מד דרך מרכז המדריך הרב ערוצי כדי לחטא את הערמונית.
הערה: ב UCLA אנו מרדים את הערמונית במישור קשת על ידי הצבת 10-20 מ"ל של לידוקאין / Marcaine בצומת של הערמונית ושלפועי הזרע. חדירה נכונה תגרום להפרדה של הווורידים הזרע והערמונית מהקיר רקטלי.
6. היתוך MRI-ארה"ב
- מקם את מערכת היתוך ההדמיה ותחנת העבודה קרוב מספיק למטופל על מנת לדמיין את מסכי תחנת העבודה תוך התבוננות במטופל.
- אם אתה משתמש בארטמיס, השתמש בטכניקה לעגינה ורישום תמונה שתוארה קודם לכן. 24 (24)
7. רכישת יעד
- לנווט את האולטרסאונד למרכז אתר אבלציה הראשון באמצעות מטרות דיגיטליות המסופקות על ידי מכשיר ההיתוך. תהליך זה דומה להנחיית אולטרסאונד לאזור MRI של עניין במהלך ביופסיה היתוך.
הערה: כל אתר אבלציה נקבע מאזור ה-MRI של עניין וליבות ביופסיה חיוביות (איור 1). יש להעביר את תוכנית הטיפול של המטופל לתחנת העבודה ומכשיר ההיתוך במהלך הכנת חדר הניתוח המתואר לעיל. - בחר את אזור אבלציה הנוכחי.
8. מיקום קטטר לייזר ובדיקת טמפרטורה
- הנח את קטטר הלייזר בעל 14 המדים בתא המרכזי של המדריך הרב-ערוצי.
הערה: המדריך הרב-ערוצי מעוקל כדי לספק חיכוך קל ובכך מונע מרכיבי הטיפול להחליק לאחור במהלך אבלציה. להתגבר על חיכוך זה על ידי סיבוב קדימה ואחורה תוך קידום קטטר לייזר לתוך הערמונית. - קדם את קטטר הלייזר עד שארבע רצועות אקוגניות יחוו וייישרו עם סמן העומק שעל המסך. עבור אבלציה של אזור היקפי, הסמנים יהיו כמה מ"מ מחוץ לכמוסת הערמונית (איור 2).
הערה: במקרה של קפסולה אחורית סיבית, קטטר הלייזר עלול להסיט במקום לחצות את כמוסת הערמונית. כל הסטה תהיה גלויה באולטרסאונד במהלך הכניסה. אם מתרחשת הסטה, הסר את קטטר הלייזר והכנס מנהיג, כגון הגשושית התרמית האיתנה, כדי ליצור פתח פיילוט בכמוסה. לאחר מכן ניתן לקדם את קטטר הלייזר כמתוכנן. - הכנס את החללית התרמית שמאלה או ימינה של קטטר הלייזר בהתאם לתוכנית הטיפול. בעומק הנכון, החללית התרמית משתלבת עם ידית קטטר הלייזר, ומאפשרת לה להתיישר בכיוון הנכון.
הערה: לאחר המיקום, בדוק כי החריץ על החללית התרמית יושב לתוך הידית של קטטר לייזר. הגשושית התרמית תינעל במקום ותמנע סיבוב במהלך הטיפול. - חבר צינורות תוך ורידי מובחרים משקית מלוחים ליציאת הזרימה הפרוקסימלית על קטטר הלייזר.
- חבר את מלוחים חוזרים מיציאת הזרימה דיסטלי לשקית ניקוז ברורה, כך נוזל חוזר ניתן לדמיין.
הערה: תמיסת מלח במחזור סביב קטטר הלייזר תקרר את הסיבים במהלך הטיפול
9. בצע את רשימת הפעולות לביצוע בנושא בטיחות
- במסך ניטור הטיפול, בחר את אתר האבלה הרצוי. לאחר בחירת ההבליה המתאימה, הקש על 'אשר בחירה'. רשימת פעולות לביצוע בנושא בטיחות תתפוס כעת את הצד השמאלי של צג תחנת העבודה.
הערה: שלב זה יתחיל במחזור מלוחים דרך קטטר לייזר. בועות קטנות הציג בעת חיבור הצינורות תוך ורידי גלויים בתחילה על אולטרסאונד סביב הלייזר. זה יכול לשמש בדיקה נוספת עבור תנוחת קטטר לייזר. - בצע את רשימת פעולות לביצוע בנושא בטיחות, תוך סימון התיבות לאחר השלמתן.
- ודא כי כל האנשים בחדר לא משקפי בטיחות לייזר כולל המטופל.
- מערכת המחשב של תחנת העבודה תבדוק באופן אוטומטי את הגשוש התרמי כדי לוודא שכל התרמוקולים קוראים טמפרטורות גוף אחידות בין 30 ל -40 מעלות צלזיוס.
- ודא שארבע הלהקות ההדגניות של צנתרי הלייזר ממוקמות בכמוסת הערמונית, שכן מיקום הבדיקה התרמית עשוי לדחוף את הערמונית הרחק מקטטר הלייזר.
הערה: אזור אבלציה מתחיל 5 מ"מ distal לסמנים echogenic ומרחיב עוד 27 מ"מ אורך ו 18 מ"מ קוטר (מקסימאלי).
10. ביצוע אבלציה רקמת לייזר
- לאחר רשימת פעולות לביצוע בטיחות הושלמה לחץ על 'התחל לייזר' כדי להתחיל את אבלציה.
- נטר את התקדמות הטיפול בזמן אמת באמצעות קריאות טמפרטורה, טיימר ומפת נזקים.
הערה: להעריך את טמפרטורת הרקמה ניצול הגרף מרובה שורות בצד שמאל של מודל הערמונית. הטמפרטורה רקטלית מסומן בלבן ולא יעלה על 42 °C (69 °F). הטמפרטורה בקצה קטטר הלייזר מסומנת בכחול (איור 3). הלייזר יכבה באופן אוטומטי אם קצה הלייזר יעלה על 75 °C (75 °F) או הקיר רקטלי עולה על 42°C.
הערה: לאחר שהלייזר פעיל, נטר את זמן הטיפול בכל אתר אבלציה באמצעות הסרגל האדום בחלק העליון של המסך. מפת נזקים מעניקה ייצוג תלת מימדי של רקמה מטופלת בהתבסס על טמפרטורה וזמן.
הערה: הערה משתנה על אולטרסאונד במצב B. רקמת הערמונית בדרך כלל לא משתנה במראה במהלך אבלציה לייזר. עם טיפולים סדרתיים הרקמה עשויה לקבל מראה היפוכואי, אבל הדמיה בארה"ב משמשת בעיקר למיקום של הלייזר.
הערה: צג לגבי תכונות אולטרסאונד כדלקמן:- מערבולת בועות מיקרו להרכיב מעבר להקות קטטר לייזר echogenic עשוי להצביע על דליפה מלוחים במחזור עקב חימום סופר. אמנם אין לכך השפעה בטיחותית, אך ניתן להאט את התקדמות הטיפול.
- עלייה בטבע hyperechoic או "הלבנה" של שומן רקטלי עלולה להתרחש אם קטטר לייזר הוא משך בשוגג לאחור, גרימת חימום של השומן perirectal.
- אם אחד מממצאי אולטרסאונד אלה נצפו טיפול לייזר צריך להיפסק.
- הלייזר מפסיק באופן אוטומטי ברגע שנגמר שעון העצר, אך מתרגל יכול לבחור לסיים את האבלה באופן ידני על-ידי לחיצה על 'עצור את הלייזר'. מלוחים ימשיכו לזרום, קירור קצה הלייזר.
הערה: שקול לעצור את אבלציה מוקדם אם רמת הטמפרטורות מעל 55 °C (60 °F) במשך יותר מ 60 שניות. - שמור על קטטר לייזר בדיקה תרמית במקום עד הטמפרטורה של קטטר לייזר ירד מתחת 42 מעלות צלזיוס, ובכך למנוע חימום קיר רקטלי במהלך נסיגה של קטטר לייזר.
11. אבלציות עוקבות
- מקם את האולטרסאונד באתר אבלציה הבא באמצעות המטרות הדיגיטליות המסופקות על ידי מכשיר ההיתוך.
- להעריך אם תמונות אולטרסאונד חי להישאר רשום MRI הערמונית, ולבצע פיצוי תנועה במידת הצורך.
הערה: אם אתה משתמש בארטמיס, הטכניקה לפיצוי תנועה מתוארת בסרטון שאליו בוצעה הפניה בעבר. 24 (24) - על מסך ניטור הטיפול, אתר אבלציה הראשונית יהיה עכשיו אפור החוצה; עם זאת ניתן לטפל בו שוב אם יש צורך בכך.
- בחר את אתר האבלה הבא מהצד הימני של המסך וחזור על התהליך המתואר בשלבים 8 - 10.
12. סיום הטיפול
- לאחר שכל אתרי אבלציה טופלו, יופיע לחצן 'סיים טיפול'. לחיצה על כפתור זה תציג מסך סקירת טיפול המציג מדדים כמותיים למפגש הטיפול.
- הסר את הגשוש TRUS מפי הטבעת של המטופל. לחץ ידני עשוי להיות מיושם על הקיר רקטלי overlying הערמונית כדי להקל על hemostasis.
תוצאות
התוצאות שפורסמו של FLA מוצגות בטבלה 2. מגוון שיטות וטכנולוגיות כלולות. יותר מ 400 חולים שעברו צורות שונות של FLA לטיפול PCa נמצאים בתוך מסד הנתונים SEER. 25 כדי לכמת את המספר והמאפיינים של FLA שדווחו בספרות ביצענו סקירה שיטתית של מדלין וספריית קוקרן. החיפוש שלנו בוצע באמצעות מונחי חיפוש בכל השדה, כולל "אבלציה של לייזר מוקדי" ו"סרטן הערמונית". בסך הכל נסקרו 247 כותרים ותקצירים. רק מקרים המדווחים על אבלציה בלייזר מוקדי, MRI ותוצאות אונקולוגיות נכללו. 13 פרסומים ביקורת עמיתים מוסמכים להכללה, המייצגים 333 חולים בסך הכל (טבלה 1).
הטיפול בוצע בלייזר דיודה 980 ננומטר בכל המחקרים פרט ל-2. 26,27 פרמטרים טיפול כללו רמות כוח בין 6 - 18 וואט ואת זמני הטיפול פורש 1 - 4 דקות לכל אתר אבלציה (טבלה 1). ניטור טמפרטורת הטיפול סופק על ידי תרמומטריית MRI ב 9 מחקרים ועל ידי מדידות בדיקה טמפרטורה ישירה ב 3 מחקרים (טבלה 1). כל המחקרים בוצעו נשא, למעט אלה על ידי לינדנר ואת המחקר מאוחר יותר על ידי Natarajan. 20,26,27
PSA בסיסי חציוני עבור הקבוצה היה 5.7 (טווח 1.1 - 14.8). בעקבות FLA, PSA החציוני ב 3, 6, 12 ו 24 חודשים היה 3.9, 5.5, 3.8, ו 3.9 בהתאמה. IPSS בסיסי חציוני עבור קבוצת ההאם היה 6. לאחר FLA, IPSS החציוני ב 3, 6, 12 ו 24 חודשים היה 5, 5.5, 7.3 ו 11.5 בהתאמה. ה- SHIM הבסיסי החציוני עבור הקוהורטה היה 20. לאחר FLA, ה-SHIM החציוני ב-3, 6, 12 ו-24 חודשים היה 19, 18, 20 ו-19 בהתאמה.
בכל המחקרים, סיבוכים דווחו באופן לא עקבי; עם זאת היה רק סיבוך אחד מסווג על ידי המחברים כמו כיתה III (זיהום בדרכי השתן). 16 המחברים לא ציינו את התכונות שסיווגו זאת כאירוע בדרגה 3. שתי פיסטולות רקטו-שופכה, שתיהן נסגרות באופן ספונטני לאחר צנתור ממושך,16 דווחו כתופעות לוואי בדרגה 2.
המעקב אונקולוגי היה מקובץ לפי תקופת מעקב: פחות מ 6 חודשים, שנה אחת, ושנתיים (טבלה 2). ביופסיית מעקב בוצעה על ידי ביופסיה מונחית MRI ב-4 מחקרים, וביופסיה של היתוך MRI-US ב-6 מחקרים. שני מחקרים השתמשו בביופסיה שיטתית ושני מחקרים ביצעו חקירות 'טיפול ו כריתה' שבהן הוערכה דגימת כריתת הערמונית. הצלחת הטיפול הוגדרה על פי פרוטוקול קונצנזוס של דלפי. 28 הצלחה בשטח הוגדרה כהיעדר ≥ GG2 PCa בתוך אתר אבלציה הקודם. כשל מחוץ לשדה הוגדר כ- GG2 ≥ מחוץ לאזור של אבלציה קודמת. בקרב חולים עם תוצאות ביופסיה מעקב, ההצלחה הכוללת בשטח לאחר הטיפול ב 6 חודשים (N = 83), 1 שנה (N = 64) ו 2 שנים (N = 39) היה 83%, 83%, ו 59% בהתאמה (טבלה 2).
ב UCLA, FLA של הערמונית בוצעה בשלושה ניסויים קליניים רצופים החל בשנת 2014. 29-31 18 גברים עם סרטן הערמונית בסיכון בינוני עברו FLA, שמונה in-bore ו 10 במרפאה, ללא כל תופעות לוואי בדרגה III. נכון לעכשיו, 10 גברים נוספים עוברים FLA באמצעות המכשיר הפגינו. 31 כל החולים הוערכו לפני FLA עם MRI 3T (סליל הגוף), וביופסיה היתוך MRI-ארה"ב עם דגימה מן ההחזר על ההשקעה ביופסיה שיטתית בתוך 6 חודשים של טיפול. ביופסיות בסיסיות ומעקב בוצעו בהנחיית היתוך MRI/US באמצעות מערכת היתוך ארטמיס עם מעקב אחר כל אתרי הביופסיה.
שולחן 1. דיווחו על מחקרים של אבלציה לייזר מוקדית.
| מספר אסמכתא | מחבר | שנה | N | גיל חציוני (טווח) | עוצמת לייזר | זמן Rx (שניות) | שוליים מתוכננים | הליך In-Bore | ניטור טמפרטורה | גליסון בסיסי | ||||
| 3+3 | 3+4 | 4+3 | 4+4 | |||||||||||
| 26 | לינדנר (199 | 2009 | 12 | 56.5 (51-52) | - | 120 | - | לא | בדיקת טמפרטורה | 12 | 0 | 0 | 0 | |
| 27 | לינדנר (199 | 2010 | 4 | 66 (61-73) | - | 120 | - | לא | בדיקת טמפרטורה | 2 | 0 | 1 | 1 | |
| 5 | אוטו (לא כולל) | 2013 | 9 | 61 (52-77) | 6 - 15 ואט | - | - | כן | תרמומטריית MRI | 8 | 1 | 0 | 0 | |
| 12 | לי | 2014 | 23 | - | 8 ואט | 30-60 | - | כן | תרמומטריית MRI | - | - | - | - | |
| 6 | לפור (לאפור) | 2015 | 25 | 66 (49-84) | - | - | - | כן | תרמומטריית MRI | 11 | 13 | 1 | 0 | |
| 18 | אל-ברקאווי | 2015 | 7 | 61 (56-69) | - | 90 | - | כן | תרמומטריית MRI | 7 | 0 | 0 | 0 | |
| 15 | בומרס (שם) | 2016 | 5 | 66 (58-70) | - | - | 9 מ"מ | כן | תרמומטריית MRI | 2 | 2 | 1 | 0 | |
| 14 | אגנר | 2016 | 27 | 62 (-) | 6 - 15 ואט | 60-120 | 0 -7.5 מ"מ | כן | תרמומטריית MRI | 23 | 3 | 1 | 0 | |
| 19 | נטרג'אן (נטאראג'אן) | 2016 | 8 | 63 (54-72) | 11 - 14 ואט | 180 | מותאם אישית* | כן | בדיקת טמפרטורה # | 1 | 7 | 0 | 0 | |
| 20 | נטרג'אן (נטאראג'אן) | 2017 | 10 | 65 (52-74) | 13.75 ואט | 180 | מותאם אישית* | לא | בדיקת טמפרטורה | 2 | 8 | 0 | 0 | |
| 35 | צ'או | 2018 | 34 | 69 (52-88) | - | - | - | כן | תרמומטריית MRI | 16 | 16 | 2 | 0 | |
| 17 | אל חאקים | 2019 | 49 | 63 (51-73) | 10 - 15 ואט | 120 | 9 מ"מ | כן | תרמומטריית MRI | 13 | 29 | 7 | 0 | |
| 16 | וולסר (1994) | 2019 | 120 | 60 (45-86) | 17 - 18 ואט | 180-240 | 5 מ"מ | כן | תרמומטריית MRI | 37 | 56 | 27 | 0 | |
טבלה 1: מקף (-) מציין מידע שאינו זמין בכתב היד שפורסם. * מציין כל שולי תוכנן בנפרד. # מציין ניטור בוצע עם בדיקת טמפרטורה ותרמומטריה MRI.
שולחן 2. תוצאות של אבלציה לייזר מוקדית.
| מספר אסמכתא | מחבר ראשון | שיטת ביופסיה להמשך טיפול | מעקב אחר ביופסיה | ≤ 6 חודשים | 12 חודשים | 24 חודשים | תופעות לוואי | ||||||
| הצלחה | כישלון | הצלחה | כישלון | הצלחה | כישלון | אני | השני | השלישי | |||||
| 26 | לינדנר (199 | MRI מודרך Bx | 12 | 12 | 0 | - | - | - | - | 2 | 0 | 0 | |
| 27 | לינדנר (199 | כריתת הערמונית | 4 | 2 | 2 | - | - | - | - | - | - | - | |
| 5 | אוטו (לא כולל) | MRI/ארה"ב Bx | 9 | 9 | 0 | - | - | - | - | 1 | 1 | 0 | |
| 12 | לי | MRI/ארה"ב Bx | 13 | - | - | 12 | 1 | - | - | - | - | - | |
| 6 | לפור (לאפור) | MRI מודרך Bx | 21 | 20 | 1 | - | - | - | - | 0 | 0 | 0 | |
| 18 | אל-ברקאווי | Bx שיטתי | 5 | - | - | 5 | 00 | - | - | - | 1 | 0 | |
| 15 | בומרס (שם) | כריתת הערמונית | 5 | 1 | 4 | - | - | - | - | - | - | - | |
| 14 | אגנר | MRI מודרך Bx # | 27 | 27 | - | 7 | 31 | - | - | 7 | 2 | 0 | |
| 19 | נטרג'אן (נטאראג'אן) | MRI/ארה"ב Bx | 8 | 6 | 53 | - | - | - | - | 23 | 7 | 0 | |
| 20 | נטרג'אן (נטאראג'אן) | MRI/ארה"ב Bx | 10 | 6 | 40 | - | - | - | - | 38 | 6 | 0 | |
| 35 | צ'או | MRI/ארה"ב Bx | 22 | - | - | - | - | 13 | 9 | - | - | - | |
| 17 | אל חאקים | MRI/ארה"ב Bx | 49 | - | - | 40 | 911 | - | - | 34 | 11 | 0 | |
| 16 | וולסר (1994) | MRI מודרך Bx | 44* | - | - | - | - | 26 | 18 | 8 | 8 | 1 | |
הערות שוליים טבלה 2. הצלחה = היעדר ≥ GG2 סרטן הערמונית בתוך אזור אבלציה. כישלון = נוכחות של ≥ GG2 סרטן הערמונית: סה"כ מחוץ למגרש (מספר כתב תחתי). # מציין ביופסיה מונחית MRI שימש במשך 6 חודשים ביופסיה אבל רק ביופסיה שיטתית שימש ביופסיה 12 חודשים. * מציין כי רק חולים עם הפחתת PSA של < 50% ו- MRI אבלציה חיובית לאחר שעבר ביופסיה; 76 חולים לא עברו ביופסיה.
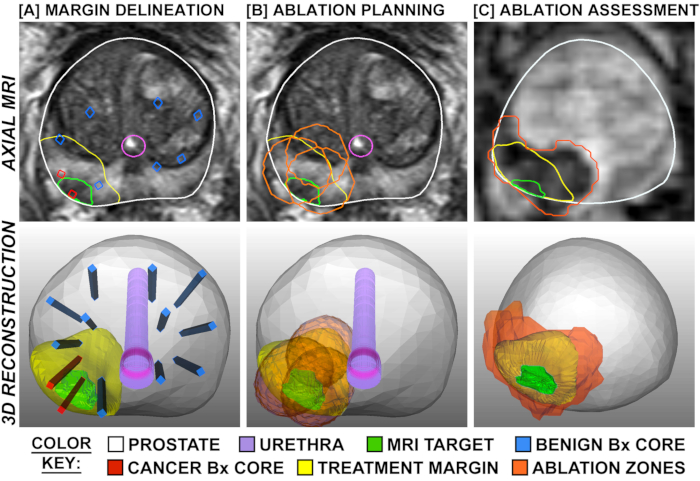
איור 1: תכנון והערכה של טיפול, המוצגים באמצעות שכבות-על ב- MRI רוחבי (שורה עליונה) ובתלת-ממד (שורה תחתונה). עמודה A מציגה את התיווך של שולי הטיפול, המורחבים סביב יעד MRI חיובי לסרטן וחסומים על ידי ליבות ביופסיה שיטתיות שליליות סמוכות (כחול). עמודה ב' מציגה תכנון של מיקומי אבלציה כך שולי הטיפול חופפים כדי למנוע אזורים 'לדלג'. עמודה C מציגה הדמיה משוקללת זלוף שנאספה שעתיים לאחר הטיפול, ומדגימה התכתבות בין היקף אבלציה המתוכנן והמצופה. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
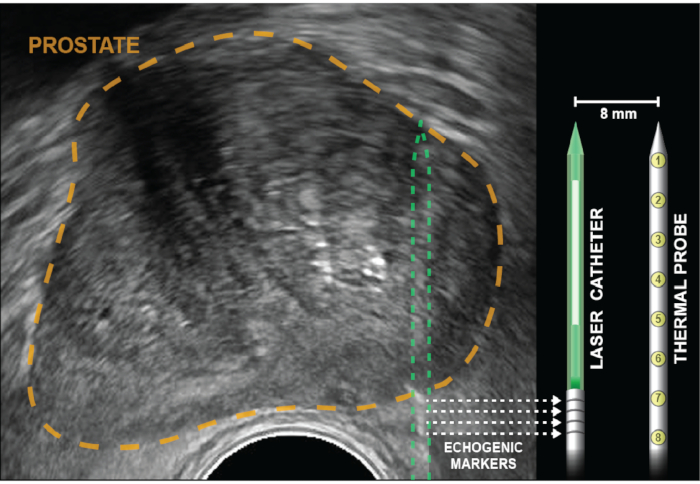
איור 2: אולטרסאונד צירי עם הערמונית מתואר בזהב. מחזירי קוביות פינתיים (רצועות אקוגניות), המצוינים על ידי חצים מנוקדים, חרוטים בקטטר הלייזר 5 מ"מ מהמפזר (לבן). בדיקת טמפרטורה מוכנסת לאותו עומק כמו סיבי הלייזר, ואז נעולה במקומה ונשארת מקבילה ללייזר 8 מ"מ זה מזה, ממישור הראייה של ארה"ב. שמונה חיישנים תרמיים, שנמצאים בתוך החללית במרחק של 4 מ"מ זה מזה, מספקים הקלטות טמפרטורה בנקודות מבסיס הרצועות ההדגניות ועד לקצה קטטר הלייזר. מדידות הטמפרטורה הקרובות ביותר לקיר פי הטבעת מסופקות על ידי מדידות תרמיות בבסיס בדיקת הטמפרטורה (עמדות 6-8). לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 3: הקלטות טמפרטורה במהלך אבלציה לייזר מוקד עבור שני אבלציות רצופות. ציר Y = טמפרטורה בצלזיוס. ציר X = זמן בדקות. פסים מוצללים אנכיים = תקופות של הפעלת לייזר. קו כחול = טמפרטורה 8 מ"מ מקצה סיבי לייזר (תרמוקופול דיסטלי). קו לבן = טמפרטורה 8 מ"מ מתרמוקופלה פרוקסימלית הקרובה ביותר לקיר רקטלי. טמפרטורה של 60 מעלות צלזיוס, מושגת אפילו לזמן קצר, מבטיח נמק קרישה. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
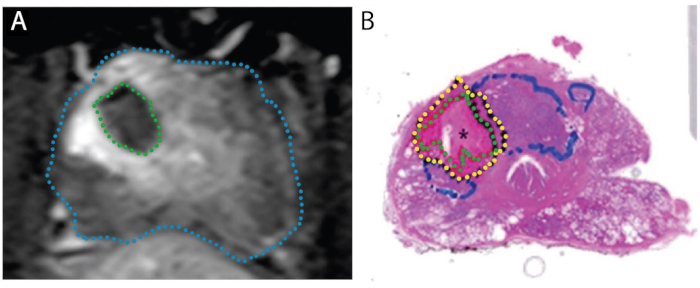
איור 4: תמונות הממחישות קונקורדנציה של אזור אבלציה ב- MRI (A) שלאחר הטיפול עם אזור נמק בפועל על דגימת הרכבה שלמה (B). המטופל הוא גבר בן 67 עם PCa באזור המעבר הימני, גליסון ציון 3 + 4 = 7, השתתפות בניסוי 'לטפל ולכרות'. א. תמונה משופרת של ניגודיות משוקללת T1 לאחר אבלציה, המציגה פגם בזלוף שנגרם על ידי טיפול לייזר (ירוק). ב. כתם H&E של הערמונית. הרקמה הנמקית מוגדרת בירוק, רקמת פרי-נמק בצהוב, וגידול שלם (לא מטופל) בכחול. משוחזר תחת רישיון Creative Commons מ Bomers ואח ', כתב העת העולמי לאורולוגיה. 15 אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
Discussion
מטרת העבודה הנוכחית היא לתאר ולהמחיש שיטה לביצוע אבלציה לייזר מוקדית (FLA) של סרטן הערמונית (PCa). השיטה שונה משיטות טיפול מוקדיות אחרות, שכן היא מיועדת להתבצע בהרדמה מקומית במסגרת מרפאה. שיטת FLA המוצגת כאן הוצגה בשנת 2017,20 ומאז היא מעודנת ברציפות. לפיכך, ההליך המתואר במאמר זה עשוי להיות בעל ערך לחוקרים עתידיים.
טיפול לייזר של רקמת הערמונית נראה עד כה מן המחקר של McNicholas ועמיתיו, עובד באוניברסיטת קולג 'בלונדון, אשר הוכיחה בשנת 1993 כי נמק קרישה מוקד יכול להיות מיוצר בערמונית כלבים עם מכשיר Nd:YAG. 32 Foreshadowing העתיד, מחברים אלה הניחו כי הטכניקה "... עשוי להוכיח ערך... להרס של גידולים פרוסטטיים מוקדיים קטנים." לאחר מכן, אבלציה בלייזר של PCa באדם תוארה בשנת 2009 על ידי לינדנר ואח 'מאוניברסיטת טורונטו. 26 במאמץ חלוצי זה, לינדנר שילב את המודאליות המתעוררת של MRI הערמונית עם תוכנת היתוך תמונה מוקדמת ובדיקות תרמיות קונבנציונליות כדי למקד בהצלחה סרטן ולנטר אבלציה לייזר ב 12 גברים.
מאז PCa החשוב ביותר ניתן לדמיין עם MRI רב פרמטרי עכשווי, פילוח in-bore וטיפול בנגעים גלויים עשוי להיות הרחבה פשוטה של הליך האבחון. מיקוד נשא של הנגע הוא ישיר, ותרמומטריית MR מאפשר ניטור מרחוק של אבלציה. רז ואח' דיווחה על שני טיפולים כאלה בשנת 2010. 33 סדרה של טיפולי FLA נשא (N = 9) דווח על ידי אוטו ועמיתיו בשנת 2013. 5 אימוץ של FLA נשא כבר הקל על ידי חומרה שפותחה למטרה זו, כפי שדווח על ידי Natarajan ואח 'בשנת 2016. 19 מספר רדיולוגים, באמצעות סיבי לייזר מקוררים במים כדי למנוע חריכה אימצו את השיטה in-bore; ומאות טיפולי FLA נשאו דווחו כעת (וולסר, פלר, ספרלינג / לפור). 6,16,34,35
בעוד תוצאות אונקולוגיות לטווח קצר של FLA נשא עשוי להיות חיובי (טבלה 1), ההליך לא צפוי להיות מאומץ נרחב, בגלל גורמים מגבילים המתוארים בהקדמה. יתר על כן, תרמומטריית MR לניטור טיפול תערוכות מספר מגבלות חשובות. 19 בנייה על ניסיון של עשור עם MRI / ארה"ב ביופסיה היתוך נהלים (N ~ 4000), אנו מאותרת כי סיב לייזר יכול להיות ממוקד לתוך נגע סרטן, בדומה להחדרת מחט ביופסיה, וכי ניטור של טיפול יכול להתבצע ישירות עם בדיקות תרמיות. לכן, בעקבות החוויה in-bore, עשרה חולים עברו FLA מחוץ לשעמום במרפאה אורולוגיה UCLA, באמצעות הרדמה מקומית בלבד, MRI / ארה"ב הדרכה היתוך, ניטור בדיקה תרמית. 20 לא רק בטיחות והיתכנות של השיטה החדשה הוכיחה, אבל בקרב החולים האחרונים שטופלו, אין ראיות של PCa ניתן למצוא בביופסיה הבאה.
אפקט הרקמה של FLA הובהר בשני מחקרים, שבהם כריתת הערמונית הרדיקלית המתוכננת בוצעה 1-3 שבועות לאחר הליך הלייזר (N = 9), כלומר, מודל 'טיפול ו כריתה' (איור 4). 15,27 בכל 9 החולים, נפח הרקמה הנמקית שנמצאה בערמונית קירב את הנפח המוערך על ידי ה- MRI שהושג לאחר סיום הטיפול. כאשר כל הערמונית נותחו, נראה מעבר פתאומי בין נמק לתאים שלמים 1-5 מ"מ מחוץ לאזור אבלציה של לייזר (איור 1). השוליים החדים והדיוק של אזורי אבלציה יש השלכות חשובות על הדיוק של MRI / ארה"ב רישום ותכנון טיפול.
חלק מרכזי במערכת Avenda הוא תוכנת תכנון הטיפול. עבור FLA יעיל, התכנון צריך לכלול לא רק את המיקום של הנגע, אלא גם את נפח הרקמה הדרושים להרס הגידול המלא. נפח אבלציה לא יכול להיות פשוט נפח נגע MRI, כי נפח הגידול בפועל עולה על זה של הנגע נראה MRI על ידי ממוצע של 3-פי. 21 יתר על כן, סרטן לעתים קרובות משתרע על תחזיות כמו אצבע לא סדירה, אשר יגרום לא אמין כל מרווח בטיחות אחיד מבוסס אך ורק על הדמיה (למשל, 1 ס"מ מעבר לגבול של נגע MRI גלוי). מערכת Avenda כוללת תוכנת תכנון טיפול המשתמשת לא רק בנגע הנראה ל- MRI, אלא גם מעקב תלת מימדי של אתרי ביופסיה (חיוביים ושליליים) כדי לספק מיקום מדויק של נפח אבלציה מינימלי שיקיף באופן מלא את הסרטן. דוגמה לתכנון טיפול כזה מוצגת באיור 3.
לסיכום, FLA היא שיטה בטוחה וישימה למיגור סרטן הערמונית במרפאה תחת הרדמה מקומית. שלבי ההליך מוצגים בסרטון הנלווה. מיקום מדויק של סיבי הלייזר בנגע נראה MRI מושגת באמצעות היתוך MRI / ארה"ב, ממש כמו מחטי ביופסיה ממוקמים לתוך נגעים כאלה. ניטור טיפול בזמן אמת מושגת באמצעות בדיקה תרמית הסמוכה לסיבי הלייזר. תוכנת תכנון טיפול, אשר מעסיקה נפחי נגע מ- MRI ומעקב אחר מיקומי אתר ביופסיה כדי לסייע למפעיל לקבוע את שולי הטיפול, היא חלק חשוב של המערכת. במרפאה FLA כמתואר ומודגם במאמר זה נראה לספק אפשרות טיפול מוקד אטרקטיבי לא זמין בעבר.
Disclosures
ד"ר מרקס וד"ר נטרג'אן הם מייסדים שותפים של Avenda Health.
Materials
| Name | Company | Catalog Number | Comments |
| Fusion Guidance System | NA | Artemis Displayed in Video | |
| Laser Catheter | Avenda Health | ||
| Orion Workstation | Avenda Health | ||
| Thermal Probe | Avenda Health | ||
| Transrectal Probe | NA | Not Platform Dependent | |
| Ultrasound | NA | Not Platform Dependent |
References
- Cooperberg, M. R., Carroll, P. R. Trends in management for patients with localized prostate cancer, 1990-2013. JAMA - Journal of the American Medical Association. 314 (1), 80-82 (2015).
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics, 2020. CA: A Cancer Journal for Clinicians. 70 (1), 7-30 (2020).
- Connor, M. J., Gorin, M. A., Ahmed, H. U., Nigam, R. Focal therapy for localized prostate cancer in the era of routine multi-parametric MRI. Prostate Cancer and Prostatic Diseases. , 1-12 (2020).
- Ahmed, H. U., et al. Focal Therapy for Localized Prostate Cancer: A Phase I/II Trial. The Journal of Urology. 185, 1246-1255 (2011).
- Oto, A., et al. MR imaging-guided focal laser ablation for prostate cancer: Phase I trial. Radiology. 267 (3), 932-940 (2013).
- Lepor, H., Llukani, E., Sperling, D., Fütterer, J. J. Complications, Recovery, and Early Functional Outcomes and Oncologic Control Following In-bore Focal Laser Ablation of Prostate Cancer. European Urology. 68 (6), 924-926 (2015).
- Johnson, D. C., et al. Detection of Individual Prostate Cancer Foci via Multiparametric Magnetic Resonance Imaging. European Urology. 75 (5), 712-720 (2019).
- Johnson, D. C., et al. Do contemporary imaging and biopsy techniques reliably identify unilateral prostate cancer? Implications for hemiablation patient selection. Cancer. 125 (17), 2955-2964 (2019).
- Liu, W., et al. Copy number analysis indicates monoclonal origin of lethal metastatic prostate cancer. Nature Medicine. 15 (5), 559-565 (2009).
- Ahmed, H. U. The Index Lesion and the Origin of Prostate Cancer. New England Journal of Medicine. 361 (17), 1704-1706 (2009).
- Stafford, R. J., et al. Magnetic resonance guided, focal laser induced interstitial thermal therapy in a canine prostate model. Journal of Urology. 184 (4), 1514-1520 (2010).
- Lee, T., Mendhiratta, N., Sperling, D., Lepor, H. Focal laser ablation for localized prostate cancer: principles, clinical trials, and our initial experience. Reviews in urology. 16 (2), 55-66 (2014).
- Johnson, D. E., Cromeens, D. M., Price, R. E. Interstitial laser prostatectomy. Lasers in Surgery and Medicine. 14 (4), 299-305 (1994).
- Eggener, S. E., Yousuf, A., Watson, S., Wang, S., Oto, A. Phase II Evaluation of Magnetic Resonance Imaging Guided Focal Laser Ablation of Prostate Cancer. Journal of Urology. 196 (6), 1670-1675 (2016).
- Bomers, J. G. R. R., et al. MRI-guided focal laser ablation for prostate cancer followed by radical prostatectomy: correlation of treatment effects with imaging. World Journal of Urology. 35 (5), 703-711 (2017).
- Walser, E., et al. Focal Laser Ablation of Prostate Cancer: Results in 120 Patients with Low- to Intermediate-Risk Disease. Journal of Vascular and Interventional Radiology. 30 (3), 401-409 (2019).
- Al-Hakeem, Y., Raz, O., Gacs, Z., Maclean, F., Varol, C. Magnetic resonance image-guided focal laser ablation in clinically localized prostate cancer: safety and efficacy. ANZ Journal of Surgery. 89 (12), 1610-1614 (2019).
- Barqawi, A., Krughoff, K., Li, H., Patel, N. U. Initial Experience of Targeted Focal Interstitial Laser Ablation of Prostate Cancer with MRI Guidance. Current Urology. 8 (4), 199-207 (2014).
- Natarajan, S., et al. Focal Laser Ablation of Prostate Cancer: Phase I Clinical Trial. Journal of Urology. 196 (1), 68-75 (2016).
- Natarajan, S., et al. Focal Laser Ablation of Prostate Cancer: Feasibility of Magnetic Resonance Imaging-Ultrasound Fusion for Guidance. Journal of Urology. 198 (4), 839-847 (2017).
- Priester, A., et al. Magnetic Resonance Imaging Underestimation of Prostate Cancer Geometry: Use of Patient Specific Molds to Correlate Images with Whole Mount Pathology. Journal of Urology. 197 (2), 320-326 (2017).
- Lightner, D. J., Wymer, K., Sanchez, J., Kavoussi, L. Best Practice Statement on Urologic Procedures and Antimicrobial Prophylaxis. Journal of Urology. 203 (2), 351-356 (2020).
- Jones, T. A., Radtke, J. P., Hadaschik, B., Marks, L. S. Optimizing safety and accuracy of prostate biopsy. Current Opinion in Urology. 26 (5), 472-480 (2016).
- Jayadevan, R., Zhou, S., Priester, A. M., Delfin, M., Marks, L. S. Use of MRI-ultrasound fusion to achieve targeted prostate biopsy. Journal of Visualized Experiments. (146), e59231 (2019).
- Zheng, X., et al. Focal Laser Ablation Versus Radical Prostatectomy for Localized Prostate Cancer: Survival Outcomes From a Matched Cohort. Clinical Genitourinary Cancer. 17 (6), 464-469 (2019).
- Lindner, U., et al. Image Guided Photothermal Focal Therapy for Localized Prostate Cancer: Phase I Trial. Journal of Urology. 182, 1371-1377 (2009).
- Lindner, U., et al. Focal Laser Ablation for Prostate Cancer Followed by Radical Prostatectomy: Validation of Focal Therapy and Imaging Accuracy. European Urology. 57 (6), 1111-1114 (2010).
- van Luijtelaar, A., et al. Focal laser ablation as clinical treatment of prostate cancer: report from a Delphi consensus project. World Journal of Urology. 37, 2147-2153 (2019).
- . Use of Laser Interstitial Thermal Therapy in the Focal Treatment of Localized Prostate Cancer - NCT02224911 Available from: https://clinicaltrials.gov/ct2/show/NCT02224911 (2020)
- . Focal Laser Ablation of Prostate Tissue - NCT02357121 Available from: https://clinicaltrials.gov/ct2/show/NCT02357121 (2020)
- . Focal Laser Ablation of Prostate Cancer -NCT04305925 Available from: https://clinicaltrials.gov/ct2/show/NCT04305925 (2020)
- McNICHOLAS, T. A., STEGER, A. C., BOWN, S. G. Interstitial Laser Coagulation of the Prostate An Experimental Study. British Journal of Urology. 71 (4), 439-444 (1993).
- Raz, O., et al. Real-Time Magnetic Resonance Imaging-Guided Focal Laser Therapy in Patients with Low-Risk Prostate Cancer. European Urology. 58 (1), 173-177 (2010).
- . Transrectally delivered, outpatient MRI-guided laser focal therapy of prostate cancer: 9.5 year interim results of NCT #02243033, Presentation at the AdMeTech 4th Global Summit on Precision Diagnosis and Treatment of Prostate Cancer Available from: https://www.admetech.org/wp-content/uploads/2019/08/DMI-FOCAL-Tx-2019-NCT-02243033.FINAL_.pdf (2020)
- Chao, B., Llukani, E., Lepor, H. Two-year Outcomes Following Focal Laser Ablation of Localized Prostate Cancer. European Urology Oncology. 1 (2), 129-133 (2018).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved