Method Article
Fokale Laserablation von Prostatakrebs: Ein Büroverfahren
In diesem Artikel
Zusammenfassung
Dieser Artikel stellt eine ambulante Behandlung von Prostatakrebs mittels fokaler Laserablation vor und beschreibt sie. Die Platzierung des Laserkatheters wird durch die MRT-Ultraschall-Fusionsbildgebung ähnlich wie bei der Prostatanadelbiopsie geleitet. Die Behandlung wird in Echtzeit mit einer thermischen Sonde überwacht, die neben der Laserfaser platziert wird.
Zusammenfassung
In diesem Artikel beschreiben und veranschaulichen wir ein ambulantes Verfahren zur fokalen Laserablation (FLA) von Prostatakrebs (PCa). Das Verfahren ähnelt konzeptionell einer Fusionsbiopsie und wird unter örtlicher Betäubung in einer Klinik durchgeführt; Die Behandlungszeit beträgt in der Regel weniger als eine Stunde. Lasereinführung wird durch Ultraschall geführt; Das Läsions-Targeting erfolgt über Magnetresonanztomographie-Ultraschall -Ultraschall (MRT / US) -Fusion, wie bei der gezielten Prostatabiopsie. Die Echtzeit-Ablationsüberwachung wird mit einer thermischen Sonde neben der Laserfaser erreicht. Das Video zeigt die Behandlungsplanung, die Patientenvorbereitung, verschiedene Schritte während des Eingriffs und die Behandlungsüberwachung. Sicherheit, Machbarkeit und Wirksamkeit dieses Ansatzes wurden in einer früheren Studie nachgewiesen. Ambulante FLA unter örtlicher Betäubung ist eine Option zur Behandlung von Prostatakrebs mit mittlerem Risiko.
Einleitung
Prostatakrebs (PCa) ist die häufigste interne Malignität bei US-Männern1. Im Jahr 2020 werden etwa 190.000 neue Fälle und 33.000 Todesfälle erwartet, was sie zur zweithäufigsten Krebstodesursache bei Männern macht2. Die meisten Fälle von PCa sind heilbar, wenn sie während der Lokalisierung in der Prostata behandelt werden. Die Identifizierung von Krebs in der Prostata ist jedoch mit herkömmlicher Ultraschallbildgebung (US) oft nicht möglich; Daher hat die Behandlung traditionell eine Operation oder Bestrahlung der gesamten Drüse beinhaltet. Das Paradigma der "ganzen Drüse" wurde mit der Einführung der Magnetresonanztomographie (MRT) verändert, die im Gegensatz zu den USA die Lokalisierung von PCa und die gezielteBiopsie ermöglicht 3,4,5,6. Während die MRT wahrscheinlich die Multifokalität von PCa7unterschätzt und kleine Läsionen8übersehen kann, kann sie die Indexläsion, die fast immer der Treiber der metastasierten Erkrankung ist, zuverlässig identifizieren9,10.
Die zuverlässige MRT-Identifizierung von Indexläsionen hat einen Weg für die fokale Behandlung von PCa (d. H. Partielle Drüsenablation (PGA)) geschaffen. Ziel von PGA ist es, die Indexläsion zu zerstören und gleichzeitig das Organ zu erhalten und so Nebenwirkungen zu minimieren. Die fokale Laserablation (FLA), die Lichtenergie verwendet, um Gewebe durch koagulative Nekrose11,12zu zerstören, ist eine Form der PGA. Die Wirksamkeit der Laserenergie zur Ablatierung von Prostatagewebe wurde 199313festgestellt, was auf die Platzierung von Laserfasern in Prostatakrebs zu diesem Zweck hindeutet. Unter Verwendung der MRT zur Führung der Faserplatzierung und der MRT-Thermografie zur Behandlungsüberwachung (d. H. In-Bore-Behandlung) scheinen sich die kurzfristigen Erfolgsraten der FLA denen der Operation oder Bestrahlung zu nähern5,6,12,14,15,16,17,18,19. Laserverfahren, die in der Bohrung oder in einer MRT-Röhre durchgeführt werden, sind jedoch oft umständlich, teuer, zeitaufwendig und ressourcenintensiv. Und In-Bore-Verfahren werden nur von subspezialisch ausgebildeten Radiologen durchgeführt.
Als Alternative zur In-Bore-FLA wird die Machbarkeit der Durchführung von FLA in einer Klinikumgebung--- unter Anwendung der MRT / US-Fusion zur Führung und eines interstitiellen Temperaturfühlers zur Behandlungsüberwachung--- seit 2014 an der UCLA untersucht19,20. Das FLA-Verfahren in einer Klinik hat sich als ähnlich wie bei einer gezielten Biopsie erwiesen, bei der eine Biopsienadel durch eine Laserfaser ersetzt wird. Im Vergleich zu HIFU und Kryotherapie, den anderen derzeit verfügbaren Methoden der PGA, ist die hier beschriebene Lasermethode schnell und kostengünstig, ohne dass ein Operationssaal oder eine Vollnarkose erforderlich ist.
Dieser Artikel zielt darauf ab, ambulante FLA unter örtlicher Betäubung in einer urologischen Klinik zu beschreiben und zu demonstrieren. Urologen, die mit der MRT/US-Fusion für eine gezielte Biopsie vertraut sind, werden die Ähnlichkeiten von FLA mit dem Biopsieverfahren zu schätzen wissen. Sekundäre Ziele sind die Beschreibung technischer Elemente, die die Benutzerfreundlichkeit erleichtern, und die Beschreibung der Vorteile der fokalen Therapie.
Protokoll
HINWEIS: Die hier beschriebenen Methoden sind diejenigen, die an der UCLA zur Durchführung von FLA der Prostata verwendet werden. Das Forschungsprojekt, einschließlich des Protokolls, wurde vom UCLA Institutional Review Board (IRB) genehmigt. Alle Patienten hatten eine gezielte Biopsie der Prostata, bei der die MRT von einem erfahrenen Uro-Radiologen interpretiert wurde. Die im MRT sichtbaren Läsionen wurden innerhalb der interessierenden Region (ROI) und außerhalb des ROI mit einer systematischen Vorlage biopsiert. Die positiven Biopsien und die MRT-Region von Interesse werden verwendet, um die Behandlung mit Laserablation zu planen, um die Indexläsion zu behandeln und einen Rand des behandelten Gewebes um den Tumor herum zu schaffen, da die MRT die Größe des Tumors unterschätzt. 21 Nur Patienten mit Prostatakrebs mit mittlerem Risiko (GG2-3 PSA < 20, Stadium < T2), einem ROI mit einem einzigen Index und keinem kontralateralen klinisch signifikanten Prostatakrebs kommen für eine Behandlung in Frage. Patienten mit Blutungsdiathese oder Unfähigkeit, eine Behandlung ohne Sedierung zu tolerieren, gelten als nicht förderfähig.
1. Behandlungsplanung
- Planen Sie vor der Behandlung Ablationsziele unter Verwendung der Beiträge aus den MRT- und Biopsiekoordinaten.
- Führen Sie die Behandlungsplanung mit der mitgelieferten Software durch.
2. Vorbereitung des Verfahrensraums
- Zeigen Sie ein Laserwarnzeichen außerhalb des Eingriffsraums an.
- Positionieren Sie die Workstation für einen bequemen Zugriff.
- Schalten Sie die Workstation, das Fusionsgerät und den transrektalen Ultraschall ein.
- Geben Sie Anmeldeinformationen ein und wählen Sie den gewünschten Patienten aus der Standardarbeitsliste mit nicht ausführenden Plänen aus.
HINWEIS: Neue Behandlungspläne können über eine USB- oder Internetverbindung hinzugefügt werden, wie im Benutzerhandbuch beschrieben. - Hängen Sie einen Beutel Mit Kochsalzlösung an den dafür vorgesehenen Haken an der Workstation; ein Abfall-Kochsalz-Rücksendebeutel ist ebenfalls angebracht.
- Grundieren Sie den Salzschlauch, indem Sie den Schwerkraftfluss der Flüssigkeit zulassen, bevor Sie den Schlauch verriegeln. Die Kochsalzlösung wird dann mit der Peristaltikpumpe verbunden und für die spätere Verwendung während des Eingriffs aufgehängt.
3. TRUS-Sondenvorbereitung
- Tragen Sie Ultraschallgelee direkt auf eine saubere TRUS-Sonde auf.
HINWEIS: An der UCLA werden alle TRUS-Sonden über ein automatisiertes System mit verdampfter Wasserstoffperoxidlösung desinfiziert. - Passen Sie ein Kondom über dem Ultraschallgelee auf die TRUS-Sonde und befesten Sie es an der Basis mit einem Gummiband.
HINWEIS: Versuchen Sie standardmäßig, Luftblasen zu entfernen, die unter dem Kondom eingeschlossen sind. - Legen Sie eine Mehrkanalführung über das Kondom und verriegeln Sie es mit der Metallklemme. Ein zweites Kondom mit internem Ultraschallgelee kann über die Mehrkanalführung gelegt werden, um den Patientenkomfort zu erhöhen.
4. Vorbereitung des Patienten
- Weisen Sie den Patienten an, sein Rektumgewölbe am Morgen der Biopsie mit und Einlauf zu reinigen.
- Stellen Sie sicher, dass der Patient 60 Minuten vor dem Eingriff prophylaktische Antibiotika erhalten hat22.
HINWEIS: An der UCLA wird 1 g Ertapenem 60 Minuten vor dem Eingriff intramuskulär verabreicht. Diese Entscheidung wurde auf der Grundlage des UCLA-Antibiogramms getroffen und hatte septische Episoden nach der Biopsie in den letzten 1500 transrektalen Biopsien verhindert. 23 Angesichts dieses Erfolgs haben wir uns entschieden, es auch für die transrektale Laserablation zu verwenden. - Patienten 60 Minuten vor dem Eingriff mit Acetaminophen 1000 mg PO, Ketorolac 30 mg IM und optional, aber empfohlen Diazepam 10 mg PO zur Verfügung stellen.
HINWEIS: Patienten können während des Eingriffs einen moderaten Wunsch nach Entleerung oder Druck im Penis verspüren. Unserer Erfahrung nach sind keine Betäubungsmittel von Vorteil. - Patienten können es nützlich finden, persönliche Musik und Kopfhörer als zusätzliches Anxiolytikum mitzubringen.
- Platzieren Sie den Patienten in der linken lateralen Dekubitusposition wie bei der transrektalen Biopsie.
- Zeichnen Sie die Vitalparameter des Patienten vor Beginn des Eingriffs und im Abstand von 30 Minuten auf.
5. Verabreichung der Prostatanervenblockade
- Setzen Sie die geschmierte TRUS-Sonde ein, bis die Mitte der Prostata deutlich sichtbar ist.
- Optimieren Sie die Ultraschallverstärkung, die Zeitverstärkungskompensation (TGC-Schieberegler rechts von den meisten Ultraschallgeräten), die Tiefe und den Fokus, so dass die Prostata im Ultraschallbetrachtungsmonitor zentriert ist.
HINWEIS: Die optimale Verstärkung führt zu einem mittelgrauen Bild innerhalb der Peripheriezone. Die TGC-Schieberegler werden am besten in einem allmählich abfallenden Winkel eingestellt, um die Wellendämpfung entfernter Gewebe zu kompensieren. Die Ultraschalltiefe und der Fokus hängen von der Größe der Prostata ab. Der Fokus sollte auf die periphere Zone gelegt werden, um die Visualisierung von akustischen Markern auf dem Laserkatheter zu optimieren. - Aktivieren Sie den Biopsieleitfaden auf dem Bildschirm und legen Sie eine 22-Gauge-Spinalnadel durch die Mitte der Mehrkanalführung, um die Prostata zu betäuben.
HINWEIS: An der UCLA betäuben wir die Prostata in der sagittalen Ebene, indem wir 10-20 ml Lidocain / Marcain an der Verbindung von Prostata und Samenbläschen platzieren. Die richtige Infiltration führt zu einer Trennung der Samenbläschen und der Prostata von der Rektalwand.
6. MRT-US-Fusion
- Positionieren Sie das bildgebende Fusionssystem und den Arbeitsplatz nahe genug am Patienten, um die Bildschirme des Arbeitsplatzes zu visualisieren und gleichzeitig den Patienten zu beobachten.
- Wenn Sie artemis verwenden, verwenden Sie eine zuvor beschriebene Technik zum Andocken und zur Bildregistrierung. 24
7. Zielakquisition
- Navigieren Sie den Ultraschall mit digitalen Zielen, die von der Fusionsvorrichtung bereitgestellt werden, in die Mitte der ersten Ablationsstelle. Dieser Prozess ähnelt der Führung des Ultraschalls zu einer MRT-Region von Interesse während der Fusionsbiopsie.
HINWEIS: Jede Ablationsstelle wird aus der interessierenden MRT-Region und positiven Biopsiekernen bestimmt (Abbildung 1). Der Behandlungsplan des Patienten sollte während der oben beschriebenen Vorbereitung des Behandlungsraums auf den Arbeitsplatz und das Fusionsgerät übertragen werden. - Wählen Sie die aktuelle Ablationszone aus.
8. Platzierung von Laserkatheter und Temperaturfühler
- Legen Sie den 14-Gauge-Laserkatheter in die Mittelkammer der Mehrkanalführung.
HINWEIS: Die Mehrkanalführung ist gekrümmt, um eine leichte Reibung zu erreichen, wodurch verhindert wird, dass Behandlungselemente während der Ablation nach hinten rutschen. Überwinden Sie diese Reibung, indem Sie sich hin und her drehen, während Sie den Laserkatheter in die Prostata vorschieben. - Bringen Sie den Laserkatheter voran, bis vier echogene Bänder visualisiert und mit dem Tiefenmarker auf dem Bildschirm ausgerichtet sind. Bei einer peripheren Zonenablation befinden sich die Marker mehrere mm außerhalb der Prostatakapsel (Abbildung 2).
HINWEIS: Im Falle einer faserigen hinteren Kapsel kann der Laserkatheter die Prostatakapsel ablenken, anstatt sie zu durchqueren. Jede Ablenkung ist während des Einsetzens auf dem Ultraschall sichtbar. Sollte es zu einer Ablenkung kommen, entfernen Sie den Laserkatheter und setzen Sie eine Führungslinie, wie die stabile Wärmesonde, ein, um eine Pilotöffnung in der Kapsel zu erzeugen. Der Laserkatheter kann dann wie geplant vorgeschoben werden. - Setzen Sie die Wärmesonde je nach Behandlungsplan links oder rechts des Laserkatheters ein. In der richtigen Tiefe verzahnt sich die Thermosonde mit dem Laserkathetergriff, so dass sie in der richtigen Ausrichtung ausgerichtet werden kann.
HINWEIS: Überprüfen Sie nach der Platzierung, ob der Schlitz an der Wärmesonde in den Griff des Laserkatheters eingesetzt wurde. Die Wärmesonde rastet magnetisch ein und verhindert eine Rotation während der Behandlung. - Verbinden Sie den grundierten intravenösen Schlauch aus dem Salzbeutel mit dem proximalen Zuflussanschluss des Laserkatheters.
- Verbinden Sie die zurückfließende Kochsalzlösung aus dem distalen Ausflussanschluss mit einem klaren Drainagebeutel, damit die zurückfließende Flüssigkeit visualisiert werden kann.
HINWEIS: Zirkulierende Kochsalzlösung um den Laserkatheter kühlt die Faser während der Behandlung
9. Führen Sie die Sicherheitscheckliste durch
- Wählen Sie auf dem Überwachungsbildschirm der Behandlung die gewünschte Ablationsstelle aus. Sobald die entsprechende Ablation ausgewählt ist, drücken Sie "AUSWAHL BESTÄTIGEN". Eine Sicherheitscheckliste befindet sich nun auf der linken Seite des Arbeitsplatzmonitors.
HINWEIS: Dieser Schritt beginnt mit der Zirkulation von Kochsalzlösung durch den Laserkatheter. Kleine Blasen, die beim Verbinden der intravenösen Röhren entstehen, sind zunächst im Ultraschall um den Laser herum sichtbar. Dies kann als zusätzliche Kontrolle für die Laserkatheterposition dienen. - Befolgen Sie die Sicherheitscheckliste und kreuzen Sie die Kästchen an, sobald Sie fertig sind.
- Stellen Sie sicher, dass alle Personen im Raum eine Laserschutzbrille tragen, einschließlich des Patienten.
- Das Workstation-Computersystem überprüft automatisch die Wärmesonde, um sicherzustellen, dass alle Thermoelemente gleichmäßige Körpertemperaturen zwischen 30 - 40 °C ablesen.
- Bestätigen Sie, dass sich die vier echogenen Bänder der Laserkatheter an der Prostatakapsel befinden, da die Platzierung der Wärmesonde die Prostata vom Laserkatheter wegdrücken kann.
HINWEIS: Die Ablationszone beginnt 5 mm distal zu den echogenen Markern und erstreckt sich um weitere 27 mm Länge und 18 mm Durchmesser (maximal).
10. Durchführung der Lasergewebeablation
- Sobald die Sicherheitscheckliste vollständig ist, drücken Sie "START LASER", um mit der Ablation zu beginnen.
- Überwachen Sie den Behandlungsfortschritt in Echtzeit mit Temperaturmesswerten, Timer und Schadenskarte.
HINWEIS: Bewerten Sie die Gewebetemperatur mithilfe des Mehrliniendiagramms links neben dem Prostatamodell. Die Rektaltemperatur ist weiß markiert und sollte 42 °C nicht überschreiten. Die Temperatur an der Spitze des Laserkatheters ist blau markiert (Abbildung 3). Der Laser schaltet sich automatisch ab, wenn die Laserspitze 75 °C oder die Rektalwand 42 °C überschreitet.
HINWEIS: Sobald der Laser aktiv ist, überwachen Sie die Behandlungszeit an jeder Ablationsstelle mit dem roten Balken oben auf dem Bildschirm. Eine Schadenskarte liefert eine 3D-Darstellung des behandelten Gewebes basierend auf Temperatur und Zeit.
HINWEIS: Beachten Sie Änderungen beim Ultraschall im B-Modus. Prostatagewebe verändert sich normalerweise nicht im Aussehen während der Laserablation. Bei seriellen Behandlungen kann das Gewebe ein hypoechoisches Aussehen annehmen, aber die US-Visualisierung dient in erster Linie der Positionierung des Lasers.
HINWEIS: Monitor für besorgniserregende Ultraschallfunktionen wie folgt:- Wirbelnde Mikroblasen, die sich jenseits der echogenen Laserkatheterbänder bilden, können auf ein Leck in der zirkulierenden Kochsalzlösung aufgrund von Überhitzung hinweisen. Während dies keine Auswirkungen auf die Sicherheit hat, kann der Behandlungsfortschritt verlangsamt werden.
- Eine Zunahme der hyperechoischen Natur oder "Aufhellung" des Rektalfetts kann auftreten, wenn der Laserkatheter versehentlich zurückgezogen wird, was zu einer Erwärmung des perirektalen Fettes führt.
- Wenn einer dieser Ultraschallbefunde beobachtet wird, sollte die Laserbehandlung abgebrochen werden.
- Der Laser stoppt automatisch, sobald der Timer abgelaufen ist, aber ein Praktiker kann die Ablation manuell beenden, indem er "STOP THE LASER" drückt. Kochsalzlösung fließt weiter und kühlt die Laserspitze.
HINWEIS: Erwägen Sie, die Ablation frühzeitig zu stoppen, wenn die Temperaturen länger als 60 Sekunden über 55 ° C liegen. - Halten Sie den Laserkatheter und die Wärmesonde an Ort und Stelle, bis die Temperatur des Laserkatheters unter 42 °C gefallen ist, und verhindern Sie so eine rektale Wanderwärmung während des Entzugs des Laserkatheters.
11. Nachfolgende Ablationen
- Positionieren Sie den Ultraschall an der nächsten Ablationsstelle mit den digitalen Zielen, die von der Fusionsvorrichtung bereitgestellt werden.
- Beurteilen Sie, ob die Live-Ultraschallbilder im Prostata-MRT registriert bleiben, und führen Sie bei Bedarf eine Bewegungskompensation durch.
HINWEIS: Wenn Sie die Artemis verwenden, wird die Technik zur Bewegungskompensation im zuvor genannten Video beschrieben. 24 - Auf dem Überwachungsbildschirm der Behandlung wird die anfängliche Ablationsstelle nun ausgegraut; Es kann jedoch erneut behandelt werden, wenn dies für notwendig erachtet wird.
- Wählen Sie die nächste Ablationsstelle auf der linken Seite des Bildschirms aus und wiederholen Sie den in den Schritten 8 - 10 beschriebenen Vorgang.
12. Beenden Sie die Behandlungssitzung
- Sobald alle Ablationsstellen behandelt wurden, erscheint die Schaltfläche "BEHANDLUNG BEENDEN". Durch Drücken dieser Schaltfläche wird ein Behandlungsüberprüfungsbildschirm angezeigt, der quantitative Metriken für die Behandlungssitzung anzeigt.
- Entfernen Sie die TRUS-Sonde aus dem Rektum des Patienten. Manueller Druck kann auf die Rektumwand über der Prostata ausgeübt werden, um die Hämostase zu erleichtern.
Ergebnisse
Die veröffentlichten Ergebnisse von FLA sind in Tabelle 2 dargestellt. Eine Vielzahl von Methoden und Technologien sind enthalten. Mehr als 400 Patienten, die sich verschiedenen Formen von FLA zur Behandlung von PCa unterzogen haben, befinden sich in der SEER-Datenbank. 25 Um die Anzahl und die Merkmale der in der Literatur berichteten FLA zu quantifizieren, führten wir eine systematische Überprüfung von Medline und der Cochrane Library durch. Unsere Suche wurde mit Suchbegriffen für ganze Felder durchgeführt, darunter "fokale Laserablation" und "Prostatakrebs". Insgesamt wurden 247 Titel und Abstracts gesichtet. Nur Fälle, die fokale Laserablation, MRT und onkologische Ergebnisse berichteten, wurden eingeschlossen. 13 Peer-Review-Publikationen, die für die Aufnahme qualifiziert sind, was insgesamt 333 Patienten entspricht (Tabelle 1).
Die Behandlung wurde mit einem 980 nm Diodenlaser in allen außer 2 Studien durchgeführt. 26,27 Behandlungsparameter bestanden aus Leistungsstufen zwischen 6 - 18 Watt und Behandlungszeiten von 1 - 4 Minuten pro Ablationsstelle (Tabelle 1). Die Überwachung der Behandlungstemperatur erfolgte durch MRT-Thermometrie in 9 Studien und durch direkte Temperaturfühlermessungen in 3 Studien (Tabelle 1). Alle Studien wurden in-bore durchgeführt, mit Ausnahme der von Lindner und der späteren Studie von Natarajan. 20,26,27
Der mediane Ausgangs-PSA für die Kohorte betrug 5,7 (Bereich 1,1 - 14,8). Nach FLA betrug der mediane PSA nach 3, 6, 12 und 24 Monaten 3,9, 5,5, 3,8 bzw. 3,9. Das mediane IPSS für die Kohorte betrug 6. Nach FLA betrug das mediane IPSS nach 3, 6, 12 und 24 Monaten 5, 5,5, 7,3 bzw. 11,5. Der mediane Basis-SHIM für die Kohorte betrug 20. Nach FLA betrug der mediane SHIM nach 3, 6, 12 und 24 Monaten 19, 18, 20 bzw. 19 Monate.
In allen Studien wurden Komplikationen inkonsistent berichtet; Es gab jedoch nur eine Komplikation, die von den Autoren als Grad III eingestuft wurde (eine Harnwegsinfektion). 16 Die Autoren haben die Merkmale, die dies als Ereignis der Stufe III eingestuft haben, nicht angegeben. Zwei rektose harnröhrenale Fisteln, die beide nach längerer Katheterisierung spontan schließen,16 wurden als unerwünschte Ereignisse des Grades II berichtet.
Die onkologische Nachbeobachtung wurde nach Follow-up-Zeitraum gruppiert: weniger als 6 Monate, ein Jahr und zwei Jahre (Tabelle 2). Die Follow-up-Biopsie wurde durch MRT-geführte In-Bore-Biopsie in 4 Studien und MRT-US-Fusionsbiopsie in 6 Studien durchgeführt. Zwei Studien verwendeten eine systematische Biopsie und zwei Studien führten "Treat-and-Resect" -Untersuchungen durch, bei denen die Prostatektomieprobe ausgewertet wurde. Der Behandlungserfolg wurde nach einem Delphi-Konsensprotokoll definiert. 28 Der Erfolg vor Ort wurde definiert als das Fehlen ≥ GG2 PCa innerhalb der vorherigen Ablationsstelle. Out-of-Field-Fehler wurde definiert als ≥ GG2 außerhalb des Bereichs der vorherigen Ablation. Bei Patienten mit Follow-up-Biopsieergebnissen betrug der Gesamterfolg vor Ort nach 6 Monaten (N = 83), 1 Jahr (N = 64) und 2 Jahren (N = 39) 83%, 83% bzw. 59% (Tabelle 2).
An der UCLA wurde die FLA der Prostata in drei aufeinanderfolgenden klinischen Studien ab 2014 durchgeführt. 29-31 18 Männer mit Prostatakrebs mit mittlerem Risiko haben sich EINER FLA, acht in der Bohrung und 10 in der Klinik unterzogen, ohne dass nebenwirkungen des Grades III aufgetreten sind. Derzeit durchlaufen weitere 10 Männer FLA mit dem demonstrierten Gerät. 31 Alle Patienten wurden vor fla mit einer 3T-MRT (Körperspule) und einer MRT-US-Fusionsbiopsie mit Probenahme aus dem ROI und systematischer Biopsie innerhalb von 6 Monaten nach der Behandlung untersucht. Sowohl Ausgangs- als auch Follow-up-Biopsien wurden unter MRT/US-Fusionsführung unter Verwendung des Artemis-Fusionssystems mit Verfolgung aller Biopsiestellen durchgeführt.
Tabelle 1. Berichtete Studien zur fokalen Laserablation.
| Aktenzeichen | Verfasser | Jahr | n | Medianalter (Bereich) | Laserleistung | Rx-Zeit (Sek.) | Geplante Marge | In-Bore-Verfahren | Temperaturüberwachung | Baseline Gleason | ||||
| 3+3 | 3+4 | 4+3 | 4+4 | |||||||||||
| 26 | Lindner | 2009 | 12 | 56.5 (51-52) | - | 120 | - | Nein | Temperaturfühler | 12 | 0 | 0 | 0 | |
| 27 | Lindner | 2010 | 4 | 66 (61-73) | - | 120 | - | Nein | Temperaturfühler | 2 | 0 | 1 | 1 | |
| 5 | Oto | 2013 | 9 | 61 (52-77) | 6 - 15 W | - | - | ja | MRT-Thermometrie | 8 | 1 | 0 | 0 | |
| 12 | Lee | 2014 | 23 | - | 8 W | 30-60 | - | ja | MRT-Thermometrie | - | - | - | - | |
| 6 | Lepor | 2015 | 25 | 66 (49-84) | - | - | - | ja | MRT-Thermometrie | 11 | 13 | 1 | 0 | |
| 18 | Al Barqawi | 2015 | 7 | 61 (56-69) | - | 90 | - | ja | MRT-Thermometrie | 7 | 0 | 0 | 0 | |
| 15 | Bomere | 2016 | 5 | 66 (58-70) | - | - | 9 mm | ja | MRT-Thermometrie | 2 | 2 | 1 | 0 | |
| 14 | Eggener | 2016 | 27 | 62 (-) | 6 - 15 W | 60-120 | 0 -7,5 mm | ja | MRT-Thermometrie | 23 | 3 | 1 | 0 | |
| 19 | Natarajan | 2016 | 8 | 63 (54-72) | 11 - 14 W | 180 | Benutzerdefiniert* | ja | Temperaturfühler # | 1 | 7 | 0 | 0 | |
| 20 | Natarajan | 2017 | 10 | 65 (52-74) | 13,75 W | 180 | Benutzerdefiniert* | Nein | Temperaturfühler | 2 | 8 | 0 | 0 | |
| 35 | Chao | 2018 | 34 | 69 (52-88) | - | - | - | ja | MRT-Thermometrie | 16 | 16 | 2 | 0 | |
| 17 | Al Hakeem | 2019 | 49 | 63 (51-73) | 10 - 15 W | 120 | 9 mm | ja | MRT-Thermometrie | 13 | 29 | 7 | 0 | |
| 16 | Walser | 2019 | 120 | 60 (45-86) | 17 - 18 W | 180-240 | 5 mm | ja | MRT-Thermometrie | 37 | 56 | 27 | 0 | |
Tabelle 1: Bindestrich (-) zeigt Informationen an, die im veröffentlichten Manuskript nicht verfügbar sind. * gibt an, dass jede Marge individuell geplant wurde. # zeigt an, dass die Überwachung sowohl mit einem Temperaturfühler als auch mit einer MRT-Thermometrie durchgeführt wurde.
Tabelle 2. Ergebnisse der fokalen Laserablation.
| Aktenzeichen | Erstautor | Follow-up-Biopsie-Methode | Follow-up-Biopsie | ≤ 6 Monate | 12 Monate | 24 Monate | Nebenwirkungen | ||||||
| Erfolg | Versagen | Erfolg | Versagen | Erfolg | Versagen | Ich | Ii | Iii | |||||
| 26 | Lindner | MRT-geführtes Bx | 12 | 12 | 0 | - | - | - | - | 2 | 0 | 0 | |
| 27 | Lindner | Prostatektomie | 4 | 2 | 2 | - | - | - | - | - | - | - | |
| 5 | Oto | MRT/US Bx | 9 | 9 | 0 | - | - | - | - | 1 | 1 | 0 | |
| 12 | Lee | MRT/US Bx | 13 | - | - | 12 | 1 | - | - | - | - | - | |
| 6 | Lepor | MRT-geführtes Bx | 21 | 20 | 1 | - | - | - | - | 0 | 0 | 0 | |
| 18 | Al Barqawi | Systematische Bx | 5 | - | - | 5 | 00 | - | - | - | 1 | 0 | |
| 15 | Bomere | Prostatektomie | 5 | 1 | 4 | - | - | - | - | - | - | - | |
| 14 | Eggener | MRT-geführtes Bx # | 27 | 27 | - | 7 | 31 | - | - | 7 | 2 | 0 | |
| 19 | Natarajan | MRT/US Bx | 8 | 6 | 53 | - | - | - | - | 23 | 7 | 0 | |
| 20 | Natarajan | MRT/US Bx | 10 | 6 | 40 | - | - | - | - | 38 | 6 | 0 | |
| 35 | Chao | MRT/US Bx | 22 | - | - | - | - | 13 | 9 | - | - | - | |
| 17 | Al Hakeem | MRT/US Bx | 49 | - | - | 40 | 91 | - | - | 34 | 11 | 0 | |
| 16 | Walser | MRT-geführtes Bx | 44* | - | - | - | - | 26 | 18 | 8 | 8 | 1 | |
Fußnoten Tabelle 2. Erfolg = Fehlen von ≥ GG2-Prostatakrebs innerhalb der Ablationszone. Versagen = Vorhandensein von ≥ GG2-Prostatakrebs: gesamt und außerhalb des Feldes (tiefgestellte Zahl). # gibt an, dass die MRT-geführte Biopsie für eine 6-monatige Biopsie verwendet wurde, aber nur eine systematische Biopsie für eine 12-monatige Biopsie. * gibt an, dass nur Patienten mit einer PSA-Reduktion von < 50% und einer positiven MRT nach der Ablation einer Biopsie unterzogen wurden; 76 Patienten wurden keiner Biopsie unterzogen.
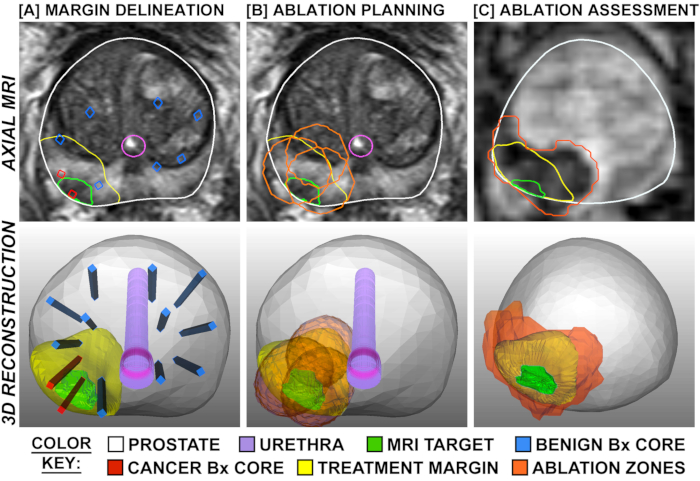
Abbildung 1: Behandlungsplanung und -beurteilung, dargestellt über Overlays auf Quer-MRT (obere Reihe) und in 3D (untere Zeile). Spalte A zeigt die Abgrenzung der Behandlungsmargen, die um das krebspositive MRT-Ziel erweitert und durch nahe gelegene negative systematische Biopsiekerne begrenzt werden (blau). Spalte B zeigt die Planung der Ablationsorte, so dass sich die Behandlungsränder überlappen, um ein "Überspringen" von Bereichen zu verhindern. Spalte C zeigt perfusionsgewichtete Bildgebung, die 2 Stunden nach der Behandlung gesammelt wurde, und zeigt die Übereinstimmung zwischen dem geplanten und dem beobachteten Ablationsausmaß. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
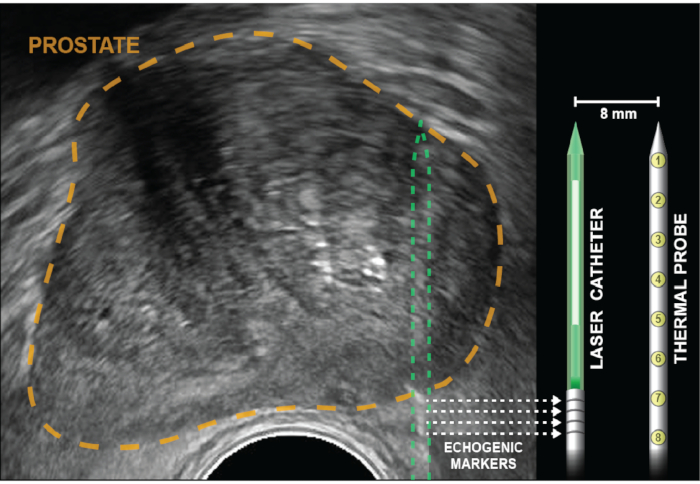
Abbildung 2: Axialer Ultraschall mit gold umrandekter Prostata. Eckwürfelreflektoren (echogene Bänder), gekennzeichnet durch gepunktete Pfeile, werden 5 mm vom Diffusor entfernt in den Laserkatheter geätzt (weiß). Der Temperaturfühler wird in die gleiche Tiefe wie die Laserfaser eingeführt, dann an Ort und Stelle arretiert und bleibt parallel zum Laser im Abstand von 8 mm, außerhalb der US-Sichtebene. Acht Thermosensoren, die sich innerhalb der Sonde in einem Abstand von 4 mm befinden, liefern Temperaturaufzeichnungen an Punkten von der Basis der echogenen Bänder bis zur Spitze des Laserkatheters. Temperaturmessungen, die der Rektalwand am nächsten sind, werden durch thermische Messungen an der Basis des Temperaturfühlers (Positionen 6-8) durchgeführt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 3: Temperaturaufzeichnungen während der fokalen Laserablation für zwei aufeinanderfolgende Ablationen. Y-Achse = Temperatur in Celsius. X-Achse = Zeit in Minuten. Vertikal schattierte Balken = Zeiträume der Laseraktivierung. Blaue Linie = Temperatur 8mm von der Spitze der Laserfaser (distales Thermoelement). Weiße Linie = Temperatur 8 mm vom proximalen Thermoelement, das der Rektalwand am nächsten liegt. Eine Temperatur von 60 Grad Celsius, die auch nur kurz erreicht wird, sorgt für eine Gerinnungsnekrose. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
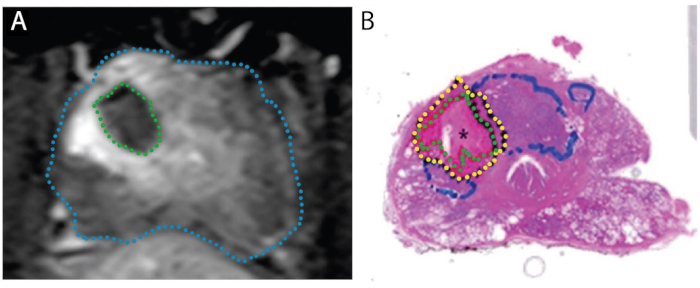
Abbildung 4: Bilder, die die Übereinstimmung der Ablationszone in der MRT nach der Behandlung (A) mit der tatsächlichen nekrotischen Zone an der ganz montierten Probe (B) zeigen. Der Patient ist ein 67-jähriger Mann mit PCa in der rechten Übergangszone, Gleason-Score 3 + 4 = 7, der an einer "Treat and Resect" -Studie teilnimmt. A. Axiales T1-gewichtetes kontrastverstärktes Bild nach der Ablation, das einen durch Laserbehandlung verursachten Perfusionsfehler zeigt (grün). B. Ganzer H & E-Fleck der Prostata. Das nekrotische Gewebe ist grün abgegrenbt, das perinekrotische Gewebe gelb und der intakte Tumor (unbehandelt) blau. Reproduziert unter einer Creative Commons Lizenz von Bomers et al, World Journal of Urology. 15 Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
Ziel der vorliegenden Arbeit ist es, eine Methode zur Durchführung der fokalen Laserablation (FLA) von Prostatakrebs (PCa) zu beschreiben und zu veranschaulichen. Die Methode unterscheidet sich von anderen fokalen Therapiemethoden, da sie unter örtlicher Betäubung in einer Klinik durchgeführt werden soll. Die hier gezeigte FLA-Methode wurde 2017,20 eingeführt und seitdem kontinuierlich weiterentwickelt. Daher kann das in diesem Papier beschriebene Verfahren für zukünftige Ermittler von Wert sein.
Die Laserbehandlung von Prostatagewebe scheint aus der Forschung von McNicholas und Kollegen am University College London zu stammen, die 1993 zeigten, dass fokale Gerinnungsnekrose in Hundestaten mit einem Nd: YAG-Gerät erzeugt werden kann. 32 Diese Autoren, die die Zukunft vorahnten, postulierten, dass die Technik "... kann sich als wertvoll erweisen... zur Zerstörung kleiner fokaler Prostatatumoren." Anschließend wurde die Laserablation von PCa beim Menschen im Jahr 2009 von Lindner et al. von der University of Toronto beschrieben. 26 In dieser Pionierarbeit kombinierte Lindner die aufkommende Modalität der Prostata-MRT mit früher Bildfusionssoftware und herkömmlichen Wärmesonden, um Krebs erfolgreich zu bekämpfen und die Laserablation bei 12 Männern zu überwachen.
Da die wichtigsten PCa mit der modernen multiparametrischen MRT visualisiert werden können, könnte das In-Bore-Targeting und die Behandlung sichtbarer Läsionen eine einfache Erweiterung des diagnostischen Verfahrens sein. Das In-Bore-Targeting der Läsion ist direkt, und die MR-Thermometrie ermöglicht die Fernüberwachung der Ablation. Raz et al berichteten 2010 über zwei solcher Behandlungen. 33 Eine Reihe von In-Bore-FLA-Behandlungen (N = 9) wurde von Oto und Kollegen im Jahr 2013 berichtet. 5 Die Einführung von In-Bore-FLA wurde durch Hardware erleichtert, die für diesen Zweck entwickelt wurde, wie Natarajan et al. im Jahr 2016 berichteten. 19 Eine Reihe von Radiologen, die eine wassergekühlte Laserfaser verwenden, um Verkohlung zu verhindern, haben die In-Bore-Methode übernommen; und Hunderte von In-Bore-FLA-Behandlungen wurden jetzt berichtet (Walser, Feller, Sperling/ Lepor). 6,16,34,35
Während kurzfristige onkologische Ergebnisse von In-Bore-FLA günstig sein können (Tabelle 1), wird das Verfahren aufgrund der in der Einleitung beschriebenen einschränkenden Faktoren wahrscheinlich nicht weit verbreitet sein. Darüber hinaus weist die MR-Thermometrie zur Behandlungsüberwachung eine Reihe wichtiger Einschränkungen auf. 19 Aufbauend auf einer jahrzehntelangen Erfahrung mit MRT/US-Fusionsbiopsieverfahren (N ~ 4000) haben wir die Theoretisiert, dass eine Laserfaser in eine Krebsläsion gezielt werden könnte, ähnlich wie das Einsetzen einer Biopsienadel, und dass die Überwachung der Behandlung direkt mit Thermischen Sonden durchgeführt werden könnte. So unterzogen sich zehn Patienten nach der In-Bore-Erfahrung einer out-of-bore FLA in der UCLA-Urologieklinik, wobei nur Lokalanästhesie, MRT / US-Fusionsführung und thermische Sondenüberwachung verwendet wurden. 20 Es wurde nicht nur die Sicherheit und Durchführbarkeit der neuen Methode nachgewiesen, sondern bei den letztgenannten behandelten Patienten konnte bei der anschließenden Biopsie kein Nachweis von PCa gefunden werden.
Die Gewebewirkung von FLA wurde in zwei Studien geklärt, in denen die geplante radikale Prostatektomie 1-3 Wochen nach dem Lasereingriff (N=9), d.h. ein "Treat-and-Resect"-Modell durchgeführt wurde (Abbildung 4). 15,27 Bei allen 9 Patienten näherte sich das Volumen des nekrotischen Gewebes in der Prostata dem Volumen an, das durch das MRT nach Abschluss der Behandlung geschätzt wurde. Wenn die gesamte Prostata durchschnitten wurde, wurde ein abrupter Übergang zwischen Nekrose und intakten Zellen 1-5 mm außerhalb des Bereichs der Laserablation beobachtet (Abbildung 1). Die klaren Ränder und die Präzision der Ablationszonen haben wichtige Auswirkungen auf die Genauigkeit der MRT/US-Registrierung und Behandlungsplanung.
Ein wesentlicher Bestandteil des Avenda-Systems ist die Behandlungsplanungssoftware. Für eine effektive FLA muss die Planung nicht nur den Ort der Läsion, sondern auch das Gewebevolumen umfassen, das für die vollständige Tumorzerstörung erforderlich ist. Das Ablationsvolumen kann nicht einfach das MRT-Läsionsvolumen sein, denn das tatsächliche Tumorvolumen übersteigt das der MRT-sichtbaren Läsion um durchschnittlich das 3-fache. 21 Darüber hinaus erstreckt sich Krebs häufig in unregelmäßigen fingerartigen Projektionen, was jeden einheitlichen Sicherheitsabstand, der ausschließlich auf der Bildgebung beruht (z. B. 1 cm über die Grenze der MRT-sichtbaren Läsion hinaus), unzuverlässig machen würde. Das Avenda-System umfasst eine Behandlungsplanungssoftware, die nicht nur die MRT-sichtbare Läsion, sondern auch die 3D-Verfolgung von Biopsiestellen (positiv und negativ) nutzt, um eine genaue Platzierung des minimalen Ablationsvolumens zu ermöglichen, das den Krebs vollständig umfasst. Ein Beispiel für eine solche Behandlungsplanung ist in Abbildung 3 zu sehen.
Zusammenfassend ist FLA eine sichere, praktikable Methode zur Ausrottung von Prostatakrebs in einer Klinik unter örtlicher Betäubung. Die Schritte des Verfahrens werden im begleitenden Video gezeigt. Die genaue Platzierung der Laserfaser in einer MRT-sichtbaren Läsion wird mit MRT / US-Fusion erreicht, ähnlich wie Biopsienadeln in solche Läsionen eingesetzt werden. Die Echtzeit-Behandlungsüberwachung erfolgt über eine wärmebildende Sonde neben der Laserfaser. Eine Behandlungsplanungssoftware, die Läsionsvolumina aus der MRT und verfolgte Biopsiestellen verwendet, um dem Bediener bei der Bestimmung der Behandlungsmargen zu helfen, ist ein wichtiger Teil des Systems. Die in diesem Artikel beschriebene und illustrierte flanierte in der Klinik scheint eine attraktive fokale Therapieoption zu bieten, die bisher nicht verfügbar war.
Offenlegungen
Dr. Marks und Dr. Natarajan sind Mitbegründer von Avenda Health.
Materialien
| Name | Company | Catalog Number | Comments |
| Fusion Guidance System | NA | Artemis Displayed in Video | |
| Laser Catheter | Avenda Health | ||
| Orion Workstation | Avenda Health | ||
| Thermal Probe | Avenda Health | ||
| Transrectal Probe | NA | Not Platform Dependent | |
| Ultrasound | NA | Not Platform Dependent |
Referenzen
- Cooperberg, M. R., Carroll, P. R. Trends in management for patients with localized prostate cancer, 1990-2013. JAMA - Journal of the American Medical Association. 314 (1), 80-82 (2015).
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics, 2020. CA: A Cancer Journal for Clinicians. 70 (1), 7-30 (2020).
- Connor, M. J., Gorin, M. A., Ahmed, H. U., Nigam, R. Focal therapy for localized prostate cancer in the era of routine multi-parametric MRI. Prostate Cancer and Prostatic Diseases. , 1-12 (2020).
- Ahmed, H. U., et al. Focal Therapy for Localized Prostate Cancer: A Phase I/II Trial. The Journal of Urology. 185, 1246-1255 (2011).
- Oto, A., et al. MR imaging-guided focal laser ablation for prostate cancer: Phase I trial. Radiology. 267 (3), 932-940 (2013).
- Lepor, H., Llukani, E., Sperling, D., Fütterer, J. J. Complications, Recovery, and Early Functional Outcomes and Oncologic Control Following In-bore Focal Laser Ablation of Prostate Cancer. European Urology. 68 (6), 924-926 (2015).
- Johnson, D. C., et al. Detection of Individual Prostate Cancer Foci via Multiparametric Magnetic Resonance Imaging. European Urology. 75 (5), 712-720 (2019).
- Johnson, D. C., et al. Do contemporary imaging and biopsy techniques reliably identify unilateral prostate cancer? Implications for hemiablation patient selection. Cancer. 125 (17), 2955-2964 (2019).
- Liu, W., et al. Copy number analysis indicates monoclonal origin of lethal metastatic prostate cancer. Nature Medicine. 15 (5), 559-565 (2009).
- Ahmed, H. U. The Index Lesion and the Origin of Prostate Cancer. New England Journal of Medicine. 361 (17), 1704-1706 (2009).
- Stafford, R. J., et al. Magnetic resonance guided, focal laser induced interstitial thermal therapy in a canine prostate model. Journal of Urology. 184 (4), 1514-1520 (2010).
- Lee, T., Mendhiratta, N., Sperling, D., Lepor, H. Focal laser ablation for localized prostate cancer: principles, clinical trials, and our initial experience. Reviews in urology. 16 (2), 55-66 (2014).
- Johnson, D. E., Cromeens, D. M., Price, R. E. Interstitial laser prostatectomy. Lasers in Surgery and Medicine. 14 (4), 299-305 (1994).
- Eggener, S. E., Yousuf, A., Watson, S., Wang, S., Oto, A. Phase II Evaluation of Magnetic Resonance Imaging Guided Focal Laser Ablation of Prostate Cancer. Journal of Urology. 196 (6), 1670-1675 (2016).
- Bomers, J. G. R. R., et al. MRI-guided focal laser ablation for prostate cancer followed by radical prostatectomy: correlation of treatment effects with imaging. World Journal of Urology. 35 (5), 703-711 (2017).
- Walser, E., et al. Focal Laser Ablation of Prostate Cancer: Results in 120 Patients with Low- to Intermediate-Risk Disease. Journal of Vascular and Interventional Radiology. 30 (3), 401-409 (2019).
- Al-Hakeem, Y., Raz, O., Gacs, Z., Maclean, F., Varol, C. Magnetic resonance image-guided focal laser ablation in clinically localized prostate cancer: safety and efficacy. ANZ Journal of Surgery. 89 (12), 1610-1614 (2019).
- Barqawi, A., Krughoff, K., Li, H., Patel, N. U. Initial Experience of Targeted Focal Interstitial Laser Ablation of Prostate Cancer with MRI Guidance. Current Urology. 8 (4), 199-207 (2014).
- Natarajan, S., et al. Focal Laser Ablation of Prostate Cancer: Phase I Clinical Trial. Journal of Urology. 196 (1), 68-75 (2016).
- Natarajan, S., et al. Focal Laser Ablation of Prostate Cancer: Feasibility of Magnetic Resonance Imaging-Ultrasound Fusion for Guidance. Journal of Urology. 198 (4), 839-847 (2017).
- Priester, A., et al. Magnetic Resonance Imaging Underestimation of Prostate Cancer Geometry: Use of Patient Specific Molds to Correlate Images with Whole Mount Pathology. Journal of Urology. 197 (2), 320-326 (2017).
- Lightner, D. J., Wymer, K., Sanchez, J., Kavoussi, L. Best Practice Statement on Urologic Procedures and Antimicrobial Prophylaxis. Journal of Urology. 203 (2), 351-356 (2020).
- Jones, T. A., Radtke, J. P., Hadaschik, B., Marks, L. S. Optimizing safety and accuracy of prostate biopsy. Current Opinion in Urology. 26 (5), 472-480 (2016).
- Jayadevan, R., Zhou, S., Priester, A. M., Delfin, M., Marks, L. S. Use of MRI-ultrasound fusion to achieve targeted prostate biopsy. Journal of Visualized Experiments. (146), e59231 (2019).
- Zheng, X., et al. Focal Laser Ablation Versus Radical Prostatectomy for Localized Prostate Cancer: Survival Outcomes From a Matched Cohort. Clinical Genitourinary Cancer. 17 (6), 464-469 (2019).
- Lindner, U., et al. Image Guided Photothermal Focal Therapy for Localized Prostate Cancer: Phase I Trial. Journal of Urology. 182, 1371-1377 (2009).
- Lindner, U., et al. Focal Laser Ablation for Prostate Cancer Followed by Radical Prostatectomy: Validation of Focal Therapy and Imaging Accuracy. European Urology. 57 (6), 1111-1114 (2010).
- van Luijtelaar, A., et al. Focal laser ablation as clinical treatment of prostate cancer: report from a Delphi consensus project. World Journal of Urology. 37, 2147-2153 (2019).
- . Use of Laser Interstitial Thermal Therapy in the Focal Treatment of Localized Prostate Cancer - NCT02224911 Available from: https://clinicaltrials.gov/ct2/show/NCT02224911 (2020)
- . Focal Laser Ablation of Prostate Tissue - NCT02357121 Available from: https://clinicaltrials.gov/ct2/show/NCT02357121 (2020)
- . Focal Laser Ablation of Prostate Cancer -NCT04305925 Available from: https://clinicaltrials.gov/ct2/show/NCT04305925 (2020)
- McNICHOLAS, T. A., STEGER, A. C., BOWN, S. G. Interstitial Laser Coagulation of the Prostate An Experimental Study. British Journal of Urology. 71 (4), 439-444 (1993).
- Raz, O., et al. Real-Time Magnetic Resonance Imaging-Guided Focal Laser Therapy in Patients with Low-Risk Prostate Cancer. European Urology. 58 (1), 173-177 (2010).
- . Transrectally delivered, outpatient MRI-guided laser focal therapy of prostate cancer: 9.5 year interim results of NCT #02243033, Presentation at the AdMeTech 4th Global Summit on Precision Diagnosis and Treatment of Prostate Cancer Available from: https://www.admetech.org/wp-content/uploads/2019/08/DMI-FOCAL-Tx-2019-NCT-02243033.FINAL_.pdf (2020)
- Chao, B., Llukani, E., Lepor, H. Two-year Outcomes Following Focal Laser Ablation of Localized Prostate Cancer. European Urology Oncology. 1 (2), 129-133 (2018).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten