È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Una guida pratica per la produzione e la formazione immagine di PET/CT di 68Ga-DOTATATE per tumori neuroendocrini nella pratica clinica quotidiana
In questo articolo
Riepilogo
Tumori neuroendocrini ben differenziati dei overexpress recettori per la somatostatina che possono essere utilizzati per la diagnostica per immagini con l' analogico radioattivi del somatostatina 68Ga-DOTATATE. Questo protocollo dettaglia la radiomarcatura di 68Ga-DOTATATE, controllo di qualità, preparazione del paziente e la formazione immagine successiva PET/CT. Sicurezza dalle radiazioni e costrizioni di tempo a causa della breve emivita di 68Ga sono presi in considerazione.
Abstract
I tumori neuroendocrini sono una rara forma di cancro che derivano da cellule neuroendocrine e possono essere presenti in quasi qualsiasi posizione in tutto il corpo. Anche se eterogenei nella presentazione, un denominatore comune tra questi tumori è la sovraespressione dei recettori della somatostatina. 68 GA-DOTATATE è un analogo del somatostatina etichettato con il positrone emettitore Gallio-68 (68Ga). Per i tumori neuroendocrini ben differenziati, 68Ga-DOTATATE tomografia a emissione di positroni (PET) / formazione immagine di tomografia computata (CT) è usata per la diagnosi, la determinazione del carico di malattia e la selezione di terapia.
Questo protocollo dettaglia la radiomarcatura di 68Ga-DOTATATE, controllo di qualità, preparazione del paziente e la formazione immagine successiva PET/CT. Radiomarcatura di 68Ga-DOTATATE viene eseguita con un modulo d'etichettatura completamente automatizzato, accoppiato ad un germanio-68 (68Ge) / generatore di68Ga. Controllo di qualità del prodotto finale valuta la purezza radiochimica con immediata cromatografia di strato sottile, cromatografia su fase solida e pH prima dell'iniezione paziente. Controllo periodico di qualità viene eseguito per determinare la svolta Ge 68, sterilità e (4-(2-hydroxyethyl)-1-piperazineethanesulfonic acido (HEPES) contenuto. Preparazione del paziente comprende istruzioni per il paziente, un protocollo per 68Ga-DOTATATE durante il trattamento con analoghi della somatostatina e somministrazione endovenosa del radiofarmaco. Per PET/CT sono descritte le impostazioni di imaging, l'acquisizione e la ricostruzione. Per ogni passaggio, sicurezza dalle radiazioni sarà evidenziata, come pure di costrizioni di tempo a causa della breve emivita di 68GA.
Completamente automatizzato di produzione interno e controllo di qualità di 68Ga-DOTATATE porta a tassi di successo molto alto (95%) e produce due di quattro dosaggi pazienti per ogni batch, a seconda del rendimento del generatore. In conclusione, la formazione immagine 68Ga-DOTATATE PET/CT è un metodo veloce e non invasivo che fornisce informazioni sull'onere del tumore dei tumori neuroendocrini (NETs) mentre l'assistenza anche nella selezione di diagnosi e terapia.
Introduzione
Le reti sono un gruppo eterogeneo di tumori che risulta dalle cellule neuroendocrine. Essi possono verificarsi in qualsiasi posizione nel corpo ma sono più comuni nel tratto gastrointestinale, pancreas e polmone1. Anche se le reti sono una malattia rara, la loro incidenza negli Stati Uniti è salito dal 1.09 per 100.000 abitanti nel 1973 a 6,98 per 100.000 abitanti nel 20122. Per una diagnosi esatta e la messa in scena di un NET, 68Ga-DOTATATE PET/CT è lo standard di cura. Questo protocollo descrive la produzione e controllo di qualità di 68Ga-DOTATATE, come pure la preparazione del paziente e l'acquisizione di immagini PET/CT.
Reti ben differenziate sono caratterizzate da una sovraespressione di recettori della somatostatina1. Gli analoghi della somatostatina che si legano a questo recettore possono essere etichettati con un isotopo radioattivo per consentire per l'imaging di medicina nucleare. In un primo momento, iodio-123 è stato utilizzato con macchina fotografica gamma imaging, che fu presto sostituito da indio-111 (111In)3,4. 111 Lo scintigraphy di octreotide è stato lo standard d'oro per l'imaging di medicina nucleare NET per oltre un decennio5. Nel frattempo, i progressi tecnici sono state fatte in PET, che ha una maggiore sensibilità e risoluzione rispetto all'imaging gamma fotocamera. Per reti, accoppiati per il positrone emettitore 68Ga, quali 68Ga-DOTATATE, gli analoghi della somatostatina sono stati sviluppati6.
68 Recettore della somatostatina GA (68Ga-SRS) PET/CT è la modalità corrente della scelta nell'imaging di medicina nucleare di reti bene-differenziate. La superiorità di 68Ga-SRS PET/CT oltre 111In-octreotide è stata dimostrata in diversi studi7,8. La segnalata sensibilità e specificità si trovano intorno 90% - 95% e 85% - 100%, rispettivamente9,10. Una meta-analisi ha mostrato che 68Ga-SRS PET/CT conduce ad un cambiamento nella gestione nel 44% dei casi, anche se preceduto da 111In-octreotide scintigraphy11. Nelle linee guida, 68Ga-SRS PET/CT è ora raccomandato sopra lo scintigraphy 111In-octreotide per NET imaging, e si è anche approvato dalla Food and Drug Administration e Agenzia europea dei medicinali12. Una guida di riferimento per l'imaging del tumore con 68Ga-coniugati peptidi è anche disponibili13.
Questo protocollo dettaglia la radiomarcatura di 68Ga-DOTATATE (conformi i requisiti di controllo di qualità della farmacopea europea14), preparazione del paziente e la formazione immagine successiva PET/CT. Sicurezza dalle radiazioni e costrizioni di tempo a causa della breve emivita di 68Ga sono presi in considerazione.
Access restricted. Please log in or start a trial to view this content.
Protocollo
1. generale radiazioni e sicurezza radiofarmaceutica
- Assicurarsi che i materiali radioattivi sono solo lavorati con e gestiti da personale addestrato. La dose per personale ospedaliero, i pazienti e tutti altro presente deve essere sempre più bassa ragionevolmente ottenibile (ALARA).
- Per quanto riguarda la preparazione di radiofarmaci, rispettare le leggi nazionali, regolamenti e linee guida, come buona pratica di fabbricazione (GMP).
Attenzione: Il seguente protocollo è per l'imaging di Ga-DOTATATE PET/CT 68di soli adulti e non è adatto per bambini o donne incinte.
2. preparativi necessari prima dell'etichettatura di 68Ga-DOTATATE
- Eluire il 68Ge / generatore di68Ga con acido cloridrico (HCl) secondo le specifiche del produttore, tra 4 e 24 h prima dell'inizio del 68Ga-DOTATATE di etichettatura.
3. etichettatura di 68Ga-DOTATATE
Nota: La preparazione e l'etichettatura di 68Ga-DOTATATE dura 90 min e dovrebbe essere iniziato 2 h prima dell'amministrazione paziente, per consentire il controllo di qualità. Il modulo etichettatura dovrebbe essere messo in una schermatura di piombo che può essere chiuso durante il processo di etichettatura per garantire la protezione dalle radiazioni del personale. Se viene utilizzato un kit registrato, il riassunto delle caratteristiche del prodotto (RCP) deve essere seguito o croce-convalidato localmente con il protocollo presentato.
- Posizionare il 68kit etichettatura Ga sul modulo etichettatura secondo le specifiche del produttore. Posizionare i tre collettori sulle unità modulo corrispondente. Allegare le soluzioni fornite nel 68il kit etichettatura Ga per i collettori.
- Preparare la fiala finale in un ambiente sterile, ad esempio un'unità downflow o a flusso laminare.
- Inserire un filtro da 0,22 µm nonvented sotto un filtro da 0,22 µm con spacchetti e collegare il filtro nonvented per un ago sterile (20 G). Inserire l'ago con due filtri collegati in una provettina sterile di 30 mL. Inserire un filtro di piegato 0,2 µm ventilato con un ago (22 G) nella stessa fiala sterile secondo passo 3.2 per consentire la ventilazione.
- Collegare il flaconcino sterile con il filtro nonvented all'output del modulo etichettatura e posizionare la cuvetta nel piombo schermatura sufficiente per emettitori di positroni.
- Collegare l'uscita del 68Ga / generatore Ge68all'ingresso del modulo etichettatura.
- Sciogliere 50 µ g di HA-DOTATATE (DOTA-3-iodo-Tyr3-octreotate) o 20 µ g di peptide DOTATATE (DOTA-0-Tyr3-octreotate) in 1,5 mL di soluzione di tampone HEPES 1,5 M fornito nel kit e posizionarlo nel flaconcino di reazione.
- Nelle vicinanze la schermatura di piombo intorno l'etichettatura modulo e inizio la produzione di 68Ga-DOTATATE tramite il tablet computer collegato al modulo d'etichettatura.
- Attendere che la sintesi di 68Ga-DOTATATE è finito (~ 36 min).
- Dopo l'etichettatura, rimuovere gli aghi con filtri dal flaconcino di vetro e chiudere la schermatura di piombo intorno il flaconcino.
- Verificare l'integrità del filtro da 0,22 µm nonvented come segue.
- Riempire una siringa (10 mL) con aria e posizionare la siringa sulla parte superiore del filtro. Posto l'ago collegato al filtro in un tubo riempito d'acqua.
- Forzare l'aria attraverso il filtro e l'ago e determinare quando le bolle cominciano a formarsi. L'aria deve essere compresso a < 20% del volume originale.
- Misura l'attività di 68Ga-DOTATATE prodotto ponendo il flacone in un calibratore di dose e prendere nota del tempo di riferimento di attività (arte).
- In un ambiente sterile come un'unità a flusso laminare, 0,5 mL di 68Ga-DOTATATE di rimuovere dal flaconcino per il controllo qualità e preparare le siringhe per la gestione dei pazienti.
Nota: Inserire la soluzione con 68Ga-DOTATATE nella schermatura di piombo. In questo protocollo, la soluzione diluita non deve essere schermato dovuto i bassi livelli di attività e breve tempo di esposizione. Tuttavia, una valutazione del rischio di radiazione dovrebbe essere eseguita prima di eseguire il controllo di qualità di 68Ga-DOTATATE.
4. controllo di qualità di 68Ga-DOTATATE prima della gestione dei pazienti
Nota: Il controllo di qualità di 68Ga-DOTATATE impiegano 30 minuti e deve essere iniziato 30 min prima della gestione dei pazienti. Le diluizioni descritte per soluzioni di riserva portano a < 5% tempi morti nell'apparecchiatura di misurazione. Questo può variare tra le diverse apparecchiature e dovrebbe essere testato prima di eseguire il controllo di qualità di 68Ga-DOTATATE. Farmacopea europea descrive il controllo di qualità delle iniezioni edotreotide gallio sulla base dei seguenti criteri di rilascio: aspetto = trasparente e incolore; pH = 4.0-8.0; sterilità; le endotossine < 175 UI per ciascun volume somministrato; etanolo < 10% v/v; purezza del radionuclide > 99.9% dell'attività totale; la purezza radiochimica > 91% dell'attività totale; assenza di altre impurità; HEPES < 200 µ g / amministrato volume14. Tutti i test sono stati valutati durante la convalida del metodo di preparazione. Per controllo di qualità di routine, un sottoinsieme selezionato di test (basato sul monitoraggio di tendenza) è eseguito e descritto di seguito. L'estrazione in fase solida in questo protocollo è stato convalidato a croce con ed ottiene gli stessi risultati come il metodo di cromatografia liquida ad alte prestazioni descritto nella farmacopea europea. Questa è stata eseguita in base GMP.
- Preparare le seguenti soluzioni in anticipo.
- Preparare una soluzione di acetato di ammonio 1 M sciogliendo 3,9 g di acetato di ammonio in 50 mL di acqua. La soluzione può essere conservata a temperatura ambiente fino a 2 settimane.
- Preparare l'acido etilendiamminotetracetico 5mm (EDTA) da sciogliere 0,1 g di EDTA in 50 mL di acqua. La soluzione può essere conservata a temperatura ambiente per fino a 1 anno.
- Preparare l'acetato di ammonio metanolo: 1 M 50: 50. La soluzione può essere conservata a temperatura ambiente per fino a 24 h.
- Ispezionare visivamente il prodotto finale 68Ga-DOTATATE per garantire che è un liquido incolore, senza particelle.
- Misurare il pH del 68soluzione Ga-DOTATATE con una striscia di indicatore di pH. Il pH deve trovarsi fra 6.5 e 7.5.
- Misurare colloidi Ga 68attraverso cromatografia di strato sottile istantanea (ITLC).
- Aggiungere 500 µ l di acqua e 20 µ l di 68Ga-DOTATATE di preparare una soluzione di riserva e omogeneizzare (68colloidi di Ga [GC]) agitando con cura il flaconcino.
- Tagliate una striscia di carta fibra ITLC - gel di silice (SG) vetro di almeno 7 cm di lunghezza e 1 cm di larghezza.
Nota: Utilizzare solo carta ITLC-SG pulita senza danni. Se la carta è danneggiata, i componenti in viaggio con il solvente possono essere ostacolati e i risultati saranno imprecisi. - Aggiungere 5 µ l di GC 1,5 cm dalla parte inferiore della carta ITLC-SG e metterlo in una provetta contenente 2 mL di acetato di ammonio di 50: 50 metanolo: 1 M. Assicurarsi che il 68Ga-DOTATATE non entrino in contatto con il liquido. Chiudere le provette per evitare l'evaporazione.
- Attendere alcuni minuti fino a quando il solvente ha viaggiato almeno 5 cm sopra cui è stato applicato il 68Ga-DOTATATE. Tagliare la carta a metà e posto sul fondo e metà superiore in provette separate (BH1 e UH1).
- Posizionare il UH1 e BH1 tubi in un pozzo del contatore e determinano il numero di conteggi in ogni flaconcino nella finestra di 400 – 600 keV energia per 30 s, per determinare la percentuale di colloide (vedere i calcoli in pochi passi 4.4.7–4.4.9).
- Ripetere i passaggi 4.4.2–4.4.5 per acquisire BH2 e UH2...
- Eseguire una misurazione di sfondo di un oggetto vuoto ben contatore e determinare il numero di conteggi nella finestra di 400 – 600 keV energia per 30 s.
- Correggere i conteggi in UH1, UH2, BH1 e BH2 per decadimento e lo sfondo (determinato nel passaggio 4.4.7) per ottenere UH1cor, UH2cor, BH1cor, BH2cor. Δt è la differenza di orario tra la misurazione del campione e l'arte (determinato nel passaggio 3.11) in pochi minuti.
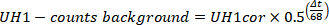
- Calcolare il numero di colloidi Ga 68con la seguente formula; Si noti che questo dovrebbe essere inferiore al 3%. UH1cor, UH2cor, BH1cor, BH2cor sono i corretti valori ottenuti nel passaggio 4.4.8.
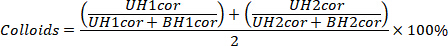
- Determinare gli ioni Ga 68attraverso la separazione della colonna.
- Diluire 20 µ l di 68Ga-DOTATATE in 1 mL di 5 mM EDTA, effettuando una soluzione di riserva.
- Preparare una cartuccia C-18 sciacquando lentamente con 1 mL di etanolo al 100%, seguita da 1 mL di acqua sterile.
- Preparare un campione (S) Diluire 10 µ l di soluzione madre in 1 mL di acqua sterile, inserendola in un contatore di ben, e determinazione del numero di conteggi nella finestra di 400 – 600 keV energia per 30 s.
- Lavare il campione lentamente (5-10 mL/min) attraverso la cartuccia di C-18 con una siringa e raccogliere la soluzione rimanente (C). Sciacquare la provetta con 1 mL di acqua e lavare questo attraverso la colonna del tubo di raccolta.
- Inserire il tubo di raccolta (C), la provetta vuota (E) e la siringa (Sy) in un contatore bene e determinare il numero di conteggi in ciascuno di essi nella finestra di energia di 400 – 600 keV per 30 s. uso questo per stimare la percentuale di ioni (Vedi il calcolo in passi 4.5.7 e 4.5 ,8.
- Ripetere i passaggi 4.5.2\u20124.5.5.
- Correggere i conteggi per decadimento e sfondo (determinato nel passaggio 4.4.7) in C, S, E e Sy per determinare C', S', E 'e Sy, per determinare il numero di conteggi al ART con la formula seguente, in cui Δt è la differenza di orario tra il campione misurato e l'arte in m inuto.
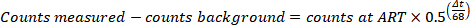
- Calcolare il 68percentuale di ioni Ga con la seguente formula; Si noti che questo dovrebbe essere inferiore al 2%.
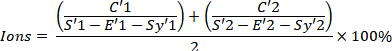
- Determinare la purezza di radiofarmaco calcolando l'importo totale di 68Ga-DOTATATE con la seguente formula, che dovrebbe essere almeno 91%.
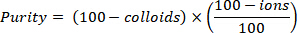
5. periodico controllo di qualità di 68Ga-DOTATATE dopo amministrazione paziente
Nota: Questa operazione deve essere eseguita > 48 h dopo la preparazione di 68Ga-DOTATATE per consentire il decadimento di 68GA.
- Preparare le seguenti soluzioni in anticipo.
- Preparare la soluzione di riferimento HEPES sciogliendo 20 mg di HEPES in 50 mL di acqua sterile. La soluzione può essere conservata a temperatura ambiente fino a 6 mesi.
Nota: Questo è basato su HEPES, la dose massima raccomandata di 200 µ g per ciascun volume somministrato. - Preparare 25: 75 v/v acqua: acetonitrile.
- Preparare la soluzione di riferimento HEPES sciogliendo 20 mg di HEPES in 50 mL di acqua sterile. La soluzione può essere conservata a temperatura ambiente fino a 6 mesi.
- Determinare la concentrazione di HEPES nel prodotto finale (settimanale).
- Trasferire 3 µ l di soluzione di 68Ga-DOTATATE in passi di 1 µ l di una carta di254 ITLC-SG F di almeno 8 cm di lunghezza. Usare un asciugacapelli per asciugare la carta tra le applicazioni di 1 µ l.
- Ripetere il passaggio 5.2.1 con la soluzione di riferimento HEPES.
- Posizionare le strisce in un solvente di 25: 75 acqua: acetonitrile. Garantire che le soluzioni applicate non entrino in contatto con il liquido.
- Attendere alcuni minuti fino a quando il solvente ha viaggiato per almeno 2/3 della lunghezza del documento.
- Sviluppare la carta per almeno 4 minuti in una camera chiusa con cristalli di iodio.
- Valutare visivamente il risultato; dovrebbe apparire una macchia gialla. Il punto sulla carta con 68Ga-DOTATATE dovrebbe essere meno intenso di quello della soluzione di riferimento.
- Determinare la svolta di Ge 68nel prodotto finale (mensile).
- Preparare un campione con 200 µ l di 68soluzione Ga-DOTATATE (G). Posto in un contatore bene e determinare il numero di conteggi in ciascuna nella finestra di 400 – 600 keV energia per 30 s.
- Ripetere il punto 5.3.1.
- Correggere i conteggi in G per determinare G' per decadimento, per determinare il numero di conteggi al ART con la formula seguente, in cui Δt è la differenza di orario tra il campione misurato e l'arte in pochi minuti.
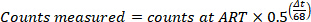
- Calcolare la svolta di Ge di 68(MBq/MBq), che dovrebbe essere meno dello 0,001%, con la seguente formula.
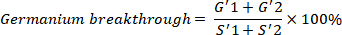
- Determinare la sterilità del prodotto finale (mensile).
- Aggiungere il restante 68soluzione Ga-DOTATATE di un mezzo di brodo (TSB) di soia triptico. Incubare per 14 d 30 – 35 ° c.
- Verifica che il supporto TSB è un liquido trasparente dopo il periodo di incubazione.
6. paziente preparazione e la somministrazione di 68Ga-DOTATATE
Nota: L'attività iniettata in questo protocollo fornisce immagini di buona qualità con il sistema di PET/CT disponibile e il protocollo di formazione immagine come descritto nella sezione 7. Con altri sistemi di imaging e protocolli, attività iniettata deve essere ottimizzato.
- Inviare in anticipo, la nomina e la cartella paziente con informazioni su 68Ga-DOTATATE PET/CT per posta ad ogni paziente. Confermare ogni appuntamento telefonicamente 1 giorno di anticipo.
- Cibo e bevande non sono limitate prima formazione immagine Ga-DOTATATE PET/CT di 68. Consigliare ai pazienti di bere un extra 1 L d'acqua in 2 h prima di formazione immagine. Si raccomanda inoltre di pazienti non portare i bambini o donne incinte con loro al reparto di medicina nucleare.
- Il giorno di 68Ga-DOTATATE PET/CT, hanno i pazienti check-in presso il dipartimento di medicina nucleare 60 min prima l'imaging. Prendere una breve storia medica.
- Informarsi circa la data dell'ultima amministrazione analogico del somatostatina. Questo non è una controindicazione per 68Ga-DOTATATE PET/CT, ma dovrebbe essere notato.
- Inserire una cannula endovenosa nel braccio e sciacquarlo con soluzione fisiologica per verificare il posizionamento della cannula.
- Iniettare 100 MBq di 68Ga-DOTATATE 45 min prima l'imaging PET/CT.
7. imaging PET/TC
- Posizionare il paziente con le braccia sopra la loro testa sullo scanner PET/CT. Istruire il paziente a rimanere ancora in tutto l'esame.
- Acquisire un'immagine di sondaggio e selezionare l'area di scansione dalla ghiandola pituitaria a metà coscia, se non diversamente specificato a causa di indicazioni cliniche.
- Eseguire una basso-dose CT scan con 40 mAs, 140 keV e fette di 5 mm per la correzione di attenuazione e correlazione anatomica.
- Eseguire una scansione PET con 150 s per la posizione del letto, a partire alla testa del paziente.
- Ricostruire le immagini di CT con le fette di 5mm e di proiezione posteriore filtrate.
- Ricostruire le immagini PET con BLOB-OS-TF, con tre iterazioni e 33 sottoinsiemi con una dimensione del voxel di 4 x 4 x 4 mm.
- Invia tutte le immagini per il sistema di archiviazione e comunicazione di immagine locale (PACS).
Access restricted. Please log in or start a trial to view this content.
Risultati
Facendo uso di un sistema di etichettatura automatizzato, 357 lotti di 68Ga-DOTATATE sono state prodotte tra dicembre 2014 e ottobre 2018. Di 357 prodotta, 17 lotti non riuscita e 340 lotti sono stati rilasciati, che conduce a un tasso di successo globale del 95,2%. Dei batch non riusciti, 11 sono stati causati da un guasto tecnico, mentre in sei casi, il prodotto 68Ga-DOTATATE non soddisfa le specifiche. La figura 1 Mostra un diagramma ...
Access restricted. Please log in or start a trial to view this content.
Discussione
Questo protocollo descrive la produzione e la formazione immagine di 68Ga-DOTATATE successiva-PET/CT. Per l'uso efficiente di ogni lotto prodotto di 68Ga-DOTATATE, un flusso di lavoro ottima con temporizzazione rigorosi è necessaria. Poiché l'emivita di 68Ga è 68 min, un ritardo di tempo relativamente piccola di 15 min conduce ad una perdita del 15% della radioattività. Ciò richiede una comunicazione attiva tra l'impianto di produzione, il personale dell'amministrazione della dose pe...
Access restricted. Please log in or start a trial to view this content.
Divulgazioni
Gli autori non hanno nulla a rivelare.
Riconoscimenti
Gli autori riconoscono che tutto il personale coinvolto nella formazione immagine Ga-DOTATATE PET/CT 68presso il dipartimento di medicina nucleare presso il Netherlands Cancer Institute.
Access restricted. Please log in or start a trial to view this content.
Materiali
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Biosolve | 012007 | > 99.9 % |
| Ammonium acetate | Merck | 101116 | ≥ 98 % |
| Aqua / Water for injections | Braun | ||
| Automated labeling system | Scintomics | GRP 3V | |
| C-18 cartridge | Waters | WAT023501 | Sep-Pak C18 Plus Light |
| Dose calibrator | Veenstra Instruments | VIK-202-5051 | |
| EDTA | Merck | 324503 | |
| Ethanol | Sigma Aldrich | 32221-M | ≥ 99.8 % |
| Ga-68 labeling kit | ABX | SC-01 | |
| Ge-68/Ga-68 generator | Eckert & Ziegler | 1850 MBq | |
| HA-DOTATATE | Scintomics | GRPC/R-000095 | |
| HCl 0.1M for elution | ABX | HCl-03 | |
| HEPES | Sigma Aldrich | H3375 | ≥ 99.5 % |
| Iodine | Sigma Aldrich | 207772 | ≥ 99.8 %, solid |
| ITLC-SG F254 plates | Merck | 105735 | TLC Silica gel 60 F254 |
| ITLC-SG paper | Agilent | SGI0001 | Glass fiber |
| Methanol | Sigma Aldrich | 32213-M | ≥ 99.8 %, Ph. Eur. |
| Non-vented filter | Merck | SLMPL25SS | Millex-MP filter 0.22 µm |
| PET/CT | Philips | Gemini TOF | |
| pH indicator strips | Merck | 109584 | MColorpHast (pH2.0-9.0) |
| Tryptic soy broth medium | Biotrading | K111F010QK | |
| Vented filter | Merck | SLGV0250S | Cathivex GV 0.22 µm |
| Well counter | Canberra (now Mirion) | Osprey Digital Tube Base MCA Detector 76 BP76/3M-X |
Riferimenti
- Oronsky, B., Ma, P. C., Morgensztern, D., Carter, C. A. Nothing but NET: A Review of Neuroendocrine Tumors and Carcinomas. Neoplasia. 19 (12), 991-1002 (2017).
- Dasari, A., et al. Trends in the Incidence, Prevalence, and Survival Outcomes in Patients With Neuroendocrine Tumors in the United States. JAMA Oncology. 3 (10), 1335-1342 (2017).
- Krenning, E. P., et al. Localistion of endocrine-related tumours with radioiodinated analogue of somatostatin. The Lancet. 333 (8632), 242-244 (1989).
- Krenning, E. P., et al. Somatostatin receptor scintigraphy with [111In-DTPA-D-Phe1]- and [123I-Tyr3]-octreotide: the Rotterdam experience with more than 1000 patients. European Journal of Nuclear Medicine. 20 (8), 716-731 (1993).
- Balon, H. R., et al. Procedure guideline for somatostatin receptor scintigraphy with (111)In-pentetreotide. Journal of Nuclear Medicine. 42 (7), 1134-1138 (2001).
- Kayani, I., et al. Functional Imaging of Neuroendocrine Tumors With Combined PET/CT Using 68Ga-DOTATATE (Dota-DPhe1,Tyr3-octreotate) and 18F-FDG. Cancer. 112 (11), 2447-2455 (2008).
- Hofman, M. S., Kong, G., Neels, O. C., Hong, E., Hicks, R. J. High management impact of Ga-68 DOTATATE (GaTate) PET/CT for imaging neuroendocrine and other somatostatin expressing tumours. Journal of Medical Imaging and Radiation Oncology. 56 (1), 40-47 (2012).
- Srirajaskanthan, R., et al. The role of 68Ga-DOTATATE PET in patients with neuroendocrine tumors and negative or equivocal findings on 111In-DTPA-octreotide scintigraphy. Journal of Nuclear Medicine. 51 (6), 875-882 (2010).
- Deppen, S. A. 68Ga-DOTATATE Compared with 111In-DTPA-Octreotide and Conventional Imaging for Pulmonary and Gastroenteropancreatic Neuroendocrine Tumors: A Systematic Review and Meta-Analysis. Journal of Nuclear Medicine. 57 (6), 872-878 (2016).
- Yang, J., et al. Diagnostic role of Gallium-68 DOTATOC and Gallium-68 DOTATATE PET in patients with neuroendocrine tumors: a meta-analysis. Acta Radiologica. 55 (4), 389-398 (2014).
- Barrio, M., et al. The Impact of Somatostatin Receptor-Directed PET/CT on the Management of Patients with Neuroendocrine Tumor: A Systematic Review and Meta-Analysis. Journal of Nuclear Medicine. 58 (5), 756-761 (2017).
- Strosberg, J. R., et al. The North American Neuroendocrine Tumor Society Consensus Guidelines for Surveillance and Medical Management of Midgut Neuroendocrine Tumors. Pancreas. 46 (6), 707-714 (2017).
- Virgolini, I., et al. Procedure guidelines for PET/CT tumour imaging with 68Ga-DOTA-conjugated peptides: 68Ga-DOTA-TOC, 68Ga-DOTA-NOC, 68Ga-DOTA-TATE. European Journal of Nuclear Medicine and Molecular Imaging. 67 (10), 2004-2010 (2010).
- European Directorate for the Quality of Medicines & Healthcare (EDQM). Monograph 01/2013:2482 Gallium (68Ga) edotreotide injection. European Pharmacopoeia 9th Edition. , (2017).
- Brogsitter, C., et al. Twins in spirit part II: DOTATATE and high-affinity DOTATATE – the clinical experience. European Journal of Nuclear Medicine and Molecular Imaging. 41 (6), 1158-1165 (2014).
- Sandström, M., et al. Comparative biodistribution and radiation dosimetry of 68Ga-DOTATOC and 68Ga-DOTATATE in patients with neuroendocrine tumors. Journal of Nuclear Medicine. 54 (10), 1755-1759 (2013).
- Aalbersberg, E. A., et al. Influence of lanreotide on uptake of 68Ga-DOTATATE in patients with neuroendocrine tumours: a prospective intra-patient evaluation. European Journal of Nuclear Medicine and Molecular Imaging. , In Press (2018).
Access restricted. Please log in or start a trial to view this content.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon