È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Automazione del test del micronucleo mediante citometria a flusso di imaging e intelligenza artificiale
In questo articolo
Riepilogo
Il test del micronucleo (MN) è un test ben consolidato per quantificare il danno al DNA. Tuttavia, la valutazione del test utilizzando tecniche convenzionali come la microscopia manuale o l'analisi delle immagini basata sulle caratteristiche è laboriosa e impegnativa. Questo articolo descrive la metodologia per sviluppare un modello di intelligenza artificiale per valutare il test MN utilizzando i dati di citometria a flusso di imaging.
Abstract
Il test del micronucleo (MN) viene utilizzato in tutto il mondo dagli organismi di regolamentazione per valutare le sostanze chimiche per la tossicità genetica. Il test può essere eseguito in due modi: segnando MN in cellule binucleate una volta divise, bloccate dalla citochinesi o cellule mononucleate completamente divise. Storicamente, la microscopia ottica è stata il metodo gold standard per valutare il test, ma è laboriosa e soggettiva. La citometria a flusso è stata utilizzata negli ultimi anni per valutare il test, ma è limitata dall'incapacità di confermare visivamente aspetti chiave delle immagini cellulari. La citometria a flusso di imaging (IFC) combina l'acquisizione di immagini ad alta produttività e l'analisi automatizzata delle immagini ed è stata applicata con successo per acquisire rapidamente immagini e valutare tutti gli eventi chiave nel test MN. Recentemente, è stato dimostrato che i metodi di intelligenza artificiale (AI) basati su reti neurali convoluzionali possono essere utilizzati per valutare i dati del saggio MN acquisiti da IFC. Questo documento descrive tutti i passaggi per utilizzare il software di intelligenza artificiale per creare un modello di deep learning per valutare tutti gli eventi chiave e applicare questo modello per assegnare automaticamente un punteggio a dati aggiuntivi. I risultati del modello di deep learning AI si confrontano bene con la microscopia manuale, consentendo quindi un punteggio completamente automatizzato del test MN combinando IFC e AI.
Introduzione
Il test del micronucleo (MN) è fondamentale nella tossicologia genetica per valutare il danno al DNA nello sviluppo di cosmetici, prodotti farmaceutici e chimici per uso umano 1,2,3,4. I micronuclei sono formati da interi cromosomi o frammenti cromosomici che non si incorporano nel nucleo dopo la divisione e si condensano in piccoli corpi circolari separati dal nucleo. Pertanto, il MN può essere utilizzato come endpoint per quantificare il danno al DNA nei test di genotossicità1.
Il metodo preferito per quantificare la MN è all'interno di cellule binucleate (BNC) una volta divise bloccando la divisione utilizzando la citocalasina-B (Cyt-B). In questa versione del test, la citotossicità viene valutata anche segnando cellule mononucleate (MONO) e polinucleate (POLY). Il test può anche essere eseguito assegnando un punteggio MN in cellule MONO non bloccate, che è più veloce e più facile da valutare, con la citotossicità valutata utilizzando la conta cellulare pre e post-esposizione per valutare la proliferazione 5,6.
Il punteggio fisico del test è stato storicamente eseguito attraverso la microscopia manuale, poiché ciò consente la conferma visiva di tutti gli eventi chiave. Tuttavia, la microscopia manuale è impegnativa e soggettiva1. Pertanto, sono state sviluppate tecniche automatizzate, tra cui la scansione del vetrino da microscopio e la citometria a flusso, ognuna con i propri vantaggi e limiti. Mentre i metodi di scansione dei vetrini consentono di visualizzare gli eventi chiave, i vetrini devono essere creati con una densità di cella ottimale, che può essere difficile da raggiungere. Inoltre, questa tecnica spesso manca di visualizzazione citoplasmatica, che può compromettere il punteggio delle cellule MONO e POLY 7,8. Mentre la citometria a flusso offre un'acquisizione di dati ad alto rendimento, le cellule devono essere lisate, quindi non consentendo l'uso della forma Cyt-B del test. Inoltre, come tecnica non-imaging, la citometria a flusso convenzionale non fornisce la convalida visiva degli eventi chiave 9,10.
Pertanto, la citometria a flusso di imaging (IFC) è stata studiata per eseguire il test MN. ImageStreamX Mk II combina la velocità e la robustezza statistica della citometria a flusso convenzionale con le capacità di imaging ad alta risoluzione della microscopia in un unico sistema11. È stato dimostrato che utilizzando IFC, le immagini ad alta risoluzione di tutti gli eventi chiave possono essere catturate e valutate automaticamente utilizzando tecniche basate su funzionalità 12,13 o intelligenza artificiale (AI) 14,15. Utilizzando IFC per eseguire il test MN, è possibile ottenere il punteggio automatico di molte più cellule rispetto alla microscopia in un lasso di tempo più breve.
Questo lavoro si discosta da un flusso di lavoro di analisi delle immagini precedentemente descritto16 e discute tutti i passaggi necessari per sviluppare e addestrare un modello di foresta casuale (RF) e / o rete neurale convoluzionale (CNN) utilizzando il software Amnis AI (d'ora in poi denominato "software AI"). Vengono descritti tutti i passaggi necessari, tra cui il popolamento dei dati di verità sul terreno utilizzando strumenti di tagging assistiti dall'IA, l'interpretazione dei risultati dell'addestramento del modello e l'applicazione del modello per classificare dati aggiuntivi, consentendo il calcolo della genotossicità e della citotossicità15.
Protocollo
1. Acquisizione dati mediante citometria a flusso di imaging
NOTA: Fare riferimento a Rodrigues et al.16 con le seguenti modifiche, notando che le regioni di acquisizione utilizzando IFC potrebbero dover essere modificate per un'acquisizione ottimale dell'immagine:
- Per il metodo non-Cyt-B, eseguire un conteggio delle cellule utilizzando un contatore di cellule disponibile in commercio seguendo le istruzioni del produttore (vedere la tabella dei materiali) su ciascuna coltura immediatamente prima della coltura e immediatamente dopo il periodo di recupero.
- Se si eseguono campioni su un citometro a flusso di imaging con una singola telecamera, posizionare il campo luminoso (BF) nel canale 4. Sostituire M01 con M04 e M07 con M01.
NOTA: "M" si riferisce al canale della telecamera sull'IFC. - Utilizzare l'ingrandimento 40x durante l'acquisizione.
- Nel grafico delle proporzioni dell'area BF rispetto a BF durante l'acquisizione, utilizzare le seguenti coordinate regionali:
Coordinate X: 100 e 900; Coordinate Y: 0,7 e 1 (metodo Cyt-B)
Coordinate X: 100 e 600; Coordinate Y: 0.7 e 1 - Nel grafico dell'intensità di Hoechst, utilizzare le seguenti coordinate regionali:
Coordinate X: 55 e 75; Coordinate Y: 9.5 e 15 (metodo Cyt-B)
Coordinate X: 55 e 75; Coordinate Y: 13 e 21 (metodo non Cyt-B) - Per rimuovere immagini di oggetti apoptotici e necrotici dai dati, avviare il pacchetto software IDEAS 6.3 (d'ora in poi denominato "software di analisi delle immagini"; vedi Tabella dei materiali).
NOTA: il software AI è stato progettato per funzionare con file .daf elaborati utilizzando la versione più recente del software di analisi delle immagini. Assicurarsi che il software di analisi delle immagini sia aggiornato. - Salvare il lavoro come file modello (.ast).
2. Creazione di file .daf per tutti i file .rif
- Il software AI consente solo l'importazione di file .daf. Creare file con estensione daf per tutti i file con estensione rif nell'esperimento tramite l'elaborazione batch.
- Nel menu Strumenti , fare clic su File di dati batch e quindi fare clic su Aggiungi batch.
- Nella nuova finestra, selezionare Aggiungi file e selezionare i file .rif da aggiungere al batch. Nell'opzione Selezionare un modello o un file di analisi dei dati (ast, daf) selezionare il file ast creato in precedenza.
- Se necessario, assegnare un nome batch e fare clic su OK per creare file .daf per tutti i file .rif caricati.
3. Creazione di un esperimento nel software AI
- Fare riferimento al diagramma di flusso nella Figura 1 che descrive il processo di creazione di un modello di deep learning utilizzando il software di intelligenza artificiale.
- Avvia il software AI e assicurati che sia installata la versione più recente facendo clic su Informazioni nell'angolo in basso a sinistra della finestra. Se non è installata la versione più recente, contattare support@luminexcorp.com per ottenerla.
- La schermata predefinita nel software è la schermata Nuovo esperimento . Utilizza l'icona Cartella per scegliere dove salvare l'esperimento e digita un nome per l'esperimento (ad esempio, "Modello MN").
- In Tipo esperimento, fai clic sul pulsante di opzione accanto a Treno per avviare un esperimento di addestramento e iniziare a creare il modello CNN. Fare clic su Avanti.
- Facoltativo: se un modello è stato precedentemente addestrato, può essere utilizzato come modello per un nuovo modello di intelligenza artificiale e può essere selezionato come modello per la creazione di un nuovo modello dalla schermata Seleziona modello modello . Se non esiste alcun modello di modello, è sufficiente ignorare questo passaggio facendo clic su Avanti.
- La schermata successiva è la schermata Definisci nuovo modello . In Modello il nome assegnato al modello nel passaggio 3.3 verrà compilato automaticamente.
- In Descrizione digitare una descrizione per il modello (facoltativo) e lasciare la dimensione massima dell'immagine a 150 pixel.
- In Canali, fare clic su Aggiungi BF per aggiungere un canale brightfield all'elenco. In Nome, fare doppio clic su Brightfield e rinominare questo canale in BF. Fare clic su Aggiungi FL per aggiungere un canale fluorescente all'elenco. In Nome, fare doppio clic su Fluorescente e rinominare questo canale in DNA.
- In Nomi delle classi, fai clic su Aggiungi. Nella finestra pop-up, digitare Mononucleated e fare clic su OK. In questo modo la classe mononucleata viene aggiunta all'elenco dei nomi delle classi. Ripetere questa procedura per assicurarsi che nell'elenco siano definite le sei classi seguenti:
Mononucleati
Mononucleato con MN
Binucleato
Binucleato con MN
Polinucleati
Morfologia irregolare
Fare clic su Avanti.
NOTA: Queste sei classi di modelli di verità di base rappresenteranno gli eventi chiave da valutare, nonché immagini con morfologia diversa dal criterio di punteggio accettato5.- Facoltativo: se lo si desidera, il modello di analisi della versione 1.7 può essere incluso per utilizzare le funzionalità del software di analisi delle immagini. Se desideri includere queste funzionalità nel modello di intelligenza artificiale, cerca il file .ast, quindi dai menu a discesa specifici del canale, scegli i sottoinsiemi di funzionalità che desideri includere.
- In Seleziona file, fai clic su Aggiungi file e cerca i file desiderati da aggiungere al software AI per creare i dati di verità di base. Fare clic su Avanti.
NOTA: è importante aggiungere più file di dati (ad esempio, dati di controllo positivi e negativi) che contengano un numero sufficiente di tutti gli eventi chiave.
- Quindi, nella schermata Seleziona popolazioni di base , individuare la popolazione non apoptotica dalla gerarchia della popolazione. Fare clic con il pulsante destro del mouse sulla popolazione non apoptotica e selezionare Seleziona tutte le popolazioni corrispondenti. Fare clic su Avanti.
NOTA: È importante escludere tutte le popolazioni che non dovrebbero essere classificate (ad esempio, perline, detriti, doppiette, ecc.) - Questa schermata è la schermata Seleziona popolazioni di verità .
- Se le popolazioni di verità taggate degli eventi chiave non sono state create nel software di analisi delle immagini, fare clic su Avanti.
- Se nel software di analisi delle immagini sono state create popolazioni di verità contrassegnate, assegnarle alla classe di modello appropriata.
- Per assegnare una popolazione di verità taggata di cellule MONO con MN, fare clic sulla classe Mononucleata con MN in Classi modello a sinistra. Quindi fare clic sulla popolazione di verità appropriata taggata sulla destra che contiene questi eventi.
- Se le popolazioni di verità contrassegnate sono state create in più di un file di dati, fare clic con il pulsante destro del mouse su una delle popolazioni di verità e selezionare Seleziona tutte le popolazioni corrispondenti per aggiungere le popolazioni contrassegnate da più file alla classe appropriata.
- Una volta assegnate tutte le popolazioni di verità appropriate, fare clic su Avanti.
- Nella schermata Seleziona canali, scegli i canali appropriati per l'esperimento. Qui, impostare BF sul canale 1 e Hoechst sul canale 7. Fai clic con il pulsante destro del mouse su un canale e seleziona Applica a tutti. Fare clic su Avanti.
- Infine, nella schermata di conferma , fai clic su Crea esperimento.
- Il software AI carica le immagini dai file di dati e crea le classi di modello definite nel passaggio 3.5.3 con le immagini di verità di base assegnate nel passaggio 3.7. Fare clic su Fine.
- Una volta creato l'esperimento, vengono presentate cinque opzioni:
Esperimento: fornisce i dettagli dell'esperimento, inclusi i file di dati caricati, i canali scelti e le classi definite del modello di verità di base.
Tagging: lancia lo strumento di tagging attraverso il quale gli utenti possono popolare i dati di verità sul terreno.
Addestramento: addestra un modello basato sui dati di verità sul terreno.
Classifica: utilizza modelli addestrati per classificare i dati.
Risultati: fornisce i risultati sia di un esperimento di addestramento che di un esperimento di classificazione.
4. Popolare i dati di verità di base utilizzando strumenti di tagging assistiti dall'intelligenza artificiale
- Fare clic su Tagging per avviare l'interfaccia dello strumento di tagging .
- Fare clic sugli strumenti di zoom (icone della lente di ingrandimento) per ritagliare le immagini e facilitarne la visualizzazione.
- Fare clic sulla barra di scorrimento per regolare le dimensioni dell'immagine e modificare il numero di immagini visualizzate nella galleria.
- Fare clic sull'opzione Impostazioni di visualizzazione e scegliere Min-Max, che fornisce la migliore immagine di contrasto per identificare tutti gli eventi chiave.
- Fare clic su Setup Gallery Display per modificare il colore dell'immagine del DNA in giallo o bianco, che migliorerà la visualizzazione di piccoli oggetti (ad esempio, MN).
- Fare clic su Cluster per eseguire l'algoritmo per raggruppare oggetti con morfologia simile. Una volta completato il clustering, i singoli cluster con il numero di oggetti per cluster vengono visualizzati in un elenco in Popolazioni sconosciute. Selezionare i singoli cluster per visualizzare gli oggetti all'interno del cluster e assegnare tali oggetti alle classi di modello appropriate.
- Dopo aver assegnato un minimo di 25 oggetti a ciascuna classe del modello, l'algoritmo Predict diventa disponibile. Fare clic su Prevedi.
NOTA: gli oggetti che non si adattano bene a nessuna popolazione rimangono classificati come sconosciuti. Man mano che più oggetti vengono aggiunti alle popolazioni di verità, l'accuratezza della previsione migliora. - Continuare a popolare le classi del modello di verità di base con immagini appropriate fino a raggiungere un numero sufficiente di oggetti in ogni classe.
- Una volta assegnato un minimo di 100 oggetti a ciascuna classe di modello, fare clic sulla scheda Formazione nella parte superiore dello schermo. Fare clic sul pulsante Treno per creare un modello utilizzando gli algoritmi Random Forest e CNN.
NOTA: Il software AI crea modelli utilizzando entrambi gli algoritmi Random Forest e CNN, le caselle di controllo consentono la creazione di modelli utilizzando solo algoritmi Random Forest of CNN.
5. Valutazione dell'accuratezza del modello
- Una volta completato il training del modello, fare clic su Visualizza risultati.
- Utilizzare la schermata dei risultati per valutare l'accuratezza del modello. Utilizzare il menu a discesa per passare da Random Forest a CNN.
NOTA: le popolazioni di verità possono essere aggiornate e il modello può essere nuovamente addestrato o utilizzato così com'è per classificare dati aggiuntivi.- Per aggiornare le popolazioni della verità, clicca su Tagging in alto e segui la sezione 4.
6. Classificazione dei dati utilizzando il modello
- Avvia il software AI. La schermata predefinita è la schermata Nuovo esperimento . Usa l'icona Cartella per scegliere dove salvare l'esperimento e digita un nome per l'esperimento.
- In Tipo di esperimento, fai clic sul pulsante di opzione accanto a Classifica per avviare un esperimento di classificazione. Fare clic su Avanti.
- Fare clic sul modello da utilizzare per la classificazione, quindi fare clic su Avanti.
- Nella schermata Seleziona file, fare clic su Aggiungi file e cercare i file da classificare in base al modello CNN. Fare clic su Avanti.
- Successivamente, nella schermata Seleziona popolazioni di base , fare clic sulla casella di controllo accanto alla popolazione non apoptotica in uno dei file caricati. Fare clic con il pulsante destro del mouse sulla popolazione non apoptotica e fare clic su Seleziona tutte le popolazioni corrispondenti per selezionare questa popolazione da tutti i file caricati. Fare clic su Avanti.
- Facoltativo: se i dati da classificare contengono popolazioni di verità, possono essere assegnati alle classi di modello appropriate nella schermata Seleziona popolazioni di verità. In caso contrario, fare clic su Avanti per ignorare questo passaggio.
- Nella schermata Seleziona canali , scegliere Canale 1 per il campo chiaro e Canale 7 per la colorazione del DNA. Fai clic con il pulsante destro del mouse su un canale e fai clic su Applica a tutti. Quindi fare clic su Avanti.
- Infine, nella schermata di conferma , fai clic su Crea esperimento. Il software AI carica il modello selezionato e tutte le immagini dai file di dati scelti. Fare clic su Fine.
- Fare clic su Classifica per avviare la schermata di classificazione. Fare clic sul pulsante Classifica. Viene avviato il processo di utilizzo del modello RF e CNN per classificare dati aggiuntivi e identificare tutti gli oggetti che appartengono alle classi di modello specificate.
NOTA: le caselle di controllo possono essere utilizzate per selezionare il modello RF e/o il modello CNN. - Una volta completata la classificazione, fare clic su Visualizza risultati.
- Fare clic sul pulsante Aggiorna DAF per visualizzare la finestra Aggiorna DAF con risultati classificazione. Fare clic su OK per aggiornare i file .daf.
7. Generazione di un report dei risultati della classificazione
- Nella schermata Risultati, fare clic su Genera report. Selezionare la casella di controllo accanto a Crea report per ogni DAF di input se è necessario un singolo report per ogni DAF di input. Fare clic su OK.
- Al termine, aprire la cartella in cui sono stati salvati i file di report. All'interno della cartella sono presenti un report .pdf dell'esperimento e una cartella Risorse .
- Aprire il .pdf per visualizzare il report. Il report contiene informazioni sul modello e sull'esperimento, l'elenco dei file .daf di input, i conteggi delle classi e le percentuali delle classi in formato tabellare e istogramma e una matrice di confusione che riassume la probabilità di previsione mediana in tutti i file .daf di input.
- Aprire la cartella Risorse e quindi la cartella CNN . All'interno di questa cartella sono .png file del conteggio delle classi e dei grafici a barre percentuali, nonché la matrice di confusione. Inoltre, sono disponibili .csv file contenenti i conteggi delle classi e le percentuali per ogni file di input.
8. Determinazione della frequenza MN e della citotossicità
- Calcolo della frequenza MN
- Metodo non Cyt-B: per determinare la frequenza MN, aprire il file class_count.csv dal passaggio 7.4. Per ogni file di input, dividere i conteggi nella popolazione "Mononucleati con MN" per i conteggi nella popolazione "Mononucleata" e moltiplicare per 100:

- Metodo Cyt-B: Per determinare la frequenza MN, aprire il file class_count.csv dal passaggio 7.4. Per ogni file di input, dividere i conteggi nella popolazione "Binucleated with MN" per i conteggi nella popolazione "Binucleated" e moltiplicare per 100:
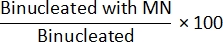
- Metodo non Cyt-B: per determinare la frequenza MN, aprire il file class_count.csv dal passaggio 7.4. Per ogni file di input, dividere i conteggi nella popolazione "Mononucleati con MN" per i conteggi nella popolazione "Mononucleata" e moltiplicare per 100:
- Calcolo della citotossicità
- Metodo non Cyt-B:
- Utilizzando la conta delle cellule iniziali e la conta delle cellule post-trattamento, calcolare prima il raddoppio della popolazione (PD) per ciascun campione2:
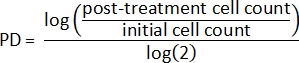
- Quindi, calcola la popolazione relativa raddoppiando2:

- Infine, calcolare la citotossicità2 per ciascun campione:
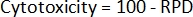
- Utilizzando la conta delle cellule iniziali e la conta delle cellule post-trattamento, calcolare prima il raddoppio della popolazione (PD) per ciascun campione2:
- Metodo Cyt-B:
- Per calcolare l'indice di proliferazione dei blocchi di citochinesi (CBPI)2, utilizzare i conteggi nelle classi mononucleata, binucleata e polinucleata per ciascun campione dal file class_count.csv :
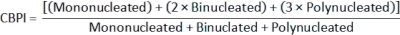
- Per calcolare la citotossicità2, utilizzare il CBPI dalle colture di controllo (C) e dalle colture esposte (T):
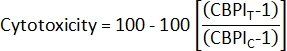
- Per calcolare l'indice di proliferazione dei blocchi di citochinesi (CBPI)2, utilizzare i conteggi nelle classi mononucleata, binucleata e polinucleata per ciascun campione dal file class_count.csv :
- Metodo non Cyt-B:
Risultati
La Figura 1 mostra il flusso di lavoro per l'utilizzo del software AI per creare un modello per il test MN. L'utente carica i file .daf desiderati nel software AI, quindi assegna gli oggetti alle classi del modello di verità di terra utilizzando gli algoritmi di tagging cluster assistito da AI (Figura 2) e predict (Figura 3). Una volta che tutte le classi del modello di verità di base sono state popolate con oggetti sufficienti, i...
Discussione
Il lavoro qui presentato descrive l'uso di algoritmi di deep learning per automatizzare il punteggio del test MN. Diverse pubblicazioni recenti hanno dimostrato che strumenti intuitivi e interattivi consentono la creazione di modelli di deep learning per analizzare i dati delle immagini senza la necessità di conoscenze computazionali approfondite18,19. Il protocollo descritto in questo lavoro utilizzando un pacchetto software basato sull'interfaccia utente è st...
Divulgazioni
Gli autori sono impiegati da Luminex Corporation, una società DiaSorin, il produttore del citometro a flusso di imaging ImageStream e del software Amnis AI utilizzato in questo lavoro.
Riconoscimenti
Nessuno.
Materiali
| Name | Company | Catalog Number | Comments |
| 15 mL centrifuge tube | Falcon | 352096 | |
| Cleanser - Coulter Clenz | Beckman Coulter | 8546931 | Fill container with 200 mL of Cleanser. https://www.beckmancoulter.com/wsrportal/page/itemDetails?itemNumber=8546931#2/10//0/25/ 1/0/asc/2/8546931///0/1//0/ |
| Colchicine | MilliporeSigma | 64-86-8 | |
| Corning bottle-top vacuum filter | MilliporeSigma | CLS430769 | 0.22 µm filter, 500 mL bottle |
| Cytochalasin B | MilliporeSigma | 14930-96-2 | 5 mg bottle |
| Debubbler - 70% Isopropanol | MilliporeSigma | 1.3704 | Fill container with 200 mL of Debubbler. http://www.emdmillipore.com/US/en/product/2-Propanol-70%25-%28V%2FV%29-0.1-%C2%B5m-filtred,MDA_CHEM-137040?ReferrerURL=https%3A%2F%2Fwww.google.com%2F |
| Dimethyl Sulfoxide (DMSO) | MilliporeSigma | 67-68-5 | |
| Dulbecco's Phosphate Buffered Saline 1X | EMD Millipore | BSS-1006-B | PBS Ca++MG++ Free |
| Fetal Bovine Serum | HyClone | SH30071.03 | |
| Formaldehyde, 10%, methanol free, Ultra Pure | Polysciences, Inc. | 04018 | This is what is used for the 4% and 1% Formalin. CAUTION: Formalin/Formaldehyde toxic by inhalation and if swallowed. Irritating to the eyes, respiratory systems and skin. May cause sensitization by inhalation or skin contact. Risk of serious damage to eyes. Potential cancer hazard. http://www.polysciences.com/default/catalog-products/life-sciences/histology-microscopy/fixatives/formaldehydes/formaldehyde-10-methanol-free-pure/ |
| Guava Muse Cell Analyzer | Luminex | 0500-3115 | A standard configuration Guava Muse Cell Analyzer was used. |
| Hoechst 33342 | Thermo Fisher | H3570 | 10 mg/mL solution |
| Mannitol | MilliporeSigma | 69-65-8 | |
| MEM Non-Essential Amino Acids 100X | HyClone | SH30238.01 | |
| MIFC - ImageStreamX Mark II | Luminex, a DiaSorin company | 100220 | A 2 camera ImageStreamX Mark II eqiped with the 405 nm, 488 nm, and 642 nm lasers was used. |
| MIFC analysis software - IDEAS | Luminex, a DiaSorin company | 100220 | "Image analysis sofware" The companion software to the MIFC (ImageStreamX MKII) |
| MIFC software - INSPIRE | Luminex, a DiaSorin company | 100220 | "Image acquisition software" This is the software that runs the MIFC (ImageStreamX MKII) |
| Amnis AI software | Luminex, a DiaSorin company | 100221 | "AI software" This is the software that permits the creation of artificial intelligence models to analyze data |
| Mitomycin C | MilliporeSigma | 50-07-7 | |
| NEAA Mixture 100x | Lonza BioWhittaker | 13-114E | |
| Penicllin/Streptomycin/Glutamine solution 100X | Gibco | 15070063 | |
| Potassium Chloride (KCl) | MilliporeSigma | P9541 | |
| Rinse - Ultrapure water or deionized water | NA | NA | Use any ultrapure water or deionized water. Fill container with 900 mL of Rinse. |
| RNase | MilliporeSigma | 9001-99-4 | |
| RPMI-1640 Medium 1x | HyClone | SH30027.01 | |
| Sheath - PBS | MilliporeSigma | BSS-1006-B | This is the same as Dulbecco's Phosphate Buffered Saline 1x Ca++MG++ free. Fill container with 900 mL of Sheath. |
| Sterile water | HyClone | SH30529.01 | |
| Sterilizer - 0.4%–0.7% Hypochlorite | VWR | JT9416-1 | This is assentually 10% Clorox bleach that can be made by deluting Clorox bleach with water. Fill container with 200 mL of Sterilzer. |
| T25 flask | Falcon | 353109 | |
| T75 flask | Falcon | 353136 | |
| TK6 cells | MilliporeSigma | 95111735 |
Riferimenti
- Fenech, M., et al. HUMN project initiative and review of validation, quality control and prospects for further development of automated micronucleus assays using image cytometry systems. International Journal of Hygiene and Environmental Health. 216 (5), 541-552 (2013).
- OECD. Test No. 487: In Vitro Mammalian Cell Micronucleus Test. Section 4. OECD Guidelines for the Testing of Chemicals. , (2016).
- Fenech, M. The in vitro micronucleus technique. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 455 (1), 81-95 (2000).
- Bonassi, S., et al. An increased micronucleus frequency in peripheral blood lymphocytes predicts the risk of cancer in humans. Carcinogenesis. 28 (3), 625-631 (2007).
- Fenech, M. Cytokinesis-block micronucleus cytome assay. Nature Protocols. 2 (5), 1084-1104 (2007).
- Fenech, M. Commentary on the SFTG international collaborative study on the in vitro micronucleus test: To Cyt-B or not to Cyt-B. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 607 (1), 9-12 (2006).
- Seager, A. L., et al. Recommendations, evaluation and validation of a semi-automated, fluorescent-based scoring protocol for micronucleus testing in human cells. Mutagenesis. 29 (3), 155-164 (2014).
- Rossnerova, A., Spatova, M., Schunck, C., Sram, R. J. Automated scoring of lymphocyte micronuclei by the MetaSystems Metafer image cytometry system and its application in studies of human mutagen sensitivity and biodosimetry of genotoxin exposure. Mutagenesis. 26 (1), 169-175 (2011).
- Bryce, S. M., Bemis, J. C., Avlasevich, S. L., Dertinger, S. D. In vitro micronucleus assay scored by flow cytometry provides a comprehensive evaluation of cytogenetic damage and cytotoxicity. Mutation Research/Genetic Toxicology and Environmental Mutagenesis. 630 (1), 78-91 (2007).
- Avlasevich, S. L., Bryce, S. M., Cairns, S. E., Dertinger, S. D. In vitro micronucleus scoring by flow cytometry: Differential staining of micronuclei versus apoptotic and necrotic chromatin enhances assay reliability. Environmental and Molecular Mutagenesis. 47 (1), 56-66 (2006).
- Basiji, D. A. Principles of Amnis imaging flow cytometry. Methods in Molecular Biology. 1389, 13-21 (2016).
- Rodrigues, M. A. Automation of the in vitro micronucleus assay using the Imagestream® imaging flow cytometer. Cytometry Part A. 93 (7), 706-726 (2018).
- Verma, J. R., et al. Investigating FlowSight® imaging flow cytometry as a platform to assess chemically induced micronuclei using human lymphoblastoid cells in vitro. Mutagenesis. 33 (4), 283-289 (2018).
- Wills, J. W., et al. Inter-laboratory automation of the in vitro micronucleus assay using imaging flow cytometry and deep learning. Archives of Toxicology. 95 (9), 3101-3115 (2021).
- Rodrigues, M. A., et al. The in vitro micronucleus assay using imaging flow cytometry and deep learning. Npj Systems Biology and Applications. 7 (1), 20 (2021).
- Rodrigues, M. A. An automated method to perform the in vitro micronucleus assay using multispectral imaging flow cytometry. Journal of Visualized Experiments. (147), e59324 (2019).
- Lovell, D. P., et al. Analysis of negative historical control group data from the in vitro micronucleus assay using TK6 cells. Mutation Research/Genetic Toxicology and Environmental Mutagenesis. 825, 40-50 (2018).
- Berg, S., et al. ilastik: interactive machine learning for (bio)image analysis. Nature Methods. 16 (12), 1226-1232 (2019).
- Hennig, H., et al. An open-source solution for advanced imaging flow cytometry data analysis using machine learning. Methods. 112, 201-210 (2017).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon