このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
制御された合成および均一性の高いポリの蛍光トラッキング(
要約
非撹拌沈殿重合は、狭いサイズ分布の刺激応答性ポリ(N -isopropylacrylamide)ミクロゲルの合成への迅速な、再現性のプロトタイピング手法を提供します。このプロトコル合成では、光散乱特性評価および広視野顕微鏡のセットアップでこれらのミクロゲルの単一粒子蛍光追跡が実証されています。
要約
刺激応答性ポリ(N -isopropylacrylamide)(PNIPAM)マイクロゲルは、様々な将来の実用的なアプリケーションを持っており、基礎研究に使用しています。本研究では、迅速な非撹拌沈殿重合法によってチューニングミクロゲルサイズのためのショーケースとしての蛍光標識したPNIPAMマイクロゲルを追跡する単一粒子を使用しています。このアプローチは、新しい反応組成物および条件を試作するため、または製品を大量に必要としないアプリケーションに適しています。動的および静的光散乱によってミクロゲル合成、粒子サイズ及び構造決意は、プロトコルに詳述されています。官能性コモノマーの添加は、粒子の核生成及び構造に大きな影響を持つことができることが示されています。広視野蛍光顕微鏡による単一粒子追跡を容易にすることによって調査されないシステム、非標識ミクロゲルの濃縮マトリックス中の標識トレーサーマイクロゲルの拡散の調査を可能にしますこのような動的光散乱などの他の方法。
概要
刺激応答性ポリ(N -isopropylacrylamide)(PNIPAM)マイクロゲル1,2は、さまざまなスマートアプリケーションでの電位に起因する過去20年間連続の関心を集めています。実証されたユースケースは、低分子量化合物と他の生物医学的用途の12のために切り替え可能なエマルジ ョン安定剤3-8、マイクロレンズ9、細胞培養簡単細胞収穫10,11のための基質、およびスマート担体を含みます。ビューの基礎研究の観点から、これらの粒子は、コロイドの相互作用13-15およびポリマー-溶媒相互作用16-18として被験体を調査するために有用であることが証明されています。
任意のアプリケーションでPNIPAMミクロゲルおよびそれらの誘導体の使用の成功は、典型的には、粒度分布の平均粒径と幅に関する知識を必要とします。 PNIPAMマイクロを含む実験結果の正しい解釈のためのゲルは、官能性コモノマーの影響を受けることができる粒子構造は、知らなければなりません。動的および静的光散乱(DLSそれぞれSLSは、)は、これらの方法は、高速で使用するのが比較的容易であるため、この情報を取得するための一意に適しています。そして彼らは彼らのネイティブ環境(分散)で非侵襲的に粒子特性を調べます。 DLSおよびSLSはまた、顕微鏡法のための典型的な小さなサンプルサイズから生じるバイアスを回避する粒子の膨大な数のデータを収集します。したがって、この研究の最初の目的は、コロイド特性評価への新たな実務家のための光散乱に関するグッドプラクティスを導入することです。
一般的に、沈殿重合は、実験室規模で行われ、特定の粒子特性のための右の反応条件を見出すことは面倒であると合成の多くの繰り返しを必要とすることができます。大きなバッチ合成とは対照的に、非撹拌沈殿重合19,20は、ARであります異なる反応体組成物のバッチは、狭いサイズ分布の粒子を得、同時に重合することができるAPID手順。同時重合実験変動を最小限にし、大きな出力が正しい反応条件は、反応をアップスケーリングするための高速見つけることができることを意味します。したがって、私たちの第二の目的は、プロトタイピングで、製品を大量に必要としないアプリケーションで非撹拌沈殿重合の有用性を実証することです。
合成と特性評価のさまざまな側面は、コロイドの相互作用の研究における蛍光標識されたPNIPAMマイクロゲルの応用例で一緒に来ます。ここでは、広いマトリックス濃度範囲にわたって非標識行列ミクロゲルの分散液中の標識トレーサーのミクロゲルの拡散を調査し、濃縮コロイド分散液中のケージの効果を解決するために、高精度の単一粒子追跡を使用します。広視野蛍光顕微鏡法は、FO適していますrをそれとして、この目的は、潜在的に異なるマトリックス種の多数の中から、いくつかのトレーサー分子の特定の動作を特徴づけることができます。これは、システムのアンサンブル平均特性を測定するため、大規模なシステムでは、プローブ粒子の数が少ないの問題を解決することができないようなDLS、SLSおよびレオロジーなどの技術とは対照的です。また、この具体例では、従来の光散乱法は、任意の標準的な分析を無効に強い多重散乱をもたらす高粒子濃度に起因利用することができません。自動データ処理及び統計的方法の使用は、大きなサンプルサイズにわたって平均単一粒子追跡のために、全体的なシステム挙動の分析を可能にします。
プロトコル
1.マイクロゲルの合成
注:N -isopropylacrylamide(NIPAM)をn-ヘキサンから再結晶しました。受信した他の試薬を使用しました。
- ポリ(NIPAM)マトリックスミクロゲルの従来のバッチ合成
- 濾過245 ml中に1.8グラムのNIPAMと24ミリグラムのN、N '-bisacrylamide(BIS)を溶解(0.2μmの再生セルロース(RC)メンブレンフィルター)還流冷却器を備えた500mlの三首丸底フラスコ中の蒸留水、撹拌機及びゴム隔膜。
- セプタムを通して窒素入力用の温度計と120ミリメートルの針を挿入します。
- 攪拌しながら、60℃に溶液を加熱します。 40分間窒素でパージすることにより溶液を脱酸素。
- 同時に酸素を除去するために二重蒸留水と気泡を窒素で溶液をろ過5ミリリットル中に155mgの過硫酸カリウム(KPS)の開始剤溶液を準備します。
- 完全な5ミリリットルKPS秒の転送120ミリメートル針を装備した、窒素洗浄シリンジ内olution。
- 三口フラスコ内の溶液レベル以上の窒素針を持ち上げて、反応器内にゴム隔膜を介して急速にKPSソリューションを追加します。
- 重合は60℃の窒素気流とゆっくり撹拌しながら1時間進行しましょう。
- 大きな凝集体を破棄するために、熱い反応液をフィルタリングするためにブフナー漏斗とろ紙を使用してください。分散がクールダウンするしてみましょう。
- 遠心分離し、257000×gで40分間分散を3回再分散し、最終的に二重蒸留水の最小実行可能な量の土砂を再分散。典型的には、この2-4 mlです。
- 保存するための分散液を凍結乾燥。
- 蛍光標識ポリ(NIPAM)ミクロゲルの非撹拌合成
- ガラス容器に257.7ミリグラムNIPAM、3.5 mgのBIS、および1.5ミリグラムメタクリルオキシエチルチオカルバモイルローダミンB(染料)を計量し、濾過し、二重にdistillの10ミリリットルを追加します。エド水。
- Ultrasonicate 15分間染料モノマー溶液を水に色素を溶解しました。
- 別のガラス容器に染料を含まない同じ溶液を調製します。
- 様々な染料濃度の濃度系列を得るために、染料なしにモノマー溶液を使用して染料とモノマー溶液の種々の希釈液を調製します。この作業では、0.02から0.1ミリモル/ Lの濃度範囲で染料を使用しています。
- 開始剤溶液を得るために蒸留水をろ過し10ミリリットル中8.4ミリグラムのKPSを溶解させます。
- 最終反応液を取得し、ゴム隔膜でそれらを密封するために、10mmの直径を有する管をテストするために濃度系列を0.5mlとKPS溶液0.5mlを転送します。
- 63℃に加熱サーキュレータに接続された二重壁ガラス容器に油浴を予熱。
- 20分間、120ミリメートルの針を介して窒素でパージすることにより反応液を酸素を除去します。
- AFにチューブを挿入しますプラットフォームをloatingし、予熱した油浴中にプラットフォームを浸します。 60℃に温度を設定します。室温ソリューションはバスをクールダウンとして浴中で最初は高い温度が必要です。高精度な粒径調整の初期反応時の温度制御は、典型的には0.1℃、±、厳密でなければなりません。
- 反応は、適切な時間で進行してみましょう。典型的には1時間で十分です。
- 60℃のオーブンに迅速に反応管に移しにDLSの特徴付けのために、PNIPAM体積相転移温度(VPTT、32 -34℃)で1上予熱蒸留水を濾過し10mlまで熱い分散液の一滴を置きます折り畳まれた状態。
- 分散液の残りは、室温まで冷却し、遠心分離管にそれらを転送してみましょう。
- 257000×gでソリューションを40分間、3回遠心分離し、再蒸留水foのフィルタリング2ミリリットルに最終的にマイクロゲルを希釈Rトレーサー粒子として使用します。
2.光散乱特性評価
- 動的光散乱による折り畳まれた状態での流体力学半径の決意
- キュベットを洗浄し、アセトン蒸気でガラス製品。
- 熱PNIPAM VPTT上で濾過( 例えば、200nm以下RCフィルタ)の二重蒸留水10ミリリットル。
- 予熱された針(0.9×40 mm)で、シリンジ(1 ml)を用いて濾過した水への熱い分散の低下を転送します。
- 50°CまでDLSゴニオメータインデックスマッチ浴を和らげるし、それがクールダウンさせることなく、機器にサンプルを移します。
- 散乱強度は、試験測定を行うことでコレを取得するのに十分である最大の散乱角を見つけます。
- 試料キュベット(粒子分散液1mLで直径10mmのガラス管)を挿入します。小さな散乱角(ここでは30°)に、検出器アームを移動します。
- foのビームプロファイルをチェックrの多重散乱: など一次ビーム、ノー多重散乱、周りのノーグローはカウント範囲が最も低い散乱角での測定に適していることを確認してください(約30〜600 kHzの間で、ソフトウェアのウィンドウの右上隅を。。)
- 最高の散乱角(ここでは120°を選択します)にゴニオメータアームを移動します。計数率は依然として(30と600 kHzの間)測定のために十分な大きさであることを確認してください。強度が低すぎる場合、散乱角下げるためにアームを移動させます。
- 最低の散乱角で視覚的にトルエン浴ガラスを通してビームを確認し、入射ビームの周りのグローが観察されている場合は、複数の散乱が起こります。この場合、レーザ強度を低下させるか、より高い希釈を使用します。
- 60秒の最小アクイジション時間で-最小と最大の散乱角(140° 例えば 、30°)との間に20相関曲線を取得します。弱い強度の大きな散乱角の取得時間を増やします必要であれば。
- データ解析37
- に従って散乱角のためのベクトルの大きさを散乱計算
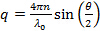 ここで、nは、分散液の屈折率であり、
ここで、nは、分散液の屈折率であり、 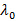 真空中でのレーザの波長と
真空中でのレーザの波長と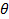 散乱角。
散乱角。 - ケースでは、測定ソフトウェアは、強度相関関数を提供します
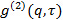 電界相関関数に変換します
電界相関関数に変換します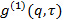 による
による 。パラメーター
。パラメーター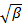 散乱光オベの空間コヒーレンスの程度に関連する興味のない楽器のパラメータであり、検出器領域rを。
散乱光オベの空間コヒーレンスの程度に関連する興味のない楽器のパラメータであり、検出器領域rを。 - コレログラムのキュムラント解析を行い、 すなわち 、それぞれの電界相関関数の対数に二次多項式にフィット
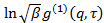 線形最小二乗によります。
線形最小二乗によります。 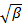 フィットの切片として表示され、その正確な値は、データ分析の点で重要ではありません。最大振幅の20% -の相関振幅が10になるように、 例えば 、意味の遅れ時間τ値に適合を制限します。一次の項の係数は、相関関数の平均減衰率であります
フィットの切片として表示され、その正確な値は、データ分析の点で重要ではありません。最大振幅の20% -の相関振幅が10になるように、 例えば 、意味の遅れ時間τ値に適合を制限します。一次の項の係数は、相関関数の平均減衰率であります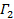 。
。 - 平均拡散係数のための最も可能性の高い値を探します
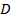 線形最小二乗することにより粒子の上にフィット
線形最小二乗することにより粒子の上にフィット 。もし
。もし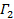 に対して
に対して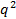 リニア表示され、誤差の範囲内で、原点を通過しない、粒度分布が広く、流体力学的半径が不十分に定義されますです。
リニア表示され、誤差の範囲内で、原点を通過しない、粒度分布が広く、流体力学的半径が不十分に定義されますです。 - ストークス - アインシュタインの関係から平均流体力学的半径を計算します
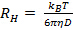 ここで、
ここで、 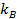 ボルツマン係数であり、
ボルツマン係数であり、 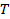 絶対温度と
絶対温度と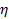 分散液の粘度に
分散液の粘度に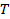 。の標準偏差を伝播
。の標準偏差を伝播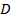 に
に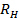 。
。
- に従って散乱角のためのベクトルの大きさを散乱計算
- 静的光散乱による粒子構造の決意
- キュベットを洗浄し、アセトン蒸気でガラス製品。シリンドリカルレンズの効果を最小にするために直径20mm以上のキュベットを使用します。
- フィルタ(200 nmのRCフィルタまたは小さい)ガラスバイアルに蒸留水の約20ミリリットルバイアルに精製された分散体の落下を転送します。製造プロセスから残存する不純物を除去するための試料調製のためにそれを使用する前に、10mlの水でフィルターを洗浄します。
- 任意の周囲の光源に対してサンプルを確認してください。青色の色相が観察された場合、サンプルも濃縮される可能性があります。それに応じて希釈します。
- キュベットを濾過し、水で複数回洗浄することにより、バックグラウンドの水のサンプルを準備した後、キュベット、機器内のレーザの位置に応じて、適切なサンプル容量に埋めます。レーザーは、メニスカスから屈折されずにサンプルを通過しなければなりません。
- instrumのキャリブレーションENTトルエンサンプルを使用。
- 利用可能な角度範囲全体にわたって水散乱(バックグラウンド)を測定します。
- 好ましくは、いくつかの波長で利用可能な角度範囲にわたって試料からの散乱強度を測定します。前方散乱強度に正規化散乱パターンは、フォームファクタとして知られています。
- 粒子構造が知られている場合、異なる波長で測定されたデータセット上のグローバルフィットを計算するために、適切なモデル式を使用します。
- (などFitIt!33)直接正則未知の粒子構造の使用、または、より一般的な間接的逆フーリエ変換のための粒子のおおよその分類(のみ球状粒子の場合)対距離分布関数の逆畳み込み23,24に関連して21,22ルーチンを変換タイプ。
- 場合フィッティングまたは反転ルーチンが多分散を計算し、粒子径分布関数の推定値を提供しますインデックス(その平均値で割った分布の標準偏差)。
広視野蛍光顕微鏡による3粒子追跡
注:20℃で465±7 nmおよび405±7nmで流体力学的半径のトレーサーとマトリックス粒子が、それぞれ、粒子追跡のために使用しました。
- 試料調製
- 二重蒸留水の既知量に凍結乾燥標識されていないミクロゲルの既知量を再分散することによって濃縮された行列のミクロゲル分散液を準備します。標識トレーサー粒子の小さな体積を追加します。
- 顕微鏡における適切なトレーサーミクロゲル濃度を確認してください。トレーサー粒子トラックが取得中に交差確率が無視できるように十分に低いトレーサ濃度を有しながら、最適な濃度は、トラックの最大数の同時取得の間の妥協です。
- 蒸発させて濃縮された分散液を調製オーブン内の水。蒸発前の試料の元の重量に分散体の重量を比較することにより、重量濃度を決定します。
- データ収集と分析
- サンプルからのトレーサーと同時蛍光コレクションの励起に所望の倍率と絞りの適切な対物レンズを使用してください。この作業では、100X / 1.3 NA油浸対物レンズを使用しています。
- 商業顕微鏡に収まるのxyzピエゾテーブル上に水分室を置きます。
- 乾燥からサンプルを防ぐために、スリップ上に所望の濃度の水分室及びポリ(NIPAM)のピペット10μlの分散にプラズマ洗浄カバースリップを配置。
- 蛍光色素の励起および発光スペクトルに応じて、励起のために適切なレーザーを使用し、適切にレーザーパワーを調整します。強度は、染料の速い光退色を避けるために十分に低いことが、でなければなりません正確な単一粒子の位置決めのために十分に強い、同じ時間(下記参照)。本研究では、561 nmのダイオード励起固体レーザーを使用し、すべての測定のために16ミリワット( 約 0.5キロワットcm -2のサンプルで)でレーザパワーを一定に保ちます。
- 均質なサンプル照明を得るために、ここで説明するクリティカル照明のセットアップを使用します。このために、カップルは、マルチモードファイバにレーザー(NA 0.22±0.02、0.6ミリメートルのコア径)は、順番にに出て、時間的に平均レーザースペックルをボルテクサーを用いた繊維を振ると、繊維が試料面に終了突出しています。
- カバースリップの後方反射からのz距離を校正し、わずかに目標を移動することにより、試料中に数マイクロメートルの焦点を合わせるとz補償器を使用して、z位置を固定します。これは、カバーガラスとの任意のインターフェイスの影響を回避することができます。
- 蛍光シグナルの強度を、そのような露出時間として検出パラメータを調整します。この場合、EMCCDカメラを使用0.1秒の露光時間で、電子がモード50のゲインを乗じます。
- サンプルの異なる領域にマイクロゲルの平均二乗変位を計算するために十分な遅延時間を得るために、フレームの適切な数を持ついくつかの映画を取得します。本研究では、500または千フレームの取得フレーム番号を使用します。
- ガウシアンフィッティング25を用いて、各フレーム中の粒子を配置することによって、データを分析し、平均二乗変位を得るために適切な粒子追跡アルゴリズム26を使用しています。27の計算すべての映画の中ですべてのトラックを平均することにより値と標準偏差を意味します。から線形回帰によって長い遅延時間拡散係数を計算します
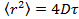 ここで、
ここで、 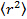 平均二乗変位、D平均拡散係数であり、遅れ時間をτ。
平均二乗変位、D平均拡散係数であり、遅れ時間をτ。 - EST(東部基準時異常拡散方程式から異常パラメータγを iMateの
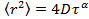 対数スケールにデータを変換することによって、得
対数スケールにデータを変換することによって、得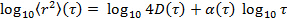 。異常パラメータ
。異常パラメータ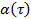 プロットの微分で与えられます。誘導体は、データ点の有限差分によって推定、または多項式関数によってデータ点を適合し、分析的に分化することができます。多項式の次数を増加させるためのフィット残差と残差ノルムをプロットすることにより多項式フィット機能の十分な程度を決定します。
プロットの微分で与えられます。誘導体は、データ点の有限差分によって推定、または多項式関数によってデータ点を適合し、分析的に分化することができます。多項式の次数を増加させるためのフィット残差と残差ノルムをプロットすることにより多項式フィット機能の十分な程度を決定します。 - マイクロゲルマトリックスの異なる濃度に対して同じ手順を繰り返します。
結果
バッチ内PNIPAMミクロゲル粒子の数、および、最終的な粒子の体積は、チオカルバモイルローダミンBは、バッチ内の粒子数密度を減少させることによって、核形成に影響を与える核形成段階20疎水性コモノマー色素メタクリロキシエチル中に早期反応で決定されます。二つの異なる初期NIPAM濃度について粒子濃度の?...
ディスカッション
官能性コモノマーの少量の添加は、PNIPAMミクロゲル由来の粒子サイズおよび構造に大きな影響を持つことができます。同時小規模試験管重合は、このような変化を考慮するための良い方法であり、急速に必要に応じて反応をアップスケーリングするための目標粒径のための右の反応組成物を見つけるのに役立ちます。粒子の質量?...
開示事項
The authors have nothing to disclose.
謝辞
The Deutsche Forschungsgemeinschaft (DFG) is acknowledged for financial support within the Sonderforschungsbereich SFB 985 "Functional Microgels and Microgel Systems".
資料
| Name | Company | Catalog Number | Comments |
| Acetone | VWR Chemicals | KRAF13455 | |
| Bisacrylamid | AppliChem | A3636 | |
| n-Hexane | Merck | 104374 | |
| N-Isopropylacrylamide | Fisher Scientific | AC412785000 | recrystallized from n-hexane |
| Methacryloxyethyl thiocarbamoyl rhodamine B | Polysciences | 23591 | |
| Potassium peroxodisulfate | Merck | 105091 | |
| Silicone oil 47 V 350 | VWR Chemicals | 83851 | |
| Toluene | Sigma Aldrich | 244511 | |
| F12 Refrigerated/heating circulator | Julabo | 9116612 | |
| Microscope | Olympus | IX83 | |
| XY(Z) Piezo System | Physik Instrumente | P-545.3R7 | |
| 100X Oil immersion objective | Olympus | UPLSAPO | |
| QuadLine Beamsplitter | AHF Analysentechnik | F68-556T | |
| Cobolt Jive 150 laser | Cobolt | 0561-04-01-0150-300 | |
| Multimode Fiber | Thorlabs | UM22-600 | |
| iXON Ultra 897 EMCCD camera | Andor | DU-897U-CS0-BV | |
| Laser goniometer | SLS Systemtechnik | Mark III | |
| CF40 Cryo-compact circulator | Julabo | 9400340 | |
| Laser goniometer system | ALV GmbH | ALV / CGS-8F | |
| Multi-tau corretator | ALV GmbH | ALV-7004 | |
| Light scattering electronics | ALV GmbH | ALV / LSE 5004 | |
| Photon counting module | PerkinElmer | SPCM-CD2969 | 2 units in pseudo cross-correlation mode |
| 633 nm HeNe Laser | JDS Uniphase | 1145P | |
| F32 Refrigerated/heating circulator | Julabo | 9312632 |
参考文献
- Pelton, R. Temperature-sensitive aqueous microgels. Adv. Colloid Interfac. 85, 1-33 (2000).
- Pich, A., Richtering, W. Microgels by Precipitation Polymerization: Synthesis, Characterization and Functionalization. Adv. Polym. Sci. 234, 1-37 (2010).
- Richtering, W. Responsive Emulsions Stabilized by Stimuli-Sensitive Microgels: Emulsions with Special Non-Pickering Properties. Langmuir. 28 (50), 17218-17229 (2012).
- Wiese, S., Spiess, A. C., Richtering, W. Microgel-Stabilized Smart Emulsions for Biocatalysis. Angew. Chem. Int. Edit. 52 (2), 576-579 (2012).
- Schmitt, V., Ravaine, V. Surface compaction versus stretching in Pickering emulsions stabilised by microgels. Curr. Opin. Colloid In. 18 (6), 532-541 (2013).
- Wellert, S., Richter, M., Hellweg, T., von Klitzing, ., R, Y., Hertle, Responsive Microgels at Surfaces and Interfaces. Z. Phys. Chem. 229 (7-8), 1-26 (2015).
- Li, Z., Harbottle, D., Pensini, E., Ngai, T., Richtering, W., Xu, Z. Fundamental Study of Emulsions Stabilized by Soft and Rigid Particles. Langmuir. 31 (23), 6282-6288 (2015).
- Deshmukh, O. S., van den Ende, D., Stuart, M. C., Mugele, F., Duits, M. H. G. Hard and soft colloids at fluid interfaces: Adsorption, interactions, assembly & rheology. Adv. Colloid Interfac. 222, 215-227 (2015).
- Serpe, M. J., Kim, J., Lyon, L. A. Colloidal Hydrogel Microlenses. Adv. Mater. 16 (2), 184-187 (2004).
- Schmidt, S., Zeiser, M., Hellweg, T., Duschl, C., Fery, A., Möhwald, H. Adhesion and Mechanical Properties of PNIPAM Microgel Films and Their Potential Use as Switchable Cell Culture Substrates. Adv. Func. Mater. 20 (19), 3235-3243 (2010).
- Xia, Y., He, X., et al. Thermoresponsive Microgel Films for Harvesting Cells and Cell Sheets. Biomacromolecules. 14 (10), 3615-3625 (2013).
- Guan, Y., Zhang, Y. PNIPAM microgels for biomedical applications: from dispersed particles to 3D assemblies. Soft Matter. 7 (14), 6375 (2011).
- Yunker, P. J., Chen, K., Gratale, M. D., Lohr, M. A., Still, T., Yodh, A. G. Physics in ordered and disordered colloidal matter composed of poly(N-isopropylacrylamide) microgel particles. Rep. Prog. Phys. 77 (5), 056601-056629 (2014).
- Lohr, M. A., Still, T., et al. Vibrational and structural signatures of the crossover between dense glassy and sparse gel-like attractive colloidal packings. Phys. Rev. E. 90 (6), 062305 (2014).
- Dreyfus, R., Xu, Y., Still, T., Hough, L. A., Yodh, A. G., Torquato, S. Diagnosing hyperuniformity in two-dimensional, disordered, jammed packings of soft spheres. Phys. Rev. E. 91 (1), 012302-012312 (2015).
- Kojima, H., Tanaka, F. Reentrant volume phase transition of cross-linked poly(N-isopropylacrylamide) gels in mixed solvents of water/methanol. Soft Matter. 8 (10), 3010-3011 (2012).
- Hofmann, C. H., Plamper, F. A., Scherzinger, C., Hietala, S., Richtering, W. Cononsolvency Revisited: Solvent Entrapment by N-Isopropylacrylamide and N, N-Diethylacrylamide Microgels in Different Water/Methanol Mixtures. Macromolecules. 46 (2), 523-532 (2013).
- Bischofberger, I., Calzolari, D. C. E., Trappe, V. Co-nonsolvency of PNiPAM at the transition between solvation mechanisms. Soft Matter. 10 (41), 8288-8295 (2014).
- Virtanen, O. L. J., Richtering, W. Kinetics and particle size control in non-stirred precipitation polymerization of N-isopropylacrylamide. Colloid Polym. Sci. 292 (8), 1743-1756 (2014).
- Virtanen, O. L. J., Ala-Mutka, H. M., Richtering, W. Can the Reaction Mechanism of Radical Solution Polymerization Explain the Microgel Final Particle Volume in Precipitation Polymerization of N-Isopropylacrylamide?. Macromol. Chem. Phys. 216 (13), 1431-1440 (2015).
- Glatter, O. A new method for the evaluation of small-angle scattering data. J. Appl. Crystallogr. 10 (5), 415-421 (1977).
- Svergun, D. I. Determination of the regularization parameter in indirect-transform methods using perceptual criteria. J. Appl. Crystallogr. 25 (4), 495-503 (1992).
- Glatter, O. Convolution Square Root of Band-Limited Symmetrical Functions and Its Application to Small-Angle Scattering Data. J. Appl. Crystallogr. 14, 101-108 (1981).
- Glatter, O., Hainisch, B. Improvements in Real-Space Deconvolution of Small-Angle Scattering Data. J. Appl. Crystallogr. 17, 435-441 (1984).
- Cheezum, M. K., Walker, W. F., Guilford, W. H. Quantitative Comparison of Algorithms for Tracking Single Fluorescent Particles. Biophys. J. 81 (4), 2378-2388 (2001).
- Wöll, D., Kölbl, C., Stempfle, B., Karrenbauer, A. A novel method for automatic single molecule tracking of blinking molecules at low intensities. Phys. Chem. Chem. Phys. 15 (17), 6196-6205 (2013).
- Saxton, M. J., Jacobson, K. Single-particle tracking: Applications to membrane dynamics. Annu. Rev. Bioph. Biom. 26, 373-399 (1997).
- Pusey, P. N., van Megen, W. Detection of small polydispersities by photon correlation spectroscopy. J. Chem. Phys. 80 (8), 3513 (1984).
- Stieger, M., Pedersen, J. S., Richtering, W., Lindner, P. Small-angle neutron scattering study of structural changes in temperature sensitive microgel colloids. J. Chem. Phys. 120 (13), 6197-6206 (2004).
- Wu, X., Pelton, R. H., Hamielec, A. E., Woods, D. R., McPhee, W. The kinetics of poly(N-isopropylacrylamide) microgel latex formation. Colloid Polym. Sci. 272, 467-477 (1994).
- Weeks, E. R., Weitz, D. A. Subdiffusion and the cage effect studied near the colloidal glass transition. Chem. Phys. 284 (1-2), 361-367 (2002).
- Ernst, D., Köhler, J., Weiss, M. Probing the type of anomalous diffusion with single-particle tracking. Phys. Chem. Chem. Phys. 16 (17), 7686-7691 (2014).
- . FitIt! (Version 1.1.4) Available from: https://www.github.com/ovirtanen/fitit (2015)
- Provencher, S. W. A Constrained Regularization Method For Inverting Data Represented By A Linear Algebraic or Integral Equations. Comput. Phys. Commun. 27 (3), 213-227 (1982).
- Holtzer, L., Meckel, T., Schmidt, T. Nanometric three-dimensional tracking of individual quantum dots in cells. Appl. Phys. Lett. 90 (5), 053902-053904 (2007).
- Diezmann, A. V., Lee, M. Y., Lew, M. D., Moerner, W. E. Correcting field-dependent aberrations with nanoscale accuracy in three-dimensional single-molecule localization microscopy. Optica. 2 (11), 985-989 (2015).
- Lindner, P., Zemb, T. . Neutrons, X-rays and Light: Scattering Methods Applied to Soft Condensed Matter. , (2002).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved