このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
虚血および非閉塞性冠動脈疾患(INOCA)患者における連続熱希釈による絶対心筋の流れと抵抗の定量化
要約
ここに提示されるのは、虚血および非閉塞性冠動脈疾患の患者において、連続的な熱希釈を使用して絶対的な心筋の流れと抵抗を測定するためのプロトコルです。
要約
狭心症または虚血性心疾患の徴候や症状のために冠動脈造影を受けている患者の約半数では、閉塞性冠動脈疾患は血管造影的に見えません。狭心症または虚血があり、閉塞性冠動脈疾患 (INOCA) を伴わないこれらの患者の大多数は、基礎的な冠動脈血管運動障害を持っており、現在のコンセンサス ドキュメントでは、診断的侵襲性冠動脈血管運動機能検査 (CFT) を推奨しています。
CFTでは、血管痙攣性冠動脈機能障害(心外膜または微小血管痙攣)、および/または血管拡張能力の障害や微小血管抵抗の増加などの微小血管血管拡張機能障害など、さまざまな血管運動機能障害のエンドタイプを評価できます。連続的な熱希釈から導き出された絶対冠動脈血流と抵抗の定量化は、現在使用されている標準的な生理学的測定と比較してより良い尺度になる可能性があります。この記事では、この連続熱希釈法の概要を説明します。
概要
狭心症または虚血性心疾患の徴候や症状のために冠動脈造影を受けている患者の約半数では、閉塞性冠動脈疾患は血管造影的に見えません1。狭心症または虚血があり、閉塞性冠動脈疾患 (INOCA) を伴わないこれらの患者の大多数は、基礎的な冠動脈運動障害を持っており、現在の ESC ガイドラインと INOCA に関する最近の ESC ポジション ペーパーでは、診断的侵襲性冠動脈血管運動機能検査 (CFT) 1,2 を推奨しています。
CFTでは、血管痙攣性冠動脈機能障害(心外膜または微小血管痙攣)、および/または血管拡張能力の障害や微小血管抵抗の増加などの微小血管血管拡張機能障害など、さまざまな血管運動機能障害のエンドタイプを評価できます。これらのエンドタイプのコンセンサス基準は、冠状動脈血管運動障害国際研究グループ(COVADIS)3,4によって定義されています。
血管痙攣性冠動脈機能障害は一般にアセチルコリン誘発試験によって示されますが、微小血管血管拡張性機能障害の診断はより複雑です。この診断は、微小血管抵抗 (IMR) および/または冠動脈血流予備能 (CFR) の異常な指標によって行われます4。
IMRまたはCFRの測定には、熱希釈またはドップラー流速の2つの方法があります。どちらもアデノシンの静脈内投与を使用して最大の充血を誘発し(したがって耐性を最小限に抑えます)、どちらの方法も広く検証されています。しかし、それらにはいくつかの重要な欠点があります:アデノシンの必要性は、重度の慢性閉塞性肺疾患または喘息の患者での使用を制限します。また、熱希釈法はCFRを過大評価し、観察者内変動が大きい場合があり、ドップラー流速法では安定したドップラー流量信号を得ることが困難となる場合がある5。最も重要なことは、CFRとIMRはどちらも代理的な手段にすぎず、真の冠動脈血流と抵抗を定量化できないということです。
絶対冠動脈血流 (Q) と抵抗 (R) は、最近検証された新しい方法を使用して直接定量化できます 室温での冠動脈内生理食塩水注入による連続熱希釈を使用して充血を誘発します。専用のモノレール輸液カテーテルと温度センサー付き圧力ワイヤーにより、アデノシンを使用せずにQとRを直接定量化できます。この新しい方法は、安全で再現性が高く、オペレーターに依存しないことが示されています6,7。
最近のコンセンサスステートメントによって促されているように、さまざまなエンドタイプ1にわたって、INOCA患者における心筋虚血の根本的なメカニズムをよりよく理解する必要があります。これは、治療と予後に大きな影響を与える可能性があります。絶対的な冠状動脈血流と抵抗の定量化は、現在使用されている標準的な生理学的手段と比較して、より優れた尺度になる可能性があります。最近、連続的な熱希釈測定がINOCAの症状と関連しているのに対し、IMRとCFRは関連していないことが示されました8。追加の結果データが続きます。この記事では、連続熱希釈プロトコルについて説明します。
プロトコル
次のプロトコルは、オランダのナイメーヘンにあるラドバウドゥム病院の地元の医療倫理委員会によって承認されました。絶対流量と絶対抵抗を計算するために連続的な熱希釈を実行する場合は、次の手順に従う必要があります。
1. 事前準備
- 血管作用薬を少なくとも24時間(カルシウムチャネル遮断薬の場合は48時間)差し控えます。.
2. 診断用冠動脈造影
- 局所麻酔(1〜2 mLの20 mg / mLリドカイン)を右橈骨動脈または左橈骨動脈の近くに注入します。.橈骨アクセスが不可能な場合は、右大腿動脈(通常は10 mLのリドカイン)または左大腿動脈の近くに局所麻酔を注入します。.
- 麻酔をかけた皮膚に針を刺して局所麻酔を確認し、痛みが残っているかどうかを確認します。
- 橈骨動脈または大腿動脈をカニューレで穿刺し、カニューレを通してワイヤーを挿入して取り外します。ワイヤーの上に6Frシースを挿入します。これは必ず無菌条件下で行ってください。
- 地域のプロトコルに従ってヘパリンを投与します (患者の体重調整済み 100 国際単位/キログラム、最小 5000 国際単位、最大 10.000 国際単位)。
- ワイヤーをシースを通して上行大動脈まで進め、診断カテーテルを大動脈弁の上に配置します。次に、ワイヤーを取り外し、カテーテルを造影剤シリンジに接続します。
- 診断用カテーテルで右の冠状動脈を噛み合わせます。0.2 mgのニトログリセリンの冠動脈内投与後、造影剤の手動注射で冠動脈造影を行います。
- 左冠状動脈をガイディングカテーテルでかみ合わせます(後で診断からガイディングに切り替えないようにするため)。0.2mgのニトログリセリンの冠動脈内投与後、造影剤の手動注射で冠動脈造影を行う。専用のモノレールカテーテルを容易にするために、6Frサイズ以上のガイディングカテーテルを使用してください(ステップ4)。
- 閉塞性冠動脈疾患の存在を除外します: 関連する心外膜狭窄症 視覚的評価、および中間心外膜狭窄症 (40-90% 血管造影狭 窄症) 9.
3. 連続熱希釈測定のセットアップ
- すべての冠動脈圧力トレースと温度がワイヤレスで送信され、QとRを自動的に計算するソフトウェアを備えた専用コンソールによって分析されることを確認します。
- 室温で100〜150mLの生理食塩水を含む圧力限界の造影剤インジェクターを準備します。
4. 連続的な熱希釈の測定
- 生理食塩水入りのシリンジを使用して、圧力センサーと温度センサー(さらに「圧力ワイヤー」と呼ばれる)を備えたガイドワイヤーを手動で洗い流します。
- 圧力ワイヤーが適切なソフトウェアに接続されていることを確認し(圧力/温度がリアルタイムで視覚化されるように)、圧力ワイヤーをガイディングカテーテルに通します。血管造影を使用して、圧力ワイヤーのX線不透過性セクションの近位部分が冠状動脈の口に配置されていることを確認します。
- 圧力ワイヤーを大動脈圧に均等化します。このステップは、測定を開始する前に完了していることが不可欠です。
- 圧力ワイヤーを目的の冠状動脈の遠位1/3まで進めます。
- 造影剤インジェクターに専用のモノレールカテーテルを接続します。
- 10 mL/分に設定された自動造影剤インジェクターを使用してモノレールカテーテルを生理食塩水で洗い流し、モノレールカテーテルから空気を取り除きます。生理食塩水がモノレールカテーテルの先端にある注入穴から出たら、フラッシングしながらモノレールカテーテルをガイディングカテーテルを通して進めます。
- モノレールカテーテルが止血コネクタを通過したら、フラッシングを停止し、モノレールカテーテルをガイディングカテーテルにさらに進めます。
- モノレールカテーテルのX線不透過性マーカーを、目的の冠状動脈の近位部分(最初のセンチメートル)に配置します。
注:血液と生理食塩水10,11の最適な混合を確保するために、近位に配置されたモノレールカテーテルのX線不透過性マーカーと遠位に配置されたガイドワイヤーのX線不透過性マーカーとの間に少なくとも3cmの距離があることを確認してください。 - 専用ソフトウェアで、 アブソリュートフロー プログラムを選択し、目的の冠状動脈を選択し、温度をゼロに設定します(人間の37°Cに匹敵する基準温度)。
- 輸液ポンプで(室温)生理食塩水(Qi)の適切な注入速度を選択し、それに応じてプログラム設定が更新されていることを確認します。
注:Qiは通常、左前下行(LAD)および左回旋動脈(LCX)で20 mL / min、右冠状動脈(RCA)で15 mL / minです。まだ注入を開始しないでください。 - 専用ソフトウェアプログラムで絶対流量測定を開始します。ステップ4.16まで測定を停止しないでください。生理食塩水の注入が開始される前に、数秒が測定されていることを確認してください。
- 選択した流量(Qi)で輸液ポンプで生理食塩水の注入を開始します。ステップ4.15まで注入を停止しないでください。.
注:生理食塩水の注入開始後、遠位冠状動脈の温度は低下します。 - 血液/生理食塩水混合物の定常状態の遠位温度が少なくとも10秒間記録されていることを確認してください。.
- ガイドワイヤーをモノレール輸液カテーテルに引き戻して、近位温度(Ti)を取得します。安定したTiが約10秒間記録されていることを確認します。
- 輸液ポンプへの室温生理食塩水の注入を停止します。
- 温度がゼロになった値に戻ることを確認します。この後、専用のソフトウェアプログラムで絶対流量測定を停止します。
注:FFR、絶対Q、およびRは、専用ソフトウェアによって自動的に計算されるようになりました。 - 専用のモノレールカテーテルを取り外します。
- ステップ4.2と同様に、圧力ワイヤーが冠状動脈の口に配置されていることを確認し、圧力測定のドリフトチェックを実行します。ドリフトが2mmHgを超える場合は、測定を繰り返してください。ドリフトがない場合は、圧力ワイヤーを取り外します。
- 目的の冠状動脈を視覚化する最終的な血管造影を 1 回または 2 回実施して、合併症の可能性 (冠動脈解離など) を確認します。
5.絶対流量と絶対抵抗の計算
注: 図1に示すように、専用のモノレール注入カテーテルは、4つの外側の穴からのみ生理食塩水を注入できるため、血液との完全かつ最適な混合が得られます。内側の2つの穴により、使用済みのガイドワイヤーで温度を測定できます。
- 絶対流量(Q)をmL/分で計算するには、次の式7を使用します。
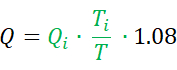
前述のように、Qiは生理食塩水の注入速度(mL/分)であり、Tiは専用のモノレールカテーテル出口付近の注入された生理食塩水の温度です。Tは、注入中の冠状動脈の遠位部における血液と生理食塩水の均質な混合物の温度です。定数1.08は、血液と生理食塩水の比温度と密度の差、および生理食塩水が血液に注入されるタイミングに関連しています。 - 木材単位(WU)またはmmHg *(L / min)で表されるRを次の式で計算します。
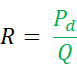
生理学的指標を測定するための高度なプラットフォームがすぐに利用でき、圧力ワイヤーと通信し、FFR、Q、R(Table of Materials)のライブ計算が可能です。
結果
図2は、冠動脈造影で閉塞性CADがない患者Aで行われた代表的な測定を示しています。LAD動脈は、絶対QとRを計算するために、連続的な熱希釈を使用して測定されました。赤と緑の線は圧力測定値を表し、青い線は温度曲線を表します。LAD動脈を測定して以来、注入速度は20mL/min(Qi)に設定しました。ポイント1で注入が開始され、遠位に配置された?...
ディスカッション
連続的な熱希釈は、絶対的な冠動脈の流れと抵抗を測定するための正確な方法であり、ゴールドスタンダード[15O2]H2O PET由来の流量と抵抗5と強く一致することが示されています。これらの測定値は INOCA 患者にとって特に興味深いものであり、現在の臨床ガイドラインでは、このグループの冠状動脈の流れと抵抗の評価が推奨...
開示事項
ピーター・ダマンは、フィリップス・アンド・アボット・ヴァスキュラーから講義料および/またはコンサルタント料を受け取りました。
謝辞
何一つ。
資料
| Name | Company | Catalog Number | Comments |
| Rayflow multipurpose infusion catheter | Hexacath | RFW61S | Only compatible with 6F guiding catheter |
| PressureWire X guidewire | Abbott | C12059 | Wireless guidewire with distal temperature and pressure sensor |
| Coroventis CoroFlow Cardiovascular System software | Coroventis | N/A | Advanced platform to measure physiological indices |
| Illumena Neo injector or similar injector system | Liebel-Flarsheim | GU01181006-E | Any injector with pressure limit (600 psi) and adjustable flow and volume injection rate |
| 100 ml NaCl 0.9% at room temperature |
参考文献
- Kunadian, V., et al. An EAPCI Expert Consensus Document on Ischaemia with Non-Obstructive Coronary Arteries in Collaboration with European Society of Cardiology Working Group on Coronary Pathophysiology & Microcirculation Endorsed by Coronary Vasomotor Disorders International Study Group. European Heart Journal. 41 (37), 3504-3520 (2020).
- Knuuti, J., et al. ESC Guidelines for the diagnosis and management of chronic coronary syndromes. European Heart Journal. 41 (3), 407-477 (2020).
- Beltrame, J. F., et al. International standardization of diagnostic criteria for vasospastic angina. European Heart Journal. 38 (33), 2565-2568 (2017).
- Ong, P., et al. International standardization of diagnostic criteria for microvascular angina. International Journal of Cardiology. 250, 16-20 (2018).
- Everaars, H., et al. Continuous thermodilution to assess absolute flow and microvascular resistance: validation in humans using [15O]H2O positron emission tomography. European Heart Journal. 40 (28), 2350-2359 (2019).
- Konstantinou, K., et al. Absolute microvascular resistance by continuous thermodilution predicts microvascular dysfunction after ST-elevation myocardial infarction. International Journal of Cardiology. 319, 7-13 (2020).
- Xaplanteris, P., et al. Catheter-Based Measurements of Absolute Coronary Blood Flow and Microvascular Resistance: Feasibility, Safety, and Reproducibility in Humans. Circulation Cardiovascular Interventions. 11 (3), 006194 (2018).
- Konst, R. E., et al. Absolute Coronary Blood Flow Measured by Continuous Thermodilution in Patients With Ischemia and Nonobstructive Disease. Journal of the American College of Cardiology. 77 (6), 728-741 (2021).
- Neumann, F. J., et al. ESC/EACTS Guidelines on myocardial revascularization. European Heart Journal. 40 (2), 87-165 (2019).
- Aarnoudse, W., et al. Direct volumetric blood flow measurement in coronary arteries by thermodilution. Journalof the American College of Cardiology. 50 (24), 2294-2304 (2007).
- van't Veer, M., et al. Novel monorail infusion catheter for volumetric coronary blood flow measurement in humans: in vitro validation. EuroIntervention: Journal of EuroPCR in collaboration with the Working Group on Interventional Cardiology of the European Society of Cardiology. 12 (6), 701-707 (2016).
- Fournier, S., et al. Normal Values of Thermodilution-Derived Absolute Coronary Blood Flow and Microvascular Resistance in Humans. EuroIntervention: Journal of EuroPCR in collaboration with the Working Group on Interventional Cardiology of the European Society of Cardiology. , (2020).
- Keulards, D. C. J., et al. Safety of Absolute Coronary Flow And Microvascular Resistance Measurements by Thermodilution. EuroIntervention: Journal of EuroPCR in collaboration with the Working Group on Interventional Cardiology of the European Society of Cardiology. , (2020).
- Konijnenberg, L. S. F., et al. Pathophysiology and diagnosis of coronary microvascular dysfunction in ST-elevation myocardial infarction. Cardiovascular Research. 116 (4), 787-805 (2020).
- Wijnbergen, I., van't Veer, M., Lammers, J., Ubachs, J., Pijls, N. H. Absolute coronary blood flow measurement and microvascular resistance in ST-elevation myocardial infarction in the acute and subacute phase. Cardiovascular Revascularization Medicine: including Molecular Interventions. 17 (2), 81-87 (2016).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved