このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
マウスにおける急性骨髄性白血病発症のための腹腔内移植
要約
ここでは、白血病細胞の腹腔内注射を利用して、マウスの急性骨髄性白血病(AML)を確立し、増殖させます。この新しい方法は、AML細胞の連続移植に効果的であり、マウスへの静脈内注射で困難や矛盾を経験する可能性のある人の代替手段として役立ちます。
要約
急性骨髄性白血病(AML)および持続性白血病幹細胞(LSC)を含む関連する再発を治療するための新しい治療法の満たされていないニーズがあります。レシピエントマウスへの眼窩後注射によるこれらの細胞の移植の成功に基づく治療法をテストするための実験的なAMLげっ歯類モデルは、課題に満ちています。この研究の目的は、腹腔内経路を使用してAMLの堅牢なマウスモデルを生成するための簡単で信頼性が高く、一貫した方法を開発することでした。本プロトコールでは、骨髄細胞を、ヒトMLL−AF9融合癌タンパク質を発現するレトロウイルスで形質導入した。原発性AMLの発症におけるドナーLSCとしての系統陰性(Lin-)およびLin-Sca-1+c-Kit+(LSK)集団の効率が検証され、AMLを生成する新しい方法として腹腔内注射が採用されました。腹腔内注射と眼窩後注射の比較は、2つの方法を比較対照するために連続移植で行われました。ヒトMLL-AF9ウイルスで形質導入されたLin細胞とLSK細胞の両方が、レシピエントの骨髄と脾臓によく生着し、本格的なAMLを引き起こしました。ドナー細胞の腹腔内注射は、連続移植時にレシピエントにAMLを確立し、AML細胞の浸潤は、フローサイトメトリー、qPCR、および組織学的分析によってレシピエントの血液、骨髄、脾臓、および肝臓で検出されました。したがって、腹腔内注射は、ドナー白血病細胞の連続移植を用いたAML誘導の効率的な方法です。
概要
急性骨髄性白血病(AML)は、予後不良の多様な病因の血液悪性腫瘍の一種です1。AML動物モデルの生成は、その複雑な変異と病理生物学を理解するための基礎を築き、新しい治療法を発見します2。マウスの白血病発生は、AMLを強力に誘導する混合系統白血病(MLL)遺伝子を含む融合癌タンパク質を発現するドナー細胞を移植して、ヒトの疾患を模倣することを含みます3。MLL遺伝子関連AML4の移植では、ドナー細胞の様々な細胞起源が報告されており、疾患起源の原因となる細胞についてはほとんど知られていない。
マウスへの移植のために複数の経路が開発されている。変異ドナー細胞を骨髄5に直接導入する大腿骨内注射ではなく、静脈副鼻腔神経叢、尾静脈、頸静脈を利用する静脈内注射がマウスAMLモデル6、7、8、9の作製に広く用いられている。眼窩後方(r.o.)注射の場合、体積制限、高い技術的要求、繰り返しの試行またはエラーの可能性の少なさ、潜在的な眼の損傷など、さまざまな固有の欠点が大きな障害であり、実行可能な代替手段が限られているか、まったくありません7。尾静脈注射は、局所的な怪我以外にも同様の問題を引き起こす可能性があります。手順を容易にするために、マウスはしばしば尾静脈を拡張するためにウォームアップする必要があります10。また、特にC57BL/6系統のマウスでは、追加の光源なしで尾静脈を見つけることは困難です。頸静脈注射の場合、研究担当者は静脈を特定し、起こりうる合併症を制限するために十分なトレーニングを必要とします。さらに、静脈洞と頸静脈の両方の注射を麻酔下で行う必要があり、これは別のレベルの複雑さを追加します。したがって、AMLマウスモデルの確立を促進するために、移植の新しいルートを模索するのは魅力的です。
腹腔内(i.p.)注射は、薬物、染料、および麻酔薬の投与に一般的に使用されます11、12、13、14、15;また、異所性造血のための造血細胞の導入16や、骨髄由来間葉系幹細胞の移植にも使用されています17、18、19、20、21。しかし、マウスの造血器悪性腫瘍の確立、特にAML疾患の進行を研究するためにめったに使用されていません。
本研究では、ドナー細胞としての系統陰性(Lin-)およびLin-Sca-1+c-Kit+(LSK)集団の移植効率を比較することに加えて、AMLマウスモデルの生成におけるi.p.注射の実現可能性について説明します。これらの知見は、AMLおよび関連する骨髄性白血病の実験モデルを簡単かつ効率的に生成する方法を提供する。このような方法は、疾患メカニズムの理解を深めるだけでなく、実験的治療法をテストするための比較的簡単なモデルを提供する可能性があります。
プロトコル
すべての実験は、ペンシルベニア州立大学の施設内動物管理および使用委員会によって事前に承認されました。
1. 緩衝液および試薬の調製
- アンピシリン補充(AP)LB寒天プレート(滅菌10cmプレート)を準備する。これを行うには、10 gのLBブロスを400 mLの蒸留水に寒天で溶解し、攪拌し、容量を500 mLまで上げます。オートクレーブ滅菌し、溶液を冷まし、溶液にアンピシリン(ストック:150 mg/mL)0.5 mLを加え、振って混合します。アルコールランプの近くの滅菌10 cmプレートに18 mLの溶液をすぐに加え、室温で固化させ、さらに使用するまでプレートを逆さまに4°Cで保管します。
- 寒天を含まないLB10 gを500 mLの蒸留水に溶解してLB培地を調製します。オートクレーブ滅菌し、溶液を冷まし、溶液にアンピシリン(ストック:150 mg/mL)0.5 mLを加え、振って混合します。
- 5 mLのペニシリン/ストレプトマイシンと10 mLの熱不活化ウシ胎児血清(hiFBS)を485 mLの1xダルベッコリン酸緩衝生理食塩水(DPBS)に加えて、フローバッファーを調製します。
注意: 加熱してFBSを不活性化するには、解凍したFBSボトルを56°Cの水浴に入れます。ボトルが転倒したり、水浴に沈んだりしないようにしてください。温度は完全な劣化にとって重要です。これを確実にするには、ボトルを水浴に入れた後、温度が56°Cで安定するまで待ちます。ボトルを10分ごとに3回静かに回転させます。血清を30分以上インキュベートしないでください。 - 440 mLのダルベッコ改変イーグル培地(DMEM)に50 mLのhiFBS、5 mLのL-グルタミン、および5 mLのペニシリン/ストレプトマイシンを加えて、維持培地を準備します。445 mLのDMEM培地に50 mLのhiFBSと5 mLのL-グルタミンを加えてトランスフェクション培地を調製します。
- 4.145 gのNH4Cl、0.504 gのNaHCO3、および16.81 mgのエチレンジアミン四酢酸(EDTA)を500 mLの蒸留水に加えて、赤血球(RBC)溶解バッファーを調製します。416.5 mLのIMDM培地に75 mLのhiFBS、5 gのウシ血清アルブミン(BSA)、0.5 mLの10 mg/mLインスリン、2.5 mLの4 mg/mLホロトランスフェリン、3.5 μLのβ-メルカプトエタノール、5 mLのL-グルタミン、および0.5 mLのシプロフロキサシンを加えて、不完全なイスコーブ改変ダルベッコ培地(IMDM)培地を調製します。
- サイトカインの濃度が1x IMDM培地の2倍の量である2x IMDM培地を10 mL調製し、50 ng/μL mr-SCFを10 μL、25 ng/μL mr-Flt3Lを20 μL、10 ng/μL mr-IL-6を20 μL、10 ng/μL mr-IL-3を20 μL、10 mg/mLインスリンを10 μL添加し、 50 μLの4 mg/mLホロトランスフェリンを9.87 mLの不完全なIMDM培地に入れます。
注:使用前に、フローバッファー、RBC溶解バッファー、メンテナンス培地、トランスフェクション培地、および不完全なIMDM培地がフィルター滅菌されていることを確認してください。
2. プラスミド形質転換
- 20 μLのα-Selectコンピテントセルを氷上で解凍します。1 μL(~2 ng)のMSCV-MLL-AF9-EF1α-luc2-P2A-EGFP-LC3プラスミド22 を融解したコンピテントセルに加え、チューブをタップして穏やかに混合します。氷上で反応を30分間インキュベートします。
- 混合物を42°Cの加熱ブロック中で40秒間インキュベートすることにより、ヒートショックを与える。すぐにチューブを氷上に2分間移します。
- 1 mLのLB培地(アンピシリンなし)をチューブに加え、37°C、200 rpmで1時間振とうします。
- チューブを室温で500 x g で4分間遠心分離し、0.9 mLの上清を廃棄します。沈殿物を残りの0.1 mLのLB培地に再懸濁します。
- 形質転換したコンピテントセルを、予め温めた(37°C)APLB寒天プレート上に広げます。プレートを逆さまにして37°Cで12〜16時間インキュベートします。
- 単一のコロニーを選び、形質転換細胞を10 mLのAP LB培地中で37°C、200 rpmで一晩消費します。
- フラスコ内の500 mLのAP LB培地に5 mLの消費形質転換コンピテントセルを加え、フラスコを37°Cおよび200 rpmで一晩インキュベートします。
- 製造元の指示に従ってプラスミド抽出キットを使用してプラスミドを抽出し、0.5 mLのオートクレーブ処理した超純水に再懸濁します。分光光度計を用いてプラスミドを定量する。
3. フェニックスエコトロピック(pECO)細胞のトランスフェクション
- 2 x 106 pECO細胞/プレートを、37°Cの加湿5%CO2 インキュベーター内の10 cmプレート内の維持培地で培養します。 pECO細胞が指数関数的成長期に維持され、継代前に活発に分裂していることを確認してください。
- 細胞が80%コンフルエントになったら、プレートを5 mLのDPBSで2回洗浄し、1 mLのトリプシンをプレートに加え、加湿した5%CO2 インキュベーター内で37°Cで2分間インキュベートします。滅菌済みの15 mLチューブで5 mLの維持培地で細胞を回収し、4°Cおよび400 x g で3分間遠心分離します。細胞ペレットを5 mLの維持培地に再懸濁します。
- 10 μLの細胞懸濁液と10 μLのトリパンブルーを混合し、10 μLを血球計算盤にロードして細胞をカウントします。
総細胞数/mL = (カウントされた細胞の総数 x 希釈係数 x 104 細胞/mL)/ カウントされたマスの数)
トランスフェクション用の5 mLの維持培地を使用して2 x 10 6細胞/ディッシュを6 cmディッシュに播種し、37°Cの加湿5%CO2 インキュベーターで細胞を培養します。 - 培養18時間後に細胞が50%〜60%コンフルエントになったら、維持培地を5 mLのトランスフェクション培地と交換します。
- トランスフェクション前に、トランスフェクション試薬を室温で少なくとも 30 分間保持してください。
- 5.5 μgのMSCV-MLL-AF9-EF1α-luc2-P2A-EGFP-LC3プラスミド22 を滅菌1.5 mLチューブ内の0.5 mLのプレーンDMEM培地に加えます。チューブを軽くたたいて穏やかに混ぜ、10分間放置します。
- 14.6 μL(プラスミド量の3倍、v/w)のトランスフェクション試薬をチューブに加え、10分ごとにチューブを3回軽くたたきます。
- トランスフェクション培地中のpECO細胞を含むディッシュのすべての領域に混合物を均一に滴下します。皿を前後に10回、横に10回ゆっくりと動かします。加湿した5%CO2 インキュベーターで皿を37°Cで48時間インキュベートします。
- 22に記載の緑色蛍光タンパク質(GFP)の蛍光顕微鏡およびフローサイトメトリーによりトランスフェクション効率を測定する。細胞は最初にFSC-A/FSC-H、FSC-AおよびSSC-Aにゲーティングされ、シングレットを獲得します。GFP+集団は、トランスフェクトされていない細胞と比較することにより、FL1プロット上でゲートされます。
- 上清を収集し、0.45 μmシリンジフィルターを通して滅菌50 mLチューブにろ過します。上清はすぐに形質導入に使用するか、液体窒素で急速凍結し、さらに使用するまで-80°Cで保存してください。
注:pECO細胞は適切に混合され、皿に均一に播種されなければなりません。播種中に皿を前後に10回、横に10回動かして、細胞を広げます。播種する細胞数は、カウントのばらつきに応じて変化し得る。培養18時間後に50%〜60%のコンフルエントを達成できる最適な播種細胞数を見つけるには、段階希釈で細胞を播種することが役立ちます。
4.レンチウイルス形質導入
- CO2チャンバーで8〜10週齢のCD45.1雌C57BL6 / Jマウス(レシピエントマウスあたり2〜3匹のドナーマウス)を安楽死させます。.
- マウスの全身を70%エタノールで滅菌する。発泡スチロールボード上の滅菌外科用パッドにマウスを置き、マウスの足パッドを通して脚を固定します。
- 正中線で腹腔の上の皮膚を切り、鋭い端の滅菌ハサミで後肢に向かって皮下空間を広げます。
- 腹部の正中線から足首まで切開を伸ばします。鋭利な滅菌ハサミの刃で後ろ足の下の皮下スペースを広げます。
- 鋭い端の滅菌ハサミでアキレス腱を切ります。歯付きの鉗子を使用して腱を保持し、大腿骨に取り付けられたもう一方の端を切断して腓腹筋を取り除きます。
- 鋭利な滅菌ハサミで膝に取り付けられた大腿四頭筋腱を切ります。歯のある鉗子を使用して腱を保持し、大腿骨に取り付けられた筋肉の頭を切断して腓腹筋を取り除きます。
- 脛骨に取り付けられた端の大腿骨を囲む他の筋肉を鋭い端の滅菌ハサミで切ります。
- 鋭い先端の滅菌ハサミで足首を切り、脛骨が無傷のままであることを確認します。歯付きの鉗子を使用して大腿骨の遠位端を保持し、鋭利な滅菌ハサミで股関節を切断し、大腿骨頭が無傷のままであることを確認します。
- 脛骨と大腿骨を滅菌15mLチューブのフローバッファーに移します。
- 脛骨と大腿骨を手で膝を折って分離します。膝蓋骨、軟骨、大腿骨顆を取り除き、脛骨プラトーと遠位大腿骨を手で露出させます。滅菌ガーゼを使用して筋肉を取り除き、骨をフローバッファーに浸します。
- 大腿骨頸部を切断し、23 G針付きの10 mLシリンジを使用して、大腿骨の両端からフローバッファーで骨髄細胞を洗い流します。
- 脛骨くるぶしを切断し、23 G針付きの10 mLシリンジを使用して、脛骨の両端からフローバッファーで骨髄細胞を洗い流します。
- 18 Gの針を備えた10 mLシリンジを使用して上下にピペッティングすることにより、細胞を分散させます。単一細胞懸濁液を4°C、400 x g で3分間遠心分離します。
- 上清を廃棄し、細胞を5 mLのRBC溶解バッファーに再懸濁して、赤血球を3分間溶解します。
- 5 mLのフローバッファーを加えて溶解を停止し、細胞懸濁液を4°C、400 x g で3分間遠心分離します。
- 70 μmのセルストレーナーを滅菌済みの50 mLチューブに置きます。ペレットを5 mLのフローバッファーで懸濁し、混合し、セルストレーナーを通過させて細胞を回収します。
- フローバッファーで細胞濃度を丸底ポリプロピレンチューブで1 x 108/mLに調整します。
- 製造元の指示に従ってマウス造血細胞分離キットを使用してLin- 細胞を選択します。
- APC結合抗マウスCD117(c-Kit)およびPE-Cy7結合抗マウスLy-6A/E(Sca-1)用の1 x 104 細胞のチューブを100 μLのバッファーに3本、単一抗体染色コントロール2本用に脇に置いておきます。単一抗体染色コントロールのそれぞれに1 μLの抗体(0.2 mg/mLストックから)を使用します。
- チューブ内の残りの細胞を、400 μL中の両方の抗体(0.2 mg/mLストックからそれぞれ4 μL)で染色します。 チューブを氷上で暗闇で0.5〜1時間インキュベートします。
- 染色後、1 mLのフローバッファーを加えて細胞を洗浄し、4°Cおよび400 x g で3分間遠心分離します。
- 非染色コントロールおよび単一抗体染色コントロールの細胞を100 μLのフローバッファーに再懸濁します。二重抗体染色細胞を1 mLのフローバッファーに再懸濁して選別します。
- 造血幹細胞(HSC)を、23、24に記載のセルソーターを用いてLSK集団として選別する。
- 染色中に、次のように滅菌した6 cmディッシュにレトロネクチンをコーティングします:PBSで100 μg/mLのレトロネクチンストックを準備し、0.9 mLのPBSと0.1 mLのレトロネクチンを6 cmディッシュに加えます。皿を滅菌フードに室温で2時間コーティングします。次に、レトロネクチンを除去し、0.5 mLのろ過した2%BSA(PBS中)で30分間皿をブロックします。皿を5 mLのPBSで2回洗浄すると、皿は形質導入の準備が整います。
- 選別されたHSCまたは選別されていないLin- 細胞を4°Cおよび400 x g で3分間遠心分離し、3 mLの2x(サイトカイン)IMDM培地と3 mLのウイルス上清(ステップ3.10から生成)にレトロネクチンコーティングディッシュに再懸濁します。加湿した5%CO2 インキュベーターで皿を37°Cで6時間または24時間インキュベートします。
注:本研究では、Lin- 細胞は実験デザインに応じて選別または未選別のいずれかでした。
5.連続移植(図1)
注:主なレシピエントマウスは、8〜10週齢の雄C57BL6 / Jマウス(CD45.2)でした。彼らは、移植の3日前から移植後7日まで、日和見消化器感染症を予防するために抗生物質を含む水を 自由摂取 で提供されました。一次レシピエントマウスは、移植25の3時間前に亜致死的照射(4.75Gy)した。イソフルランは腹腔内注射のマウスには適用されなかった。
- 6時間または24時間形質導入後、室温および400 x g で3分間遠心分離して細胞を回収します。必要に応じて、トリプシンを使用して皿の底に付着した細胞を収集します。上清を廃棄し、細胞を予熱したPBSに再懸濁します。レシピエントの数に応じてPBSの容量を決定します(すなわち、眼窩後注射と腹腔内注射のレシピエントの場合はそれぞれ0.1 mL /マウスと0.5 mL /マウス)。
- 致死下照射されたレシピエントマウスをイソフルランチャンバーに入れます(酸素の流量は1.0 L / minに設定され、イソフルランの気化器は5%に設定されます)。麻酔下での乾燥を防ぐために、目に湿った軟膏を塗ります。マウスは、心拍が毎分60拍に低下すると、さらなる処置の準備ができている。
- 一次レシピエントマウスに、眼窩後(0.1 mL/マウス)7 または腹腔内(0.5 mL/マウス)26 に27 G1/2針で細胞を注入します。マウスが胸骨横臥を維持するのに十分な意識を得るまで、マウスを継続的に観察します。移植後の健康状態についてマウスを毎日監視します。
- 1か月後、眼窩後出血によって毎週採血し、以下に説明するようにヘマベットで全血球数(CBC)を評価することにより白血球増加症を監視します。
- 麻酔後、イソフルランでマウスを横方向に置きます(酸素の流量は1.0 L / minに設定され、アイソフルランスの気化器は5%に設定されます)。マウスは、心拍が毎分60拍に低下すると、さらなる処置の準備ができている。
- 親指と人差し指で目を支えます。内眼窩を通して無菌ヘマクリット毛細血管で静脈洞叢を貫通する。
- 20〜25μLの血液をEDTA採血管に採取し、まぶたを閉じて出血を止めます。硫酸ゲンタマイシン点眼液を1滴目に塗ります。
- エンドポイントで、白血球(WBC)が4 x 10 4細胞/ μLに達したら、マウスをCO2チャンバーで安楽死させ、大腿骨と脛骨をフローバッファーで洗い流して骨髄細胞を分離し、続いてステップ4で述べたようにRBC溶解を行います。
- エンドポイントで、下記のように脾細胞を採取します。
- マウスをCO2 チャンバーで安楽死させる。発泡スチロールボード上の滅菌外科用パッドにマウスを置き、マウスの足パッドを通して脚を固定します。マウスの全身を70%エタノールで滅菌する。
- 正中線で皮膚と筋肉を切り、鋭い端の滅菌ハサミで腹腔を露出させます。鋭利な滅菌ハサミで脾臓を単離し、滅菌15 mLチューブのフローバッファーに入れます。
- 3 mLのフローバッファーを含む6 cmディッシュ内の70 μm滅菌ストレーナーを通して脾臓をメッシュします。細胞をディッシュから滅菌15 mLチューブに移し、単一細胞懸濁液を4°Cおよび400 x g で3分間遠心分離します。
- 上清を廃棄し、細胞を5 mLのRBC溶解バッファーに再懸濁して、赤血球を3分間溶解します。5 mLのフローバッファーを加えて溶解を停止し、細胞懸濁液を4°C、400 x g で3分間遠心分離します。
- 70 μmのセルストレーナーを滅菌済みの50 mLチューブに置きます。ペレットを5 mLのフローバッファーで懸濁し、混合し、セルストレーナーを通過させて細胞を回収します。
- 脾細胞と骨髄細胞をFITC結合抗マウスCD45.1抗体で染色し、フローサイトメーターで検出することにより、初代(1°)AML細胞を同定します。細胞は最初にFSC-A/FSC-H、FSC-AおよびSSC-Aにゲーティングされ、シングレットを獲得します。CD45.1+集団は、染色されていない細胞と比較することにより、FL1プロット上でゲートされます。
- 二次(2°)移植の場合は、1°レシピエントのCD45.1 AML脾臓細胞をPBS(0.1 mL /マウス)に再懸濁し、CD45.2雄C57BL6 / Jマウスに眼窩後注射します。並行して、1°I.p.レシピエントのAML脾臓細胞をPBS(0.5 mL /マウス)に再懸濁し、8〜12週齢の赤色蛍光タンパク質(RFP)発現 Ai14TdTomato 雄マウスに腹腔内注射します27。
- 三次(3°)移植の場合、2°I.p.レシピエントの骨髄または腹腔から分離したAML細胞を再懸濁し、それぞれ Ai14TdTomato (RFP+)またはCD45.2マウスに腹腔内注射します。2°レシピエントの腹腔から単離したAML細胞を再懸濁し、 Ai14TdTomato (RFP+)マウスにr.o.注射により移植します。
注:2°移植では、末梢血中のCBCをモニタリングすることにより、2°レシピエントの疾患進行を特定しました。AMLの確立をさらに確認するために、心臓穿刺による末梢血全体、骨髄、脾臓、肝臓を採取しました。さらに、i.p.細胞を回収するためにi.p.洗浄を行った。単一細胞懸濁液は、上記のように骨髄、脾臓、およびi.p.洗浄から獲得した。これらの部位からの細胞を、RBC溶解後にフローサイトメーターで分析した。AML細胞はRFP陰性(RFP−)細胞として認識された。3°移植では、エンドポイントで血液、骨髄、脾臓、肝臓、およびi.p.細胞をサンプリングしました。RFPまたは CD45.1+ 細胞をAML細胞として同定し、フローサイトメトリーで調べました。2°および3°レシピエントマウスに照射または抗生物質水を与えなかった。
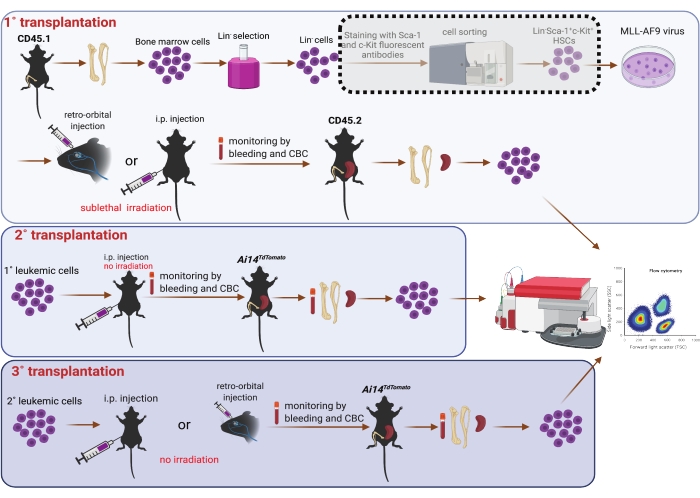
図1:骨髄造血幹細胞および連続移植におけるMLL-AF9ウイルス形質導入の概略図(1°、2°、および3°)。点線の網掛けボックスに示されているセルソーターを使用したSca-1およびc-Kitダブルポジティブ集団のソートは、リソースが許せばオプションと見なされます。図はBioRender(https://biorender.com/)を使用して作成されました。この図の拡大版を表示するには、ここをクリックしてください。
6.腹腔内洗浄
- 5 mLの不完全なIMDM培地を腹腔に2回注入し、15 mLの滅菌チューブに細胞を採取します。細胞懸濁液を室温および400 x g で3分間遠心分離する。AML細胞(4 x 105 細胞/マウス)を2°レシピエントの腹腔からi.p.注射 を介して 3°CD45.2レシピエントマウス(n = 3)に移植します。
7. 組織学的解析 28
- 安楽死時にマウスから脾臓、肝臓、大腿骨を分離します。それらを5 mLの10%(v / v)緩衝ホルマリンで固定します。比較のために健康な対応物から脾臓と肝臓をサンプリングします。
- 固定組織をパラフィンに埋め込み、それらを切片に切断する。切片をヘマトキシリンおよびエオジン(H&E)色素で染色する。
- 組織学的分析用の互換性のあるソフトウェアをインストールした20倍の倍率で顕微鏡下で画像を取得します。
8. 半定量PCR(qPCR)の実施
- 製造元の指示に従ってRNA試薬中のRNAを調製します。
- 0.5〜1.0 μgのRNAを使用して、製造元の指示に従ってcDNA逆転写キットを使用してcDNAを合成します。
- cDNAを使用してqPCRキットを使用してqPCRを実行し、qPCRシステムでサンプルを実行します。次の事前検証済みの TaqMan プローブを使用します: KMT2A (MLL;参照シーケンス:NM_001197104(2)、IDT)29 および 18S リボソームRNA(Hs99999901_s1)。
- KMT2Aおよび18Sアンプリコンを2%アガロースゲルにロードして、発現を視覚化します。互換性のあるソフトウェアプログラムがインストールされているイメージャで画像を取得します。
9. データ処理
- 統計分析ソフトウェアを使用して結果を分析し、SEM±平均値として結果を提示します。 市販のイラストレーターツールを使用して図を生成します。
結果
r.o.とi.p.移植経路を用いたマウスAML細胞の移植効率の比較
これまで、MLL-AF9形質導入LSK細胞を眼窩後移植したレシピエントマウスで1°AMLの樹立が報告され、連続移植によって1°AML細胞の移植能が実証されました30。本研究は、骨髄リン細胞 を使用して移植を行う可能性を評価した最初の研究です。異常な白血球増加症の存在(図2A)?...
ディスカッション
これらの上記の研究は、Lin細胞の 移植が1°マウスAMLの生成においてLSK細胞に匹敵するという支持的な証拠を提供します。さらに、現在のデータは、i.p.注射が静脈内(またはr.o.)注射と比較してマウスAMLを確立するための効率的で便利な方法であることも示しています。
LSK細胞に加えて、顆粒球単球前駆細胞(GMP)、共通リンパ系前駆細胞(CLP)、および共通骨髄系前駆...
開示事項
著者は利益相反を宣言しません。
謝辞
著者らは、ペンシルベニア州立大学獣医生物医科学部動物診断研究所のハック研究所のフローサイトメトリーコアファシリティと組織病理学コアファシリティがタイムリーな技術サポートを提供してくれたことに感謝します。この研究は、米国がん研究所(KSP)、ペンシルベニア州立農業科学大学、ペンシルベニア州立がん研究所、USDA-NIFAプロジェクト4771、K.S.P.およびRFPへのアクセッション番号00000005からの助成金によってサポートされました。
資料
| Name | Company | Catalog Number | Comments |
| a-Select competent cells | Bioline | BIO-85027 | |
| Ammonium chloride (NH4Cl) | Sigma Aldrich | Cat# A-9434 | |
| Ampicillin | Sigma Aldrich | Cat# A0797 | |
| Bovine Serum Albumin (BSA), Fraction V—Low-Endotoxin Grade | Gemini bio-products | Cat# 700-102P | |
| Ciprofloxacin HCl | GoldBio.com | Cat# C-861-100 | |
| DMEM, high glucose, no glutamine | Gibco | Cat# 11960-044 | |
| Dulbecco’s Phosphate-Buffered Saline (PBS) | Corning | Cat# 21-031-CV | |
| EDTA, Disodium Salt (EDTA-2Na), Dihydrate, Molecular Biology Grade | Calbiochem | Cat# 324503 | |
| Fetal Bovine Serum - Premium Select | Atlanta Biologicals | Cat# S11550 | |
| Holo-transferrin, bovine | Sigma Aldrich | Cat# T1283 | |
| Insulin solution human | Sigma | Cat# I-9278 | |
| Iscove's Modified Dulbecco's Medium (IMDM) | Gibco | Cat# 12440-053 | |
| L-glutamine 200 mM (100×) solution | HyClone, Gelifesciences | Cat# SH30034.01 | |
| LB broth, Lennox | NEOGEN | Cat #: 7290A | |
| LB Broth with agar (Miller) | Sigma Aldrich | Cat# L-3147 | |
| Mouse anti-mouse CD45.1 (FITC) | Miltenyi Biotec | Cat# 130-124-211 | |
| Mouse Interleukin-3 (IL-3) | Gemini bio-products | Cat# 300-324P | |
| Mouse Interleukin-6 (IL-6) | Gemini bio-products | Cat# 300-327P | |
| Mouse Stem Cell Factor (SCF) | Gemini bio-products | Cat# 300-348P | |
| Penicillin-Streptomycin Solution, 100x | Corning | Cat# 30-002-CI | |
| Phenix-Eco (pECO) cells | ATCC | CRL-3214 | |
| Potassium Bicarbonate (KHCO3), Granular | JT. Baker | Cat# 2940-01 | |
| Rat anti-mouse CD117 (c-kit) (APC) | BioLegend | Cat # 105812 | |
| Rat anti-mouse Ly-6A/E (Sca-1) (PE-Cy7) | BD Pharmingen | Cat# 558162 | |
| Recombinant Murine Flt3-Ligand | Pepro Tech, INC. | Cat# 250-31L | |
| RetroNectin Recombinant Human Fibronectin Fragment | TaKaRa | Cat# T100A | |
| TransIT-293 Reagent | MirusBio | Cat# MIR 2705 | |
| TRI Reagent | Sigma Aldrich | Cat# T9424 | |
| Trypan Blue Solution, 0.4% | Gibco | Cat # 15250061 | |
| Trypsin-EDTA (0.25%), phenol red | Gibco | Cat# 25200-056 | |
| β-Mercaptoethanol (BME) | Sigma Aldrich | Cat# M3148 | |
| Commercial Assays | |||
| EasySep Mouse Hematopoietic Progenitor Cell Isolation Kit | StemCell technologies | Cat# 19856A | |
| High-Capacity cDNA Reverse Transcription Kit | Thermo Fisher | Cat# 4368813 | |
| PerfeCTa qPCR SuperMix | Quanta Bio | Cat# 95051-500 | |
| Plasmid Maxi Kit (25) | Qiagen | Cat#:12163 | |
| Animals | |||
| Ai14TdTomato mice | Jackson Laboratory | Strain # 007914 | |
| CD45.1 C57BL6/J mice | Jackson Laboratory | Strain # 002014 | |
| CD45.2 C57BL6/J mice | Jackson Laboratory | Strain # 000664 | |
| Instruments and Softwares | |||
| Adobe illustrator | Version 25.2.3 | ||
| BD accuri C6 flow cytometer | BD Biosciences | ||
| FlowJo 10.8.0 | BD | ||
| GeneSys software program | Version 1.5.7.0 | ||
| GraphPad Prism version 6 | GraphPad | ||
| Hemavet 950FS | Drew Scientific | ||
| 7300 Real time PCR system | Applied Biosystems | ||
| Syngene G:BOX Chemi XR5 Chemiluminescence Fluorescence Imaging | G:Box Chemi |
参考文献
- Dohner, H., Weisdorf, D. J., Bloomfield, C. D. Acute myeloid leukemia. The New England Journal of Medicine. 373 (12), 1136-1152 (2015).
- Fortier, J. M., Graubert, T. A. Murine models of human acute myeloid leukemia. Cancer Treatment and Research. 145, 183-196 (2010).
- Ernst, P., et al. Definitive hematopoiesis requires the mixed-lineage leukemia gene. Developmental Cell. 6 (3), 437-443 (2004).
- Fisher, J. N., Kalleda, N., Stavropoulou, V., Schwaller, J. The Impact of the cellular origin in acute myeloid leukemia: learning from mouse models. Hemasphere. 3 (1), 152 (2019).
- Zhan, Y., Zhao, Y. Hematopoietic stem cell transplant in mice by intra-femoral injection. Methods in Molecular Biology. 430, 161-169 (2008).
- Price, J. E., Barth, R. F., Johnson, C. W., Staubus, A. E. Injection of cells and monoclonal antibodies into mice: comparison of tail vein and retroorbital routes. Proceedings of the Society for Experimental Biology. 177 (2), 347-353 (1984).
- Yardeni, T., Eckhaus, M., Morris, H. D., Huizing, M., Hoogstraten-Miller, S. Retro-orbital injections in mice. Lab Animal. 40 (5), 155-160 (2011).
- Suckow, M. A., Danneman, P., Brayton, C. . The Laboratory Mouse. , (2001).
- Barr, J. E., Holmes, D. B., Ryan, L. J., Sharpless, S. K. Techniques for the chronic cannulation of the jugular vein in mice. Pharmacology, Biochemistry, and Behavior. 11 (1), 115-118 (1979).
- Kang, Y. Analysis of cancer stem cell metastasis in xenograft animal models. Methods in Molecular Biology. 568, 7-19 (2009).
- Nungestee, W., Wolf, A., Jourdonais, L. Effect of gastric mucin on virulence of bacteria in intraperitoneal injections in the mouse. Proceedings of the Society for Experimental Biology and Medicine. 30 (2), 120-121 (1932).
- Gargiulo, S., et al. Mice anesthesia, analgesia, and part I: anesthetic considerations in preclinical research. ILAR journal. 53 (1), 55-69 (2012).
- Leong, S. -. K., Ling, E. -. A. Labelling neurons with fluorescent dyes administered via intravenous, subcutaneous or intraperitoneal route. Journal of Neuroscience Methods. 32 (1), 15-23 (1990).
- Ma, P., et al. Intraperitoneal injection of magnetic Fe3O4-nanoparticle induces hepatic and renal tissue injury via oxidative stress in mice. International Journal of Nanomedicine. 7, 4809-4918 (2012).
- Schwarze, S. R., Ho, A., Vocero-Akbani, A., Dowdy, S. F. In vivo protein transduction: delivery of a biologically active protein into the mouse. Science. 285 (5433), 1569-1572 (1999).
- Muench, M. O., Chen, J. C., Beyer, A. I., Fomin, M. E. Cellular therapies supplement: the peritoneum as an ectopic site of hematopoiesis following in utero transplantation. Transfusion. 51, 106-117 (2011).
- Zhao, W., et al. Intravenous injection of mesenchymal stem cells is effective in treating liver fibrosis. World Journal of Gastroenterology. 18 (10), 1048 (2012).
- Yousefi, F., Ebtekar, M., Soleimani, M., Soudi, S., Hashemi, S. M. Comparison of in vivo immunomodulatory effects of intravenous and intraperitoneal administration of adipose-tissue mesenchymal stem cells in experimental autoimmune encephalomyelitis (EAE). International Immunopharmacol. 17 (3), 608-616 (2013).
- Cheng, K., et al. Transplantation of bone marrow-derived MSCs improves cisplatinum-induced renal injury through paracrine mechanisms. Experimental and Molecular Pathology. 94 (3), 466-473 (2013).
- Castelo-Branco, M., et al. Intraperitoneal but not intravenous cryopreserved mesenchymal stromal cells home to the inflamed colon and ameliorate experimental colitis. PLoS One. 7 (3), 33360 (2012).
- Bazhanov, N., et al. Intraperitoneally infused human mesenchymal stem cells form aggregates with mouse immune cells and attach to peritoneal organs. Stem Cell Research & Therapy. 7, 27 (2016).
- Liu, Q., Chen, L., Atkinson, J. M., Claxton, D. F., Wang, H. G. Atg5-dependent autophagy contributes to the development of acute myeloid leukemia in an MLL-AF9-driven mouse model. Cell Death & Disease. 7 (9), 2361 (2016).
- Wognum, A. W., Eaves, A. C., Thomas, T. E. Identification and isolation of hematopoietic stem cells. Archives of Medical Research. 34 (6), 461-475 (2003).
- Randall, T. D., Weissman, I. L. Characterization of a population of cells in the bone marrow that phenotypically mimics hematopoietic stem cells: resting stem cells or mystery population. Stem Cells. 16 (1), 38-48 (1998).
- Gott, K. M., et al. A comparison of Cs-137 gamma rays and 320-kV X-rays in a mouse bone marrow transplantation model. Dose Response. 18 (2), 1559325820916572 (2020).
- Miner, N. A., Koehler, J., Greenaway, L. Intraperitoneal injection of mice. Applied Microbiology. 17 (2), 250-251 (1969).
- Madisen, L., et al. A robust and high-throughput Cre reporting and characterization system for the whole mouse brain. Nature Neuroscience. 13 (1), 133-140 (2010).
- Cardiff, R. D., Miller, C. H., Munn, R. J. Manual hematoxylin and eosin staining of mouse tissue sections. Cold Spring Harbor Protocols. 2014 (6), 655-658 (2014).
- Ronan, J. L., Wu, W., Crabtree, G. R. From neural development to cognition: unexpected roles for chromatin. Nature Review Genetics. 14 (5), 347-359 (2013).
- Qian, F., et al. Interleukin-4 treatment reduces leukemia burden in acute myeloid leukemia. FASEB Journal. 36 (5), 22328 (2022).
- Krivtsov, A. V., et al. Transformation from committed progenitor to leukaemia stem cell initiated by MLL-AF9. Nature. 442 (7104), 818-822 (2006).
- Chen, W., et al. Malignant transformation initiated by Mll-AF9: gene dosage and critical target cells. Cancer Cell. 13 (5), 432-440 (2008).
- Somervaille, T. C. P., Cleary, M. L. Identification and characterization of leukemia stem cells in murine MLL-AF9 acute myeloid leukemia. Cancer Cell. 10 (4), 257-268 (2006).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved