Method Article
in vivoでのB細胞活性化の阻害とin vitroでのガラクトース欠損IgA1産生の減少によるジオシン媒介性IgA腎症の緩和
要約
この研究は、免疫グロブリンA腎症(IgAN)をDioscin(DIO)で治療するための実験データを提供します、 Dioscin (DIO)、 DioDio 、漢方薬の効果と基礎となるメカニズムを研究するためのパラダイム in vivo および in vitro。
要約
循環ガラクトース欠損IgA1(Gd-IgA1)の増加は、粘膜免疫応答の過程におけるIgA陽性分泌細胞の過剰な活性化によって引き起こされ、これはIgA腎症(IgAN)の病因における重要なリンクです。Peyerのパッチは、Bリンパ球がIgA分泌形質細胞に変換される顕著な場所であり、IgAの主要な供給源です。また、コア1β-1,3-ガラクトシルトランスフェラーゼ(C1GalT1)とその分子シャペロンであるC1GalT1特異的分子シャペロン(Cosmc)の発現低下は、IgAN患者におけるIgA1の異常なグリコシル化に関連しています。私たちの臨床経験では、Dioscoreae Nipponicae Rhizoma (DNR) の漢方薬は、IgAN 患者のタンパク尿と血尿を緩和し、腎機能を改善することができることが示されています。ディオシン(DIO)は、さまざまな薬理活性を持つDNRの主要な有効成分の1つです。この研究では、IgANの治療におけるDIOの可能なメカニズムを探ります.IgANモデルマウスは粘膜免疫誘導によって確立されました。マウスは、コントロールグループ、モデルグループ、およびDIO強制グループに分けられました。マウスの糸球体IgA沈着、腎病理学的変化、およびPeyerのパッチにおけるB細胞マーカーCD20およびCXCR5の発現を、免疫蛍光および免疫組織化学によって検出しました。リポ多糖(LPS)刺激後、DAKIKI細胞の増殖、IgAおよびGd-IgA1分泌、C1GalT1、およびCosmc発現に対するDIOの影響を、Cell Counting kit-8(CCK-8)アッセイ、酵素結合免疫吸着アッセイ(ELISA)テスト、定量的リアルタイムポリメラーゼ連鎖反応(QRT-PCR)、およびウェスタンブロッティング(WB)により検討しました。 in vivo 研究では、糸球体メサンギウム過形成を伴うIgA沈着と、IgANモデルマウスのパイエルパッチにおけるCD20およびCXCR5の発現増加は、DIOによって緩和されました。 In vitro 試験では、0.25 μg/mLから1.0 μg/mLのDIOがLPSによるDAKIKI細胞の増殖、IgAおよびGd-IgA1の分泌を阻害し、C1GalT1およびCosmcのmRNAおよびタンパク質発現をアップレギュレーションすることが示されました。この研究は、DIOがIgA分泌細胞の過剰な活性化を阻害し、C1GALT1/Cosmc発現をアップレギュレーションすることにより、Gd-IgA1産生を減少させる可能性があることを示しています。
概要
IgA腎症(IgAN)は、原発性糸球体腎炎の最も一般的なタイプであり、特定の治療法はなく、依然として末期腎疾患の重大な原因となっています1。IgANの病因はまだ完全には理解されていませんが、「マルチヒット仮説」は一般的に受け入れられており、多くの臨床的および実験的研究の証拠によって支持されています2。IgANの病因には、B細胞の活性化とガラクトース欠損IgA1(Gd-IgA1)の産生が含まれます3。粘膜免疫応答中のIgA分泌細胞の過剰な増殖と活性化による循環Gd-IgA1の増加は、IgAN4,5,6の病因における重要なリンクです。Bリンパ球の表現型からIgA分泌細胞への変換の増殖と活性化の中心的な場所として、パイエルパッチはIgA分泌の主要な供給源であり、IgANの発生と発達と密接に関連しています7,8。さらに、IgA1分泌細胞の増殖、およびCore 1β-1,3-galactosyltransferase(C1GalT1)およびC1GalT1特異的分子シャペロン(Cosmc)の発現は、IgA1の異常なグリコシル化と関連しており、これはIgAN患者におけるGD-IgA1産生を引き起こします6,9。
近年、漢方薬によるIgAN治療の臨床研究が進んでいます。Yiqi Qingjie Formulaは、広安門病院の腎臓内科によるIgANの治療に不可欠な処方です。私たちのグループの以前の研究では、Yiqi Qingjie Formula による治療後に IgAN 患者の血清中の Gd-IgA1 が減少することがわかりました。Yiqi Qingjieフォーミュラで最も使用されているハーブの1つとして、Dioscoreae Nipponicae Rhizoma(DNR)は、免疫の調節、炎症の抑制、咳や喘息の緩和などのさまざまな機能を持つDioscorea Nipponica Makinoの乾燥根茎です10,11。何人かの学者がIgANをDNRで治療し、良好な結果を達成しました12,13,14。DNR15の主な有効成分として、ダイオシン(DIO)は尿酸を下げ、線維化を抑制し、炎症反応を抑制し、抗酸化ストレスを抑制します16,17。したがって、DIOは、過剰なGd-IgA1の細胞分泌を阻害し、特定の腎臓保護効果を発揮する新しい作用機序を持っている可能性があります。それでも、IgANを治療するためのDIOの作用機序に関する研究は報告されていません。
DIOのIgANに対する治療メカニズムの可能性を探り、IgANの新たな治療法を提供するために、DIOのIgANに対する治療効果を in vivo および in vitroで実験しました。
プロトコル
広安門病院の倫理委員会は、この実験を承認しました(動物実験倫理承認番号:IACUC-GAMH-2023-003)。
1. 実験手順のためのマウスの準備
- SPFグレードの雄Balb/cマウス22匹(生後6-7週齢、体重20-25g)を病院/研究センターの動物施設で飼育します。乱数表法を使用して、動物を制御群(n = 8)とモデル群(n = 14)に分けます。
- 実験室のケージで1週間の適応飼育を行った後、モデルグループ(IgANグループ)に0.1%ウシガンマグロブリン(BGG)溶液を6mmol / L HClを含む酸性水に9週間与えます。
- 0.1 mLの生理食塩水入り0.1 mLを尾静脈に注入し、BGG溶液を飲み続けながら3日間連続して注入し、IgAN実験マウスモデル18を調製します。
- 対照群にBGGを含まない6mmol / L HCl酸性水を9週間自由に飲ませます。対応する量の生理食塩水を尾静脈に連続して3日間注入します。
注:コントロールグループとモデルグループには、通常のフィードと同じ品質が供給されました。 - 尾静脈注射後、対照群のマウス2匹とモデル群のマウス2匹をランダムに選択し、タンパク尿、光学顕微鏡、免疫蛍光法で調べてモデリングが成功したかどうかを判断します。
注:動物には食べ物は提供されませんが、水を飲むことは禁止されていません。尿量を記録します。 - 代謝ケージで24時間尿を採取し、400 x g で5分間遠心分離します。尿沈殿物を捨てます。上清を10倍に希釈した後、尿タンパク質アッセイキットを使用してタンパク尿濃度を測定し、希釈係数と尿量を掛けて、24時間の総尿タンパク質を取得します。.
注:顕微鏡法と免疫蛍光法は、それぞれセクション3と4に示されています。 - モデルの準備に成功したら、モデルグループ内の12匹のマウスを、乱数表法に従って、モデルグループ(IgANグループ)とDIO強制グループ(DIOグループ)のそれぞれ6匹のマウスに分割します。
- 対照群にBGGなしで6mmol/L HCl酸性水を飲み続けさせ、6mmol/L HClを含む酸性水で構成されたモデル群0.1%BGG溶液を飲ませます。薬理学的実験方法論の用量換算式に従ってDIO群強制経口投与の用量を計算します(人体の70kgの体重に応じて換算)19。DIO錠0.06g / kgを1日1回8週間強制経口投与します。.
- 8週間の強制経口投与後、マウスを0.4%ペントバルビタールナトリウム(60 mg / kg)で腹腔内に麻酔し、つま先をつまんで適切な麻酔を確認した後、腎臓とパイエルパッチを分離して、その後の光学顕微鏡検査および免疫組織化学分析。.
注: in vivo モデルのスキームは 、補足 図1にあります。
2. 組織学的解析
- 腎臓のパラフィン切片とパイエルパッチ
- 厚さ3 mmの腎臓組織または1つのパイエルパッチを4%パラホルムアルデヒドで24時間固定し、グラジエントエタノールとキシレンで脱水します。ワックスに2時間浸し、密封して凍結します。
- 厚さ2 μmの腎臓切片と厚さ4 μmのパイエルパッチ切片を切開し、温水に広げます。広げたスライスをきれいなスライドガラスですくい取り、40°Cの恒温オーブンで1時間焼きます。試料の前処理後に染色を開始します。
注:腎臓の肺門部分の冠状表面を、厚さ3mmの組織ブロックで取ります。
- パラフィン切片を脱ワックスし、室温(RT)で過ヨウ素酸溶液で10分間、光を避けて染色します。蒸留水ですすぎ、光を避けながら、シッフの染色液で20〜30分間乾燥染色した状態で拭きます。顕微鏡下で切片が赤くなるまで蒸留水ですすいでください。
- 切片をヘマトキシリン染色溶液に入れ、核を3分間染色し(深く染色しすぎる核は塩酸エタノールで分割できます)、スライドが無色になるまで流水ですすいでください。
- エタノールとキシレンのグラジエン濃度で日常的な脱水を行い、切片を中性ガムで密封し、顕微鏡で観察します。PAS陽性は赤、核は青です。
3. パイエル板の免疫組織化学的解析
- ステップ2.1で説明したように、パイエルパッチのパラフィン切片を調製します。
注:免疫組織化学およびその後の免疫蛍光染色の切片の厚さは4μmです。 - パラフィン切片を脱ろうします。
- 切片をキシレンIに5分間、キシレンIIに5分間、キシレンIIIに5分間入れます。
- さらに、スライドを無水エタノールIで5分間、無水エタノールIIで5分間、85%アルコールで5分間、75%アルコールで5分間すすぎます。次に、スライドを蒸留水ですすいでください。
- 抗原賦活化
- クエン酸ナトリウムの50倍ストック溶液を調製し、蒸留水で1倍に希釈して使用します。オートクレーブで2分間加熱した後、スライスをオートクレーブに入れ、液面がスライスのレベルを超えることを確認します。
- 高温で5分間加熱した後、スライドを自然に冷まします。スライスをPBS溶液で3回、それぞれ5分間洗浄します。
- 内因性ペルオキシダーゼのブロッキング:免疫組織化学ペンで組織の境界を円でマークします。切片を3%過酸化水素溶液中で室温で15分間インキュベートし、光から保護し、切片をPBS溶液で毎回5分間3回洗浄します。
- 血清ブロッキング:RTで30分間マークされた組織切片に10%ヤギ血清を滴下して切片をブロックします。
- 一次抗体のインキュベーション:ブロッキング溶液を静かに振り落とし、調製した一次抗体(CD20 [1:800];CXCR5 [1:800]) をセクションに追加しました。切片をウェットボックスに平らに置き、4°Cで一晩インキュベートします。
注:抗体の蒸発を防ぐために、ウェットボックスに少量の水を加えてください。 - 二次抗体インキュベーション:切片をPBS溶液で毎回5分間3回洗浄します。切片を振ってPBSを除去し、一次抗体の関連種の二次抗体(HRP標識)を組織に一滴垂らし、室温で50分間インキュベートします。
- 3,3'-ジアミノベンジジン(DAB)の均質化:切片をPBS溶液で5分間ずつ3回洗浄します。切片を振って乾かした後、新たに調製したDAB発色性溶液を切片に滴下します。顕微鏡で発色時間を観察します。ポジは茶色がかった黄色です。水道水ですすいで発色を終了します。
- 核の染色:ヘマトキシリンで約1分間再染色し、水道水で洗浄した後、水道水で10分間すすぎ、青色に戻します。
- 脱水とシーリング:
- 切片をアルコール75%に5分間、アルコール85%に5分間入れます。切片を無水エタノールIに5分間、無水エタノールIIに5分間、無水エタノールIIIに5分間入れます。
- 切片をキシレンIで5分間洗い、取り出して少し乾かし、切片を中性ガムで密封します。
- 画像取得:顕微鏡検査で画像を収集し、ハローソフトウェアで分析して組織のパノラマ画像分析を行います。
注:ヘマトキシリン染色された核は青色で、DAB陽性発現は茶色がかった黄色で観察されます。
4. 腎IgA免疫蛍光法
- ステップ2.1で説明されているように、腎臓のパラフィン切片を準備します。
- 脱ワックスパラフィンセクション:
- 切片をキシレンIに5分間、キシレンIIに5分間、キシレンIIIに5分間入れます。無水エタノールI、無水エタノールII、95%エタノール、90%エタノール、80%エタノール、70%エタノール、および50%エタノールの切片をそれぞれ5分間処理し、蒸留水で洗浄します。.
- プロテイナーゼKの賦活化:切片を振って乾かし、組織化学ペンで組織切片の周りに円を描きます。プロテイナーゼKワーキング溶液(ストック溶液とPBSの比率1:9)を滴下して組織を覆い、37°Cで30分間インキュベートします。切片をPBSで3回、それぞれ5分間洗浄します。
- 細胞膜への浸透:切片を少し振って乾かし、0.1%トリトンで覆います。室温で20分間インキュベートし、切片をPBSで3回、それぞれ5分間洗浄します。
- ブロッキング:10%のヤギ血清を滴下して組織を均一に覆い、RTで30分間ブロッキングします。
- 一次抗体のインキュベーション:ヤギ抗マウスAF488-標識IgA抗体(1:500)を適量滴下して組織を均一に覆い、4°Cで一晩インキュベートします。
- 核の染色:スライスをPBSで3回、それぞれ5分間洗浄します。PBSを除去した後、切片に4′,6-ジアミジノ-2-フェニルインドール(DAPI)染色液を滴下し、光から保護された室温で15分間インキュベートします。
- 切片の洗浄と密封:切片をPBSで5分間3回洗浄した後、退色防止剤封入剤で密封します。
- 顕微鏡と写真撮影:蛍光顕微鏡で切片を観察し、画像を撮影します。
注意: DAPIの場合、紫外線励起は波長330〜380 nm、発光波長は420 nm、青色光です。フルオレセインイソチオシアネート(FITC)の励起波長は465-495 nmで、発光波長は515-555 nm、緑色光です。
5. 細胞培養
- ヒトBリンパ球株DAKIKIを米国ATCCから入手します。10% FBSと1%ペニシリン-ストレプトマイシンを添加したRPMI-1640培地でDAKIKI細胞を培養します。
- 細胞を37°C、5%CO2 インキュベーターで培養し、2〜3日ごとに継代培養します。すべての実験で対数成長期の細胞を使用してください。
- 70%〜80%のコンフルエントで、滅菌ピペットで細胞を回収し、細胞を140 x g で5分間遠心分離します。上清を廃棄し、無血清培地で再懸濁し、24時間後、すべての細胞をその後の治療のために静止期間に放置します。.
6. 正常なDAKIKI細胞上の安全な濃度のDIOをスクリーニングするためのLDH細胞毒性アッセイ
- 96ウェルプレートに4x105 細胞/ウェルの密度でDAKIKI細胞を播種し、低コントロール群、高コントロール群、および異なる濃度のDIO(0.25、0.5、1.0、2.0、4.0、8.0μg/mL)を設定します。5% CO2, 37 °Cインキュベーターで、対応する処理後、グループ化方法に従って24時間インキュベートします。
- 細胞毒性検出キットの指示に従って、高対照群のウェルあたり5 μLのライセートを加え、プレートを5% CO2, 37 °Cインキュベーターに15分間置きます。
- プレートを取り出し、各ウェルに反応混合物100μLを加え、室温で10分間暗所でインキュベートした後、停止反応液50μLを加えます。できるだけ早くマイクロプレートリーダーで490nmのOD値を測定してください。
- さまざまな濃度のDIOのLDH放出率を計算し、最大投与量として≤10%を次の式に従って計算します:LDH放出率=(実験井LDH - 低制御LDH)/(高制御LDH - 低制御LDH)x 100%。
7. DIOのDAKIKI細胞増殖への影響を検出するためのCCK-8アッセイ
- これまでの実験結果20に基づき、LPS 40 μg/mLを用いたIgANモデルを確立し、DAKIKI細胞を誘導する。
- 次に、96ウェルプレートに4x105 細胞/ウェルを播種し、コントロール、モデル、およびDIOの低、中、高濃度グループ(0.25 μg/mL、0.5 μg/mL、および1.0 μg/mL)に分けます。プレートを5% CO2、37°Cインキュベーターで24時間インキュベートします。
- 次に、20 μLのCCK-8試薬を各ウェルに加え、プレートをインキュベーター(5% CO2、37°C)に2時間戻します。インキュベーション後、できるだけ早くマイクロプレートリーダーで波長450nmのODを検出します。
8. DAKIKI細胞によるIgAおよびGd-IgA1の分泌に対するDIOの影響を検出するためのELISA
- DAKIKI細胞を6×106 細胞/ウェルの密度で6ウェルプレートに播種し、ステップ7.2に従って細胞をグループ化して処理します。細胞を24時間培養した後、850 x g で4°Cで10分間遠心分離し、上清を得ます。
- キットの指示に従って、IgAおよびGd-IgA1濃度を検出します。
9.DAKIKI細胞のC1GALT1およびCosmc mRNAレベルに対するDIOの影響を検出するためのqRT-PCR
- DAKIKI細胞を6ウェルプレートに6x106 細胞/ウェルの密度で播種し、ステップ7.2で述べたCCK8として細胞をグループ化して処理し、24時間インキュベートします。DAKIKI細胞からtotal RNAをtotal RNA抽出キットの指示に従って抽出します。
- 各サンプル群から抽出したRNA1 μLを採取し、その濃度を測定した後、キットの指示に従って、各サンプルからtotal RNAの1 μgを逆方向にcDNAに転写します。
- 次に、RT-PCR増幅を行い、各遺伝子の発現を検出します(95°Cで15分間、95°Cで10秒間、60°Cで30秒間)。β-アクチンを内部参照とする2-ΔΔCT 法を用いて、各遺伝子の発現量を計算します。
注:プライマー配列は以下の通りである。
C1GALT1: 5'-AAGGTTGACACCCAGCCTAA-3', 5'-CTTTGACGTGTTTGGCCTTT-3';
Cosmc: 5'-GCTCCTTTTTGAAGGGTGTG-3', 5'-TACTGCAGCCCAAAGACTCA-3';
β-アクチン:5'-TCACCCACACTGTGCCCATCTACGA-3'、5'-CAGCGGAACCGCTCATTGCCAATGG-3'。
10. DAKIKI細胞におけるDIOのC1GALT1およびCosmcタンパク質発現に対するDIOの影響を検討するためのウェスタンブロッティング
- DAKIKI細胞を6×106 細胞/ウェルの密度で6ウェルプレートに播種します。手順7.2で説明したようにグループ化して扱います。インキュベーションの24時間後、細胞の各グループを収集します。
- 細胞溶解液(PMSF:ホスファターゼ阻害剤:RIPA溶解液=1:1:100)を適量加え、氷上で30分間インキュベートします。次に、13,500 x g で4°Cで10分間遠心分離し、上清を回収します。
- BCAタンパク質濃度アッセイキットを使用してタンパク質濃度を測定します。
- タンパク質サンプルをボルテックスにより5x SDS-PAGEローディングバッファーと4:1でボルテックスして混合し、混合サンプルを100°Cで5分間加熱してタンパク質を変性させます。
- 分子量の異なるタンパク質を検出するには、タンパク質マーカー(5 μL/well)とサンプル(20 μg/well)を12% SDS-PAGEゲルの異なるレーンに添加し、SDS-PAGE電気泳動を行い、ゲルをPVDFメンブレンに移します。
- 5%脱脂乳でメンブレンを室温で2時間ブロックし、対応する一次抗体(C1GALT1 [1:1000]、Cosmc [1:2000])と24時間インキュベートします。β-アクチン抗体(1:100000)を内部コントロールとして使用します。
- ポリフッ化ビニリデン(PVDF)メンブレンを1x Tris-Buffered Saline、0.1% Tween 20界面活性剤(TBST)で3回(10分/回)洗浄し、対応する二次ヤギ抗ウサギIgG抗体(1:10000)と室温で2時間インキュベートします。
- メンブレンをTBSTで再度洗浄し(各10分間を3回)、タンパク質バンド検出のために適切な量の増強化学発光(ECL)ワーキング溶液(製造元の指示に従って)で処理します。
- 化学発光イメージングシステムを使用して画像を取得し、Image J画像解析システムを使用してタンパク質のグレー値の半定量的分析を実行します。
11. 統計分析
- データの分析には、適切なソフトウェアアプリケーションを使用してください。すべてのデータをSD(標準偏差)±平均値として表し、グループ間の比較のために一元配置ANOVA検定によって複数のサンプルを評価します。
注:統計分析には、SPSS統計ソフトウェア26.0を使用しました。分散が等しい場合のグループ間の二元配置比較にはLSD法を使用し、分散が等しくない場合のグループ間の二元配置比較にはDunnett T3法を使用しました。P<0.05は統計学的に有意な差を示すと考えられた。
結果
IgANモデルにおけるDIOの腎臓組織への影響
対照群と比較して、粘膜免疫誘導IgANモデルマウス(モデル群)ではタンパク尿が有意に増加し(補足 図2)、メサンギアル領域にIgA沈着が見られ、蛍光はメサンギウム領域全体にクラスター状に均一に分布しており (図1A)、腎組織のPAS染色ではメサンギアル細胞の増殖と間質過形成が認められた (図1B)これは、DIO強制品群(DIOグループ)で減少しました。
パイエルパッチのBリンパ球に対するDIOの影響
パイエルパッチは、Bリンパ球のIgA分泌細胞への変換の主要な部位です。Peyerのパッチを研究対象として取り、B細胞マーカーCD20とCXCR5の発現を検出することにより、DIOのBリンパ球への影響を観察しました。免疫組織化学的結果から、CD20およびCXCR5の発現は、対照群と比較してモデル群で有意に高かったことが示されました。DIOは、上記の分子マーカーの発現を阻害する可能性があります (図2A、B)。
DAKIKI細胞上のDIOの安全濃度範囲
LDHは、原形質膜の完全性のマーカーであり、細胞死の指標であり、LDHの放出率が高いほど、細胞の損傷がより深刻であることを示します。LDH放出アッセイを使用して、DIOの安全な濃度範囲を決定しました。DIOの最大安全濃度は、LDH放出率が10%未満であることで決定されました。結果(図3)では、0.25〜1.0μg/mLの濃度でDIOによって誘発される有意な細胞毒性は示されませんでした。したがって、次の研究では、0.25、0.5、および 1.0 μg/mL DIO を投与レベルとして使用しました。
DIOがDAKIKI細胞の増殖に及ぼす影響
実験結果(図4)から、DIOはモデル群(LPS刺激群)と比較して、LPSによるDAKIKI細胞の増殖を濃度依存的に阻害することが示されました。0.5 μg/mL および 1.0 μg/mL 濃度の DIO は、LPS による DAKIKI 細胞の増殖を有意に阻害しました (P < 0.01)。
DIOがDAKIKI細胞の分泌機能に及ぼす影響
Gd-IgA1レベルはIgANの病理学的プロセスと密接に関連しており、総IgAは細胞分泌機能の指標として一緒にテストされます。ELISAアッセイを用いて、DAKIKI細胞培養の上清中のIgAおよびGd-IgA1含量を検出しました。その結果(図5A、B)、LPSで刺激されたDAKIKI細胞は、対照群と比較してIgAを多く分泌する(P < 0.01)ことが示されました(図5A、B)。これに対し、DIOはDAKIKI細胞のIgA分泌を有意に阻害しました(P < 0.01)。対照群と比較して、LPS刺激DAKIKI細胞は統計学的傾向(P < 0.10)でGd-IgA1を多く分泌し、DIOはLPS刺激DAKIKI細胞からのGd-IgA1分泌を濃度依存的に阻害(P < 0.05、P < 0.01)し、このうちDIO1.0μg/mLはGd-IgA1の分泌を有意に阻害し、阻害率は25%であった。
DIOのメカニズムはDAKIKI細胞によるGd-IgA1分泌を阻害する
DIOがDAKIKI細胞による過剰なGd-IgA1分泌を阻害するメカニズムの可能性をさらに調べるために、DAKIKI細胞のグリコシル化トランスフェラーゼC1GALT1とシャペロンタンパク質Cosmc mRNAのレベルをqRT-PCRで検出し、その結果(図6A、B)、モデル群のDAKIKI細胞では、C1GALT1とCosmcの相対的なmRNA発現が対照群と比較してダウンレギュレーションされていることが示されました(P < 0.01)。DIOは、モデル群と比較して、C1GALT1とCoscの相対的なmRNA発現を異なる程度にアップレギュレーションし、DIO 1.0 μg /mLは、C1GALT1とCoscの相対的なmRNA発現を大幅にアップレギュレーションしました(P < 0.05)。
同時に、DAKIKI細胞におけるC1GALT1およびCosmcのタンパク質発現に対するDIOの影響を検出するために、WB法を使用しました。対照群と比較して、モデル群のDAKIKI細胞におけるC1GALT1およびCosmcのタンパク質発現は明らかに減少しました(P < 0.05)。モデル群と比較して、DIO介入後のC1GALT1とCoscのタンパク質発現はアップレギュレーションされていました。C1GALT1およびCosmcのタンパク質発現は、DIOによって1.0 μg/mL(P < 0.05)の濃度で大幅にアップレギュレーションされました(図7A-C)。
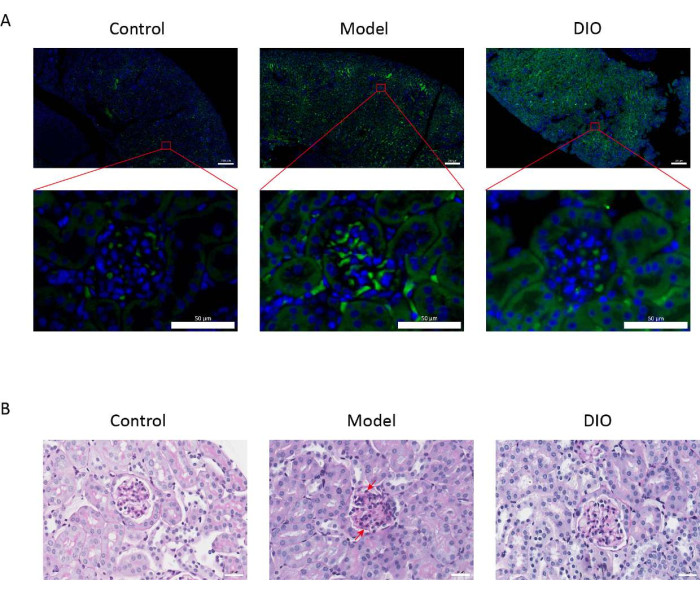
図1:腎臓の組織病理学( (A)免疫蛍光顕微鏡。各群のマウスの腎臓切片を抗IgA(緑)とDAPI(青)で染色しました。上の画像スケールバー= 200μm。下の画像スケールバー= 50μm。n = グループあたり 6。(B)対照群、モデル群、およびDIO群のマウスの腎臓組織のPAS染色の代表的な写真。スケールバー = 30 μm。下向きの矢印はメサンギウム細胞を示し、上向きの矢印は間質を示します。スケールバー = 30 μm。n = グループあたり 6。 この図の拡大版を表示するには、ここをクリックしてください。
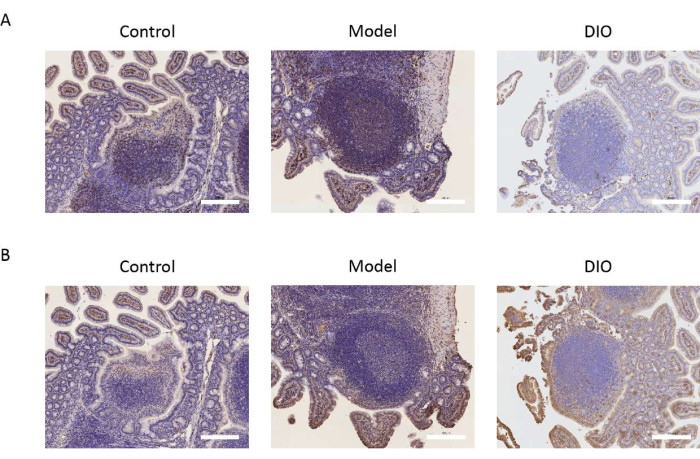
図2:Bリンパ球マーカーに対するDIOの影響 (A)パイエル板におけるCD20の発現。スケールバー = 200 μm。n = グループあたり 6。(B)パイエルパッチにおけるCXCR5の発現。スケールバーは画像の右下隅にあります。スケールバー = 200 μm。n = グループあたり 6。 この図の拡大版を表示するには、ここをクリックしてください。
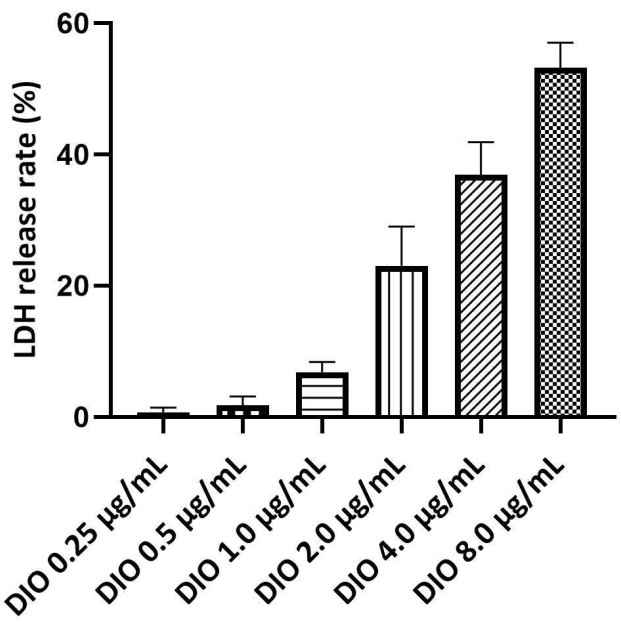
図 3.DAKIKI細胞上のDIOの安全濃度のスクリーニング。 統計値は、3つの独立した実験からの平均±SDとして表されます。 この図の拡大版を表示するには、ここをクリックしてください。
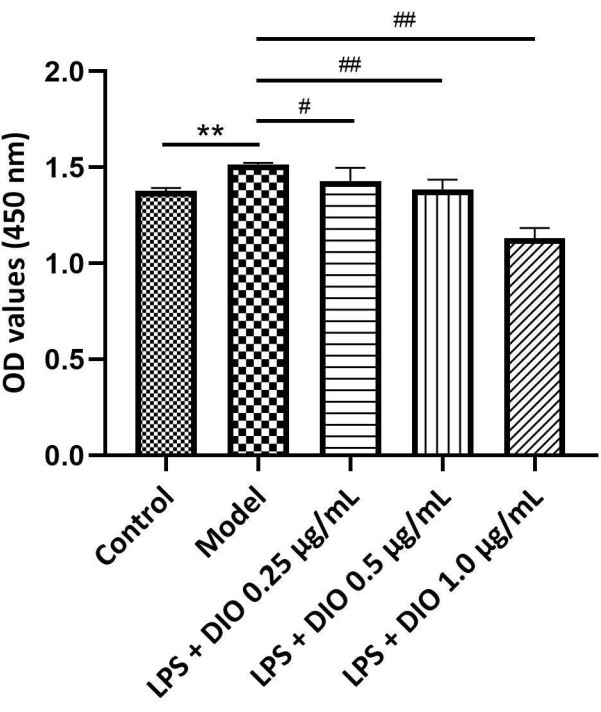
図 4.DIOの濃度が異なると、DAKIKI細胞の増殖に影響が及びます。 データは平均±SDとして表され、対照群と比較して、**P < 0.01;モデルグループと比較すると、 #P < 0.05' ##P < 0.01;すべての実験の結果が3回繰り返されました。 この図の拡大版を表示するには、ここをクリックしてください。
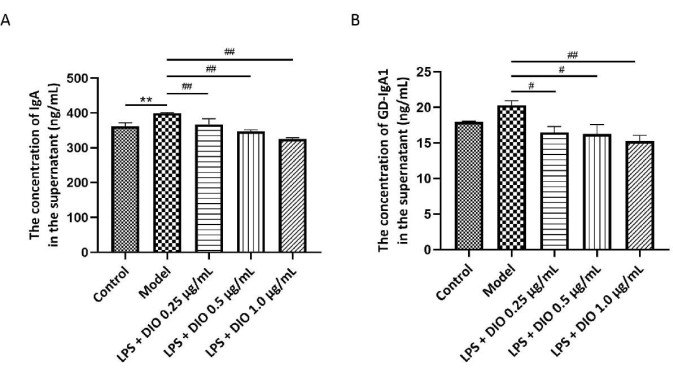
図 5.DIOは、DAKIKI細胞によるIgAおよびGd-IgA1の分泌を阻害します。 (A)ELISA法により、各群でIgAの発現を検出した。(B)ELISA法により、各群でGd-IgA1の発現を検出した。データはSD±平均として表されました。対照群と比較すると、**P < 0.01;モデルグループと比較すると、 #P < 0.05、 ##P < 0.01;すべての実験結果を3回繰り返しました。 この図の拡大版を表示するには、ここをクリックしてください。
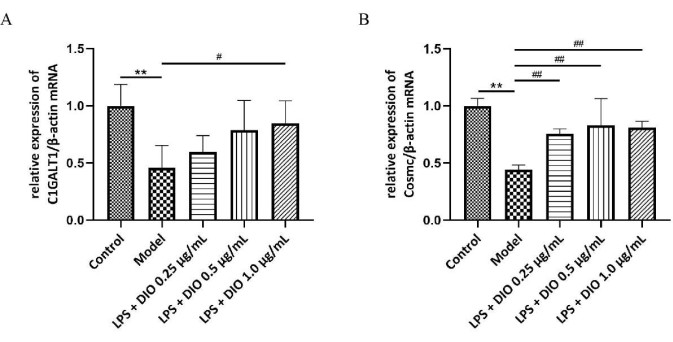
図 6.DIOのメカニズムは、DAKIKI細胞による過剰なGd-IgA1分泌を阻害します。 (A)QRT-PCRはC1GALT1のmRNA発現を検出しました。(B)QRT-PCRはCosmcのmRNA発現を検出しました。データはSD±平均として表されました。対照群と比較して、**P<0.01;モデルグループと比較すると、 #P < 0.05、 ##P < 0.01;すべての実験結果を3回繰り返しました。 この図の拡大版を表示するには、ここをクリックしてください。
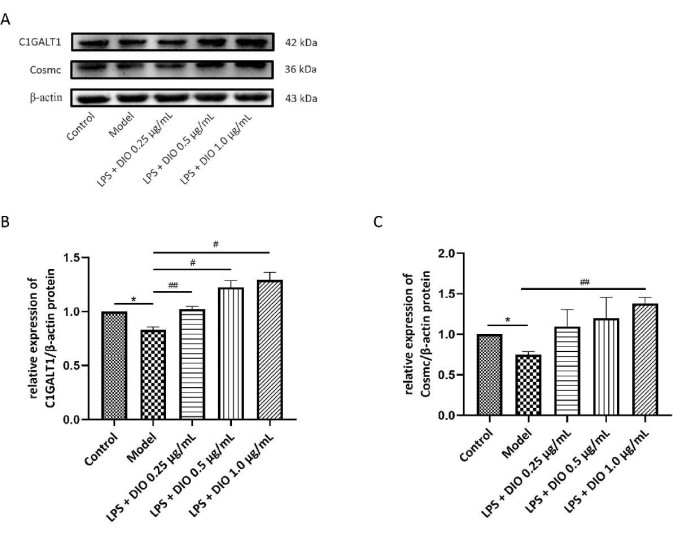
図 7.DIOは、DAKIKI細胞におけるC1GALT1とCosmcのタンパク質発現に影響を与えます。(A)WBは、DIOによるC1GALT1およびCosmcのタンパク質発現のアップレギュレーションを検証しました。(B)画像Jを用いたC1GALT1発現の半定量解析 (C)画像Jを用いたCosmc発現の半定量解析データは平均±SD.として表され、対照群と比較して、*P < 0.05;モデル群#P < 0.05、##P < 0.01と比較すると、すべての実験結果を3回繰り返しました。この図の拡大版を表示するには、ここをクリックしてください。
補足図1.in vivo モデルのスキーマ。この図をダウンロードするには、ここをクリックしてください。
補足 図2.タンパク尿の変化。 データは平均±SDとして表されました。n = グループあたり 6。 この図をダウンロードするには、ここをクリックしてください。
ディスカッション
IgANの特徴的な病理学的特徴は、糸球体のメサンギウム領域にIgA1およびGD-IgA1を含む免疫複合体が沈着することです21,22。免疫複合体の形成を減らすことで、腎障害を軽減し、IgANの臨床症状を緩和することができます。in vivo実験では、DIOのIgANに対する治療効果を検討し、DIOがIgANモデルマウスの腎臓でのIgA沈着を抑制できることを発見しました。腎臓におけるIgA分泌細胞の蓄積は、IgAN23の病因に関連していることが実証されています。Bリンパ球の増殖と活性化の重要な部位として、パイエル板はIgA分泌細胞の重要な供給源であることから、パイエル板におけるBリンパ球マーカー(CD20、CXCR5)の発現を調べたところ、IgANマウスモデルのパイエル板では、DIOがBリンパ球の発現を阻害できることを発見しました。これらの実験結果は、IgANの治療にDIOを適用するための基礎を提供する可能性があります。
私たちは、IgANに対するDIOの作用機序をさらに調べるために、以下の実験を In vitro で行いました。まず、IgA1(その一部がGD-IgA124)を分泌するEBV不死化B細胞株である「DAKIKI」が、IgANに対する薬物の作用機序の in vitro 研究に理想的であることは、以前に実証されました。私たちは、IgANの治療におけるDIOの分子メカニズムを調べるためにDAKIKI細胞を選びました。さらに、粘膜炎症性免疫応答は、IgANの病因に不可欠な役割を果たします。前述したように、LPSを用いてDAKIKI細胞を刺激することで、炎症誘発性因子を放出し、炎症反応を媒介することで、IgANの粘膜免疫応答のメカニズムをより模倣することができます。 in vitro 細胞モデルは、IgANを治療するための他の薬剤の可能性とメカニズムを調査するのに役立つ可能性があります。その結果、DIOはLPSによって刺激されたDAKIKI細胞の増殖を濃度依存的に阻害することが示されました。DIOは、LPS刺激によるDAKIKI細胞におけるIgAおよびGd-IgA1の分泌を阻害し、DAKIKI細胞におけるC1GalT1およびそのシャペロンCosmcのmRNAおよびタンパク質の発現をアップレギュレートすることが可能であり、DIOがC1GALT1/Cosmc発現をアップレギュレーションすることによりGd-IgA1の分泌を減少させ、DAKIKI細胞の過剰な活性化を阻害する可能性が示唆されました。
実験手順では、主要なステップに注意する必要があります。DAKIKI細胞上清中のGd-IgA1の濃度がELISAキットの検出範囲(1.56~100 ng/mL)内にないため、濃縮されたGd-IgA1を得るためには、採取した上清を限外ろ過管で遠心分離する必要があります。また、各グループから始まる上清の量が同じであり、限外ろ過後に得られる濃縮物の最終量が同じであることを確認してください。
本研究では、 in vitro 法と in vivo 法を同時に用いたため、薬理学的効果が相互に支え合うことができ、漢方薬の効果とそのメカニズムを研究するための例となりました。このプロトコルでは、いくつかの点を改善できます。まず、マウスのDIO強制群の血中濃度は検出されませんでした。したがって、DIOの血中濃度に相当する濃度は、 in vitro 実験では使用されません。次に、DNRの活性成分であるDIOモノマーのみが調査されました。DNRの他の成分がIgANに及ぼす影響については、さらに研究が必要である。
結論として、この研究は、DNRの有効成分であるDIOでIgANを治療するための実験的基礎を提供します。この研究では、 in vitro と in vivo の両方で IgAN の粘膜免疫応答を模倣することにより、IgAN の細胞病理学的モデルを確立しました。これは、IgANを予防および治療するための伝統的な中国医学を研究するための新しいアイデアを提供します。
開示事項
著者らは、競合する金銭的利益がないことを宣言します。
謝辞
この研究は、中国国家自然科学基金会(81973675)の支援を受けました。
資料
| Name | Company | Catalog Number | Comments |
| Anti-CD20/MS4A1 Antibody | Boster Biotechnology Company | A03780-3 | |
| Antifade mounting medium | Beyotime, Shanghai, China | P0128S | |
| Balb/c mice | Beijing Weitong Lihua Laboratory Animal Technology Co., Ltd. | 110322220101424000 | |
| blocking serum | Solarbio, Beijing, China | SL038 | |
| Bovine gamma globulin | ShangHai YuanYe Biotechnology Company | S12031 | |
| C1GALT1 polyclonal antibody | Proteintech Group, Inc,USA | 27569-1-AP | |
| Citrate antigen retrieval solution(50×) | Phygene Biotechnology Company | PH0422 | |
| COSMC polyclonal antibody | Proteintech Group, Inc,USA | 19254-1-AP | |
| Cytotoxiciy detection kit | Roche Company | 4744926001 | |
| Dako REAL EnVision detection system, Peroxidase/DAB+ | Dako | K5007 | |
| DAPI | Invitrogen | D1306 | |
| Dioscin | National Institute For Food and Drug Control | 111707-201703 | |
| DIO tablets | Chengdu No 1 Pharmaceutical Co. Ltd. | H51023866 | |
| ECL working solution | Merck Biotechnology, Inc | WBKLS0100 | |
| Enhanced cell counting kit-8 | Beyotime, Shanghai, China | C0043 | |
| Fasking one-step removal of gene cDNA first-strand synthesis premix | TIANGEN,Beijing, China | KR118-02 | |
| Glycogen Periodic acid Schiff (PAS) stain kit | BaSO Biotechnology Company | BA4080A | |
| Goat anti-mouse IgA-AF488 | SouthernBiotech | 1040-30 | |
| Goat anti-rabbit IgG antibody (H+L), HRP conjugated | BeiJing Bioss Biotechnology Company | BS-0295G-HRP | |
| Human Gd-IgA1 ELISA kit | IBL | 27600 | |
| Human IgA ELISA kit | MultiSciences (LiankeBio) | 70-EK174-96 | |
| Pierce BCA protein assay kit | Thermo Scientific | 23227 | |
| PMSF solution | Beyotime, Shanghai, China | ST507 | |
| Proteinase K | Phygene Biotechnology Company | PH1521 | |
| Rabbit anti-CXCR5 polyclonal antibody | BeiJing Bioss Biotechnology Company | bs-23570R | |
| RIPA lysis buffer | Beyotime, Shanghai, China | P0013B | |
| RNAsimple total RNA extraction kit | TIANGEN,Beijing, China | DP419 | |
| RPMI Medium 1640 | Solarbio, Beijing, China | 31800 | |
| Super-Bradford protein assay kit | CWBIO, Beijing, China | CW0013 | |
| Triton X-100 | Beyotime, Shanghai, China | ST795 | |
| β-Actin Rabbit mAb | Abclonal, Wuhan, China | AC026 |
参考文献
- Knoppova, B., et al. The origin and activities of IgA1-containing immune complexes in IgA nephropathy. Frontiers in Immunology. 7, 117(2016).
- Suzuki, H., et al. The pathophysiology of IgA nephropathy. Journal of The American Society of Nephrology. 22 (10), 1795-1803 (2011).
- He, L., et al. Synthetic double-stranded RNA poly(I:C) aggravates IgA nephropathy by triggering IgA class switching recombination through the TLR3-BAFF axis. American Journal of Nephrology. 42 (3), 185-197 (2015).
- Zhao, N., et al. The level of galactose-deficient IgA1 in the sera of patients with IgA nephropathy is associated with disease progression. Kidney International. 82 (7), 790-796 (2012).
- Xing, Y., et al. C1GALT1 expression is associated with galactosylation of IgA1 in peripheral B lymphocyte in immunoglobulin a nephropathy. BMC Nephrology. 21 (1), 18(2020).
- Qin, W., et al. External suppression causes the low expression of the Cosmc gene in IgA nephropathy. Nephrology Dialysis Transplantation. 23 (5), 1608-1614 (2008).
- Sakai, F., et al. Lactobacillus gasseri SBT2055 induces TGF-β expression in dendritic cells and activates TLR2 signal to produce IgA in the small intestine. PLoS One. 9 (8), 105370(2014).
- Gutzeit, C., Magri, G., Cerutti, A. Intestinal IgA production and its role in host-microbe interaction. Immunological Reviews. 260 (1), 76-85 (2014).
- Serino, G., et al. In a retrospective international study, circulating miR-148b and let-7b were found to be serum markers for detecting primary IgA nephropathy. Kidney International. 89 (3), 683-692 (2016).
- Lu, F., et al. Therapeutic effect of Rhizoma Dioscoreae Nipponicae on gouty arthritis based on the SDF-1/CXCR 4 and p38 MAPK pathway: an in vivo and in vitro study. Phytotherapy research: PTR. 28 (2), 280-288 (2014).
- Wang, W., Xu, L., Zhou, L., Wan, S., Jiang, L. A Network pharmacology approach to reveal the underlying mechanisms of Rhizoma Dioscoreae Nipponicae in the treatment of asthma. Evidence-Based Complementary and Alternative Medicine: eCAM. 2022, 4749613(2022).
- Tian, W. W., Wei, Y. Professor TONG Xiaolin used the experience of Dioscoreae Nipponicae. Jilin Journal of Chinese Medicine. 40 (05), 589-592 (2020).
- Rao, X. R., Bai, Y. W. Das Xiwen's experience in treating IgA nephropathy. Beijing Journal of Traditional Chinese Medicine. 9, 691-693 (2008).
- Si, Y., Zhang, Y. A data mining study on the pattern of medication use in the treatment of IgA nephropathy by Professor Zhang Yu. Journal of Chinese Physician. 20 (01), 109-111 (2018).
- Jiang, H., et al. Optimization of the enzymatic extraction technology of Diosgenin from Dioscorea nipponica. Chinese Traditional Patent Medicine. 39 (03), 621-624 (2017).
- Qi, M., et al. Dioscin alleviates lipopolysaccharide-induced inflammatory kidney injury via the microRNA let-7i/TLR4/MyD88 signaling pathway. Pharmacological Research. 111, 509-522 (2016).
- Yang, L., et al. Recent advances in the pharmacological activities of Dioscin. BioMed Research International. 2019, 5763602(2019).
- Nal Zou, J., et al. Toll-like receptor 4 signaling pathway in the protective effect of Pioglitazone on experimental immunoglobulin A nephropathy. Chinese Medical Journal. 130 (8), 906-913 (2017).
- Xu, S. Y., Bian, R. L., Chen, X. Pharmacological experiments methodology. Chinese Pharmacological Bulletin. 1, 19(1992).
- Shen, J. C., Ren, Y., Rao, X. R., You, Y., Li, S. Network pharmacology, molecular docking, and in vitro experiments to explore the molecular mechanism of Dioscorea Nipponica Makion in the treatment of IgA nephropathy. World Journal of Integrated Traditional and Western Medicine. 16 (12), 2246-2254 (2021).
- Mestecky, J., et al. IgA nephropathy: molecular mechanisms of the disease. Annual Review of Pathology. 8, 217-240 (2013).
- Novak, J., et al. IgA1-containing immune complexes in IgA nephropathy differentially affect proliferation of mesangial cells. Kidney International. 67 (2), 504-513 (2005).
- Nihei, Y., et al. Identification of IgA autoantibodies targeting mesangial cells redefines the pathogenesis of IgA nephropathy. Science Advances. 9 (12), (2023).
- Raska, M., et al. Identification and characterization of CMP-NeuAc: GalNAc-IgA1 alpha2,6-sialyltransferase in IgA1-producing cells. Journal of Molecular Biology. 369 (1), 69-78 (2007).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved